锂/钠离子电池用水系电解液以及锂/钠离子电池的制作方法
本发明涉及一种锂/钠离子电池用水系电解液以及具备该电解液的锂/钠离子电池。
背景技术:
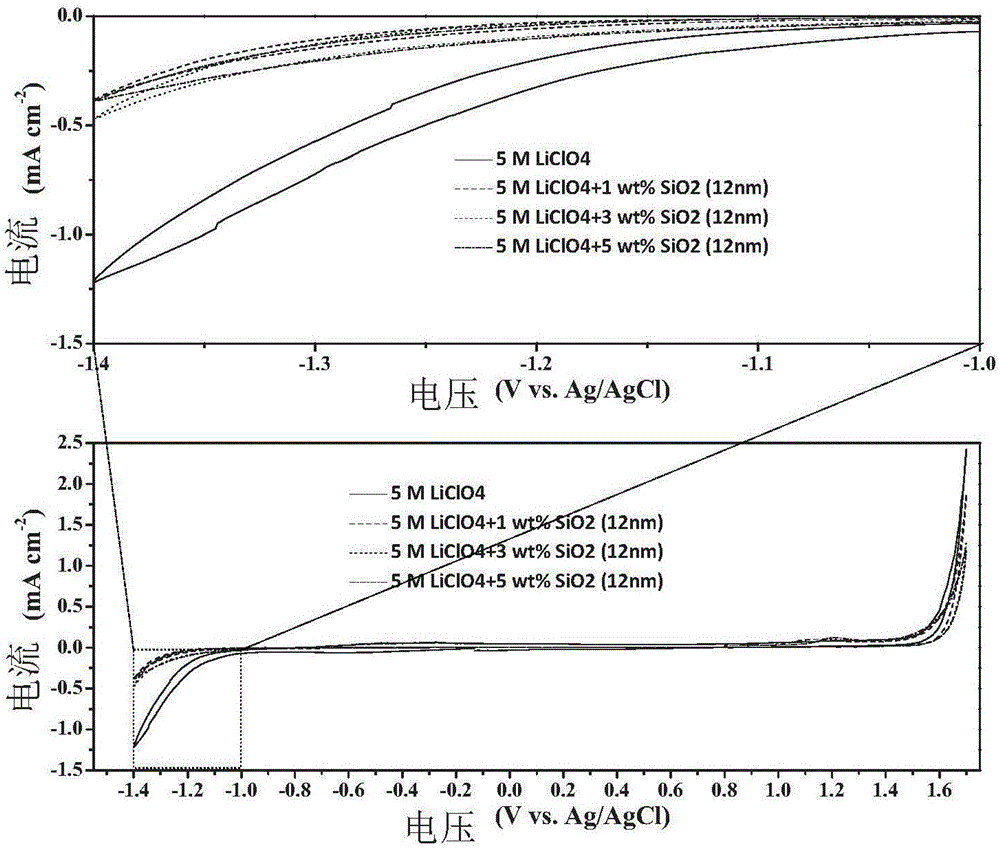
:随着现代社会对能源需求紧迫性的增加,高能量密度的二次电池已经成为未来能源产业发展的重点,锂/钠离子电池以其突出的性能优势成为研究的热点。然而,现有锂/钠离子电池所用电解液均为有机电解液,它存在电导率低以及易于燃烧爆炸的高安全隐患。为此,人们考虑使用水系电解液来替代有机电解液。水系电解液具有低成本、高安全性以及环境友好的优势。并且,具有更高的电导率,能够改善电池的功率特性。水系电解液存在的最大问题是其电化学窗口较窄,这是因为水的电化学稳定窗口较窄,在负极易发生析氢反应,而在正极发生析氧反应。目前拓宽水系电解液电化学窗口最常见的办法就是采用高浓度的锂/钠盐水溶液,形成一种“盐包水”的结构,能够有效地抑制水分解,从而拓宽电解液的电化学窗口。但是此方法具有很高的成本,使电解液粘度上升,并造成盐析现象。因此,寻找一种简单、易行、廉价的拓宽水系电解液电化学窗口的方法显得尤为必要。技术实现要素:本发明的目的是提供一种电化学窗口拓宽的锂/钠离子电池用水系电解液以及具备该电解液的锂/钠离子电池。水系电解液具有高电导率、高安全性、环境友好等优点,但是其电化学窗口较窄,从而导致基于水系电解液的锂/钠离子电池的能量密度较低。本发明采用廉价的氧化物纳米粒子作为水系电解液添加剂,能够显著的拓宽水系电解液电化学窗口。该操作简单、易行、低成本,非常有利于实现工业化生产。本发明是通过以下技术方案实现的:本发明提供了一种锂/钠离子电池用水系电解液,其特征在于,在锂/钠离子盐水溶液中均匀分散有亲水性氧化物纳米粒子。作为优选方案,锂离子盐采用liclo4、litfsi、lifsi、li2so4、lino3中的一种或者几种。作为优选方案,锂离子盐的浓度为1-5mol/l。浓度5mol/l时,电导率已经超出仪器测试量程,且成本增加,而不优选。浓度小于1mol/l时,电导率过低,而不优选。作为优选方案,钠离子盐种类为naclo4、natfsi、nafsi、na2so4、nano3中的一种或者几种。作为优选方案,钠离子盐的浓度为1-5mol/l。浓度5mol/l时,电导率已经超出仪器测试量程,且成本增加,而不优选。浓度小于1mol/l时,电导率过低,而不优选。作为优选方案,亲水性氧化物纳米粒子采用sio2、al2o3、tio2、zro2中的一种或几种。作为优选方案,亲水性氧化物纳米粒子的颗粒尺寸为7~40nm。大于40nm时,氧化物颗粒过大会导致其在电解液中沉降,小于7nm时,价格高,因而不优选。作为优选方案,亲水性氧化物纳米粒子的含量大于零且小于10wt%,优选为1-3wt.%。大于3wt%时,会使电解液过于黏稠,流动性变差;小于1wt%时效果不明显,因而不优选。与现有技术相比,本发明具有如下的有益效果:1、以廉价氧化物纳米粒子作为添加剂,避免使用高浓度锂/钠离子盐水溶液作为水系电解液,且能够扩宽电位窗口。2、操作简单易行,容易实现工业化生产。附图说明通过阅读参照以下附图对非限制性实施例所作的详细描述,本发明的其它特征、目的和优点将会变得更明显:图1为本发明中实施例7-9制得水系电解液的循环伏安曲线图及局部放大图;图2为本发明中实施例16-18制得水系电解液的循环伏安曲线图及局部放大图;图3为本发明中实施例25-27制得水系电解液的循环伏安曲线图及局部放大图。具体实施方式下面结合具体实施例对本发明进行详细说明。以下实施例将有助于本领域的技术人员进一步理解本发明,但不以任何形式限制本发明。应当指出的是,对本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进。这些都属于本发明的保护范围。实施例1-9以liclo4为锂离子盐,分别制备浓度为1、3、5m(mol/l)的锂离子盐水溶液,并且相对于锂离子盐水溶液分别以1、3、5wt%的含量添加作为添加剂的sio2并通过搅拌或超声波使其均匀分散于锂离子盐水溶液,从而制备实施例1-9的锂离子电池用水系电解液,其中,sio2尺寸为12nm。并且针对实施例7-9的锂离子电池用水系电解液进行了循环伏安测试,测试时工作电极为不锈钢,参比电极为ag/agcl。在实施例1-9中制备的锂离子电池用水系电解液,其ph值及电导率如下表1所示:表1实施例7-9制备的锂离子电池用水系电解液,其循环伏安曲线如图1所示,可以看出,在水系电解液中加入sio2添加剂后,与不加添加剂的情况相比,阴极还原电位明显负移,具体数值如下表2:表2sio2含量阴极还原电位负移值实施例71wt%190mv实施例83wt%160mv实施例95wt%190mv实施例10-18以naclo4为钠离子盐,分别制备浓度为1、3、5m(mol/l)的钠离子盐水溶液,并且相对于钠离子盐水溶液分别以1、3、5wt%的含量添加作为添加剂的sio2并通过搅拌或超声波使其均匀分散于钠离子盐水溶液,从而制备实施例10-18的钠离子电池用水系电解液,其中,sio2尺寸为12nm。并且针对实施例16-18的钠离子电池用水系电解液进行了循环伏安测试,测试时工作电极为不锈钢,参比电极为ag/agcl。实施例16-18制备的钠离子电池用水系电解液,其ph值及电导率如下表3所示:表3实施例16-18制备的钠离子电池用水系电解液,其循环伏安曲线如图2所示,可以看出,在水系电解液中加入sio2添加剂后,与不加添加剂的情况相比,阴极还原电位明显负移,具体数值如下表4:表4sio2含量阴极还原电位负移值实施例161wt%90mv实施例173wt%60mv实施例185wt%50mv实施例19-27相对于实施例1-8,除了作为锂离子盐变更为采用litfsi以外,采用相同的方式分别制备了如下实施例19-27的锂离子电池用水系电解液,并采用与实施例1-8相同的方式进行了循环伏安测试。实施例19-27制备的锂离子电池用水系电解液,其ph值及电导率如下表5所示:表5实施例25-27制备的锂离子电池用水系电解液,其循环伏安曲线如图3所示,可以看出,在水系电解液中加入sio2添加剂后,与不加添加剂的情况相比,阴极还原电位明显负移,具体数值如下表6:表6sio2含量阴极还原电位负移值实施例251wt%120mv实施例263wt%60mv实施例275wt%20mv实施例28-36相对于实施例10-18,除了将钠离子盐变更为natfsi以外,采用相同的方式分别制备了如下实施例28-36的锂离子电池用水系电解液,并采用与实施1-8相同的方式进行了循环伏安测试。实施例28-36制备的钠离子电池用水系电解液,其ph值及电导率如下表7所示:表7实施例34-36制备的钠离子电池用水系电解液,在其中加入sio2添加剂后,与不加添加剂的情况相比,阴极还原电位明显负移,具体数值如下表8:表8sio2含量阴极还原电位负移值实施例341wt%100mv实施例353wt%48mv实施例365wt%17mv实施例37-38相对于实施例7,除了将作为添加剂的sio2的尺寸分别变更为30、40nm之外,采用相同的方式分别制备了如下实施例37-38的锂离子电池用水系电解液,并采用与实施1-8相同的方式进行了循环伏安测试。实施例37、38制备的锂离子电池用水系电解液,其ph值及电导率如下表9所示:表9sio2尺寸ph电导率实施例712nm4.43大于200实施例3730nm4.38大于200实施例3840nm4.40大于200实施例37、38制备的锂离子电池用水系电解液,在其中加入1wt%sio2添加剂后,与不加添加剂的情况相比,阴极还原电位明显负移,具体数值如下表10:表10sio2尺寸阴极还原电位负移值实施例712nm190mv实施例3730nm192mv实施例3840nm187mv实施例39相对于实施例7,除了作为添加剂变为采用尺寸为15nm的al2o3之外,采用相同的方式分别制备了如下实施例39的锂离子电池用水系电解液,并采用与实施7相同的方式进行了循环伏安测试。实施例39制备的锂离子电池用水系电解液,其ph值为4.88,电导率大于200ms/cm。实施例39制备的锂离子电池用水系电解液,在其中加入al2o3添加剂后,与不加添加剂的情况相比,阴极还原电位负移了156mv。综上所述,本发明提供了锂/钠离子电池用水系电解液,含义氧化物纳米粒子作为水系电解液添加剂。本发明的锂/钠离子电池用水系电解液,能够显著地拓宽水系电解液电化学的窗口。并且本发明的锂/钠离子电池用水系电解液制备简单、易行、低成本,非常有利于实现工业化生产。以上对本发明的具体实施例进行了描述。需要理解的是,本发明并不局限于上述特定实施方式,本领域技术人员可以在权利要求的范围内做出各种变形或修改,这并不影响本发明的实质内容。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1