一种尖晶石铁氧体/碳复合材料的制备方法
1.本发明涉及一种尖晶石铁氧体的制备方法。
背景技术:
2.尖晶石纳米复合材料凭借其特殊的结构和优越的吸波性能,在医药、国防、航空、及化工等相关领域得到广泛研究。通过对各种尖晶石结构的金属氧化物进行包覆与复合,可提高尖晶石纳米复合材料的电损耗和磁损耗值,从而实现吸波材料“厚度薄、质量轻、吸收强、频率宽”的目的。目前研发出的尖晶石纳米复合材料虽然能满足电磁波吸收领域的常规应用,但是其制备方法复杂并且成本较高,从而很难大面积应用推广。因此,市场急需一种在能保证吸波性能的同时制备步骤简单且成本低廉的尖晶石铁氧体吸波材料。
3.中国专利《一种双壳层结构的纳米铁氧体复合材料及其制备方法》(公开号:cn108101114b)中利用纳米铁氧体颗粒、乙醇、去离子水、硝酸、表面活性剂、酚醛树脂、二氧化硅和二氧化钛等原材料,通过球磨、烘干等方法制备一种的双壳层结构的纳米铁氧体复合材料。但是所需原材料较多、步骤繁琐很难规模化生产并应用。
4.中国专利《一种新型多孔炭材料负载纳米铁氧体吸波材料的制备方法》(公开号:cn102134470b)利用柠檬酸、无机金属盐、去离子水、活性碳纤维凝胶、氮气等原材料,通过搅拌、烘干、高温煅烧等制备方法制成一种新型多孔炭材料负载纳米铁氧体吸波材料。但是所需制备成本高、流程复杂、不符合大规模生产需求。
5.中国专利《一步法制备三层复合吸波材料的方法》(公开号:cn109208091b)中利用feb金属块、zr金属块、co金属块、cu粉、pan纤维和石墨粉进行熔炼、球磨、烧结等制备方法制成制备三层复合吸波材料。但是所需条件苛刻,成本价格高、所需制备环境苛刻、不适合规模化生产并应用。
6.中国专利《一种纳米铁氧体吸波材料》(公开号:cn103755333a)中利用介孔泡沫氧化硅、氯仿、铁金属盐、铝金属盐、钡金属盐、镁金属盐、氨水等原材料,通过过滤、水洗、干燥、高温煅烧等制备方法制成一种纳米铁氧体吸波材料。但是所需原材料成本较高、原料种类繁多、制备流程复杂、不适合规模化生产。
7.材料导报2009年11月第23卷专辑14第19到24页中利用弱酸聚丙烯酸系阳离子交换树脂、铁二价离子、镍二价离子等原材料,通过搅拌、水洗、烘干、热分解等制备方法制成吸收率为15.7ghz的碳包裹纳米铁粒子。但是流程复杂、成本较高、吸波频率较低。
8.纳米技术与精密工程2010年1卷第八卷1期第16到19页中利用纤维素、去离子水、fe(no3)3·
9h2o、naoh等原材料,通过搅拌、洗涤、过滤、烘干、煅烧等方法制成碳包覆铁纳米颗粒。但是制备成本高,条件苛刻,制备流程复杂。
技术实现要素:
9.本发明的目的是要解决现有方法制备的吸波材料成本高,流程复杂,条件苛刻和吸波性能差的问题,而提供一种尖晶石铁氧体/碳复合材料的制备方法。
10.尖晶石铁氧体作为一种原料广泛、价格低廉、磁性能优越的材料,与碳材料复合后可呈现优良的电磁波吸收性能,容易实现吸波材料的批量生产并应用。本发明是通过有机金属盐在管式加热炉中煅烧,以简单低成本的方法得到尖晶石铁氧体/碳复合材料,通过尖晶石铁氧体的磁损耗和碳材料的电损耗,吸收电磁波的能量,从而达到电磁波吸收材料的“厚度薄、质量轻、吸收强、频率宽”的需求,可以解决军用设备的隐身问题和日常生活中的电磁污染问题。
11.一种尖晶石铁氧体/碳复合材料的制备方法,是按以下步骤完成的:
12.一、制备前驱体:
13.将有机金属盐加入到低挥发类溶剂中或将有机金属盐与有机碳源共同加入到低挥发类溶剂中,混合,低挥发性溶剂挥发完,得到前驱体;
14.步骤一中所述的有机碳源为硬脂酸或离子交换树脂;
15.步骤一中将有机金属盐与有机碳源共同加入到低挥发类溶剂中得到的前驱体中有机金属盐与有机碳源的摩尔比为1:(0.01~2);
16.步骤一中将有机金属盐加入到低挥发类溶剂中得到的前驱体中有机金属盐与低挥发类溶剂的质量比为1:(1~20);
17.步骤一中将有机金属盐与有机碳源共同加入到低挥发类溶剂中得到的前驱体中有机金属盐与有机碳源的总质量与低挥发类溶剂的质量比为1:(1~20);
18.二、煅烧:将前驱体放入瓷舟中,并置于管式加热炉中,在通入气体的条件下升温至400℃~1000℃,在400℃~1000℃下煅烧一定时间,再降至室温,得到尖晶石铁氧体/碳复合材料初始产品;
19.三、将瓷舟中的尖晶石铁氧体/碳复合材料初始产品取出,对尖晶石铁氧体/碳复合材料初始产品进行离心清洗,得到高纯度的尖晶石铁氧体/碳复合材料。
20.本发明的优点:
21.一、本发明通过采用有机金属盐,可同时提供金属粒子和碳源,在高温条件下反应可以一次性制备磁性碳复合材料,从而减少了实验流程并且降低原料的成本,还可以用增加另外的有机碳源来调控碳含量,从而控制碳的电损耗和铁氧体的磁损耗能力大小;
22.二、本发明可通过替换不同金属元素的有机金属盐,制备不同元素掺杂的尖晶石型碳复合材料,从而提高了碳复合材料的性能,金属离子作为尖晶石铁氧体/碳复合材料中的磁性材料,有机碳链提供碳源;两者可以形成紧密结构,从而一次性制备磁性碳复合材料;
23.三、本发明通过利用低挥发溶剂来保证有机金属盐之间的混合均匀,并通过高温挥发,降低对实验过程的影响;
24.四、本发明通过利用有机金属盐与有机碳源的比例,来控制碳包裹尖晶石铁氧体的程度,从而控制碳的电损耗和铁氧体的磁损耗能力大小;
25.五、本发明所需要的原材料简单、价格低廉、反应环境简单、流程简单、易于调控、可实现规模化生产;
26.六、本发明采用两种吸波材料的复合,可以通过铁氧体的磁损耗和碳的电损耗,提高了复合材料的吸波性能;
27.七、本发明所使用的原料和试验过程绿色且环保,从而避免对环境的破坏;
28.八、本发明制备的高纯度的尖晶石铁氧体/碳复合材料的最佳反射率为:-34db~-18db。
附图说明
29.图1为实施例1制备的fe3o4/c复合材料的xrd图;
30.图2为实施例2制备的mnfe2o4/c复合材料的xrd图;
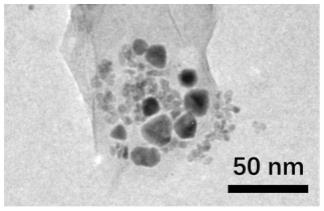
31.图3为实施例1制备fe3o4/c复合材料的透射电镜图;
32.图4为实施例2制备mnfe2o4/c复合材料的透射电镜图;
33.图5为实施例1制备fe3o4/c复合材料的磁场强度与比饱和强度图;
34.图6为实施例2制备mnfe2o4/c复合材料的磁场强度与比饱和强度图;
35.图7为实施例1制备的fe3o4/c复合材料的电磁波吸收图;
36.图8为对比实施例制备的mnfe2o4/c复合材料的电磁波吸收图。
具体实施方式
37.以下实施例进一步说明本发明的内容,但不应理解为对本发明的限制。在不背离本发明实质的情况下,对本发明方法、步骤或条件所作的修改和替换,均属于本发明的范围。
38.具体实施方式一:本实施方式一种尖晶石铁氧体/碳复合材料的制备方法是按以下步骤完成的:
39.一、制备前驱体:
40.将有机金属盐加入到低挥发类溶剂中或将有机金属盐与有机碳源共同加入到低挥发类溶剂中,混合,低挥发性溶剂挥发完,得到前驱体;
41.步骤一中所述的有机碳源为硬脂酸或离子交换树脂;
42.步骤一中将有机金属盐与有机碳源共同加入到低挥发类溶剂中得到的前驱体中有机金属盐与有机碳源的摩尔比为1:(0.01~2);
43.步骤一中将有机金属盐加入到低挥发类溶剂中得到的前驱体中有机金属盐与低挥发类溶剂的质量比为1:(1~20);
44.步骤一中将有机金属盐与有机碳源共同加入到低挥发类溶剂中得到的前驱体中有机金属盐与有机碳源的总质量与低挥发类溶剂的质量比为1:(1~20);
45.二、煅烧:将前驱体放入瓷舟中,并置于管式加热炉中,在通入气体的条件下升温至400℃~1000℃,在400℃~1000℃下煅烧一定时间,再降至室温,得到尖晶石铁氧体/碳复合材料初始产品;
46.三、将瓷舟中的尖晶石铁氧体/碳复合材料初始产品取出,对尖晶石铁氧体/碳复合材料初始产品进行离心清洗,得到高纯度的尖晶石铁氧体/碳复合材料。
47.具体实施方式二:本实施方式与具体实施方式一不同点是:步骤一中所述的有机金属盐为有机金属盐ⅰ或有机金属盐ⅱ;所述的有机金属盐ⅰ为三价有机金属盐或三价有机金属盐与一种或多种二价有机金属盐的混合物,混合物中三价有机金属盐与二价有机金属盐的摩尔比为(1.5~2.5):1。其它步骤与具体实施方式一相同。
48.具体实施方式三:本实施方式与具体实施方式一或二之一不同点是:所述的三价
有机金属盐为硬脂酸铁、柠檬酸铁、油酸铁或二茂铁。其它步骤与具体实施方式一或二相同。
49.具体实施方式四:本实施方式与具体实施方式一至三之一不同点是:步骤一中所述的二价有机金属盐为硬脂酸锰、硬脂酸铜、硬脂酸锌、硬脂酸镁、硬脂酸钡、硬脂酸铬、柠檬酸锌、柠檬酸钡、油酸锌、油酸钡、二茂铬、二茂钴或二茂镍。其它步骤与具体实施方式一至三相同。
50.具体实施方式五:本实施方式与具体实施方式一至四之一不同点是:步骤一中所述的有机金属盐ⅱ为多种相同酸根的有机金属盐的混合物。其它步骤与具体实施方式一至四相同。
51.具体实施方式六:本实施方式与具体实施方式一至五之一不同点是:步骤一中所述的低挥发类溶剂为无水乙醇、乙醚、丙酮或氯仿;步骤一中所述的混合方式为使用磁力搅拌或使用球磨机进行球磨,磁力搅拌的速度为50r/min~500r/min,磁力搅拌的温度为40℃~90℃。其它步骤与具体实施方式一至五相同。
52.具体实施方式七:本实施方式与具体实施方式一至六之一不同点是:步骤二中所述气体为空气、氮气、氧气或氩气;步骤二中所述气体的流速为0.1l/min~5l/min。其它步骤与具体实施方式一至六相同。
53.具体实施方式八:本实施方式与具体实施方式一至七之一不同点是:步骤二中所述的升温的速率为5℃/min~20℃/min;步骤二中所述的煅烧的时间为2h~5h。其它步骤与具体实施方式一至七相同。
54.具体实施方式九:本实施方式与具体实施方式一至八之一不同点是:步骤三中所述的离心清洗的速度为1000r/min~5000r/min,离心清洗的时间为5min~30min;步骤三中所述的离心清洗的次数为3次~10次,离心清洗使用的溶剂为去离子水、乙醇、庚烷或己烷。其它步骤与具体实施方式一至八相同。
55.具体实施方式十:本实施方式与具体实施方式一至九之一不同点是:步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的比饱和磁化强度为20emu/g~70emu/g;步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料中尖晶石铁氧体直径为10nm~500nm。其它步骤与具体实施方式一至九相同。
56.采用以下实施例验证本发明的有益效果:
57.实施例1:高纯度的fe3o4/c复合材料的制备方法,是按以下步骤完成的:
58.一、煅烧:将硬脂酸铁放入瓷舟中,并置于管式加热炉中,在通入氮气的条件下升温至550℃,在550℃下煅烧3h,再降至室温,得到尖晶石铁氧体/碳复合材料初始产品;
59.步骤一中所述的氮气的流速为5l/min;
60.步骤一中所述的升温的速率为5℃/min;
61.二、将瓷舟中的尖晶石铁氧体/碳复合材料初始产品取出,对尖晶石铁氧体/碳复合材料初始产品进行离心清洗,得到高纯度的fe3o4/c复合材料;
62.步骤二中所述的离心清洗的速度为2500r/min,离心清洗的时间为10min;
63.步骤二中所述的离心清洗的次数为8次,离心清洗使用的溶剂为去离子水;
64.步骤二中所述的高纯度的尖晶石铁氧体/碳复合材料的比饱和磁化强度为58emu/g;
65.步骤二中所述的高纯度的尖晶石铁氧体/碳复合材料中尖晶石铁氧体直径为20nm~50nm;
66.步骤二中所述的高纯度的尖晶石铁氧体/碳复合材料的最佳反射率为:-34db。
67.实施例2:高纯度的mnfe2o4/c复合材料的制备方法,是按以下步骤完成的:
68.一、制备前驱体:
69.将有机金属盐和有机碳源加入到低挥发类溶剂中,在70℃和搅拌速度为500r/min的条件下磁力搅拌至低挥发性溶剂挥发完,得到前驱体;
70.步骤一中所述的低挥发类溶剂为氯仿;
71.步骤一中所述的有机金属盐为硬脂酸铁和硬脂酸锰的混合物,其中硬脂酸铁与硬脂酸锰的摩尔比为2:1;
72.步骤一中所述的有机碳源为硬脂酸;
73.步骤一中所述的前驱体中有机金属盐与有机碳源的摩尔比为1:0.5;
74.步骤一中所述的前驱体中有机金属盐与有机碳源的总质量与低挥发类溶剂的质量比为1:10;
75.二、煅烧:将前驱体放入瓷舟中,并置于管式加热炉中,在通入气体的条件下升温至500℃,在500℃下煅烧2h,再降至室温,得到尖晶石铁氧体/碳复合材料初始产品;
76.步骤二中所述气体为氧气;
77.步骤二中所述气体的流速为5l/min;
78.步骤二中所述的升温的速率为5℃/min;
79.三、将瓷舟中的尖晶石铁氧体/碳复合材料初始产品取出,对尖晶石铁氧体/碳复合材料初始产品进行离心清洗,得到高纯度的mnfe2o4/c复合材料;
80.步骤三中所述的离心清洗的速度为3000r/min,离心清洗的时间为8min;
81.步骤三中所述的离心清洗的次数为3次,离心清洗使用的溶剂为无水乙醇;
82.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的比饱和磁化强度为50emu/g;
83.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料中尖晶石铁氧体直径为50nm~100nm;
84.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的最佳反射率为:-30db。
85.实施例3:高纯度的znfe2o4/c复合材料的制备方法是按以下步骤完成的:
86.一、制备前驱体:
87.将有机金属盐和有机碳源溶解到低挥发类溶剂中,在65℃和搅拌速度为600r/min的条件下磁力搅拌至低挥发性溶剂挥发完,得到前驱体;
88.步骤一中所述的有机金属盐为硬脂酸铁和硬脂酸锌的混合物,其中硬脂酸铁和硬脂酸锌的摩尔比为2:1;
89.步骤一中所述的低挥发类溶剂为乙醚;
90.步骤一中所述的有机碳源为离子交换树脂;
91.步骤一中所述的前驱体中有机金属盐与有机碳源的摩尔比为1:0.6;
92.步骤一中所述的前驱体中有机金属盐与有机碳源的总质量与低挥发类溶剂的质量比为1:7;
93.二、煅烧:将前驱体放入瓷舟中,并置于管式加热炉中,在通入气体的条件下升温至600℃,在600℃下煅烧3h,再降至室温,得到尖晶石铁氧体/碳复合材料初始产品;
94.步骤二中所述气体为空气;
95.步骤二中所述气体的流速为5l/min;
96.步骤二中所述的升温的速率为5℃/min;
97.三、将瓷舟中的尖晶石铁氧体/碳复合材料初始产品取出,对尖晶石铁氧体/碳复合材料初始产品进行离心清洗,得到高纯度的znfe2o4/c复合材料;
98.步骤三中所述的离心清洗的速度为3500r/min,离心清洗的时间为8min;
99.步骤三中所述的离心清洗的次数为4次,离心清洗使用的溶剂为己烷;
100.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的比饱和磁化强度为21emu/g;
101.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料中尖晶石铁氧体直径为10nm~20nm;
102.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的最佳反射率为:-18db。
103.实施例4:高纯度的cufe2o4/c复合材料的制备方法是按以下步骤完成的:
104.一、制备前驱体:
105.将有机金属盐和有机碳源溶解到低挥发类溶剂中,在70℃和搅拌速度为600r/min的条件下磁力搅拌至低挥发性溶剂挥发完,得到前驱体;
106.步骤一中所述的有机金属盐为硬脂酸铁和硬脂酸铜的混合物,其中硬脂酸铁与硬脂酸铜的摩尔比为2:1;
107.步骤一中所述的低挥发类溶剂为丙酮;
108.步骤一中所述的有机碳源为硬脂酸;
109.步骤一中所述的前驱体中有机金属盐与有机碳源的摩尔比为1:0.3;
110.步骤一中所述的前驱体中有机金属盐与有机碳源的总质量与低挥发类溶剂的质量比为1:7;
111.二、煅烧:将前驱体放入瓷舟中,并置于管式加热炉中,在通入气体的条件下升温至450℃,在450℃下煅烧3h,再降至室温,得到尖晶石铁氧体/碳复合材料初始产品;
112.步骤二中所述气体为氮气;
113.步骤二中所述气体的流速为3l/min;
114.步骤二中所述的升温的速率为5℃/min;
115.三、将瓷舟中的尖晶石铁氧体/碳复合材料初始产品取出,对尖晶石铁氧体/碳复合材料初始产品进行离心清洗,得到高纯度的cufe2o4/c复合材料;
116.步骤三中所述的离心清洗的速度为2500r/min,离心清洗的时间为10min;
117.步骤三中所述的离心清洗的次数为5次,离心清洗使用的溶剂为去离子水;
118.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的比饱和磁化强度为23emu/g;
119.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料中尖晶石铁氧体直径为10nm~20nm;
120.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的最佳反射率为:-25db。
121.实施例5:高纯度的为cdfe2o4/c复合材料的制备方法是按以下步骤完成的:
122.一、制备前驱体:
123.将有机金属盐和有机碳源溶解到低挥发类溶剂中,在60℃和搅拌速度为600r/min的条件下磁力搅拌至低挥发性溶剂挥发完,得到前驱体;
124.步骤一中所述的有机金属盐为硬脂酸铁和硬脂酸铬的混合物,其中硬脂酸铁与硬脂酸铬的摩尔比为2:1;
125.步骤一中所述的低挥发类溶剂为无水乙醇;
126.步骤一中所述的有机碳源为离子交换树脂;
127.步骤一中所述的前驱体中有机金属盐与有机碳源的摩尔比为1:0.7;
128.步骤一中所述的前驱体中有机金属盐与有机碳源的总质量与低挥发类溶剂的质量比为1:1;
129.二、煅烧:将前驱体放入瓷舟中,并置于管式加热炉中,在通入气体的条件下升温至550℃,在550℃下煅烧2h,再降至室温,得到尖晶石铁氧体/碳复合材料初始产品;
130.步骤二中所述气体为空气;
131.步骤二中所述气体的流速为4l/min;
132.步骤二中所述的升温的速率为5℃/min;
133.三、将瓷舟中的尖晶石铁氧体/碳复合材料初始产品取出,对尖晶石铁氧体/碳复合材料初始产品进行离心清洗,得到高纯度的为cdfe2o4/c复合材料;
134.步骤三中所述的离心清洗的速度为3000r/min,离心清洗的时间为9min;
135.步骤三中所述的离心清洗的次数为6次,离心清洗使用的溶剂为无水乙醇;
136.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的比饱和磁化强度为24emu/g;
137.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料中尖晶石铁氧体直径为30nm~40nm;
138.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的最佳反射率为:-28db。
139.实施例6:高纯度的bafe2o4/c复合材料的制备方法是按以下步骤完成的:
140.一、制备前驱体:
141.将有机金属盐和有机碳源溶解到低挥发类溶剂中,在70℃和搅拌速度为600r/min的条件下磁力搅拌至低挥发性溶剂挥发完,得到前驱体;
142.步骤一中所述的有机金属盐为硬脂酸铁和硬脂酸钡的混合物,其中硬脂酸铁与硬脂酸钡的摩尔比为2:1;
143.步骤一中所述的低挥发类溶剂为乙醚;
144.步骤一中所述的有机碳源为硬脂酸;
145.步骤一中所述的前驱体中有机金属盐与有机碳源的摩尔比为1:0.9;
146.步骤一中所述的前驱体中有机金属盐与有机碳源的总质量与低挥发类溶剂的质量比为1:12;
147.二、煅烧:将前驱体放入瓷舟中,并置于管式加热炉中,在通入气体的条件下升温至550℃,在550℃下煅烧3h,再降至室温,得到尖晶石铁氧体/碳复合材料初始产品;
148.步骤二中所述气体为氧气;
149.步骤二中所述气体的流速为5l/min;
150.步骤二中所述的升温的速率为5℃/min;
151.三、将瓷舟中的尖晶石铁氧体/碳复合材料初始产品取出,对尖晶石铁氧体/碳复合材料初始产品进行离心清洗,得到高纯度的bafe2o4/c复合材料;
152.步骤三中所述的离心清洗的速度为2500r/min,离心清洗的时间为10min;
153.步骤三中所述的离心清洗的次数为6次,离心清洗使用的溶剂为无水乙醇;
154.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的比饱和磁化强度为30emu/g;
155.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料中尖晶石铁氧体直径为40nm~60nm;
156.步骤三中所述的高纯度的尖晶石铁氧体/碳复合材料的最佳反射率为:-31db。
157.对比实施例:本实施例与实施例2的区别为:步骤一中将无机金属盐和有机碳源加入到低挥发类溶剂中,在70℃和搅拌速度为500r/min的条件下磁力搅拌至低挥发性溶剂挥发完,得到前驱体;所述的无机金属盐为硝酸铁和硝酸锰的混合物,其中硝酸铁和硝酸锰的摩尔比为2:1,得到mnfe2o4/c复合材料。其它步骤及参数与实施例2均相同。
158.对比实施例制备的mnfe2o4/c复合材料的最佳反射率为:-12db。
159.图1为实施例1制备的fe3o4/c复合材料的xrd图;
160.从图1可以得出,产物在衍射角度等于30.5
°
,35.6
°
43.5
°
,57.4
°
,62.6
°
的衍射峰分别对应fe3o4(220)(311)(400)(511)(440)的结构晶面,与标准pdf卡片88-0315的衍射峰位置一致,说明成功制备出四氧化三铁。在26
°
附近对应的是碳材料(jcpds.41-1487)的(002)晶面峰。
161.图2为实施例2制备的mnfe2o4/c复合材料的xrd图;
162.通过图2谱可以得出,产物在衍射角度等于22.5
°
、30.1
°
,35.5
°
,41.2
°
,44.8
°
,52.2
°
,57.8
°
,62.3
°
的衍射峰分别对应mnfe2o4(111)(220)(311)(222)(400)(422)(511)(440)的结构晶面,与标准pdf卡片70-0319的衍射峰位置一致,说明本发明成功制备出mnfe2o4。在26
°
附近对应的是碳材料(jcpds.41-1487)的(002)晶面峰。
163.图3为实施例1制备fe3o4/c复合材料的透射电镜图;
164.从图3中可以看出,纳米fe3o4分布在碳材料表面或内部。尺寸分布在40nm~80nm。由于没有加入多余碳源,因此fe3o4分布密集。
165.图4为实施例2制备mnfe2o4/c复合材料的透射电镜图;
166.从图4中可以看出,纳米mnfe2o4分布在碳材料表面或内部。尺寸分布在20nm~50nm。由于加入多余碳源,因此mnfe2o4颗粒较少,由于加入锰源,制备的纳米颗粒尺寸较小,复合材料中的碳呈现多层薄结构。
167.为分析fe3o4/c样品的磁学性能,本发明使用振动样品磁强计(vsm)在室温下、最大磁场强度为20000oe的条件下测试了fe3o4/c的磁滞曲线,具体图像如图5。
168.图5为实施例1制备fe3o4/c复合材料的磁场强度与比饱和强度图;
169.从图5可以得出,fe3o4/c的比饱和磁化强度(ms)约为58emu/g,矫顽力与剩磁接近0,具有超顺磁性。呈现高比饱和磁化强度的原因是,复合材料中碳含量较少,以磁性四氧化三铁为主。
170.本发明为分析mnfe2o4/c样品的磁学性能,使用振动样品磁强计(vsm)在室温下、最大磁场强度为20000oe的条件下测试了mnfe2o4/c的磁滞曲线,具体图像如图6。
171.图6为实施例2制备mnfe2o4/c复合材料的磁场强度与比饱和强度图;
172.从图6可以得出,mnfe2o4/c的比饱和磁化强度值(ms)约为50emu/g,矫顽力与剩磁接近为0,具有超顺磁性。
173.图7为实施例1制备的fe3o4/c复合材料的电磁波吸收图;
174.图7为样品(实施例1制备的fe3o4/c复合材料含量在20%,其余80%是石蜡)时的反射率数据;由图7可知,不同厚度有不同频段的吸收最高值,在1-5mm厚度时均出现-10以下的反射率(90%以上的吸收率),并且在4mm厚度时的最佳反射率为-34db。由此得知可以通过调节其厚度来改变吸收频段,表明fe3o4/c复合材料在低含量的情况下可以达到很好的电磁波吸收效果。
175.图8为对比实施例制备的mnfe2o4/c复合材料的电磁波吸收图。
176.图8为样品(对比实施例制备的锰铁氧体/c复合材料含量在20%,其余80%是石蜡)时的反射率数据;由图8可知,不同厚度有不同频段的吸收最高值,只有在2mm和3mm厚度时均出现-10以下的反射率(90%以上的吸收率),并且在2mm厚度时的最佳反射率为-12db。由此得知对比实施例制备的锰铁氧体/c复合材料电磁波吸收性能不如实施方法1-6的效果,表明实施例7制备的对比实施例制备的锰铁氧体/c复合材料由于金属离子和有机体是混合烧制的原因,碳化过程中只是物理结合。而实施方法1-6中由于硬脂酸金属化合物中金属离子和硬脂酸至今是以化学键链接的,在制备过程中形成物理和化学链接,因此提高了界面极化作用而能提高电磁波吸收值。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1