一种季铵盐改性壳聚糖微球及其制备方法和应用与流程
本发明属于杀菌剂领域,具体涉及一种季铵盐改性壳聚糖微球及其制备方法和应用。
背景技术:
中国的水资源短缺已经敲响了警钟,更重要的是水安全的现状不容乐观。近几年来,饮用不合格水威胁人体健康的新闻层出不穷。这主要是由于人们以前饮用煮沸的凉开水,现在饮用桶装水。桶装水从制作到售卖要经过多道的工序和运输才能到达消费者手中。此过程虽然会经过严格把关,但难免会在某些环节出现纰漏造成污染。桶装水的污染大多是由细菌或其他微生物引起的中毒或感染。
目前,常见的灭菌剂包括氧化性灭菌剂、非氧化性灭菌剂、复合型灭菌剂、壳聚糖灭菌剂、固定化灭菌等等。其中氧化性灭菌剂具有灭菌力强、来源广泛、价格低廉等优点,是应用最广泛的灭菌剂。但是氧化性灭菌剂也有缺点:当水中有机物含量较高时,氯气灭菌将会产生氯代有机物质,稳定性欠佳,可致癌;运输贮藏成本高;处理工业水时,对菌垢作用能力差。非氧化性杀菌剂杀生作用持久性强、受水中环境ph值影响较小、对沉积物或黏泥有渗透、剥离作用。但费用却较高,并且容易引起污染,也会使水中的微生物产生抗药性。在水处理过程中,氧化性灭菌剂分解后会产生毒副产物,而非氧化性灭菌剂会有残留在水中无法降解,造成“二次污染”。复配型杀菌剂最主要的功能是使各组分复配比的协调作用达到最大。对于壳聚糖灭菌剂,分子量在8-10万的壳聚糖抗菌效果,防腐效果与山梨酸钾、苯甲酸钠相匹敌。但是该状态的杀菌剂会残留在水体中,不能被有效回收更不能循环使用,存在资源浪费的问题。
壳聚糖是以广泛存在于自然界的甲壳素为基料,经过化学反应脱乙酰制得的高分子材料,化学名称为β-(1,4)-2-氨基-2-脱氧-d-葡萄糖。一般而言,脱乙酰度(degreeofdeacetylation)大于50%或能溶于稀酸的脱乙酰基产物统称为壳聚糖。壳聚糖储量丰富、成本低廉、可生物降解、不易造成污染,本身具有良好的生物相容性,且无毒副作用。壳聚糖的游离氨基在一定环境下,氮原子带有1对孤对电子,使基团氨基表现出弱碱性。游离氨基基团能够与1个氢离子结合,从而使壳聚糖变成带有正电荷的线形的聚电解质。吸附在负电荷表面,同时由于壳聚糖的弱碱性,其表面会带有弱的正电荷。所以,壳聚糖是少数具有电荷性性质的天然产物,从而壳聚糖成为研究的热点。为了提高壳聚糖的抗菌能力,科研人员把研究重点放在对其结构的改性上。
壳聚糖因具有许多优良的特性,广泛应用化妆品、食品、化妆品、纺织、环保、农业、医药、电分析化学等领域。为了进一步拓展壳聚糖的应用范围,使壳聚糖分子改性,另活泼的氨基和羟基基团得以修饰,赋予壳聚糖更多的特殊功能是现在壳聚糖开发应用的热点领域。
因此,开发一种高效安全、使用方便、经济实惠,同时又能不破坏营养成分,无残留的杀菌剂成了提高水质的关键问题之一。
技术实现要素:
本发明的目的在于解决现有技术中存在的上述技术和成本问题,提供一种季铵盐改性壳聚糖微球及其制备方法和应用,以交联壳聚糖为母体,与氯化胆碱为配体进行合成反应,能够获得具有较高功能基转化率的季铵盐改性壳聚糖微球,该改性对饮用水具有良好的杀菌效果。
为解决上述技术难题,本发明采用以下技术方案:
一种季铵盐改性壳聚糖微球,具有如式(ⅰ)所示的结构:
式中,n=1,2,3…;
所述季铵盐改性壳聚糖微球以壳聚糖为原料,经交联后用氯化胆碱改性得到,壳聚糖的脱乙酰度为80%~95%;粘度为50~800mpa·s。
季铵盐改性壳聚糖微球易溶于水又有较强的抗菌活性。其配体中n+具有正电性,吸附带有负电荷的细菌,是细菌细胞壁和细胞膜上的负电荷分布不均,干扰细胞壁和细胞膜上的负电荷分布不均干扰细胞壁或者细胞膜的合成,最终使细菌溶解而死亡。
所述季铵盐改性壳聚糖微球的制备方法,包括:以具有如(ⅱ)所示结构的交联壳聚糖微球为母体,经充分溶胀后,加入结构如(ⅲ)所示的配体,调节体系ph,进行改性反应,反应完成后经洗涤、干燥得具有如式(ⅰ)所示结构的季铵盐改性壳聚糖微球;
式中,n=1,2,3…;
优选地,交联壳聚糖微球置于溶剂中充分溶胀,所述溶剂为1,4-二氧六环、dmf、dmso、水和甲苯中的至少一种。
溶剂对配体的转化率影响较大,主要原因有:(1)不同溶剂的极性不同,对母体溶胀性带来的影响也不同;(2)配体在溶剂中的溶解度和分散度不同,造成功能基转化率不同;(3)溶剂本身的物理性质产生的影响,如沸点等限制了溶剂的使用。作为优选,所述溶剂为1,4-二氧六环,在该溶剂中进行溶胀和反应,功能基转化率最高。
优选地,配体氯化胆碱的投加量为交联壳聚糖微球质量的2~6倍。交联壳聚糖是大分子物质,反应物质量比是影响微球功能基转化率的重要因素之一,随着配体投加比例的增加,功能基转化率先增加,然后转换率趋于平缓的趋势,进一步优选,配体氯化胆碱的投加量为母体质量的4~6倍,在该投加比例下,功能基转化率最高。
优选地,改性反应中,调节体系ph至7.5~8.5。
优选地,改性反应中,反应温度为50~90℃,在该温度范围内,随着温度的升高,功能基转化率先增加后趋于平缓。进一步优选,反应温度为70~90℃,由于反应溶剂对母体和配体溶解度产生影响,使得配体分子和母体活性位点之间的反应在此温度范围内很快达到饱和状态。
优选地,改性反应中,反应时间为6~10h。
所述洗涤包括依次用丙酮、无水乙醇和去离子水进行反复洗涤。
所述交联壳聚糖微球的制备包括:在壳聚糖中加入甲醛进行预交联反应,预交联反应后加入交联剂环氧氯丙烷进行交联反应,反应结束后经洗涤得具有如(iv)所示结构的交联壳聚糖微球中间体;交联壳聚糖微球中间体经活化后得交联壳聚糖微球;
式中,n=1,2,3…。
所述交联壳聚糖微球的制备方法具体包括以下步骤:
(1)将壳聚糖溶解在乙酸溶液中,加入液体石蜡和乳化剂,分散均匀后加入甲醛,使甲醛与壳聚糖c2上的氨基进行预交联反应,得混合液;
(2)调节步骤(1)的混合液至ph为9~10,加入环氧氯丙烷,通过反相悬浮交联法得交联壳聚糖微球中间体;
(3)将交联壳聚糖微球中间体用盐酸加热至60~80℃处理6~10h,洗涤至中性,得交联壳聚糖微球。
优选地,壳聚糖的脱乙酰度为80%~95%;粘度为50~800mpa·s。
步骤(1)中,乙酸溶液的质量分数为3~5%,每g壳聚糖中加入50~70ml乙酸溶液。
优选地,步骤(1)中,每g壳聚糖中加入液体石蜡150~250ml。
优选地,步骤(1)中,所述乳化剂为span80,每g壳聚糖中加入乳化剂0.1~0.3ml。
优选地,步骤(1)中,每g壳聚糖中加入甲醛2~5ml。
优选地,步骤(1)中,预交联反应的温度为50~80℃,反应时间为1~2h。
优选地,步骤(2)中,用质量分数为4~6%的naoh水溶液调节混合液的ph。
优选地,步骤(2)中,环氧氯丙烷的加入量以步骤(1)中壳聚糖的用量为基准,每g壳聚糖中加入环氧氯丙烷3~7ml。
优选地,步骤(2)中,反相悬浮交联法的温度为50~80℃,反应时间为4~6h。
本发明还提供了一种上述季铵盐改性壳聚糖微球作为灭菌剂在饮用水中的应用。
本发明季铵盐改性壳聚糖微球作为固定化灭菌剂,与可溶性杀菌剂相比,固定化灭菌剂因为空间立体原因导致与细菌细胞作用力减弱,进而造成灭菌效果下降,本发明通过引入强杀菌能力的功能基团,增强固体杀菌剂与细菌的作用效果。
与现有技术相比,本发明具有如下有益效果:
1、本发明的原材料壳聚糖储量丰富、成本低廉、可生物降解、不易造成污染,本身具有良好的生物相容性,且无毒副作用。并且壳聚糖是天然高分子材料,具有大量的氨基和羟基,c-2位上的氨基、c-3和c-6位上的羟基性质活泼,易于发生各种化学反应。
2、本发明制备的季铵盐改性壳聚糖微球可作为新型改性杀菌剂,通过引入具有优良的杀菌效果且带正电荷的季铵盐,来增强灭菌效果。
3、本发明提供的季铵盐改性壳聚糖微球可回收,可重复使用,能够提高资源的利用率,且原料价格便宜,能够多次使用并且可以有效降低“二次污染”,符合我国倡导的资源节约、可持续发展观念,有广阔的应用前景。
4、本发明在灭菌的同时负载一定量的银离子或铜离子,既能保证降低水中银、铜的含量又能提升灭菌微球的功能,用于回收环境中的银、铜离子,更好的提高了灭菌微球的附加值。
附图说明
图1为壳聚糖(ncts)、氯化胆碱(cc)、季铵盐改性壳聚糖微球(ccc)的红外光谱图;
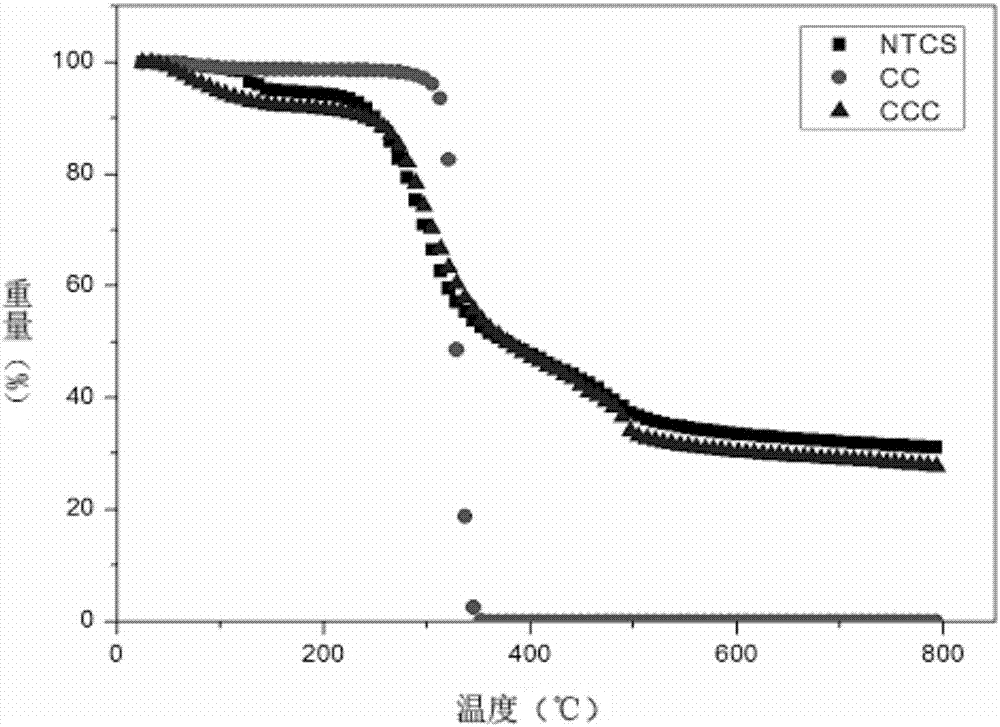
图2为交联壳聚糖微球(ncts)、氯化胆碱(cc)和季铵盐改性壳聚糖微球(ccc)的热重曲线;
图3为季铵盐改性壳聚糖微球(ccc)灭菌前后的扫描电镜图,其中,(a)为ccc灭菌前的扫描电镜图,3(b)为ccc灭菌后的扫描电镜图;
图4为实施例1制备的季铵盐改性壳聚糖微球对ag+、cu2+、大肠杆菌(e.coil)和金黄色葡萄球菌(s.aureus)的重复利用率。
具体实施方式
本发明中,计算功能基转化率(%)的方法如下:
通过百万分之一的天平准确称取1.000mg~2.000mg季铵盐改性壳聚糖微球,用锡箔纸包裹后依次放入托盘中等待样品分析。利用varioeliii型元素分析仪测定出季铵盐改性壳聚糖微球中的n元素的含量,并通过以下公式计算季铵盐改性壳聚糖微球中功能基转化率(functionalgroupconversion,%)。
上式中,x为功能基转化率,
f0为壳聚糖中氨基含量(mmol/g),
n0为壳聚糖的含氮量(%),
nc为季铵盐改性壳聚糖微球的含氮量(%),
ml为配体的摩尔质量(g/mol),
nn为配体分子中氮原子的数目。
下面结合附图和具体实施方式对本发明作进一步详细的说明。
实施例1
(1)将1.0g壳聚糖(cts)置于50ml质量分数为4%的乙酸溶液中,搅拌至溶解,以250r/min转动速率搅拌15min,加入200ml的液体石蜡,再搅拌10min后升温至50℃,滴加4滴乳化剂span80,乳化10min。
(2)在步骤(1)中加入2ml甲醛,50℃下反应1.5h,之后升温至70℃,滴加质量分数为10%的naoh水溶液,调节溶液ph值至9。之后缓慢地滴加4ml环氧氯丙烷,反应5h后,用蒸馏水洗涤,再依次用石油醚、无水乙醇洗涤,之后反复水洗至ph值达到中性。放于50℃的真空干燥器中干燥至恒重。
(3)将步骤(2)中已制得的交联壳聚糖微球用30ml1mol/l的盐酸水溶液加热至60℃处理9h。随后用碱洗,水洗至中性。将反应后的产物置于50℃真空干燥,干燥至恒重,得交联壳聚糖微球(ncts)。
(4)称取0.5g步骤(3)中制备的交联壳聚糖微球(ncts)悬浮于装有1,4-二氧六环的三颈瓶中使其充分溶胀,升高温度至70℃,再加入2.0g氯化胆碱(cc),调节反应体系为弱碱性,温度为70℃反应8h后,用丙酮、无水乙醇、去离子水反复洗涤,将产物放于50℃的真空干燥箱干燥至恒重。即得所述季铵盐改性壳聚糖微球(ccc)。
经检测,所得季铵盐改性壳聚糖微球的功能基转化率为44.2%。
所得季铵盐改性壳聚糖微球的红外谱图如图1所示,图中,ncts为步骤(3)中制备得到的交联壳聚糖微球,cc为配体氯化胆碱,ccc为季铵盐改性壳聚糖微球。1485cm-1是季铵盐分子中-ch2的特征吸收峰,1080cm-1是-ch2oh结构中c-o的特征峰。而在季铵盐改性壳聚糖微球的图谱中,母体中原1595cm-1处的氨基吸收峰消失了,但是出现了1465cm-1处新的吸收峰,这是由于氯化胆碱分子的引入,使得交联壳聚糖微球中出现了其特征峰。改性后的图谱中没有出现c-o的特征吸收峰,说明羟基参与了反应。同时,甲基和亚甲基峰明显增强。以上分析充分证明氯化胆碱已成功合成到交联壳聚糖微球。
所得季铵盐改性壳聚糖微球的热重曲线如图2所示,从图2可以看出,在0~250℃范围内,氯化胆碱cc的重量基本没有变化。但当温度在250~350℃时,cc开始急剧失重,重量损失非常明显,失重率为77.2%。350℃后,cc彻底分解。季铵盐改性壳聚糖微球的tga曲线与交联壳聚糖曲线相比,失重曲线极其相似,平衡后失重率不再发生变化,剩余的灰分和残渣约为28%。但ccc的分解温度偏高一些,这说明cc的引入能使微球自身的热稳定性有所提升。
实验1:
杀菌实验
本实验以革兰氏阴性代表细菌大肠杆菌(e.coli)cicc21524和革兰氏阳性代表细菌金黄色葡萄球菌(s.aureus)cicc10384作为受试菌,这两种菌种均由浙江工商大学食品质量与安全重点实验室提供。
具体实验操作步骤及评价方法如下:
所用菌株均作为储备培养物置于辅以15%(v/v)甘油的营养肉汤培养基中,保持于-20℃储存。然后将菌株接种于营养肉汤培养基(以下简称lb培养基)内,于37℃恒温振荡器中培养12h;待菌种活化后用移液枪取出一定量菌液,在4000rpm下进行离心洗涤。将所得菌斑用0.85%的生理盐水通过十倍稀释法稀释成浓度约为106cfu·ml-1的菌悬液备用。
杀菌活性测试
在250ml的锥形瓶中制备适当的菌悬液,并将其分为实验组与对照组。在实验组的锥形瓶中,加入已充分溶胀的ncts微球及季铵盐改性壳聚糖微球ccc。对照组不加灭菌微球,振荡使其混合均匀。在微球与受试菌充分接触一定时间后,按照gb/t4789.3-2010提供的方法,将上述各组上清液分别逐级地稀释,稀释到适宜浓度后,用移液枪吸取1ml上清液,置于琼脂培养基上,并用玻璃涂布棒涂匀,倒置平板并于37℃下培养,进行平板活菌计数。通过以下公式计算微球的杀菌率:
其中:b%表示杀菌率;m0为对照组活菌数;m1为实验组活菌数。
为提高杀菌率的准确性,杀菌率由同一时间点对照组和样品组取样进行平板计数后结果根据公式计算得到。
mic为最小抑菌浓度,是指抗菌药物能抑制培养基中细菌生长的最低浓度;mbc为最小杀菌浓度,指抗菌药物杀死99%以上的供试微生物所需要的最小浓度,即使活菌数量降低三个数量级。mic值与mbc值是杀菌剂抗菌活性的指标,显示了灭菌剂抑制杀死微生物的能力。
表1是交联壳聚糖微球ncts和季铵盐改性壳聚糖微球ccc对两种受试菌株的mic值与mbc值测试结果。
表1杀菌微球ccc对大肠杆菌和金黄色葡萄球菌的mic及mbc
实验结果显示,季铵盐改性壳聚糖微球杀菌性能优于改性前的交联壳聚糖微球,且较少的灭菌剂量就能达到理想的杀菌效果。ccc的灭菌作用可能是与两种受试菌表面的电负性有关,ccc带有正电荷,可和菌体静电吸附,破坏细胞膜,使细胞破裂死亡。
季铵盐改性壳聚糖微球ccc灭菌前后的扫描电镜图如图3所示,其中,图3(a)为ccc灭菌前的扫描电镜图,图3(b)为ccc灭菌后的扫描电镜图。由图可知,ccc灭菌前表面光滑且较为平整,说明功能基试剂的接入有助于改善微球的表面结构;微球灭菌后表面同样出现片状物质。这些片状物应为经ccc作用,细菌活细胞破裂,内容物流出后与细胞膜碎片共同覆于微球表面。更进一步证明灭菌微球ccc的灭菌机理是基于破坏活细胞完整性以达到杀死细菌的目的。
实验2:
灭菌微球对ag+、cu2+的吸附测试
准确称取15.0mg的季铵盐改性壳聚糖微球于100ml的碘量瓶中,再加入25.0mlph为5的hac-naac缓冲液充分溶胀后,分别加入浓度为3.0mg·ml-1的ag+、cu2+溶液5.0ml,常温下恒温振荡,转速为100rpm·min-1,待吸附达到平衡后,分别得负载银离子后的季铵盐改性壳聚糖微球ccc-ag+和负载铜离子后的季铵盐改性壳聚糖微球ccc-cu2+。
微球负载银、铜离子后对其杀菌效果会产生一定的影响。银、铜离子本身就具有杀菌效果,但负载离子后灭菌微球的活性功能基就会减少,这些变化都会对微球杀菌效果有影响,所以要进行负载微球的杀菌效果测试。
将负载银、铜离子后的季铵盐改性壳聚糖微球作为实验对象,按照实验1中的测试方法进行实验,观察每种微球的mic值与mbc值的变化,实验结果如表2所示。
表2负载ag+和cu2+的ccc对大肠杆菌和金黄色葡萄球菌的mic、mbc值
实验结果表明,吸附铜离子后的微球杀菌作用于金黄色葡萄球菌时,mbc值和mic值成4倍关系。说明作用于金黄色葡萄球菌灭菌微球数量的需求增加。这可能是因为吸附离子后,对细菌起作用的活性位点减少了,故而降低了杀菌效果。但ccc-ag+的大肠杆菌和金黄色葡萄球菌的mbc值与ccc的mbc值相比,数值更小,进一步说明该发明既能保证降低水中银的含量又能提升灭菌的效果。
实验3:
季铵盐改性壳聚糖微球的再生
将2mol/lhcl和etoh以1:3的体积混合制备再生洗脱液,对季铵盐改性壳聚糖微球进行再生,使微球功能基恢复原来的活性。对重生后的微球进行重复吸附和灭菌操作,测试微球的重复使用次数,结果如图4所示。
由图4可知,ccc对ag+重复吸附5次,其吸附率分别是99.69%、98.24%、97.51%、96.13%和95.27%。而对cu2+的吸附率依次为99.75%、98.26%、97.59%、96.27%及95.34%。很显然,5次的重复使用,离子吸附率都在95%以上。由此可认为洗脱5次对微球的损伤不大。
实验4:
季铵盐改性壳聚糖灭菌微球在自来水、桶装水中的应用
称取150mg季铵盐改性壳聚糖灭菌微球装入玻璃柱中,对其进行高压灭菌处理,然后将灭菌后的过滤柱放到超净工作台中备用。取自来水和放置7天后的桶装水各50ml,并在超净工作台中将其分别以正常速度流经灭菌柱,并快速取出1ml过滤后的水,进行涂布平板检测细菌。结果显示没有细菌出现,该结果证明灭菌微球具有良好的吸附杀菌能力。
实施例2
(1)将1.0g壳聚糖(cts)置于50ml质量分数为4%的乙酸溶液中,搅拌至溶解,以250r/min转动速率搅拌15min,加入200ml的液体石蜡,再搅拌10min后升温至50℃,滴加4滴乳化剂span80,乳化10min。
(2)在步骤(1)中加入2.0ml甲醛,50℃下反应1.5h,之后升温至60℃,滴加质量分数为10%的naoh水溶液,调节溶液ph值至9。之后缓慢地滴加4ml环氧氯丙烷,反应5h后,用蒸馏水洗涤,再依次用石油醚、无水乙醇洗涤,之后反复水洗至ph值达到中性。放于50℃的真空干燥器中干燥至恒重。
(3)将步骤(2)中已制得的交联壳聚糖微球用40ml1mol/l的盐酸水溶液加热至70℃处理9h。随后用碱洗,水洗至中性。将反应后的产物置于50℃真空干燥,干燥至恒重。
(4)称取0.5g步骤(3)中制备的交联壳聚糖微球(ncts)悬浮于装有n,n-二甲基甲酰胺的三颈瓶中使其充分溶胀,升高温度至60℃,再加入2.0g氯化胆碱(cc),调节反应体系为弱碱性,温度为60℃反应8h后,用丙酮、无水乙醇、去离子水反复洗涤,将产物放于50℃的真空干燥箱干燥至恒重。即得所述季铵盐改性壳聚糖微球(ccc)。
经检测,所得季铵盐改性壳聚糖微球的功能基转化率为25.16%。
实施例3
(1)将1.0g壳聚糖(cts)置于50ml质量分数为4%的乙酸溶液中,搅拌至溶解,以250r/min转动速率搅拌15min,加入150ml的液体石蜡,再搅拌10min后升温至50℃,滴加4滴乳化剂span80,乳化10min。
(2)在步骤(1)中加入3.0ml甲醛,在60℃下反应2h,之后升温至70℃,滴加质量分数为10%的naoh水溶液,调节溶液ph值至9。之后缓慢地滴加4ml环氧氯丙烷,反应5h后,用蒸馏水洗涤,再依次用石油醚、无水乙醇洗涤,之后反复水洗至ph值达到中性。放于50℃的真空干燥器中干燥至恒重。
(3)将步骤(2)中已制得的交联壳聚糖微球用40ml1mol/l的盐酸水溶液加热至70℃处理9h。随后用碱洗,水洗至中性。将反应后的产物置于50℃真空干燥,干燥至恒重。
(4)称取0.5g步骤(3)中制备的交联壳聚糖微球(ncts)悬浮于装有二甲亚砜的三颈瓶中使其充分溶胀,升高温度至50℃,再加入2.0g氯化胆碱(cc),调节反应体系为弱碱性,温度为50℃反应8h后,用丙酮、无水乙醇、去离子水反复洗涤,将产物放于50℃的真空干燥箱干燥至恒重。即得所述季铵盐改性壳聚糖微球(ccc)。
经检测,所得季铵盐改性壳聚糖微球的功能基转化率为15.66%。
实施例4
(1)将1.0g壳聚糖(cts)置于50ml质量分数为4%的乙酸溶液中,搅拌至溶解,以250r/min转动速率搅拌15min,加入250ml的液体石蜡,再搅拌10min后升温至50℃,滴加4滴乳化剂span80,乳化10min。
(2)在步骤(1)中加入4.0ml甲醛,在70℃下反应1h,之后升温至80℃,滴加质量分数为10%的naoh水溶液,调节溶液ph值至10。之后缓慢地滴加4ml环氧氯丙烷,反应4h后,用蒸馏水洗涤,再依次用石油醚、无水乙醇洗涤,之后反复水洗至ph值达到中性。放于50℃的真空干燥器中干燥至恒重。
(3)将步骤(2)中已制得的交联壳聚糖微球用30ml1mol/l的盐酸水溶液加热至80℃处理6h。随后用碱洗,水洗至中性。将反应后的产物置于50℃真空干燥,干燥至恒重。
(4)称取0.5g步骤(3)中制备的交联壳聚糖微球(ncts)悬浮于装有水的三颈瓶中使其充分溶胀,升高温度至60℃,再加2.0g氯化胆碱(cc),调节反应体系为弱碱性,温度为80℃反应8h后,用丙酮、无水乙醇、去离子水反复洗涤,将产物放于50℃的真空干燥箱干燥至恒重。即得所述季铵盐改性壳聚糖微球(ccc)。
经检测,所得季铵盐改性壳聚糖微球的功能基转化率为28.2%。
实施例5
(1)将1.0g壳聚糖(cts)置于50ml质量分数为4%的乙酸溶液中,搅拌至溶解,以250r/min转动速率搅拌15min,加入250ml的液体石蜡,再搅拌10min后升温至50℃,滴加4滴乳化剂span80,乳化10min。
(2)在步骤(1)中加入5ml甲醛,在50℃下反应2h,之后升温至70℃,滴加质量分数为10%的naoh水溶液,调节溶液ph值至10。之后缓慢地滴加4ml环氧氯丙烷,反应5h后,用蒸馏水洗涤,再依次用石油醚、无水乙醇洗涤,之后反复水洗至ph值达到中性。放于50℃的真空干燥器中干燥至恒重。
(3)将步骤(2)中已制得的交联壳聚糖微球用50ml1mol/l的盐酸水溶液加热至60℃处理10h。随后用碱洗,水洗至中性。将反应后的产物置于50℃真空干燥,干燥至恒重。
(4)称取0.5g步骤(3)中制备的交联壳聚糖微球(ncts)悬浮于装有甲苯的三颈瓶中使其充分溶胀,升高温度至50℃,再加入2.0g氯化胆碱(cc),调节反应体系为弱碱性,温度为70℃反应8h后,用丙酮、无水乙醇、去离子水反复洗涤,将产物放于50℃的真空干燥箱干燥至恒重。即得所述季铵盐改性壳聚糖微球(ccc)。
经检测,所得季铵盐改性壳聚糖微球的功能基转化率为11.33%。
实施例6
(1)将1.0g壳聚糖(cts)置于50ml质量分数为4%的乙酸溶液中,搅拌至溶解,以250r/min转动速率搅拌15min,加入200ml的液体石蜡,再搅拌10min后升温至50℃,滴加4滴乳化剂span80,乳化10min。
(2)在步骤(1)中加入2.0ml甲醛,在50℃下反应1.5h,之后升温至70℃,滴加质量分数为10%的naoh水溶液,调节溶液ph值至9。之后缓慢地滴加4ml环氧氯丙烷,反应5h后,用蒸馏水洗涤,再依次用石油醚、无水乙醇洗涤,之后反复水洗至ph值达到中性。放于50℃的真空干燥器中干燥至恒重。
(3)将步骤(2)中已制得的交联壳聚糖微球用30ml1mol/l的盐酸水溶液加热至70℃处理9h。随后用碱洗,水洗至中性。将反应后的产物置于50℃真空干燥,干燥至恒重。
(4)称取0.5g步骤(3)中制备的交联壳聚糖微球(ncts)悬浮于装有1,4-二氧六环的三颈瓶中使其充分溶胀,升高温度至70℃,再加入1.0g氯化胆碱(cc),调节反应体系为弱碱性,温度为70℃反应8h后,用丙酮、无水乙醇、去离子水反复洗涤,将产物放于50℃的真空干燥箱干燥至恒重。即得所述季铵盐改性壳聚糖微球(ccc)。
经检测,所得季铵盐改性壳聚糖微球的功能基转化率为15.8%。
实施例7
(1)将1.0g壳聚糖(cts)置于50ml质量分数为4%的乙酸溶液中,搅拌至溶解,以250r/min转动速率搅拌15min,加入200ml的液体石蜡,再搅拌10min后升温至50℃,滴加3滴乳化剂span80,乳化10min。
(2)在步骤(1)中加入2.0ml甲醛,在50℃下反应1.5h,之后升温至70℃,滴加质量分数为10%的naoh水溶液,调节溶液ph值至9。之后缓慢地滴加4ml环氧氯丙烷,反应5h后,用蒸馏水洗涤,再依次用石油醚、无水乙醇洗涤,之后反复水洗至ph值达到中性。放于50℃的真空干燥器中干燥至恒重。
(3)将步骤(2)中已制得的交联壳聚糖微球用30ml1mol/l的盐酸水溶液加热至70℃处理9h。随后用碱洗,水洗至中性。将反应后的产物置于50℃真空干燥,干燥至恒重。
(4)称取0.5g步骤(3)中制备的交联壳聚糖微球(ncts)悬浮于装有1,4-二氧六环的三颈瓶中使其充分溶胀,升高温度至70℃,再加入3.0g氯化胆碱(cc),调节反应体系为弱碱性,温度为70℃反应8h后,用丙酮、无水乙醇、去离子水反复洗涤,将产物放于50℃的真空干燥箱干燥至恒重。即得所述季铵盐改性壳聚糖微球(ccc)。
经检测,所得季铵盐改性壳聚糖微球的功能基转化率为44.8%。
实施例8
(1)将1.0g壳聚糖(cts)置于50ml质量分数为5%的乙酸溶液中,搅拌至溶解,以250r/min转动速率搅拌15min,加入200ml的液体石蜡,再搅拌10min后升温至50℃,滴加4滴乳化剂span80,乳化10min。
(2)在步骤(1)中加入4.0ml甲醛,在50℃下反应2h,之后升温至70℃,滴加质量分数为10%的naoh水溶液,调节溶液ph值至9。之后缓慢地滴加7ml环氧氯丙烷。反应6h后,用蒸馏水洗涤,再依次用石油醚、无水乙醇洗涤,之后反复水洗至ph值达到中性。放于50℃的真空干燥器中干燥至恒重。
(3)将步骤(2)中已制得的交联壳聚糖微球用40ml1mol/l的盐酸水溶液加热至70℃处理7h。随后用碱洗,水洗至中性。将反应后的产物置于50℃真空干燥,干燥至恒重。
(4)称取0.5g步骤(3)中制备的交联壳聚糖微球(ncts)悬浮于装有1,4-二氧六环的三颈瓶中使其充分溶胀,升高温度至5℃,再加入2.0g氯化胆碱(cc),调节反应体系为弱碱性,温度为50℃反应8h后,用丙酮、无水乙醇、去离子水反复洗涤,将产物放于50℃的真空干燥箱干燥至恒重。即得所述季铵盐改性壳聚糖微球(ccc)。
经检测,所得季铵盐改性壳聚糖微球的功能基转化率为17.1%。
实施例9
(1)将1.0g壳聚糖(cts)置于70ml质量分数为3%的乙酸溶液中,搅拌至溶解,以250r/min转动速率搅拌15min,加入250ml的液体石蜡,再搅拌10min后升温至70℃,滴加5滴乳化剂span80,乳化10min。
(2)在步骤(1)中加入2.5ml甲醛,在70℃下反应1.5h,之后升温至70℃,滴加质量分数为10%的naoh水溶液,调节溶液ph值至10。之后缓慢地滴加4ml环氧氯丙烷,反应5h后,用蒸馏水洗涤,再依次用石油醚、无水乙醇洗涤,之后反复水洗至ph值达到中性。放于50℃的真空干燥器中干燥至恒重。
(3)将步骤(2)中已制得的交联壳聚糖微球用30ml1mol/l的盐酸水溶液加热至80℃处理9h。随后用碱洗,水洗至中性。将反应后的产物置于50℃真空干燥,干燥至恒重。
(4)称取0.5g步骤(3)中制备的交联壳聚糖微球(ncts)悬浮于装有1,4-二氧六环的三颈瓶中使其充分溶胀,升高温度至90℃,再加入3.0g氯化胆碱(cc),调节反应体系为弱碱性,温度为90℃反应8h后,用丙酮、无水乙醇、去离子水反复洗涤,将产物放于50℃的真空干燥箱干燥至恒重。即得所述季铵盐改性壳聚糖微球(ccc)。
经检测,所得季铵盐改性壳聚糖微球的功能基转化率为45.1%。
- 还没有人留言评论。精彩留言会获得点赞!