紫檀茋用于抗真菌生物被膜药物的应用的制作方法
本发明涉及医药技术领域,是紫檀茋在抗真菌生物被膜中的新用途。
背景技术:
紫檀茋来源于是血竭制品中抗真菌活性成分,属多羟基二苯乙烯类化合物,为白藜芦醇的同系物,其结构如式(I)所示,类白色结晶状粉末,对空气敏感,熔点89~92°C,有着丰富的药用价值,对于癌症,高血压,高血脂的治疗都有一定的效果。北京大学中医药现代研究中心屠鹏飞等有关于紫檀茋抗真菌的报道,(胡迎庆,屠鹏飞,剑叶龙血树中茋类化合物及其抗真菌活性的研究,中草药,2001,32(2):104-105)。生物被膜是一个微生物聚集群体,是微生物不可逆地与无活力物体或活组织表面接触,由自身产生的细胞外基质包裹着活菌细胞形成的微生态,其具有高度耐药性的特异表型,是相对于单个分散游离状态真菌细胞而言的另一种独特的微生物生存方式。从患者体内取出的导管或生物装置表面可见真菌以生物被膜的形式黏附生长。对体外建立的真菌形成生物被膜的模型进行抗真菌药物敏感性实验时发现,菌株对常用药物均表现为高度耐药。因此,以生物被膜形式生长并表现出高度耐药性的体内导管或生物装置相关性真菌感染给临床治疗带来很大难度,迫使临床医师在进行抗真菌治疗的同时必须从患者体内取出导管或生物装置,从而影响到患者的预后。然而,现有技术中,具有抗真菌活性的药物往往不具备抗生物被膜活性,导致其被用于以生物被膜形式生长的真菌治疗时不能得到预期的效果。综上所述,本领域迫切需要一种具有抗生物被膜活性的药物组合物。
技术实现要素:
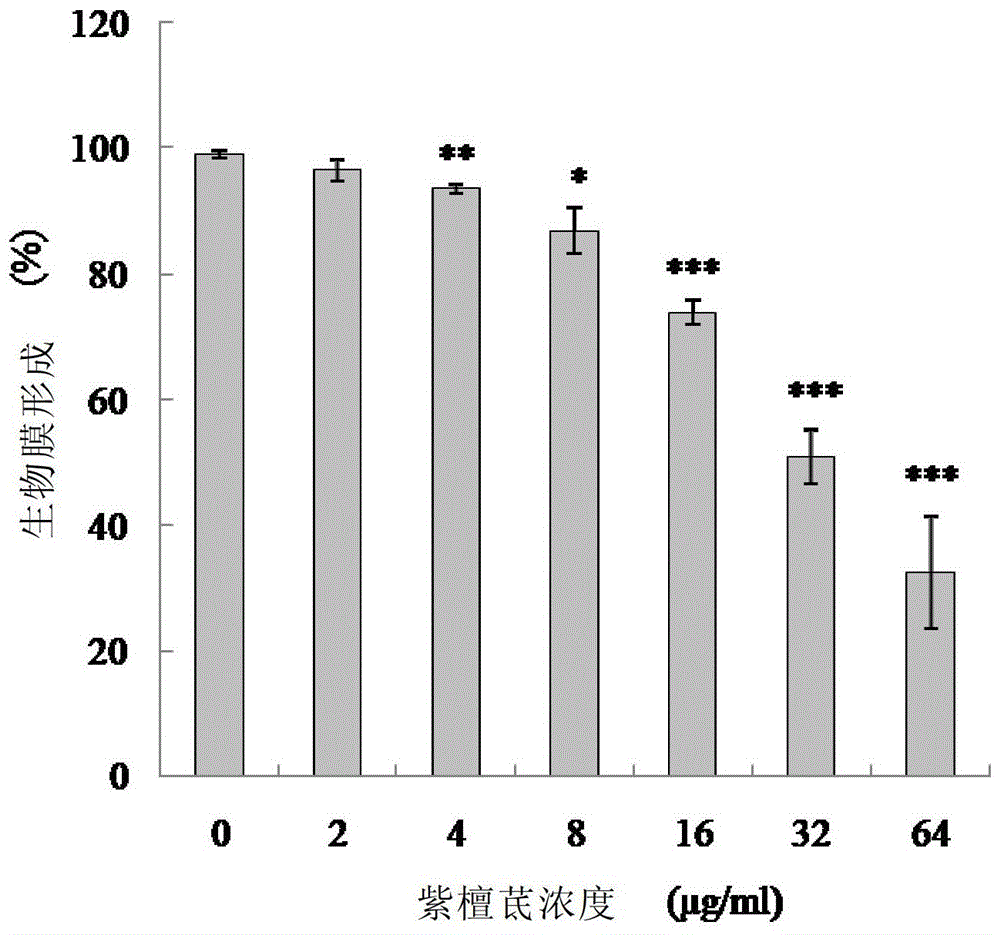
本发明的目的是提供一种紫檀茋用于抑制真菌生物被膜的用途。本发明的第一方面,提供了一种紫檀茋的用途,其特征在于,用于制备抗真菌生物被膜的药物或药物组合物。在另一优选例中,所述药物包括治疗有效量的紫檀茋。在另一优选例中,所述药物还可以包括其他具有抗真菌活性的药物组分。在另一优选例中,所述药物用于抑制真菌生物被膜的生长增殖,或用于抑制已形成的真菌生物被膜。在另一优选例中,所述紫檀茋为具有下式(I)结构的化合物,或其药学上可接受的盐:在另一优选例中,所述的盐选自下组:盐酸盐、硫酸盐、磷酸盐、醋酸盐等。在另一优选例中,所述的真菌选自下组:念珠菌、新型隐球菌、和/或曲霉菌。在另一优选例中,所述药物中紫檀茋的含量为0.1-99wt%,较佳地为0.5-90wt%。在另一优选例中,所述紫檀茋在抗念珠菌生物被膜药物中的有效浓度为≥16微克/毫升或微克/毫克;所述紫檀茋在抗新型隐球菌生物被膜药物中的有效浓度为≥32微克/毫升或微克/毫克;所述紫檀茋在在抗曲霉菌生物被膜药物中的有效浓度为≥32微克/毫升或微克/毫克。在另一优选例中,当所述念珠菌生物被膜为成熟生物被膜时,所述紫檀茋在药物中的有效浓度为≥32微克/毫升或微克/毫克。在另一优选例中,当所述新型隐球菌生物被膜为成熟生物被膜时,所述紫檀茋在药物中的有效浓度为≥64微克/毫升或微克/毫克。在另一优选例中,当所述曲霉菌生物被膜为成熟生物被膜时,所述紫檀茋在药物中的有效浓度为≥64微克/毫升或微克/毫克。在另一优选例中,所述药物为涂抹剂、乳剂、膏剂、气雾剂、膜剂。本发明的第二方面,提供了一种紫檀茋的用途,其特征在于,用于制备抗生物被膜的医疗器械或医用材料。在另一优选例中,所述医疗器械包括:医疗导管(如输液管、导尿管)、输氧面罩、鼻氧管、钳、敷料、护创材料、可吸收性止血/防粘连材料、手术用品(如医用的钳、钩、或针)、植入物等。在另一优选例中,所述医疗器械的制备方法包括:(1)提供一医疗器械;(2)将包含灭菌有效量紫檀茋的组合物涂覆于医疗器械上,形成抗生物被膜的医疗器械。在另一优选例中,所述抗生物被膜包括抑制真菌生物被膜的生长增殖(形成)或用于抑制(或破坏)已形成的真菌生物被膜。本发明的第三方面,提供了一种体外非治疗性抑制真菌生物被膜的方法,其特征在于,在需要抑制的场合,施用紫檀茋或其药学上可接受的盐,从而抑制真菌生物被膜。在另一优选例中,当待抑制的生物被膜是念珠菌生物被膜时,施用的紫檀茋的有效浓度为≥32微克/毫升或微克/毫克。在另一优选例中,当待抑制的生物被膜是隐球菌成熟生物被膜时,施用的紫檀茋的有效浓度为≥64微克/毫升或微克/毫克。在另一优选例中,当待抑制的生物被膜是曲霉菌成熟生物被膜时,施用的紫檀茋的有效浓度为≥64微克/毫升或微克/毫克。本发明的第四方面,提供了紫檀茋,化学结构通式如下:在另一优选例中,所述的紫檀茋在体外能有效抑制真菌生物被膜的生长增殖,且对已形成真菌生物被膜有很好的抑制作用。本发明的第五方面,提供了紫檀茋作为抗真菌生物被膜药物的用途,其特征在于,所述的真菌为念珠菌、新型隐球菌、曲霉菌。在另一优选例中,紫檀茋在抗念珠菌生物被膜的用途中有效浓度为32微克/毫升或微克/毫克、16微克/毫升或微克/毫克;或紫檀茋在在抗新型隐球菌生物被膜的用途中有效浓度为64微克/毫升或微克/毫克、32微克/毫升或微克/毫克;或紫檀茋在在抗曲霉菌生物被膜的用途中有效浓度为64微克/毫升或微克/毫克、32微克/毫升或微克/毫克。应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。附图说明图1为本发明实施例1中紫檀茋以0~32μg/ml浓度单独使用抑制白念珠菌SC5314生物被膜形成的效果。其中,横坐标为紫檀茋浓度(μg/ml),纵坐标为生物被膜形成率(%)。*代表P<0.05,**代表P<0.01,***代表P<0.001。图2为本发明实施例1中紫檀茋以0~64μg/ml浓度单独使用抑制白念珠菌SC5314成熟24h生物被膜的效果。其中,横坐标为紫檀茋浓度(μg/ml),纵坐标为生物被膜形成率(%)。*代表P<0.05,**代表P<0.01,***代表P<0.001。图3为本发明实施例4中实验标本的扫描电镜图。具体实施方式本发明人经过长期而深入的研究,意外地发现,化合物紫檀茋在低浓度下就能够表现出很好的抗生物被膜活性,因此可以非常有效地用于预防真菌形成生物被膜,或抑制和破坏已形成的生物被膜。基于上述发现,发明人完成了本发明。术语如本文所用,术语“紫檀茋”为具有如式(I)所示结构的化合物,及其药学上可接受的盐:其中,优选的代表性的盐包括(但并不限于):与有机酸或无机酸所形成的盐,例如盐酸盐、硫酸盐、磷酸盐、醋酸盐等。术语“抗真菌生物被膜”包括抑制真菌生物被膜的生长增殖(或形成)或用于抑制(或破坏)已形成的真菌生物被膜。菌株本发明提供了一种紫檀茋抑制真菌生物被膜的用途。其中,所述的真菌可以是任何具有被膜的真菌,较佳的例子包括(但并不限于):念珠菌、新型隐球菌、曲霉菌等。本发明的真菌可以位于生物体外,如需要灭菌的医疗器械内壁;也可以位于生物体内,其中,所述的生物包括(但并不限于):人、猫、狗、小鼠、大鼠、兔、豚鼠、猴等。在本发明中,所用的真菌可以通过常规方法取得或培养,也可以通过市售途径得到,如从患有相应疾病的患者的体细胞或组织中分离,或从任何市售标准菌株的机构或公司,如ATCC购买得到。应理解,在本发明的实施例中所使用的菌株样本仅为示范性的例子,任何可形成生物被膜的真菌均可以用于测试本发明化合物的抗生物被膜活性,而不受实施例范围的限制。真菌生物被膜生物被膜是微生物聚集群体,是微生物不可逆地与无活力物体或活组织表面接触,由自身产生的细胞外基质包裹着活菌细胞形成的微生态,其具有高度耐药性的特异表型,是相对于单个分散游离状态真菌细胞而言的另一种独特的微生物生存方式。从患者体内取出的导管或生物装置表面,可观察到真菌以生物被膜的形式黏附生长。对体外建立的真菌形成生物被膜的模型进行抗真菌药物敏感性实验时发现,菌株对常用药物均表现为高度耐药。因此,以生物被膜形式生长并表现出高度耐药性的体内导管或生物装置相关性真菌感染给临床治疗带来很大难度,迫使临床医师在进行抗真菌治疗的同时必须从患者体内取出导管或生物装置,从而影响到患者的预后。通常,真菌生物被膜对一般抗真菌药物高度耐药,目前大多数有抗真菌活性的物质并不具有抗生物被膜活性。例如,目前临床最广泛应用的抗真菌药物氟康唑对生物被膜完全没有抑制作用。此外,目前抗真菌作用最强的两性霉素B在常用浓度下对生物被膜没有抑制作用,仅在高浓度时对生物被膜有一定的抑制作用,而在此浓度下会导致受体严重的不良反应,因而几乎不可能被临床应用于抗生物被膜。抗真菌生物被膜活性本发明的紫檀茋作用于真菌,可以有效地起到抑制真菌生物被膜的生长增殖的作用,或起到破坏已形成的真菌生物被膜的作用。真菌在聚苯乙烯等材料表面形成生物被膜后,对多数抗真菌药耐药,氟康唑单用抗白念珠菌生物被膜的SMIC(SessileMinimumInhibitoryConcentration)值>1024μg/ml,两性霉素B单用抗白念珠菌生物被膜的SMIC值为0.25~4μg/ml,具有抗酵母相真菌活性的中药单体化合物大多无抗真菌生物被膜活性。经实验证明,紫檀茋在体外具有显著的抗真菌生物被膜活性,不仅能抑制真菌生物被膜的粘附、生长增殖,而且对已形成真菌生物被膜具有抑制作用,SMIC值为8μg/ml~64μg/ml。在本发明中,用于制备药物或药物组合物的紫檀茋需要达到一定的浓度,通常为≥16μg/ml(或μg/mg)。较佳地,在本发明的实施例中:所述紫檀茋在抗念珠菌生物被膜药物中的有效浓度为≥16μg/ml(或μg/mg);当所述念珠菌生物被膜为成熟生物被膜时,所述紫檀茋在药物中的有效浓度为≥32μg/ml(或μg/mg)。所述紫檀茋在抗新型隐球菌生物被膜药物中的有效浓度为≥32μg/ml(或μg/mg),当所述新型隐球菌生物被膜为成熟生物被膜时,所述紫檀茋在药物中的有效浓度为≥64μg/ml(或μg/mg);所述紫檀茋在在抗曲霉菌生物被膜药物中的有效浓度为≥32μg/ml(或μg/mg),当所述曲霉菌生物被膜为成熟生物被膜时,所述紫檀茋在药物中的有效浓度为≥64μg/ml(或μg/mg)。应理解,在本发明的实施例中,仅写明了有效抑制真菌生物被膜的生长时,活性成分的最低浓度。结合本领域的公知常识可知,当抗真菌的活性药物组分浓度增大时,所述的抗真菌效果会有一定的改善。因此,任何本领域的技术人员在阅读了本说明书后,通过结合本领域的公知常识,均可以采用高于所述的最低浓度的剂量来抑制真菌生物被膜生长,这种改变同样落于本发明的公开范围内。抗真菌生物被膜制品本发明提供的抗真菌生物被膜活性化合物可以直接应用于生物体,也可用于制备药物或药物组合物,以及需要抑制真菌的医疗器械。所述的药物或药物组合物可以是任何剂型,如汤剂、散剂、丸剂、酒剂、锭剂、胶剂、膏药、茶剂、曲剂、糕剂、露剂、棒剂、线剂、条剂、钉剂,灸熨剂,膏剂、丹剂、微型胶囊、静脉乳剂、脂质体制剂、气雾剂、前体药制剂、注射剂、合剂、口服安瓿剂、片剂、胶囊剂、滴丸剂、乳剂、软膏剂、橡胶硬膏、膜剂、海绵剂、离子透入剂、透皮吸收剂等;较佳地为涂抹剂,乳剂、膏剂、气雾剂、膜剂等剂型。所述的药物或药物组合物可直接用于生物体,也可制成涂覆剂而应用于各种需要抑制真菌的医疗器械中,如涂覆于医疗器械上以抑制真菌的活性。所述的医疗器械可以是任何需要抑制真菌的医疗器械,如外科手术器械、眼科手术器械、耳鼻喉科手术器械、口腔科设备、器具及手术器械、矫形外科(骨科)手术器械、妇产科用、计划生育手术器械、注射穿刺器械、烧伤(整形)科手术器械、普通诊察器械、临床检验分析仪器、医用化验和基础设备器具、体外循环及血液处理设备、植入材料、手术室、急救室、诊疗室设备及器具、病房护理设备及器具、消毒和灭菌设备及器具、医用冷疗、低温、冷藏设备及器具、口腔科材料、医用卫生材料及敷料、医用缝合材料及粘合剂、医用高分子材料及制品、介入器材等。在另一优选例中,所述的医疗器械包括(但并不限于):医疗导管(如输液管、导尿管)、输氧面罩、鼻氧管、钳、敷料、护创材料、可吸收性止血/防粘连材料、手术用品(如医用的钳、钩、或针)、植入物等。本发明的主要优点包括:(1)提供了一种有效的破坏真菌被膜的方法,本发明所用的化合物紫檀茋即使在低浓度下也能有效地抑制真菌被膜生长,或者抑制已成熟生物被膜,最低有效施用浓度仅为16μg/ml(或μg/mg),且不会导致受体产生不良反应。(2)提供了一种有效的抗真菌药物组合物,通过在药物组合物中加入紫檀茋,可以更加高效地杀灭真菌。下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。实施例1:紫檀茋单用对不同白念珠菌菌株生物被膜的作用材料和方法1、试药紫檀茋:由中科院广州化学有限公司提供。氟康唑:购自Sigma公司。两性霉素B:购自生工生物工程有限公司。XTT:购自Sigma公司。甲萘醌(menadione):购自Sigma公司。二甲亚砜(DMSO):中国医药(集团)上海化学试剂公司,用前重蒸。丙酮:购自Sigma公司。紫檀茋用二甲亚砜配成6.4mg/ml溶液,两性霉素B用二甲亚砜配成4mg/ml溶液,氟康唑用二甲亚砜配成102.4mg/ml溶液,受试药物于-20°C保存。实验前,将药物贮存液取出置35°C温箱融化,充分混匀,分别进行药效学实验。XTT用灭菌的PBS配成0.5mg/ml的饱和溶液,用0.22μm孔径的滤器滤过除菌,甲萘醌(menadione)用100%丙酮配成10mM溶液,XTT、甲萘醌(menadione)于-80°C保存。实验前,将药物贮存液取出置4°C冰箱、35°C温箱梯度融化,充分混匀,进行药效学实验。2、菌株ATCC标准株:白念珠菌(Candidaalbicans)SC5314(可购自ATCC)。临床株:白念珠菌(C.albicans)由长海医院真菌室提供,分别采自长海医院不同科室临床样本,并经形态学和生化学鉴定。所有实验用菌株均于沙堡葡萄糖琼脂培养基(SDA)划板活化,白念珠菌于35°C培养48h后,分别挑取单克隆再次划板活化,取第二次所得单克隆置SDA斜面,用上述方法培养后于4°C保存备用。3、培养液RPMI1640培养液:RPMI1640(GibcoBRL)10g,NaHCO32.0g,吗啡啉丙磺酸(morpholinepropanesulfonicacid,MOPS)(Sigma)34.5g(0.165M),加三蒸水900ml溶解,1NNaOH调pH至7.0(25°C),定容至1000ml,滤过除菌,4°C保存。沙堡葡萄糖琼脂培养基(SDA):蛋白胨10g,葡萄糖40g,琼脂18g,加三蒸水900ml溶解,加入2mg/ml氯霉素水溶液50ml,调整pH至7.0,定容至1000ml,高压灭菌后4°C保存。YEPD培养液:酵母浸膏10g,蛋白胨20g,葡萄糖20g,加三蒸水900ml溶解定容至1000ml,高压灭菌后4°C保存。4、仪器隔水式电热恒温培养箱(上海跃进医疗器械厂);THZ-82A台式恒温振荡器(上海跃进医疗器械厂);511型酶标分析仪(上海第三分析仪器厂);5、白念珠菌生物被膜制备实验前,用接种圈从4°C保存的SDA培养基上挑取白念珠菌少量,接种至1mlYEPD培养液,于30°C,200rpm振荡培养,活化16h,使真菌处于指数生长期后期。取该菌液至玻璃试管中,离心(3000g,5min,4°C),吸弃上清液,用1mlPBS吹打混匀,离心(3000g,5min,4°C),吸弃上清液,重复用PBS洗一次,用1mlRPMI1640培养液吹打混匀,用血细胞计数板计数,调整菌液浓度至106cells/ml,将菌液接种到96孔板1~11号孔,37°C恒温箱中静置培养90min或24h。6、抗白念珠菌生物被膜药敏板制备(1)抗白念珠菌生物被膜增殖药敏板制备取无菌96孔板,于每排11号孔加RPMI1640培养液150μl作阳性对照;2~10号孔各加RPMI1640培养液150μl;1号孔分别加RPMI1640培养液298.5μl和紫檀茋溶液1.5μl或RPMI1640培养液297μl和氟康唑溶液3μl或RPMI1640培养液298.8μl和两性霉素B溶液1.2μl。1~10号孔10级倍比稀释,使各孔的紫檀茋最终药物浓度分别为32、16、8、4、2、1、0.5、0.25、0.125和0.0625μg/ml,氟康唑最终药物浓度分别为1024、512、256、128、64、32、16、8、4和2μg/ml,两性霉素B最终药物浓度分别为16、8、4、2、1、0.5、0.25、0.125、0.0625和0.03125μg/ml,各孔中DMSO含量均低于1%;取出培养90min的生物被膜板,用PBS洗3次,取配好的含药物培养液100μl加入到被膜板对应的孔中,12号孔不培养生物被膜,作阴性对照。各药敏板于37°C培养。(2)抗白念珠菌成熟生物被膜药敏板制备24h之后,取无菌96孔板,于每排11号孔加RPMI1640培养液150μl作阳性对照;2~10号孔各加RPMI1640培养液150μl;1号孔分别加RPMI1640培养液297μl和紫檀茋溶液3μl或RPMI1640培养液297μl和氟康唑溶液3μl或RPMI1640培养液298.8μl和两性霉素B溶液1.2μl。1~10号孔10级倍比稀释,使各孔的紫檀茋最终药物浓度分别为64、32、16、8、4、2、1、0.5、0.25和0.125μg/ml,氟康唑最终药物浓度分别为1024、512、256、128、64、32、16、8、4和2μg/ml,两性霉素B最终药物浓度分别为16、8、4、2、1、0.5、0.25、0.125、0.0625和0.03125μg/ml,各孔中DMSO含量均低于1%;取出培养24h的生物被膜板,用PBS洗3次,取配好的含药物培养液100μl加入到被膜板对应的孔中,12号孔不培养生物被膜,作阴性对照。各药敏板于37°C培养。7、SMIC值判定白念珠菌于37°C培养24h后,取出生物被膜板,用PBS轻轻洗3次,每孔加入200μlXTT/menadione(12号孔也加),避光,37°C孵育2-3h,取出生物被膜板,吸取100μlXTT/menadione至无菌96孔板中,用酶标分析仪于492nm测各孔OD值。与阳性对照孔比,以OD值下降80%以上的最低浓度孔中的药物浓度为SMIC80(生物被膜生长80%被抑制时的药物浓度)。当药物的SMIC80值超过紫檀茋测定浓度范围时,按以下方法进行统计:SMIC80值高于最高浓度32或64μg/ml时,计为“>32或64μg/ml”;SMIC80值为最低浓度或在最低浓度以下时,不作区别,均计为“≤0.0625或0.125μg/ml”。上述实验均平行操作5到6次,当SMIC80值能准确重复或只差一个浓度时才被接受,并以较高浓度作为SMIC80值;当SMIC80值相差两个浓度以上时,则需重新实验,直到符合要求为止。实验结果见表1和表2。表1紫檀茋、两性霉素B与氟康唑单用对白念珠菌生物被膜增殖的抑制效果(PTE表示紫檀茋,AmB表示两性霉素B,FLu表示氟康唑,下同。)表2:紫檀茋单用对5株白念珠菌成熟生物被膜的抑制效果结论:表1、表2结果显示:紫檀茋对白念珠菌生物被膜单独用药使用,当紫檀茋的浓度为16、32μg/ml时,均表现出良好的抗白念珠菌生物被膜的增殖作用,当紫檀茋的浓度为32、64μg/ml时,均表现出良好的抗白念珠菌成熟生物被膜作用。实施例2:紫檀茋单用对不同新型隐球菌菌株生物被膜的作用材料和方法1、试药紫檀茋:由中科院广州化学有限公司提供。氟康唑:购自Sigma公司。两性霉素B:购自生工生物工程有限公司。XTT:购自Sigma公司。甲萘醌(menadione):购自Sigma公司。二甲亚砜(DMSO):中国医药(集团)上海化学试剂公司,用前重蒸。丙酮:购自Sigma公司。紫檀茋用二甲亚砜配成6.4mg/ml,两性霉素B用二甲亚砜配成4mg/ml,氟康唑用二甲亚砜配成102.4mg/ml,受试药物于-20°C保存。实验前,将药物贮存液取出置35°C温箱融化,充分混匀,分别进行药效学实验。XTT用灭菌的PBS配成0.5mg/ml的饱和溶液,用0.22μm孔径的滤器滤过除菌,甲萘醌(menadione)用100%丙酮配成10mM溶液,XTT、甲萘醌(menadione)于-80°C保存。实验前,将药物贮存液取出置4°C冰箱、35°C温箱梯度融化,充分混匀,进行药效学实验。2、菌株ATCC标准株:新型隐球菌(Cryptococcusneoformans)ATCC32609、ATCC56992(可购自ATCC)。临床株:新型隐球菌(C.neoformans)9406204、9701041、0208558均由上海长海医院真菌室提供,分别采自该医院不同科室临床样本,并经形态学和生化学鉴定。所有实验用菌株均于沙堡葡萄糖琼脂培养基(SDA)划板活化,新型隐球菌于35°C培养一周后,分别挑取单克隆再次划板活化,取第二次所得单克隆置SDA斜面,用上述方法培养后于4°C保存备用。3、培养液DMEM高糖培养基:购自Invitrogen公司。沙堡葡萄糖琼脂培养基(SDA):蛋白胨10g,葡萄糖40g,琼脂18g,加三蒸水900ml溶解,加入2mg/ml氯霉素水溶液50ml,调整pH至7.0,定容至1000ml,高压灭菌后4°C保存。YEPD培养液:酵母浸膏10g,蛋白胨20g,葡萄糖20g,加三蒸水900ml溶解定容至1000ml,高压灭菌后4°C保存。4、仪器隔水式电热恒温培养箱(上海跃进医疗器械厂);THZ-82A台式恒温振荡器(上海跃进医疗器械厂);511型酶标分析仪(上海第三分析仪器厂);5、新型隐球菌生物被膜制备实验前,用接种圈从4°C保存的SDA培养基上挑取新生隐球菌少量,接种至1mlYEPD培养液,于30°C,200rpm振荡培养,活化24h,使真菌处于指数生长期后期。取该菌液至玻璃试管中,离心(3000g,5min,4°C),吸弃上清液,用1mlPBS吹打混匀,离心(3000g,5min,4°C),吸弃上清液,重复用PBS洗一次,用1mlDMEM培养液吹打混匀,用血细胞计数板计数,调整菌液浓度至107cells/ml,将菌液接种到96孔板,37°C恒温箱中静置培养90min或24h。6、抗新型隐球菌生物被膜药敏板制备(1)抗新型隐球菌生物被膜增殖药敏板制备取无菌96孔板,于每排11号孔加DMEM培养液200μl作阳性对照;2~10号孔各加DMEM培养液150μl;1号孔分别加DMEM培养液298.5μl和紫檀茋溶液1.5μl或DMEM培养液297μl和氟康唑溶液3μl或DMEM培养液298.8μl和两性霉素B溶液1.2μl。1~10号孔10级倍比稀释,使各孔的紫檀茋最终药物浓度分别为32、16、8、4、2、1、0.5、0.25、0.125和0.625μg/ml,氟康唑最终药物浓度分别为1024、512、256、128、64、32、16、8、4和2μg/ml,两性霉素B最终药物浓度分别为16、8、4、2、1、0.5、0.25、0.125、0.0625和0.03125μg/ml,各孔中DMSO含量均低于1%;取出培养90min的生物被膜板,用PBS洗3次,取配好的含药物培养液200μl加入到被膜板对应的孔中,12号孔不培养生物被膜,作阴性对照。各药敏板于37°C培养。(2)抗白念珠菌成熟生物被膜药敏板制备24h之后,取无菌96孔板,于每排11号孔加DMEM培养液200μl作阳性对照;2~10号孔各加DMEM培养液150μl;1号孔分别加DMEM培养液297μl和紫檀茋溶液3μl或DMEM培养液297μl和氟康唑溶液3μl或DMEM培养液298.8μl和两性霉素B溶液1.2μl。1~10号孔10级倍比稀释,使各孔的紫檀茋最终药物浓度分别为64、32、16、8、4、2、1、0.5、0.25和0.125μg/ml,氟康唑最终药物浓度分别为1024、512、256、128、64、32、16、8、4和2μg/ml,两性霉素B最终药物浓度分别为16、8、4、2、1、0.5、0.25、0.125、0.0625和0.03125μg/ml,各孔中DMSO含量均低于1%;取出培养24h的生物被膜板,用PBS洗3次,取配好的含药物培养液200μl加入到被膜板对应的孔中,12号孔不培养生物被膜,作阴性对照。各药敏板于37°C培养。7、SMIC值判定新型隐球菌于37°C培养24h、48h、72h后,取出生物被膜板,用PBS轻轻洗3次,每孔加入200μlXTT/menadione(12号孔也加),避光,37°C孵育2-3h,取出生物被膜板,吸取100μlXTT/menadione至无菌96孔板中,用酶标分析仪于492nm测各孔OD值。与阳性对照孔比,以OD值下降80%以上的最低浓度孔中的药物浓度为SMIC80(生物被膜生长80%被抑制时的药物浓度)。当药物的SMIC80值超过紫檀茋测定浓度范围时,按以下方法进行统计:SMIC80值高于最高浓度32或64μg/ml时,计为“>32或64μg/ml”;SMIC80值为最低浓度或在最低浓度以下时,不作区别,均计为“≤0.0625或0.125μg/ml”。上述实验均平行操作5到6次,当SMIC80值能准确重复或只差一个浓度时才被接受,并以较高浓度作为SMIC80值;当SMIC80值相差两个浓度以上时,则需重新实验,直到符合要求为止。实验结果见表3。表3:紫檀茋单用对5株新型隐球菌菌株生物被膜生长增殖的SMIC80值表4:紫檀茋单用对5株新型隐球菌菌株成熟生物被膜的SMIC80值结论:表3、表4结果显示:紫檀茋对5株新型隐球菌菌株生物被膜的增殖、成熟生物被膜进行单独用药,当紫檀茋浓度为32μg/ml时,表现出良好的抗新型隐球菌生物被膜增殖作用,当紫檀茋浓度为64μg/ml时,表现出良好的抗新型隐球菌成熟生物被膜作用。实施例3:紫檀茋单用对不同曲霉菌菌株生物被膜的作用材料和方法1、试药紫檀茋:由中科院广州化学有限公司提供。氟康唑:购自Sigma公司。两性霉素B:购自生工生物工程有限公司。XTT:购自Sigma公司。甲萘醌(menadione):购自Sigma公司。二甲亚砜(DMSO):中国医药(集团)上海化学试剂公司,用前重蒸。丙酮:购自Sigma公司。紫檀茋用二甲亚砜配成6.4mg/ml,两性霉素B用二甲亚砜配成4mg/ml,氟康唑用二甲亚砜配成102.4mg/ml,受试药物于-20°C保存。实验前,将药物贮存液取出置35°C温箱融化,充分混匀,分别进行药效学实验。XTT用灭菌的PBS配成0.5mg/ml的饱和溶液,用0.22μm孔径的滤器滤过除菌,甲萘醌(menadione)用100%丙酮配成10mM溶液,XTT、甲萘醌(menadione)于-80°C保存。实验前,将药物贮存液取出置4°C冰箱、35°C温箱梯度融化,充分混匀,进行药效学实验。2、菌株临床株:烟曲霉菌(Aspergillusfumigatus)7544、060796、YQA、YQB均由上海长海医院真菌室提供,分别采自该医院不同科室临床样本,并经形态学和生化学鉴定。3、培养液RPMI1640培养液:RPMI1640(GibcoBRL)10g,NaHCO32.0g,吗啡啉丙磺酸(morpholinepropanesulfonicacid,MOPS)(Sigma)34.5g(0.165M),加三蒸水900ml溶解,1NNaOH调pH至7.0(25°C),定容至1000ml,滤过除菌,4°C保存。沙堡葡萄糖琼脂培养基(SDA):蛋白胨10g,葡萄糖40g,琼脂18g,加三蒸水900ml溶解,加入2mg/ml氯霉素水溶液50ml,调整pH至7.0,定容至1000ml,高压灭菌后4°C保存。YEPD培养液:酵母浸膏10g,蛋白胨20g,葡萄糖20g,加三蒸水900ml溶解定容至1000ml,高压灭菌后4°C保存。4、仪器隔水式电热恒温培养箱(上海跃进医疗器械厂);THZ-82A台式恒温振荡器(上海跃进医疗器械厂);511型酶标分析仪(上海第三分析仪器厂);5、烟曲霉菌生物被膜制备将烟曲霉菌菌接种至SDA斜面,35°C,培养一周。按本方法活化两次后,加适量RPMI1640培养液于SDA斜面,用吸管吹打菌落,使烟曲霉菌菌孢子游离于RPMI1640培养液中,然后经四层无菌纱布过滤。培养液经血细胞计数板计数后,加RPMI1640培养液调整孢子浓度至105cells/ml,将菌液接种到96孔板,37°C恒温箱中静置培养90min或24h。6、抗烟曲霉菌生物被膜药敏板制备(1)抗烟曲霉菌生物被膜增殖药敏板制备取无菌96孔板,于每排11号孔加RPMI1640培养液200μl作阳性对照;2~10号孔各加菌液150μl;1号孔分别加RPMI1640培养液298.5μl和紫檀茋溶液1.5μl或RPMI1640培养液297μl和氟康唑溶液3μl或RPMI1640培养液298.8μl和两性霉素B溶液1.2μl。1~10号孔10级倍比稀释,使各孔的紫檀茋最终药物浓度分别为32、16、8、4、2、1、0.5、0.25、0.125和0.0625μg/ml,氟康唑最终药物浓度分别为1024、512、256、128、64、32、16、8、4和2μg/ml,两性霉素B最终药物浓度分别为16、8、4、2、1、0.5、0.25、0.125、0.0625和0.03125μg/ml,各孔中DMSO含量均低于1%;取出培养90min的生物被膜板,用PBS洗3次,取配好的含药物培养液200μl加入到被膜板对应的孔中,12号孔不含药物,作阴性对照。各药敏板于37°C培养。(2)抗烟曲霉菌成熟生物被膜药敏板制备24h之后,取无菌96孔板,于每排11号孔加RPMI1640培养液200μl作阳性对照;2~10号孔各加菌液150μl;1号孔分别加RPMI1640培养液297μl和紫檀茋溶液3μl或RPMI1640培养液297μl和氟康唑溶液3μl或RPMI1640培养液298.8μl和两性霉素B溶液1.2μl。1~10号孔10级倍比稀释,使各孔的紫檀茋最终药物浓度分别为64、32、16、8、4、2、1、0.5、0.25和0.125μg/ml,氟康唑最终药物浓度分别为1024、512、256、128、64、32、16、8、4和2μg/ml,两性霉素B最终药物浓度分别为16、8、4、2、1、0.5、0.25、0.125、0.0625和0.03125μg/ml,各孔中DMSO含量均低于1%;取出培养24h的生物被膜板,用PBS洗3次,取配好的含药物培养液200μl加入到被膜板对应的孔中,12号孔不含药物,作阴性对照。各药敏板于37°C培养。7、SMIC值判定烟曲霉菌于37°C培养24h、48h后,取出生物被膜板,用PBS轻轻洗3次,每孔加入200μlXTT/menadione(12号孔也加),避光,37°C孵育2-3h,取出生物被膜板,吸取100μlXTT/menadione至无菌96孔板中,用酶标分析仪于492nm测各孔OD值。与阳性对照孔比,以OD值下降80%以上的最低浓度孔中的药物浓度为SMIC80(生物被膜生长80%被抑制时的药物浓度)。当药物的SMIC80值超过紫檀茋测定浓度范围时,按以下方法进行统计:SMIC80值高于最高浓度32、64μg/ml时,计为“>32、64μg/ml”;SMIC80值为最低浓度或在最低浓度以下时,不作区别,均计为“≤0.0625、0.125μg/ml”。上述实验均平行操作5到6次,当SMIC80值能准确重复或只差一个浓度时才被接受,并以较高浓度作为SMIC80值;当SMIC80值相差两个浓度以上时,则需重新实验,直到符合要求为止。实验结果见表5、表6。表5:紫檀茋单用对4株烟曲霉菌菌株生物被膜生长增殖的SMIC80值表6:紫檀茋单用对4株烟曲霉菌菌株成熟生物被膜的SMIC80值结论:表5、表6结果显示:紫檀茋对烟曲霉菌生物被膜的增殖、成熟生物被膜进行单独用药,当紫檀茋浓度为32μg/ml时,表现出良好的抗烟曲霉菌生物被膜增殖作用,当紫檀茋浓度为64μg/ml时,表现出良好的抗烟曲霉菌成熟生物被膜作用。实施例4紫檀茋单用对体内白念珠菌菌株生物被膜的作用材料和方法1、试药及实验动物、材料紫檀茋:由中科院广州化学有限公司提供。雌性SD大鼠:上海斯莱克实验动物有限责任公司。PE90聚乙烯导管:购自SmithsMedical公司。羟丙基β环糊精:购自Sigma公司。肝素:购自Sigma公司。紫檀茋用生理盐水溶解,并加入羟丙基β环糊精助融,受试药物于-20°C保存。实验前,将药物贮存液取出置35°C温箱融化,充分混匀,分别进行药效学实验。肝素用生理盐水溶解至100U/ml。聚乙烯导管灭菌后用肝素化生理盐水充盈。2、菌株ATCC标准株:白念珠菌(Candidaalbicans)SC5314由WilliamA.Fonzi(DepartmentofMicrobiologyandImmunology,GeorgetownUniversity,Washington,DC)赠送。实验用菌株均于沙堡葡萄糖琼脂培养基(SDA)划板活化,白念珠菌于35°C培养48h后,分别挑取单克隆再次划板活化,取第二次所得单克隆置SDA斜面,用上述方法培养后于4°C保存备用。3、仪器隔水式电热恒温培养箱(上海跃进医疗器械厂);THZ-82A台式恒温振荡器(上海跃进医疗器械厂);扫描电镜:XL—30环境扫描电子显微镜(荷兰飞利浦公司生产)干燥仪:CPD030(德国徕卡)溅射仪:LDM150D(上海电子光学技术研究所)4、聚乙烯导管植入大鼠体内:安定氯胺酮和地西泮以1:1混合,大鼠腹腔注射(0.2ml/100g)以麻醉大鼠。大鼠的肩胛骨,前胸和颈部剃毛。大鼠置于仰卧位。手术区域进行无菌处理(碘伏擦拭,然后75%乙醇脱碘)。在前颈部中线右侧剪开一个纵形切口约1.5cm。剥离出颈内静脉(约1mm直径),用静脉剪(尖头)在血管壁上剪一个纵形切口。PE90聚乙烯导管(肝素化生理盐水填充,导管另一侧用回形针针头封管。)小心插入血管近心端约2cm。用缝合线结扎,同时导管另一端绕过颈部置于背颈部,穿过小口,置于皮肤外侧。先用缝合线结扎。待大鼠苏醒后放入鼠笼饲养。5、菌液准备菌株SC5314于YPD培养基中30℃培养16h,后稀释于肝素化生理盐水中,计数,调整菌浓度至1×106cells/ml,预热至35℃。6、白念珠菌感染大鼠导管植入大鼠体内24h之后,拔去封导管用的回形针针头,减去上面部分已变形的导管,后将导管先用肝素化生理盐水冲管,以确保管子通畅后可回抽血液以确定。后将菌液注入导管至500ul(充满整个导管)。再次用回形针封管。7、给药菌液感染4h之后,用肝素化的生理盐水溶解的药液35℃预热,充满导管,方法同上。8、检测样品制备在给药后72h将大鼠二氧化碳窒息处死,将导管无菌条件下取出,用1ml生理盐水冲洗。末端2cm被剪下,置于1ml生理盐水中。纵向剪5mm分成两半,样品放到2%的戊二醛里浸2小时,扫描电镜检测。9、结果检测样品放到2%的戊二醛里浸2小时后,再用二甲砷酸钠洗涤二次,再用1%的锇酸浸2小时,接下来用30%、50%、70%、90%、100%的酒精进行梯度脱水,再用中间液置换后,再把标本放到临界点干燥仪进行干燥,然后把干燥好的标本用双面胶贴到专用样品台上。最后把样品台放到离子溅射仪里进行表面镀金处理。接下来就可以把样品台(台上有标本)放到扫描电镜里进行观察,结果如图3所示。结论:结果显示:紫檀茋对体内白念珠菌生物被膜单独用药表现出良好的抗白念珠菌生物被膜的作用。在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 卷柏素类化合物在作为抗真菌药物增效剂中的应用的制作方法与工艺
- 一种抗细菌兼抗真菌作用的十一烯酸接枝多聚赖氨酸轭合物胶束制剂及制备方法与流程
- 一种抗真菌药物泊沙康唑的固体分散体及制备方法与应用与流程
- Ternatusine A在制备抗人体真菌药物中的应用的制作方法与工艺
- 白薇作为抗真菌类药物的新用途的制作方法与工艺
- 一种抗真菌增效药物体内筛选方法与流程
- 一种抗真菌感染的药物组合物及其制备方法、制剂与应用与流程
- 由杂环衍生物取代的抗真菌5,6‑二氢‑4H‑吡咯并[1,2‑a][1,4]苯并‑二氮杂*类及6H‑吡咯并[1,2‑a][1,4]苯并二氮杂*类的制作方法与工艺
- 包含抗真菌剂和甾类化合物的药物组合物的制作方法与工艺
- 一种具有协同抗耐药真菌的药物组合物、制备方法以及应用与流程