营养组合物及在制备治疗再生障碍性贫血药物中的应用的制作方法
本发明涉及生命科学领域预防医学与治疗医学,尤其是一种营养组合物及在制备治疗再生障碍性贫血药物中的应用。
背景技术:
再生障碍性贫血(再障)是一组由化学物质、生物因素、放射线或不明原因引起的骨髓造血功能衰竭,以造血干细胞损伤、骨髓脂肪化、外周血全血细胞减少为特征的疾病。再障发病机制极为复杂,目前认为与以下几方面有关:
(1)造血干细胞内在增殖缺陷
①再障骨髓中造血干细胞明显减少,造血干细胞集落形成能力显著降低,异常造血干细胞可抑制正常造血干细胞功能;
②SAA患者(重型再障)DNA修复能力明显降低,用抗淋巴细胞球蛋白(ALG)治疗后仍不能纠正;
③部分经免疫抑制剂治疗有效的病例,在长期随访过程中演变为克隆性疾病;
④再障患者体内均有一定数量的补体敏感细胞,体外实验也证明再障造血干/祖细胞对补体敏感性增强。
(2)异常免疫反应损伤造血干细胞
再障患者经免疫抑制治疗后其自身造血功能可能得到改善,此为异常免疫反应损伤造血干细胞最直接的证据。
(3)造血微环境支持功能缺陷
造血微环境包括基质细胞及其分泌的细胞因子,起支持造血细胞增殖及促进各种细胞生长发育的作用。虽然造血微环境不是引起AA的始因,但可加重病情。
(4)遗传倾向
再障常有HLA-DR2型抗原连锁倾向,儿童再障HLA-DPW3型抗原显著增高,患者家属中常有造血祖细胞增殖能力明显降低,并可见家族性再障。
再障严重危害人体健康,中国医学科学院血液学研究所(1985)分析住院再障患者392例,随访时间1~26年,病死率为42.6%,其中急性再障为91.6%,慢性再障为24.6%,再障的预后与治疗方法密切相关。
中国专利号专利号为200710012788.8的中国发明专利公开了一种“促进造血干细胞增殖与血红蛋白合成的营养组合物”。该营养组合物的原料及重量比如下:核苷酸90~110、精氨酸20~30、赖氨酸20~30、半胱氨酸10~20、甘氨酸25~35、组氨酸20~30、卵磷脂110~130、脑磷脂50~70、维生素E 0.4~0.6、维生素C 5~7、叶酸0.02~0.04、维生素B2 0.05~0.07、维生素B6 0.07~0.08、维生素B12 0.0001~0.0002、铁0.5~1.5、锌0.5~0.7、锰0.4~0.6、枸杞多糖14~16、葡萄籽提取物14~16。可明显提高血中血红蛋白(Hb)、红细胞(RBC)、白细胞(WBC)及血小板(Plt)数量;可刺激骨髓造血干细胞的增殖,使造血干细胞明显增多;明显提高细胞内线粒体数目;对肝、脾的损伤具有明显的恢复作用。专利号为201010129033.8的中国发明专利公开了该营养组合物作为药物可为错配修复基因损伤的恢复提供基本营养条件,从而达到恢复错配修复基因损伤的目的。专利号为201010129027.2的中国发明专利公开了上述营养组合物可对线粒体损伤的恢复提供基本营养条件,进而充分发挥机体对线粒体损伤的自主修复本能,达到恢复线粒体损伤的目的,但是仅局限于对肝脏、脾脏的线粒体增值及修复。专利号为201010129030.4的中国发明专利还公开了该营养组合物可促进肝脏干细胞增殖。尽管上述营养组合物具有所述的功能,但是由于作用的局限性,该营养组合物仅适用于治疗营养不良性贫血(缺铁性贫血及叶酸与维生素B12营养不良性贫血)、红细胞生成减少所致贫血以及红细胞破坏过多或丢失所致贫血,而不能够作为治疗再生障碍性贫血的药物。
技术实现要素:
本发明是为了解决现有技术所存在的上述技术问题,提供一种营养组合物及在制备治疗获得性再生障碍性贫血药物中的应用,
本发明的技术解决方案是:一种营养组合物,其特征在于各组分质量比如下:赖氨酸200~1200、甲硫氨酸100~1600、苯丙氨酸150~1400、苏氨酸50~600、色氨酸50~400、精氨酸200~1500、组氨酸100~1000、甘氨酸100~600、天冬氨酸100~600、亮氨酸100~600、异亮氨酸100~600、缬氨酸100~800、丝氨酸100~400、谷氨酰胺200~600、牛磺酸100~500、乳清酸100~300、核苷酸200~1200、维生素A 0.2~0.6、维生素D 0.002~0.006、维生素B2 1~4、维生素B6 1~4、维生素B12 0.001~0.006、烟酸 5~20、叶酸0.01~1.2、维生素C 50~150、铁2~10、锌2~10、锰2~10、铜 0.5~2、硒0.01~0.1、铬0.01~0.02、钾10~300、钙100~300、镁100~200、肌醇50~60、大豆磷脂100~2500。
各组分最佳质量比如下:赖氨酸600、甲硫氨酸800、苯丙氨酸700、苏氨酸300、色氨酸200、精氨酸760、组氨酸500、甘氨酸300、天冬氨酸300、亮氨酸300、异亮氨酸300、缬氨酸400、丝氨酸200、谷氨酰胺300、牛磺酸500、乳清酸300、核苷酸400、维生素A 0.6、维生素D0.006、维生素B22、维生素B62、维生素B12 0.004、烟酸12、叶酸0.9、维生素C100、铁10、锌10、锰 8、铜2、硒0.1、铬 0.02、钾 300、钙300、镁 200、肌醇60、大豆磷脂1200。
上述营养组合物在制备治疗再生障碍性贫血药物中的应用。
本发明的营养组合物对DNA切除修复基因损伤、DNA错配修复基因损伤、DNA同源重组修复基因损伤及DNA 错误倾向修复基因损伤等均有恢复作用;可使肝细胞、脾脏B细胞、肾小管上皮细胞及脑海马部神经元细胞线粒体增殖,对肝细胞、脾脏B细胞线粒体基因损伤进行修复;具有促进造血干细胞、肝脏干细胞、间充质干细胞、肾脏干细胞增殖及胃粘膜干细胞增殖的作用;对肝脏损伤、脾脏损伤、肾脏损伤、大脑损伤及骨骼损伤等具有修复作用;对再障大鼠高表达的多个蛋白分子有明显的抑制作用。即可以全面修复再障机体,从而达到治疗再生障碍性贫血的效果。
附图说明
图1是本发明实施例对再障大鼠体重的影响示意图。
图2 是本发明实施例对再障大鼠肝、骨髓、脑核苷酸切除修复基因的影响示意图。
图3是本发明实施例对再障大鼠肝、骨髓、脑碱基切除修复基因的影响示意图。
图4是本发明实施例对再障大鼠肝脏、骨髓以及脑组织中错配修复基因的影响示意图。
图5是本发明实施例对再障大鼠肝、骨髓、脑同源重组修复基因的影响示意图。
图6是本发明实施例对再障大鼠肝、骨髓、脑SOS修复基因的影响示意图。
图7是本发明实施例对再障大鼠肝脏细胞线粒体的影响示意图(电镜)。
图8 是本发明实施例对再障大鼠脾脏细胞线粒体的影响示意图(电镜)。
图9 是本发明实施例对再障大鼠肾小管上皮细胞线粒体的影响示意图(电镜)。
图10是本发明实施例对再障大鼠脑海马部的影响示意图(电镜)。
图11是本发明实施例对再障大鼠线粒体膜电位的影响示意图。
图12是本发明实施例对再障大鼠线粒体DNA含量的影响。
图13 是本发明实施例对再障大鼠骨髓造血干细胞的影响示意图。
图14是本发明实施例对再障大鼠肝脏干细胞的影响示意图。
图15是本发明实施例对再障大鼠肾脏干细胞的影响示意图。
图16是本发明实施例对再障大鼠胃干细胞的影响示意图。
图17是本发明实施例对再障大鼠肠粘膜干细胞的影响示意图。
图18是本发明实施例对再障大鼠神经干细胞的影响示意图。
图19是本发明实施例对再障大鼠胰腺干细胞的影响示意图。
图20是本发明实施例对再障大鼠肌肉干细胞的影响示意图。
图21是本发明实施例对再障大鼠骨髓间充质干细胞的影响示意图。
图22 是本发明实施例对再障大鼠肝、脾、肾、脑的影响示意图(HE染色)。
图23 是本发明实施例对再障大鼠肠、肌肉的影响示意图(HE染色)。
图24是本发明各实验组的肾切片透射电镜图。
图25是本发明实施例对再障大鼠骨髓间充质干细胞生长的影响示意图。
图26是本发明各实验组脂肪细胞的诱导及成脂细胞相关基因的表达示意图。
图27是本发明各实验组成骨细胞的诱导及成骨细胞相关基因的表达示意图。
图28是本发明实施例对再障大鼠骨髓造血细胞的影响示意图。
图29-1、图29-2、图29-3是本发明实施例对再障大鼠间充质干细胞蛋白表达的影响示意图(蛋白芯片谱图)。
图30-1、图30-2、图30-3是本发明实施例对再障大鼠骨髓细胞蛋白表达的影响示意图(蛋白芯片谱图)。
图31-1、图31-2、图31-3是本发明实施例对再障大鼠肝脏细胞蛋白表达的影响示意图(蛋白芯片谱图)。
具体实施方式
实施例1:本发明的营养组合物各组分质量(mg)比如下:赖氨酸200~1200、甲硫氨酸100~1600、苯丙氨酸150~1400、苏氨酸50~600、色氨酸50~400、精氨酸200~1500、组氨酸100~1000、甘氨酸100~600、天冬氨酸100~600、亮氨酸100~600、异亮氨酸100~600、缬氨酸100~800、丝氨酸100~400、谷氨酰胺200~600、牛磺酸100~500、乳清酸100~300、核苷酸200~1200、维生素A 0.2~0.6、维生素D 0.002~0.006、维生素B2 1~4、维生素B6 1~4、维生素B120.001~0.006、烟酸 5~20、叶酸0.01~1.2、维生素C 50~150、铁2~10、锌2~10、锰2~10、铜 0.5~2、硒0.01~0.1、铬0.01~0.02、钾10~300、钙100~300、镁100~200、肌醇50~60、大豆磷脂100~2500。
实施例2:各组分质量(mg)比如下:赖氨酸600、甲硫氨酸800、苯丙氨酸700、苏氨酸300、色氨酸200、精氨酸760、组氨酸500、甘氨酸300、天冬氨酸300、亮氨酸300、异亮氨酸300、缬氨酸400、丝氨酸200、谷氨酰胺300、牛磺酸500、乳清酸300、核苷酸400、维生素A 0.6、维生素D0.006、维生素B22、维生素B62、维生素B12 0.004、烟酸12、叶酸0.9、维生素C100、铁10、锌10、锰 8、铜2、硒0.1、铬 0.02、钾 300、钙300、镁 200、肌醇60、大豆磷脂1200。
所述营养组合物可在制备治疗再生障碍性贫血药物中应用。
原料来源如表1:
表1
实验:
一.再生障碍性贫血大鼠模型的建立
本实验采用SD大鼠。实验步骤:第一天X射线2.5Gy照射后,于第4、6、8天分别给予环磷酰胺35mg/kg,氯霉素45 mg/kg腹腔注射。第15天重复以上步骤。以单纯等量生理盐水相应部位注射为正常对照组。
实验分组:根据动物药理学的药品剂量和综合试验的设计分析,分为:①正常对照组;②再障模型组;③实施例2营养组合物高剂量组,以2266.95mg/kg.d对大鼠灌胃;④实施例2营养组合物中剂量组,以1511.3mg/kg.d对大鼠灌胃;⑤实施例2营养组合物低剂量组,以1057.91mg/kg.d对大鼠灌胃。
试验流程:首先,按前述再障大鼠模型的建立方法建立模型,从第5天开始,营养组合物高、中、低剂量组分别以相应剂量对大鼠进行灌胃,每天一次,直至第60天,拉颈处死大鼠,采样进行检测。同时每日进行整体观察,测量体重。
二.实验方法
1. 外周血检测
各实验组第60天, 称重动物,经眼眶取血,采用全自动血细胞分析仪测定外周血血红蛋白含量、红细胞、白细胞及血小板数;显微镜下观察外周血涂片。
2.促红细胞生成素(Epo)检测
酶标板每孔加入标准液,对照液及预先用样品稀释液稀释的待测样品100ul,封板,37°C孵育90分钟。反应后甩干孔内液体后,将准备好的生物素抗小鼠EPO抗体工作液按每孔100ul依次加入(TMB空白显色孔除外),封板后37°C反应60分钟,0.01M PBS洗涤3次,每次浸泡1分钟左右。加入准备好的亲和素-过氧化物酶复合物工作液按每孔100ul依次加入(TMB空白显色孔除外),37°C反应30分钟。按每孔90µl依次加入已在37℃中平衡30分钟TMB显色液,37°C避光反应,每孔100µl依次加入TMB终止液。用酶标仪于450nm波长处读取吸光度(OD值), 根据标准曲线测得样本Epo浓度(pg/ml)。
3. 骨髓检测
颈椎脱臼处死大鼠, 分离双侧股骨打开骨髓腔进行骨髓涂片、骨髓单个核细胞计数、骨髓病理检查、骨髓间充质干细胞增殖及分化趋势的分析。
4. 骨髓间充质干细胞(BMSCs)的分离提取
SD大鼠腹腔注射麻醉药后脱颈处死,75% 乙醇浸泡大鼠20 min;无菌取双后肢,放入75% 的乙醇中浸泡5 min;清除下肢肌肉,从膝关节断离股骨,剪开股骨两端;用10 mL注射器吸取10% 胎牛血清的F-12K培养液冲洗骨髓腔,收集骨髓冲洗液,制成单细胞悬液,200目筛网滤过后以1×108接种于培养瓶中。置于37°C、5% CO2培养箱中培养。72 小时首次更换培养液,去除未贴壁细胞,以后每隔2天换液1次。当细胞铺满整个培养瓶底面积的80%~90%时,传代培养。
5.间充质干细胞(BMSCs)的成脂诱导分化
成脂诱导法:将分离纯化的骨髓间充质干细胞常规培养,消化传代,以1×105/孔的密度,400ul/孔接种于预先放置有盖玻片的6孔培养板中,制备细胞爬片,当细胞生长达80% 融合时,加入10%的胎牛血清、1μmol/L地塞米松、0.5 mmol/L IBMX、10 mg/L牛胰岛素的H-DMEM诱导3天,再用10% 的胎牛血清、10 mg/L牛胰岛素的H-DMEM处理1天,如此循环3次后,用10%的胎牛血清、10 mg/L牛胰岛素的H-DMEM处理7天,每隔三四天换液1次。对照组始终加入含体积分数为10% 的胎牛血清、10 mg/L牛胰岛素的H-DMEM,每隔三四天换液1次。诱导后细胞用PBS洗涤2~3次,10% 甲醛室温固定40min。PBS洗2~3次,饱和油红O染液用一蒸水以3:2稀释,室温染色30min,PBS洗数次直至无肉眼观察到沉渣,光镜观察。
6. 间充质干细胞(BMSCs)成骨细胞培养及鉴定
取P2代骨髓间充质干细胞,按2×105个/孔接种于12孔板,当细胞贴壁生长达80% 融合时,吸除孔中培养液,换为成骨细胞诱导液 (含高糖DMEM、体积分数为10% 胎牛血清、10-8mol/L地塞米松、10-2 mol/L β-甘油磷酸钠、50 mg/L抗坏血酸),每3天更换诱导液1次。培养14天后,吸除培养液,PBS洗2次,10%甲醛室温固定40 min,PBS洗3次,加入0.1% 茜红素(3:2稀释),室温染色10min,去除染液,PBS洗3次后,显微镜下观察。
7. RNA提取和RT-PCR分析
常规应用Trizol 法提取各标本的总RNA,紫外分光光度计测定A260和A280,以检测RNA含量和纯度,并置放于-70°C保存。
反转录体系20μl,包含样品RNA 1μl,按照TaKaRa 的反转录试剂盒提供的说明书进行操作。反转录反应条件为:65°C 1min,30°C 5min,65°C 15min,98°C 5min,5°C 5min。
PCR反应体系50 μl,包含反转录液10 μl。PCR反应条件: 94°C预变性1min;97°C 变性 20s,64°C退火20s,72°C 20s延伸,循环30次;72°C 延伸5min,4°C恒定。取5μl PCR扩增产物经1%琼脂糖凝胶电泳, 紫外灯下凝胶成像。
8. 透射电镜观察
将大鼠部分肝、脾、脑、肾组织标本上取不同部位的3张切片进行透射电镜(JEM-100CXE 型) 超微结构的观察,每张切片分别随机观察5-6个部位,并按相同放大倍数摄片,每组随机抽取l0张照片,采用Epson微机和Summa Sketch PIus 数字化仪,并使用Sigmascan软件,对各组照片作电镜图像的形态进行分析,同时计数线粒体的平均数目。
9. 线粒体膜电位测定
细胞(5×105个)接种于25cm2培养瓶中, 37℃培养24 h后,加入不同浓度的姜黄素分别作用1 h和 6 h 后,收获细胞,PBS洗两遍,重悬于2ml 含1.0 µM 罗丹明123的新鲜培养液中,37°C 水浴振摇孵育10 min,离心去掉细胞,荧光比色计测定培养液中罗丹明123的强度,激发波长490 nm,发射波长520 nm,结果以细胞吸收的罗丹明123的荧光强度表示。
10. 线粒体DNA含量测定
将骨髓单个核细胞(5×107)、新鲜组织肝脏、脾、脑、肾匀浆、裂解、离心,获取线粒体。按照DNA提取试剂盒说明提取线粒体中的DNA,采用紫外分光光度计测量其含量。计算公式如下:
DNA浓度(μg/μl)= A260 × 50μg/ml × 稀释倍数 × 10-3
11. 病理学观察
将大鼠部分肝、脾、脑、肾、肠、肌肉置于4 %多聚甲醛中固定,依次经过常规脱水、石蜡浸泡包埋、切片、HE 染色, 显微镜观察各组织细胞的形态结构。
12. 免疫组化染色
石蜡切片脱蜡、水化;PBS洗2-3次各5分钟;3% H2O2(80%甲醇)滴加在玻片上,室温静置10分钟;PBS洗2-3次各5分钟;抗原修复;PBS洗2-3次各5分钟;滴加正常山羊血清封闭液,室温20分钟。甩去多余液体,滴加一抗50μl,4°C过夜。过夜后需在37°C复温45分钟。PBS洗3次各5分钟;滴加二抗40-50μl,室温静置,或37°C 1小时;PBS洗3次各5分钟;DAB显色5-10分钟,在显微镜下掌握染色程度;PBS或自来水冲洗10分钟;苏木精复染2分钟,盐酸酒精分化;自来水冲洗10-15分钟;脱水、透明、封片、镜检。
13. 流式细胞仪分析
取大鼠左胫骨,去除表面肌肉组织,修剪骨垢,用18 号针插入胫骨踝端,用PBS 5mL 冲洗入试管内,以200目筛网过滤。1000 r/min 离心 5min,弃上清液。将细胞加入5mL Percoll分离液(相对比重1.073g/L),2000r/min,离心25min,取中间单个核细胞层。PBS洗涤后调整单个核细胞数为l×106/管,每样本3管,测定管加入FITC标记的CD34或CD45抗体,37°C孵育2小时。然后PBS洗涤一次。用流式细胞仪检测表达CD34/45阳性细胞数量变化,以标记抗体呈阳性的细胞百分率作为表达CD34/45 蛋白(骨髓造血干细胞标志物)的计量标准。同时以只加标记荧光素的羊抗兔IgG和不加抗体的细胞作阴性对照。
14. 蛋白芯片分析
将大鼠部分骨髓单个核细胞、骨髓间充质干细胞、肝脏组织进行蛋白芯片分析,此部分工作由上海康城公司完成。
15. 统计学分析
所有数据均用SPSS 17.0软件进行统计分析。每一项分析至少有三次结果。数值用均数±SD表示,采用t检验。P<0.05认为有显著性差异,并在统计学上有意义。
三、实验结果
(一)营养组合物对再障大鼠全身情况的影响
与正常对照组相比,再障模型组大鼠自6天起陆续出现皮毛松弛蓬乱,光泽度降低,部分大鼠有脱毛及皮损。同时大鼠消瘦、精神渐显不佳,唇色眼睑苍白、活动减少、少食、体重下降。其中再障模型组大鼠体重(218.23±33.52 g)与正常对照组(366.54±49.68 g,*p <0.05)相比下降明显。
不同剂量的营养组合物组与再障模型组比较,大鼠精神状态渐佳,进食量增大,体重增加(见图1)。表明营养组合物对再生障碍性贫血小鼠全身有显著恢复作用。
(二)营养组合物对再障大鼠外周血的影响
与正常对照组相比,再障模型组外周血中红细胞 (RBC)、白细胞 (WBC)、血小板 (PLT) 及血红蛋白 (Hb) 均显著下降 (表 1,#p<0.05);不同剂量营养组合物组与再障模型组比较,其外周血中各项指标均显著升高 (表2,*p<0.05),并呈量效依赖性。
与正常对照组相比,再障模型组大鼠促红细胞生成素(EPO)含量明显升高,且EPO与 RBC、 Hb的降低呈负相关,r=-0.91及r=-0.93(*p <0.05),表明EPO水平与再障骨髓红系生成能力降低,EPO反应性能力减弱,EPO呈代偿性升高有关。(表1,*p <0.01)。EPO是一种重要的造血调控因子,具有促进红系祖细胞增殖、分化和成熟,维持外周血中红细胞,血红蛋白恒定的作用,血液中EPO水平能反映机体中的红细胞生成能力。而不同剂量的营养组合物组与再障模型组比较,促红细胞生成素(Epo)由于代偿作用含量降低 (*p <0.01);并呈剂量-效应关系。
以上结果提示,营养组合物对再障大鼠外周血各种血细胞有促进升高作用。
表2营养组合物对再障大鼠外周血的影响
# P<0.05 再障组与正常组;*P<0.05 营养组合物组与再障组
(三)本发明实施例营养组合物对再障大鼠基因损伤恢复的影响
1. 切除修复基因
1.1 核苷酸切除修复基因
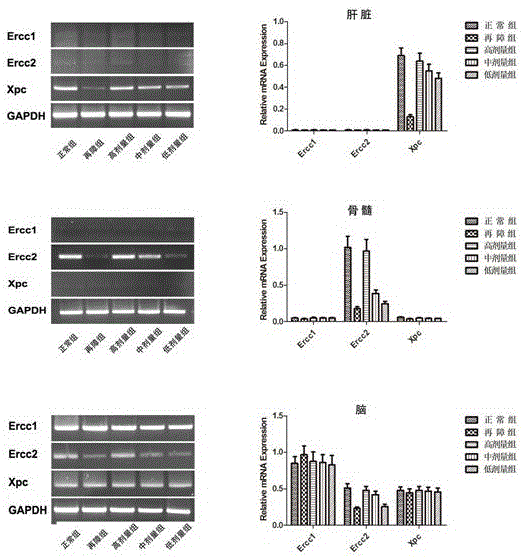
核苷酸切除修复 (NER) 通路被认为是机体内最主要及最重要的损伤修复通路,主要修复外源性物质导致的DNA损伤,例如嘧啶二聚体、光化合物及其它大的化合物及交联所导致的损伤。本实验选取了3 个 NER 基因 (Ercc1, Ercc2, Xpc),从转录水平检测了其在营养组合物组中肝脏、骨髓以及脑中的表达变化(见图2)。
在肝脏组织中,与正常对照组相比,再障模型组大鼠肝脏组织中核苷酸切除修复基因Xpc 表达量下调;营养组合物处理再障大鼠后,大鼠肝脏组织中Xpc 的表达量随营养组合物剂量增加而增加。核苷酸切除修复基因Ercc1、Ercc2 无明显变化。
在骨髓中,与正常对照组相比,再障模型组大鼠骨髓造血细胞核苷酸切除修复基因Ercc2 表达量下调;营养组合物处理再障大鼠后,大鼠骨髓造血细胞Ercc2 的表达量随营养组合物剂量增加而增加。核苷酸切除修复基因Ercc1、Xpc 无明显变化。
在脑组织中,与正常对照组相比,再障模型组大鼠脑组织中核苷酸切除修复基因Ercc2 表达量下调;营养组合物处理再障大鼠后,大鼠脑组织中Ercc1 的表达量随营养组合物剂量增加而增加。核苷酸切除修复基因Ercc1、Xpc无明显变化。
结果表明本发明实施例营养组合物对再障大鼠核苷酸切除修复基因损伤具有一定的恢复作用。
1.2 碱基切除修复基因
碱基切除修复 (base excision repair, BER) 基因主要参与修复内源性烷化剂和外源性致癌剂如亚硝氨引起的 DNA 碱基的烷化以及细胞内自发的和由于电离辐射及紫外线辐射引起的 DNA 碱基的氧化。本实验选取了4 个 BER 基因 (Apex1, Ogg1, Polb, MTH1),从转录水平检测了其在营养组合物组中的表达变化(见图3)。
在肝脏组织中,各组碱基切除修复基因无明显变化。
在骨髓中,与正常对照组相比,再障模型组大鼠骨髓造血细胞碱基切除修复基因Ogg1、MTH1表达量下调;营养组合物处理再障大鼠后,大鼠骨髓造血细胞碱基切除修复基因Ogg1、MTH1的表达量随营养组合物剂量增加而增加。碱基切除修复基因Apex1、Polb 无明显变化。
在脑组织中,与正常对照组相比,再障模型组大鼠骨髓造血细胞碱基切除修复基因Ogg1、MTH1表达量下调;营养组合物处理再障大鼠后,大鼠骨髓造血细胞中碱基切除修复基因Ogg1、MTH1的表达量随营养组合物剂量增加而增加。碱基切除修复基因Apex1、Polb 无明显变化。
结果表明本发明实施例营养组合物对再障大鼠碱基切除修复基因损伤具有一定的恢复作用。
2. 错配修复基因
DNA错配修复系统 (MMR) 是人体细胞的一种能修复DNA碱基错配的安全保障体系,由一系列特异性修复DNA碱基错配的酶分子 (错配修复基因产物) 组成。该系统能消除DNA合成错误,保持遗传物质的完整性和稳定性,避免遗传物质发生突变,保证DNA复制的忠实性。本实验选用最常用的4个错配修复基因MSH2、MSH3、MLH1、PMS2。
在肝脏,骨髓以及脑组织中,与正常对照组相比,再障模型组大鼠中4个错配修复基因的蛋白表达量均下调;营养组合物处理再障大鼠后,大鼠肝脏,骨髓以及脑组织中错配修复基因的表达量随营养组合物剂量增加而增加(见图4)。
结果表明本发明营养组合物对再障大鼠错配修复基因的损伤具有恢复作用。
3. 同源重组修复基因(双链断裂修复)
当细胞暴露在电离辐射、 DNA交联剂及缺氧等各种致 DNA 损伤的条件下时,常出现染色体DNA双链断裂。在真核生物细胞中,已知存在两种修复染色体 DNA双链断裂的主要途径,即同源重组和非同源 DNA末端连接。准确的DNA修复是维持染色体完整性的前提,同源重组则在 DNA修复过程中发挥关键作用。本实验选用最常用的4个同源重组修复基因 Rad51、Rad52、Xrcc1、Xrcc2。
在肝脏,骨髓以及脑组织中,与正常对照组相比,再障模型组大鼠同源重组修复基因Rad51、Rad52、Xrcc1表达量均下调;营养组合物处理再障大鼠后,大鼠重组修复基因Rad51、Rad52、Xrcc1的表达量随营养组合物剂量增加而增加,而Xrcc2无明显变化(见图5)。
结果表明本发明实施例营养组合物对再障大鼠同源重组修复基因的损伤具有恢复作用。
4. 错误倾向修复(SOS修复)基因
当DNA两条链都有损伤并且损伤位点邻近时,损伤不能被切除修复或重组修复,这时在Restriction Endoneuclease和Exoneuclease的作用下造成损伤处的DNA链空缺,再由损伤诱导产生的一整套的特殊DNA聚合酶─SOS修复酶类,催化空缺部位DNA的合成,这时补上去的核苷酸几乎是随机的,仍然终于保持了DNA双链的完整性,使细胞得以生存。本实验选用最常用的两个SOS修复基因RecA、LexA。
在肝脏,骨髓组织中,与正常对照组相比,再障模型组大鼠SOS修复基因RecA 表达量均下调;营养组合物处理再障大鼠后,大鼠SOS修复基因RecA的表达量随营养组合物剂量增加而增加。SOS修复基因LexA 无明显变化(见图6)。
在脑组织中,各组之间SOS修复基因无明显变化。
结果表明本发明实施例营养组合物对再障大鼠SOS修复基因的损伤具有恢复作用。
(四)营养组合物对再障大鼠线粒体的影响
1. 线粒体形态观察
肝组织(汇管区)透射电镜显示(图7),与正常对照组相比,再障模型组大鼠肝细胞内线粒体数目明显减少,嵴不清楚或消失,细胞浆疏松;不同剂量的营养组合物组与再障模型组比较, 大鼠肝细胞内线粒体数目明显增多,胞浆逐渐恢复正常。
脾透射电镜显示(图8),与正常对照组相比,再障模型组大鼠脾脏B细胞内线粒体数目明显减少;不同剂量的营养组合物组与再障模型组比较,细胞内线粒体数目明显增多。
肾小管上皮细胞透射电镜显示(图9),与正常对照组相比,再障模型组大鼠肾小管上皮细胞内线粒体数目明显减少,排列紊乱;不同剂量的营养组合物组与再障模型组比较,肾小管基底部上皮细胞线粒体数目明显增多,排列整齐。
脑透射电镜显示(图10),与正常对照组相比,再障模型组大鼠脑海马部神经元细胞内线粒体数目明显减少;不同剂量的营养组合物组与再障模型组比较, 大鼠脑细胞内线粒体数目略有增多。
结果表明本发明实施例营养组合物可促进再障大鼠肝细胞线粒体、脾脏B细胞线粒体、肾小管上皮细胞线粒体及脑海马部神经元细胞线粒体的增加。
2. 线粒体膜电位测定
线粒体膜电位是观察线粒体功能的重要指标,线粒体功能的改变多表现为膜电位降低和膜的不稳定。采用荧光探针罗丹明123(Rh123)测定营养组合物对线粒体膜电位的影响。Rh123为亲脂性阳离子荧光素,能顺利通过活细胞的细胞膜和线粒体膜,进入线粒体后,由于线粒体膜的负电位差使Rh123选择性富集在线粒体上,胞浆中结合的非常少。线粒体对Rh123的摄入量取决于其膜电位的高低,一定的膜电位形成一定的荧光强度,成正比,强度的大小反映线粒体膜受损程度。
与正常对照组相比,再障模型组大鼠骨髓造血细胞、肝细胞及脾细胞内线粒体膜电位呈明显下降趋势,表明线粒体功能缺失(表2);不同剂量的营养组合物组与再障模型组比较,大鼠骨髓造血细胞、肝细胞及脾细胞内线粒体膜电位明显增高,呈量效关系(表3)。
表3
# P<0.05 再障组与正常组;*P<0.05 营养组合物组与再障组
与正常对照组相比,再障模型组大鼠脑、肾细胞线粒体膜电位减少(图11),但无显著差异;不同剂量的营养组合物组与再障模型组比较, 大鼠脑、肾细胞线粒体膜电位略有增加,但无显著差异(图11)。
结果表明营养组合物可促进再障大鼠骨髓单个核细胞、肝细胞及脾细胞线粒体膜电位升高;而对再障大鼠的脑、肾细胞线粒体膜电位无显著影响。
3. 紫外分光光度计检测线粒体DNA含量
与正常对照组相比,再障模型组大鼠骨髓造血细胞、肝细胞及脾细胞mtDNA的含量明显下降趋势;不同剂量的营养组合物组与再障模型组比较,大鼠骨髓造血细胞、肝细胞及脾细胞mtDNA的含量明显增高,呈量效关系(表4)。
表4
# P<0.05 再障组与正常组;*P<0.05 营养组合物组与再障组
与正常对照组相比,再障模型组大鼠脑、肾细胞线粒体mtDNA的含量减少(图12),但无显著差异;不同剂量的营养组合物组与再障模型组比较,大鼠脑、肾细胞mtDNA的含量略有增加,但无显著差异(图12)。
以上结果表明营养组合物对再障大鼠骨髓单个核细胞、肝细胞及脾细胞mtDNA的损伤具有恢复作用;而对再障大鼠的脑、肾细胞mtDNA含量无显著影响。
(五)本发明实施例营养组合物对再障大鼠干细胞的影响
1. 骨髓造血干细胞
CD34抗原选择地表达于造血干细胞膜上,是造血干细胞的标志。CD45是单链跨膜糖蛋白,属于蛋白络氨酸磷酸酶家族成员,广泛存在于造血干细胞表面。本实验采用免疫组化检测再障大鼠骨髓造血干细胞标志物CD34、CD45的表达情况。结果如图13所示,与正常对照组相比,再障模型组大鼠骨髓造血干细胞CD34、CD45的表达量明显减少,表明再障大鼠骨髓造血干细胞数量减少;营养组合物干预再障大鼠后,大鼠骨髓造血干细胞CD34、CD45的表达量与营养组合物呈剂量依赖性,表明营养组合物具有促进再障大鼠骨髓造血干细胞增殖的作用。
2. 肝脏干细胞
CD90是一种细胞表面糖蛋白,是肝脏干细胞的标志物,同时也是血液干细胞的抗原决定簇。肝卵圆细胞是目前研究较多的一种肝脏干细胞,其表面具有特异性标记细胞角蛋白19(CK19)表达较高。本实验采用免疫组化检测再障大鼠肝干细胞标志物CD90、CK19的表达情况。结果如图14所示,与正常对照组相比,再障模型组大鼠肝脏干细胞数量明显减少,营养组合物处理再障大鼠后,大鼠肝脏干细胞的含量随营养组合物剂量增加而增加,表明营养组合物可促进再障大鼠肝脏干细胞的增殖。
3. 肾脏干细胞
肾脏中,CD133分布在肾髓质乳头区,细胞增殖能力强,认为该区为肾脏干细胞定居点。OCT4是维持干细胞多能性和自我更新的转录因子。本实验采用免疫组化检测再障大鼠肾脏干细胞标志物CD133、OCT4的表达情况,结果如图15所示,与正常对照组相比,再障模型组大鼠CD133、OCT4的表达量显著降低,营养组合物处理再障大鼠后,其表达量随营养组合物剂量增加而增加,表明营养组合物促进再障大鼠肾脏干细胞的增殖。
4. 胃干细胞
Lgr5又名GPR49,近年来研究表明,Lgr5是结直肠癌、胶母细胞瘤等肿瘤干细胞标记,均较既往的标记物CD133、CD44更具特异性。Musashi-1主要表达在胃粘膜上皮峡部,可作为人类正常胃肠道上皮干细胞的标记物。本实验采用免疫组化检测再障大鼠胃干细胞标志物Lgr5的表达。结果如图16所示,与正常对照组相比,再障模型组大鼠胃干细胞数量明显减少;营养组合物处理再障大鼠后,大鼠胃干细胞Lgr5的表达随营养组合物剂量增加而增多,表明营养组合物具有促进再障大鼠胃干细胞的增殖。然而各组胃干细胞Musashi-1的无明显变化。
5. 肠粘膜干细胞
小肠干细胞是一种未分化的初始细胞,位于小肠隐窝近基底部。具有自我更新和增殖分化为各种成熟肠道上皮细胞的功能。研究表明,Musashi-1是肠道干细胞的选择性标记。Lgr5 在鼠类的小肠和大肠隐窝中局限性表达,是肠道干细胞的标志物之一。本实验采用免疫组化检测再障大鼠肠道干细胞标志物Musashi-1、 Lgr5 的表达。结果如图17所示,各组小肠干细胞数量无明显变化。表明营养组合物对再障大鼠小肠干细胞的增殖无显著作用。
6. 神经干细胞
Nestin是中枢神经系统发育过程中神经干细胞或神经前体细胞的标志之一。CD133是造血干细胞、内皮祖细胞的标志物,后来CD133被证实其作为一种干细胞标记物,也是目前比较公认的脑肿瘤干细胞和神经干细胞的表面标志物。本实验采用免疫组化检测再障大鼠神经干细胞标志物Nestin、CD133的表达情况,结果如图18所示,营养组合物处理再障大鼠后,Nestin、CD133的表达无显著变化。表明营养组合物对再障大鼠脑神经干细胞的增殖无显著影响。
7. 胰腺干细胞
细胞角蛋白19(CK19)是上皮细胞特有的标志物,在胰腺干细胞有阳性表达。
Nestin在神经上皮干细胞特异性的表达,而目前研究显示,Nestin在胰腺干细胞中也呈高表达。本实验采用免疫组化检测再障大鼠胰腺干细胞标志物CK19、Nestin的表达情况,结果如图19所示,各组胰腺干细胞数量无明显变化。表明营养组合物对再障大鼠胰腺干细胞的增殖无显著作用。
8. 肌肉干细胞
目前,肌干细胞尚缺乏特异性标志物。Desmin被认为与肌细胞的早期分化关系密切,在肌源性干细胞中Desmin的阳性率可达90%,常作为肌干细胞的标志物。CD34是细胞表面的唾液粘蛋白,被认为是造血干细胞的标记物,但在肌干细胞中也有明显表达。本实验采用免疫组化检测再障大鼠肌肉干细胞标志物Desmin、CD34的表达。结果如图20所示,各组肠道干细胞数量无明显变化。表明营养组合物对再障大鼠肠道干细胞的增殖无明显作用。
9.骨髓间充质干细胞
各组骨髓间充质干细胞增殖能力结果见图21,再障组显著低于正常组,低剂量组与再障组无差异,中剂量组,高剂量组与再障组有明显差异。表明营养组合物对再障大鼠骨髓间充质干细胞的增殖有明显作用。
(六)本发明实施例营养组合物对再障大鼠器官损伤修复的影响
1.对于肝、脾、肾、脑、肠及肌肉等器官损伤修复的影响从图22可以看出:
肝的病理切片HE染色显示,与正常对照组相比,再障模型组大鼠肝脏组织小叶结构欠清晰,肝细胞核固缩,染色质深染,肝血窦及中央静脉扩张,充血。不同剂量的营养组合物组与再障模型组比较, 肝脏组织小叶结构明显清晰,肝细胞形态接近正常。
脾的病理切片HE染色显示,与正常对照组相比,再障模型组大鼠脾脏略微肿大,脾组织结构疏松,脾小体个数减少,生发中心不明显,白髓减少,脾血窦扩张、充血,部分区域可见脾小动脉壁增厚及玻璃样变。不同剂量的营养组合物组与再障模型组比较,脾小体数量增多,白髓增多。
肾的病理切片HE染色显示,与正常对照组相比,再障模型组大鼠肾小球体积减小,部分大小不一,肾小管水肿。不同剂量的营养组合物组与再障模型组比较,肾小球体积趋于正常,肾小管水肿减轻。
脑的病理切片HE染色显示,与正常对照组相比,再障模型组大鼠脑部海马区域的神经元细胞排列紊乱。不同剂量的营养组合物组与再障模型组比较,神经元细胞排列趋于整齐。
从图23中可以看出:
肠、肌肉的组织切片显示未见明显变化。
图24是本发明各实验组的肾切片透射电镜图。从图24可以看出:与正常对照组相比,再障模型组大鼠肾小球基底膜足突大面积融合;不同剂量的营养组合物组与再障模型组比较, 大鼠肾小球基底膜足突融合程度减低,排列趋于正常。
结果显示,本发明实施例营养组合物对再障大鼠肝、脾、肾、脑损伤有显著恢复作用。
2.对于骨骼损伤修复的影响
2.1 本发明实施例营养组合物对再障大鼠骨髓间充质干细胞生长的影响
各组骨髓间充质干细胞增殖能力结果见图25,再障组显著低于正常组,低剂量组与再障组无差异,中剂量组,高剂量组与再障组有明显差异。
2.2 本发明实施例对再障大鼠骨髓间充质干细胞分化趋势的影响
2.2.1 脂肪细胞的诱导及成脂细胞相关基因的表达
如图26所示:
正常组,再障组,高剂量组,中剂量组和低剂量组P2代骨髓间充质干细胞分别用成脂肪细胞诱导培养液进行诱导培养,再障组诱导形成的脂肪滴出现时间 第7天早于正常组第12 d左右。继续诱导培养,脂肪滴明显增大并发生融合。诱导19天后,融合的脂肪滴被油红O染色为明亮的红色;显微镜下观察,再障组骨髓间充质干细胞成脂肪细胞分化诱导能力高于正常组,营养组合物处理再障大鼠后,间充质干细胞成脂肪细胞分化诱导能力下降,且随着营养组合物剂量增加而下降,表明营养组合物减弱再障大鼠间充质干细胞成脂肪细胞分化诱导能力。
为更客观地比较营养组合物对大鼠骨髓间充质干细胞成脂肪细胞的影响,进一步检测了成脂肪细胞相关基因Pparr mRNA,Fabp4 mRNA的表达水平。结果显示,Fabp4和Pparr的表达水平与营养组合物干预的计量呈负相关。
以上结果表明再障组与正常对照组相比,再障鼠骨髓间充质干细胞向脂肪细胞分化能力增强;而营养组合物干预后,再障鼠骨髓间充质干细胞向成脂细胞分化能力减弱。
2.2.2 成骨细胞的诱导及成骨细胞相关基因的表达
如图27所示:
正常组,再障组,高剂量组,中剂量组和低剂量组P2代骨髓间充质干细胞分别用成骨细胞诱导培养液诱导培养,连续培养5~7天,可见细胞集落中心出现黑色沉积物,14天后茜红素染色。再障组骨髓间充质干细胞黑色沉积物出现较晚,钙结节数量明显少于正常组。营养组合物处理再障大鼠后,间充质干细胞成骨细胞分化诱导能力增强,且随着营养组合物剂量增加而增加,表明营养组合物能增强再障大鼠间充质干细胞成骨细胞分化诱导能力。
为比较营养组合物对再障大鼠骨髓间充质干细胞成骨细胞过程的影响,进一步检测了成骨细胞相关基因mRNA和Bglap mRNA的表达水平。结果显示,Alp和Bglap的表达水平与营养组合物干预的计量呈正相关。
结果表明再障组与正常照组相比,再障鼠骨髓间充质干细胞向成骨细胞分化能力减弱;而营养组合物干预后,再障鼠骨髓间充质干细胞向成骨细胞分化能力增强。
2.3 本发明实施例对再障大鼠骨髓造血细胞的影响
骨髓涂片(图28)显示,与正常对照组相比,再障模型组大鼠部分骨髓涂片出现油滴,骨髓全面衰竭呈增生障碍,造血细胞减少,非造血细胞增多;成熟红细胞大小一致,无明显淡染区;巨核细胞缺如,血小板减少,散在分布(图28A);骨髓单个核细胞计数显示,再障模型组明显低于正常对照组(图28B、表5)。各营养组合物组与再障模型组比较,骨髓病理变化逐渐改善,骨髓细胞明显增多(图28A);各营养组合物组单个核细胞数明显高于再障模型组(图28B、表5)。
表5
# P<0.05 再障组与正常组;*P<0.05 营养组合物组与再障组
结果显示,营养组合物可促进再障大鼠骨髓造血细胞的增殖,对再障大鼠骨髓损伤状态有显著修复作用。
综上所述,本发明实施例营养组合物对再障大鼠骨骼损伤状态有显著修复作用。
(七)营养组合物对再障大鼠蛋白表达的影响(蛋白芯片)
1. 再障大鼠间充质干细胞蛋白表达的影响
再障组与正常组相比(图29-1),17个蛋白分子表达量升高,其中包括:RELM beta (RELM-β),beta-Catenin (β- Catenin),MIP-2,CNTF,Growth Hormone R (GHR),beta-NGF (β-NGF),Neuropilin-2 (NRP-2),Leptin (OB),IL-2,IL-12/IL-23 p40,IP-10,Fas Ligand/TNFSF6 (CD178),GFR alpha-2,IFN-gamma,MIP-1 alpha (MIP-1α),MIP-3 alpha (MIP-3α),Growth Hormone (GH)。
高剂量组与正常组相比(图29-2),2个蛋白分子表达量降低,其中包括RALT/MIG-6 (SG-16),Follostatin-like -1 (FSL1)。
高剂量组与再障组相比(图29-3),11个蛋白分子表达量降低,其中包括:RELM beta,RALT/MIG-6,IL-2,TIMP-1,GFR alpha-2,Fractalkine, Follostatin-like -1(FSL1),TGF-beta1,IFN-gamma,VEGF,beta-NGF。
以上结果显示,营养组合物对再障大鼠间充质干细胞高表达的5个蛋白分子 (RELM-β,β-NGF,IL-2,GFR alpha-2,IFN-gamma) 的表达有明显的抑制作用。此外,高剂量组与正常组相比,差异蛋白数目明显减少,证明了营养组合物对再障大鼠间质干细胞的蛋白表达有一定的恢复作用。
2. 再障大鼠骨髓细胞蛋白的表达影响
再障组与正常组相比(图30-1),12个蛋白分子表达量升高,其中包括:VEGF-C,TAL1A,MIP-2,MIF,Adiponectin/Acrp30,MuSK,NGFR,RALT/MIG-6,FGF-BP,TIMP-1,Fas/TNFRSF6,IL-4。 8个蛋白分子表达量降低,Fas Ligand/TNFSF6,IL-3,CD106,TNF-alpha,Activin A,GM-CSF,IL-1 alpha,B7-1/CD80。
高剂量组与正常组相比(图30-2),7个蛋白分子表达量升高,其中包括Adiponectin/Acrp30,IL-12/IL-23 p40,TAL1A,ICAM-1/CD54,VEGF-C,VEGF,MDC。23个蛋白分子表达量降低:IL-1 R6/IL-1 R rp2,Follostatin-like -1(FSL1),Fractalkine,RAGE,L-Selectin/CD62L,PDGF-AA,IL-2,IFN-gamma,GFR alpha-1,Fas Ligand/TNFSF6,Hepassocin,CD106,Leptin (OB),beta-Catenin,IL-3,CNTF,CNTF R alpha,IL-1 alpha,LIX,IL-13,CXCR4,MIP-1 alpha,B7-1/CD80。
高剂量组与再障组相比(图30-3),3个蛋白分子表达量升高,其中包括:IL-12/IL-23 p40,VEGF,RELM beta。10个蛋白分子表达量降低:Hepassocin, beta-Catenin,MIP-1 alpha,IFN-gamma,RAGE,NGFR,Follostatin-like -1 (FSL1),IL-2,MuSK,CNTF。
以上结果显示,再障组升高的MuSK 蛋白分子表达量在高剂量组都有所下降,得到一定的恢复,说明营养组合物对再障大鼠骨髓细胞高表达的MuSK蛋白的表达有明显的抑制作用。
3. 再障大鼠肝脏蛋白的表达影响
再障组与正常组相比(图31-1),IL-6表达量升高,IL-1 R6/IL-1 R rp2表达量降低。
高剂量组与正常组相比(图31-2),MCP-1,IL-4表达量升高。ADFP,Prolactin R,BDNF表达量降低。
高剂量组与再障组相比(图31-3),IL-13,Neuropilin-2表达量降低。
- 还没有人留言评论。精彩留言会获得点赞!