预防或减轻非酒精性脂肪肝疾病的组合物的制作方法
本发明涉及一种包含阿洛酮糖作为活性成分的预防或改善非酒精性脂肪肝疾病的药物组合物和食品组合物,更具体地,涉及一种通过施用阿洛酮糖抑制肝脏脂肪蓄积来预防或改善非酒精性脂肪肝疾病的组合物。
背景技术:
脂肪肝疾病,也称为脂肪肝,是一种由于脂肪(例如甘油三酸酯)在肝细胞中的异常蓄积而引起肝衰竭的疾病。已知脂肪肝疾病的初始病状是单纯性脂肪肝,单纯性脂肪肝仅表现为脂肪在肝细胞中的沉积,然后发展为脂肪性肝炎(包括肝纤维化)以及肝硬化或肝细胞癌。通常,肝脏中脂肪沉积的原因包括酒精摄入、肥胖、糖尿病、脂质代谢异常、药物(类固醇、四环素等)、库欣综合征、中毒(黄磷等)、高度营养失调等。
脂肪肝疾病的病因大致分为酒精性和非酒精性的,由前者引起的肝脏疾病称为酒精性脂肪肝疾病(也称为酒精性肝衰竭),由后者引起的肝脏疾病称为非酒精性脂肪肝疾病(nafld,或非酒精性脂肪性肝炎)。
非酒精性脂肪肝疾病是指在不消耗过量酒精的患者中不伴有炎症反应的单纯性脂肪肝,其意指包括非酒精性脂肪性肝炎(nash)(表现为由单纯性脂肪肝发展的肝细胞炎症)、肝纤维化和肝硬化在内的多种疾病,非酒精性脂肪肝疾病与既往使用的非酒精性脂肪性肝炎相比是一个宽泛的概念(ludwigjetal.,mayoclinproc1980,55(7):434-438)。
非酒精性脂肪肝疾病是指尽管没有被认为是对肝脏有害的酒精摄入史,但在肝脏活检中表现出脂肪变化(脂肪变性)和小叶性肝炎(脂肪性肝炎)等酒精性肝炎的特征的疾病。肝脏的病理学表现出从单纯性脂肪肝(非酒精性脂肪肝,nafl)到脂肪性肝炎(非酒精性脂肪性肝炎,nash)、伴随脂肪性肝炎的纤维化、肝硬化等的各种谱,并且使用非酒精性脂肪肝疾病意为包括所有这些。
由于这种非酒精性脂肪肝与多种因素有关,例如糖尿病、肥胖症、冠状动脉疾病、久坐习惯等,因此对于这种非酒精性脂肪肝尚无确定的治疗方法。肥胖是非酒精性脂肪肝疾病的重要治疗目标,因为与胰岛素抵抗相关的因素(引起肝脏损害的风险因素)、进入肝脏的脂肪酸的量以及炎症性或纤维化脂肪因子的减少均可通过减肥而诱导。饮食控制和运动减肥可以降低肝脏中的丙氨酸氨基转移酶(alt)水平和甘油三酸酯含量,但是对于坏死性炎症或肝纤维化患者,减肥的改善作用鲜为人知。
如上所述,尚未确立用于充分治疗非酒精性脂肪肝疾病的方法。提前预防或避免非酒精性脂肪肝疾病很重要。
技术实现要素:
【技术问题】
本发明的一个实施方案提供了一种用于预防或改善非酒精性脂肪肝疾病的药物组合物或食品组合物,该药物组合物或食品组合物包含阿洛酮糖作为活性成分。
本发明的一个实施方案提供了一种预防或改善非酒精性脂肪肝疾病的方法,该方法包括向有需要的个体施用阿洛酮糖。
本发明的另一个实施方案提供了一种通过抑制肝脏脂肪蓄积来减轻、预防、改善或抑制非酒精性脂肪肝疾病的药物组合物或食品组合物,该药物组合物或食品组合物包含阿洛酮糖作为活性成分。
本发明的一个实施方案提供了一种通过抑制肝脏脂肪蓄积来减轻、预防、改善或抑制非酒精性脂肪肝疾病的方法,该方法包括向有需要的个体施用阿洛酮糖。
【技术方案】
本发明涉及一种用于抑制肝脏脂肪蓄积、预防或改善非酒精性脂肪肝疾病的组合物,例如药物组合物或食品组合物,该组合物包含阿洛酮糖作为活性成分。
另外,本发明涉及一种用于预防或改善非酒精性脂肪肝疾病的方法,该方法包括向有需要的个体施用阿洛酮糖。个体可以是包括动物和人类的哺乳动物。个体可以是患有非酒精性脂肪肝疾病的患者。
根据本发明的包含阿洛酮糖作为活性成分的组合物抑制肝脏脂肪蓄积并抑制肌肉组织的减少,从而起到改善身体组成的作用。
非酒精性脂肪肝疾病是指在不过度饮酒的患者中不伴有炎症反应的单纯性脂肪肝,其意指包括非酒精性脂肪性肝炎(nash)(表现为由单纯性脂肪肝发展的肝细胞炎症)、肝纤维化和肝硬化在内的具有宽泛概念的疾病,非酒精性脂肪肝疾病与既往使用的非酒精性脂肪性肝炎相比是一个宽泛的概念(ludwigjetal.,mayoclinproc1980,55(7):434-438)。
非酒精性脂肪肝疾病是指尽管没有被认为是对肝脏有害的酒精摄入史,但在肝脏活检中表现出脂肪变化(脂肪变性)和小叶性肝炎(脂肪性肝炎)等酒精性肝炎的特征的疾病。肝脏的病理学表现出从单纯性脂肪肝(非酒精性脂肪肝,nafl)到脂肪性肝炎(非酒精性脂肪性肝炎,nash)、伴随脂肪性肝炎的纤维化,肝硬化等的各种谱,并且使用非酒精性脂肪肝疾病意指包括所有这些。
对于根据本发明的包含阿洛酮糖作为活性成分的组合物,通过dxa在与基准时间相比12周时测得的体脂肪重量的变化在三个组之间显示出统计学上的显著差异。瘦体重(leanbodyweight)是指从体重中排除脂肪的量后的水分、肌肉蛋白、骨骼等的测得量,并且可以解释体重减轻是由体脂肪以外的其他身体成分的变化引起的还是由体脂肪的变化引起的。对于根据本发明的包含阿洛酮糖作为活性成分的组合物,在与基准时间相比12周时的分析中,在12周时通过dxa测得的瘦体重在低剂量组和高剂量组中没有显示出显著差异,但在对照组中显示出显著差异,在与基准时间相比12周时具有降低的值。可以确认,体重减轻是由体脂肪变化引起的,因为体脂肪量的减少是统计学上显著的。可以实现非常理想的健康结果,因为它可以有效抑制体内脂肪的蓄积,但不会伴有其他有益身体成分(水分、肌肉、骨骼等)的变化或变化很小。
所述阿洛酮糖可以是统计学上显著抑制瘦体重降低的药剂。在抑制瘦体重降低方面,在与基准时间相比12周时测得的施用前/后的瘦体重的平均变化可以为1.5%以下,优选为1.0%以下。
在肝脏ct中,在所有肝脏hu平均值、肝-脾hu和肝/脾hu方面,对照组均呈下降趋势,并且在施用前后显示出统计学上的显著差异。在本发明的试验中,反映肝功能的血液肝酶指标在服用阿洛酮糖后显示出普遍改善的结果。非酒精性脂肪肝疾病被认为是由肥胖引起的代谢综合征的其他表型。总之,根据对人体成分的分析结果,阿洛酮糖抑制了体脂肪的蓄积和肌肉质量的减少。
此外,在体外试验中,碱性磷酸酶和γ-gtp在三组之间显示出统计学上的显著差异,因为在与基准时间相比12周时它们在高剂量组和低剂量组中减少,而在对照组中增加。alt在三组之间显示出统计学上的显著差异,因为在高剂量组和低剂量组中alt降低了,而对照组中alt增加了,且在高剂量组中在施用前/后alt显示出统计学上的显著差异。非酒精性脂肪性肝炎是由肥胖引起的代谢综合征的其他表型。
基于组合物的总重量,本发明的实施方案的组合物中的阿洛酮糖的含量可以为例如0.01至100重量%,但不特别限于此。
施用本发明的组合物的个体可以是需要抑制肝脏脂肪蓄积的个体,并且可以是包括正常人或患者在内的动物。另外,可能是需要抑制肝脏脂肪蓄积、患有非酒精性脂肪肝疾病、具有患病风险或具有诸如肥胖、超重等病因的人。
在本文中,术语“施用”是指通过某些适当的方法将本发明的组合物引入个体的行为,并且可以通过各种口服或肠胃外途径来施用,优选口服施用,只要其能够达到目标组织即可。
本发明的组合物的施用频率可以是一天一至四次,或者可以将日剂量分为数次,但不特别限于此。例如,当阿洛酮糖一天施用1-4次时,可以将该剂量分成相等的量或不同的量来施用。
阿洛酮糖的日剂量可以为个体的每单位重量kg,0.05至0.75g,或优选为0.05至0.75g,并且对于平均体重为60kg的人,日剂量可以为3至45g,优选为3至25g,或更优选为6至12g。
在本发明的组合物中的阿洛酮糖可以是粉末或糖浆形式,或者例如,阿洛酮糖可以是纯度为90重量%以上的粉末,或使用该粉末以各种浓度制备的溶液,或通过化学或生物学方法将含果糖的溶液转化为阿洛酮糖而获得的溶液。
另外,阿洛酮糖可以单独使用,或者可以是包括其他糖类在内的混合糖,并且基于100重量份的所述混合糖的总固体含量,所述混合糖的实例可以包含1至99.9重量份的阿洛酮糖,并且可以进一步包含选自果糖、葡萄糖和低聚糖中的一种或多种。
基于100重量份的所述混合糖的总固体含量,包含阿洛酮糖的混合糖的具体实例可包含2至55重量份的阿洛酮糖、30至80重量份的果糖、2至60重量份的葡萄糖和0至15重量份的低聚糖,并且它可以不包含低聚糖。阿洛酮糖、果糖和葡萄糖均优选为d-异构体。
可以通过化学合成或使用阿洛酮糖差向异构酶的生物学方法来制备所述阿洛酮糖,并且优选地,可以通过生物学方法来制备阿洛酮糖。因此,可以通过使含果糖的原料与用于产生阿洛酮糖的包含选自以下物质中的一种或多种的组合物反应来制备阿洛酮糖:阿洛酮糖差向异构酶、产生差向异构酶的微生物的细胞、微生物的培养物、微生物的裂解物、以及裂解物或培养物的提取物。在本发明的一个实施方案中,作为根据生物学方法制备阿洛酮糖的方法,阿洛酮糖可以通过使用产生阿洛酮糖差向异构酶的微生物或重组微生物或其中引入了编码阿洛酮糖差向异构酶的基因的微生物或重组微生物,并使由此获得的阿洛酮糖差向异构酶与含果糖的原料反应而制备。阿洛酮糖差向异构酶可以用于使用固定化酶的液相反应或固相反应中。
为了在制备阿洛酮糖的方法中有效地制备阿洛酮糖,基于总的反应物,用作底物的果糖的浓度可以为20w/w%或更高,例如,40-98%(w/v),或40-95%(w/v),或特别地,为40-75%或50-95%(w/v)。考虑到该方法的经济可行性和果糖的溶解度,可以适当选择果糖的浓度。果糖可以以溶于缓冲溶液或水(例如蒸馏水)的溶液形式使用。
在韩国专利公开第2014-0021974号、韩国专利公开第2014-0080282号和韩国专利第10-1318422号中对阿洛酮糖及其制备方法进行了详细描述。
本发明的食品组合物可以通过本领域已知的普通方法以各种形式制备,并且可以通过将其制成食品、饮料、食品添加剂、饮料添加剂、健康功能食品等来提供。例如,它可以是诸如茶、果汁、碳酸饮料、离子饮料和饮品的饮料,诸如粉剂、片剂和胶囊剂的保健食品制剂,诸如口香糖、点心、面包和面条等的食品。在本发明的食品组合物中,除活性成分外,还可包含甜味剂、香料、调味剂等。另外,如果需要的话,本发明的食品组合物可以包含防腐剂、乳化剂、增稠剂等。为了预防或改善非酒精性脂肪肝疾病,本发明的食品组合物可以以片剂、胶囊剂、粉剂、颗粒剂、液体剂、丸剂等形式制备和加工。
本文中,“保健功能食品”是指使用根据保健功能食品法对人体具有有用功能的原料或成分制作(包括加工)的食品,“功能”是指在维持人体正常功能或通过激活生理功能来维持和改善健康等方面取得有益的效果。另外,功能是指营养功能,其是营养物在人体生长和增强以及正常功能方面的生理作用;生理活性功能,其是通过对人体的正常功能或生物活动有特殊效果而有益于健康、提高功能、改善健康或保持健康的作用;或通过食物摄入减少疾病发生和风险的功能。
对食品没有特别限制,只要它是阿洛酮糖适用的食品即可,例如,可以是加工谷物、加工豆类、加工土豆、加工糖、加工鱼产品、其他加工产品、糕点糖果、糖果(例如硬糖、果冻、橡皮糖)、面包、饺子、加工肉、加工蛋、果冻食品、加工油、其他面条、炒面、固体茶、液态茶、咖啡、果汁、果汁饮料、其他发酵饮料、人参红参饮料、混合饮料、饮料基料、调味味噌、红辣椒酱、发酵大豆酱、酱汁、复合调味食品、白菜泡菜、调味咸鱼、咸菜、糖渍菜、水煮农产品、水煮畜产品、调味干鱼、干鱼、花生或坚果加工产品、水果加工产品、调味海藻、提取食品、即食食品、蒸米饭、蘑菇果体加工食品饮料、肉加工产品、巧克力、糕点糖果、比萨饼、面条(拉面、挂面等)、口香糖、冰淇淋、酒精饮料、维生素复合物和健康补品等。
根据本发明的食品可以包含通用食品添加剂,并且食品添加剂的适用性是根据由韩国食品药品管理局批准的食品添加剂法典的一般规则和一般测试方法,通过相应项目的标准和准则来确定的,除非另有规定。
“食品添加剂法典”中描述的项目包括诸如酮、甘氨酸、柠檬酸钙、烟酸、肉桂酸等的化合物;诸如铬色素、甘草提取物、结晶纤维素、高粱色素、瓜尔豆胶等的天然添加剂;以及诸如l-谷氨酸钠制剂、面条用碱性剂、防腐剂和焦油着色剂等的混合制剂。根据本发明的用于预防或改善非酒精性脂肪肝的组合物可以用作药物组合物或食品组合物。
在本发明的一个实施方案中,可以将用于预防或改善非酒精性脂肪肝的药物组合物制备为药物组合物。根据本发明的药物组合物可以口服或肠胃外施用,优选口服施用。
根据本发明的药物组合物包含药学上可接受的载体。载体通常用于制剂,包括乳糖、右旋糖、蔗糖、山梨醇、甘露糖醇、淀粉、阿拉伯胶、磷酸钙、藻酸盐、明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、水、糖浆、甲基纤维素、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石粉、硬脂酸镁和矿物油等,但不限于此。根据本发明的药物组合物可以进一步包含润滑剂、保湿剂、甜味剂、调味剂、乳化剂、助悬剂、防腐剂等。作为参考,可药用载体和制剂在remington’spharmaceuticalsciences(第19版,1995)中有具体描述。
通过考虑诸如制剂方法、施用方法、患者的年龄、体重、性别和疾病状况、食物、施用时间、施用途径、排泄率以及反应灵敏性等因素,可以不同地规定根据本发明的药物组合物的合适剂量。
本发明的药物组合物可以通过与药学上可接受的载体和/或赋形剂一起配制来制备成单剂形式或多剂容器。
【有益效果】
本发明涉及用于预防或改善非酒精性脂肪肝疾病的药物组合物和食品组合物,所述药物组合物和食品组合物包含阿洛酮糖作为活性成分,并且更具体地,涉及一种通过施用阿洛酮糖来抑制肝脏脂肪蓄积而用于预防或改善非酒精性脂肪肝疾病的组合物。
附图说明
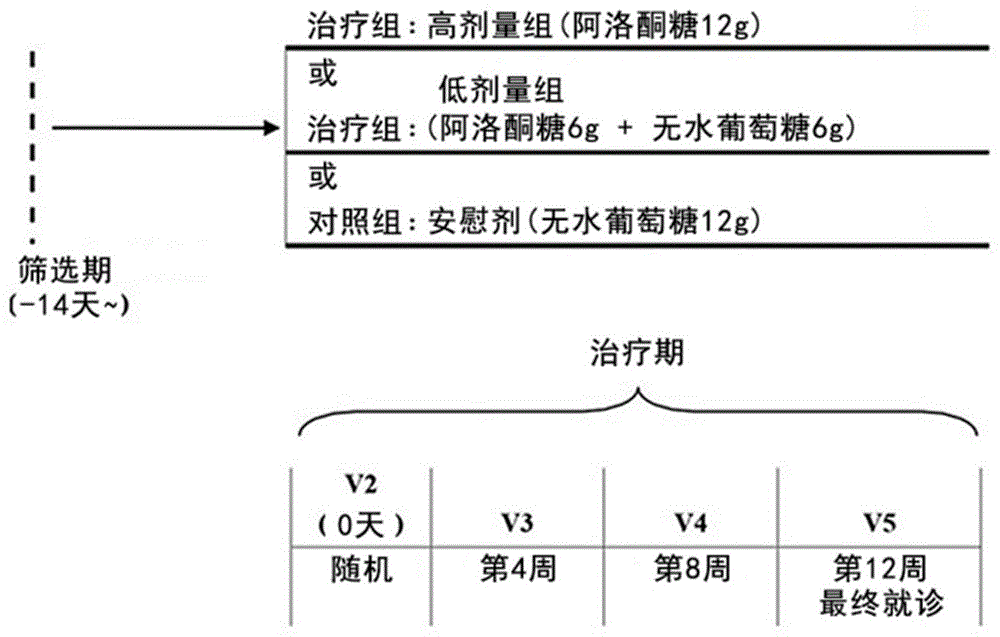
图1为示出根据本发明的实施方案的人体应用方法的示意图。
具体实施方式
在下文中,将通过以下实施例更详细地描述本发明。但是,这些实施例仅用于举例说明本发明,本发明的范围不受这些实施例的限制。
制备例1.阿洛酮糖的制备
通过韩国专利公开第2014-0021974号、韩国专利公开第2014-0080282号和韩国授权专利第10-1318422号中所述的方法制备以下实施例中使用的阿洛酮糖粉。
实施例1:功效测试
(1)对象选择
在对听取了本实施例的目的和研究方法的详细描述并书面同意作为对象的个体进行筛选测试之后,选择了符合选择/排除标准的对象。具体的选择标准如下所述,最终入选的对象为99名体重超重或肥胖的男性和女性,下表1示出了选定对象的人口统计信息。
选择标准
1.年龄在19至75岁之间的成年男性和女性;
2.bmi为23kg/m2以上至小于30kg/m2的超重成年男性和女性;
3.如果是育龄妇女,则筛查期间的妊娠试验为阴性;
4.可以控制的患者(糖尿病或高血压等):包括通过药物使疾病得到良好控制的患者,其中10%的对象患有高血压,5%的对象患有糖尿病。
参加本次人体应用测试的对象的性别为在高剂量组中5名男性(15.15%)和28名女性(84.85%),在低剂量组中6名男性(18.18%)和27名女性(81.82%),在对照组中2名男性(6.06%)和31名女性(93.94%)。高剂量组的平均年龄为45.06岁(范围:25-65岁),低剂量组的为41.52岁(范围:26-61岁),对照组的为44.61岁(范围:26-63岁)。性别和年龄在个体分布上均无统计学明显差异。
通过将99名入选对象分为3组,最终将测试对象确定为高剂量组(33人)、低剂量组(33人)和对照组(33人)。
【表1】
p-值:kruscal-wallis检验
1)fisher精确检验
(2)测试产品
通过将99名选定的测试对象分为3组,并分别向高剂量组(33人)、低剂量组(33人)和对照组(33人)提供三种产品来进行功效测试。向高剂量测试组提供阿洛酮糖高剂量产品,向低剂量测试组提供阿洛酮糖低剂量产品,向对照组提供安慰剂产品。
将产品存放在干燥且通风良好处的室温(1-30℃)下的密闭容器中。
【表2】
(3)摄入方法
九十九(99)名对象被随机分配至高剂量组、低剂量组或对照组,每个测试组包括33名对象。在三个测试组中,将产品混合在100毫升水中,每天口服两次。
作为一个测试对象的日剂量,将高剂量组中的12g阿洛酮糖、低剂量组中的6g阿洛酮糖和6g无水葡萄糖以及对照组中的12g无水葡萄糖每天分为两次提供。从随机分配日(0天)后的第二天开始服用,早晨和傍晚两次随餐用饮用水送服,服用12周。
在随机分配日(0天),检查疗效评估项目和安全评估项目(例如dxa测量等),并且还在测试品的起始服用日起的第4周、第8周和第12周通过医院门诊就诊来检查评估项目。此外,在人体应用测试期间,使用韩文版的国际体育锻炼问卷(ipaq)对受试者的日常体育活动进行了调查。在人体应用测试期间,对受试者进行了训练,以保持其活动量与正常的体育锻炼相似。在每次医院门诊就诊时,通过受试者制作的记录板(recordingboard)检查进餐量。训练受试者以保持与通常量相似的进餐量,避免暴饮暴食的情况。
实施例2:功效评估方法
(1)通过dxa测得的体脂肪和瘦体重
在第二次医院就诊(就诊2)和最终医院就诊(就诊5)时,使用美国lunar公司的prodigydxa测量体脂肪比和体脂肪。
对于通过dxa测得的体脂肪,在计算出与基准时间相比12周后的体脂肪的变化之后,获得了技术统计数据(平均值、标准差、中值、最小值、最大值)。使用anova或kruscal-wallis检验通过测试数据是否呈正态分布来对三个组进行比较统计检验。当三个组之间存在显著差异时,通过tukey-kramer方法进行多重比较。为了确定组中平均值变化是否存在差异,使用配对t检验或wilcoxon符号秩检验进行了分析。
(2)葡萄糖指数测试
在筛查性医院就诊(就诊1)、就诊2和最终就诊(就诊5)时,对采集的血液进行了fbs、胰岛素和hba1c测试。
在计算出与基准时间相比12周后的葡萄糖指数(fbs、胰岛素、hba1c)的平均变化之后,获得了技术统计数据(平均值、标准差、中值、最小值、最大值)。使用anova或kruscal-wallis检验通过测试数据是否呈正态分布来对三个组进行比较统计检验。当三个组之间存在显著差异时,通过tukey-kramer方法进行多重比较。为了确定组中平均值变化是否存在差异,使用配对t检验或wilcoxon符号秩检验进行了分析。
(3)肝脏ct
为了评估在医院就诊2和就诊5时肝脏中脂肪沉积的程度,在与基准时间相比12周后,测量了肝脏的hu、脾脏的hu、肝脏和脾脏的hu差(肝脏减脾脏)以及肝脏和脾脏的hu比(肝脏与脾脏之间的比值)。在一个未造影增强的腹部ct图像(包括肝脏和脾脏)中,在肝脏的右叶和脾脏中选作为避开血管的均匀位置的关注区域(roi)中对ct衰减值(hounsfield单位,hu)进行了三次测量,将平均值作为各ct衰减值。然后,将每个关注区域的大小均等地指定为120mm2。
通过肝脏ct,对12周后肝脏的hu、脾脏的hu、肝脏和脾脏的hu差(肝脏减脾脏)以及肝脏和脾脏的hu比(肝脏与脾脏之间的比值),对于与基准时间相比的平均变化提出了技术统计数据(平均值、标准差、中值、最小值、最大值)。使用anova或kruscal-wallis检验通过测试数据是否呈正态分布来对三个组进行比较统计检验。当三个组之间存在显著差异时,通过tukey-kramer方法进行多重比较。为了确定组中平均值变化是否存在差异,使用配对t检验或wilcoxon符号秩检验进行了分析。
(4)血液化学检测结果
在筛查性就诊(就诊1)、就诊2和最终就诊(就诊5)时执行的测试项目为碱性磷酸酶、ast、alt和γ-gtp。
在连续数据的情况下,对于与基准时间相比的平均变化,提出了技术统计数据(平均值、标准差、中值、最小值、最大值)。使用anova或kruscal-wallis检验通过测试数据是否呈正态分布来对三个组进行比较统计检验。当三个组之间存在显著差异时,通过tukey-kramer方法进行多重比较。为了确定组中平均值变化是否存在差异,使用配对t检验或wilcoxon符号秩检验进行了分析。在分类数据的情况下,提出了技术统计数据(频率、百分比),并使用卡方检验或fisher精确检验在三个组之间进行比较统计检验。
实施例3:功效评价结果
(1)通过dxa测得的体脂肪和瘦体重
对于99位8itt分析对象,与基准时间相比12周时的体脂肪平均变化在高剂量组中增加了0.25±1.34kg,在低剂量组中增加了0.16±0.91kg,在对照组中增加了0.95±1.65kg,显示出三个组之间的统计学上的显著差异(p-值=0.0358)。此外,与基准时间相比,对照组在12周前后显示出统计学上的显著差异(p-值≤0.0001)。
瘦体重项目的平均变化在三个组之间没有统计学上的显著差异,在对照组中,与基准时间相比,12周时的平均变化降低了-0.61±1.28kg,因此显示出统计学上的显著差异(p-值=0.0048)。通过dxa测得的体脂肪的结果示于下表3中。
【表3】
p-值(a):anova
p-值(b):配对t检验
1)kruskal-wallis检验
2)wilcoxon符号秩检验
+p-值<0.05,统计学上显著的,采用tukey法的事后比较(posthoc)方法低剂量组与对照组
对于通过dxa测得的体脂肪项目,与基准时间相比,12周时的变化显示出三个组之间的统计学上的显著差异。在对照组中,在施用前后体脂肪的增加显示出统计学上的显著差异。然而,阿洛酮糖低剂量组和高剂量组均略有增加,但施用前后没有统计学上的显著差异。
在对照组中,在12周后,瘦体重减少了-0.61±1.28kg,但是阿洛酮糖施用组在施用前后没有显示出差异。由于超重被纳入本研究的受试者选择标准,所有受试者均属于轻度肥胖组(平均体重指数为27或更低),并且认为由于每个组的受试者数不足,未能观察体重或体重指数的统计学上的显著变化。肌肉质量的减少受到抑制。
(2)葡萄糖指数
作为对99名itt分析对象的葡萄糖指数测试的结果,在葡萄糖、胰岛素和hba1c的所有项目上,高剂量组、低剂量组和对照组之间的、与基准时间相比12周时的平均变化的差异并不显著,且组内的施用前后的差异不是统计学上显著的,因此在血糖正常的分析对象中没有降血糖效果。下表4、表5和表6示出了分析对象的葡萄糖指数分析的结果。
【表4】
p-值(a):kruskal-wallis检验
p-值(b):wilcoxon符号秩检验
1)anova
2)配对t检验
【表5】
p-值(a):kruskal-wallis检验
p-值(b):wilcoxon符号秩检验
1)anova
2)配对t检验
【表6】
p-值(a):kruskal-wallis检验
p-值(b):wilcoxon符号秩检验
1)anova
2)配对t检验
(3)肝脏ct
作为对99名itt分析对象进行的ct测试的结果,在所有项目上,与基准时间相比12周时的平均变化在三个组之间未显示出统计学上的显著差异。所有的肝脏hu平均值、肝脏-脾脏hu和肝脏/脾脏hu项目在肝脏ct中均呈下降趋势,并且在施用前后均显示出统计学上的显著差异(p-值=0.0300,0.0027,0.0029)。
【表7】
+肝脏和脾脏的差(肝脏减脾脏)
++肝脏和脾脏的比(肝脏与脾脏之间的比值)
§r012受试者被排除在测试之外,因为未在基准时间测量脾脏扫描。
p-值(a):kruskal-wallis检验
p-值(b):wilcoxon符号秩检验
1)anova
2)配对t检验
(4)血液化学检测结果
分析在每个血液化学检测项目上各组之间的、与基准时间相比12周时的平均变化的差异,血液化学检测项目中的碱性磷酸酶(p-值≤0.0001)、alt(sgpt)(p-值=0.0127)和γ-gtp(p-值=0.0043)在三个组之间显示出统计学上的显著差异。
碱性磷酸酶和γ-gtp在三个组中显示出统计学上的显著差异,因为在高剂量组和低剂量组中它们降低了,且在高剂量组和低剂量组中在施用前/后显示出统计学上的显著差异,而在对照组中它们都升高了。alt在三个组之间显示出统计学上的显著差异,因为在高剂量组和低剂量组中alt降低了,而在对照组中则升高了,在高剂量组中在施用前/后alt显示出统计学上的显著差异。
【表8】
p-值:anova
1)kruskal-wallis检验
*p-值<0.05,统计学上显著的
碱性磷酸酶和γ-gtp项目在三个组之间显示出统计学上的显著差异,因为在高剂量组和低剂量组中它们均降低了,而在对照组中它们均增加,且在高剂量组和低剂量组中在施用前/后显示出统计学上的显著差异。alt在三个组之间显示出统计学上的显著差异,因为在高剂量组和低剂量组中alt降低了,而在对照组中则升高了,在高剂量组中施用前/后的alt显示出统计学上的显著差异。在该检测中,反映肝功能的血液肝酶指标通常在服用阿洛酮糖后显示出改善的结果,非酒精性脂肪肝疾病被认为是由肥胖引起的代谢综合征的另一个表型。总之,对上述身体成分的分析结果表明,阿洛酮糖抑制了体脂肪的蓄积和肌肉质量的减少。
实施例4:安全性试验
在安全性理化试验中,低剂量组和高剂量组各项检查意见均为正常或为无临床上显著的异常,三个组之间没有统计学上的显著差异。十二(12)个特定理化试验项目(itt、耳/鼻/喉、眼睛/头/颈部、心血管系统、腹部、呼吸系统、乳房/生殖器、神经系统、淋巴结、皮肤、肌肉骨骼等)被分为“正常、异常(非临床上显著的)和异常(临床上显著的)”三(3)类,并且所有项目的检查意见均为正常或为无临床上显著的异常。三个组之间没有统计学上的显著差异。
此外,在生命体征的试验结果中,在与基准时间相比8周时,高剂量组中收缩压的平均变化降低了4.15±10.30mmhg,低剂量组中收缩压的平均变化降低了2.67±9.71mmhg,对照组中收缩压的平均变化升高了1.73±9.63mmhg,在三个组之间显示出统计学上的显著差异(p-值=0.0349)。三个组之间的舒张压和脉搏率未显示出统计学上的显著差异。
此外,在实验室试验中分析了三个组之间的、在与基准时间相比12周时各项目的平均变化的差异。在血液化学检测项目中,碱性磷酸酶(p-值≤0.0001)、alt(sgpt)(p-值=0.0127)和γ-gtp(p-值=0.0043)在三个组之间显示出统计学上的显著差异。比较尿液检测的正常性的结果为,没有临床上显著异常的受试者,并且所有项目在三个组之间均未显示出统计学上显著的差异。
- 还没有人留言评论。精彩留言会获得点赞!