东莨菪素在制备抑制神经炎症药物中的应用的制作方法
本发明涉及东莨菪素在抑制神经炎症以及预防和/或治疗由神经炎症导致的急慢性神经退行性疾病中的应用,尤其是一种东莨菪素在制备抑制神经炎症药物中的应用。
背景技术:
神经退行性疾病(neurodegeneration disorders,ND)是一组以原发性神经元变性为基础的慢性进行性神经系统疾病,主要包括阿尔茨海默病(Alzheimer’s disease,AD)、帕金森病(Parkinson’s disease,PD)、多发性硬化症(multiple sclerosis,MS)、亨廷顿氏舞蹈症(Huntington’s disease,HD)等。随着世界人口的老龄化,神经退行性疾病的发病率呈明显上升趋势,如我国60岁以上人群的AD患病率是5.1%,85岁以上者患病率是30%,全国患病人数在800万人以上,而全世界约有3500万AD病人。PD的患病率仅次于AD,主要发生于中年以上人群,65岁以上人群中患病率为2%。患者发病后病情呈进行性加重,逐渐丧失独立生活能力,最终因并发症而死亡。由于ND发病机制复杂、部位特殊,至今仍缺乏有效的治疗药物。因此,寻找一种安全性高、能够防治ND的新药已经迫在眉睫。
大量临床研究和动物实验证据表明,脑内神经炎症与多种急慢性神经退行性疾病如阿尔茨海默病、帕金森病、多发性硬化症和亨廷顿氏舞蹈症等的发生和发展密切相关。炎症反应介导的神经退行性病变主要是由小胶质细胞的活化继而导致炎症因子如NO、ROS、TNF-α、IL-1β等过量释放所引起的。有研究发现,抑制神经炎症反应能减弱受损脑区的神经元病变或者推迟神经退行性疾病的进程。因此,寻找和研究脑内神经炎症抑制剂,对于开发具有治疗多种急慢性神经退行性疾病的新型药物具有重要的意义。
中药是中华文明历经千年流传下来的宝贵文化遗产,中药中的天然化合物不仅来源具有生物多样性,而且代谢产物结构复杂多变,蕴含着无穷无尽的结构多样性。从中药所含的天然化合物中筛选能够抑制神经炎症的化合物是该领域药物研发的重要途径。
东莨菪素结构上属于香豆素类化合物,其在茄科和伞形科植物中的含量较高。药用的东莨菪素则大部分提取自旋花科植物(丁公藤、光叶丁公藤等)与伞形科植物(防风、白云花等)。现有的研究发现,东莨菪素具有抗癌、降血压、降血脂、降血糖、抗关节炎以及抗氧化等药理活性。但目前未见东莨菪素用于防治神经炎症相关疾病的报道。
技术实现要素:
本发明的目的是提供一种东莨菪素在制备抑制神经炎症药物中的应用,东莨菪素具有显著的抑制神经炎症活性,能够用于制备预防和/或治疗神经炎症及其相关疾病的药物。
东莨菪素在制备抑制神经炎症药物中的应用,其中东莨菪素的结构式如下:
一种东莨菪素在制备预防或治疗由神经炎症导致的急慢性神经退行性疾病药物中的应用,其中东莨菪素的结构式如下:
其中神经退行性疾病包括帕金森病、多发性硬化症和亨廷顿氏舞蹈症。
本发明首次通过药理实验证明东莨菪素具有显著的抑制神经炎症活性,可用于制备预防和/或治疗神经炎症及其相关疾病的药物,因此其具有较高的临床应用价值和开发前景。
本发明公开了东莨菪素在抑制神经炎症方面的新用途。通过药理实验证明:东莨菪素可显著抑制LPS诱导的小胶质细胞炎症介质NO、ROS、TNF-α和IL-1β的释放,具有显著的抑制神经炎症活性。因此,该化合物可用于制备预防和/或治疗神经炎症以及相关的中枢神经退行性疾病的药物,具有较高的临床应用价值和开发前景。
附图说明
图1是本发明实施例1中不同处理组的小胶质细胞NO浓度的统计结果图;
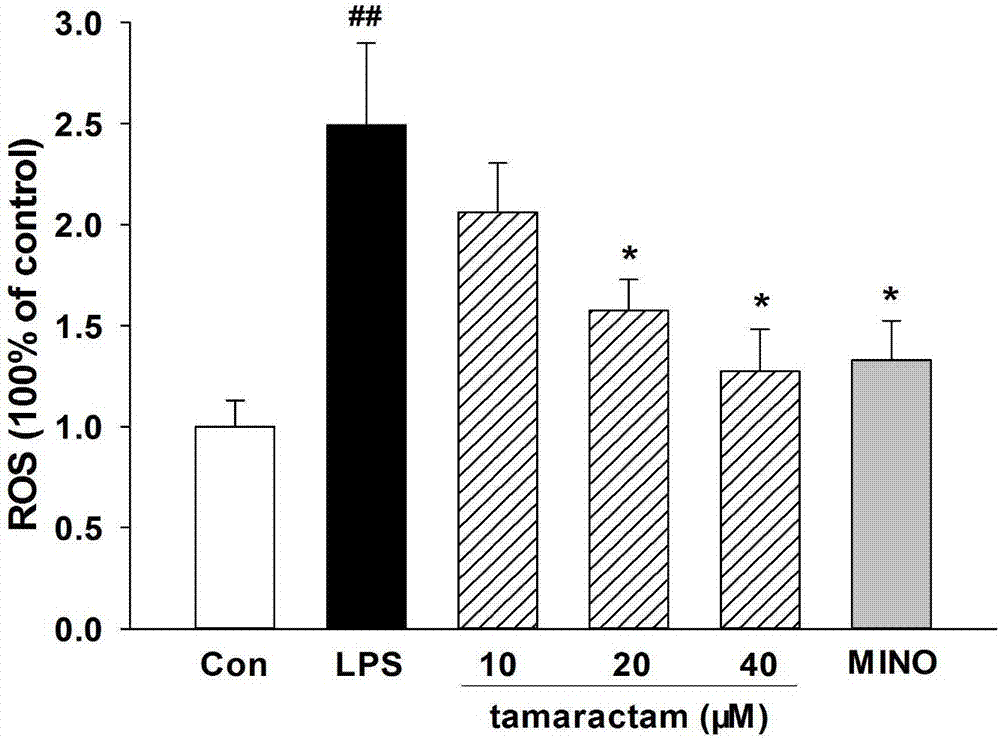
图2是本发明实施例2中不同处理组的小胶质细胞ROS含量的统计结果图;
图3是本发明实施例3中不同处理组的小胶质细胞TNF-α浓度的统计结果图;
图4是本发明实施例3中不同处理组的小胶质细胞IL-1β浓度的统计结果图。
具体实施方式
本发明提供了一种东莨菪素在抑制神经炎症以及预防和/或治疗由神经炎症导致的急慢性中枢神经退行性疾病中的新用途。
本发明涉及的化合物东莨菪素结构式如式I所示:(东莨菪素购于宝鸡市辰光生物科技有限公司)
本发明所提供的东莨菪素的应用包括两方面:1)为其在制备抑制神经炎症的产品中的应用;2)为其在制备预防和/或治疗由神经炎症导致的急慢性神经退行性疾病的产品中的应用。
具体表现在东莨菪素对细菌脂多糖(LPS)诱导的小胶质细胞一氧化氮(NO)、活性氧(ROS)、肿瘤坏死因子α(TNF-α)和白介素1β(IL-1β)的释放均有显著抑制作用,具有显著的抑制神经炎症活性。
本发明还保护一种抑制神经炎症的产品,它的有效成分为东莨菪素。
此外,以东莨菪素为有效成分制备的预防和/或治疗由神经炎症导致的急慢性神经退行性疾病的产品,也属于本发明的保护范围。
本发明中抑制神经炎症的药物以及预防和/或治疗由神经炎症导致的急慢性神经退行性疾病的药物均可通过注射、喷射、滴鼻、滴眼、渗透、吸收、物理或化学介导的方法导入机体如肌肉、皮内、皮下、静脉、粘膜组织;或是被其他物质混合或包裹后导入机体。
需要的时候,在上述药物中还可以加入一种或多种药学上可接受的载体。所述载体包括药学领域常规的稀释剂、赋形剂、填充剂、粘合剂、湿润剂、崩解剂、吸收促进剂、表面活性剂、吸附载体、润滑剂等。
上述药物可以制成注射液、片剂、粉剂、颗粒剂、胶囊、口服液、膏剂、霜剂等多种形式。以上各种剂型的药物均可以按照药学领域的常规方法制备。
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。
通过以下的实施例对本发明的应用效果做进一步的说明:
实施例1:
Griess比色法考察东莨菪素对LPS诱导的小胶质细胞一氧化氮(NO)释放的抑制作用;
细胞株:小鼠小胶质细胞株BV-2;
药物:LPS;东莨菪素;米诺环素(MINO)。
方法:
(1)小鼠小胶质细胞系BV-2的培养:
细胞培养液以DMEM培养基作为基础配制而成,内含10%FBS、100U青霉素和100U链霉素及50μM 2-巯基乙醇(均为终浓度)。在5%CO2,37℃条件下将BV-2小胶质细胞以约4×105cells/ml的细胞密度置于细胞培养箱中培养,定时观察细胞生长情况,至细胞贴壁面积约占培养瓶底面积50-60%时,以胰酶消化细胞并传代,之后继续培养。取3-7代细胞进行实验。
(2)亚硝酸盐含量的测定:
实验原理:NO含量测定一般是通过检测其稳定的氧化产物亚硝酸盐的含量来确定,利用Griess比色法可以检测培养液中亚硝基NO2-的含量从而确定亚硝酸盐的含量。该测定方法的原理是在弱酸性条件下,对氨基苯磺酸可与溶液中的NO2-发生重氮化反应,生成的重氮盐再与N-(1-萘基)-乙二胺发生偶联反应,生成的偶氮化合物显紫红色,该产物在540~550nm处存在较大吸收峰,使用酶标仪测量产物溶液在540nm处的吸光强度,该吸光度值与溶液中NO2-的含量成正比,由此可以测得NO2-的含量,从而反映出NO生成量的变化。
检测方法:取对数生长期的BV-2细胞,以新鲜的无血清DMEM培养液将细胞接种于96孔板内,细胞密度为3×105cells/ml,接种量100μl/well,置于培养箱内在37℃、5%CO2的条件下培养。细胞贴壁培养3h后小心吸出培养液,按照实验分组,分别换成无血清的DMEM培养液配置的不同药物来孵育细胞,同时设空白对照组,每组设五个复孔,置于37℃培养箱中孵育24h,之后取50μl的细胞培养上清液加入96孔板中,再加入50μl的Griess试剂(以5%磷酸配制的1%对氨基苯磺酸溶液,以蒸馏水配制的0.1%萘乙二胺溶液,使用时将二者1:1等体积混合),室温下反应15min,使用酶标仪测定540nm处吸光度。
NO2-含量与吸光度值的线性关系为:
NO2-浓度(μmol/L)=OD值/0.0099;
实验结果:东莨菪素可显著抑制LPS诱导的小胶质细胞NO的释放。
实施例2:
DCFH oxidation法考察东莨菪素对LPS诱导的小胶质细胞活性氧(ROS)释放的影响;
细胞株:小鼠小胶质细胞株BV-2;
药物:LPS;东莨菪素;MINO。
实验原理:DCFH-DA(2′,7′-dichlorodihydro fluororescein diacetate)可以进入细胞内,经过脱乙酰基反应生成DCFH。DCFH是一种非荧光性物质,它可以被细胞内的ROS氧化生成荧光物质DCF,通过检测荧光强度可反映出ROS释放的量。具体操作步骤为:DCFH-DA以纯甲醇溶解,配制成浓度为10mM的母液,临用前再用Hank's平衡盐溶液(HBSS)将母液稀释500倍至20μM的终浓度。取加药处理过后的BV-2细胞,吸除上清液,用该20μM的DCFH-DA溶液孵育1h,HBSS洗三次以除去未进入细胞内的DCFH-DA,最后用多功能酶标仪检测激发波长485nm、发射波长528nm处的荧光强度。
检测方法:取对数生长期的BV-2细胞,以新鲜的无血清DMEM培养液将细胞接种于6孔板内,细胞密度为3×105cells/ml,接种量600μl/well,置于培养箱内在37℃、5%CO2的条件下培养。细胞贴壁培养3h后小心吸出培养液,按照实验分组,分别换成无血清的DMEM培养液配置的不同药物来孵育细胞,同时设空白对照组,每组设3个复孔,之后吸除上清液,用20μM的DCFH-DA溶液孵育1h,PBS洗去未进入细胞内的DCFH-DA,最后用多功能酶标仪检测激发波长485nm、发射波长528nm处的荧光强度。
实验结果:东莨菪素可显著抑制LPS诱导的小胶质细胞ROS的释放。
实施例3:
ELISA法考察东莨菪素对LPS诱导的小胶质细胞肿瘤坏死因子α(TNF-α)和白介素1β(IL-1β)释放的影响;
细胞株:小鼠小胶质细胞株BV-2;
药物:LPS;东莨菪素;MINO。
检测方法:取对数生长期的BV-2细胞,以新鲜的无血清DMEM培养液将细胞接种于6孔板内,细胞密度为3×105cells/ml,接种量600μl/well,置于培养箱内在37℃、5%CO2的条件下培养。细胞贴壁培养3h后小心吸出培养液,按照实验分组,分别换成无血清的DMEM培养液配置的不同药物来孵育细胞,同时设空白对照组,每组设3个复孔,细胞加药继续培养2~4h后,收集上清液,根据试剂盒说明书中所述ELISA法操作步骤,检测培养上清液中TNF-α和IL-1β的含量。
ELISA法操作步骤:在已包被好抗体的酶标板上加样品和标准品,37℃下孵育90min,之后加入生物素标记抗体,孵育60min,后用PBS洗涤3次。加入过氧化酶标记的亲和素孵育30min后洗涤5次,用TMB显色呈蓝色,之后在酸的作用下转化成黄色,用酶标仪在450nm下测量OD值,OD值与炎症因子含量成正相关,用标准品的OD值数据制作标准曲线,并计算样品中TNF-α和IL-1β的含量。
实验结果:东莨菪素可显著抑制LPS诱导的小胶质细胞炎症因子TNF-α和IL-1β的释放。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
本发明的东莨菪素在制备抑制神经炎症药物中的应用中东莨菪素的剂量为0.5~2.0mg/kg/day,用法为口服。
- 还没有人留言评论。精彩留言会获得点赞!