亚砜类化合物在预防胸腹部肿瘤放疗并发症中的用途的制作方法
本申请要求2018年7月20日提交的,题目为“二甲亚砜在预防放射性口腔黏膜炎中的用途”的中国申请201810800390.9的优先权,其内容援引加入本申请。
本发明涉及医药领域,具体涉及亚砜类化合物,特别是二甲亚砜在将接受放射治疗的肿瘤对象中预防放射性心脏损伤、放射性胰腺损伤和放射性胃炎发生中的用途。
背景技术:
肿瘤放射治疗是利用放射线治疗肿瘤的一种局部治疗方法。射线在杀伤肿瘤细胞的同时对正常细胞亦有杀伤作用,导致受照射的组织器官损伤,出现各种并发症。放射性心脏损伤或称为放射诱发心脏疾病(radiation-inducedheartdisease,rihd)是胸部肿瘤患者进行放疗时经常产生的一种严重副反应。据相关资料显示:胸部实施照射的恶性肿瘤的生存者中30%有放射性心包损害,57%出现照射后的无症状性心功能减退,如照射总剂量超过40~60gy,则有50%发生心肌炎,出现心电图改变的患者更多。
随着放射治疗在肝癌、食管癌、胰腺癌、胆管癌等上腹部肿瘤中的应用,作为相邻器官的胃会受到一定剂量的照射。胃是消化道中对射线最为敏感的组织之一,放射性胃炎是上腹部接受放射治疗后引起的严重并发症。严重的放射性胃炎不仅给患者带来极大痛苦,影响进食,甚至导致放射治疗的中断,从而增加肿瘤复发的机会。
胰腺癌恶性程度高,预后差,治疗效果有限。随着放射治疗技术的不断进步,放射治疗已成为胰腺癌治疗的的重要手段,可改善胰腺癌患者的局控率和生存质量。近年的研究认识到胰腺也是放射敏感器官之一。上腹部肿瘤患者行放疗时,术中放射治疗剂量超过25gy或外照射常规分割剂量超过40gy就会导致放射性胰腺损伤。胰腺损伤主要表现在外、内分泌功能降低,前者发生率远高于后者。据报道螺旋断层调强放射治疗(tomo)高剂量少分次模式放射治疗后重度胰腺外分泌功能不全(epi)发生率为73.3%,严重影响患者的生活质量。
放射性心脏损伤、放射性胰腺损伤和放射性胃炎是胸腹部肿瘤放疗的主要剂量限制组织器官,发病机制复杂,尚缺乏特异性的防治药物。传统治疗方法如高压氧、糖皮质激素、手术等可有效缓解患者临床症状,但无法逆转放射损伤的进程。
考虑到上述方法的这些缺陷,仍然需要开发新的能够预防胸腹部肿瘤放疗并发症发生的药物,特别是能够是在将接受放射治疗的胸腹部肿瘤对象中有效预防放射性心脏损伤、放射性胰腺损伤和放射性胃炎发生的药物。
技术实现要素:
一方面,本发明提供了亚砜类化合物在制备用于预防将接受放射治疗的患胸腹部肿瘤对象的放射性心脏损伤、放射性胰腺损伤和/或放射性胃损伤的药物组合物中的用途。
在一个实施方式中,所述亚砜类化合物选自以下的一种或多种:二甲基亚砜(dmso)、四亚甲基亚砜(tetramethylenesulfoxide)、二乙基亚砜、甲基乙基亚砜,丙亚砜,二异丙基亚砜,正丁基亚砜,二异丁基亚砜,二异戊基亚砜,二苯基亚砜、和二苄基亚砜。
在一个实施方式中,所述亚砜类化合物为dmso或四亚甲基亚砜。在一个实施方式中,所述亚砜类化合物为dmso。
在一个实施方式中,所述胸腹部肿瘤选自以下的一种或多种:呼吸系统肿瘤、消化系统肿瘤、乳腺肿瘤、胰腺肿瘤、纵隔肿瘤、霍奇金淋巴瘤和非霍奇金淋巴瘤。
在一个实施方式中,所述呼吸系统肿瘤选自以下的一种或多种:支气管癌和肺癌。
在一个实施方式中,所述消化系肿瘤肿瘤选自以下的一种或多种:食管癌、胃癌、胰腺癌、肝癌和胆管癌。
在一个实施方式中,所述乳腺肿瘤为乳腺癌。
在一个实施方式中,所述胰腺肿瘤选自以下的一种或多种:胰腺癌、胰腺肉瘤,胰腺囊腺瘤和胰腺囊腺癌。
在一个实施方式中,所述胸腹部肿瘤选自以下的一种或多种:支气管癌、肺癌、乳腺癌、食管癌、胃癌、肝癌、胆管癌、胰腺癌、乳腺癌、胰腺肉瘤,胰腺囊腺瘤、胰腺囊腺癌、纵隔肿瘤、霍奇金淋巴瘤和非霍奇金淋巴瘤。
在一个实施方式中,所述放射性心脏损伤选自以下的一种或多种:放射性心包炎、放射性心肌纤维化、放射性全心炎、放射性无症状性心功能减退、放射性心绞痛、放射性心肌梗死、放射性心电图异常、和放射性瓣膜功能异常。
在一个实施方式中,所述放射性胰腺损伤选自以下的一种或多种:放射性胰腺外分泌功能不全、放射性胰腺内分泌功能不全、和放射性胰腺体积缩小。
在一个实施方式中,所述放射性胃损伤为放射性胃炎。
在一个实施方式中,进一步包括预防将接受放射治疗的患胸腹部肿瘤对象的放射性十二指肠损伤、放射性肝损伤、放射性肾炎和/或放射性肾病。
在一个实施方式中,所述对象为哺乳动物,优选人类。
在一个实施方式中,所述对象为将在8小时内,优选4小时内,更优选2小时内,最优选1小时内接受放化疗的胸腹部肿瘤对象。
在一个实施方式中,所述药物组合物为适合于选自以下一种的给药方式的剂型:静脉注射给药、口腔黏膜给药、经皮给药和口服给药。
在一个实施方式中,所述药物组合物为选自以下的一种剂型:输液剂、注射液、漱口剂,膜剂、气雾剂、片剂、粘附剂、贴剂、舌下剂、崩解剂、棒剂、粉剂、软膏、凝胶、水溶液、混悬液和胶囊剂。
在一个实施方式中,所述药物组合物的施用剂量为0.1-10.0g亚砜类化合物,优选0.2-5.0g亚砜类化合物,更优选0.4-2.0g亚砜类化合物,最优选1.0g亚砜类化合物,以每kg体重计。
在一个实施方式中,所述放射治疗包括使用选自以下放射线的治疗:α射线、β射线、γ射线、x射线、中子、电子线、质子束、粒子束和其组合。
在一个实施方式中,所述放射治疗包括外照射放射治疗和内照射放射治疗。
在一个实施方式中,所述放射治疗方法包括常规分割放射治疗和一次大剂量放射治疗。
在一个实施方式中,所述放射治疗的一次照射剂量为1-50gy,更优选1-8gy,最优选2gy。
在一个实施方式中,所述所述放射治疗包括使用放射增敏剂。
在一个实施方式中,所述放射增敏剂为乏氧细胞放射增敏剂和非乏氧细胞放射增敏剂,
其中所述乏氧细胞放射增敏剂选自以下一种或多种:硝基咪唑类(nitroimidazoles),如甲硝唑、咪嗦哒唑、miso(ro-07-0582)、rsu-1096、替拉扎明(tirapazamine)等;和生物还原剂,如甘氨双唑钠、氮氧化合物、醌类化合物以及烟酰胺及其衍生物;
其中所述非乏氧细胞放射增敏剂选自以下一种或多种:铂类药物,如顺铂、卡铂、奥沙利铂等;抗代谢药物,如5-fu、卡培他滨、吉西他滨等;拓扑异构酶抑制剂,如喜树碱(camptothecin)、伊立替康(irinotecan)、托泊替康(topotecan),cpt417,bms-286309、依托泊苷(vp-16)等;微管稳定药物,如紫杉醇,多西紫杉醇,帕土匹龙(patupilone)、pbox-15等;第二个线粒体来源的胱氨酸酶激活剂(smac)类似物,如tat-smacn7、sm-164、lcl161等;肿瘤靶向治疗药物,如索拉非尼(sorafenib),埃罗替尼(erlotinib),西妥昔单抗(cetuximab),贝伐珠单抗(bevacizumab),曲妥单抗(trastuzumab)等;光敏剂,如5-氨基酮戊酸、血卟啉单甲醚、血卟啉衍生物(hpd)、二血卟啉醚(dhe)、photofrinⅱ等;dna烷化剂,如替莫唑胺等;和中药提取物,如马蔺子素等。
本发明证实亚砜类化合物,特别是dmso对胸腹部肿瘤病人放射性心脏损伤、放射性胰腺损伤和放射性胃炎有很好的预防作用。
附图说明
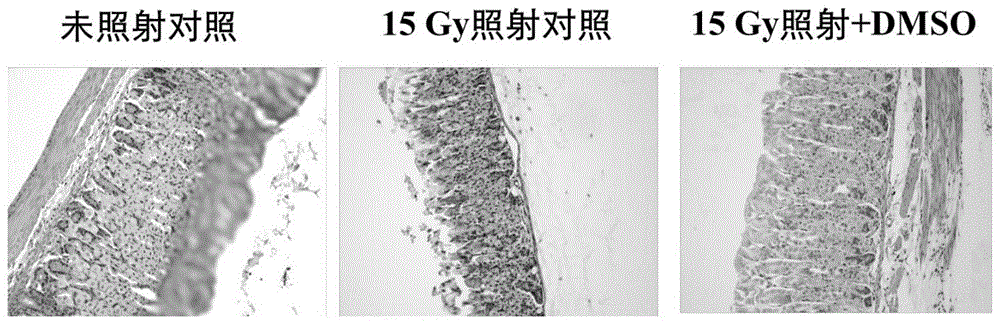
图1:dmso对胸腹部照射小鼠胃黏膜损伤的预防作用
图2a-d:dmso对荷瘤小鼠肿瘤细胞无放射防护作用。
具体实施方式
本发明人在筛选新型放射防护剂的时候,意外发现dmso腹腔给药或口服给药可以有效预防将接受放射治疗的患胸腹部肿瘤对象的放射性心脏损伤、放射性胰腺损伤和放射性胃炎。
第一方面,本发明提供了亚砜类化合物在制备用于预防将接受放射治疗的患胸腹部肿瘤对象的放射性心脏损伤、放射性胰腺损伤和/或放射性胃损伤的药物组合物中的用途。
术语“亚砜类化合物”是含亚硫酰基(>s=o)官能团的一类有机化合物,其通式为r-s=o-r',其中r和r'是有机基团,例如可选被取代的甲基、可选被取代的乙基、可选被取代的丙基、可选被取代的丁基、可选被取代的苯基、可选被取代的烯丙基等。本发明的“亚砜类化合物”是指包含亚砜基团的亚砜类化合物。
术语“二甲亚砜”(dmso)是指以下结构的化合物。
dmso是一种常见的溶剂,常温下为无色无臭的透明液体,热稳定性好且毒性很低。
在一个实施方式中,所述亚砜类化合物选自以下的一种或多种:二甲基亚砜(dmso)、四亚甲基亚砜(tetramethylenesulfoxide)、二乙基亚砜、甲基乙基亚砜,丙亚砜,二异丙基亚砜,正丁基亚砜,二异丁基亚砜,二异戊基亚砜,二苯基亚砜、和二苄基亚砜。在一个实施方式中,所述亚砜类化合物为dmso或四亚甲基亚砜。在一个实施方式中,所述亚砜类化合物为dmso。
术语“对象”是指包括人和非人的哺乳动物,包括但不限于人、猪、狗、兔子、猴子、猫等。本发明的对象选自患有肿瘤的对象。在一个实施方式中,所述对象为人。在本文中,除非特殊说明,术语“对象”、“患者”和“受试者”可以互换。
术语“肿瘤”是指机体在各种致瘤因子作用下,局部组织细胞增生所形成的赘生物。所述肿瘤的定义及分类可参见如由世界卫生组织(who)制定的肿瘤组织学分类第二版(1989-2000年)。在一个实施方式中,所述患肿瘤对象为患胸腹部肿瘤对象。
术语“胸腹部肿瘤”包括例如呼吸系统肿瘤、消化系统肿瘤、乳腺肿瘤、纵隔肿瘤、淋巴瘤等。呼吸系统肿瘤包括例如支气管癌、肺癌等;消化系肿瘤肿瘤包括食管癌、胃癌、胰腺癌、肝癌、胆管癌等。
术语“纵隔肿瘤”是临床胸部常见疾病,包括原发性肿瘤和转移性肿瘤。原发性纵隔肿瘤包括位于纵隔内各种组织结构所产生的肿瘤和囊肿;转移性肿瘤较常见,多数为淋巴结的转移。
术语“淋巴瘤”是起源于淋巴造血系统的恶性肿瘤,根据瘤细胞分为非霍奇金淋巴瘤(nhl)和霍奇金淋巴瘤(hl)两类。
由于人体解剖学位置,放射治疗胸腹部部肿瘤时会对心脏、胰腺和胃造成损伤。
在一个实施方式中,所述呼吸系统肿瘤选自以下的一种或多种:支气管癌和肺癌。在一个实施方式中,所述消化系肿瘤肿瘤选自以下的一种或多种:食管癌、胃癌、胰腺癌、肝癌和胆管癌。在一个实施方式中,所述乳腺肿瘤为乳腺癌。在一个实施方式中,所述胰腺肿瘤选自以下的一种或多种:胰腺癌、胰腺肉瘤,胰腺囊腺瘤和胰腺囊腺癌。
在一个实施方式中,所述胸腹部肿瘤选自以下的一种或多种:支气管癌、肺癌、乳腺癌、食管癌、胃癌、肝癌、胆管癌、胰腺癌、乳腺癌、胰腺肉瘤,胰腺囊腺瘤、胰腺囊腺癌、纵隔肿瘤、非霍奇金淋巴瘤和霍奇金淋巴瘤。
术语“放射性心脏损伤”或称为“放射诱发心脏疾病”(radiation-inducedheartdisease,rihd)是恶性肿瘤如乳腺癌、食管癌、肺癌、纵隔肿瘤、霍奇金病等胸部放疗引发的心脏放射损伤性病变,受损部位包括心包、心外膜、心内膜、甚至含有心脏瓣膜,还有传导系统及冠状动脉的损伤都容易造成放射性心脏损害。受照射后的24h内,患者的心脏就可产生急性反应,迟发性反应约发生在照射后6个月或更长时间后。放射性心脏损伤的表现可以分为心包炎、心肌纤维化或全心炎、无症状性心功能减退、心绞痛与心肌梗死、心电图异常、瓣膜功能异常等类型。放射性心脏损伤患者可以以其中一种或几种为首发症状并贯穿主要临床过程。
术语“放射性心包炎”分急性心包炎与迟发性心包炎两种,也可能以迟发性心包炎急性发作的形式出现,或者呈反复发作的心包炎形式。主要的临床表现为发热,胸痛,乏力等症状,渗出少时可无症状或仅为轻度活动后气短,渗出多时则可以表现为进行性胸闷,呼吸困难等心脏压塞症状。
术语“放射性心肌纤维化或全心炎”临床表现类似缩窄性心包炎,患者以胸闷,气短,乏力等为主诉,伴有颈静脉怒张及周围水肿,肝、肾等脏器淤血的表现。
术语“放射性无症状性心功能减退”表现为患者接受放射治疗后几年甚至几十年的时间内并没有明显的症状发生,但经核素及超声心动图随访可见射血分数有逐渐下降的趋势,还可出现选择性右心功能障碍表现;血流动力学检查可发现右室压力升高,且这种改变与年龄无关。
术语“放射性心绞痛与心肌梗死”是指放射治疗促使冠状动脉粥样硬化及严重狭窄所致的并发症。临床表现同冠心病,可出现反复的心绞痛发作,还曾有过心肌梗死的报道。
术语“放射性心电图异常”表现为患者的心电图异常st-t改变及束支和房室传导阻滞,也可出现期前收缩,个别有发生阿-斯综合征的报道,是放射线损害心肌及传导系统的表现。
术语“放射性瓣膜功能异常”指放射治疗可引起瓣膜增厚,但出现瓣膜功能异常者少见。
在一个实施方式中,所述放射性心脏损伤选自以下的一种或多种:放射性心包炎、放射性心肌纤维化、放射性全心炎、放射性无症状性心功能减退、放射性心绞痛、放射性心肌梗死、放射性心电图异常、和放射性瓣膜功能异常。
术语“放射性胰腺损伤”是恶性肿瘤如胰腺癌、胃癌、肝癌、胆管癌、纵隔肿瘤、霍奇金病等腹部放疗引发的胰腺放射损伤性病变,临床上可表现为胰腺外分泌功能不全和胰腺内分泌功能不全。
术语“放射性胰腺外分泌功能不全”(exocrinepancreaticinsufficiency,epi)是腹部肿瘤患者接受放射治疗时引起的一种并发症,指射线在杀死癌细胞的同时也对正常的胰腺组织造成一定的损伤,进一步影响胰腺癌患者的胰腺外分泌功能,引起人体自身的胰酶分泌不足或胰酶分泌不同步而导致患者出现消化、吸收障碍和营养不良等临床表现。
术语“放射性胰腺内分泌功能不全”(eendocrinepancreaticinsufficiency)是腹部肿瘤患者接受放射治疗晚期出现的一种少见并发症,表现为b细胞功能减低,胰岛素分泌减少,糖尿病发生的风险明显增加。
术语“放射性胰腺体积缩小”指胸腹部肿瘤放疗1年后正常胰腺组织体积缩小,是胰腺功能丧失的一种病理表现。
在一个实施方式中,所述放射性胰腺损伤选自以下的一种或多种:放射性胰腺外分泌功能不全、放射性胰腺内分泌功能不全、和放射性胰腺体积缩小。
术语“放射性胃炎”是上腹部肿瘤放射治疗引起的的最常见并发症之一,其主要临床表现为恶心、呕吐及上腹部胀痛,进食后加重,严重者可表现为胃黏膜出血。早期放射性胃炎主要表现为胃黏膜的急性炎症,黏膜的充血、水肿伴片状渗血,病变常为弥漫性;随着损伤的进一步加重,黏膜下血管也发生病变,最终发展为闭塞性动脉内膜炎、血管炎及内皮增生,导致黏膜缺血、溃疡、毛细血管扩张和纤维化。
在一个实施方式中,所述放射性胃损伤为放射性胃炎。
对于患胸腹部肿瘤的对象,接受放射治疗也会导致对于胸腹部其它器官,例如十二指肠、肝、肾等的损伤。因此,在一个实施方式中,本发明进一步提供了亚砜类化合物在制备用于预防将接受放射治疗的患胸腹部肿瘤对象的放射性十二指肠损伤、放射性肝损伤、放射性肾炎和/或放射性肾病中的用途。
术语“预防”包括降低患有、感染或经历疾病、障碍、病症或病征、其发展和/或进展、和/或其症状的风险。预防的效果可包括潜在疾病的部分的或完全的预防。在本发明中,术语预防无意指疾病被完全避免。在本发明中,术语“预防”不包括对于疾病的治疗。在本发明中,亚砜类化合物(优选dmso)以及包含其的药物需要在疾病发作之前被施用,具体为在对象接受放射治疗前被施用。在一个实施方式中,对象接受放射治疗前接受亚砜类化合物(优选dmso)可选地包括对象同时接受放射治疗和亚砜类化合物(优选dmso)。本发明证实通过在放射治疗前对患肿瘤对象施用亚砜类化合物(优选dmso),可以有效预防所述患肿瘤对象在接受放射治疗后发生放射性心脏损伤、放射性胰腺损伤和放射性胃炎。
在一个实施方式中,所述患肿瘤对象为将在8小时至1小时内接受放射治疗的胸腹部肿瘤对象。在一个实施方式中,所述患肿瘤对象为将在6小时内接受放射治疗的胸腹部肿瘤对象。在一个实施方式中,所述患肿瘤对象为将在5小时内接受放射治疗的胸腹部肿瘤对象。在一个实施方式中,所述患肿瘤对象为将在4小时内接受放射治疗的胸腹部肿瘤对象。在一个实施方式中,所述患肿瘤对象为将在3小时内接受放射治疗的胸腹部肿瘤对象。在一个实施方式中,所述患肿瘤对象为将在2小时内接受放射治疗的胸腹部肿瘤对象。在一个实施方式中,所述患肿瘤对象为将在1小时内接受放射治疗的胸腹部肿瘤对象。在一个实施方式中,所述患肿瘤对象为将在30分钟内接受放射治疗的胸腹部肿瘤对象。
术语“剂量”以向对象施用的亚砜类化合物(优选dmso)或药物/药物组合物中所含的亚砜类化合物(优选dmso)的含量计。剂量可根据本领域已知的因素例如待预防的人的疾病状态、年龄、性别和体重而变化。
在一个实施方式中,依据对象的体重确定亚砜类化合物(优选dmso)的剂量。在一个实施方式中,亚砜类化合物(优选dmso)的施用剂量为0.1-10.0g/kg体重。在一个实施方式中,dmso的施用剂量为0.2-5.0g/kg体重。在一个实施方式中,亚砜类化合物(优选dmso)的施用剂量为0.4-2.0g/kg体重。在一个实施方式中,亚砜类化合物(优选dmso)的施用剂量为0.5g/kg体重。在一个实施方式中,亚砜类化合物(优选dmso)的施用剂量为1.0g/kg体重。
术语“放射治疗”包括利用放射线照射肿瘤组织,通过射线激发可直接作用于细胞dna等靶点或与细胞内水分子等相互作用,产生自由基间接作用于细胞dna等靶点,导致肿瘤细胞死亡的肿瘤治疗方法。放射治疗施用的放射线包括放射性同位素产生的α、β、γ射线和各类x射线治疗机或加速器产生的x射线、电子线、质子束及其他粒子束等。放射治疗的作用机制与化学药物治疗不同。在本文中,除非特殊说明,术语“放射治疗”、“放射疗法”和“放疗”可以互换。在一个实施方式中,放射治疗包括使用选自以下放射线的治疗:α射线、β射线、γ射线、x射线、中子、电子线、质子束、粒子束和其组合。
放射治疗技术分为外照射和内照射。外照射放射治疗指射线从体外经由身体各种组织进入体内,在肿瘤靶区产生放射效应,杀灭肿瘤。常规外照射放疗是以临床实践经验为基础建立的分割放射治疗(每周5次,每次2gy),被认为是肿瘤放射治疗的标准方法。内照射放射治疗也称为近距离放疗,包括放射性粒子植入放疗和放射性核素靶向肿瘤治疗。
根据照射剂量的不同,放射治疗对象可以分为放射高度敏感肿瘤、放射中度敏感肿瘤和放射低度敏感肿瘤。在一个实施方式中,所述放射治疗的一次照射剂量为1-50gy。在一个实施方式中,所述放射治疗的照射剂量为1-8gy。在一个实施方式中,所述放射治疗的照射剂量为2gy。
术语“化疗治疗”又称为“化疗”或“化学药物治疗”,其是指使用化学治疗药物杀灭癌细胞达到治疗目的的手段。术语“放射和化疗联合治疗”是指共同采用放射治疗和化学治疗的方法治疗肿瘤。放化疗联合治疗是临床肿瘤治疗中应用最广的治疗手段之一。放化疗联合治疗就是利用放疗治疗直接打击肿瘤的病灶部位,而化疗治疗对患者体内的癌细胞进行消灭,从而达到治疗的效果。在本发明中,将接受治疗的对象预期将会同时接受放射治疗和化学治疗,或者先接受放射治疗随后再接受化学治疗,或者先接受化学治疗随后再接受放射治疗;前提是上述治疗均在接受本发明的亚砜类化合物(优选dmso)之前进行。
在一个实施方式中,所述将接受放射治疗的患胸腹部肿瘤对象可选地将进一步接受化疗治疗,包括同时接受放化疗联合治疗,或者在接受放射治疗后接受化疗治疗,或者在接受放射治疗前接受化疗治疗。
在一个实施方式中,可以用于化学治疗药物包括但不限于:直接作用于dna的烷化剂或铂化合物,如美法仑(melphalan)、环磷酰胺(cyclophosphamide)、氧氮磷杂环己烯(oxazaphosphorine)、顺铂(cisplatin)、卡铂(carboplatin)、奥沙利铂(oxaliplatin)、沙铂(satraplatin)、四铂(tetraplatin)、异丙铂(iproplatin)、丝裂霉素(mitomycin)、链佐星(streptozocin)、卡莫司汀(carmustine)(bcnu)、洛莫司汀(lomustine)(ccnu)、白消安(busulfan)、异环磷酰胺(ifosfamide)、链佐星(streptozocin)、噻替派(thiotepa)、苯丁酸氮芥(chlorambucil);氮芥,如二氯甲基二乙胺(mechlorethamine);乙烯亚胺化合物;烷基磺酸盐(alkylsulfonate);干扰dna和rna合成的抗代谢药,如阿糖胞苷(cytarabine)、5-氟脲嘧啶(5-fu)、培美曲塞(pemetrexed)、替加氟(tegafur)、尿嘧啶(uracil)、尿嘧啶氮芥(uracilmustard)、氟达拉滨(fludarabine)、吉西他滨(gemcitabine)、卡培他滨(capecitabine)、巯嘌呤(mercaptopurine)、克拉屈滨(cladribine)、硫鸟嘌呤(thioguanine)、甲氨喋呤(methotrexate)、喷司他丁(pentostatin)、羟基脲(hydroxyurea)、或叶酸;通过抑制酶的作用和有丝分裂或改变细胞膜来干扰dna的抗肿瘤抗生素,福来霉素(phleomycin)、博来霉素(bleomycin)或其衍生物或其盐、chpp、bzpp、mtpp、bapp、利苯霉素(liblomycin)、利福霉素(rifamycin)、放线菌素(actinomycin)、甲烯土霉素(adramycin)、阿霉素、表阿霉素、吡喃阿霉素、柔红霉素、丝裂霉素;来源于动植物成分的植物类抗癌药:如紫杉醇(paclitaxel)[泰素(taxol)]、多西紫杉醇(docetaxel)或泰索帝(taxotere);长春花生物碱,如诺维本(navelbine)、长春碱(vinblastin)、长春新碱(vincristin)、长春地辛(vindesine)或长春瑞滨(vinorelbine);托酚酮生物碱,如秋水仙碱(colchicine)或其衍生物;大环内酯(macrolide),如症登素(maytansine);柄型菌素(ansamitocin)或根霉素(rhizoxin);抗有丝分裂肽,如拟茎点霉毒素(phomopsin)或朵拉司他汀(dolastatin);表鬼臼毒素或鬼臼毒素衍生物,如依托泊苷(etoposide)或替尼泊苷(teniposide);斯的甘辛(steganacin);抗有丝分裂氨基甲酸酯衍生物,如考布他汀(combretastatin)或安非替尼(amphetinile);丙卡巴肼(procarbazine);喜树碱(camptothecin),如依立替康(irinotecan)(盐酸伊立替康和山梨醇注射剂camptosar)或托泊替康(topotecan);激素类抗肿瘤药,如孕酮或雌激素,如雌氮芥(t-66)或甲地孕酮(megestrol);抗雄激素,如氟他胺(flutamide)、康士德(casodex)、尼鲁米特(anandron)或醋酸环丙孕酮(cyproteroneacetate);芳香酶抑制剂,如氨鲁米特(aminogluthetimide)、阿那曲唑(anastrozole)、福美坦(formestan)或来曲唑(letrozole);ghrh类似物,如亮丙瑞林(leuprorelin)、布舍瑞林(buserelin)、戈舍瑞林(goserelin)或曲普瑞林(triptorelin);抗雌激素,如他莫昔芬(tamoxifen)或其枸橼酸盐、屈洛昔芬(droloxifene)、曲沃昔芬(trioxifene)、雷洛昔芬(raloxifene)或秦哚昔芬(zindoxifene);17β-雌二醇衍生物,如ici164,384或ici182,780、氨鲁米特(aminoglutethimide)、福美坦(formestan)、法倔唑(fadrozole)、非那雄胺(finasteride)、酮康唑(ketoconazole);lh-rh拮抗剂,如醋酸亮丙瑞林(leuprolide);甾族化合物,如泼尼松(prednisone)、泼尼松龙(prednisolone)、甲泼尼龙(methylprednisolone)、地塞米松(dexamethasone)、布地奈德(budenoside)、氟考龙(fluocortolone)或氟羟氢化泼尼松(triamcinolone);其它杂类抗肿瘤药,如蛋白酶体抑制剂,如波替单抗(bortezomib);酶,如天门冬酰胺酶,聚乙二醇化天门冬酰胺酶(培门冬酶(pegaspargase))或胸苷磷酸化酶抑制剂;干扰素,如干扰素β;白介素,如il-10或il-12;抗-tnfα抗体,如依那西普(etanercept);以及靶向抗肿瘤药物,如vegf受体小分子拮抗剂,如瓦他拉尼(vatalanib)、su-5416、su-6668、su-11248、su-14813、azd-6474,egfr/her2拮抗剂,如ci-1033或gw-2016;egfr拮抗剂,如易瑞沙(iressa)[吉非替尼(gefitineb)zd-1839]、特罗凯(tarceva)、pki-166、ekb-569、hki-272或赫赛汀(herceptin);和靶向癌细胞表面分子的抗体,如阿泊利单抗(apolizumab)或1d09c3等。
在本发明中,亚砜类化合物(优选dmso)可以被制备成为适用于不同施用方式的药物剂型。在一个实施方式中,所述药物为选自适用于以下的一种或多种给药方式的剂型:静脉注射给药、口腔黏膜给药、经皮给药和口服给药。
术语“静脉注射剂型”又称为输液剂,是指由静脉滴注输入人体内大剂量注射液。
在一个实施方式中,所述药物通过静脉注射给药。在一个实施方式中,亚砜类化合物(优选dmso)静脉给药浓度范围为1%-100%,优选5%-50%,再优选10-20%,最优10%。在一个实施方式中,包含亚砜类化合物(优选dmso)的静脉注射剂型可进一步包含注射稀释剂,所述注射稀释剂可选自碳酸氢钠注射液,氯化钠注射液,葡萄糖注射液,枸橼酸钠注射液,甘油磷酸钠注射液,优选1.4%碳酸氢钠注射液。在一个实施方式中,包含亚砜类化合物(优选dmso)的静脉注射剂型可进一步包含注射附加剂,所述注射附加剂可选自渗透压调节剂(葡萄糖、氯化钠、磷酸盐或枸橼酸盐等);ph调节剂(盐酸、硫酸、枸橼酸、氢氧化钠(钾)、碳酸氢钠、磷酸氢二钠、磷酸二氢钠等);助悬剂(丙二醇、甘油、吐温-80、司盘-85、普流罗尼f-68,羧甲基纤维素、海藻酸钠、聚乙烯吡咯烷酮、明胶、甘露醇、山梨醇、单硬脂酸铝、硅油等);和止痛剂(苯甲醇(1%左右)、盐酸普鲁卡因(0.5%-2.0%)、盐酸利多卡因(0.2%-1.0%)、三氯叔丁醇(0.3%-0.5%))。
术语“口腔粘膜给药剂型”是指药物经口腔黏膜吸收后直接进入循环系统的给药剂型。药物经口腔粘膜给药可发挥局部和全身的治疗作用。
在本发明中,适用于口腔粘膜给药的剂型包括局部治疗剂型:漱口剂,膜剂、气雾剂和片剂,优选漱口剂和膜剂;全身治疗剂型:粘附片、贴膏、舌下片和口腔崩解片,优选粘附片和贴膏。
在一个实施方式中,适用于口腔粘膜给药的剂型选自以下:漱口剂,膜剂、气雾剂、片剂、粘附片、贴膏、舌下片和口腔崩解片。
在一个实施方式中,所述药物为选自以下的一种或多种剂型:漱口剂(mouthwash,或oralrinse)、膜剂、气雾剂、片剂、粘附片、贴膏、舌下片、口腔崩解片、棒剂、粉剂、软膏、混悬液、胶囊剂、凝胶、透粘膜贴剂(transmucosalpatches)、透粘膜胶质(transmucosalpectin)、胶片(films)、喷雾剂、胶剂(colloid)、乳剂(emulsion),药膏(ointment)、橡胶膏剂(rubberplaster)、海绵剂(sponge)、霜剂(cream)、乳膏剂(ointment)、糊剂(paste)、涂膜剂和泡沫剂(foam)。
在一个实施方式中,亚砜类化合物(优选dmso)口腔黏膜给药浓度范围为1%-100%,优选5%-90%,再优选10-70%,最优10-50%。
术语“经皮给药”(transdermaldrugdelivery,tdd)是以皮肤为给药途径,连续地将药物传递到皮肤表面或循环系统中,从而发挥皮肤局部或全身治疗的作用的给药方式。
术语“经皮给药系统”(transdermaldrugdeliverysystemtdds)是指在皮肤表面给药,使药物以恒定速度(或接近恒定速度)通过皮肤各层,进入体循环产生全身或局部治疗作用的剂型。
经皮给药系统的剂型包括但不限于膏药、搽剂、涂膜剂、巴布剂、骨架型贴片、膜控型贴片、微乳、脂质体、包合物、前体药物与低并融物等,这些药物可以施用在皮肤较薄的部位,如耳后、臂内侧、胸前区、阴囊等处。
在一个实施方式中,适用于经皮给药的剂型可以选自以下一种或多种:膏药、搽剂、涂膜剂、巴布剂、骨架型贴片、膜控型贴片、微乳、脂质体和包合物。
在一个实施方式中,适用于经皮给药的剂型可以施用在皮肤较薄的部位,如耳后、臂内侧、胸前区、阴囊等处。
经皮给药系统优选基于纳米载体的被动经皮给药系统。在一个实施方式中,基于纳米载体的被动经皮给药系统可以选自以下一种或多种:纳米囊泡(vesicles)、脂质纳米粒(lipidnanoparticles)、微乳(microemulsion)及聚合物类纳米粒(polymericnanoparticles)。
促进药物透皮渗透的方法有化学方法与物理方法。化学方法主要是透皮吸收促进剂,物理方法包括超声波法,离子导入法,电穿孔法等。
促渗剂是指能帮助药物穿过皮肤角质层和表皮扩散的物质,或称为透皮促进剂、吸收促进剂等。
在一个实施方式中,包含亚砜类化合物(优选dmso)的药物可进一步包含促渗剂。促渗剂可分为亲脂性溶酶类、表面活性剂类、二组分及多组分系统类。在一个实施方式中,所述促渗剂选自以下一种或多种:桂氮卓酮(azone)、亚油酸、尿素、α-吡咯烷酮、丙二醇、丁二醇、二甲基甲酰胺、油酸(oa)、十二醇(la)等;中药促修剂有薄荷油、桉叶油、冰片、松节油、薄荷醇、樟脑、薄荷脑等;n,n-二甲氨基异丙酸十二烷酯(ddaip)和n,n-二甲氨基乙酸十二烷酯(ddaa)。
在一个实施方式中,亚砜类化合物(优选dmso)经皮给药浓度范围为1%-100%,优选5%-90%,再优选25-70%,最优60%。
术语“口服给药剂型”包括水溶液、水性混悬液、片剂和胶囊剂。在一个实施方式中,包含亚砜类化合物(优选dmso)的口服给药剂型可进一步包含矫味剂、抑菌剂等附加剂。术语“矫味剂”是指药品中用以改善或屏蔽药物不良气味和味道,使病人难以觉察药物的强烈苦味(或其它异味如辛辣、刺激等等)的药用辅料,一般包括甜味剂、芳香剂、胶浆剂和泡腾剂四类。
在一个实施方式中,亚砜类化合物(优选dmso)口服给药浓度范围为1%-100%,优选10%-90%,再优选20-70%,最优50%。
在一个实施方式中,所述药物的施用剂量为0.1-10.0gdmso/kg体重,优选0.2-5.0g亚砜类化合物(优选dmso)/kg体重,更优选0.4-2.0g亚砜类化合物(优选dmso)/kg体重,最优选0.5-1.0g亚砜类化合物(优选dmso)/kg体重。
在本发明中,包含亚砜类化合物(优选dmso)的药物可以进一步包含药学上可接受的辅料。在一个实施方式中,所述药学上可接受的辅料选自以下的一种或多种:d-泛醇(dexpanthenol)、海藻酸钠、聚维酮碘(povidoneiodine),透明质酸钠,果胶、粘稠木聚糖和硫糖铝(sucralfate)。在本文中,除非特殊说明,术语“药物”和“药物组合物”可以互换。
在一个实施方式中,包含亚砜类化合物(优选dmso)的药物可进一步与放射增敏剂同时施用。术语“放射增敏剂”是一种化学或药物制剂,当与放射治疗同时应用时可以改变肿瘤细胞对放射的反应性,从而增加对肿瘤细胞的杀伤效应,包括乏氧细胞放射增敏剂和非乏氧细胞放射增敏剂。
在一个实施方式中,放射增敏剂为乏氧细胞放射增敏剂或非乏氧细胞放射增敏剂。在一个实施方式中,乏氧细胞放射增敏剂选自以下:硝基咪唑类(nitroimidazoles),如甲硝唑、咪嗦哒唑、miso(ro-07-0582)、rsu-1096、替拉扎明(tirapazamine)等;和生物还原剂,如甘氨双唑钠、氮氧化合物、醌类化合物以及烟酰胺及其衍生物。在一个实施方式中,非乏氧细胞放射增敏剂选自以下:铂类药物,如顺铂、卡铂、奥沙利铂等;抗代谢药物,如5-fu、卡培他滨、吉西他滨等;拓扑异构酶抑制剂,如喜树碱(camptothecin)、伊立替康(irinotecan)、托泊替康(topotecan),cpt417,bms-286309、依托泊苷(vp-16)等;微管稳定药物,如紫杉醇,多西紫杉醇,帕土匹龙(patupilone)、pbox-15等;第二个线粒体来源的胱氨酸酶激活剂(smac)类似物,如tat-smacn7、sm-164、lcl161等;肿瘤靶向治疗药物,如索拉非尼(sorafenib),埃罗替尼(erlotinib),西妥昔单抗(cetuximab),贝伐珠单抗(bevacizumab),曲妥单抗(trastuzumab)等;光敏剂,如5-氨基酮戊酸、血卟啉单甲醚、血卟啉衍生物(hpd)、二血卟啉醚(dhe)、photofrinⅱ等;dna烷化剂,如替莫唑胺等;和中药提取物,如马蔺子素等。
本发明证实了dmso对于肿瘤细胞本身没有保护作用,但是亚砜类化合物(优选dmso)可以有效预防因肿瘤放疗产生的放射性心脏损伤、放射性胰腺损伤和放射性胃炎。亚砜类化合物(优选dmso)可以显著改善放射引起的心肌酶谱异常和胰腺损伤后生化标志物异常,减轻放射引起的胃粘膜损伤。而且,dmso在预防上的施用时间窗很宽,预期在照射前4小时施用均能起到预防效果。dmso在预防给药有效的剂量范围内,潜在毒副作用低。
实施例
将参考以下实施例更详细地描述本发明。然而,提供以下实施例仅用于解释本发明,不应被理解为是对本发明的范围和精神的限制。
材料和方法:
1.1材料、试剂与仪器
1.1.1实验动物
spf级c57bl/6j雄性小鼠,体重22~24g,购自北京华阜康生物科技股份有限公司,动物质量合格证号:scxk(京)2009-0004。所有动物均在spf级屏障动物房分笼饲养,每笼5只,灭菌水和维持饲料供其自由采食。保持每日开灯12h,关灯12h循环,动物饲养设施合格证号:syxk-(军)-2007-004。小鼠进行约7天的适应性饲养后分组实验。
1.1.2主要试剂
(1)dmso(南京康满林医药科技有限公司):0.9%医用生理盐水溶解成特定浓度,现用现配。
(2)甲醛溶液:量筒取80ml甲醛加入720ml蒸馏水里,配制成10%甲醛溶液。
(3)生化分析试剂,购自迈瑞医疗。
1.1.3仪器与耗材
x射线机(美国radsourcetechnologies,型号rs-2000)。
bs-200全自动生化分析仪(迈瑞医疗)
生物组织自动脱水机(浙江省金华市科迪仪器设备有限公司,型号kd-ts1a)。
生物组织冷冻包埋机(浙江省金华市科迪仪器设备有限公司,型号kd-bm、bl)。
电脑生物组织摊片机(浙江省金华市科迪仪器设备有限公司,型号kd-p)。
电脑生物组织烘片机(浙江省金华市科迪仪器设备有限公司,型号kd-p)。
轮转式切片机(德国leica公司,型号rm2235)。
正置荧光显微镜(德国leica公司,型号db4000)。
数码照相机(日本佳能公司,型号)。
1.2实验方法
1.2.1照射前准备
照射前一周,将实验动物每5只分笼饲养于spf级实验动物中心,标准饲料经60coγ射照射除菌后喂养。照射前两天,将实验动物称重,并根据实验设计随机分组。
1.2.2照射条件
照射前1%戊巴比妥钠(0.2ml/只,腹腔注射)麻醉小鼠,将鼠仰放入自制照射盒,铅板屏蔽头颈部和下腹部(或腹部),照射条件为电压220kv,电流25ma,剂量率1.379gy/min,一次照射剂量分别为12、14和16gy。每次照射6-7只小鼠。
1.2.3生化指标分析
按照bs-200全自动生化分析仪操作手册实施。
1.2.4胃组织病理学观察
脱臼处死小鼠,刨开腹腔取出胃组织,置于4%多聚甲醛中固定7天,经脱水,石蜡包埋后,切片,he染液,光学显微镜下观察胃黏膜的变化。
1.2.5统计学处理
数据结果以x±s表示。应用统计软件spss17.0(spssinc.,chicago)进行数据统计分析,p<0.05认为差异具有统计学意义。
实施例1.dmso对胸部照射小鼠心肌细胞损伤的防护作用
1.实验分组1:
雄性c57小鼠随机抽取分成下列4组:
未照射对照组(non-ir):6只;
未照射dmso组(non-ir):50%dmso生理盐水灌胃给药,每只0.2ml,剂量为10g/kg,6只;
照射对照组(vehicle):0.9%生理盐水灌胃,每只0.2ml,每个时间点6只;
照射dmso组:50%dmso生理盐水灌胃给药,每只0.2ml,剂量为10g/kg,照射前1小时施用,每个时间点6只;
照射剂量:16.0gy胸部照射。
2.实验分组2:
雄性c57小鼠随机抽取分成下列3组:
未照射对照组(non-ir):6只;
照射对照组:0.9%生理盐水灌胃,每只0.2ml,每个时间点6只;
照射dmso组:50%dmso生理盐水灌胃给药,每只0.2ml,剂量为10g/kg,照射前1小时施用,每个时间点6只;
照射剂量:12.0gy胸部照射。
3.实验方法:
参见“材料和方法”部分的1.2节
4.实验结果:
心肌酶谱是心脏疾病临床辅助诊断的系列心肌蛋白酶,包括肌酸磷酸激酶(ck)、肌激酶同工酶(ck-mb)、乳酸脱氢酶(ldh)、α-羟丁酸脱氢酶(α-hbdh)等。当心肌细胞因多种原因发生无菌性炎症(心肌炎)、坏死(心肌梗死)时,心肌细胞中所含的酶类即可进入血中,血液内这些酶的活性增高。研究发现,如表1和表2所示,16gy胸部照射小鼠照后3天和5天心肌酶ldh和a-hbdh的酶活性显著升高,照前给予dmso预防后,ldh和α-hbdh酶活性明显降低;如表3和表4所示,12gy胸部照射小鼠照后3天和5天心肌酶ck和ck-mb的酶活性也显著升高,照前给予dmso预防后,ck和ck-mb酶活性也明显降低。这些结果表明,胸部大剂量照射可引起小鼠心肌细胞损伤,细胞膜结构破坏及通透性增加,最终导致细胞内大量的心肌酶释放入血,照前给予dmso预防后可降低血中心肌酶含量,减轻放射引起的心肌细胞损伤。
表1.dmso对16gy胸部照射小鼠心肌酶ldh的影响
表2.dmso对16gy胸部照射小鼠心肌酶α-hbdh的影响
表3.dmso对12gy胸部照射小鼠心肌酶ck的影响
表4.dmso对12gy胸部照射小鼠心肌酶ck-mb的影响
实施例2.dmso对腹部照射小鼠胰腺细胞损伤的防护作用
1.实验分组1:
雄性c57小鼠随机抽取分成下列3组:
未照射对照组(non-ir):6只;
照射对照组(vehicle):0.9%生理盐水灌胃,每只0.2ml,每个时间点6只;
照射dmso组:50%dmso生理盐水灌胃给药,每只0.2ml,剂量为10g/kg,照射前1小时施用,每个时间点6只;
照射剂量:14.0gy腹部照射。
2.实验分组2:
雄性c57小鼠随机抽取分成下列3组:
照射对照组(vehicle):0.9%生理盐水灌胃,每只0.2ml,每个时间点6只;
照射dmso5g/kg组:50%dmso生理盐水灌胃给药,每只0.2ml,剂量为5g/kg,照射前1小时施用,每组6只;
照射dmso10g/kg组:50%dmso生理盐水灌胃给药,每只0.2ml,剂量为10g/kg,照射前1小时施用,每组6只;
照射剂量:12.0gy腹部照射。
3.实验方法:
参见“材料和方法”部分的1.2节
4.实验结果:
胰腺分为外分泌腺和内分泌腺两部分,其中外分泌腺分泌的胰液中含有胰蛋白酶原、脂肪酶、淀粉酶等。胰腺损伤时如急性胰腺炎,从胰腺腺泡分泌的淀粉酶、脂肪酶、胰蛋白酶原等进入血液;血清α-淀粉酶(α-amy)和脂肪酶(lip)是胰腺急性损伤的生化标志物。研究发现,如表5和表6所示,14gy腹部照射小鼠照后3天和5天血清lip和照后5天血清α-amy酶活性较未照射组显著升高,照前给予dmso预防后,lip和α-amy酶活性明显降低;如表7所示,12gy腹部照射小鼠照前给予dmso5g/kg和10g/kg预防后,照后5天血清lip和α-amy酶活性较照射对照组显著减低,并具有较好的剂量效应。
c反应蛋白(crp)是机体非特异性免疫机制的一部分,crp在健康小鼠血清中浓度很低,而在急性炎症或组织损伤时,其浓度显著升高。如表7所示,12gy腹部照射小鼠照前给予dmso5g/kg和10g/kg预防后,照后5天血清crp含量较照射对照组显著减低,并具有较好的剂量效应。
这些结果表明,腹部大剂量照射可引起小鼠胰腺细胞损伤,导致血中lip、α-amy和crp含量显著增加,照前给予dmso预防后可降低血中lip、α-amy和crp含量,减轻放射引起的胰腺细胞的损伤。
表5.dmso对14gy腹部照射小鼠照后不同时间血清lip的影响
表6.dmso对14gy腹部照射小鼠照后不同时间血清α-amy的影响
表7.不同剂量dmso对12gy腹部照射小鼠胰腺损伤生化标志物的影响
实施例3.dmso对胸腹部照射小鼠胃黏膜损伤的防护作用
1.实验分组:
雄性c57小鼠随机抽取分成下列3组:
未照射对照组(non-ir):3只;
照射对照组(vehicle):0.9%生理盐水灌胃,每只0.2ml,3只;
照射dmso组:50%dmso生理盐水灌胃给药,每只0.2ml,剂量为10g/kg,照射前1小时施用,3只;
照射剂量:15.0gy胸腹部照射。
2.实验方法:
参见“材料和方法”部分的1.2节
3.实验结果:
胃黏膜由上皮层、固有层及黏膜肌层组成。上皮层位于胃黏膜层内面,为单层柱状上皮。胃上皮下陷构成大量的胃腺,如胃底腺、贲门腺、幽门腺,位于固有层内,其分泌液到胃混合后叫胃液。如图1所示,小鼠15gy胸腹部照射照后5天,胃粘膜上皮层结构破坏,固有层胃腺细胞数量减少,炎性细胞浸润,黏膜肌层变薄;照前给予dmso预防后,胃粘膜上皮层结构较完整,固有层胃腺细胞数量显著增加,炎性细胞浸润减少,黏膜肌层增厚,结果表明dmso照前预防给药可显著减轻放射引起的胃黏膜损伤。
实施例4.dmso对荷瘤小鼠的肿瘤细胞没有放射防护作用
1材料及方法
1.1材料与试剂
1.1.1实验动物
雄性balb/c裸鼠,体重22~24g,购自北京华阜康生物科技股份有限公司,动物质量合格证号:scxk(京)2009-0004。所有小鼠均用洁净运输箱送至军事医学科学院实验动物中心spf级屏障动物房后分笼饲养,每笼5只,灭菌水和维持饲料供其自由采食。保持每日开灯12h,关灯12h循环,动物饲养设施合格证号:syxk-(军)-2007-004。小鼠进行约7天的适应性饲养后分组实验。
1.1.2细胞株:人肿瘤细胞株cal27细胞购自武汉大学生命科学学院中国典型培养物保藏中心(细胞库),本实验室保存。
1.1.3试剂及细胞培养相关试剂:dmso(中国伊诺凯化学生物公司,货号d3855),mem培养基(北京中科迈晨公司,货号10010),胎牛血清(fetalbovineserum,fbs)(中国excellbio公司,货号fsp500),0.25%胰蛋白酶消化液(中国excellbio公司,货号03.13005a)。
1.2方法
用lml注射器将配置好的人肿瘤细胞株cal27细胞悬液接种于裸鼠右颈部,每只注射0.2ml(细胞密度1×106/ml),共接种20只裸鼠。接种完毕将裸鼠放回超净层流架,饲养同前。
待裸鼠肿瘤直径达5mm时,荷瘤小鼠腹腔给予dmso(6g/kg)或等量生理盐水,1小时后接受局部屏蔽照射12gy。另两组荷瘤小鼠给予等量dmso(6g/kg)或生理盐水后而不接受照射。每3d观测记录肿瘤大小1次,肿瘤体积用游标卡尺测量,按体积计算公式v=(d1×d1×d2)/2(d1为肿瘤短径,d2为与d1垂直的最长直径)计算肿瘤体积,描绘肿瘤生长曲线图,并用电子天平称量裸鼠体重。待照后30d时,用颈椎脱臼法处死裸鼠,用眼科剪刀,镊子等手术器械将肿瘤组织剥出,电子天平称重。
2结果
非照射的荷瘤小鼠体重随肿瘤的增长而缓慢下降,dmso组和生理盐水对照组之间无明显差异。接受12gy局部照射的两组荷瘤小鼠在照后6天内体重均明显下降,照射对照组小鼠体重一直维持在较低水平,照后25天体重略有回升,并有一只小鼠死亡,而dmso组小鼠照后12天体重明显回升,与照射对照组相比具有显著差异(图2a)。
从图2b-d看出,非照射荷瘤小鼠给予dmso后,瘤体体积以及给药30天后瘤体重量与对照组间没有明显差异。12gy局部照射可明显抑制肿瘤生长,与非照射的两组荷瘤小鼠相比,瘤体体积与照后30天后瘤体重量均明显降低,但dmso预防组与对照组相比仍没有明显差异。这些结果表明dmso预防给药对肿瘤放射治疗的疗效没有影响。
尽管已用于解释说明的目的公开了本发明的优选实施方式,但本领域技术人员可理解,可做出各种改变、增添和替换,而不脱离如后附权利要求所公开的本发明的范围和精神。
- 还没有人留言评论。精彩留言会获得点赞!