一种纳米自组装体及其制备方法与应用与流程
本发明涉及光学成像领域,具体是一种纳米自组装体及其制备方法与应用。
背景技术:
光动力治疗是一种氧分子参与的伴随生物效应的光敏化反应,其基本原理是在特定波长的光激发下,在肿瘤内富集的光敏剂发生光化学反应,生成单线态氧(1o2)或者超氧自由基
技术实现要素:
本发明的目的在于提供一种纳米自组装体及其制备方法与应用,通过胰岛素样生长因子1与两亲性聚合物进行化学耦合,制备得到主动靶向肝癌细胞的两亲性聚合物,将有机染料与abc-igf1混合,通过自组装技术形成主动靶向肝癌细胞光响应性纳米自组装体,不仅可以有效提高有机染料的稳定性和光学活性,还赋予其主动靶向肝癌细胞的能力;在激光的照射下可产生大量单线态氧有效抑制肝癌细胞增殖,进而应用于肝癌的治疗。
本发明的目的可以通过以下技术方案实现:
一种纳米自组装体,所述自组装体为igf1与abc进行化学耦合,并与dye自组装而成,igf1为胰岛素样生长因子1,dye为有机染料,abc为两亲性聚合物。
进一步的,所述abc为羧基聚乙二醇、聚乳酸-羟基乙酸共聚物、海藻酸钠、透明质酸、肝素、硫酸软骨素、聚乙醇酸、聚天冬氨酸、聚赖氨酸、聚谷氨酸、聚丙烯酸中的一种或多种组合。
进一步的,所述dye为2,5-二(4-溴丁基)-3,6-二(2-噻吩基)-2,5二氢吡咯并[3,4-c]吡咯-1,4-二酮、3,6-二(2-噻吩基)-2,5-二氢吡咯并[3,4-c]吡咯-1,4-二酮、卟啉、二氢卟吩、吲哚菁绿、ir783、ir820、ir780中的一种或多种组合。
进一步的,所述abc的分子量范围为1000-100000。
一种纳米自组装体的制备方法,所述自组装体的制备方法具体包括以下步骤:
s1:将abc、edc与hobt共同溶解于n,n-二甲基甲酰胺溶液中,abc、edc和hobt的摩尔比为1:(1-10):(1-10);在20-55℃条件下搅拌反应1-5h后,得到活化的abc溶液;
s2:将igf1加入活化的abc溶液,igf1与活化的abc溶液的摩尔比为1:(5-20);反应温度控制在20-55℃之间搅拌2-12h,得到含有abc-igf1的混合物;
s3:将s2制得的含有abc-igf1的混合物通过硅胶柱,用n,n-二甲基甲酰胺溶液和乙醇混合液洗脱,进行分离纯化,得到纯化后的abc-igf1;n,n-二甲基甲酰胺溶液和乙醇混合液中n,n-二甲基甲酰胺和乙醇的体积比为1:(3-9);
s4:将s3制得的纯化后的abc-igf1用旋转蒸发仪浓缩至1-5mg/ml,加入dye的乙醇溶液搅拌0.5-1h充分混合;其中abc-igf1与dye的摩尔比为100:(0.5-5);
s5:将s4制得的含有abc-igf1与dye的混合液用旋转蒸发仪除去有机溶剂,得到一层abc-igf1与dye混合固化膜;
s6:将s5制得的abc-igf1与dye混合固化膜加入去离子水,置于涡旋振荡器上进行混合,得到dye-abc-igf1自组装体;其中其离子水的体积为1-10ml。
进一步的,所述edc为1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,hobt为1-羟基苯并三唑。
一种纳米自组装体的应用,自组装体用于肝癌细胞、体内、离体实时荧光成像和肝癌光学治疗。
本发明的有益效果:
本发明自组装体通过胰岛素样生长因子1与两亲性聚合物进行化学耦合,制备得到主动靶向肝癌细胞的两亲性聚合物,将有机染料与abc-igf1混合,通过自组装技术形成主动靶向肝癌细胞光响应性纳米自组装体,不仅可以有效提高有机染料的稳定性和光学活性,还赋予其主动靶向肝癌细胞的能力;在激光的照射下可产生大量单线态氧有效抑制肝癌细胞增殖,进而应用于肝癌的治疗。
附图说明
下面结合附图对本发明作进一步的说明。
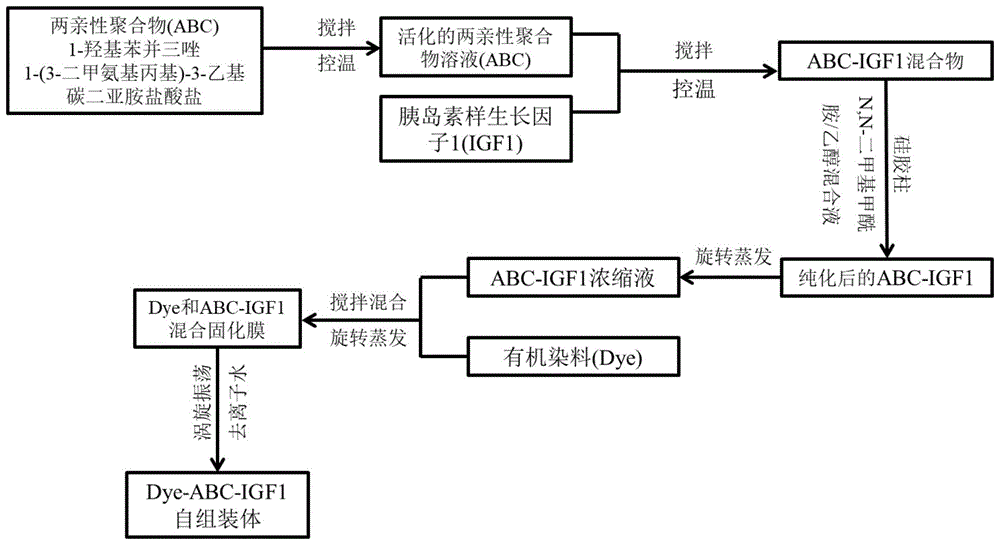
图1是本发明自组装体制备方法的流程图;
图2是本发明自组装体的吸收光谱图;
图3是本发明自组装体的发射光谱图;
图4是本发明自组装体的水合粒径图;
图5是本发明自组装体的单线态氧测定图;
图6是本发明自组装体的体外抑制肝癌细胞增殖图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
一种纳米自组装体,自组装体为igf1与abc进行化学耦合,并与dye自组装而成,igf1为胰岛素样生长因子1,dye为有机染料,abc为两亲性聚合物。
abc为羧基聚乙二醇、聚乳酸-羟基乙酸共聚物、海藻酸钠、透明质酸、肝素、硫酸软骨素、聚乙醇酸、聚天冬氨酸、聚赖氨酸、聚谷氨酸、聚丙烯酸中的一种或多种组合,abc的分子量范围为1000-100000。
dye为2,5-二(4-溴丁基)-3,6-二(2-噻吩基)-2,5二氢吡咯并[3,4-c]吡咯-1,4-二酮、3,6-二(2-噻吩基)-2,5-二氢吡咯并[3,4-c]吡咯-1,4-二酮、卟啉、二氢卟吩、吲哚菁绿、ir783、ir820、ir780中的一种或多种组合。
一种纳米自组装体的制备方法,如图1所示,自组装体的制备方法具体包括以下步骤:
s1:将abc、edc与hobt共同溶解于n,n-二甲基甲酰胺溶液中,abc、edc和hobt的摩尔比为1:(1-10):(1-10);在20-55℃条件下搅拌反应1-5h后,得到活化的abc溶液,edc为1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,hobt为1-羟基苯并三唑;
s2:将igf1加入活化的abc溶液,igf1与活化的abc溶液的摩尔比为1:(5-20);反应温度控制在20-55℃之间搅拌2-12h,得到含有abc-igf1的混合物;
s3:将s2制得的含有abc-igf1的混合物通过硅胶柱,用n,n-二甲基甲酰胺溶液和乙醇混合液洗脱,进行分离纯化,得到纯化后的abc-igf1;n,n-二甲基甲酰胺溶液和乙醇混合液中n,n-二甲基甲酰胺和乙醇的体积比为1:(3-9);
s4:将s3制得的纯化后的abc-igf1用旋转蒸发仪浓缩至1-5mg/ml,加入dye的乙醇溶液搅拌0.5-1h充分混合;其中abc-igf1与dye的摩尔比为100:(0.5-5);
s5:将s4制得的含有abc-igf1与dye的混合液用旋转蒸发仪除去有机溶剂,得到一层abc-igf1与dye混合固化膜;
s6:将s5制得的abc-igf1与dye混合固化膜加入去离子水,置于涡旋振荡器上进行混合,得到dye-abc-igf1自组装体;其中其离子水的体积为1-10ml。
一种纳米自组装体的应用,自组装体用于肝癌细胞、体内、离体实时荧光成像和肝癌光学治疗。
实施例:
本实施例中两亲性聚合物采用羧基聚乙二醇(以下简称peg);有机染料采用2,5-二(4-溴丁基)-3,6-二(2-噻吩基)-2,5二氢吡咯并[3,4-c]吡咯-1,4-二酮(thdpp);
s1:分别称取1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)100mmol,1-羟基苯并三唑(hobt)100mmol和羧基聚乙二醇10mmol混合后溶于20mln,n-二甲基甲酰胺溶液中,在32℃下搅拌1h后得到活化的peg溶液。
s2:将胰岛素样生长因子1(igf1)加入活化的peg溶液中搅拌混合均匀,在30℃条件下反应6h,得到含有peg化igf1,即peg-igf1的混合物。
s3:将上述peg-igf1的混合物采用硅胶柱分离纯化,洗脱剂为n,n-二甲基甲酰胺和乙醇混合液,n,n-二甲基甲酰胺与乙醇体积比为1:5,得到纯化后的peg-igf1溶液。
s4:将装有纯化后的peg-igf1的溶液的圆底烧瓶置于旋转蒸发仪上,除去大部分有机溶剂浓缩至1mg/ml,加入有机染料(thdpp)的乙醇溶液20μl,搅拌1h充分混合,得到peg-igf1与thdpp的混合液。
s5:将装有peg-igf1与thdpp的混合液的圆底烧瓶置于旋转蒸发仪上,除去有机溶剂,得到peg-igf1与thdpp混合固化膜。
s6:将含有peg-igf1与thdpp混合固化膜的圆底烧瓶置于涡旋振荡器上,向其中加入10ml去离子水涡旋振荡进行水化,制备得到thdpp-peg-igf1自组装体。
如图2所示,胰岛素样生长因子1、2,5-二(4-溴丁基)-3,6-二(2-噻吩基)-2,5二氢吡咯并[3,4-c]吡咯-1,4-二酮(thdpp)和thdpp-peg-igf1自组装体在450-900nm的可见吸收光谱图;胰岛素样生长因子1基本没有吸收,2,5-二(4-溴丁基)-3,6-二(2-噻吩基)-2,5二氢吡咯并[3,4-c]吡咯-1,4-二酮和thdpp-peg-igf1自组装体在560nm和612nm有一个明显的吸收峰,表明thdpp-peg-igf1自组装体能够维持thdpp的光学性能;
如图3所示,2,5-二(4-溴丁基)-3,6-二(2-噻吩基)-2,5二氢吡咯并[3,4-c]吡咯-1,4-二酮(thdpp)和thdpp-peg-igf1自组装体在560nm激发下的荧光光谱图;从图中可以看出thdpp和thdpp-peg-igf1自组装体在631nm和680nm发出强烈的荧光,表明thdpp-peg-igf1自组装体适合作为生物成像的造影剂;
如图4所示,thdpp-peg-igf1自组装体的动态光散射粒径分布图;thdpp-peg-igf1自组装体的平均水化粒径为23.2±1.9nm,表明thdpp-peg-igf1是纳米自组装体;
如图5所示,thdpp-peg-igf1自组装体的单线态氧测定图;采用1,3-二苯基异苯并呋喃(dpbf)作为探针考察thdpp-peg-igf1的光动力性质,取20μl游离thdpp和thdpp-peg-igf1溶液(dtdpp浓度为5μg/ml)加入样品瓶中,然后加入dpbf溶液(10mm,1.8ml)混匀,用510nm激光(0.6w/cm2)照射,检测样品在410nm处的吸光度值变化,计算体系中产生的单线态氧(1o2),以去离子水作为阴性对照;去离子水组的吸光度没有发生明显变化,游离thdpp和thdpp-peg-igf1自组装体在激光的照射下产生的单线态氧与dpbf结合后会导致其在410nm处吸收光度降低,表明游离thdpp和thdpp-peg-igf1自组装体在560nm激光的照射下均能够产生单线态氧。
如图6所示,thdpp-peg-igf1自组装体的体外抑制肝癌细胞增殖图;thdpp-peg-igf1溶液用dmem稀释成不同浓度的溶液。hepg2细胞接种于96孔板中并置于二氧化碳培养箱中,37℃下过夜贴壁生长。随后,去除旧培养基并用磷酸盐缓冲液(pbs)洗涤两次,然后加入含有thdpp-peg-igf1自组装体的新鲜培养基继续培养12h后,用560nm激光(60mw/cm2)照射5min,加入mtt(2.5mg/ml,10μl)继续孵育4h。去除培养基,加入150μldmso震荡溶解甲瓒,用酶标仪测定样品在570nm处的吸光度。以pbs组中作为阴性对照计算细胞相对活力;从图中可以看出thdpp-peg-igf1自组装体在暗黑条件下几乎没有细胞毒性,表现出良好的生物安全性,但是在激光照射后hepg2细胞的活力明显降低,并且与thdpp-peg-igf1自组装体的浓度呈正相关趋势。
在本说明书的描述中,参考术语“一个实施例”、“示例”、“具体示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。
- 还没有人留言评论。精彩留言会获得点赞!