一种从含镁碳酸盐矿中提取镁/和联产硫酸钙的方法与流程
本发明属于化工生产技术领域,具体涉及一种从含镁碳酸盐矿中提取镁/和联产硫酸钙的方法。
背景技术:
金属镁及镁化合物产品在国民经济建设中有着举足轻重的作用和地位。我国的镁资源虽然丰富,但由于发展起点较低,生产方式较为粗放,得到的镁盐产品品质低端,应用领域受限。随着社会经济的发展,使得镁盐行业原有技术逐渐向精细化、高附加值、节能环保的技术工艺路线转型。
生产镁化合物的固体矿主要以菱镁矿、白云石矿、水镁石矿。针对固体镁矿资源特别是以菱镁矿和白云石矿为代表的碳酸盐类矿石,为获得其中的镁,传统工艺首先是通过高温煅烧的方式将碳酸镁分解成氧化镁,然后依据不同的产品需求进入后续的处理工艺。
一般含镁碳酸盐矿石的分解都需要较高的温度,如菱镁矿在650℃左右开始分解,完全分解则需约900℃,为得到不同类型的产品,有的煅烧温度甚至近2000℃。白云石由于含有碳酸钙,相应煅烧温度较菱镁矿会更高,工业上常规的煅烧温度在1100~1250℃。因此,含镁碳酸盐矿的煅烧过程是一个高能耗的工艺过程。另外,矿石中其它各类杂质如氧化钙、氧化硅、氧化铁、氧化铝、锰等在煅烧过程中容易被带入产品氧化镁中,这不仅增加了分离提纯的难度,也影响了产品品质。随着镁盐产品的精细化和市场对更多高附加价值的镁盐产品的需求,采用固相煅烧分离难以达到产品要求,研究者们试图通过液相分离的方式,得到高品质的镁盐产品。
为了解决煅烧含镁碳酸盐矿工艺的高能耗及产品品质低的问题,专利cn104843756a提供了一种类似填料塔方案的液相碳酸盐矿的分解方法。该方法将一定粒径的碳酸盐矿石作为填料/反应物装填到反应塔中,然后用铵盐溶液从塔顶进入反应塔参与反应,在一个反应塔内实现碳酸盐矿的分解和氨的回收同步进行。但该方法铵盐及矿石的转化率偏低,并且作为填料的矿石在反应过程中由于反应生成物容易包裹在填料表面阻碍反应,导致固体板结成块,物料反应不彻底,运行效率低,卸料困难。
为了解决上述这种湿法分解填料塔在分解矿石中出现的粒径大、反应接触面小、反应效率低、结块、卸料困难等方面的问题,专利cn105347703a介绍了一种采用铵盐溶液分解钙镁碳酸盐矿的方法。该方法将含镁碳酸盐矿粉与硫酸铵形成的浆料通入多级逆流串联的反应器中反应,解决了填料塔式液相分解运行效率和提取率低、单级反应釜水蒸发量大、碳铵浓度偏低且不稳定等问题。但该方法需采用三个及以上个数的反应釜串联才能达到较好的反应效果,设备投资大,工艺流程长。其次,由于该反应体系的反应温度有接近200℃,压力1.0mpa,固液相体系,釜与釜之间很难找到合适的输送设备实现长期连续稳定的运行。
申请号为2019111830530的发明专利提出了一种从钙/镁碳酸盐矿中提取镁和/或钙的塔式反应器生产碳酸镁和/或碳酸钙。所述反应塔在结构上带有搅拌、多层塔板和特殊气体分布器,从而实现含钙镁矿粉和铵盐溶液及蒸汽良好的气液传质效果,实现连续生产,同时由于蒸汽和物料逆向接触,塔顶可得到高浓度的碳铵蒸汽。但该方案在碳酸盐矿分解过程中出现“拖尾”现象,即随着碳酸盐矿转化率提升,反应速率快速下降,使碳酸镁很难完全分解转化为硫酸镁,因而导致得到的碳酸钙产品中夹带较多的镁,影响其品质。其次,为了实现将so42-全循环,需要将得到的caso4用碳铵溶液置换,得到caco3和(nh4)2so4,由于caco3产品相对caso4并未有明显的增值,因此,在此过程中,增加了工作量,消耗了碳铵,但没有起到增值增效的目的。
综上所述,采用湿法技术从含镁碳酸盐中提取相比较传统高温煅烧技术已有很大的突破和技术改进,但目前已报道的湿法提取技术仍存在一些技术缺陷。结合上述液相提取镁的不同工艺特点,探索一种从碳酸盐矿中高效、低成本、高产出的提取镁的技术仍有很大的提升空间。
技术实现要素:
为了解决上述申请号为2019111830530的专利提到的含镁碳酸盐矿出现的“拖尾”现象,及产物品质低,效益差等问题,本发明提供了一种从含镁碳酸盐矿中提取镁/和联产硫酸钙的方法,该方法通过引入硫酸,碳酸盐矿中镁的提取率和提取效率大幅度提高,产品品质也得到提升,同时优化产品结构,提升经济效益。
本发明通过以下技术方案实现的:
本发明提供一种从含镁碳酸盐矿中提取镁/和联产硫酸钙的方法,包括如下步骤:
1)将硫酸铵溶液和含镁碳酸盐矿粉反应,分别得到碳铵蒸汽,以及,硫酸镁溶液和未反应的含镁碳酸盐矿粉,或者,分别得到碳铵蒸汽,以及,硫酸镁溶液、未反应的含镁碳酸盐矿粉和硫酸钙固体;
mgco3+(nh4)2so4→mgso4+(nh4)2co3/和
caco3+(nh4)2so4→caso4+(nh4)2co3
2)将步骤1)得到的碳铵蒸汽冷凝,得到碳铵溶液;
3)将步骤1)得到的硫酸镁溶液和未反应的含镁碳酸盐矿粉与硫酸溶液反应,得到硫酸镁溶液;或者,将步骤1)得到的硫酸镁溶液、未反应的含镁碳酸盐矿粉和硫酸钙固体与硫酸溶液反应,过滤,分别得到硫酸镁溶液和硫酸钙固体;
mgco3+caco3+h2so4→mgso4+caso4+co2↑+h2o
4)将步骤3)得到的硫酸镁溶液与步骤2)得到的碳铵溶液反应,得到碳酸镁产品和硫酸铵溶液。
mgso4+(nh4)2co3→mgco3+(nh4)2so4
优选地,还包括如下技术特征中的至少一项:
1)步骤1)在反应塔中进行,反应塔塔顶得到碳铵蒸汽,反应塔塔底得到硫酸镁溶液、未反应的含镁碳酸盐矿粉/和硫酸钙固体;
2)步骤3)在硫酸反应釜中进行;
3)步骤4)在碳酸镁合成釜中进行;
4)将步骤3)得到的硫酸镁溶液除杂处理后再与步骤2)得到的碳铵溶液反应。
更优选地,特征4)中,除杂处理为:调节ph值后过滤,或者,调节ph值,加入氧化剂后过滤。有些低价的金属离子需要氧化为高价后沉淀,加入氧化剂的作用是将这些低价金属离子氧化为高价金属离子,例如二价铁、二价锰等,现有技术中能实现此作用的氧化剂均可适用。
进一步更优选地,还包括如下技术特征中的至少一项:
1)ph值为7~9,如7~8、8~8.5或8.5~9;
2)氧化剂加入的量为步骤3)得到的硫酸镁溶液的0.5~10wt‰,如0.5~2wt‰、2~5wt‰或5~10wt‰。
优选地,步骤1)中,还包括如下技术特征中的至少一项:
1)所述含镁碳酸盐矿粉选自白云石和菱镁石中的至少一种;
2)所述硫酸铵溶液的浓度为20~50wt%,如20~35wt%、35~40wt%或40~50wt%;
3)硫酸铵与含镁碳酸盐矿粉中镁/和钙的摩尔比为1:1.8~2,如1:1.8~1.9或1:1.9~2;
4)控制镁的转化率在50~60%之间,如50~55%或55~60%;
5)反应温度为130~250℃,如130~183℃、183~200℃或200~250℃;
6)反应压力为0.4~1.6mpa,如0.4~1mpa、1~1.2mpa或1.2~1.6mpa;
7)反应时间为2~8h,如2~3h、3~4h或4~8h。
优选地,步骤2)中,还包括如下技术特征中的至少一项:
1)冷凝温度为20~50℃,如20~30℃、30~35℃或35~50℃;
2)碳铵溶液的浓度为35~50wt%,如35~45wt%或45~50wt%。
优选地,步骤3)中,还包括如下技术特征中的至少一项:
1)所述硫酸溶液的浓度为40~98wt%,如40~80wt%、80~90wt%或90~98wt%;
2)h2so4与未反应的含镁碳酸盐矿粉中镁/和钙的摩尔比为1~1.2:1,如1~1.1:1或1.1~1.2:1。
优选地,所述方法还包括:将步骤3)得到的硫酸钙固体经后处理得到硫酸钙产品。
优选地,步骤4)中,还包括如下技术特征中的至少一项:
1)反应温度为20~90℃,如20~30℃、30~60℃或60~90℃;
2)硫酸镁和碳铵的摩尔比为1:1.0~1.5,如1:1.0~1.2或1:1.2~1.5。
优选地,所述方法还包括:将步骤4)得到的硫酸铵溶液循环至步骤1)继续和含镁碳酸盐矿粉反应。
与现有技术相比,本发明具有如下有益效果中的至少一项:
1、提高湿法含镁碳酸盐矿中镁的提取效率,减少能耗。由于现有湿法提取碳酸盐矿中镁的技术提取时拖尾严重,如当矿石中镁的提取率达到90%以上,需8~15小时,效率低。本发明引入硫酸,大幅度提高镁的提取效率,如矿石中镁的提取率达到95%以上,只需2~8小时。同时,由于反应时间缩短,单位镁提取所需的能耗也相应减少。
2、将未反应的含镁碳酸盐矿粉/和硫酸钙固体与硫酸溶液反应,可以将残余的碳酸镁固体转化为硫酸镁溶液,使镁分离干净,还可以将硫酸钙中铁、铝等杂质除掉,使硫酸钙产品纯度得到提升,同时可以得到高浓度的硫酸镁溶液,有利用后续工艺。
3、优化产品结构,提升工艺价值和生产效益。原有铵盐湿法提取分离钙镁碳酸盐矿时,为了实现铵盐的循环,必须将硫酸钙转化为碳酸钙,此过程并未产生附加值。由于碳酸镁的价值远高于碳酸钙,增加碳酸镁产能,可大幅度提升工艺的价值。本发明正通过引入硫酸,使碳铵全部转化为高附加值的碳酸镁,碳酸镁的产能翻倍,同时还可联产高品质硫酸钙,优化产品结构,大幅度提升工艺价值和经济效益。
附图说明
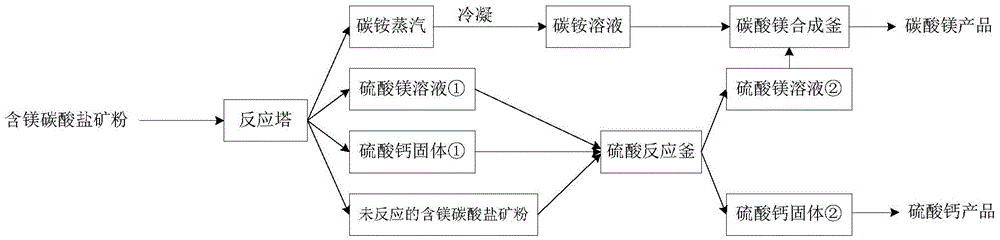
图1是本发明从含镁碳酸盐矿中提取镁和联产硫酸钙的方法示意图。
具体实施方式
以下通过特定的具体实例说明本发明的技术方案。应理解,本发明提到的一个或多个方法步骤并不排斥在所述组合步骤前后还存在其他方法步骤或在这些明确提到的步骤之间还可以插入其他方法步骤;还应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。而且,除非另有说明,各方法步骤的编号仅为鉴别各方法步骤的便利工具,而非为限制各方法步骤的排列次序或限定本发明可实施的范围,其相对关系的改变或调整,在无实质变更技术内容的情况下,当亦视为本发明可实施的范畴。
以上所述,仅为本发明的较佳实施例,并非对本发明任何形式上和实质上的限制,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还将可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。凡熟悉本专业的技术人员,在不脱离本发明的精神和范围的情况下,当可利用以上所揭示的技术内容而做出的些许更动、修饰与演变的等同变化,均为本发明的等效实施例;同时,凡依据本发明的实质技术对上述实施例所作的任何等同变化的更动、修饰与演变,均仍属于本发明的技术方案的范围内。
本发明一实施例提供一种从含镁碳酸盐矿中提取镁和联产硫酸钙的方法,如图1所示,包括如下步骤:
(1)将硫酸铵和含镁碳酸盐矿粉混合均匀后打入反应塔中反应,反应后,反应塔塔顶得到碳铵蒸汽,反应塔塔底得到硫酸镁溶液①、硫酸钙固体①及未反应的含镁碳酸盐矿。
mgco3+(nh4)2so4→mgso4+(nh4)2co3
caco3+(nh4)2so4→caso4+(nh4)2co3
(2)将步骤1)得到的碳铵蒸汽冷凝,得到碳铵溶液;
(3)将步骤1)反应塔塔底得到的硫酸镁溶液①、硫酸钙固体①及未反应的含镁碳酸盐矿转移至硫酸反应釜中,加入硫酸溶液继续反应,反应完全后,过滤,滤液为硫酸镁溶液②,滤渣为硫酸钙固体②。
mgco3+caco3+h2so4→mgso4+caso4+co2↑+h2o
(4)将步骤3)得到的硫酸镁溶液②除杂处理后,与步骤2)得到的碳铵溶液转移至碳酸镁合成釜中反应,得到碳酸镁产品和硫酸铵溶液。
mgso4+(nh4)2co3→mgco3+(nh4)2so4
对比例1
(1)将1.5吨40wt%的硫酸铵溶液与412kg白云石粉(约200目,含氧化镁20%、氧化钙31%)在原料罐混合均匀。其中硫酸铵与白云石中钙和镁的摩尔配比为(nh4)2so4:(ca+mg)=1.05:1。混合均匀的浆料进入反应塔中反应,反应条件控制在反应压力1.0mpa,反应温度160℃,反应时间12h,矿石粉中镁和钙的转化率为90%。反应得到硫酸镁222kg、未反应的白云浆和硫酸钙的混合湿固体及碳铵356kg;
(2)将上步得到的硫酸镁、湿固体分别与碳铵进行如下反应,完成循环过程。
mgso4+(nh4)2co3→mgco3+(nh4)2so4
caso4+(nh4)2co3→caco3+(nh4)2so4
硫酸镁与碳铵反应摩尔配比1:1,反应温度80℃,反应转化率90%,即镁的提取率为90%。反应得到碳酸镁140kg。而反应得到的碳酸钙中还含有未反应的矿石碳酸镁8.2kg(剩余未被提取的部分)。
按照分解效率计算得单位时间碳酸镁产能为11.7kg/h。
实施例1
(1)将813kg40wt%的硫酸铵溶液与412kg白云石粉(约200目,含氧化镁20%、氧化钙31%)在原料罐混合均匀,其中硫酸铵与白云石粉中钙和镁的摩尔配比为(nh4)2so4:(ca+mg)=1:1.8。混合均匀的浆料进入反应塔中反应,反应条件控制在反应压力1.0mpa,反应温度183℃,反应时间4h,矿石粉中镁和钙的转化率为55%。反应得到硫酸镁136kg、硫酸钙177.3kg和碳铵蒸汽,还有约185kg未反应的白云石粉,其中碳酸镁约为78kg,碳酸钙约为107kg;
(2)将步骤1)得到的碳铵蒸汽在30℃下冷凝,得到520kg浓度为45wt%的碳铵溶液;
(3)将步骤1)反应得到的硫酸钙和未反应完全的碳酸盐矿转移至硫酸反应釜中,加入244kg80wt%的硫酸,控制h2so4:(ca+mg)=1.1:1,继续反应,得到247kgmgso4和322kgcaso4。
(4)将步骤3)得到的硫酸镁溶液的ph值控制在7,加入硫酸镁溶液质量10‰的氧化剂,过滤除杂后与步骤2)得到的碳铵溶液混合,控制反应温度为60℃,硫酸镁与碳铵,反应摩尔配比1:1.2,反应得到171kg碳酸镁。
mgso4+(nh4)2co3→mgco3+(nh4)2so4
按照分解效率计算得单位时间碳酸镁产能为42.7kg/h。
实施例2
(1)将1540kg20wt%的硫酸铵溶液与412kg白云石粉(约200目,含氧化镁20%、氧化钙31%)在原料罐混合均匀,其中硫酸铵与白云石中钙和镁的摩尔配比为(nh4)2so4:(ca+mg)=1:1.9。混合均匀的浆料进入反应塔中反应,反应条件控制在反应压力0.4mpa,反应温度130℃,反应时间8h,矿石粉中镁和钙的转化率为50%。反应得到硫酸镁123.6kg、硫酸钙161kg和碳铵蒸汽,还有206kg未反应的白云石粉,其中碳酸镁约为87kg,碳酸钙约为118.5kg;
(2)将步骤1)得到的碳铵蒸汽在35℃下冷凝,得到607kg浓度为35wt%碳铵溶液;
(3)将步骤1)得到的未反应的碳酸镁、碳酸钙和反应得到的硫酸钙转移至硫酸反应釜中,加入244kg98wt%的硫酸,控制h2so4:(ca+mg)=1.1:1,继续反应,得到247kg硫酸镁和322kg硫酸钙。
mgco3+caco3+h2so4→mgso4+caso4+co2↑+h2o
(4)将步骤3)得到的硫酸镁溶液的ph值控制在9,加入硫酸镁溶液质量的5wt‰的氧化剂,过滤除杂后与步骤2)得到的碳铵溶液混合,控制反应温度为90℃,硫酸镁与碳铵反应摩尔配比1:1,反应得到173.6kg碳酸镁。
mgso4+(nh4)2co3→mgco3+(nh4)2so4
按照分解效率计算得单位时间碳酸镁产能为21.7kg/h。
实施例3
(1)将585kg50wt%的硫酸铵溶液与412kg白云石粉(约200目,含氧化镁20%、氧化钙31%)在原料罐混合均匀,其中硫酸铵与白云石中钙和镁的摩尔配比为(nh4)2so4:(ca+mg)=1:2。混合均匀的浆料进入反应塔中反应,反应条件控制在反应压力1.6mpa,反应温度250℃,反应时间2h,矿石粉中镁和钙的转化率为60%。反应得到硫酸镁148.3kg、硫酸钙193.4kg和碳铵蒸汽,还有165kg未反应的白云石粉,其中碳酸镁约为70kg,碳酸钙约为95kg;
(2)将步骤1)得到的碳铵蒸汽在20℃下冷凝,得到510kg浓度为50wt%碳铵溶液;
(3)将步骤1)得到的未反应的碳酸镁、碳酸钙和反应得到的硫酸钙转移至硫酸反应釜中,加入521kg40wt%的硫酸,控制h2so4:(ca+mg)=1.2:1,继续反应,得到247kg硫酸镁和322kg硫酸钙。
mgco3+caco3+h2so4→mgso4+caso4+co2↑+h2o
(4)将步骤3)得到的硫酸镁溶液的ph值控制在8,加入硫酸镁溶液质量2‰的氧化剂,过滤除杂后与步骤2)得到的碳铵溶液混合,控制反应温度为20℃,硫酸镁与碳铵反应摩尔配比1:1.5,反应得到149.4kg碳酸镁。
mgso4+(nh4)2co3→mgco3+(nh4)2so4
按照分解效率计算得单位时间碳酸镁产能为74.7kg/h。
实施例4
(1)将755kg35wt%的硫酸铵溶液与338kg菱镁石粉(约200目)在原料罐混合均匀,其中硫酸铵与菱镁矿粉中镁的摩尔配比为(nh4)2so4:mg=1:2。混合均匀的浆料进入反应塔中反应,反应条件控制在反应压力1.2mpa,反应温度200℃,反应时间3h,矿石粉中镁的转化率为50%。反应得到硫酸镁240kg和碳铵蒸汽,还有169kg未反应的菱镁石粉;
(2)将步骤1)得到的碳铵蒸汽在50℃下冷凝,得到426kg浓度为45wt%碳铵溶液;
(3)将步骤1)得到的未反应的菱镁石粉和反应得到的硫酸镁转移至硫酸反应釜中,加入218kg90wt%的硫酸,控制h2so4:mg=1:1,继续反应,得到480kg硫酸镁。
mgco3+h2so4→mgso4+co2↑+h2o
(4)将步骤3)得到的硫酸镁溶液的ph值控制在8.5,加入硫酸镁溶液质量0.5‰的氧化剂,过滤除杂后与步骤2)得到的碳铵溶液混合,控制反应温度为30℃,硫酸镁与碳铵反应摩尔配比为1:1,反应得到168kg碳酸镁。
mgso4+(nh4)2co3→mgco3+(nh4)2so4
按照分解效率计算得单位时间碳酸镁产能为56.2kg/h。
- 还没有人留言评论。精彩留言会获得点赞!