一种酸性氧化制备六氟锑酸锂的方法与流程
本发明涉及一种六氟锑酸锂的制备方法,特别是在酸性体系用三氧化二锑原料氧化制备六氟锑酸锂的方法。
背景技术:
锂离子电池作为一种先进的新能源装置,具有能量密度高、输出电压高、输出功率大、自放电小、无记忆效应和工作温度范围宽及能快速充放电等优点,因而被广泛应用于电子产品、交通工具、国防军事和航空航天等方面。在锂离子电池的主要组成中,电解质锂盐的研究对推动锂电池的发展具有重要意义(刘旭等.锂离子电池电解质锂盐的研究进展.电源技术,2016,40(01):218-220.)。
目前锂离子电池中主要使用的电解质锂盐分为有机锂盐和无机锂盐,无机锂盐有LiClO4、LiBF4、LiPF6 和LiAsF6这四类,它们的电导率次序为LiAsF6≥LiPF6>LiClO4>LiBF4,热稳定性次序为LiAsF6 >LiBF4>LiPF6,耐氧化性次序为LiAsF6≥LiPF6≥ LiBF4>LiClO4。其中LiClO4氧化性强且有爆炸危险,在商品化电池中已经不再使用,但仍可用于实验室电池测试;LiAsF6具有较高的氧化及还原稳定性,离子导电率高是一种极具有前景的锂盐,然而它本身为含砷化合物,有毒元素砷会对人及环境造成危害进而限制了其商品化应用。
LiBF4比LiPF6具有更好的化学稳定性和热稳定性,因此安全性好。但是其阴离子半径相对较小,与锂离子的相互作用较强,离子导电性较弱,当单独作为电解质锂盐用于锂离子电池的性能较差,所以常作为一种添加性锂盐加入,提高电池的应用温度和循环性能。LiPF6综合性能较好是目前主要使用的锂离子电解质锂盐,具有较高的离子电导率、较优的氧化稳定性和较低的环境污染等优点,但是热稳定性较差,很容易分解为LiF和气体PF5,这限制了锂离子电池对温度的适应性。所以,对新型锂盐的研究与商品化是锂电行业发展的新方向。
六氟锑酸锂(LiSbF6)作为一种重要的锂盐已经应用于锂离子电池研究中。LiSbF6是一种斜六面体结构的晶体,该晶体中Sb-F键长为1.88Å,Li-F键长为2.03Å,Li-Sb-F间的夹角为147.5°,整个晶体结构呈扭曲的立方NaSbF6排列。LiSbF6晶体容易吸水而发生潮解,通常需要在干燥环境中保存。
利用溶剂-模板法将三亚基碳酸酯(p(TMC))(摩尔质量3 × 105 g/mol)与LiSbF6加入到乙腈中,在氮气气氛中搅拌混合形成均匀溶液,然后转移到玻璃模中缓慢地蒸发,除去溶剂后得到厚度为150um的聚合物电解质薄膜(TMC)nLiSbF6,该六氟锑酸锂基电解质的热稳定性更好。在电导率方面还表现为锂盐含量增加后电解质的离子导电率上升,但是也会使热稳定性和机械性能下降。该聚合物电解质薄膜的微电极伏安循测试还表明在电压低于5V(Li/Li+)后电解质的电化学性能稳定不会氧化分解(Silva M M, et al. Novel solid polymer electrolytes based on poly(trimethylene carbonate) and lithium hexafluoroantimonate. Solid State Sciences, 2006, 8(11): 1318-1321.)。
通过溶胶-凝胶法用聚氧乙烯/硅氧烷和LiSbF6形成聚合物电解质(d-U(2000)nLiSbF6)的热分解温度至少可达200℃。玻璃转化温度(Tg)是随着LiSbF6含量的增加而增加,在30℃下d-U(2000)30LiSbF6离子导电率达1.32×10-5S/cm,在95℃下d-U(2000)15LiSbF6的离子电导率为5.62×10-4S/cm,用微电极进行伏安循环测试表现为在5V(vs Li/Li+)以下该电解质能稳定存而不氧化分解(Rodrigues L C, et al. Structural studies of novel di-ureasilormolytes doped with lithium hexafluoroantimonate. Solid State Ionics, 2012, 226(16):7-14.)。
虽然六氟锑酸锂作为电解质用锂盐表现出优良的性能,在电池材料方面具有良好的应用前景。但是有关LiSbF6的制备方法的报道并不多,文献报道了在无水氢氟酸体系中加入SbF5和LiF反应,反应产物经过浓缩结晶析出LiSbF6的方法(Burns J H. The crystal structure of lithium fluoroantimonate(V). ActaCrystallographica, 1962, 15(11): 1098-1101)。该方法采用无水氢氟酸为反应介质,腐蚀性强且条件苛刻,制备成本高。因此,开发一种反应条件温和、综合成本低和产品质量较好的六氟锑酸锂制备方法迫在眉睫。
技术实现要素:
为了克服六氟锑酸锂传统制备方法的不足,本发明提供一种在氢氟酸水溶液中用三氧化二锑氧化制备六氟锑酸锂,且工艺过程短、产品质量好和成本低的制备方法。
为达到上述目的本发明采用的技术方案是:首先三氧化二锑在氢氟酸水溶液中通入双氧水氧化溶解,使水溶液中锑以六氟锑酸形式存在,其次向六氟锑酸溶液中通入硫化氢气体净化脱除重金属杂质,再次向净化后液中加入锂盐中和至要求pH值后得到六氟锑酸锂溶液,最后六氟锑酸锂溶液经过浓缩结晶和干燥得到六氟锑酸锂产品。本发明的实质是利用Sb(Ⅴ)易与F-形成SbF6-配合离子的性质,在氢氟酸水溶液中使三氧化二锑中的Sb(Ⅲ)氧化为Sb(Ⅴ)溶解,六氟锑酸溶液用锂盐中和得到六氟锑酸锂溶液,最后经过浓缩结晶和干燥后得到六氟锑酸锂产品。这些工序紧密关联,共同作用实现了用三氧化二锑氧化制备六氟锑酸锂的目的。
具体的工艺过程和参数如下:
1氧化溶解
三氧化二锑在氢氟酸水溶液中通入双氧水氧化溶解得到六氟锑酸溶液;将三氧化二锑用去离子水浆化,控制水体积L与三氧化二锑质量kg的液固比为1~3/1,然后加入分析纯氢氟酸,氢氟酸质量为三氧化二锑质量的1.8~2.2倍,当温度升高至70~90℃时,向溶液中加入分析纯双氧水,控制双氧水质量为三氧化二锑质量的1.5~2.5倍,待双氧水加入完成后,继续保持溶液温度70~90℃搅拌反应30~90min后,采用真空抽滤方式液固分离,六氟锑酸溶液送净化过程;氧化溶解过程发生的主要化学反应如下:
Sb2O3+6HF=2SbF3+3H2O(1)
SbF3+H2O2+3HF=HSbF6+2H2O(2)
Sb2O3+12HF+2H2O2=2HSbF6+8H2O(3)
2净化
向六氟锑酸溶液中通入H2S气体脱除重金属杂质;上述六氟锑酸溶液升温至70~85℃,然后向溶液中通入H2S气体,控制H2S气体流速为0.05~0.15L/min和反应时间1~10min,继续搅拌60~180min,采用真空抽滤方式实现液固分离,净化后液送中和过程;净化过程发生的主要化学反应如下:
Me2++H2S=MeS↓+2H+(Me为Pb或Fe)(4)
3中和
向净化后液加入锂盐中和至要求pH值得到六氟锑酸锂溶液;净化后液升高温度至70~85℃,然后向溶液中加入碳酸锂或者氢氧化锂中和至pH=6.0~8.0,继续搅拌反应1.0~3.0h,采用真空抽滤方式实现液固分离,中和后液送浓缩结晶干燥过程;中和过程发生的化学反应如下:
HSbF6+LiOH=LiSbF6+H2O (5)
2HSbF6+Li2CO3=2LiSbF6+CO2↑+H2O (6)
4浓缩结晶干燥
中和后液经过浓缩、结晶和干燥得到六氟锑酸锂产品;中和后液加热至80~130℃蒸发浓缩,当料液比重达到1.5~3.0时,降温至25℃冷却结晶,结晶物在温度101~150℃下干燥6~24h得到六氟锑酸锂产品,结晶母液返回净化过程。
本发明所述的三氧化二锑中主要成分质量百分含量为(%):Sb2O3≥99.90、Pb≤0.005和Fe≤0.003。
本发明所述的氢氟酸和双氧水均为分析纯试剂,它们的质量百分含量分别不小于40.0%和30.0%;硫化氢气体纯度大于99.0%。
所述的锂盐为分析纯碳酸锂或氢氧化锂中的一种或两种。
本发明与六氟锑酸锂传统制备方法比较,有以下优点:1、本发明在水溶液体系用锑白氧化制备出六氟锑酸锂产品,产品纯度达到99.9%以上,克服了传统制备方法对非水体系的苛刻要求;2、在氢氟酸水溶液中用双氧水氧化溶解锑白,化学计量准确,锑溶解完全,锑的溶解率达到99.9%;3、采用硫化氢净化脱除重金属杂质,产品中Pb的含量小于0.001%;4、本发明具有工艺过程短、产品质量好和生产成本低等优点。
附图说明
图1:本发明工艺流程示意图。
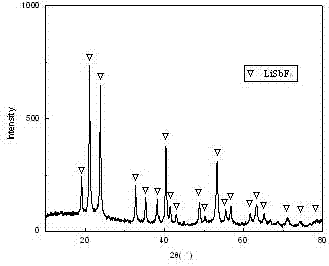
图2:本发明六氟锑酸锂产品的XRD图。
图3:本发明六氟锑酸锂产品的SEM图。
具体实施方式
实施例1:
本发明所述的三氧化二锑中主要成分质量百分含量为(%):Sb2O399.95、Pb0.0045和Fe0.002,分析纯氢氟酸(HF≥40%),分析纯过氧化氢(H2O2≥30%),硫化氢气体纯度大于99.0%。将三氧化二锑用去离子水浆化,控制水体积L与三氧化二锑质量kg的液固比为2/1,然后加入分析纯氢氟酸,氢氟酸质量为三氧化二锑质量的1.8倍,当温度升高至80℃时,向溶液中加入分析纯双氧水,控制双氧水质量为三氧化二锑质量的1.5倍,待双氧水加入完成后,继续保持溶液温度80℃搅拌反应60min后,采用真空抽滤方式液固分离;
六氟锑酸溶液升温至80℃,然后向溶液中通入H2S气体,控制H2S气体流速为0.10L/min和反应时间2min,继续搅拌120min,采用真空抽滤方式实现液固分离;净化后液升高温度至80℃,然后向溶液中加入氢氧化锂中和至pH=7.0,继续搅拌反应2.0h,采用真空抽滤方式实现液固分离,中和后液加热至120℃蒸发浓缩,当料液比重达到2.5时,降温至25℃冷却结晶,结晶物在温度135℃下干燥12h得到六氟锑酸锂产品,结晶母液返回净化过程。
六氟锑酸锂产品的结晶形态和微观形貌分别见图2和图3。图2表明LiSbF6晶体的衍射峰清晰,晶型完整。图3表明LiSbF6晶体呈现规则的六边形,夹杂存在较多细颗粒晶体。
- 还没有人留言评论。精彩留言会获得点赞!