改性的聚(苯乙烯‑共‑马来酸酐)及其用途的制作方法与工艺
改性的聚(苯乙烯-共-马来酸酐)及其用途技术领域本发明涉及改性形式的聚(苯乙烯-共-马来酸酐)。
背景技术:
聚(苯乙烯-共-马来酸酐)是以不同的等级存在的市售的聚合物,具有6%到50%的马来酸酐含量并且分子量在1000到300000g/mol之间。针对亲核试剂,在该共聚物中的马来酸酐基团的高反应性可以根据需要的应用制备具有不同功能性的新材料。聚(苯乙烯-共-马来酸酐)衍生物目前的用途包括处理纸,塑料,玻璃,指甲,头发和其它表面,从而改进这些表面的特性。本发明的目的是提供改性形式的聚(苯乙烯-共-马来酸酐),这使得它可以被用于相同或其它的应用中。
技术实现要素:
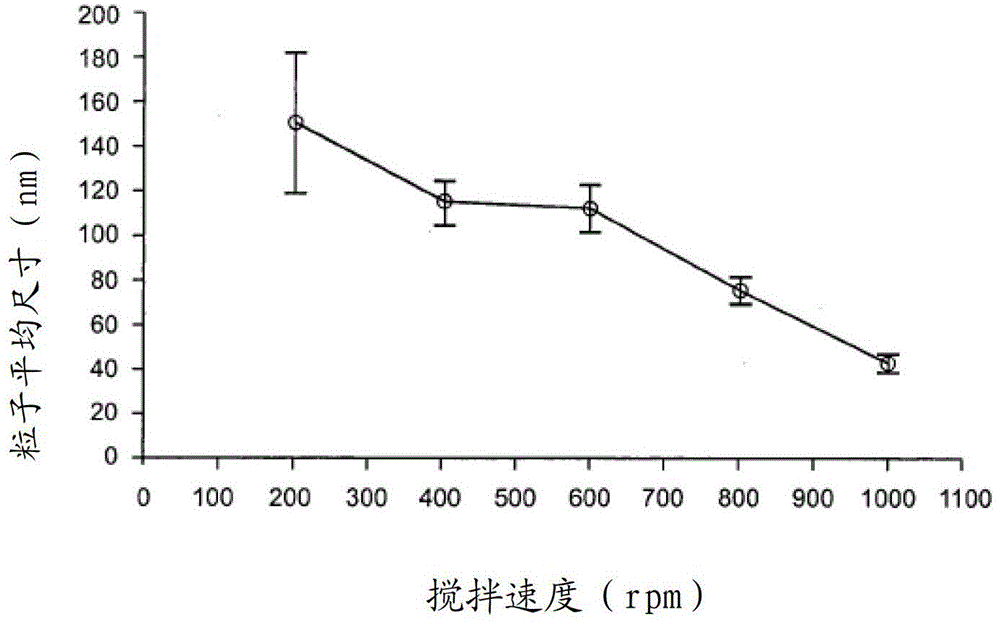
根据本发明的一个方面,提供了一种制备具有下面通式A的聚合物的方法。其中R是烷基链,该烷基链可以是饱和的或不饱和的,并且可以具有被连接到该烷基链的取代基,并且R′和R″选自取代的或非取代的烷基,它们互相可以是相同的或不同的,或者R′和R″被连接以生成含有相邻的氮原子的饱和的或不饱和的环状单体,在该环中具有或不具有额外的杂原子,所述的方法包括将苯乙烯和马来酸酐共聚以生成苯乙烯-马来酸酐共聚物,并且使用适合的取代型胺在水中将该共聚物进行热亚胺化以生成相应的酰亚胺。本发明的另一个特征提供的R是C1到C6烷基链,更优选的是丙基链;并且R′和R″选自C1到C4烷基链,优选甲基和乙基;或者可选的是,R′和R″被连接到一起以生成包括额外的氮原子的环。通式A的聚合物优选以微粒形式提供,较优选是纳米微粒。在磁场可以影响或提高分离技术的情况下,微粒可以包括超顺磁性材料,其中该聚合物优选将该超顺磁性材料封装。该超顺磁性材料可以是磁铁矿。根据本发明的第二方面,提供了一种分离由一种或多种金属构成的或包括一种或多种金属的离子种类的方法,该方法包括将通式A的适合的聚合物与包括需要的离子种类的溶液接触,从而将所需要的种类吸附到该聚合物上;从该溶液中分离该聚合物;并处理该聚合物以回收该需要的金属。本发明的第二方面的另一个特征提供了微粒形式的聚合材料,特别是纳米尺寸的微粒,并且任选包括超顺磁性材料的微粒以通过使用磁场辅助从该溶液中分离可能需要或适合的被装载的聚合材料;提供了要生成阴离子金属络合物的离子种类,例如贵金属的金属络合物,特别是在适合的溶液中的氯化物络合物或氰化物络合物;还提供了要被回收的需要的金属,其通过将该聚合材料用选自硝酸,盐酸,硫酸和酸化硫脲,和特别是具有5到10摩尔HNO3浓度的浓缩硝酸的适合的萃取剂进行萃取回收。下面将参考附图,特别是参考本发明已经证实可进行应用程度的贵金属的分离的应用描述本发明。附图说明其中:图1是根据本发明的聚(苯乙烯-共-马来酰亚胺)纳米粒子的一个实施例的透射电子显微镜(TEM)图像;图2是显示了聚(苯乙烯-共-马来酰亚胺)纳米粒子尺寸作为反应容器的搅拌速度的函数的图表,反应容器是装配有机械搅拌器的双壁油加热的高压锅形式;图3是聚(苯乙烯-共-马来酰亚胺)共聚物(实线)和母体聚(苯乙烯-共-马来酸酐)共聚物(虚线)的FTIR(ATR)光谱;图4是显示了萃取原理的草图,其显示了氯化金与胺功能化的聚(苯乙烯-共-马来酰亚胺)共聚物的质子化的氨基位点的静电互相作用/离子对。M表示位于该聚合物链上的质子化位点的络合的[AuCl4]-阴离子;图5显示了在下列所列的一组特定的条件下从2M的HCl溶液中萃取的金[AuCl4]-(批次吸附);图6显示了使用以下说明的其它试验条件以100rpm和250rpm的转速在不同接触时间下从2HCl萃取的[AuCl4]-的效果;图7显示了最初存在于液相中的[AuCl4]-浓度的平衡以及对于相同系统装载能力的平衡之间的关系;图8显示了对于不同强度的硝酸作为萃取剂从该聚合物中萃取出被吸附的金的效果的柱状图;图9显示了被选择的铂族金属正在装载到正在被试验的聚合物上的柱状图;以及图10显示了从贵金属的混合物中选择的装载的金的柱状图。具体实施例在本发明的一个实施例中,制备具有通式A的聚合物,其中R是丙基,并且R’和R”是甲基和乙基。该化合物在装配有机械搅拌器的用双壁油加热的高压锅中通过聚(苯乙烯-共-马来酸酐)共聚物的热亚胺化获得相应的聚(苯乙烯-共-马来酰亚胺)。具体地,该聚(苯乙烯-共-马来酰亚胺)通过使用二甲氨基丙胺化学修饰聚苯乙烯-共-马来酸酐被合成。该亚胺化反应通常产生包括46±4.9nm的聚(苯乙烯-共-马来酰亚胺)纳米粒子的白色的稳定的分散体,该粒子尺寸取决于使用的搅拌速度。通常的反应条件是在150°–180℃温度下使用5到7巴的压力进行6小时。在亚胺化过程中显示了酰胺化和环化的总反应方程式如下:聚(苯乙烯-共-马来酸酐)和3-二甲氨基-丙胺(1:1)的亚胺化获得了包括良好分散性的纳米尺寸的聚(苯乙烯-共-马来酰亚胺)的稳定的分散体,其粒子尺寸从约200rpm的低搅拌速度下的约150nm到约1000rpm的较高搅拌速度下的约50nm。图1显示了具有77.4±6.08nm的粒子尺寸的产品的透射电子显微镜(TEM)图像。由搅拌速度决定的球形粒子尺寸的变化在图2中显示。注意到在合成过程中随着搅拌速度的降低,聚(苯乙烯-共-马来酰亚胺)纳米粒子的尺寸明显增大。由于纳米粒子提供了高表面积与质量比并且相比较大的粒子其具有较好的萃取效率,因此优选纳米粒子。使用冷冻干燥/真空烤箱干燥技术从该分散体中分离该聚(苯乙烯-共-马来酰亚胺)共聚物以产生细小的白色粉末物质。获得的苯乙烯马来酰亚胺共聚物基质具有叔胺官能团。它具有带有H+的阴离子形式并且具有约50nm的粒子尺寸的该粉末具有4.30±0.40mmol/g的总交换能力。相同粉末的BET比表面积是60±2.20m2/g;平均孔径(BET)是86.94埃;并且BJH孔体积是0.1299cm3/g。如图3所示,聚(苯乙烯-共-马来酸酐)的酸酐单元的特征振动双峰出现在1780和1850cm-1。但是,在和3-二甲氨基-丙胺反应之后,对应于该酰亚胺官能团的新的强烈的宽峰出现在1690和1770cm-1。在胺修饰之后,在1780和1850cm-1没有再观察到明显的双峰,说明聚(苯乙烯-共-马来酸酐)成功并完全转化为聚(苯乙烯-共-马来酰亚胺)衍生物。应该注意的是,在全部例子中都实现了完全的亚胺化。根据反应介质和工艺,制备对磁场易感的聚(苯乙烯-共-马来酰亚胺)的粒子是有利的,并且在这种情况下,可以在该聚合物中封装磁铁矿纳米粒子。该磁铁矿可以通过已知的技术从氨水溶液中的FeCl2和FeCl3中制备出来。随后,过量的氨水被去除,并且磁铁矿分散体可以与苯乙烯和顺丁烯二酸酐的酰胺酸以及脂肪族胺共聚物的溶液混合。可以使用加热以生成聚(苯乙烯-共-马来酰亚胺)。其在水中不能溶解并且自然地生成了可以封装磁铁矿的纳米粒子。这样产生的纳米粒子具有的优点是它们可以由磁场操作。例如,聚(苯乙烯-共-马来酰亚胺)可以通过对悬浮液简单的施加适合的磁场从该悬浮液中去除。当在吸附活性之后,需要从悬浮液中分离该聚(苯乙烯-共-马来酰亚胺)粒子时,这可能是有用的。设计两种方法用于制备包括该聚合物和超顺磁性材料的粒子材料。用于聚(苯乙烯-共-马来酸酐)的一种方法是首先与官能化的胺反应以生成聚(苯乙烯-共-马来酰亚胺)共聚物,随后聚(苯乙烯-共-马来酰亚胺)共聚物在氨水被去除之后与磁铁矿分散体反应。对于全部工艺的其它方法是在氨水中完成的以生成未取代的马来酰亚胺,其易于与甲醛反应并且随后在类似三聚氰胺-甲醛聚合物的生成工艺中与伯胺反应。现在回到以上述方式制备的聚(苯乙烯-共-马来酰亚胺)本身,已经发现这种聚合物对于从酸性水溶液中萃取阴离子氯化金特别有用。在盐酸溶液中,该聚合物的骨架中的胺单体被充分地质子化,这使得溶液中的带负电荷的物质发生交互作用。这一过程在图4中被显示并且萃取机制的简化表示也同时被显示。固相的聚(苯乙烯-共-马来酰亚胺)共聚物材料使用批次吸附技术与10ml(该剂量用于全部例子中除非另有说明)液相的,2M的HCl的氯化金的标准溶液接触。随后,在这个例子中,使用离心和后续的移注将该固相从液相中分离。回收上清液并使用感应耦合等离子体--光学发射光谱法和质量平衡法分析金属含量。应该注意到,作为阴离子物质被萃取的金[AuCl4]-通过图4显示出机制。在萃取之前,该聚(苯乙烯-共-马来酰亚胺)共聚物是白色的,并且在萃取之后,深黄色表示吸附了金。同时已经发现的是,上述的聚合物对于从溶液吸附的其它阴离子贵金属络合物也是有用的。全部萃取过程包括以下的步骤:使用批次吸附技术,将包括金属离子的溶液与该吸附材料接触;从该溶液中分离该被装载的吸附剂;并且从该吸附材料中回收该被吸附的金属。进行一系列的萃取/吸附试验以获得关于阴离子贵金属络合物的萃取效率,萃取和回收的信息。通常影响萃取的因素是要被吸附的金属种类的粒子尺寸,表面积,孔结构,配合基浓度,酸度和本性。通常,吸附平衡和吸附的速度在萃取中被认为是有效的应用。为了确定对于最大装载能力需要的吸附剂的数量,研究了由上述制备的聚(苯乙烯-共-马来酰亚胺)对[AuCl4]-的萃取作为聚(苯乙烯-共-马来酰亚胺)剂量的函数。使用24小时的接触时间以确保吸附平衡已经达到并且使用了包括450mg/l[AuCl4]-的合成原料液。结果在图5中显示并且如预期的示出了[AuCl4]-的吸附取决于吸附剂的质量。如从图5中可以看到的,随着吸附剂剂量的增加,[AuCl4]-的萃取规律性地增加。使用1到7.5mg之间的聚(苯乙烯-共-马来酰亚胺)剂量增加了吸附密度。但是,进一步增加吸附剂的剂量导致了吸附密度的降低。这意味着,对于在试验条件使用的[AuCl4]-浓度,7.5mg的剂量足以针对该吸附剂的有效的胺位点实现饱和状态。这意味着合成原料液中萃取了约57.6%的原始[AuCl4]-。吸附密度的降低可以被归结于这一事实,随着吸附剂的剂量从7.5到100mg的增加,更多的吸附位点保持未饱和状态。显然,50mg的聚(苯乙烯-共-马来酰亚胺)从最初存在于合成原料液中萃取了99.2%(0.992mmol/g)的[AuCl4]-离子。对于超过50mg的剂量,没有观察到萃取效率的明显增加。使用100mg的聚(苯乙烯-共-马来酰亚胺)的吸附剂剂量,从该溶液中萃取了99.6%的[AuCl4]-的最大数量。从这一数据可以看出,50mg的吸附剂足以从溶液中几乎定量萃取[AuCl4]-。研究接触时间(以不同的搅拌速度)对于从溶液中萃取[AuCl4]-的效果以确定后续试验需要的最佳时间。在使用10±0.1和50±0.2mg的聚(苯乙烯-共-马来酰亚胺)剂量的批次吸附过程中分别使用了100和250rpm的搅拌速度。在23±1.0℃的温度,使用含有450mg/L[AuCl4]-的溶液与聚(苯乙烯-共-马来酰亚胺)接触0.5到15分钟。图6显示了萃取动力非常快并且一定程度取决于搅拌速度。该数据显示,使用100rpm的搅拌速度,萃取效率从88到99.8%的增加发生在自0.5分钟的时间。相比较,在250rpm的搅拌速度下,对于相同的时间长度,[AuCl4]-的萃取稍微快些,显示了97.52到99.8%的增加的萃取效率。据信,萃取的非常快速的动力可以归结于:(i)液相中的吸附材料和金属种类之间的碰撞速度;(ii)吸附材料的尺寸—吸附材料的粒子尺寸越小,接近表面积越容易,并且萃取动力的速度越快;(iii)孔隙度-(基于电子显微镜(结果在此未示出),发现每个粒子紧密地聚集以生成薄膜状的结构材料从而几乎生成平坦的表面。但是,复杂材料清晰地显示了中孔的伸长的线(约86埃的孔径尺寸)。这些孔对于吸附的发生提供了极好的条件,因为被吸附物可以同时与许多表面互相作用。);(iv)吸附剂和被吸附物之间的互相作用的本质—互相作用的真正本质取决于被包括的物质的细节,但是预期吸附过程由于静电吸引而发生。图6显示了增加接触时间超过5分钟没有萃取效率的明显变化,显示了仅仅15分钟的较短的暴露时间对于吸附平衡是足够的。因此,除非另有说明,这一时间用于其余的试验工作。研究由聚(苯乙烯-共-马来酰亚胺)吸附的[AuCl4]-的最初金属离子浓度的效果以建立该吸附剂的平衡装载能力。使用从1-935mg/L的变化的最初[AuCl4]-的浓度和10mg的聚(苯乙烯-共-马来酰亚胺)剂量进行试验。图7显示了最初存在于液相中的平衡的[AuCl4]-浓度和平衡装载能力之间的关系。如可以看到的,结果显示被吸附的[AuCl4]-的数量随着最初[AuCl4]-的浓度增加。因此,由聚(苯乙烯-共-马来酰亚胺)吸附的[AuCl4]-的等温线类似朗缪尔型曲线。从1mg/l到约80mg/l,观察到定量萃取。这显示出在这一浓度范围,10mg剂量的聚(苯乙烯-共-马来酰亚胺)足以从溶液中定量萃取出[AuCl4]-。由试验数据值得注意的是,饱和状态没有完全达到,这意味着过量有效的胺位点的存在。通过该结果,发现最大吸附能力是343.9mg/g或1.746mmol/g(每克干燥吸附剂吸附的[AuCl4]-的数量)。应该注意的是,674mg/l的平衡吸附数据点是异常值并且这一差异可能归结于试验误差。为了在萃取之后将聚(苯乙烯-共-马来酰亚胺)材料上残留的被吸附的[AuCl4]-洗脱,各种浓度的HNO3溶液作为洗脱液进行试验。对于这些试验应该注意的是,使用的样品包括大于99%的几乎定量吸附的[AuCl4]-。图8表示的是[AuCl4]-回收曲线作为0.1到10M范围的HNO3浓度的函数。如第一回收周期所示,使用低于4M的HNO3的回收效率几乎是不合理的。出于这一原因,仅仅第一回收周期使用0.1-4M的范围完成,而后续的两个回收周期使用5-10M的HNO3溶液。图8还显示了对于5-10M的HNO3溶液的后续的两个回收周期回收的[AuCl4]-总量。如可见的,使用10M的HNO3在回收中稳定的增加达到了约93%最大值。从图8中明显的显示随着HNO3浓度的增加,回收的[AuCl4]-数量也随之增加。在0.1M到4M的HNO3之间的曲线的下限,仅仅约1.2到21.5%的被吸附的[AuCl4]-可以在一个洗脱周期从吸附剂中被回收。5到10M的HNO3溶液显示出[AuCl4]-回收相当大的增加,对于第一回收周期达到了76.5%的最大值。进行第二洗脱周期(5到10M的HNO3),在第一洗脱周期之后,残留的被吸附的其它的[AuCl4]-被回收,虽然这次的数量比第一洗脱周期回收的[AuCl4]-数量要少。该结果在下表1中被总结。表1使用10%的HNO3/1%的HCl的混合物进行质量平衡并且在230℃的温度和41.37bar(600psi)的压力微波消化30分钟。在上述相同的条件下由聚(苯乙烯-共-马来酰亚胺)材料吸附的[AuCl4]-消化,随后添加去离子水,获得的沉淀物是高纯度的金粉。用扫描电子显微镜研究该金色沉淀物的形态学,并发现它是薄片状的结构。通过X射线粉末衍射证实了其结晶度和相纯度。还研究了对于贵金属络合物(即[AuCl4]-,[PdCl4]2-,[IrCl6]2-,[PtCl6]2-和[RhCl6]3-)的聚(苯乙烯-共-马来酰亚胺)的萃取特性作为吸附剂剂量的函数,并且结果在图9中显示。该结果清楚地显示,该萃取取决于聚(苯乙烯-共-马来酰亚胺)的剂量。使用的聚(苯乙烯-共-马来酰亚胺)的剂量是10,50,100和150mg。通常,对于10和50mg的聚(苯乙烯-共-马来酰亚胺)的剂量,发现萃取的选择性的顺序是[IrCl6]2->[PtCl6]2-≈[PdCl4]2->[RhCl6]3-。在100和150mg的剂量情况下,选择性几乎分别是[PdCl4]2-≈[PtCl6]2->[IrCl6]2->[RhCl6]3的顺序。这些金属的“萃取率”可能与该络合物阴离子的尺寸和电荷有关。图10所示的结果显示了高于其它阴离子PGM氯络合物的[AuCl4]-的良好的选择性。试验的贵金属所显示的萃取曲线使用了50mg的聚(苯乙烯-共-马来酰亚胺)吸附剂剂量。从图10中可见,可以推论出在[AuCl4]-存在或不存在的多元素溶液中没有观察到PGM萃取效率的明显降低。但是,如之前发现的,即使在竞争性萃取环境中[AuCl4]-被定量萃取。在这种情况下,发现的“萃取率”顺序是[AuCl4]->[IrCl6]2->[PtCl6]2->[PdCl4]2->[RhCl6]3-。似乎聚(苯乙烯-共-马来酰亚胺)吸附剂对于[AuCl4]-比PGM更具选择性并具有高度的吸引力,并且对[IrCl6]2-,[PtCl6]2-和[PdCl4]2-的选择性高于[RhCl6]3-。据信,后者观察的原因被归结于这一事实,即使在萃取试验使用的酸性条件下,[RhCl6]3-络合物大量地与水化合以生成[RhCl6-n(H2O)n]3-n物质(其中n=0,1,2和3)。可以理解通式A的聚合物将被用于从溶液中萃取许多其它的金属或金属化合物,包括金属络合物,特别是阴离子形式的那些物质。聚合物可以具有许多不同的形式,特别是涉及R,R′和R″的种类。例如,这些可以还包括氨基或例如三氮唑和咪唑的其它金属配基,并且这些可以通过氨基烷基连接体被包括于该聚合物中。针对亲核试剂在该共聚物中的顺丁烯二酸酐基团的高反应性使得可以根据需要的应用制备具有各种功能性的材料。本发明的聚合物的制备是相对简单的并且在从溶液中萃取金和其它金属时提供了非常高的效率。优选可以使用通过封装添加在该聚合物粒子中的超顺磁性材料,从而这些聚合物可以高效地从悬浮液中容易地分离出来。因此,应当理解存在的许多的其它的实施例都将落入本发明的范围中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1