用于鉴定多种癌症类型和亚型的糖基转移酶基因表达谱的制作方法
本发明涉及一种鉴定受试者中的癌症类型的方法,其包括使用已经训练的监督算法评价来自所述受试者的样品中的量化糖基转移酶基因表达。另外,所述方法涉及癌症亚型分类和/或鉴定特定癌症类型中的癌症亚型的方法,该方法包括使用已经训练的无监督和监督算法评价量化糖基转移酶基因表达。本发明还涉及包含与所述方法一起使用的糖基转移酶基因捕获探针或引物的试剂盒,及治疗癌症的方法,该方法包括使用本发明的方法和/或试剂盒来为受试者选择适当的治疗方案和/或监测受试者对癌症治疗的反应。
发明背景
癌症是是本世纪最可怕的疾病之一,可危及生命。与癌症类型有关的早期诊断和治疗可以改善对癌症患者的预后。每种类型或亚型的癌症的分子特征影响其对治疗的敏感性,这表示精确预后在使功效最大化和使治疗毒性最小化中的重要性。尽管通过使用高通量技术的基因组和表观遗传学研究证明使用全基因表达分析的影响,在阐明癌症的分子特征时,在生物学行为、临床预后、治疗敏感性和治疗靶点上常常观察到广泛的多样性。这突出了表征癌症类型中这些可能的亚类的重要性。通过鉴定癌症生物学中的关键驱动因素,可以在基因表达的背景下实现这种分类。
肿瘤细胞具有改变的细胞生物化学性质,其有利于避开生长抑制因子和凋亡以及获得侵袭性、血管生成和转移性质。更明确地说,具体糖基化机制的程度在多大程度上与这些途径相互关联是不清楚的。已知在聚糖中发生变化,并且包括在癌细胞中和癌细胞上的蛋白质和脂质上的聚糖,使这些改变的聚糖成为有前景的候选物,以用作可用于癌症患者的早期诊断、监测和治疗的癌症生物标志物。然而,由于缺乏适于聚糖-生物标志物鉴定和检测的分析方法,大多数现有的癌症标志物是糖基化蛋白本身,因为敏感性和特异性差而不推荐用于早期检测。
此外,尽管在不同癌症亚型分型方法中使用的特征选择算法上有进展,但是涉及不同类型癌症的驱动基因的鉴定仍具有挑战性。因此,为改进早期诊断和有效的癌症治疗显著需要开发新型策略。
发明概要
根据本发明的第一个实施方案,提供了一种鉴定受试者中的癌症类型的方法,其通过由来自所述受试者的试样中的糖基转移酶基因集合获得糖基转移酶基因表达谱,并且将来自所述试样的基因表达谱与来自已知癌症类型的糖基转移酶基因表达质心的参考集进行对比,其中将所述受试者的癌症类型鉴定为对应于与来自所述试样的糖基转移酶基因表达谱相比最近的参考集糖基转移酶基因质心的癌症类型。
所述方法可包括以下步骤:
(a)由来自所述受试者的试样中的糖基转移酶基因集合获得糖基转移酶基因表达谱,其中所述糖基转移酶基因选自表1中所列的糖基转移酶基因;
(b)计算所述试样的基因表达谱与来自已知癌症类型的参考糖基转移酶基因表达质心集合中的每一个的距离;和
(c)将所述试样分配为一个癌症类型,其中所述癌症类型确定为对应于与来自所述试样的糖基转移酶基因表达谱相比最近的参考集糖基转移酶基因质心的类型。
所述方法还可包括以下步骤:
(a)获得来自具有已知癌症类型的受试者的癌症样品训练集中每一份的糖基转移酶基因表达谱,其中所述糖基转移酶基因选自表1中所列的糖基转移酶基因;
(b)使用监督算法构建所述训练集中每种癌症类型的基因表达质心;
(c)由来自所述受试者的试样中的糖基转移酶基因集合获得糖基转移酶基因表达谱,其中所述糖基转移酶基因选自表1中所列的糖基转移酶基因;
(d)计算所述试样的基因表达谱与来自已知癌症类型的所述训练集的每个糖基转移酶基因表达质心的距离;和
(e)将所述试样分配为一个癌症类型,其中所述癌症类型确定为对应于与来自所述试样的糖基转移酶基因表达谱相比最近的训练集糖基转移酶基因质心的类型。
所述糖基转移酶基因可由表1中所列的至少任意5个或更多个、任意10个或更多个、任意20个或更多个、任意30个或更多个、任意40个或更多个、任意50个或更多个、任意60个或更多个、任意63个或更多个、任意70个或更多个、任意80个或更多个、任意90个或更多个、任意100个或更多个、任意110个或更多个、任意120个或更多个、任意130个或更多个、任意140个或更多个、任意150个或更多个、任意160个或更多个、任意170个或更多个、任意177个或更多个,任选地任意178个或更多个,进一步任选地任意179个或更多个,再进一步任选地任意180个或更多个、181个或更多个、182个或更多个、183个或更多个、184个或更多个、185个或更多个等,及再进一步任选地全部210个糖基转移酶基因组成。
优选地,所述糖基转移酶基因由表1中所列的全部210个糖基转移酶基因组成。
具体而言,所述210个糖基转移酶基因全部使用时,本发明的方法可用于鉴定选自以下的癌症类型:乳腺癌,包括乳腺浸润性癌;脑癌,包括多形性成胶质细胞瘤;结肠癌,包括结肠腺癌;肾癌,包括肾透明细胞癌;肺癌,包括肺鳞状细胞癌;和卵巢癌,包括卵巢浆液性囊腺癌。
使用至少50个糖基转移酶基因时,本发明的方法可用于鉴定选自以下的癌症类型:乳腺癌,包括乳腺浸润性癌;脑癌,包括多形性成胶质细胞瘤;结肠癌,包括结肠腺癌;和卵巢癌,包括卵巢浆液性囊腺癌。
使用至少5个糖基转移酶基因时,本发明的所述方法可用于鉴定选自以下的癌症类型:脑癌,包括多形性成胶质细胞瘤;和卵巢癌,包括卵巢浆液性囊腺癌。
来自已知癌症类型的参考糖基转移酶基因表达质心或糖基转移酶基因训练集或两者可包括或任选地由选自以下的癌症类型组成:乳腺癌,包括乳腺浸润性癌;脑癌,包括多形性成胶质细胞瘤;结肠癌,包括结肠腺癌;肾癌,包括肾透明细胞癌;肺癌,包括肺鳞状细胞癌;和卵巢癌,包括卵巢浆液性囊腺癌。
所述样品可为任何身体样品,例如但不限于组织、血液、血浆或血清样品。
优选用由提取自所述样品的rna扩增的cdna或mrna进行所述方法的步骤(a)。本领域的技术人员已知由rna模板扩增cdna或mrna的许多方式并且用于rna提取及cdna和mrna扩增的许多商用试剂盒可用。
步骤(a)中表达水平的测定或量化可以使用本领域技术人员熟知的斑点印迹法,包括但不限于基于膜的northern印迹法或southern印迹法,或借助于小型斑点印迹法如微阵列进行。用于此类程序中的许多商用试剂盒为本领域的技术人员可用。
可选地,可借助于定量聚合酶链式反应(pcr)方法进行量化。用于rna和dna定量pcr的不同方法为本领域技术人员已知并且用于此类程序中的商用试剂盒是可用的。此类程序的实例包括但不限于定量逆转录酶pcr(rt-qpcr),其可能是或可能不是实时的。
在本发明的一个特定实施方案中,所述方法可包括以下步骤:
(a)由所述受试者的样品提纯总rna;
(b)通过逆转录将所述rna转化为cdna并且用荧光染料标记所述cdna或由所述rna扩增mrna并且用荧光染料标记所述mrna;
(c)使印有对选自表1中所列的糖基转移酶基因的所述糖基转移酶基因或每一个的基因片段有特异性的靶寡核苷酸探针的微阵列载玻片与所述荧光标记的cdna或mrna接触;
(d)使所述荧光标记的cdna或mrna与所述靶寡核苷酸探针杂交;
(e)量化与微阵列载玻片上的其靶寡核苷酸探针结合的cdna或mrna的荧光强度,由此每个靶标处的荧光强度对应于每个受试者糖基转移酶基因的mrna转录物的相对丰度,即所述受试者样品糖基转移酶基因表达谱;
(f)计算所述受试者样品的基因表达谱与来自已知癌症类型的糖基转移酶基因表达质心集合中的每一个的距离,其中所述糖基转移酶基因表达质心基因选自表1中所列的糖基转移酶基因;和
(g)将所述受试者样品分配为一个癌症类型,其中所述癌症类型确定为对应于与来自所述受试者样品的糖基转移酶基因表达谱相比最近的糖基转移酶基因表达质心的类型。
在本发明的一个替代性特定实施方案中,所述方法可包括以下步骤:
(a)由所述受试者的样品提纯总rna;
(b)通过逆转录将所述rna转化为cdna并且用荧光染料或生色底物标记所述cdna,或由所述rna扩增mrna并且用荧光染料或生色底物标记所述mrna;
(c)使印有对选自表1中所列的糖基转移酶基因的所述糖基转移酶基因或每一个的基因片段有特异性的靶寡核苷酸探针的斑点印迹与所述标记的cdna或mrna接触;
(d)使所述标记的cdna或mrna与所述靶寡核苷酸探针杂交;
(e)量化与所述斑点印迹上的其靶寡核苷酸探针结合的所述杂交标记cdna或mrna的强度,由此每个靶标处所述标记的强度对应于每个基因的mrna转录物的相对丰度,即所述受试者样品糖基转移酶基因表达谱;
(f)计算所述受试者样品的基因表达谱与来自已知癌症类型的糖基转移酶基因表达质心集合中的每一个的距离;和
(g)将所述受试者样品分配为一个癌症类型,其中所述癌症类型确定为对应于与来自所述受试者样品的糖基转移酶基因表达谱相比最近的糖基转移酶基因表达质心的类型。
在本发明的另一个替代性特定实施方案中,所述方法可包括以下步骤:
(a)由所述受试者的样品提纯总rna;
(b)通过rt-qpcr用选自表1中所列的糖基转移酶基因的所述糖基转移酶基因或每一个的基因片段的特异性引物,由所述rna扩增cdna;
(c)量化所述扩增cdna;
(d)评估所述每个基因的扩增cdna的相对丰度,由此所述扩增cdna的丰度对应于每个基因的mrna转录物的相对丰度,即所述受试者样品糖基转移酶基因表达谱;
(e)计算所述受试者样品的基因表达谱与来自已知癌症类型的糖基转移酶基因表达质心集合中的每一个的距离;和
(f)将所述受试者样品分配为一个癌症类型,其中所述癌症类型确定为对应于与来自所述受试者样品的糖基转移酶基因表达谱相比最近的糖基转移酶基因表达质心的类型。
所述方法还可包括对具有已知癌症类型的受试者中的癌症亚型分类的步骤,其中所述亚型分类包括以下步骤:
(a)由来自具有已知癌症类型的受试者的癌症样品获得测试糖基转移酶基因表达谱,其中所述糖基转移酶基因选自表1中所列的糖基转移酶基因;
(b)提供来自对应于所述受试者的癌症亚型的糖基转移酶基因表达谱参考集,其中所述糖基转移酶基因选自表1中所列的糖基转移酶基因;
(c)对所述测试糖基转移酶基因表达谱和所述糖基转移酶基因表达谱参考集进行无监督聚类分析,从而将所述测试糖基转移酶基因表达谱和所述参考糖基转移酶基因表达谱分成一个或多个亚型。
优选地,先前已借助于本发明的方法鉴定了所述受试者的癌症类型。
任选地,亚型分型方法还可包括以下步骤:
(d)由来自具有已知癌症类型的受试者的试样中的糖基转移酶基因集合获得糖基转移酶基因表达谱,其中所述糖基转移酶基因选自表1中所列的糖基转移酶基因;
(e)计算所述试样的基因表达谱与来自对应于所述受试者的癌症亚型的参考糖基转移酶基因表达质心集合中的每一个的距离;和
(f)将所述试样分配为一个癌症亚型,其中所述癌症亚型确定为对应于与来自所述试样的糖基转移酶基因表达谱相比最近的参考集糖基转移酶基因质心的亚型。
进一步任选地,所述方法还可包括以下步骤:
(f)获得来自具有已知癌症类型的受试者的癌症样品训练集中每一份的糖基转移酶基因表达谱,其中所述糖基转移酶基因选自表1中所列的糖基转移酶基因;
(g)使用监督算法构建所述训练集中每种癌症类型的基因表达质心;
(h)由来自所述受试者的试样中的糖基转移酶基因集合获得糖基转移酶基因表达谱,其中所述糖基转移酶基因选自表1中所列的糖基转移酶基因;
(i)计算所述试样的基因表达谱与步骤(b)中构建的每个糖基转移酶基因表达质心的距离;和
(j)将所述试样分配为一个癌症亚型,其中所述癌症亚型确定为对应于与来自所述试样的糖基转移酶基因表达谱相比最近的训练集糖基转移酶基因质心的亚型。
对于糖基转移酶基因表达谱的参考或训练集可已知生存信息,在这种情况下所述方法可任选地包括基于所述测试糖基转移酶基因表达谱分组所在的亚型聚类的生存预后来鉴定所述受试者的生存预后的步骤。
具体而言,在鉴定癌症类型后对来自鉴定为患有乳腺癌、脑癌或卵巢癌的受试者的样品进行鉴定癌症亚型的步骤。
根据本发明的另一方面,提供了一种根据本发明的方法鉴定受试者中的癌症类型和任选地亚型的试剂盒,所述试剂盒包含:
(a)用于扩增cdna或mrna的引物;
(b)用于斑点印迹法中与cdna或mrna杂交的糖基转移酶基因特异性寡核苷酸探针;或
(c)印在微阵列载玻片上,在微阵列法中可与标记的cdna或rna杂交的糖基转移酶基因特异性寡核苷酸探针;
(d)指示剂装置;和
(e)任选地,使用说明书。
所用的斑点印迹法可为cdna或mrna斑点印迹法。优选地,该程序为小型斑点印迹如微阵列。
在本发明的一个替代性实施方案中,所述试剂盒包含:
(a)用于通过定量实时pcr扩增cdna或mrna的糖基转移酶基因特异性引物;和
(b)指示剂装置;和
(c)任选地,使用说明书。
所述试剂盒还可包括来自已知癌症类型或特定癌症类型中的亚型的糖基转移酶多核苷酸参考集。
所述引物可为序列特异性引物、寡聚(dt)引物或随机引物。例如,序列特异性引物可为糖基转移酶基因或基因片段特异性引物。用于引物设计和标记的各种方法和网站是本领域技术人员熟知的。此外,用于扩增cdna或mrna的方法和试剂盒也是本领域技术人员熟知并且可用的。
寡核苷酸探针可为dna、rna或其经修饰的或衍生化寡核苷酸,通常最少有靶糖基转移酶基因序列的25个互补碱基。设计和产生此类寡核苷酸探针及进行northern或southern印迹和微阵列程序的方法是本领域技术人员熟知的。
通过3’、5’或序列修饰对寡核苷酸进行修饰的各种方法为本领域技术人员已知,包括但不限于氨基修饰、羧基修饰、硫醇修饰、醛修饰、化学磷酸化修饰、间隔区、接头或树状大分子修饰和许多其它方法。
指示剂装置可以是本领域技术人员已知的任何指示剂装置,包括但不限于生色、放射性标记或荧光指示剂分子。通常,指示剂装置在扩增期间掺入步骤(a)的cdna或mrna中。
用于在扩增期间标记cdna或mrna的许多熟知方法和试剂盒为本领域技术人员已知。
所述试剂盒还包含用于以下任一项或多项的计算机可读指令:
(a)测定所述受试者样品糖基转移酶基因表达谱;
(b)通过以下鉴定癌症类型:
i.计算所述受试者样品的基因表达谱与来自已知癌症类型的糖基转移酶基因表达质心集合中的每一个的距离;和
ii.将所述受试者样品分配为一个癌症类型,其中所述癌症类型确定为对应于与来自所述受试者样品的糖基转移酶基因表达谱相比最近的糖基转移酶基因表达质心的类型;和
(c)通过以下对癌症亚型进行分类和/或鉴定:
i.与来自对应于所述受试者的癌症亚型的参考或训练糖基转移酶基因集合的糖基转移酶基因表达谱相比,对来自具有已知癌症类型的所述受试者的所述糖基转移酶基因表达谱进行无监督共识聚类分析;
ii.计算所述受试者样品的基因表达谱与来自对应于所述受试者的癌症亚型的糖基转移酶基因表达质心集合中的每一个的距离;和
iii.将所述受试者样品分配为一个癌症亚型,其中所述癌症亚型确定为对应于与来自所述受试者样品的糖基转移酶基因表达谱相比最近的糖基转移酶基因表达质心的亚型。
对于来自对应于所述受试者的癌症亚型的所述糖基转移酶基因表达谱参考或训练集或糖基转移酶基因表达质心,生存信息可已知,在这种情况下,所述方法可任选地包括基于测试糖基转移酶基因表达谱分组所在的所述亚型聚类的生存预后来鉴定所述受试者的生存预后的计算机可读指令。
根据本发明的另一个方面,提供了本发明的方法在为疑似患有或已知患有癌症的受试者选择治疗方案中的用途,其包括对来自所述受试者的样品进行本发明的方法,然后对所述受试者中鉴定的癌症类型或亚型选择适当的治疗方案。
本发明的方法可在受试者接受对癌症的治疗性治疗之前进行,然后在所述受试者接受了对癌症的治疗性治疗之后再次进行,其中治疗之前与治疗之后所述糖基转移酶基因表达水平的差异表明所述治疗性治疗的功效。
根据本发明的另一个方面,提供了一种为疑似患有或已知患有癌症的受试者选择治疗方案的方法,其包括对来自所述受试者的样品进行本发明的方法,然后对所述受试者中鉴定的癌症类型或亚型选择适当的治疗方案。
所选择的方法可在受试者接受对癌症的治疗性治疗之前进行,然后在所述受试者接受了对癌症的治疗性治疗之后再次进行,其中治疗之前与治疗之后所述糖基转移酶基因表达水平的差异表明所述治疗性治疗的功效。
根据本发明的另一个方面,提供了一种治疗疑似患有或已知患有癌症的受试者的方法,所述方法包括:
(a)对来自所述受试者的样品进行本发明的方法;
(b)通过本发明的方法鉴定所述受试者的癌症类型和任选地所述受试者的癌症亚型;
(c)基于步骤(b)的结果,确定是否开始治疗、修改所述治疗方案或中断所述受试者的治疗;和
(d)任选地,开始治疗、修改所述治疗方案或中断治疗。
本发明的方法可在受试者接受对癌症的治疗性治疗之前进行,然后在所述受试者接受了对癌症的治疗性治疗之后再次进行,其中治疗之前与治疗之后所述糖基转移酶基因表达水平的差异表明所述治疗性治疗的功效。
根据本发明的另一个方面,提供了一种根据本发明,用于治疗癌症或为受试者选择治疗方案的方法中的试剂盒,所述方法包括以下步骤:
(a)对来自所述受试者的样品进行本发明的方法;
(b)通过本发明的方法鉴定所述受试者的癌症类型和任选地为所述受试者的癌症亚型分类;
(c)基于步骤(b)的结果,确定是否开始治疗、修改所述治疗方案或中断所述受试者的治疗;和
(d)任选地,开始治疗、修改所述治疗方案或中断治疗。
根据本发明的另一个方面,提供了选自表1中所列的糖基转移酶基因的糖基转移酶基因多核苷酸序列或其片段,其与本发明的方法一起使用。
附图简述
图1显示使用对210个糖基转移酶基因的表达谱的无监督聚类分离六种tcga癌症类型。三维(3d)图显示对六种研究的癌症类型的区分(即乳腺癌:乳腺浸润性癌[brca,n=531];卵巢癌:卵巢浆液性囊腺癌[ov,n=546];结肠癌:结肠腺癌[coad,n=153];肺癌:肺鳞状细胞癌[lusc,n=154];脑癌:多形性成胶质细胞瘤[gbm,n=400];和肾癌:肾透明细胞癌[kirc,n=72]);
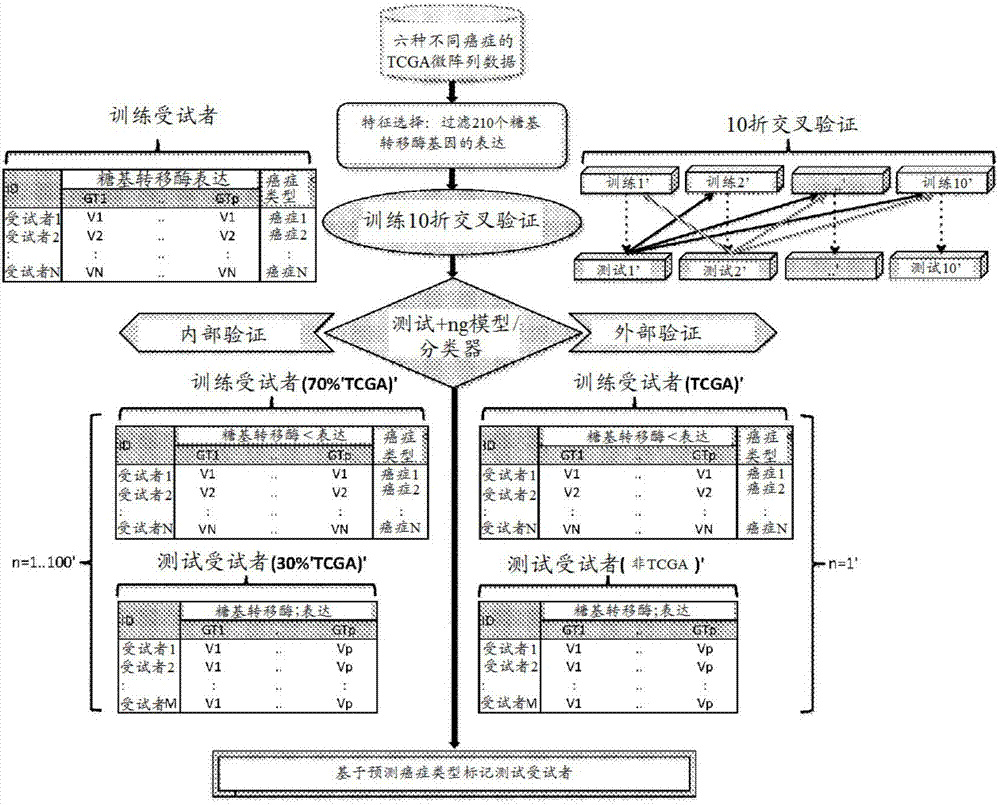
图2显示对六种tcga癌症类型的监督分类/类别预测连同验证步骤的流程图。使用10折交叉验证(10-foldcrossvalidation)、内部和外部测试检查pam分类器的性能。为了在将样品分配为正确癌症类型中进行分类器误差估计的目的,进行10折交叉验证。此外,为了内部验证的目的,将糖基转移酶表达数据集随机分裂几百次,分成训练集(70%)和测试集(30%)。训练集用于建立模型/分类器,然后将其应用于测试集。最后,中位值用于将每个样品分配为特定的癌症类型。由于训练算法在训练数据集中寻找模式,所以依赖于这些虚假模式的分类器对训练实例的准确度要高于整个群体。因此,评估分类器对独立测试集的性能是绝对重要的。为此,已将tcga数据用作外部(独立)测试的训练集,检查gse20624的gpl1390平台中存在的293份乳腺癌样品(anders等人,2011)。gse20624(gpl1390)数据未包括在tcga中,而使用与tcga数据集相同的微阵列平台,然而,只有177种糖基转移酶在训练集(基于tcga)和该数据集之间是常见的;
图3显示对六种tcga癌症类型中通过210个糖基转移酶基因表达产生的pam模型/分类器的评估。a)10折交叉验证。表总结了10折交叉验证的结果,其估计了使用独立数据集进行肿瘤类型预测时所述模型/分类器的准确度。表下方的图显示每个样品分配为每个癌症类型中的正确癌症类型的可能性。阈值图用于决定训练集中基因的数量,这样产生更低的错误率。在这项研究中,阈值设为零(t=0),其在10折交叉验证中产生最低的总误差率并且也防止内部验证的偏差结果。b)内部验证。100个内部测试的结果的环状热图示意图。热图中间的百分比值显示样品的分数,其分配为正确肿瘤类型的后验概率≥0.95。侧边栏上的值表示后验概率的中位数,其将每个样品分配为特定的癌症类型。源自混淆矩阵的准确性度量,受试者工作特征(roc)曲线下面积和内部测试的置信区间(ci)(下表),清楚地显示了糖基转移酶基因表达谱在肿瘤类型鉴定/区分中的潜力,对所有研究的癌症类型具有高准确度、灵敏度和特异性。c)外部验证。模型/分类器对独立测试集(gse20624,非tcga)的性能评估。已将tcga数据集用作外部(独立)测试的训练,检查gse20624的gpl1390平台中存在的293份乳腺癌样品(anders等人,2011)。gse20624(gpl1390)数据未包括在tcga中,而使用与tcga数据集相同的微阵列平台,然而,只有177种糖基转移酶在训练集(基于tcga)和该数据集之间是常见的;
图4显示通过210个糖基转移酶基因的表达谱分析发现五种乳腺癌亚型的类别。(a)使用k-均值聚类法,467份乳腺癌(乳腺浸润性癌)样品的共识聚类矩阵与tcga中k=3至k=6的生存和pam50亚型分型信息。(b)k=2至k=10的共识聚类cdf(箭头显示随着聚类数量从2增加到10,cdf曲线的移动方向)。(c)五个聚类/组的所有配对比较的sigclustp值。(d)对数秩检验p值,研究亚型数(k=2至k=10)与生存信息的关系。g1:第1组(n=97),g2:第2组(n=91),g3:第3组(n=93),g4:第4组(n=103),g5:第5组(n=83);
图5显示比较通过分析210个糖基转移酶基因的表达谱而发现的五种乳腺癌mrna表达亚型(g1-g5)的临床数据和体细胞突变模式连同生存曲线。基于其糖基转移酶表达,具有tcgaagilent微阵列乳腺癌(乳腺浸润性癌)数据集中的临床数据和体细胞突变信息的肿瘤样品(n=467)分为五个亚型(g1-g5):第1组(g1,n=97),第2组(g2,n=91),第3组(g3,n=93),第4组(g4,n=103)和第5组(g5,n=83)(基于tcga2012研究的样品分组用单独的彩色侧边栏进行说明,管腔a:蓝色,管腔b:浅蓝色,基底样:红色及her2富集型:粉红色)。从左至右列显示her2、pr和er样品中的临床数据(上)和以百分比计的频率(下)(阳性:白色,阴性:黑色)。显著突变基因的体细胞突变模式和频率(野生型:白色,截短突变:黑色和错义突变:灰色)。左图说明了tcga乳腺癌样品相对于鉴定的亚型的生存分析结果;
图6显示通过210个糖基转移酶基因的表达谱分析发现六种卵巢癌亚型的类别。(a)使用k-均值聚类法,529份卵巢癌(卵巢浆液性囊腺癌)样品的共识聚类矩阵与tcga中k=2至k=8的生存信息。(b)k=2至k=10的共识聚类cdf(箭头显示随着聚类数量从2增加到10,cdf曲线的移动方向)。(c)六个聚类/组的所有配对比较的sigclustp值。(d)对数秩检验p值,研究亚型数(k=2至k=10)与生存信息的关系。g1:第1组(n=59),g2:第2组(n=97),g3:第3组(n=107),g4:第4组(n=78),g5:第5组(n=79);g6:第6组(n=109);
图7显示通过210个糖基转移酶基因的表达谱分析发现七种脑癌亚型的类别。(a)使用k-均值聚类法,399份脑癌(多形性成胶质细胞瘤)样品的共识聚类矩阵与tcga中k=3至k=9的生存信息。(b)k=2至k=10的共识聚类cdf(箭头显示随着聚类数量从2增加到10,cdf曲线的移动方向)。(c)七个聚类/组的所有配对比较的sigclustp值。(d)对数秩检验p值,研究亚型数(k=2至k=10)与生存信息的关系。g1:第1组(n=48),g2:第2组(n=33),g3:第3组(n=73),g4:第4组(n=33),g5:第5组(n=93);g6:第6组(n=34);g7:第7组(n=85);及
图8显示就使用210个糖基转移酶基因的基因表达谱发现的亚型而言,卵巢癌和脑癌的生存分析。根据卵巢(高级浆液性卵巢癌)(a)和脑癌(多形性成胶质细胞瘤)(b)的六个和七个亚型的对数秩检验分析的kaplan-meier生存图和p值。
具体实施方式
本发明涉及一种鉴定受试者中的癌症类型的方法,其包括使用已经训练的监督算法评价来自所述受试者的样品中的量化糖基转移酶基因表达。另外,所述方法涉及癌症亚型分类和/或鉴定特定癌症类型中的癌症亚型的方法,该方法包括使用已经训练的无监督和监督算法评价量化糖基转移酶基因表达。本发明还涉及包含与所述方法一起使用的糖基转移酶基因捕获探针或引物的试剂盒,及治疗癌症的方法,该方法包括使用本发明的方法或试剂盒来为受试者选择适当的治疗方案和/或监测受试者对癌症治疗的反应。
术语“癌症”用来描述可能不具有相同致病物、病因或分子谱的复杂恶性疾病。实体肿瘤的复杂性质接近正常组织的复杂性质,并与已发现构成其微环境的细胞类型家族进行了比较。在对充分引用的癌症标志的更新中,hanahan和weinberg总结了目前对肿瘤细胞在疾病进展中发挥的不同作用的理解(hanahan和weinberg,2011b)。肿瘤细胞具有改变的细胞生物化学性质,其有利于避开生长抑制因子和凋亡以及获得侵袭性、血管生成和转移性质。更明确地说,具体糖基化机制的程度在多大程度上与这些途径相互关联是不清楚的。肿瘤细胞必须首先侵入周围细胞才能转移。癌症相关的寡糖变化已经与癌细胞的侵入性质有关(dall'olio,1996b)。在过去几十年中已经记录了处于向恶性肿瘤转化路径上的正常细胞上的复杂寡糖的结构被改变。这些通过糖基转移酶基因调控而策划的翻译后修饰(ptm)和糖基转移酶的后续生物化学作用在依赖于肿瘤发生、肿瘤进展和转移的向恶性肿瘤的进展中发挥关键作用(ohtsubo和marth,2006;wang等人,2009;li等人,2010;li等人,2013;liu等人,2013)。
发明人认为与肽、蛋白质和脂质共价偶合的聚糖结构的糖基转移酶工程化变化被强烈地暗示为恶性肿瘤分型和可能的亚型分型中的特征。因此,发明人已经进行了评估,通过在基因组规模上监测糖基转移酶基因的表达,评估该基因子集是否提供了癌症分离和进一步鉴定癌症类型的准确手段。令人吃惊的是,发明人已经表明,使用糖基转移酶基因的表达谱不但可以从未知的试样中鉴定出不同的癌症类型,而且可以对特定癌症类型中的癌症亚型分类并且任选地预测具有特定癌症亚型的受试者的可能结果。
如本文中所用,术语“基因”是指遗传单位,包括蛋白质编码和非编码转录区、上游和下游调控区、转录区和成熟转录物的所有变体。
如本文中所用,术语“cdna”意指在逆转录酶催化的反应中由信使rna(mrna)模板合成的合成dna。
如本文中所用,术语“mrna”和“mrna转录物”可互换使用并且意指由基因的dna转录的rna分子。
如本文中所用,短语“聚类算法”意指在计算或其它解决问题的操作中要特别遵循的生物信息数学方法或一套规则,特别是通过计算机,基于指定特征将给定数据集划分成组,使得组内的数据点比不同组中的点相互更为相似。
如本文中所用的“质心”意指每个癌症类别(即每种癌症类型)中每个基因的平均基因表达除以该基因的类内标准差。
如本文中所用的“参考糖基转移酶基因表达质心”意指对于每种癌症类型已通过以下计算的标准化糖基转移酶基因表达质心:(i)计算每种癌症类型中选自表1中所列的糖基转移酶基因的每个糖基转移酶基因的平均基因表达值,并且(ii)用平均基因表达值除以该基因的类内标准差。
“最近质心分类”意指(i)获得试样的糖基转移酶基因表达谱,(ii)将其与每个参考糖基转移酶基因表达质心进行对比,并且(iii)将试样的癌症类型鉴定为在平方距离上试样最接近的质心的癌症类型。
“共识聚类”意指提供用于确定数据集中的可能聚类的数量和成员的定量证据的方法。共识聚类方法涉及从一组项目(例如微阵列)进行二次抽样,并确定指定簇计数(k)的聚类。然后,计算配对共识值,即两个项目占用相同聚类占它们在相同子样品中出现的次数的比例并存储在每个k的对称共识矩阵中(monti等人,2006)。
如本文中所用,术语“寡核苷酸”意指短单链核酸链(呈寡脱氧核苷酸或寡核糖核苷酸)。如本文中所用,术语“多核苷酸”意指其分子由许多核苷酸单元组成的线性聚合物。
如本文中所用,术语“癌症类型”意指由癌症来源的组织类型(组织学类型)或原发部位或身体中癌症首先发展的位置或其来源的细胞种类,以及癌细胞的外观而确定的癌症的类型。
如本文中所用,术语“癌症亚型”意指癌症类型的二级分类,属于该癌症类型。可将其称为癌症的分子分类。具体而言,癌症亚型可能与分子改变、癌症生存率、不同的临床和病理特征、特异性基因表达特征和失调的信号传导途径相关。
介导发生在肿瘤进展各个阶段的关键病理生理事件的聚糖被认为是癌症生物学的关键驱动因素之一。申请人已经评估是否,因为特定聚糖结构的变化对于肿瘤发生、肿瘤进展和转移是必需的,所以鉴定其糖基转移酶基因的表达模式的差异可能是用于了解癌症复杂性的描述性方法。糖基转移酶基因调节聚糖结构的组织特异性生物合成,导致聚糖的结构变化。
有趣的是,申请人已经确定,糖基转移酶基因表达谱确实不但可以用于鉴定试样或盲样的特定癌症类型,而且还可用于将测试癌症分类或鉴定为亚型,包括将亚型与特定的生存预后联系起来。
本文提到的分子技术,包括rna提取、纯化扩增、cdna扩增、mrna和cdna标记、引物和探针设计、northern和southern印迹法、微阵列印刷和方法、rt-pcr、rt-qpcr和实时rt-pcr都是本领域技术人员已知的标准方法。许多参考资料来源可用,包括但不限于:http://www.qiagen.com/resources/molecular-biology-methods/,green和sambrook,2012以及本领域技术人员已知的其它参考资料。
将通过以下实施例来描述本发明,这些实施例不应被解释为以任何方式限制本发明的范围。
实施例1:癌症基因组图谱(tcga)中体现的六种癌症
1.方法
为了该研究的目的,合并了来自tcga(http://tcga-data.nci.nih.gov/tcga/),代表六种癌症类型的1893个样品的agilent微阵列(agilent244k自定义基因表达)数据,六种癌症类型包括乳腺癌:乳腺浸润性癌[brca,n=531];卵巢癌:卵巢浆液性囊腺癌[ov,n=578];脑癌:多形性成胶质细胞瘤[gbm,n=403];肾癌:肾透明细胞癌[kirc,n=72];结肠癌:结肠腺癌[coad,n=154]和肺癌:肺鳞状细胞癌[lusc,n=155],而正常和对照样品被排除。
通过过滤几个公开可用的数据库如京都基因与基因组百科全书数据库(kegg/genes)(http://www.genome.jp/kegg/genes.html)、碳水化合物活性酶数据库(cazy)(http://www.cazy.org/)和文献搜索来检索人糖基转移酶基因列表。kegg/genes是主要从ncbirefseq(pruitt等人,2005;kanehisa等人,2006;pruitt等人,2007)检索的人工策划基因库。此外,cazy提供对与genbank每日发布的蛋白质(ftp://ftp.ncbi.nih.gov/genbank/daily-nc)相对应的cazymes家族分类的在线和定期更新访问(lombard等人,2014)。表1包含210个糖基转移酶基因符号及其entrez数的列表。
糖基转移酶的表达数据集是通过合并六种研究的癌症类型(即乳腺癌、脑癌、结肠癌、肾癌、肺癌和卵巢癌)的tcga表达数据集建立的,并进一步由合并数据集检索了210个糖基转移酶基因的表达。批次效应分析的结果清楚地说明,数据集中没有显著的批次效应(数据未示出)。
为了说明基于糖基转移酶基因表达对癌症类型的分离,使用r中的‘psych’包(revelle,2014)进行主成分分析(参见图1)。
为了评估糖基转移酶表达谱在鉴定癌症类型中的潜力,使用r中的‘pamr’包(hastie等人,2003)建立模型/分类器并进一步使用10折交叉验证、内部和外部测试进一步评估(参见图s2)。构建2x2混淆矩阵(也称为列联表),其代表样品集合的配置,更多信息和方程式,参见fawcett(2006)。此外,还研究了roc(受试者工作特征)曲线和roc下面积(auc)(bradley,1997)以使用r中的‘proc’包(robin等人,2011)评估分类器的性能。此外,使用独立测试集评估分类器的性能。为此,已将tcga数据集用作外部(独立)测试的训练集,检查gse20624的gpl1390平台中存在的293份乳腺癌样品(anders等人,2011)。
2.结果和讨论
从癌症基因组图谱(tcga)项目(http://tcga-data.nci.nih.gov/tcga/)检索1893个样品的微阵列表达数据,其代表6种癌症类型,包括乳腺癌:乳腺浸润性癌[brca,n=531];卵巢癌:卵巢浆液性囊腺癌[ov,n=578];脑癌:多形性成胶质细胞瘤[gbm,n=403];肾癌:肾透明细胞癌[kirc,n=72];结肠癌:结肠腺癌[coad,n=154]和肺癌:肺鳞状细胞癌[lusc,n=155]。申请人进一步合并并过滤数据以得出210个糖基转移酶基因的表达。
表1提供数据集中存在的210个糖基转移酶基因的列表。
表1:agilent微阵列表达数据集中存在的210个糖基转移酶基因的列表。
为评估糖基转移酶表达谱在区分不同癌症类型中的能力进行主成分分析(pca)(hotelling,1933),其中具有最高方差(pc1、pc2和pc3)的前三个主要成分解释了评估的癌症类型之间28%的变化并且被清楚地显示以区分不同的癌症类型(参见图1)。
为了评估糖基转移酶表达谱在鉴定癌症类型中的潜力,使用‘pamr’包建立模型/分类器(参见图2)。为了在将样品分配为正确癌症类型中进行误差估计的目的,使用‘pamr’包进行10折交叉验证技术(参见图3a)。
另外,进行内部和独立/外部测试以使用糖基转移酶基因的表达来评估pam分类器的性能。为了内部验证的目的,将糖基转移酶表达数据集随机分裂几百次,分成训练集(70%)和测试集(30%)。训练集用于建立模型/分类器,然后将其应用于测试集。最后,中位值(质心)用于将每个样品分配为特定的癌症类型。该分析的结果用于图3b中总结的准确度测量计算。源自混淆矩阵的准确性度量,受试者工作特征(roc)曲线下面积和内部测试的置信区间(ci)(参见图3b),清楚地显示了糖基转移酶基因表达谱分析在肿瘤类型预测/鉴定中的潜力,对所有研究的癌症类型具有高准确度(>98%)、灵敏度(>93%)和特异性(>98%)(参见图3b中的表),在内部测试中将至少93%的试样分配为正确的癌症类型(参见图3b中的环状热图)。
由于训练算法在训练数据集中寻找模式,所以依赖于这些虚假模式的分类器对训练实例的准确度要高于整个群体。因此,评估分类器对独立测试集的性能是绝对重要的。为此,已将先前测试(内部测试)的训练集用于外部(独立)测试,检查gse20624的gpl1390平台中存在的293份乳腺癌样品(anders等人,2011)。gse20624(gpl1390)数据未包括在tcga中,而使用与tcga数据集相同的微阵列平台,然而,只有177种糖基转移酶在训练集(基于tcga)和该数据集之间是常见的。这个测试的结果示为环状热图(参见图3)。
因此,我们确定在内部和外部测试中肿瘤类型区分的估计值分别超过93%和71%(后验概率≥0.95)(参见图3b和c中的环状热图)。
3.结论
dna微阵列实验产生大型数据集,同时监测成千上万的基因表达。在这种高维数据中,从未知样品中准确鉴定不同肿瘤类型和亚型是困难的,但对于成功诊断和治疗往往至关重要。
这项研究的结果表明,糖基转移酶基因的表达谱在不同的癌症类型之间显著改变并且这些差异足以鉴定受试者中的癌症类型和任选的亚型。因此,与目前的癌症诊断技术相比,本研究提供了一种新型且改进的替代方法。
实施例2:癌症亚型分型
1.方法
发明人评估了糖基转移酶基因表达谱在亚型分类鉴定中的用途。获得了来自三种不同癌症的样品:乳腺癌、卵巢癌和脑癌,并对这些样品进行了分析,以提供定量证据以通过共识聚类加上类发现技术(wilkerson和hayes,2010)使用r中的‘consensusclusterplus’包(monti等人,2003)预测每个癌症数据集中的许多可能亚型。共识累积分布函数(cdf)是分别用于说明cdf达到近似最大值的聚类数和cdf曲线中无显著增加的k(组数)的图示。此外,为了基于糖基转移酶基因的表达将样品分组为亚型,使用r中的‘聚类’包(maechler等人,2012)进行k均值聚类。另外,使用r中的‘sigclust’包(huang等人,2012)评估聚类显著性。为了研究每种癌症类型特异性的鉴定组(使用k-均值聚类)是否可以代表临床上不同的患者亚群;使用r中的‘生存’包(therneau,2013)进行单变量生存分析(就总生存期而言比较亚型,k=2至k=10)。
在乳腺癌的情况下,先前鉴定的正常样(tcga,2012)、转移性样品和相应患者中生存信息缺失的样品被排除。此外,通过糖基转移酶基因的表达,在发现的五种亚型的情况下比较临床和体细胞突变模式连同生存曲线。
在卵巢癌和脑癌的方面,相应患者中生存信息缺失的样品被排除。
2.结果和讨论
在解决每种癌症类型中糖基转移酶基因提供亚型分类的能力方面,发明人进行了共识平均连接聚类,其允许对特定癌症中无监督亚型的估计数量的定量和视觉评估(prat等人,2013a)。结果表明,聚类稳定性从k=2增加到k=10(参见图4、6和7),并且它可以解释在每种癌症类型中观察到的异质性,同时进一步鉴定先前鉴定的类别中或除先前鉴定的类别之外的分子亚型。
乳腺癌亚型
发明人关于使用糖基转移酶基因表达谱对乳腺癌亚型的预后评估的结果表明,当乳腺癌样品分为五组时,亚型之间的生存曲线显著不同(参见图4d和5)。根据perou等人(2000),sorlie等人(2001)进行的研究和几项其它研究,存在四种主要乳腺癌亚型(管腔a型、管腔b型、基底样和her2富集型)在乳腺癌分类中已成为共识。此外,由癌症基因组图谱网络tcga(2012)进行的一项研究提供了对这四个先前定义的乳腺癌亚型的重要见解,并解释了每种亚型中的显著分子异质性。
根据这些发现,发明人的结果显示,当数据分为五组(对数秩检验p值=5.79e-03)时,乳腺癌亚型之间的差异最显著。此外,使用糖基转移酶基因的表达谱,在五种检测到的亚型(g1-g5)的情况下比较临床和体细胞突变模式连同生存曲线(参见图5)。该分析结果表明,g1和her2富集型之间,及g5和基底样亚型之间存在显著重叠,而管腔型(a和b)主要分布在其它三种亚型(g2、g3和g4)之间。与其它三种亚型相比,在g1(her2+:45%,pr-:44%和er-:25%,被视为her2富集型)和g5(her2+:2%,pr-:93%和er-:84%,被视为基底样)中临床模式明显更保守。g1和g5亚型中的样品主要突变为tp53(分别为62%和84%),而g1和g5不同地突变为pik3ca(分别为37%和7%)。tp53突变在her2+或er-肿瘤中显著富集,而在her+肿瘤中报道了高频率的pik3ca突变(tcga,2012)。因此,除了临床数据证实使用糖基转移酶表达谱鉴定的这两种亚型可能是her2富集和基底样亚型并且它们不同于官腔亚型外,对g1(分别为62%和37%)和g5(分别为84%和7%)中tp53和pik3ca突变频率的研究是额外的证据。此外,在本研究中与其它组相比,g1(1%)中的gata3突变很少发现(g1到g4分别为10%、13%、14%和15%)。因为gata3突变仅在管腔亚型或er+肿瘤中观察到(tcga,2012),这对于被视为基底样亚型的g5而言,可能是糖基转移酶表达谱清楚地鉴定并将该亚型与其它亚型区分开的额外支持。
在管腔亚型(g2、g3和g4)中,g4具有最低的her2+和er-比率(her2+:7%和er-:1%),而g2和g3具有最高的er-(7%)和最低的pr-(5%)比率。g4(被视为管腔/er+/her2-)亚型中的样品中度突变为tp53(14%)和pik3ca(31%),其次是gata3(15%)、map3k1(11%)和mll3(10%)。雌激素是er阳性乳腺癌的主要生长调节因子并且gata3是er调控基因并在er介导的靶基因调控中起关键作用,并且对于er的基因组作用是重要的(ma等人,2013)。该基因的突变可能潜在地标志对内分泌治疗敏感的疾病(ellis等人,2012a)。
此外,管腔亚型中的gata3突变率(g2:13%,g3:14%和g4:15%)与其它研究结果一致,研究大量的管腔肿瘤,报道了~10%频率的gata3突变(banerji等人,2012;ellis等人,2012a;stephens等人,2012;tcga,2012)。er+/her2-乳腺癌中的体细胞突变基因列表的另一个特征是存在先前涉及白血病和脊髓发育不良的其它基因如mll3和runx1(ellis和perou,2013)。mll家族成员编码组蛋白三甲基转移酶-被视为基因转录的正全局调节因子,其功能包括调节雌激素受体基因表达(wonjeong等人,2012)。理论上,mll突变体肿瘤以及具有为基因表达的表观遗传调节因子的基因突变的其它突变体肿瘤可能对靶向翻译后组蛋白修饰的新药类敏感(huang等人,2011)。
g2和g3亚型对于管腔amrna亚型显著富集。g3亚型(被视为管腔/er+/her2+)中的样品很少突变为tp53(10%),但大多数突变为pik3ca(45%),然后是gata3(14%)、cdh1(13%)和map3k1(18%),而g2亚型(被视为管腔/er-/her2+)中的样品与其它管腔亚型相比大多数突变为tp53和pik3ca(分别为18%和48%),然后是mll3(11%)、gata3(13%)和cdh1(14%)。cdh1突变与her2的显著改变相关(ross等人,2013),而map3k1突变常常与管腔a中的pi3kca突变共存,并显示与雌激素剥夺治疗前后的低增殖指数相关(ellis等人,2012a)。在tp53之后,map3k1的突变率在g2和g3亚型之间显著变化(分别为9%和18%)。map3k1突变是管腔a疾病的高频驱动突变,因此也是可能的因果分子事件(ellis和perou,2013),这可能产生管腔疾病的分子亚型。
总之,研究糖基转移酶基因的表达谱提供了对乳腺癌亚型管腔a/b、基底样和her2富集)之间的明确区别,并且考虑到亚型相关的基因突变,可以提供对管腔亚型分子异质性的重要见解。
卵巢癌和脑癌亚型
为了研究所鉴定的(使用已经对乳腺癌解释的相同方法)卵巢癌和脑癌类型特异性的组是否可以代表临床上不同的患者亚组,发明人进行了单变量生存分析(就总生存期而言比较亚型)。划分卵巢癌和脑癌时,发现生存曲线在不同癌症亚型之间差异显著(参见图8)。
在卵巢癌方面,尽管癌症基因组图谱网络,tcga(2011),tan等人(2013)和tothill等人(2008)先前已经分别报道了四种、五种和六种分子亚型,但是当数据分为六个亚型(对数秩检验p值=1.51e-02)(参见图6和图8)时,得到亚型生存曲线之间最显著的差异。
此外,本发明人证实存在七种脑癌亚型(对数秩检验p值=5.75e-03)(参见图7和8),而verhaak等人(2010)和brennan等人(2013)先前报道的脑癌亚型数量分别为四种和五种。
结论
总之,发现的乳腺癌亚型之间呈现的异质性和每种亚型中展现的同质性在临床和突变模式方面可以证实在癌症亚型分型和结果预测中使用糖基转移酶基因表达谱的潜力。此外,发明人的发现的意义不仅在于发现先前报道的癌症亚型,而且其与临床结果(和乳腺癌情况下的突变模式)的显著相关性为糖基转移酶基因表达谱在癌症类别亚型分型中的潜在用途提供了支持性证据。
4.最终结论
在癌症背景下的个性化医学与准确地鉴定受试者中的癌症类型和进一步鉴定特定癌症亚型的概念密切相关,以便进行准确的诊断,预测结果,从而提供更好的治疗。
虽然聚糖改变可表明聚糖表位对其相关癌症组的特异性,但聚糖的基本和精确结构是复杂的并且在很大程度上未被了解。因此,在没有这种信息的情况下,使用糖基转移酶基因表达谱是具有诊断潜力的引人注目的替代方案,对翻译水平上不同癌症类型的复杂性有深入了解。
其表达与癌症患者生存显著相关的糖基转移酶基因的表达改变代表了这些基因在癌症类型鉴定和亚型分型中的作用的有力证据。因此,糖基转移酶基因代表用于临床测定的有用靶标,引起改善早期诊断的发展。
参考文献
[1].d.hanahan,r.a.weinberg,cell144,(2011a)
[2].f.dalr′olio,clinmolpathol.49,(1996a)
[3].k.ohtsubo,j.d.marth,cell126,(2006)
[4].w.wang,etal.,procnatlacadsciusa106,(2009)
[5].m.li,etal.,jbiosci35,(2010)
[6].s.li,etal.,plosone8,(2013)
[7].l.liu,etal.,plosone8,(2013)
[8].c.k.anders,etal.,journalofclinicaloncology29,(2011)
[9].j.t.leek,etal.,bioinformatics28,(2012)
[10].d.hanahan,r.a.weinberg,cell144,(2011b)
[11].f.dall′olio,clinicalmolecularpathology49,(1996b)
[12].k.d.pruitt,etal.,nucleicacidsres33,(2005)
[13].m.kanehisa,etal.,nucleicacidsres34,(2006)
[14].k.d.pruitt,etal.,nucleicacidsres35,(2007)
[15].v.lombard,etal.,nucleicacidsres42,(2014)
[16].w.revelle,rpackage(2014)
[17].m.r.greenandj.sambrook,molecularcloning:alaboratorymanual,(2012)
[18].t.hastie,etal.,rpackage(2003)
[19].t.fawcett,patternrecognitionletters27,(2006)
[20].a.p.bradley,patternrecognition30,(1997)
[21].x.robin,etal.,bmcbioinformatics12,(2011)
[22].h.hotelling,journalofeducationalpsychology24,(1933)
[23].a.prat,etal.,scientificreports3,(2013a)
[24].m.d.wilkerson,d.n.hayes,bioinformatics26,(2010)
[25].m.maechler,etal.,rpackage(2012)
[26].s.monti,etal.,machinelearning52,(2003)
[27].h.huang,etal.,rpackage(2012)
[28].t.therneau,rpackage(2013)
[29].tcga,nature490,(2012)
[30].a.prat,etal.,scirep3,(2013b)
[31].c.m.perou,etal.,nature406,(2000)
[32].t.sorlie,etal.,procnatlacadsciusa98,(2001)
[33].c.x.ma,etal.,breastcancerresearchandtreatment139,(2013)
[34].m.j.ellis,etal.,nature486,(2012a)
[35].m.j.ellis,etal.,nature486,(2012b)
[36].s.banerji,etal.,nature486,(2012)
[37].p.j.stephens,etal.,nature486,(2012)
[38].m.j.ellis,c.m.perou,cancerdiscovery3,(2013)
[39].k.wonjeong,etal.,molecularendocrinology26,(2012)
[40].y.huang,etal.,breastcancerresearch:bcr13,(2011)
[41].j.s.ross,etal.,clinicalcancerresearch19,(2013)
[42].tcga,nature474,(2011)
[43].t.z.tan,etal.,embomolecularmedicine5,(2013)
[44].r.w.tothill,etal.,clinicalcancerresearch14,(2008)
[45].r.verhaak,etal.,cancercell17,(2010)
[46].c.w.brennan,etal.,cell155,(2013)
- 还没有人留言评论。精彩留言会获得点赞!