2-(5-溴-4-(4-环丙基萘-1-基)-4H-1,2,4-三唑-3-基硫基)乙酸轴手性对映体的晶型III的制作方法
本发明属于制药领域,具体涉及药物lesinurad(即2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸)的轴手性对映体的晶型,特别涉及s构型对映体的晶型iii及其在医药领域中的应用。
背景技术:
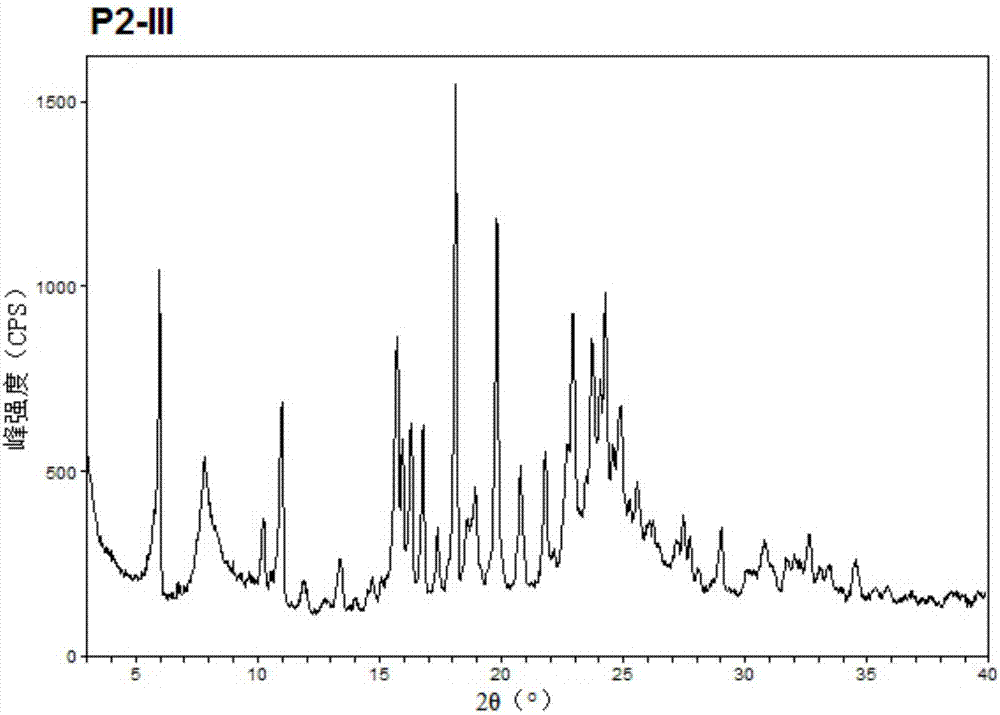
:ardeabiosciences公司研发了一种新型urat1抑制剂lesinurad,其结构如式i所示,化学名:2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸、或者2-[[5-溴-4-(4-环丙基-1-萘)-4h-1,2,4-三唑-3-基]硫代]乙酸,cas:878672-00-5。lesinurad是一种促尿排泄口服药,通过抑制肾近曲小管的尿酸转运子urat1而治疗有高尿酸血症的痛风患者。中国专利申请201510918016.5公开了如式ii和式iii所示的lesinurad轴手性对映异构体:两种轴手性对映异构体存在显著的活性差异,该专利申请中公开的r或者s构型对映体均以无定形形式存在。在研究过程中,本发明人发现无定形形式存在的2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸轴手性对映体在稳定性方面存在缺陷,比如热力学不 稳定、流动性差、吸湿性强等问题,这给药物的制备及储存带来一定困难。因此,急需开发具有稳定性的晶型作为药物晶型形态。技术实现要素:为了克服无定形r-和s-构型lesinurad轴手性对映体的上述缺陷,本发明对于它们的晶型进行了研究,开发出一种稳定性好的s构型对映体的晶型iii。因此,本发明的一个目的在于提供式iii所示s构型lesinurad轴手性对映体的晶型iii。本发明的另一个目的在于提供上述晶型iii的制备方法。本发明的又一个目的在于提供上述晶型iii在制备用于治疗组织尿酸水平异常病症的药物中的用途。本发明的再一个目的在于提供一种包含上述晶型iii作为活性成分的药物组合物。为达到上述目的,本发明提供如下技术方案。1.式iii所示的2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s构型轴手性对映体的晶型iii:其使用cukα辐射、以2θ角度表示的x射线粉末衍射光谱至少在6.04°±0.2°、7.88°±0.2°、11.04°±0.2°、15.78°±0.2°、16.36°±0.2°、16.84°±0.2°、18.18°±0.2°和19.86°±0.2°处存在衍射峰。2.上述1项的晶型iii,其中,还至少在2θ值为10.30°±0.2°、13.44°±0.2°、16.00°±0.2°、17.44°±0.2°、18.98°±0.2°、20.84°±0.2°、21.86°±0.2°、22.98°±0.2°、23.76°±0.2°和24.32°±0.2°处存在衍射峰。3.优选地,上述1项的晶型iii,其至少在2θ值为6.04°±0.1°、7.88°±0.1°、11.04°±0.1°、15.78°±0.1°、16.36°±0.1°、16.84°±0.1°、18.18°±0.1°和19.86°±0.1°处存在衍射峰。4.优选地,上述1项的晶型iii具有与图1中所示x射线粉末衍射图实质相同的x射线粉末衍射图。非限制性地、并且优选地,上述1或3项所述的晶型iii,其还至少在2θ值为 10.30°±0.1°、13.44°±0.1°、16.00°±0.1°、17.44°±0.1°、18.98°±0.1°、20.84°±0.1°、21.86°±0.1°、22.98°±0.1°、23.76°±0.1°和24.32°±0.1°处存在衍射峰。5.进一步地,上述1项的晶型iii,其中,由差示扫描量热法(dsc)测得的熔点峰顶值为106.4℃。6.进一步地,上述1项的晶型iii,其中,其热重分析(tga)图如图3所示,在室温至150℃范围内基本上无质量损失。7.一种制备上述1-6项的晶型iii的方法,包括如下步骤:将无定形的2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s构型轴手性对映体加入二甲苯、甲苯、或者二甲苯和环己烷的混合溶剂中,于30~70℃、优选35~60℃、更优选40~50℃加热溶解,制成饱和溶液,降温、优选降温至0~20℃析出晶体,或静置析出晶体,即得晶型iii。优选地,当采用混合溶剂溶解无定形的s构型轴手性对映体时,二甲苯:其他溶剂的体积比为20~100:1。进一步地,降温析晶后,优选对过滤或离心所得的晶型iii固体进行干燥、比如烘干。干燥温度为30~90℃,优选30~70℃,更优选40~60℃,更优选40~50℃。8.上述1-6项的晶型iii可用于制备药物,所述药物用于治疗组织尿酸水平异常的病症。9.优选地,上述病症可选自痛风、高尿酸血症、降低血清尿酸等。10.基于上述8或9项的用途,本发明可提供一种药物组合物,其包括1-6项中所述的晶型iii作为活性成分。优选地,上述药物组合物除了治疗有效量的晶型iii,还包含至少一种药用赋形剂或者药用载体。优选地,所述赋形剂为润湿剂、分散剂、ph调节剂、抗氧剂、填充剂、稀释剂、润滑剂、增溶剂、助悬剂、矫味剂、粘合剂、崩解剂、渗透压调节剂、絮凝剂、抗粘剂、助悬剂、乳化剂和防腐剂中的一种或几种。本发明的研究表明,无定形的式iii所示的2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s构型轴手性对映体具有引湿性,而晶型iii则几乎无引湿性,因此更具有稳定性,并且具有较好的热稳定性,便于药物制造、存储和运输。附图说明图1为2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s构型轴手性对映体晶型iii的x射线粉末衍射图(xprd图)。图2为2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s构型轴手性对映体晶型iii的差示扫描量热法图(dsc图)。横坐标是温度(℃);纵坐标是热流量(w/g)。图3为2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s构型轴手性对映体晶型iii的热重分析图(tga图)。横坐标是温度(℃);纵坐标是重量保持率(%)。图4为2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s构型轴手性对映体的绝对构型模型图。具体实施方式以下结合具体实施例及附图,对本发明作进一步说明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。本文中涉及到多种物质的添加量、含量及浓度,其中所述的百分含量,除特别说明外,皆指质量百分含量。本发明的实施例中,如果对于反应温度或操作温度没有做出具体说明,则该温度通常指室温(20-25℃)。本文中,(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸、2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s(构)型轴手性对映体、lesinurad的s(构)型对映体均指同一化合物,即式iii所示的化合物。本文中,无定形形式的s构型轴手性对映体和晶型iii形式的s构型轴手性对映体的化学结构式都是式iii所示,但物理形态不同。在本发明中,术语“轴手性对映体”、“对映体”、“轴手性对映体异构体”、“轴手性异构体”和“对映体异构体”表示相同的意义。某些化学物质在结晶时由于受各种因素影响,使分子内或分子间键合方式发生改变,致使分子或原子在晶格空间排列不同,形成不同的晶体结构。同一药物的不同晶型在外观、溶解度、熔点、溶出度、生物有效性等方面可能会有显著不同,从而影响了药物的稳定性、生物利用度及疗效,该种现象在口服固体制剂方面表现得尤为明显。药物晶型是影响药品质量、临床疗效和安全性的重要因素之一,因此对药物晶型的研究,可发现有利于发挥药物作用的药物优势晶型,同时根据晶型的特点确定制剂工艺,有效保证生产的批间药物等效性等,为制剂工作者在处方开发、新药剂型设计、生产工艺的优化、药品质量控制以及临床药效方面提供参考。晶型可由x射线粉末衍射(xprd)光谱图来表征,不同晶型的xprd图是不同的,以2θ角度表示的衍射峰或称吸收峰的位置和/或相对强度(i/i0)会有变化。本发明的2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s构型轴手性对映体的晶型iii的x射线粉末衍射图,表现为衍射峰位置即衍射角2θ(°)、晶面间距衍射峰相对强度(i/i0),概述于表1中。表1lesinurad的s构型轴手性对映体的晶型iii的x射线粉末衍射结果众所周知,有时同样一种晶型,在不同的测试条件下,x射线粉末衍射图会稍有不同。影响x射线粉末衍射图效果的因素有:晶体的纯度、晶化程度、粉末样品自身颗粒的大小、样品架装填粉末样品量、粉末装填到样品架中所处的表面平整度等。在优选的实施方式中,晶型iii具有与图1中所示x射线粉末衍射图实质相同的x射线粉末衍射图。应该理解,x射线粉末衍射图的2θ值可在机器之间、或样品之间稍有变化,其数值可能相差大约0.2个单位(°),或者相差大约0.1个单位(°),因此所引用的数值不能解释为绝对值。同样应该理解,衍射峰相对强度的大小同样可能相差大约5%,或者相差大约4%,或者相差大约3%,或者相差大约2%,或者相差大约1%,因此包括于本发明中的xrpd迹线(trace)强度是说明性的,并非意欲用于绝对比较。作为优选的实施方式,本发明提供的2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的s构型轴手性对映体的晶型iii使用cukα辐射、以2θ角度表示的x射线粉末衍射光谱至少在6.04°±0.1°、7.88°±0.1°、11.04°±0.1°、15.78°±0.1°、16.36°±0.1°、16.84°±0.1°、18.18°±0.1°和19.86°±0.1°处存在衍射峰。更优选x射线粉末衍射光谱至少在2θ值为6.04°、7.88°、11.04°、15.78°、16.36°、16.84°、18.18°和19.86°处存在衍射峰。进一步地,作为另一种优选的实施方式,本发明提供的上述晶型iii使用cukα辐射、以2θ角度表示的x射线粉末衍射光谱还至少在2θ值为10.30°±0.1°、13.44°±0.1°、16.00°±0.1°、17.44°±0.1°、18.98°±0.1°、20.84°±0.1°、21.86°±0.1°、22.98°±0.1°、23.76°±0.1°和24.32°±0.1°处存在衍射峰。更优选x射线粉末衍射光谱还至少在2θ值为10.30°、13.44°、16.00°、17.44°、18.98°、20.84°、21.86°、22.98°、23.76°和24.32°处存在衍射峰。此外,本发明还通过差示扫描量热技术对所述的新晶型进行了分析,在使用差示扫描量热技术进行分析时,表现为当升温速率为每分钟10℃的dsc图谱中存在1个吸热峰在106.4℃处,其谱图基本如图2所示。应该理解,与x射线粉末衍射图数值可能有偏差具有相似情况,差示扫描量热技术所引用的数值也不能解释为绝对值。当指图谱和/或图中数据时,术语“衍射峰”是指本领域的技术人员不会归属于背景噪音的特征峰。术语“相对强度”是指x-射线粉末衍射图的所有衍射峰中强度最高的峰的强度为100%时,其它峰的强度与强度最高的峰的强度的比值。应理解,本文中在表述数值特征时,术语“约”或者“大约”是指所表示的本数可以有±5%、±4%、±3%、±2%或±1%的误差范围或浮动范围。术语“实质相同”是指x射线粉末衍射图中至少70%、至少80%、至少90%、至少95%、或至少99%的峰出现在所给出的示例性x-射线粉末衍射图中。本发明所述的晶型iii是基本上纯净的,术语“基本上纯净的”是指晶型iii基本上不含有其它晶型或者无定形形式(或称非晶体形式)、以及/或者其它物质比如式ii所示lesinurad的r-构型轴手性对映体,所述其它物质是指在生产所述晶型iii过程、以及生产无定形形式的lesinurad的s构型轴手性对映体过程中带来的杂质。优选地,晶型iii的纯度以重量百分比计为至少80%、至少85%、至少90%、至少93%、至少95%、至少98%或至少99%,更优选为100%。除此主要晶型,还可以混合少量的其它晶型、无定形形式和式ii所示lesinurad的r-构型轴手性对映体,但它们的重量百分比少于20%、少于10%、少于5%、少于3%、少于1%、少于0.5%、少于0.1%、或少于0.01%。术语“基本上不含有其它晶型”是指其它晶型的含量在晶体中重量百分比少于20%,或少于10%,或少于5%,或少于3%,或少于1%,或少于0.5%,或少于0.1%,或少于0.01%。药物的吸湿性(即引湿性)是影响晶型稳定性的一个重要因素。本发明中,术语“吸湿性”和“引湿性”、“引湿”意义相同。通过引湿性实验,即吸水等温线测定,可用于确定多晶型或单晶型药物特别是水合物的相对稳定区域。中国药典2010版附录对药物引湿性试验指导原则为:潮解:吸收足量水分形成液体;极具引湿性:引湿增重不小于15%;具有引湿性:引湿增重2%-15%;略有引湿性:引湿增重0.2%-2%;无或者几乎无引湿性:引湿增重小于0.2%。本发明在80%相对湿度的室温环境中进行了lesinurad的s构型对映体晶型iii与无定形的引湿性对比研究,结果显示:14天之内,无定形具有引湿性;而晶型iii几乎无引湿性。可见晶型iii比无定形引湿性小,更具有稳定性。在本发明的药物组合物中,包括药用赋形剂或者药用载体。本发明中,所述赋形剂是指在药物制剂中除主药以外的附加物,也可称为辅料。如片剂中的黏合剂、填充剂、崩解剂、润滑剂;半固体制剂软膏剂、霜剂中的基质部分;液体制剂中的防腐剂、抗氧剂、矫味剂、芳香剂、助溶剂、乳化剂、增溶剂、渗透压调节剂、着色剂等均可称为赋形剂,具体到本发明,优选的,本发明所述赋形剂为润湿剂、分散剂、ph调节剂、抗氧剂、填充剂、稀释剂、润滑剂、增溶剂、助悬剂、矫味剂、粘合剂、崩解剂、渗透压调节剂、絮凝剂、抗粘剂、助悬剂、乳化剂和防腐剂中的一种或几种,更优选为填充剂、稀释剂、润滑剂、崩解剂、润湿剂和粘合剂中的一种或几种,更优选地,填充剂优选为淀粉比如预胶化淀粉、微晶纤维素、乳糖和磷酸氢钙中的一种或几种;所述润滑剂优选为硬脂酸镁、滑石粉或二 氧化硅;所述崩解剂如干淀粉、羧甲基纤维素钠和交联聚维酮中的一种或几种;所述粘合剂优选为淀粉糊浆、甲基纤维素、羟丙基纤维和明胶中的一种或几种。药用赋形剂或者药用载体的具体种类和用量可以根据本领域公知常识来筛选、或者通过简单实验来确定。本发明的药物组合物可以制成本领域技术人员公知的常规形式,选择的制备方法取决于预期的给药途径。例如,作为口腔给药药物,可以呈片剂、胶囊、微胶囊、丸剂、微丸剂、粉剂、缓释调配物、溶液、悬浮液形式;作为无菌溶液、悬浮液或乳液用于非经肠注射;作为软膏或乳霜用于局部投予或作为栓剂用于直肠投予。实施例试剂:本发明实施例中使用的反应物和催化剂均为化学纯,可直接使用或根据需要经过简单纯化;有机溶剂等均为分析纯,直接使用。试剂均购自中国医药(集团)上海化学试剂公司。无定形的lesinurad的s构型轴手性对映体通过制备液相色谱仪进行制备,即使用制备液相色谱仪,对外消旋的2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸进行对映体分离,得到无定形的s构型轴手性对映体。仪器:sfc-80(thar,waters);制备手性柱型号:oj柱20×250mm,5μm(dacel);柱温:35℃;流动相:co2/meoh=75/25,流速:80g/min;检测波长:214nm;柱压:100bar;进样量:0.2ml;循环时间:2.5min;配样方式:将6000mg消旋的lesinurad溶解在50ml甲醇中。富集收集轴手性为s型的lesinurad,浓缩得到无定形,即式iii所示的(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸。无定形的lesinurad的s构型轴手性对映体还可以通过其他方法制备,比如对消旋体进行化学拆分等,并且不局限于此。检测方法及仪器:x射线衍射仪型号:rigakud/max-2550pc,测试条件:功率40kv×250ma,2θ3~40°,步宽(stepwidth):0.02°,扫描方式:连续扫描。差示扫描量热法(dsc)表征:仪器:ta公司,dscq100,测试条件:吹扫气:氮气50ml/min,升温速度:10℃/min,温度范围:30~150℃。热重分析仪器:ta公司,型号sdtq600,测试条件:吹扫气:氮气120ml/min,升温速度:10℃/min,温度范围:30~420℃。动态水分吸附仪(dvs):型号lhh-80sdp,参数:rh%:80%。实施例1晶型iii的制备取无定形(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸样品0.2g,加入10ml二甲苯中,加热至50℃溶解2小时,制成饱和溶液,搅拌降温至10℃析晶、或者静置析晶,过滤,45℃烘2小时,得到0.16g的(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的晶型iii样品。实施例2晶型iii的制备取无定形(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸样品0.2g,加入20ml二甲苯和1ml环己烷的混合溶剂中,50℃加热溶解2小时,制成饱和溶液,搅拌降温至10℃析晶、或者静置析晶,过滤,45℃烘2小时,得到0.1g的(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的晶型iii样品。实施例3晶型iii的制备取无定形(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸样品0.2g,加入30ml二甲苯和1ml环己烷的混合溶剂中,30℃加热溶解2小时,制成饱和溶液,搅拌降温至10℃析晶、或者静置析晶,过滤,45℃烘2小时,得到0.16g的(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的晶型iii样品。实施例4引湿性实验分别取晶型iii和无定形各50mg,置于80%相对湿度的室温环境中,进行动态水分吸附(dvs)测试,测试结果如表2所示。表2晶型iii与无定形的引湿性对比结果上述结果表明,结果显示:14天之内,无定形具有引湿性;而晶型iii几乎无引湿性。可见晶型iii比无定形引湿性小,更具有稳定性。实施例5制备药物组合物制备包含(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的晶型iii的药物组合物:采用00号胶囊,装填下表所示比例的成分。原料质量百分比加入量(mg)晶型iii60%300预胶化淀粉39%195硬脂酸镁1%5总计100%500药物组合物制备方法:预胶化淀粉和(s)-2-(5-溴-4-(4-环丙基萘-1-基)-4h-1,2,4-三唑-3-基硫基)乙酸的晶型iii粉末,通过150目过筛,然后装入混合器中,混合15min,将硬脂酸镁添加到合器中。然后使dosator型胶囊填充机将混合物转入00号胶囊中,得500mg/胶囊的胶囊剂,批量生产。另外,需强调的是,本说明书中对先前公开的文献的列举和论述不应视为承认这些信息是现有技术或者是公知常识。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1