一种葡萄斑点病毒荧光定量PCR检测的专用引物和方法与流程
本发明属于分子生物学领域,具体地说,涉及一种葡萄斑点病毒荧光定量PCR检测的专用引物和方法。
背景技术:
葡萄是一种及具经济价值和营养价值的水果,近年来随着种植面积的不断扩大,病毒病已成为限制其产量和质量提高的重要因素。葡萄斑点病为世界性分布的病毒病,在我国仅见辽宁、山东、新疆等地有该病的零星报道。葡萄斑点病毒(Grapevine fleck virus,GFkV)为芜菁黄花叶病毒目(Tymovirus)成员,长期以来,葡萄斑点病毒的分类地位一直未能明确,随着分子生物学和计算机技术逐步深入地渗透到葡萄斑点病毒的研究中,直到2002年6月经国际病毒分类委员会批准,在植物病毒分类中新增一个属即斑点属(Maculavirus),并把GFkV作为该属的模式种。GFkV于1966年被Vuittenez首次发现,随后对其危害症状、寄主范围和理化特性进行了研究,发现该病毒在栽培品种上潜伏侵染,在沙地葡萄和嫁接砧木上引起危害,可以引起寄主果实产量和品质的降低,但是作为一种潜隐性病毒,其侵染寄主植物后没有明显的症状表现,给该病毒的早期诊断带来较大的困难,目前,世界范围内只有该病毒的一条基因组序列和三条全长CP基因序列,由此可见对该病毒的研究是非常少的。与此同时,GFkV常与其他葡萄病毒伴随发生,关于其病毒与病毒、病毒与植物互作机制的基础研究也逐渐受到重视。因此,有必要建立一种高效、灵敏的对GFkV进行定量检测的方法。
技术实现要素:
有鉴于此,本发明针对上述的问题,提供了一种葡萄斑点病毒荧光定量PCR检测的专用引物和方法,该检测方法可实现对供试葡萄样品中GFkV基因组拷贝数的绝对定量。
为了解决上述技术问题,本发明公开了一种葡萄斑点病毒荧光定量PCR检测的专用引物,包括引物GFkV23和引物GFkV24;其中,所述引物GFkV23的核苷酸序列如SEQ ID NO.1所示;所述引物GFkV24的核苷酸序列如SEQ ID NO.2所示。
本发明还公开了一种葡萄斑点病毒荧光定量PCR检测方法,通过PCR扩增、克隆获得阳性质粒标准品,然后以已知浓度的目的基因作为模板进行荧光定量PCR反应,作出标准曲线,用于测算出待测样品中的病毒含量。
进一步地,该方法包括以下步骤:
1)提取GFkV毒源材料的总RNA,用Oligo(dT)反转录得到cDNA,以该cDNA为模板,以GFkV23和GFkV24为引物进行PCR扩增,扩增产物经1.5%琼脂糖凝胶电泳后割胶回收,连接克隆载体,转化大肠杆菌感受态细胞,筛选并挑取含阳性克隆的大肠杆菌进行培养,提取质粒得到阳性质粒标准品;
2)阳性质粒标准品分别梯度稀释至108,107,106,105,104copy/μL为模板,以GFkV23和GFkV24为引物进行荧光定量PCR扩增,以Ct值为纵坐标,以质粒拷贝数为横坐标,绘制得到标准曲线;
3)提取待测样品的总RNA,以Oligo(dT)为引物反转录得到cDNA,以该cDNA为模板,按照与步骤2)中完全相同的条件进行荧光定量PCR扩增,所得Ct值代入标准曲线公式得到待测样品中GFkV基因组RNA的含量。
进一步地,在步骤1)中,所述PCR反应体系为:2×Ex Taq Mix 12.5μL,10μM GFkV23和GFkV24引物各1.0μL,cDNA 2.0μL,双蒸水补足至25μL。
进一步地,在步骤1)中,所述PCR反应条件为:94℃3min;94℃30s,60℃30s,72℃20s,35cycles;72℃10min。
进一步地,在步骤2)中,阳性质粒标准品拷贝数与浓度的换算方式按照如下公式:拷贝数=浓度×10-9×6.02×1023/(质粒碱基数×660),其中,拷贝数的单位为copy/μL,浓度的温单位为ng/μL。
进一步地,在步骤2)中,所述荧光定量PCR反应体系为:2×SYBR Green qPCR Mix 10.0μL,10μM GFkV23和GFkV24各1.4μL,模板1.0μL,双蒸水补足至20μL。
进一步地,在步骤2)中,所述荧光定量PCR反应条件为:94℃3min;94℃5s,60℃15s,72℃20s,read,40cycles;65℃to 94℃,0.5℃/10s,read。
与现有技术RT-PCR和ELISA两种检测方法相比,本发明创建的GFkV荧光定量PCR检测方法可以获得包括以下技术效果:
1)简化了操作步骤,并节省了检测时间;与RT-PCR相比,RT-PCR需要将扩增产物经过琼脂糖凝胶电泳、EB染色后在紫外凝胶系统下成像后才能看到检测结果,肉眼无法直接看到,ELISA整个检测过程下来需要2天。该有点主要是由于我们采用了与RT-PCR接近的常规分子操作单结合了荧光定量的分子特性使检测结果直接在定量PCR仪上显示。
2)但琼脂糖凝胶成像需要在EB中染色,EB极易污染实验室环境,对操作人员健康有不利影响;本优点主要是由于我们采用了的应该定量相关试剂无毒无害。
3)ELISA和RT-PCR只能对病毒进行定性检测,无法定量检测,我们创建的方法可以实现对病毒的定量检测。荧光定量PCR随着反应的进行荧光的衰退实现对模板拷贝数的监测,从而实现对检测病毒的定量化。
4)本方法与目前最常用的分子检测方法和血清学检测方法相比极大的简化了检测步骤,节约了检测时间;提高了检测的灵敏度,增强了检测效果;降低了实验危害,保护了实验操作者。
当然,实施本发明的任一产品并不一定需要同时达到以上所述的所有技术效果。
附图说明
此处所说明的附图用来提供对本发明的进一步理解,构成本发明的一部分,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
图1是本发明以108,107,106,105,104copy/μL不同浓度质粒标准品为模板扩增获得的标准曲线;
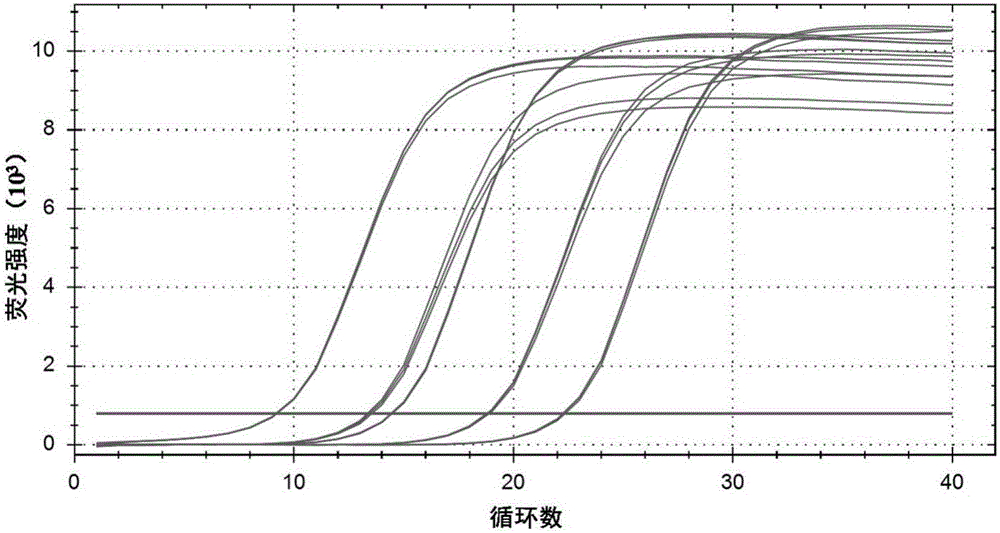
图2是本发明以108,107,106,105,104copy/μL不同浓度质粒标准品为模板扩增的扩增曲线;
图3是本发明以108,107,106,105,104copy/μL不同浓度质粒标准品为模板扩增的溶解曲线。
具体实施方式
以下将配合实施例来详细说明本发明的实施方式,藉此对本发明如何应用技术手段来解决技术问题并达成技术功效的实现过程能充分理解并据以实施。
实施例1
1.引物合成
由生工生物工程(上海)股份有限公司合成引物GFkV23(5’-TTCCTGTGGTATGACATCACG-3’,如SEQ ID NO.1所示)和GFkV24(5’-CAGTGGGTTGGACGAAGGCT-3’,如SEQ ID NO.2所示),用双蒸水溶解至10μM备用。
2.质粒标准品构建
2.1.感染GFkV的葡挞枝条样品由中国农业科学院果树研究所病毒课题组保存。使用RNAprep Pure植物总RNA提取试剂盒(TIANGEN,DP140916)提取样品总RNA,具体步骤参照试剂盒说明书。
2.2.使用Oligo(dT)为引物反转录,反转录酶购自Promega,具体步骤如下:
70℃水浴5min,冰置5min,加入下列成分:
42℃反应1h,95℃灭活5min,得到的cDNA;
2.3.以cDNA为模板,以GFkV23和GFkV24为引物进行PCR扩增,所使用的Ex Taq Mix购自康为世纪,反应体系如下:
PCR反应程序为:94℃预变性3min;94℃变性30s,65℃退火30s,72℃延伸30s,35个循环;72℃补充延伸10min。
2.4.PCR产物在1.5%琼脂糖凝胶中120V恒压电泳15min,凝胶在EB染液中染色5min后用紫外凝胶成像系统成像拍照;用洁净刀片割下大小约为693bp的产物,使用普通琼脂糖凝胶DNA回收试剂盒(TIANGEN,DP209)纯化回收目标产物,具体方法参照说明书;回收片段连接pGEM-T easy(Promega)克隆载体,转化大肠杆菌DH5α感受态细胞(康为世纪),在含50μg/mL氨苄青霉素的LB平板上筛选得到阳性克隆,具体方法参照相关说明书;经PCR验证阳性的单克隆菌落扩大培养后,使用质粒小提试剂盒(TIANGEN,DP103)提取质粒得到阳性质粒标准品并测定质粒浓度。
3.标准曲线绘制
3.1.参照公式:拷贝数(copy/μL)=(浓度(ng/μL)×10-9×6.02×1023)/(质粒碱基数×660),将质粒标准品稀释至108copy/μL,再将108copy/μL的质粒标准品依次稀释至107,106,105,104copy/μL。
3.2.分别以各浓度的质粒标准品为模板,使用Quant One Step RT-qPCR Kit(SYBR Green)试剂盒(TIANGEN,FP303)进行荧光定量PCR,反应体系如下:
使用Bio-Rad iQTM5实时荧光定量PCR仪按如下反应程序进行:94℃3min;94℃5s,60℃15s,72℃20s,read,40cycles;65℃to 94℃,0.5℃/10s,read。程序运行结束后由软件自动生成标准曲线:Y=-3.156×log(X)+34.564,R2=0.976。
实施例2待测植物材料的定量检测
待测葡萄枝条样品采自辽宁省葫芦岛市兴城市,按照上述方法提取样品总RNA,以Oligod(T)为引物反转录得到cDNA,以cDNA为模板,GFkV23和GFkV24为引物,完全按照上述体系和程序进行荧光定量PCR扩增,得到平均Ct值为24.30,代入上述标准曲线公式,得到待测样品CVA拷贝数为1.79×103copy/μL。
上述说明示出并描述了发明的若干优选实施例,但如前所述,应当理解发明并非局限于本文所披露的形式,不应看作是对其他实施例的排除,而可用于各种其他组合、修改和环境,并能够在本文所述发明构想范围内,通过上述教导或相关领域的技术或知识进行改动。而本领域人员所进行的改动和变化不脱离发明的精神和范围,则都应在发明所附权利要求的保护范围内。
SEQUENCE LISTING
<110> 中国农业科学院果树研究所
<120> 一种葡萄斑点病毒荧光定量PCR检测的专用引物和方法
<130> 2016
<160> 2
<170> PatentIn version 3.5
<210> 1
<211> 21
<212> DNA
<213> 人工序列
<400> 1
ttcctgtggt atgacatcac g 21
<210> 2
<211> 20
<212> DNA
<213> 人工序列
<400> 2
cagtgggttg gacgaaggct 20
- 还没有人留言评论。精彩留言会获得点赞!
- 一种C型EV71病毒的TaqMan荧光实时定量PCR检测方法
- 一种鲤春病毒血症病毒的荧光定量pcr检测方法
- 一种利用实时荧光pcr检测偏肺病毒的方法和组合物的制作方法
- 一种病毒三重荧光定量rt-pcr检测方法及其试剂盒的制作方法
- 一种麻疹病毒一步实时荧光定量rt-pcr试剂盒的制作方法
- 一种用于检测日本乙型脑炎病毒的荧光rt-pcr试剂盒的制作方法
- 尼帕病毒和猪瘟病毒二重荧光rt-pcr检测试剂及其制备方法与用图
- 尼帕病毒和猪繁殖与呼吸综合症病毒二重荧光rt-pcr检测试剂及其制备方法与用图
- 用于辛德比斯病毒荧光rt-pcr检测的引物和lna探针及其试剂盒的制作方法
- 鸭痘病毒的实时荧光pcr检测方法及检测用引物和探针的制作方法
- 猪瘟病毒、牛病毒性腹泻病毒双重荧光定量RT‑PCR检测方法与流程
- 一种南瓜花叶病毒实时荧光RT‑PCR检测试剂盒及其方法与流程
- 鹿流行性出血病病毒实时荧光RT‑PCR检测试剂盒的制作方法与工艺
- 用于盖塔病毒实时荧光定量PCR检测体系及检测方法与流程
- 用于盖塔病毒实时荧光定量PCR检测体系及检测方法与流程
- 一种燕麦花叶病毒的实时荧光RT‑PCR检测方法、引物和探针及试剂盒与流程
- 一种检测羊边界病毒的实时荧光定量RT‑PCR试剂盒及应用的制造方法与工艺
- 检测口蹄疫病毒的荧光定量PCR试剂盒及系统的制造方法与工艺
- 五种猪腹泻病毒多重实时荧光定量PCR快速诊断试剂盒及应用的制造方法与工艺
- Sweepoviruses病毒实时荧光定量PCR检测的通用引物、探针及其检测方法与流程
- 一种鹅星状病毒实时荧光定量PCR检测的引物和探针的制作方法与工艺
- 一种葡萄斑点病毒荧光定量PCR检测的专用引物和方法与流程
- 一种樱桃病毒A荧光定量PCR检测的专用引物和方法与流程
- 猪瘟病毒、牛病毒性腹泻病毒双重荧光定量RT‑PCR检测方法与流程
- 一种南瓜花叶病毒实时荧光RT‑PCR检测试剂盒及其方法与流程
- 检测禽呼肠孤病毒的通用PCR引物及其检测试剂盒的制作方法与工艺
- 鹿流行性出血病病毒实时荧光RT‑PCR检测试剂盒的制作方法与工艺
- 用于盖塔病毒实时荧光定量PCR检测体系及检测方法与流程
- 用于盖塔病毒实时荧光定量PCR检测体系及检测方法与流程
- 一种用于绝对定量检测猪繁殖与呼吸综合征病毒的ddPCR方法、引物及其应用和试剂盒与流程
- 高灵敏监测POPs的转荧光蛋白基因鱼的制作与应用的制造方法与工艺
- 一种收发一体式开放光路大气检测系统的制造方法与工艺
- 一种用于鉴别西红花的荧光PCR检测引物组、试剂盒及检测方法和应用与流程
- 转基因玉米MON87403品系特异性实时荧光PCR检测引物、探针、方法和试剂盒与流程
- 一种具有蓝色荧光的手性有机染料分子及其制备方法与应用与流程
- 一种基于直接竞争荧光免疫法定量检测叶酸功能化二氧化硅靶向纳米药物载体的方法与流程
- 螯合剂的定量方法及螯合剂定量系统与流程
- 一种棒状杆菌属细菌和克氏棒状杆菌多重荧光定量PCR引物、探针、试剂盒和检测方法与流程
- 一种染料定量输送装置的制造方法
- 一种基于半阈值追踪算法的荧光分子断层成像重建方法与流程