用于核酸测序的珠子的制作方法
交叉引用
本申请要求于2015年10月15日提交的美国临时专利申请序列号62/241,954、于2015年7月23日提交的美国临时专利申请序列号62/196,224、于2015年6月8日提交的美国临时专利申请序列号62/172,647和于2015年3月30日提交的美国临时专利申请序列号62/140,399的优先权,这些申请通过引用以其全文并入于此用于所有目的。
背景
阐明整个人类基因组的目标已使得人们对快速核酸(例如,dna)测序技术产生关注,无论是小规模还是大规模应用。重要的参数是测序速度、测序精确度、可以在单个测序运行过程中读取的序列长度以及产生测序信息所需的核酸模板的量。大规模基因组项目目前过于昂贵,以至于不能针对大量的受试者(例如,患者)实际地开展。此外,由于对人类疾病的遗传基础的了解增多,对于临床应用负担得起的精确的、高通量dna测序的需求将会不断增加。用于确定核酸单分子的碱基对序列的实用方法(优选高速、高精确度和长读取长度)可提供测量能力。
核酸测序是一种可以用来提供核酸样品的序列信息的过程。这样的序列信息可帮助诊断和/或治疗患有病症的受试者。例如,受试者的核酸序列可以用来鉴定、诊断遗传病以及可能地开发其治疗。作为另一示例,对病原体的研究可导致对接触传染病的治疗。然而遗憾的是,现有技术中存在的测序技术是昂贵的,并且可能无法在一定的时间段内和/或以一定的精确度提供序列信息,从而可能无法足以诊断和/或治疗患有病症的受试者。
技术实现要素:
在此认识到需要用于核酸和其他生物分子的测序、扩增、检测、分析和/或进行样品制备程序的改进装置和方法。本文所述的传感器能够以高准确度检测核苷酸掺入或其他生物反应。
本公开内容的方面提供了用于制备引物缀合的磁珠的方法,该方法包括:(a)将包含多个第一反应性基团的多个聚合物链接枝至胺化的珠子上,以提供各自通过各自一个所述聚合物链偶联至所述珠子的多个第二反应性基团;以及(b)将胺封端或羟基封端的引物与所述第二反应性基团共价附接,其中所述多个聚合物链中的单个聚合物链包含重复单元,该重复单元包含与所述第一反应性基团和所述第二反应性基团的官能团不同的官能团,其中所述官能团是亲水的,并且其中所述单个聚合物链包含大于或等于40摩尔%(mol%)的所述官能团。在一些实施方案中,(a)包括将所述包含多个第一反应性基团的多个聚合物链共价接枝至所述胺化珠子上,以提供各自通过各自一个所述聚合物链偶联至所述珠子的多个第二反应性基团。
在本文提供的方面的一些实施方案中,所述第一和第二反应性基团是相同的。在本文提供的方面的一些实施方案中,所述珠子是磁性的。在本文提供的方面的一些实施方案中,所述聚合物是预先制备的。在本文提供的方面的一些实施方案中,所述方法进一步包括对偶联至所述胺封端或羟基封端的引物的多个克隆核酸分子进行测序。在本文提供的方面的一些实施方案中,在(a)之前,所述聚合物链包含浓度小于或等于约60mol%的反应性酯重复单元。在本文提供的方面的一些实施方案中,所述方法进一步包括对包含羧酸基团的珠子进行胺化,以提供所述胺化的珠子。在本文提供的方面的一些实施方案中,所述官能团为–nh2;–nh(ch3)、–n(ch3)2;–nh(ch2)t—oh,其中‘t’=1至4;–(och2ch2)v—oh,其中‘v’=1至100;–(och2ch2)v—ch3,其中‘v’=1至100;–(och2ch2)v—och3,其中‘v’=1至100;或—och3。
本公开内容的另一方面提供了包含用聚合物链官能化的珠子的试剂,其中每一个所述聚合物链均包含下式的碳骨架:
其中‘r’为
其中‘t’选自nh2、nh(ch3)、n(ch3)2、nh(ch2)toh、(och2ch2)vch3、(och2ch2)voh、(och2ch2)voch3和och3,其中‘t’=1至4,‘v’=1至100;
其中‘r2’和‘r3’独立地为h或ch3;
其中‘y’和‘z’为摩尔百分比,其中(‘y’+‘z’)=100摩尔%,其中‘y’小于或等于60摩尔%,‘z’大于或等于40摩尔%;并且
其中‘w’为单键或
在本文提供的方面的一些实施方案中,‘r’为
在本文提供的方面的一些实施方案中,‘r’为
在本文提供的方面的一些实施方案中,‘q’为no2。在本文提供的方面的一些实施方案中,‘q’为fx。
在本文提供的方面的一些实施方案中,‘w’为
在本文提供的方面的一些实施方案中,‘di’为h。在本文提供的方面的一些实施方案中,‘di’为ch3。在本文提供的方面的一些实施方案中,‘t’为nh2。在本文提供的方面的一些实施方案中,‘t’为nh(ch2)toh。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)voh。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)voch3。在本文提供的方面的一些实施方案中,‘t’为nh(ch3)。在本文提供的方面的一些实施方案中,‘t’为nh(ch3)2。在本文提供的方面的一些实施方案中,‘t’为och3。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)vch3。
在本文提供的方面的一些实施方案中,‘r2’为h。在本文提供的方面的一些实施方案中,‘r2’为ch3。在本文提供的方面的一些实施方案中,‘r3’为h。在本文提供的方面的一些实施方案中,‘r3’为ch3。在本文提供的方面的一些实施方案中,所述聚合物链中的单个聚合物链具有约50千道尔顿(kda)至约2500kda的分子量。在本文提供的方面的一些实施方案中,所述珠子为磁珠。在本文提供的方面的一些实施方案中,核酸分子通过‘r’偶联至所述珠子。在本文提供的方面的一些实施方案中,所述核酸分子为引物。
本公开内容的另一方面提供了用于将引物偶联至珠子的方法,该方法包括:(a)提供珠子,该珠子包含连接(例如,共价连接)至其表面的胺基团;(b)使至少一部分所述胺基团与包含下式的碳骨架的聚合物链反应:
其中‘r’为
其中‘t’选自nh2、nh(ch3)、n(ch3)2、nh(ch2)toh、(och2ch2)vch3、(och2ch2)voh、(och2ch2)voch3和och3,其中‘t’=1至4,‘v’=1至100;
其中‘r2’和‘r3’独立地为h或ch3;
其中‘y’和‘z’为摩尔百分比,其中(’y’+‘z’)=100摩尔%,其中‘y’小于或等于60摩尔%,‘z’大于或等于40摩尔%;并且
其中‘w’为单键或
(c)使所固定化的聚合物链与包含胺基团的引物反应,从而提供偶联至所述固定化聚合物链的至少一部分上的固定化引物。
在本文提供的方面的一些实施方案中,‘r’为
在本文提供的方面的一些实施方案中,‘r’为
在本文提供的方面的一些实施方案中,‘q’为no2。
在本文提供的方面的一些实施方案中,‘q’为fx。
在本文提供的方面的一些实施方案中,‘w’为
在本文提供的方面的一些实施方案中,‘di’为h。在本文提供的方面的一些实施方案中,‘di’为ch3。在本文提供的方面的一些实施方案中,‘t’为nh2。在本文提供的方面的一些实施方案中,‘t’为nh(ch2)toh。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)voh。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)voch3。在本文提供的方面的一些实施方案中,‘t’为nh(ch3)。在本文提供的方面的一些实施方案中,‘t’为nh(ch3)2。在本文提供的方面的一些实施方案中,‘t’为och3。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)vch3。
在本文提供的方面的一些实施方案中,‘r2’为h。在本文提供的方面的一些实施方案中,‘r2’为ch3。在本文提供的方面的一些实施方案中,‘r3’为h。在本文提供的方面的一些实施方案中,‘r3’为ch3。在本文提供的方面的一些实施方案中,所述聚合物链中的单个聚合物链具有约50千道尔顿(kda)至约2500kda的分子量。在本文提供的方面的一些实施方案中,所述珠子为磁珠。在本文提供的方面的一些实施方案中,所述方法进一步包括,在(c)之后,将所述固定化聚合物链上的至少一部分任意游离‘r’基团加帽(capping)。在本文提供的方面的一些实施方案中,通过使至少一部分任意剩余的‘r’基团在三乙胺的存在下与氢氧化铵反应来实现所述加帽。在本文提供的方面的一些实施方案中,所述方法进一步包括对一个或多个额外的珠子重复(a)-(c)。
本公开内容的另一方面提供了包含用聚合物链官能化的珠子的试剂,其中每一个所述聚合物链均包含下式的碳骨架:
其中‘t’选自nh2、nh(ch3)、n(ch3)2、nh(ch2)toh、(och2ch2)vch3、(och2ch2)voh、(och2ch2)voch3和och3,其中‘t’为1至4,‘v’为1至100;
其中‘r2’、‘r3’、‘r4’和‘r5’独立地为h或ch3;并且
其中‘y’和‘z’为摩尔百分比,其中(’y’+‘z’)=100摩尔%,其中‘y’小于或等于60摩尔%,‘z’大于或等于40摩尔%。
在本文提供的方面的一些实施方案中,‘t’为nh2。在本文提供的方面的一些实施方案中,‘t’为nh(ch2)toh。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)voh。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)voch3。在本文提供的方面的一些实施方案中,‘t’为nh(ch3)。在本文提供的方面的一些实施方案中,‘t’为nh(ch3)2。在本文提供的方面的一些实施方案中,‘t’为och3。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)vch3。在本文提供的方面的一些实施方案中,所述聚合物链中的单个聚合物链具有约50千道尔顿(kda)至约2500kda的分子量。在本文提供的方面的一些实施方案中,所述珠子为磁珠。
在本文提供的方面的一些实施方案中,核酸分子通过
在本文提供的方面的一些实施方案中,所述核酸分子为引物。
本公开内容的另一方面提供了用于将引物偶联至珠子的方法,该方法包括:(a)提供珠子,该珠子包含连接至其表面的胺基团;
(b)使至少一部分所述胺基团与包含下式的碳骨架的聚合物链反应:
其中‘t’选自nh2、nh(ch3)、n(ch3)2、nh(ch2)toh、(och2ch2)vch3、(och2ch2)voh、(och2ch2)voch3和och3,其中‘t’=1至4,‘v’=1至100;
其中‘r2’、‘r3’、‘r4’和‘r5’独立地为h或ch3;并且
其中‘y’和‘z’为摩尔百分比,其中(’y’+‘z’)=100摩尔%,其中‘y’小于或等于60摩尔%,‘z’大于或等于40摩尔%;以及
(c)使所固定化的聚合物链与包含胺基团的引物反应,从而提供偶联至所述固定化聚合物链的至少一部分上的固定化引物。
在本文提供的方面的一些实施方案中,‘t’为nh2。在本文提供的方面的一些实施方案中,‘t’为nh(ch2)toh。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)voh。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)voch3。在本文提供的方面的一些实施方案中,‘t’为nh(ch3)。在本文提供的方面的一些实施方案中,‘t’为nh(ch3)2。在本文提供的方面的一些实施方案中,‘t’为och3。在本文提供的方面的一些实施方案中,‘t’为(och2ch2)vch3。
在本文提供的方面的一些实施方案中,所述聚合物链中的单个聚合物链具有约50千道尔顿(kda)至约2500kda的分子量。在本文提供的方面的一些实施方案中,所述珠子为磁珠。在本文提供的方面的一些实施方案中,所述方法进一步包括对一个或多个额外的珠子重复(a)-(c)。
本发明内容的另一方面提供了引物包覆的珠子,其包含珠子、附接至所述珠子的连接体和附接至所述连接体的引物。所述连接体可包含具有离散数目的重复单元的聚合物链。在一些情况下,所述珠子是磁性的。在一些情况下,所述聚合物链包含聚乙二醇(peg)重复单元。在一些情况下,所述聚合物链包含至少约20个重复单元。在一些情况下,所述引物通过酰胺键附接至所述连接体。在一些情况下,所述珠子包含相同数目的引物和连接体。
本公开内容的另一方面提供了用于产生引物包覆的珠子的方法。所述方法可包括提供具有第一羧基基团的珠子;通过使第一胺基团与所述第一羧基基团反应,将包含第一胺基团、包含离散数目的重复单元的聚合物链和第二羧基基团的连接体附接至所述珠子;以及通过使第二胺基团与所述第二羧基基团反应,将包含第二胺基团的引物附接至所述连接体。
本公开内容的另一方面提供了用于产生引物包覆的珠子的方法。所述方法可包括提供具有第一胺基团的珠子;通过使第一羧基基团与所述第一胺基团反应,将包含第一羧基基团、包含离散数目的重复单元的聚合物链和第二胺基团的连接体附接至所述珠子;以及通过使第二羧基基团与所述第二胺基团反应,将包含所述第二羧基基团的引物附接至所述连接体。
在一些方面,所述珠子是磁性的。在一些方面,所述聚合物链包含聚乙二醇(peg)重复单元。在一些方面,所述聚合物链包含至少约20个重复单元。在一些方面,使用相同数目的引物和连接体。
本公开内容的另一方面提供了包含用聚合物链官能化的珠子的试剂。每个所述聚合物链均可包含下式的碳骨架:
其中‘x’为卤素;
其中‘r1’为oh;(och2ch2)voh,其中v=1至200;nh(ch2)aoh,其中‘a’=1至6;nh(ch2ch2o)tch2ch2oh,其中‘t’=0至200;
其中‘t’选自nh2、nh(ch3)、n(ch3)2、n(ch2ch3)2、nhch2ch2(och2ch2)boch3和(och2ch2)doch3,其中‘b’=0至200,‘d’=1至200;
其中‘r2’和‘r3’独立地为h或ch3;
其中‘x’和‘y’为摩尔百分比,其中(’x’+‘y’)=100mol%并且‘x’在0.01mol%至100mol%的范围内,并且
其中‘w’为单键或
在一些实施方案中,‘x’为溴。在一些实施方案中,‘r1’为
在一些实施方案中,所述聚合物链中的单个聚合物链具有约50千道尔顿(kda)至约2500kda的分子量。在一些实施方案中,所述珠子为磁珠。在一些实施方案中,核酸分子通过‘r1’偶联至所述珠子。在一些实施方案中,所述核酸分子为引物。
本公开内容的另一方面提供了包含用聚合物链官能化的珠子的试剂。每个所述聚合物链均可包含下式的碳骨架:
其中‘x’为卤素;
其中‘r1’为oh;(och2ch2)voh,其中v=1至200;nh(ch2)aoh,其中‘a’=1至6;nh(ch2ch2o)tch2ch2oh,其中‘t’=0至200;
其中‘t’选自nh2、nh(ch3)、n(ch3)2、n(ch2ch3)2、nhch2ch2(och2ch2)boch3和(och2ch2)doch3,其中‘b’=0至200,‘d’=1至200;
其中‘r2’和‘r3’独立地为h或ch3;
其中‘y’、‘p’、‘q’和‘x’为摩尔百分比,其中(‘x’+‘y’)=100mol%,(‘p’+‘q’)=x,x在0.01mol%至100mol%的范围内,并且‘p’在0.01mol%至100mol%的范围内,并且
其中‘w’为单键或
在一些实施方案中,‘x’为溴。在一些实施方案中,‘r1’为
在一些实施方案中,所述聚合物链中的单个聚合物链具有约50千道尔顿(kda)至约2500kda的分子量。在一些实施方案中,所述珠子为磁珠。在一些实施方案中,核酸分子通过‘r1’偶联至所述珠子。在一些实施方案中,所述核酸分子为引物。
本公开内容的另一方面提供了包含用聚合物链官能化的珠子的试剂。每个所述聚合物链均可包含下式的碳骨架:
其中‘x’为卤素;
其中‘r2’、‘r3’、‘r4’和‘r5’独立地为h或ch3;
其中‘t’选自nh2、nh(ch3)、n(ch3)2、n(ch2ch3)2、nhch2ch2(och2ch2)boch3和(och2ch2)doch3,其中‘b’=0至200,‘d’=1至200;并且
其中‘x’和‘y’为摩尔百分比,其中(‘x’+‘y’)=100mol%并且‘x’在0.01mol%至100mol%的范围内。
在一些实施方案中,‘x’为溴。在一些实施方案中,‘t’为nh2。在一些实施方案中,‘t’为nh(ch3)。在一些实施方案中,‘t’为n(ch3)2。在一些实施方案中,‘t’为n(ch2ch3)2。在一些实施方案中,‘t’为nhch2ch2(och2ch2)boch3。在一些实施方案中,‘t’为(och2ch2)doch3。
在一些实施方案中,所述聚合物链中的单个聚合物链具有约50千道尔顿(kda)至约2500kda的分子量。在一些实施方案中,所述珠子为磁珠。在一些实施方案中,核酸分子通过
本公开内容的另一方面提供了包含用聚合物链官能化的珠子的试剂。每个所述聚合物链均可包含下式的碳骨架:
其中‘x’为卤素;
其中‘r2’、‘r3’、‘r4’和‘r5’独立地为h或ch3;
其中‘t’选自nh2、nh(ch3)、n(ch3)2、n(ch2ch3)2、nhch2ch2(och2ch2)boch3和(och2ch2)doch3,其中‘b’=0至200,‘d’=1至200;并且
其中‘y’、‘p’、‘q’和‘x’为摩尔百分比,其中(‘x’+‘y’)=100mol%,(‘p’+‘q’)=x,x在0.01mol%至100mol%的范围内,并且‘p’在0.01至100mol%的范围内。
在一些实施方案中,‘x’为溴。在一些实施方案中,‘t’为nh2。在一些实施方案中,‘t’为nh(ch3)。在一些实施方案中,‘t’为n(ch3)2。在一些实施方案中,‘t’为n(ch2ch3)2。在一些实施方案中,‘t’为nhch2ch2(och2ch2)boch3。在一些实施方案中,‘t’为(och2ch2)doch3。
在一些实施方案中,所述聚合物链中的单个聚合物链具有约50千道尔顿(kda)至约2500kda的分子量。在一些实施方案中,所述珠子为磁珠。在一些实施方案中,核酸分子通过
本公开内容的另一方面提供了用于将寡核苷酸偶联至珠子的方法,该方法包括:(a)提供所述珠子,该珠子包含连接至其表面的
其中‘r1’为oh;(och2ch2)voh,其中v=1至200;nh(ch2)aoh,其中‘a’=1至6;nh(ch2ch2o)tch2ch2oh,其中‘t’=0至200;
其中‘t’选自nh2、nh(ch3)、n(ch3)2、n(ch2ch3)2、nhch2ch2(och2ch2)boch3和(och2ch2)doch3,其中‘b’=0至200,‘d’=1至200;
其中‘r2’、‘r4’和‘r5’独立地为h或ch3;并且
其中‘w’为单键或
(ii)所述第二单体包括:
其中‘t’选自nh2、nh(ch3)、n(ch3)2、n(ch2ch3)2、nhch2ch2(och2ch2)boch3和(och2ch2)doch3,其中‘b’=0至200,‘d’=1至200,
其中‘r3’为h或ch3;并且
(iii)所述聚合物链经由所述第一单体和/或所述第二单体与所述珠子的
在一些实施方案中,所述第一单体为
其中‘x’和‘y’为摩尔百分比,其中(’x’+‘y’)=100mol%并且‘x’在0.01mol%至100mol%的范围内。
在一些实施方案中,所述聚合物链包含下式的碳骨架:
其中‘y’、‘p’、‘q’和‘x’为摩尔百分比,其中(‘x’+‘y’)=100mol%,(‘p’+‘q’)=x,x在0.01mol%至100mol%的范围内,并且‘p’在0.01mol%至100mol%的范围内。
在一些实施方案中,所述聚合物链包含下式的碳骨架:
其中‘x’和‘y’为摩尔百分比,其中(’x’+‘y’)=100mol%并且‘x’在0.01mol%至100mol%的范围内。
在一些实施方案中,‘w’为单键并且‘r1’为nh(ch2)2oh。在一些实施方案中,所述方法进一步包括使nh(ch2)2oh与n-(5-氨基-1-羧基戊基)亚氨基二乙酸反应以生成包含下式的聚合物链:
在一些实施方案中,所述聚合物链包含下式的骨架:
其中‘y’、‘p’、‘q’和‘x’为摩尔百分比,其中(‘x’+‘y’)=100mol%,(‘p’+‘q’)=x,x在0.01mol%至100mol%的范围内,并且‘p’在0.01至100mol%的范围内。
在一些实施方案中,‘r1’为
在一些实施方案中,所述一个或多个寡核苷酸为引物。在一些实施方案中,所述一个或多个寡核苷酸包含与‘r1’共价偶联的游离胺基团。在一些实施方案中,所述珠子的
对于本领域技术人员,本发明的额外方面和优点将会从以下的详细描述中变得显而易见,其中仅示出和描述了本公开内容的说明性实施方案。应当意识到,本公开内容能够具有其他的和不同的实施方案,并且其若干细节能够在各种明显的方面进行修改,所有这些都不偏离本公开内容。因此,附图和描述将被视为说明性的而不是限制性的。
援引并入
本说明书中所提及的所有出版物、专利和专利申请均通过引用而并入于此,其程度如同具体地和个别地指出要通过引用而并入每一单个出版物、专利或专利申请。
附图简述
本发明的新颖特征在所附权利要求中具体阐明。通过参考以下对在其中利用到本发明原理的说明性实施方案加以阐述的具体描述和附图(在本文中也称为“图”),将会对本发明的特征和优点获得更好的理解;在附图中:
图1为集成式测序平台的示意图。
图2a示出了示例传感器阵列的示意图。
图2b示出了具有固定至传感器阵列的载体(carrier)的示例传感器阵列的示意图。
图2c示出了具有固定至传感器阵列的载体并与适合于核酸扩增的试剂相接触的示例传感器阵列的示意图。
图2d示出了示例传感器阵列示意图,其中核酸扩增发生在传感器阵列的每一阵列像素处。
图2e示出了从示例传感器阵列移除试剂的示意性示例。
图2f示出了示例传感器阵列的示意图,其中在传感器阵列的每一像素处对核酸进行测序。
图3示出了示例生物检测装置,其包含外壳、可移除的芯片和可移除的试剂储器。
图4示出了示例计算机系统,其被编程或以其他方式配置用于控制、调节或实现本公开内容的装置、系统和方法。
图5示出了引物缀合的珠子的制备示例。
图6示出了用于在表面上测序的引物缀合的磁珠示例。
图7示出了羧基磁珠的胺化示例。
图8a示出了反应性接枝聚合物的制备示例。
图8b示出了反应性聚合物的接枝和引物缀合示例。
图9a示出了反应性接枝聚合物的制备示例。
图9b示出了反应性聚合物的接枝和引物缀合示例。
图9c示出了接枝聚合物的制备示例。
图10示出了显示聚合物接枝的磁珠上的引物加载示例的数据。
图11示出了100%活性聚合物和15-聚体引物对扩增的加载影响示例。
图12示出了20%活性聚合物和15-聚体引物对扩增的加载影响示例。
图13示出了引物包覆的、具有peg连接体的珠子的制备示例。
图14示出了使用谷氨酸来增加活性位点以供引物包覆的、具有peg连接体的珠子上的引物加载的示例。
图15示出了采用原子转移自由基聚合(atrp)产生的引物包覆的磁性颗粒的示例。
图16示出了包含atrp生成的聚合物的珠子的制备示例。
图17示出了包含atrp生成的聚合物的珠子的示例。
图18示出了包含与寡核苷酸相附接的atrp生成的聚合物的珠子的制备示例。
图19示出了包含与寡核苷酸相附接的atrp生成的聚合物的珠子的制备示例。
图20a-20c图示了带有peg化寡核苷酸的珠子的制备示例。
具体实施方式
尽管本文已经示出和描述了本发明的各种实施方案,但对于本领域技术人员而言显而易见的是,这些实施方案只是以示例的方式提供的。本领域技术人员可以想到不偏离本发明的许多变化、改变和替换。应当理解,可以采用对本文所述的本发明实施方案的各种替代方案。
本文所使用的术语“相邻于”一般是指紧邻于、接近于或者在感测或电子范围(或距离)(electronicvincityorproximity)内的。例如,相邻于第二物体的第一物体可以与所述第二物体接触,或者可以不与所述第二物体接触但可以接近该第二物体。在一些示例中,邻近于第二物体的第一物体处于第二物体的约0微米(“百万分之一米”)、0.001微米、0.01微米、0.1微米、0.2微米、0.3微米、0.4微米、0.5微米、1微米、2微米、3微米、4微米、5微米、10微米或100微米内。
如本文所用的,术语“核酸”或“多核苷酸”通常是指包含一个或多个核酸亚单位或核苷酸的分子。核酸可包含选自腺苷(a)、胞嘧啶(c)、鸟嘌呤(g)、胸腺嘧啶(t)和尿嘧啶(u)或它们的变体的一个或多个核苷酸。核苷酸通常包含核苷和至少1、2、3、4、5、6、7、8、9、10个或更多个磷酸(po3)基团。核苷酸可包含核碱基、五碳糖(核糖或脱氧核糖)和一个或多个磷酸基团。核糖核苷酸是其中糖为核糖的核苷酸。脱氧核糖核苷酸是其中糖为脱氧核糖的核苷酸。核苷酸可为核苷单磷酸或核苷多磷酸。核苷酸可为脱氧核糖核苷多磷酸,例如,可选自脱氧腺苷三磷酸(datp)、脱氧胞苷三磷酸(dctp)、脱氧鸟苷三磷酸(dgtp)、尿苷三磷酸(dutp)和脱氧胸苷三磷酸(dttp)的脱氧核糖核苷三磷酸(dntp),其包含可检测标签,如发光标签或标志物(例如,荧光团)。核苷酸可包含可掺入正在生长的核酸链中的任何亚单位。这样的亚单位可为a、c、g、t或u,或对一种或多种互补a、c、g、t或u为特异性的或与嘌呤(例如,a或g或其变体)或嘧啶(例如,c、t或u或其变体)互补的任何其他亚单位。在一些示例中,核酸为脱氧核糖核酸(dna)、核糖核酸(rna)或它们的衍生物或变体。核酸可以是单链或双链的。在一些情况下,核酸分子是环状的。
如本文所用的,术语“核酸分子”、“核酸序列”、“核酸片段”、“寡核苷酸”和“多核苷酸”通常是指可具有不同长度的多核苷酸,如脱氧核糖核苷酸或核糖核苷酸(rna),或它们的类似物。核酸分子可具有至少约100个碱基、200个碱基、300个碱基、400个碱基、500个碱基、1千碱基(kb)、2kb、3、kb、4kb、5kb、10kb或50kb的长度。寡核苷酸通常由以下四种核苷酸碱基的特定序列构成:腺嘌呤(a);胞嘧啶(c);鸟嘌呤(g);和胸腺嘧啶(t)(在多核苷酸为rna时,尿嘧啶(u)代替胸腺嘧啶(t))。因此,术语“寡核苷酸序列”是多核苷酸分子的字母表示;或者,该术语可应用于该多核苷酸分子本身。可将该字母表示输入至具有中央处理器单元的计算机的数据库中并用于生物信息学应用,如功能基因组学和同源性检索。寡核苷酸可包含一个或多个非标准核苷酸、核苷酸类似物和/或修饰的核苷酸。如本文所用的,术语“核苷酸”通常是指充当核酸分子如脱氧核糖核酸(dna)分子或核糖核酸(rna)分子的单体或亚单位的有机分子。
修饰的核苷酸的示例包括但不限于二氨基嘌呤、5-氟尿嘧啶、5-溴尿嘧啶、5-氯尿嘧啶、5-碘尿嘧啶、次黄嘌呤、黄嘌呤、4-乙酰胞嘧啶、5-(羧基羟甲基)尿嘧啶、5-羧甲基氨基甲基-2-硫尿苷、5-羧甲基氨基甲基尿嘧啶、二氢尿嘧啶、β-半乳糖基辫苷、肌苷、n6-异戊烯腺嘌呤、1-甲基鸟嘌呤、1-甲基肌苷、2,2-二甲基鸟嘌呤、2-甲基腺嘌呤、2-甲基鸟嘌呤、3-甲基胞嘧啶、5-甲基胞嘧啶、n6-腺嘌呤、7-甲基鸟嘌呤、5-甲基氨基甲基尿嘧啶、5-甲氧基氨基甲基-2-硫尿嘧啶、β-d-甘露糖基辫苷、5'-甲氧基羧基甲基尿嘧啶、5-甲氧基尿嘧啶、2-甲硫基-d46-异戊烯基腺嘌呤、尿嘧啶-5-氧基乙酸(v)、怀丁苷(wybutoxosine)、假尿嘧啶、辫苷、2-硫胞嘧啶、5-甲基-2-硫尿嘧啶、2-硫尿嘧啶、4-硫尿嘧啶、5-甲基尿嘧啶、尿嘧啶-5-氧基乙酸甲酯、尿嘧啶-5-氧基乙酸(v)、5-甲基-2-硫尿嘧啶、3-(3-氨基-3-n-2-羧丙基)尿嘧啶、(acp3)w、2,6-二氨基嘌呤,等等。核酸分子还可在碱基部分(例如,在通常可与互补核苷酸形成氢键的一个或多原子处和/或在通常不能与互补核苷酸形成氢键的一个或多个原子处)、糖部分或磷酸骨架处被修饰。核酸分子还可含有胺修饰的基团,如氨基烯丙基-dutp(aa-dutp)和氨基己基丙烯酰胺-dctp(aha-dctp),以允许胺反应性部分如n-羟基琥珀酰亚胺酯(nhs)的共价附接。在本公开的寡核苷酸中,标准dna碱基对或rna碱基对的替代物可提供更高的密度(每立方毫米的比特数)、更高的安全性(耐受天然毒素的意外或有目的的合成)、更容易在光编程的聚合酶中区分,或更少的二级结构。与用于从头合成和/或扩增合成的天然和突变聚合酶兼容的替代碱基对在betzk,malyshevda,lavergnet,weltew,diederichsk,dwyertj,ordoukhanianp,romesbergfe,marxa(2012)中描述。
如本文所用的,术语“聚合酶”通常是指能够催化聚合反应的任何酶。聚合酶的示例包括但不限于核酸聚合酶。聚合酶可以是天然存在的或合成的。示例聚合酶为φ29聚合酶或其衍生物。聚合酶可为聚合作用酶(polymerizationenzyme)。在一些情况下,使用转录酶或连接酶(例如,催化键的形成的酶)。聚合酶的示例包括dna聚合酶、rna聚合酶、热稳定聚合酶、野生型聚合酶、修饰的聚合酶、大肠杆菌dna聚合酶i、t7dna聚合酶、噬菌体t4dna聚合酶φ29(phi29)dna聚合酶、taq聚合酶、tth聚合酶、tli聚合酶、pfu聚合酶、pwo聚合酶、vent聚合酶、deepvent聚合酶、ex-taq聚合酶、la-taq聚合酶、sso聚合酶、poc聚合酶、pab聚合酶、mth聚合酶、es4聚合酶、tru聚合酶、tac聚合酶、tne聚合酶、tma聚合酶、tca聚合酶、tih聚合酶、tfi聚合酶、platinumtaq聚合酶、tbr聚合酶、tfl聚合酶、tth聚合酶、pfutubo聚合酶、pyrobest聚合酶、pwo聚合酶、kod聚合酶、bst聚合酶、sac聚合酶、klenow片段、具有3'至5'核酸外切酶活性的聚合酶,以及它们的变体、修饰产物和衍生物。在一些实施方案中,该聚合酶为单亚基聚合酶。该聚合酶可具有高持续性,即,聚合酶持续将核苷酸掺入核酸模板中而不释放核酸模板的能力。
如本文所用的,术语“引物”通常是指在诸如引物延伸反应期间充当核酸合成起点的核酸链,该引物延伸反应可以是核酸扩增反应的组成部分。通常,引物与模板链杂交,并且核苷酸被添加至引物的末端,该添加有时在聚合作用酶如聚合酶的帮助下进行。在示例中,在dna样品的复制期间,催化复制的酶在附接至dna样品的引物的3’端开始复制并拷贝相反链。引物可具有一个或多个官能团,该官能团可用于使该引物偶联至支持体或载体,如珠子或颗粒。
如本文所用的,术语“受试者”通常是指其生物样品正经历处理或分析的个体。受试者可为动物或植物。受试者可为哺乳动物,如人。受试者可患有或疑似患有疾病,如癌症(例如,乳腺癌、结肠直肠癌、肺癌、皮肤癌或子宫颈癌)或传染病。
如本文所用的,术语“颗粒”和“珠子”可互换使用,并且通常是指可能近似为球形并且/或者较小(例如,直径小于约1mm、小于约0.1mm、小于约0.01mm或小于约0.005mm)的固体支持体。
术语“连接至”通常是指两种物质彼此物理关联。两种物质可直接或间接地彼此连接。例如,当物质a连接至物质b时,物质a可直接连接至物质b或间接连接至物质b。物质a可通过共价键或非共价键(例如,电荷相互作用、范德华力等)直接连接至物质b。在一些情况下,物质a可通过一种或多种中间体如连接体间接连接至物质b。
集成式测序平台
本公开内容提供了可包含多个组件的集成式测序平台。该集成式测序平台可用于多种应用,如对来自受试者的核酸样品进行测序。
集成式测序平台可包括核酸(例如,dna)提取系统、文库构建系统、扩增系统、富集系统和测序系统。在一些实施方案中,所述系统可以是单独的和/或是模块化形式的。在一些实施方案中,集成式测序平台可包括这些系统中的一个、两个、三个、四个或所有五个系统。在一些情况下,所述系统可以集成在单一微流体装置和/或单一阵列(例如,可重复使用的阵列)内。在图1中示出了这样的集成式平台的示例。这样的集成式测序平台的其他示例可在以下文献中找到:pct专利申请号pct/us2011/054769、pct专利申请号pct/us2012/039880、pct专利申请号pct/us2012/067645、pct专利申请号pct/us2014/027544和pct专利申请号pct/us2014/069624,上述每一文献均通过引用而全文并入于。
集成式系统可包括文库构建系统(例如,核酸文库构建系统),该文库构建系统可包含片段化和/或大小选择元件。文库构建系统的示例在图1中示出。如图1所示,文库构建系统可包含核酸(例如,dna)片段化和大小选择元件116。片段化和大小选择元件116可被配置用于经由下文所述的元件和方法产生可具有或可不具有平端的双链核酸片段。片段化和大小选择元件116可包含一个或多个微流体通道122,其中可以安设核酸以及一组片段化珠子124。可通过任何合适的方法(例如,加压注射、电泳运动、重力进料、热诱导的运动、超声运动等)将核酸(例如,dna)提取系统(例如,图1所示的)中收集的核酸112输送或“注射”至核酸(例如,dna)片段化和大小选择元件116中。类似地,可通过任何合适的方法将片段化珠子124输送至核酸(例如,dna)片段化和大小选择元件116中。
片段化和/或大小选择元件116可包含泵126,以在微流体通道122内产生流体(例如,包含核酸(例如,dna)和片段化珠子124的流体)移动。例如,泵126可为蠕动泵。在一些实施方案中,泵126可包含与微流体通道122流体连通的一个或多个微流体元件,并且其可具有柔性的侧壁,该柔性侧壁在变形时于微流体通道122内产生流动。然而,在其他实施方案中,作为替代或除此之外,任何其他合适的机构可用于在微流体通道122内产生移动流体,非限制性示例包括流体的选择性加热和冷却、微流体通道的气动加压、电泳运动等。
可从适用于将核酸(例如,dna)分离、切割和/或以其他方式细分成核酸片段(例如,dna片段)的任何材料构建片段化珠子124。在一些实施方案中,可从玻璃、聚二甲基硅氧烷(pdms)、陶瓷等构建片段化珠子124。此外,片段化珠子124可具有任何合适的大小和/或几何形状,使得片段化元件产生具有所需特征(例如,长度、链特征等)的片段。例如,在一些实施方案中,片段化珠子124可以基本上是球形的,并且可具有50μm或更小的直径。在其他实施方案中,片段化珠子可具有500nm或更小的直径,或50μm至500nm之间的任何直径。
此外,可以选择微流体通道122的大小和/或几何形状(例如,横截面形状、纵横比等),使得核酸(例如,dna)在微流体通道122内的移动和核酸与片段化珠子124片段(例如,经由剪切)的接触是期望的。在一些实施方案中,微流体通道122的水力直径可在1至500μm的范围内(例如,微流体通道122的横截面积可以基本上是矩形的,因此大小可以用水力直径表示)。在其他实施方案中,微流体通道122的水力直径可在10至200μm的范围内。在又一其他实施方案中,微流体通道122的水力直径可在500nm或更小的范围内。在其他实施方案中,微流体通道122可具有任何合适的形状,如半圆形、椭圆形、锥形等。在一些实施方案中,可进行剪切的核酸(例如,dna)末端的酶促抛光(polishing),使得该端是平端。
在其他实施方案中,可将酶溶液输送至微流体通道122中,以至少部分地产生核酸(例如,dna)的酶促片段化。
在一些实施方案中,核酸(例如,脱氧核糖核酸(dna))扩增和测序可在同一系统内按顺序进行。在这样的情况下,样品核酸可关联于多个载体,举例而言,诸如珠子或其他类型的颗粒。在一些情况下,载体可以是磁性载体,举例而言,诸如磁珠或顺磁珠。在一些情况下,磁性载体可进入到磁性特征的阵列(例如,包含基本平坦的衬底的基本平坦的阵列)中,使得磁性载体由阵列的每一位置(例如,像素)处的局部磁场保持就位。在一些实施方案中,由于载体或关联的核酸的电荷,载体(包括磁性载体)可经由一个或多个电极通过静电力在阵列(例如,基本平坦的阵列)的每一位置处保持就位。在其他实施方案中,载体可由物理沟槽或孔在阵列的每个位置处保持就位。在一些实施方案中,载体可通过结合至载体的物质与结合至阵列的物质的相互作用(例如,寡核苷酸的杂交或通过配体-捕获部分对)而在阵列的每个位置处保持就位。在载体向阵列的固定之后,可以按顺序或同时完成关联的核酸的扩增和扩增的核酸的测序。
在一些实施方案中,可首先使载体进入到阵列中(例如,经由穿过与阵列相关联的微流体通道的流)并由阵列将其捕获。在载体捕获之后,可使样品核酸与阵列接触(例如,经由穿过与阵列相关联的微流体通道的流)并继而由载体将其捕获。捕获可例如经由与载体相关联并能够与样品核酸杂交的核酸而发生。这样的核酸还可被用作本文其他各处所描述的扩增反应的引物。在一些实施方案中,待扩增和/或测序的核酸在被阵列捕获之前与载体相关联。
或者,阵列的表面(例如,传感器表面、阵列衬底表面等)可包含适合于捕获样品核酸(包括能够与样品核酸杂交的核酸)的元件。这样的核酸还可以能够充当本文其他各处所描述的扩增反应的引物。这样的配置可适合于在没有载体的情况下对核酸进行扩增和测序。
在一些实施方案中,为了获得样品核酸分子与载体的所需比例,可以将样品核酸以极稀浓度提供至阵列。例如,一个核酸分子比一个载体(例如,珠子)、一个核酸分子比两个载体、一个核酸分子比三个载体、一个核酸分子比五个珠子或者更小的比例可能是期望的。
在扩增反应期间,位于阵列的传感器位置处的一个或多个电极可以用于浓缩对于核酸扩增有用的试剂,从而经由电场形成与阵列位置处的载体、传感器或衬底相关联的“虚拟孔”。虚拟孔可以允许在没有反应物与阵列的其他传感器的反应物的交叉污染的情况下在传感器位置处的核酸扩增。在某些实施方案中,虚拟孔内的扩增可生成与关联于该虚拟孔的载体、传感器表面或衬底相关联的核酸的克隆群。
如果需要,核酸扩增可以在多个循环中进行。一旦在使阵列与样品核酸接触之后完成第一轮扩增,就可以洗涤该阵列以便移除任何未结合的扩增子和溶液中的其他试剂。在洗涤后,通过使阵列与样品核酸接触并使捕获的样品核酸经受适当的条件,可以完成第二轮扩增。当生成克隆群时,样品可以仅结合至尚未包含扩增子的位点(例如,载体、传感器表面等),这是因为具有来自第一轮扩增的扩增子的位点可能完全加载了扩增子。该过程可以重复任意数目的扩增循环,直到捕获位点耗尽。利用多轮扩增可以帮助消除双泊松分布问题,并帮助确保每个传感器位点仅关联于核酸序列,诸如附接至载体(例如,珠子)的扩增子的克隆群。这样的附接可以是扩增子与载体的直接附接,或是扩增子通过连接体如直接结合至载体的核酸分子与载体的附接。此外,多轮扩增还可帮助使阵列的使用率最大化,这是因为每轮扩增可以更好地确保阵列的所有像素均由扩增子占据以供测序。
此外,在测序反应期间,可以使用一个或多个相同电极和/或不同电极来检测感兴趣的反应,诸如核苷酸掺入。在一些情况下,可以使用纳米针(nanoneedle)和/或纳米桥(nanobridge)传感器,或者其他适合用于检测的电传感器或光传感器来完成感测。如在通过引用而全文并入于此的名称为“biosensordevices,systemsandmethodstherefor”美国专利申请公开us2012/0138460中所述,纳米桥传感器可发挥ph传感器或电荷传感器的作用。如在各自通过引用而全文并入于此的pct专利申请号pct/us2011/054769、pct专利申请号pct/us2012/039880、pct专利申请号pct/us2012/067645、pct专利申请号pct/us2014/027544和pct专利申请号pct/us2014/069624中所述,传感器(例如,纳米针传感器)可发挥电荷传感器、电导率传感器和/或阻抗传感器的作用。在一些实施方案中,感兴趣的测序反应可以是dna测序。
检测可以基于下列各项中的至少一项:局部ph变化、局部阻抗变化、局部热检测、局部电容变化、局部电荷浓度(或其变化)和局部电导率变化。在一些实施方案中,检测可以基于载体、核酸或与该载体和/或传感器关联的其他分析物的局部电导率变化、局部阻抗变化、局部电容变化、局部电荷浓度(或其变化)。这样的测量可通过直接检测以下各项(或检测指示出以下各项的信号)而作出:局部ph变化、局部阻抗变化、局部热检测、局部电容变化、局部电荷浓度(或其变化)和局部电导率变化,诸如载体、与该载体和/或传感器关联的核酸(或其他分析物)的局部电导率变化。在一些情况下,检测发生在(i)载体、(ii)与载体或传感器关联的核酸,和/或(iii)传感器的德拜长度(debyelength)(例如,德拜层)内。德拜长度可以是围绕载体、与载体或传感器关联的核酸,和/或传感器的电荷或导电性边界层(例如,德拜层)的厚度的特征。例如,检测发生在载体的德拜层内。作为另一示例,检测发生在传感器(例如,传感器的一个或多个电极)的德拜层内。作为另一示例,检测发生在跨越传感器和载体的德拜层内。这样的传感器配置例如在pct专利申请号pct/us2011/054769、pct专利申请号pct/us2012/039880、pct专利申请号pct/us2012/067645、pct专利申请号pct/us2014/027544和pct专利申请号pct/us2014/069624中有述,上述每个文献均通过引用而全文并入于此。
在测序完成之后,可以将载体/核酸从阵列分离,任选地将载体和阵列与结合的物质分离并对其进行洗涤,并且随后重新使用载体和阵列中的任一个或全部两者以进行另一轮扩增和/或测序。载体从阵列的分离可例如通过移除/逆转用于将载体保持就位的磁场和/或电场而完成。除此之外或作为替代,还可以使用能够施加足够克服用于将载体保持就位的磁力和/或静电力的力的流体流动和/或其他类型的场(例如,外部磁场、外部电场)来从阵列分离载体。当核酸直接关联于阵列(不存在载体)时,可以用适当的试剂或能量(例如,酶试剂、化学试剂、热能等)处理阵列,以从该阵列移除结合的核酸。然而在一些情况下,可能期望在扩增和/或测序之前从阵列移除载体或核酸。这样的移除可按与本文所述相似的方式实现。
在一些实施方案中,组合式扩增和测序系统可以包含磁性阵列,该磁性阵列可在多个阵列位置处通过磁力捕获磁珠或颗粒。在一些情况下,磁珠可以是顺磁珠。每个阵列位置还可以包含能够产生电场和/或发挥传感器功能的电极。每个磁珠或颗粒可以包含可例如借助由每个阵列位置处的一个或多个电极生成的电场而克隆扩增的核酸(例如,dna)片段。
在一些实施方案中,组合式扩增和测序系统可以包含电极阵列,该电极阵列可在多个阵列位置处通过静电力捕获磁珠或颗粒。在一些情况下,磁珠可以是顺磁珠。每个阵列位置处的一个或多个相同或不同的电极还可以能够产生电场和或发挥传感器的作用。每个磁珠或颗粒可以包含可例如借助由每个阵列位置处的一个或多个电极生成的电场而克隆扩增的核酸(例如,dna)片段。
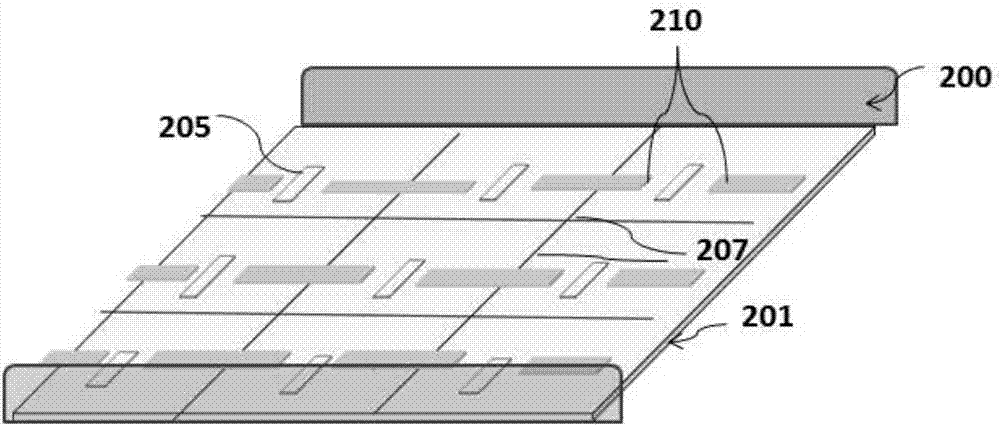
在图2中描绘了组合式扩增和测序系统的示例以及示例系统的使用。如图2a中所示,系统200可以包括位于衬底201上的阵列,该阵列可以包含传感器(例如,纳米传感器)205,该传感器有时与平台内限定的微流体通道连通。传感器205可关联于衬底201,而衬底201还可关联于磁性元件210以及电极元件205和207。磁珠可以由磁性元件210或者电极元件205和207定位于传感器205上。磁性元件可以形成局部磁场并且电极元件可以形成局部电场,以便在阵列的每个传感器205处定位载体。此外,磁场和/或电场可以在阵列的每个位置处创建针对载体的约束区。
如图2b中所示,可以将包含dna240(例如,dna片段)的样品输送到系统200中。应理解,dna240作为示例示出并且可以是任何合适的核酸类型,包括本文其他各处描述的核酸类型。在一些情况下,dna240的引入可以经由与阵列相关联的微流体通道进行。如图所示,阵列可配置有预局域化的磁珠220,并且磁珠可以关联于能够与dna240杂交的引物,使得dna240被珠子220捕获并变得与之相关联。磁珠220可以经由磁性元件210和/或电极元件205和207而定位于阵列上。替代地或除此之外,引物可以附接于、结合于或关联于阵列的位置处的传感器,并用于在该传感器处捕获dna240。
如图2c中所示,可以同时地、预先地或随后地向阵列中引入试剂260(例如,聚合酶、脱氧核苷酸(dtnp)和额外的引物)。在一些情况下,试剂260的引入可以经由穿过与阵列相关联的微流体通道的流进行,使得试剂260通过流动而与磁珠220接触。经由来自适当的阵列元件的磁力和/或静电力,可以在试剂260通过流动而与磁珠220相接触时将磁珠220保持在所需的位置。
如图2d中所示,可以克隆扩增与磁珠220相关联的dna240,以在磁珠220的表面上产生扩增的dna245和255。克隆扩增可以使用任何合适的方法来完成,该方法包括聚合酶链反应(pcr)、引物延伸反应、等温扩增或其他技术。
如图2e中所述,在dna240的扩增之后,可以洗涤280阵列中的磁珠220,从而移除溶液中未结合的扩增子245和试剂260。结果可以是包含与阵列位置相关联的扩增的dna255的克隆组的磁珠220。洗涤280可通过任何合适的方法来完成,举例而言,诸如在足以移除溶液中未结合的扩增子245和试剂260但不足以使磁珠220从其在阵列上的相应位置脱离的流速下用缓冲溶液洗涤。
如图2f中所示,继而可以使另一等份的试剂260(例如,聚合酶、引物等)和单独核苷酸185的顺序循环与传感器阵列相接触(例如,通过流动),从而使核苷酸掺入磁珠220的扩增的dna255中。核苷酸能够以单独的循环引入(例如,循环1=a、循环2=t等),其中在每个循环之间可存在使用缓冲液的洗涤步骤以帮助减少来自未掺入的核苷酸的污染的机会。用于测序反应的聚合酶可以是与用于扩增反应的聚合酶相同类型的聚合酶,或者可以是不同种类的聚合酶,并且可以在引入核苷酸之前或与其一起引入。对每个循环期间掺入的核苷酸的检测可以用于对扩增的dna255进行测序,并且因此用于对原始样品dna240进行测序。检测可例如经由电极205和207中之一或全部两者而发生。在一些情况下,电极205和207可通过测量磁珠220和/或与磁珠220相关联的扩增的dna(或其他核酸)255的局部阻抗变化来检测核苷酸掺入事件。例如,这样的测量可通过直接测量局部阻抗变化或测量指示出局部阻抗变化的信号而进行。在一些情况下,阻抗的检测发生在磁珠220和/或与磁珠220相关联的扩增的dna255的德拜长度(例如,德拜层)内。还可以通过直接测量局部电荷变化或局部电导率变化或指示如本文其他各处所述的那些变化中的一种或多种的信号来测量核苷酸掺入事件。电荷变化或电导率变化的检测可以在磁珠220和/或与磁珠220相关联的扩增的dna255的德拜长度(例如,德拜层)内发生。
组合式扩增和测序系统的其他示例可例如在以下文献中找到:pct专利申请号pct/us2011/054769、pct专利申请号pct/us2012/039880、pct专利申请号pct/us2012/067645、pct专利申请号pct/us2014/027544和pct专利申请号pct/us2014/069624,上述文献均通过引用而全文并入于此。
在一些实施方案中,在样品核酸扩增到载体上之后但在测序之前,可以在富集系统(例如,电泳分选器,其中分选经由施加于载体的电泳力而实现)中对经受扩增条件的载体进行分选。电泳分选器可以是用于进行扩增和测序的系统的一部分,或者其可以是不同系统的一部分。在电泳分选器中,可以将空载体(例如,无扩增子的载体)以及经受不完全扩增的载体或包含过短扩增子的载体从包含所需扩增子的载体分选出来。富集系统和电泳分选器的其他示例在以下文献中有述:pct专利申请号pct/us2011/054769、pct专利申请号pct/us2012/039880、pct专利申请号pct/us2012/067645、pct专利申请号pct/us2014/027544和pct专利申请号pct/us2014/069624,上述文献均通过引用而全文并入于此。
电泳分选器可包含能够接受经分选的载体的通道。带有适量扩增产物并带有足够长的扩增子的载体可以具有充足的电荷以被拉出至出口通道。当电泳分选器是单独的系统时,可以从出口通道收集此类载体并将其提供回扩增/测序系统中用于测序,其中引入试剂和检测核苷酸掺入事件的步骤可如上所述发生。
没有适量扩增产物和/或没有足够长的扩增子的载体(例如,珠子)可以流过电泳分选器并且相反地被导向至废物通道内。可以从废物通道收集载体并在适当清洗以移除任何不期望的物质后将其重新用于另一扩增循环或其他用途。例如,可以用漂白剂如过氧化氢来洗涤载体,以帮助确保在载体上没有残留的污染物,以便其可以重新使用。
本文所述的阵列和方法可以用于多种应用,并且除了核酸之外还可用于不同生物或生化部分的检测,诸如抗体-抗原检测、蛋白质检测、细胞分析、药物发现或筛选、配体、小分子或其他类型的分析。此外,本文所述的装置和方法并不限于dna应用,而是可以用于针对rna、蛋白质检测、小分子等或者其他生物分子的感兴趣的反应和分析。
除了测序反应和/或核苷酸掺入事件之外,阵列和关联的传感器还可以用于使用本文所述的任何方法和装置来感测其他生物分子(例如,寡核苷酸、蛋白质、小分子、肽等)和/或感兴趣的反应,包括直接测量局部阻抗变化、局部电荷变化或局部电导率变化或测量指示出局部阻抗变化、局部电荷变化或局部电导率变化的信号。
在一些实施方案中,传感器可以检测核酸杂交反应。例如,可以将载体(例如,珠子)连接至核酸,并且可以检测该核酸与另一核酸(例如,引物或寡核苷酸探针)的杂交。在一些实施方案中,传感器可以检测蛋白质-蛋白质相互作用。例如,可以将载体(例如,珠子)耦合至能够与附加蛋白质(例如,配体)结合的蛋白质物质(例如,抗体、抗体片段、肽等)。可以检测其他蛋白质与耦合至载体的蛋白质物质的结合。还可以检测小分子与连接至载体的物质的结合。在一些情况下,可以采用多种检测方法来检测感兴趣的生物分子或生物反应。另外的检测方法的非限制性示例包括酶联免疫吸附测定(elisa)、标签(例如,光学染料、荧光染料)的检测、在感兴趣的生物反应期间释放或生成的物质的检测等。
本文所述的传感器(例如,单独的传感器)可以是可独立寻址的。本文所使用的可独立寻址的传感器可以指阵列中的这样的单独传感器:其可独立于阵列中其他传感器的响应而检测其响应。可独立寻址的传感器还可以指阵列中的这样的单独传感器:其可独立于阵列中的其他传感器而得到控制。
在一些实施方案中,所述核酸不在载体(例如珠子)上。该核酸可以直接固定到表面如芯片和/或传感器表面上。例如,为了在芯片上集成检测,多种类型的生物分子可在芯片上图案化。本文描述的方法可用于将核酸(例如,dna)直接共价地固定至微通道表面上,这是一种可用于例如酶联dna杂交测定的配置。在一些实施方案中,dna或其他核酸可以直接附接到pdms(聚二甲基硅氧烷)微流体通道上,并且这些pdms固定的捕获探针的使用可以用于蛋白质的进一步固定。这样的方法可与其他用于控制pdms表面性质的方法和利用表面修饰固定dna、rna和蛋白质的应用一起使用,诸如在d.liu,r.k.perdue,l.sun,r.m.crooks,langmuir20,5905中描述的那些应用,其通过引用全文并入本文。
在一些实施方案中,核酸(例如,dna)向pdms表面上的固定可涉及多个步骤,其可包括:pdms表面的等离子体诱导的氧化,用带有远端巯基的硅烷偶联剂(巯基丙基硅烷,mps)对经氧化的表面的官能化,和随后巯基与丙烯酰胺修饰的dna的反应。硅烷化步骤可使用汽相反应方法进行。等离子体处理的pdms可以在mps蒸气之前暴露于酸(例如,hcl)蒸气,因为酸可以作为提高mps在pdms表面上的固定速率的催化剂。随后pdms连接的dna暴露于其生物素化的互补体可为蛋白质(例如,碱性磷酸酶(ap))的固定提供平台。物质的pdms固定可以兼容多种物质,包括那些本文描述的物质。在一些情况下,pdms固定可以提供用于任何合适的寡核苷酸或链霉亲和素修饰的蛋白质向pdms表面上的固定。
用于生物检测的装置
本文所述的方法和系统可在装置中实施。该装置可实施方法的任一种或多种操作,包括但不限于核酸提取、片段化、文库制备、固定化(例如,在载体上)、扩增、约束、珠子富集、测序或数据分析和通信。
图3示出了生物检测装置301,具有传感器阵列的可移除芯片302,和试剂储器303,该试剂储器303可插入至该生物检测装置301中并可从生物检测装置301中取出。在一些示例中,试剂储器303包含引物、核苷酸和聚合酶,以供核酸测序。
生物检测装置301可包含屏幕304,该屏幕304可包含用户界面,如图形用户界面。屏幕304可使得用户能够操作装置301,如进行核酸测序。
生物检测装置301可包含配置用于接受可移除芯片302的端口305。在一些示例中,当可移除芯片302插入至装置301中时,可使用芯片302的传感器阵列和试剂储器303中的试剂来进行核酸测序。
本公开内容的一个方面提供了一种感测装置,其包含在外壳中具有多个传感器的感测阵列,其中所述多个传感器的至少一个亚组是可单独寻址的,其中所述多个传感器中的每一个均适于直接测量与溶液中的生物物质相关联的电子指征(signature),其中所述外壳具有小于或等于约250,000mm2的占地面积(footprint),并且其中所述装置具有小于或等于约200磅、175磅、150磅、125磅、100磅、75磅、50磅、25磅、10磅或更低的重量。在一些实施方案中,所述感测装置不包含孔。作为替代,所述感测装置可包含孔。所述感测阵列可以是可从外壳中取出的。
在一个实施方案中,所述装置可以进一步包含与感测阵列流体连通的流体流动路径。该流体流动路径可与包含用于核酸测序的一种或多种试剂的贮库(repository)连通。在一些情况下,该流体流动路径可在乳液中或在没有乳液的情况下向感测阵列提供珠子。
在一些情况下,所述多个传感器中的至少一些、全部或基本全部可以是可单独寻址的。例如,所述阵列的每个传感器均可与该阵列中的其他传感器分开地寻址(例如,读取)。每个传感器可具有用于测量电子指征的一个或多个电极。可用于与本公开内容的传感器一起使用的电极和电极配置的示例在pct专利申请号pct/us2011/054769、pct专利申请号pct/us2012/039880、pct专利申请号pct/us2012/067645、pct专利申请号pct/us2014/027544和pct专利申请号pct/us2014/069624中提供,所述申请中的每一个均通过引用全文并入于此用于所有目的。
在一些实施方案中,所述生物物质可为分子物质,如生物分子,其非限制性示例包括多核苷酸、多肽、蛋白质、碳水化合物和脂肪酸。在一些示例中,该生物物质为核酸,包括本文其他各处所述的任何类型的核酸。在一些实施方案中,该核酸可以是单链或双链的。在一些示例中,该核酸是环状的。
在一些实施方案中,所述感测阵列可提供至少约50%、60%、70%、80%、90%、95%、96%、97%、98%、99%或99.9%的单通珠子装载填充因数。该填充因数为具有珠子的阵列的百分比。在一些实施方案中,所述感测阵列可提供至少约20个碱基对(bp)、25bp、30bp、31bp、32bp、33bp、34bp、35bp、40bp、50bp、100bp、500bp、1000bp、5000bp、10,000bp或100,000bp的非线性度小于或等于约10个碱基、5个碱基、4个碱基、3个碱基、2个碱基、1个碱基或0.5个碱基的核酸测序读取长度。该读取长度可以是核酸均聚物(例如,全部的a、c、t或g)的读取长度。
所述感测阵列可以是可从外壳中取出的芯片的部分。该芯片可为一次性使用芯片或多次使用芯片。该芯片可以是一次性的(例如,由环境友好的材料形成)和/或可重复使用。所述感测阵列可以基本是平面的。
所述感测阵列可在少于或等于约2天、1天、12小时、6小时、3小时、2小时、1小时、45分钟、30分钟、15分钟、10分钟或5分钟的时间段内提供至少约100个碱基对(bp)、500bp、1000bp、20,000bp或100,000bp的核酸测序通量。在一些情况下,感测阵列可用于进行靶向测序和/或全基因组测序。
在一些情况下,所述装置进一步包含耦接至感测阵列的计算机处理器(或其他电子逻辑)。该计算机处理器可被编程用于从感测阵列接收信号,该信号指示物质的直接电子指征。
在一些情况下,所述感测阵列适于进行核酸测序、质子检测、蛋白质检测或病原体检测。所述感测阵列可适于进行核酸扩增和/或流体富集。
所述装置可以是是便携式的,使得其可以容易地由用户或机器运输。例如,该机器可以是可在载具上运输的。在一些示例中,该载具为汽车、摩托车、踏板车、直升机、飞机、卡车、军用载具、航天器或机器人。
所测量的电子指征可为与以下各项相关联的阻抗或阻抗变化:(i)邻近于传感器的珠子,(ii)传感器的电极,或(iii)邻近于传感器的流体中的物质。作为替代或除此之外,该电子指征可为与以下各项相关联的电荷或电荷变化:(i)邻近于传感器的珠子或其他类型的颗粒,(ii)传感器的电极,或(iii)邻近于传感器的流体中的物质。作为替代或除此之外,该电子指征可为与以下各项相关联的电导率或电导率变化:(i)邻近于传感器的珠子或其他类型的颗粒,(ii)传感器的电极,或(iii)邻近于传感器的流体中的物质。关于测量电子指征的许多细节可以如pct专利申请号pct/us2011/054769、pct专利申请号pct/us2012/039880、pct专利申请号pct/us2012/067645、pct专利申请号pct/us2014/027544和pct专利申请号pct/us2014/069624中所述,所述申请中的每一个均通过引用全文并入于此用于所有目的。
在一些情况下,所述装置为用于生物检测的系统的部分。该系统可包含多个装置中的单个装置。每个装置均可进行相同的生物检测或不同的生物检测。所述装置可通过包括例如无线连接在内的任何适当类型的连接来彼此通信。
本公开内容的另一方面提供了用于生物检测的方法,其包括提供感测装置,该感测装置包含在外壳中具有多个传感器的感测阵列,其中所述多个传感器的至少一个亚组是可单独寻址的,其中所述多个传感器中的每一个均适于直接测量与溶液中的生物物质相关联的电子指征,其中所述外壳具有小于或等于约250,000mm2、200,000mm2、150,000mm2、100,000mm2、50,000mm2、10,000mm2、5,000mm2或1,000mm2的占地面积,并且其中所述装置具有小于或等于约200磅、175磅、150磅、125磅、100磅、75磅、50磅、25磅或10磅的重量。接下来,可将包含生物物质的溶液引导至感测阵列。可使用流体流动系统来引导该溶液,该流体流动系统包含例如一个或多个泵和/或流动致动器。在一些实施方案中,如本文其他各处所述,可使用传感器来直接测量与生物物质相关联的电子指征。该感测装置可以如上文或本文其他各处所述。
在一些情况下,所述感测装置可提供在载具上。该载具可为汽车、摩托车、踏板车、直升机、飞机、卡车、军用载具、航天器或机器人。该载具可从第一位置移动至可不同于第一位置的第二位置。在一些情况下,当载具从第一位置移动至第二位置时,(i)将溶液引导至感测阵列并且(ii)使用传感器直接测量与生物物质相关联的电子指征。
所述装置可以可由用户运输。在一些情况下,当用户从第一位置移动至第二位置时,(i)将溶液引导至感测阵列并且(ii)使用传感器直接测量与生物物质相关联的电子指征。
控制系统
本公开内容提供了被编程用于实现本公开内容的方法的计算机控制系统。图4示出了计算机系统401,其被编程或以其他方式配置用于生物检测。计算机系统401可调节本公开内容的感测装置、系统和方法(例如,用于生物检测的方法)的各个方面。在一些实施方案中,如本文其他各处所述,计算机系统401可从传感器接收信号并确定局部阻抗、局部电荷和/或局部电导率的变化。
例如,图4为核酸测序反应期间信号(mv,y轴)相对于所添加的核酸碱基(x轴)的变化的示例图。数据显示出约33个碱基对的均聚物读取长度。
计算机系统401可为用于生物检测的装置或系统的部分,或者是与该装置或系统分开的。在一些示例中,系统401与用于生物检测的装置或系统如核酸测序装置集成。例如,系统401可被包含在还含有感测阵列的外壳中,该感测阵列可经由可移除的芯片提供。
计算机系统401包括中央处理器(cpu,本文也称为“处理器”和“计算机处理器”)405,该中央处理器405可以是单核或多核处理器,或者是用于并行处理的多个处理器。计算机系统401还包括存储器或存储器位置410(例如,随机存取存储器、只读存储器、闪速存储器)、电子存储单元415(例如,硬盘)、用于与一个或多个其他系统通信的通信接口420(例如,网络适配器)以及外围设备425,诸如高速缓存、其他存储器、数据存储和/或电子显示适配器。存储器410、存储单元415、接口420和外围设备425通过诸如主板等通信总线(实线)而与cpu405通信。存储单元415可以是用于储存数据的数据存储单元(或数据存储库)。计算机系统401可以借助于通信接口420而可操作地耦接到计算机网络(“网络”)430。网络430可以是因特网、互联网和/或外联网,或者是与因特网通信的内联网和/或外联网。在一些情况下,网络430是电信和/或数据网络。网络430可以包括一个或多个计算机服务器,这可以支持分布式计算,诸如云计算。在一些情况下,网络430可借助于计算机系统401实现点对点网络,这可以使得耦接到计算机系统401的设备能够起到客户端或服务器的作用。
cpu405可以执行一系列机器可读指令,这可以体现于程序或软件中。所述指令可储存在存储器位置,诸如存储器410中。由cpu405执行的操作的示例可以包括读取、解码、执行和回写。
存储单元415可以储存文件,诸如驱动程序、文库和保存的程序。存储单元415可以储存用户数据,例如,用户偏好和用户程序。在一些情况下,计算机系统401可以包括一个或多个附加的数据存储单元,所述附加数据存储单元位于计算机系统401的外部,诸如位于通过内联网或因特网而与计算机系统401通信的远程服务器上。
计算机系统401可以通过网络430而与一个或多个远程计算机系统通信。例如,计算机系统401可以与用户(例如,操作者)的远程计算机系统通信。远程计算机系统的示例包括个人计算机(例如,便携式pc)、平板或板状计算机(例如,
本文所述的方法可通过储存在计算机系统401的电子位置上(例如,存储器410或电子存储单元415上)的机器(例如,计算机处理器)可执行代码的方式来实现。该机器可执行或机器可读代码能够以软件的形式提供。在使用过程中,该代码可由处理器405执行。在一些情况下,该代码可以从存储单元415检索并储存在存储器410中用于由处理器405随时访问。在一些情况下,可以排除电子存储单元415,并且机器可执行指令储存在存储器410上。
所述代码可被预编译并配置用于与具有适于执行该代码的处理器的机器一起使用,或者可以在运行时编译。该代码能够以编程语言来提供,该编程语言可被选择用以使该代码能够以预编译或即时编译的方式执行。
本文提供的系统和方法的各方面,诸如计算机系统401,可以体现在编程中。所述技术的各个方面可以被认为是通常被携载或体现于某种类型的机器可读介质中的机器(或处理器)可执行代码和/或相关数据的形式的“产品”或“制品”。机器可执行代码可以储存在电子存储单元上,诸如存储器(例如,只读存储器、随机存取存储器、闪速存储器)或硬盘上。“存储”型介质可以包括计算机的任何或所有的有形存储器、处理器等,或者其关联的模块,诸如各种半导体存储器、磁带驱动器、磁盘驱动器等,其可以随时为软件编程提供非暂时性存储。全部的软件或其部分可以不时通过因特网或各种其他电信网络进行通信。这样的通信例如可以支持软件从一个计算机或处理器向另一计算机或处理器的加载,例如,从管理服务器或主机加载到应用服务器的计算机平台。因此,可承载软件元素的另一类型的介质包括光波、电波和电磁波,诸如跨本地设备之间的物理接口、通过有线和光陆线网络以及在各种空中链路上使用的光波、电波和电磁波。携带这些波的物理元件,诸如有线或无线链路、光链路等,也可以被认为是承载软件的介质。如本文所用,除非限于非暂时性的,否则诸如术语计算机或机器“可读介质”等有形“存储”介质是指参与向处理器提供用以执行的指令的任何介质。
因此,机器可读介质,诸如计算机可执行代码等,可以采取许多形式,包括但不限于有形存储介质、载波介质或物理传输介质。非易失性存储介质例如包括光盘或磁盘,诸如在任何一个或多个计算机中的任何存储设备等,诸如可用于实现附图中所示数据库的存储设备等。易失性存储介质包括动态存储器,诸如这样的计算机平台的主存储器。有形传输介质包括同轴线缆;铜线和光纤,其包括构成计算机系统内的总线的导线。载波传输介质可采取电信号或电磁信号或者声波或光波的形式,诸如在射频(rf)和红外(ir)数据通信期间生成的波。因此,计算机可读介质的常见形式例如包括:软盘、柔性盘、硬盘、磁带、任何其他磁介质、cd-rom、dvd或dvd-rom、任何其他光学介质、穿孔卡片纸带、具有孔洞图案的任何其他物理存储介质、ram、rom、prom和eprom、flash-eprom、任何其他存储器芯片或匣、传送数据或指令的载波、传送这样的载波的线缆或链路,或者计算机可以从中读取编程代码和/或数据的任何其他介质。这些形式的计算机可读介质中的许多介质可参与向处理器传送一个或多个系列的一个或多个指令以供执行。
计算机系统401可包括电子显示器435或与其通信,该电子显示器435包括用于提供例如耦接至该计算机系统401的系统的感测装置的输出或读出的用户界面(ui)。这样的读出可包括核酸测序读出,如构成给定核酸样品的核酸碱基的序列。ui的示例包括但不限于图形用户界面(gui)和基于网络的用户界面。电子显示器435可为计算机显示屏,或电容式或电阻式触摸屏。
本公开内容的装置、方法和系统可与其他装置、系统和/或方法组合,或被它们改进,例如,pct专利申请号pct/us2011/054769、pct专利申请号pct/us2012/039880、pct专利申请号pct/us2012/067645、pct专利申请号pct/us2014/027544和美国专利申请序列号13/481,858描述的那些,所述申请中的每一个均通过引用全文并入于此用于所有目的。这些申请提供了用于直接测量与溶液中的生物物质相关联的电子指征(如阻抗或电荷测量)以及用于进行生物测量以供用于例如核酸测序(包括靶向测序和全基因组测序)的示例装置和方法。
本公开内容的装置、系统和方法可用于多种类型的测量,如病原体检测、蛋白质检测和核酸测序,包括测量核酸序列和单核苷酸多态性(snp)检测。这样的方法可由受试者使用,由健康护理提供者使用以诊断和/或治疗受试者,或用于法医分析。
珠子、其合成及用途
通过将生物分子如dna和蛋白质直接被动或共价地附接于衬底的平坦表面上而制备的微阵列的用途可能受限,因为所附接的生物分子例如寡核苷酸的有效表面密度较低。此外,所附接的生物分子通常未被有效利用,特别是在酶促反应中,其中相对较大的靠近的酶分子可能将下方的生物分子与外部环境屏蔽。如本文所述,针对该缺点的一种解决方法是将所附接的生物分子栓系得远离表面。
包含(1)亲水性重复单元、(2)热化学反应性重复单元和(3)光化学反应性重复单元的三元共聚物可用作连接体,以将生物分子缀合至平坦表面上。在uv辐射下,一部分激发的光化学活性重复单元从衬底的脂族表面抽取氢,从而导致偶联反应以共价结合该三元共聚物。热化学反应性重复单元可为能够与含有氨基或羟基基团的任何生物分子分别形成酰胺键或酯键的反应性酯。为了与水相反应相匹配,亲水性重复单元通常超过约40摩尔%,并且光化学反应性重复单元通常少于约4摩尔%。该体系的一个劣势在于,热化学反应性重复单元为水解不稳定的n-羟基琥珀酰亚胺的反应性酯。
包含(1)亲水性重复单元和(2)反应性重复单元(例如,热化学反应性重复单元)的共聚物可用作连接体,以将生物分子缀合到表面(例如,平坦表面)上。在一些情况下,反应性重复单元为水解稳定的氟化苯酚的反应性酯。该反应性酯的一部分可与将聚合物共价附接于衬底上的衬底的表面氨基基团或羟基基团反应。剩余的反应性酯基团可结合任何其他的含有氨基或羟基的生物分子。在一些情况下,亲水性重复单元超过约40mol%。
可使用类似的共聚物将复合糖缀合至含有表面氨基基团的磁珠上。所附接的复合糖充当被动结合至病原体细胞上的捕获探针。在一些情况下,本公开内容采用所附接的生物分子(例如,核酸,如单链dna)的间隔来优化磁珠表面上扩增和测序的效率。
在一些实施方案中,使用五氟苯基丙烯酸酯的均聚物和共聚物作为连接体将ssdna缀合至磁珠上。yu.p.gorelov在1979年(“thermaldecompositionofpoly(phenylacrylate)andpoly(pentafluorophenylacrylates),”yu.p.gorelov等人,vysokomolekulyarnyesoedineniya,seriyab:kratkiesoobshcheniya,第21卷,第6期,第410-13页,期刊,1979)首先报道了聚(五氟苯基丙烯酸酯)的热稳定性,该文献通过引用全文并入于此。tsutsumi等人在1986年(halogen-containingpolyacrylatederivative,”tsutsumi等人,ep0230656a,1986)报道了五氟苯基甲基丙烯酸酯的共聚物,该文献通过引用全文并入于此。
图6示出了示例磁珠“mb”,其具有可用于核酸测序的引物缀合的表面。引物缀合的珠子可与模板(例如,来自核酸样品的分析物)退火,并且该模板可被扩增(例如,经由在聚合酶存在下的引物延伸反应),以在珠子表面上产生多个扩增的模板。然后,可通过将测序引物退火至扩增的模板上并在聚合酶和dntp的存在下进行引物延伸反应而对扩增的模板进行测序(图6)。可采用如本文其他各处所述的传感器/传感器阵列和感测方法来测量或检测引物延伸反应期间核苷酸向扩增的模板中的掺入。
本文描述了用于制备引物缀合的珠子(例如,磁珠)的方法,及其在核酸测序中的用途。该方法可包括(a)对带有羧基的珠子(例如,磁珠)进行胺化,(b)将包含多个反应性基团的预先制备的聚合物(例如,共聚物)接枝(例如,共价接枝)至胺化的珠子,以及(c)经一个或多个剩余的反应性基团,将氨基封端或羟基封端的引物共价附接至预先制备的聚合物。然后,所生成的引物偶联的珠子可参与核酸扩增反应,由此模板核酸与引物杂交,并且继续进行扩增,以生成如本文其他各处所述的核酸的克隆群。然后,该克隆核酸群可通过在如本文其他各处所述的合成测序反应中充当模板而被测序。
在一些实施方案中,预先制备的聚合物可包含具有亲水性官能团的重复单元,该亲水性官能团不同于反应性基团。在一些实施方案中,预先制备的聚合物可包含大于或等于约40mol%、大于或等于约45mol%、大于或等于约50mol%、大于或等于约55mol%、大于或等于约60mol%、大于或等于约65mol%、大于或等于约70mol%、大于或等于约75mol%、大于或等于约80mol%、大于或等于约85mol%、大于或等于约90mol%,或大于或等于约95mol%的亲水性官能团。
图5示出了制备引物缀合的磁珠的示例。如图5所示,磁珠“mb”包含羧酸基团。如本文其他各处所述,该羧酸基团可转化成氨基基团(例如,图7所示的方案)。具有表面氨基基团的磁珠是可商购的。然而,具有表面氨基基团的磁珠的保存期可能相对较短。例如,表面氨基基团可能易于氧化,这可能产生不期望的特性,从而导致功能化的不可重复性。
然后,具有游离氨基或羟基基团的引物(例如,具有末端氨基或羟基基团的引物)可与偶联至珠子的接枝聚合物上的其他反应性重复单元反应(经由游离氨基基团或游离羟基基团),使得引物偶联至该接枝聚合物。可以理解,图5所示的示例方法和本文所述的其他方法均可用于将具有游离氨基或羟基基团的引物或任何其他类型的核酸偶联至最初具有羧酸基团的表面(包括非磁性珠子)。在一些实施方案中,反应性重复单元可包含一个或多个反应性官能团。
如图7所示,在一些情况下,珠子(例如,磁珠,图7中的“mb”)上的表面羧酸基团可被n,n-二琥珀酰亚胺基碳酸酯活化,以形成反应性酯。在一些情况下,如图7所示,可利用双(4-硝基苯基)碳酸酯、双(三氟苯基)碳酸酯、双(四氟苯基)碳酸酯和/或双(五氟苯基)碳酸酯将珠子(例如,磁珠)的羧酸基团活化,形成水解稳定的反应性酯基团。此外,反应性酯基团可经由与过量的含有连接体“a”的二胺进行反应而经历胺化(如图7所示)。例如,连接体“a”可为线性脂族连接体或亲水性聚(环氧乙烷)连接体。连接体物质的非限制性示例在图7中示出。具有连接体的优势可包括(a)使末端氨基基团延伸得进一步远离珠子表面,以便可被如下文所述待接枝的、靠近的、预先制备的活性聚合物接近,以及(b)在亲水性聚(环氧乙烷)连接体的情况下,减少或消除其他疏水性实体的非特异性吸附。
可将具有聚合物骨架和反应性重复单元的反应性接枝聚合物经由氨基基团偶联至珠子(例如,磁珠),由此将接枝聚合物偶联至珠子表面。在一些情况下,接枝聚合物经由酰胺键共价偶联至珠子表面。在一些情况下,可通过在引发剂(例如,热引发剂,例如,2,2'-偶氮二(2,4-二甲基戊腈)、偶氮二异丁腈(aibn)或二苯甲酮)的存在下将水溶性共聚单体与包含反应性酯的另一共聚单体共聚,以生成反应性接枝聚合物来制备预先制备的接枝聚合物(例如,参见如下所述的图8a、9a和9c的示例)。可通过将珠子的表面氨基基团(例如,如采用本文其他各处所述的方法生成的)和反应性接枝聚合物在接枝反应中偶联来进行反应性接枝聚合物向珠子的接枝以及随后向偶联的反应性接枝聚合物的引物缀合。在接枝反应期间,反应性接枝聚合物的一部分反应性酯基团可与珠子的表面氨基基团反应,以形成接枝聚合物与珠子表面的多点共价附接(例如,参见图8b和9b的示例)。聚合物链的物理缠结可形成包裹珠子的三维(3d)支架。可通过将剩余的反应性酯基团与氨基封端或羟基封端的引物反应以分别在接枝聚合物与引物之间形成酰胺键或酯键而实现引物缀合。在一些情况下,在引物偶联后剩余的残留反应性酯基团可转化(如图8b所示的“加帽”)成亲水性酰胺部分,例如,在三乙胺(tea,et3n)的存在下利用氢氧化铵进行。
在一些情况下,可控制反应性接枝聚合物的组成、其分子量和/或该反应性接枝化合物的一种重复亚单元与另一种重复亚单元的比例。对反应性接枝聚合物组成、其分子量和/或其重复亚单元比例的控制可控制聚合物偶联至珠子(例如,磁珠)表面时的厚度,可控制反应性酯基团沿聚合物骨架的间隔。这样的控制可随后用于控制所缀合的引物的间隔和量。富裕的引物间隔可改善引物对在核酸扩增和/或后续测序反应中使用的酶(例如,聚合酶)的可及性。改善的可及性可同时改善核酸扩增反应和核酸测序反应。
在一些情况下,包括图8a、8b、9a、9b和9c的示例中所示的那些在内,反应性接枝聚合物的分子量可在10千道尔顿(kda)至3000kda、50kda至2500kda、100kda至1,500kda,或500kda至1,000kda的范围内。在一些实施方案中,接枝聚合物的分子量可为约10kda、25kda、50kda、100kda、150kda、200kda、250kda、300kda、350kda、400kda、450kda、500kda、550kda、600kda、650kda、700kda、750kda、800kda、850kda、900kda、950kda、1000kda、1050kda、1100kda、1150kda、1200kda、1250kda、1300kda、1350kda、1400kda、1450kda、1500kda、1550kda、1600kda、1650kda、1700kda、1750kda、1800kda、1850kda、1900kda、1950kda、2000kda、2050kda、2100kda、2150kda、2200kda、2250kda、2300kda、2350kda、2400kda、2450kda、2500kda、2550kda、2600kda、2650kda、2700kda、2750kda、2800kda、2850kda、2900kda、2950kda或3000kda。
反应性接枝聚合物可包含沿着其聚合物链随机分布的多个反应性酯基团,其能够形成包裹具有表面氨基基团的珠子(例如,磁珠)的三维物理缠结的聚合物支架。该聚合物支架可适应相对较高的引物加载。本文所述的方法允许通过控制反应性接枝共聚物的组成来定制引物加载,该组成包括反应性酯重复单元少于约60mol%、少于约50mol%、少于约40mol%、少于约30mol%、少于约20mol%或少于约10mol%。还可通过调节待接枝至珠子上的反应性接枝共聚物的量和/或在缀合反应中使用的引物的量来控制引物加载。
在一个示例中,如图8a所示,具有反应性“r”基团(例如,n-琥珀酰亚胺基、4-硝基苯基、氟苯基、二氟苯基、三氟苯基、四氟苯基或五氟苯基)的反应性酯可在引发剂(例如,热引发剂,例如,2,2'-偶氮二(2,4-二甲基戊腈))的存在下与包含“t”基团(例如,—nh2、—nh(ch3)、—nh(ch2oh)、—nh(ch2oh)、—nh(ch2ch2oh)、—nme2、—(ch2ch2o)n—ch3)的水溶性共聚单体共聚,以生成反应性接枝聚合物。如图8a所示,(y+z)=100mol%,其中y对应于图8a所示的反应性重复亚单元的摩尔百分比,而“z”对应于图8a所示的水溶性重复亚单元的摩尔百分比。在一些情况下,y摩尔百分比可在约0.1mol%至约80mol%、0.1mol%至约60mol%、约1mol%至约60mol%,或约10mol%至约60mol%的范围内,剩余的比例为“z”。在一些情况下,y摩尔百分比可小于或等于约80mol%、75mol%、70mol%、65mol%、60mol%、55mol%、50mol%、45mol%、40mol%、35mol%、30mol%、25mol%、20mol%或更少,剩余的比例为z。在一些情况下,如图8a的示例所示,y摩尔百分比小于或等于约60%,而z摩尔百分比大于或等于约40%。
将如通过图8a所示的示例方法生成的反应性接枝聚合物接枝至珠子的示例在图8b中图示。如图8b所示,包含表面结合的氨基基团(例如,经由包含–(r1)x的连接体,其中–(r1)x可为例如—(ch2)m(m=2至10)或—(ch2ch2o)n—ch2ch2—(n=1至100))的珠子(例如,磁珠“mb”)与反应性接枝聚合物反应。该反应性接枝聚合物可包含图8b中的具有反应性五氟苯基“r”基团和–nme2“t”基团(以“r2”示出)的反应性酯。反应性接枝聚合物的一部分反应性五氟苯基基团可与珠子的氨基基团反应,使得该反应性接枝聚合物附接(例如,共价附接)至珠子。在第二步中,该反应性接枝聚合物的剩余反应性五氟苯基基团的全部或一部分可与带有氨基或带有羟基的引物反应,使得所述引物附接至该反应性接枝聚合物,并由此附接至珠子。在一些情况下,如本文其他各处所述,可在氢氧化铵和tea的存在下将反应性接枝聚合物的剩余反应性五氟苯基基团“加帽”。此外,可以理解,图8b所示的示例方法可用于将具有游离氨基或羟基基团的任何其他类型的核酸或其他物质偶联至也具有游离氨基基团和/或羟基基团的表面(包括非磁性珠子)。
在另一个示例中,如图9a所示,具有反应性“r”基团(例如,n-琥珀酰亚胺基、4-硝基苯基、氟苯基、二氟苯基、三氟苯基、四氟苯基或五氟苯基)、“r2”基团(例如,h或ch3)和“w”基团(例如,单键或具有“di”取代基(例如,h或ch3)的苯基基团)的反应性酯可在引发剂(例如,热引发剂,例如,2,2'-偶氮二(2,4-二甲基戊腈))的存在下与包含“t”基团(例如,—nh2、—n(ch3)2、—nh(ch3)、—nh(ch2)t—oh(t=1至4)、—(och2ch2)v—oh(v=1至100)、—(och2ch2)v—ch3(v=1至100)、—(och2ch2)v—och3(v=1至100)和—och3)和“r3”基团(例如,h或ch3)的水溶性共聚单体共聚,以生成反应性接枝聚合物。如图9a所示,(y+z)=100mol%,其中y对应于图9a所示的反应性重复亚单元的摩尔百分比,而“z”对应于图9a所示的水溶性重复亚单元的摩尔百分比。在一些情况下,y摩尔百分比可在约0.1mol%至约80mol%、0.1mol%至约60mol%、约1mol%至约60mol%,或约10mol%至约60mol%的范围内,剩余的比例为“z”。在一些情况下,y摩尔百分比可小于或等于约80mol%、75mol%、70mol%、65mol%、60mol%、55mol%、50mol%、45mol%、40mol%、35mol%、30mol%、25mol%、20mol%或更少,剩余的比例为z。在一些情况下,如图9a的示例所示,y摩尔百分比小于或等于约60%,而z摩尔百分比大于或等于约40%。
将如通过图9a所示的示例方法生成的反应性接枝聚合物接枝至珠子的示例在图9b中图示。如图9b所示,包含表面结合的氨基基团(例如,经由包含例如—(ch2)m(m=2至10)或—(ch2ch2o)n—ch2ch2—(n=1至100)的“a”连接体)的珠子(例如,磁珠“mb”)与反应性接枝聚合物反应。该反应性接枝聚合物可包含图9b中的具有反应性“r”基团和“t”基团的反应性酯。该反应性接枝聚合物的一部分反应性r基团可与珠子的氨基基团反应,使得该反应性接枝聚合物附接至珠子。在第二步中,该反应性接枝聚合物的剩余反应性r基团的全部或一部分可与带有氨基或带有羟基的引物反应,使得所述引物附接至该反应性接枝聚合物,并由此附接至珠子。在一些情况下,如本文其他各处所述,可在氢氧化铵和tea的存在下将该反应性接枝聚合物的剩余反应性r基团“加帽”。此外,可以理解,图9b所示的示例方法可用于将具有游离氨基或羟基基团的任何其他类型的核酸或其他物质偶联至也具有游离氨基基团和/或羟基基团的表面(包括非磁性珠子)。
在一个示例中,如图9c所示,具有反应性二氢唑酮基团(包含可独立地为例如h或ch3的“r4”和“r5”基团)和“r2”基团(例如,h或ch3)的反应性重复单元可在引发剂(例如,热引发剂,例如,偶氮二异丁腈(aibn)或二苯甲酮)的存在下与包含“t”基团(例如,—nh2、—nh(ch3)、—n(ch3)2、—nh(ch2)t—oh(t=1至4)、—(och2ch2)v—oh(v=1至100)、—(och2ch2)v—och3(v=1至100)、—(och2ch2)v—ch3(v=1至100)和–och3)和“r3”基团(例如,h或ch3)的水溶性共聚单体共聚,以生成反应性接枝聚合物。如图9c所示,(y+z)=100mol%,其中y对应于图9c所示的反应性重复亚单元的摩尔百分比,而“z”对应于图9c所示的水溶性重复亚单元的摩尔百分比。在一些情况下,y摩尔百分比可在约0.1mol%至约80mol%、0.1mol%至约60mol%、约1mol%至约60mol%,或约10mol%至约60mol%的范围内,剩余的比例为“z”。在一些情况下,y摩尔百分比可小于或等于约80mol%、75mol%、70mol%、65mol%、60mol%、55mol%、50mol%、45mol%、40mol%、35mol%、30mol%、25mol%、20mol%或更少,剩余的比例为z。在一些情况下,如图9c的示例所示,y摩尔百分比小于或等于约60%,而z摩尔百分比大于或等于约40%。
图9c所示的接枝聚合物可经由一个或多个珠子氨基基团与接枝聚合物的一部分反应性二氢唑酮基团的反应而偶联至带有氨基的颗粒。该反应性接枝聚合物的剩余反应性二氢唑酮基团的全部或一部分可与带有氨基或带有羟基的引物反应,使得所述引物附接至该反应性接枝聚合物,并由此附接至珠子。在一些情况下,如本文其他各处所述,可在氢氧化铵和tea的存在下将该反应性接枝聚合物的剩余反应性二氢唑酮基团“加帽”。此外,可以理解,图9c所示的接枝聚合物可用于将具有游离氨基或羟基基团的任何其他类型的核酸或其他物质偶联至也具有游离氨基基团和/或羟基基团的表面(包括非磁性珠子)。
图10比较了本文所述的引物加载的示例与通过经由2臂和4臂聚(环氧乙烷)胺peg-nh2(具有2,000da分子量的连接体)将相同引物缀合至从lifetechnologies(myone)和bangs(pro-mag)获得的羧基磁珠上而制备的那些。2臂和4臂peg连接体通过单价附接(单点)将其自身附接至氨基珠子,导致随后引物以接近2d的方式缀合。这种类型的缀合产生每2亿个缀合的珠子有400至3000个荧光信号的引物加载。本文所述的方法将引物缀合至3d支架上,产生高150x至350x的荧光信号。
图10还示出了在聚合物接枝的磁珠上的引物加载的示例。此外,如图10所示,利用20%活性聚合物(例如,图8a中的y=20mol%)制备的高度空间间隔的引物缀合可导致为1.96的高hp1(模板)与引物之比(图10)。相反,利用100%活性聚合物(例如,图8a中的z=100mol%)制备的高加载的引物缀合可产生为0.88或更低的低hp1与引物之比(图10)。在一些情况下,前者对测序是有利的。
图11示出了100%反应性接枝聚合物和15-聚体引物对利用先前如图7所示制备的胺化myone珠子生成的引物缀合磁珠的制备的加载影响的示例。100%活性接枝聚合物和15-聚体引物的增加伴随着珠子表面的缀合引物(tib)和hp1/tib比的增加(图11)。在超过阈值之后,100%活性接枝聚合物和引物的增加可继以hp1/tib比的降低。不希望受任何特定理论的限制,这种效果可以用如下原因来解释:引物和模板的过度拥挤使靠近的酶不能利用埋没(buried)的tib进行扩增。
图11示出了100%活性聚合物和15-聚体引物对扩增的加载影响示例。当使用20%活性接枝聚合物和15-聚体引物制备利用胺化myone珠子(先前通过采用双(五氟苯基)碳酸酯(bpfpc)和二琥珀酰亚胺基碳酸酯dcs(图7)作为活化剂制备的)生成的引物缀合磁珠时,如图12的示例所示观察到相同的趋势。由于引物沿着20%活性聚合物的聚合物链在空间上分隔,因此所缀合的引物可在扩增中被有效利用,并因此可产生有利的hp1/tib比。
图12示出了20%活性聚合物和15-聚体引物对扩增的加载影响示例。简言之,本文描述了用于提高和控制引物与共价附接于磁珠表面上的3d聚合物支架的缀合度的技术。通过将引物在空间上分隔,可在扩增后获得较高的模板(例如,hp1)与引物(例如,tib引物)之比。
经由扩增反应得到的测序模板的加载可以被测量为在扩增反应后从用于检测模板的标记物(例如,荧光染料)获得的信号与从用于检测引物的标记物(例如,荧光染料)获得的信号之比。在一些情况下,在珠子扩增后针对模板检测到的信号(例如,经由与hp1模板相关联的标记物)与针对引物检测到的信号(例如,经由与tib引物相关联的标记物)之比为至少约1.1、至少约1.2、至少约1.3、至少约1.4、至少约1.5、至少约1.6、至少约1.7、至少约1.8、至少约1.9、至少约2.0、至少约2.1、至少约2.2、至少约2.3、至少约2.4、至少约2.5、至少约2.6、至少约2.7、至少约2.8、至少约3.0、至少约4.0、至少约5.0或至少约6.0。在一些情况下,磁珠上过度加载的引物在扩增期间通常是不可接近的,从而导致针对模板检测到的信号与针对引物检测到的信号之比小于1。
聚乙二醇(peg)珠子
包覆的磁性颗粒可以是有用的分子载体,因为可通过磁场对其进行空间操控。该性质可使其能够从反应混合物中快速分离并在磁阵列上分散。包覆的磁性颗粒是可商购的,并且本文所述的用于改变涂层类型的方法可用于以有用的方式操控颗粒的性质。在一些情况下,颗粒包覆有疏水性涂层或亲水性涂层。
含有羟基、羧基和/或胺官能团的亲水性涂层可赋予亲水性,并可用作附接其他有用官能团的把手(反应性基团)。如本文所述,包含乙烯基、炔属和/或叠氮基基团的较不亲水的把手也可用于涂层。
具有胺、羟基和羧基官能性涂层的磁珠是可商购的。这些涂层可采取能以其大小和价态为特征的不同形式。在一些实施方案中,本公开内容的方法采用包覆有聚丙烯酸的珠子(例如,具有约1微米的直径)。这些珠子的示例可从lifetechnologiestm(myone羧基珠子)和bangslaboratories(pmc1hc珠子)获得。如本文所述,将引物附接至这些珠子的具体方式对核酸测序可能是重要的。
单链寡核苷酸如引物可经由氨基-peg-羧基连接体附接至珠子(例如,参见图13和14以及下文所述的示例)。在一些情况下,连接体的peg部分具有离散的长度(例如,单分子量)。这样的连接体可从quantabiodesign商购并被称为“dpegtm”或“离散peg”连接体(例如,氨基-dpeg24-羧基)。peg(包括dpeg)重复单元的数目可为任何合适的数目,包括约5个、约10个、约12个、约15个、约20个、约24个、约30个、约40个、约50个、约60个、约70个、约80个、约90个、约100个、约120个、约140个、约160个、约180个、约200个或更多。在一些情况下,peg(包括dpeg)重复单元的数目为至少约5个、至少约10个、至少约12个、至少约15个、至少约20个、至少约24个、至少约30个、至少约40个、至少约50个、至少约60个、至少约70个、至少约80个、至少约90个、至少约100个、至少约120个、至少约140个、至少约160个、至少约180个、至少约200个或更多。在一些情况下,peg(包括dpeg)重复单元的数目为至多约5个、至多约10个、至多约12个、至多约15个、至多约20个、至多约24个、至多约30个、至多约40个、至多约50个、至多约60个、至多约70个、至多约80个、至多约90个、至多约100个、至多约120个、至多约140个、至多约160个、至多约180个或至多约200个。
可通过以三丁胺作为碱,利用在无水nmp中的二琥珀酰亚胺基碳酸酯将珠子的羧酸酯转化成nhs酯而将氨基-peg-羧酸酯连接体附接于珠子。可洗涤珠子(例如,用去离子水洗涤一次)(例如,在1-10mg珠子/ml的浓度下)。在一些情况下,用无水nmp(例如,在1-10mg珠子/ml的浓度下)洗涤珠子(例如,四次)。该反应可在约5%w/vdsc和5%v/v三丁胺下于20℃下进行两小时(例如,在每ml5%dsc/nmp溶液1-10mg珠子的情况下)。然后,可用无水dmso(例如,每mldmso1-10mg珠子)洗涤珠子(例如,四次)。然后,可以以(例如,10%w/v)三丁胺作为碱,用在无水dmso中的较大摩尔过量(例如,每mg珠子1-3mg)的氨基-peg-羧酸酯(例如,作为10%w/v溶液)处理珠子(例如,在室温下持续16小时(hr))。然后,可将dpeg/dmso溶液去除,并可用(例如,1m)氢氧化钠(naoh)溶液处理珠子(例如,在20度下持续20至60分钟)。然后,可用水(例如,1-10mg珠子/ml)洗涤珠子(例如,4次),并将其储存在水中(例如,在1-10mg珠子/ml的浓度下)。
然后,可将引物缀合至氨基-peg-羧酸酯连接体。可用无水nmp洗涤具有连接体的珠子(例如,在1-10mg/ml的浓度下4次)。然后,可将它们转化成nhs酯形式(例如,通过用5%w/v的dcs在无水nmp中的溶液,5%w/v三丁胺在20℃下处理2hr)。然后,可洗涤珠子(例如,用无水dmso洗涤四次,每ml无水dmso1-10mg珠子)。然后,可用四丁基铵交换的引物在无水dmso中的(例如,10%w/v)溶液处理珠子(例如,10%w/v三丁胺,20℃下持续16hr,在每30ul引物/dmso溶液1mg珠子的浓度下)。在反应后,将引物/dmso溶液去除,并用浓缩的氨处理珠子(例如,浓度为1-10mg珠子/ml,在20-35℃下持续20min至2hr)。然后,用水(例如,3次)、tet缓冲液(例如,2次)和te缓冲液(例如,2次)洗涤珠子(例如,全部在1-10mg珠子/ml的浓度下)。然后,可将珠子储存在珠子储存缓冲液(例如,浓度为1mg珠子/ml的te缓冲液,ph8.0,含有0.05%tritonx-100和0.01%叠氮化钠)中。在一些情况下,反应在非水性溶剂中进行(例如,以减少水解副反应的量)。
引物溶液可以如下制备:将引物的钠盐溶解在四丁基铵溶液中(例如,5mm,调节至ph7.0,抗衡离子为氯离子、溴离子或醋酸根离子),随后相对于同一缓冲液进行透析直到完成阳离子交换。然后将引物相对于水进行透析以去除过量的缓冲盐,并可将其冻干成干燥粉末。然后可将该材料溶解在无水dmso或nmp中并用于引物官能化。典型的浓度为约10%w/v。可在较高或较低的温度下使用更多或更少的引物持续较短或较长的时间段,从而改变所缀合的引物的量。
图13示出了引物包覆的、具有聚乙二醇(peg)(例如,dpeg)连接体的珠子的制备示例。在该示例中,用n,n-二琥珀酰亚胺基碳酸酯(dsc)将珠子(例如,磁珠“mb”,例如,myonetm磁珠)上的一个或多个羧酸基团活化,从而将所述一个或多个羧酸基团转化成反应性酯,例如,n-羟基琥珀酰亚胺(nhs酯)。该反应性酯可与可包含末端胺和羧酸官能团的异双官能dpeg物质反应。在反应性酯为nhs酯的情况下,nhs酯可经由其末端胺基团与h2n-(peg)n-co2h反应,从而经由酰胺键的形成将该peg物质共价连接至珠子表面。然后,该peg物质的末端羧酸可被活化(例如,经由dsc),并且其产生的反应性酯(例如,nhs酯)随后与氨基封端的引物反应,从而经由酰胺键将该引物共价偶联至该peg物质(并因此偶联至珠子表面)。
图14示出了与图13的示例类似的制备引物包覆的珠子的另一示例,其中谷氨酸与珠子结合的peg物质的dsc活化的羧酸基团反应,并经由酰胺键共价偶联至该peg物质(并因此偶联至珠子表面)。谷氨酸每与一个活化peg羧酸反应,其添加为珠子表面增加两个羧酸基团,从而使可用于后续dsc活化和与氨基封端引物反应的羧酸基团的数目翻倍。这样的策略可增加结合至珠子的引物分子的数目。
采用如本文所述的dpeg策略进行的珠子的加载可根据例如偶联至珠子的dpeg分子的数目和可用于引物附接的所附接dpeg的官能团数目而变化。在一些情况下,附接至peg化珠子的引物的数目可为至少约2个、至少约5个、至少约10个、至少约50个、至少约100个、至少约500个、至少约1000个、至少约5000个、至少约10,000个、至少约25,000个、至少约50,000个、至少约60,000个、至少约70,000个、至少约80,000个、至少约90,000个、至少约100,000个、至少约125,000个、至少约150,000个、至少约200,000个、至少约250,000个、至少约300,000个、至少约350,000个、至少约400,000个、至少约450,000个、至少约500,000、至少约1,000,000个或更多。
在一些情况下,附接至peg化珠子的引物的数目可为至少约2个、至少约5个、至少约10个、至少约50个、至少约100个、至少约500个、至少约1000个、至少约5000个、至少约10,000个、至少约25,000个、至少约50,000个、至少约60,000个、至少约70,000个、至少约80,000个、至少约90,000个、至少约100,000个、至少约125,000个、至少约150,000个、至少约200,000个、至少约250,000个、至少约300,000个、至少约350,000个、至少约400,000个、至少约450,000个、至少约500,000、至少约1,000,000个或更多。
在一些情况下,附接至peg化珠子的引物的数目可为至多约1,000,000个、至多约500,000个、至多约450,000个、至多约400,000个、至多约350,000个、至多约300,000个、至多约250,000个、至多约200,000个、至多约150,000个、至多约125,000个、至多约100,000个、至多约90,000个、至多约80,000个、至多约70,000个、至多约60,000个、至多约50,000个、至多约25,000个、至多约10,000个、至多约5,000个、至多约1,000个、至多约500个、至多约100个、至多约50个、至多约10个、至多约5个或更少。
尽管图13和14示出的示例是关于引物分子向珠子的附接而示出的,但包含胺官能团的任何合适的寡核苷酸均可采用该方法并且以上文所述和图13和14中所示的数目偶联至珠子。
原子转移自由基聚合(atrp)珠子
原子转移自由基聚合(atrp)是一种可控的可逆灭活自由基聚合方法。在atrp中,自由基的灭活包括可逆的原子或基团转移,该转移可由过渡金属络合物(例如,cu、fe、ru、ni、os等的过渡金属络合物)催化。引发剂(例如,卤代烷烃,如溴代烷烃)可被过渡金属络合物活化以生成自由基。然后,单体可与该自由基反应,以将单体与该自由基相附接。然后,所附接的单体可被活化以形成另一自由基,并针对其他单体重复该过程,从而导致生成聚合的物质。
在一些情况下,引发剂被过渡金属络合物活化以生成自由基,该自由基随后引发添加至该引发剂的第一单体的聚合。在第一单体耗尽后,可添加第二单体以继续聚合,从而产生嵌段共聚物。形成间隔嵌段的第一单体可以是水溶性的,而第二单体可以是能够在聚合后进行化学反应的反应性单体。在一些情况下,第一单体和第二单体是相同的,而在其他情况下,第一单体和第二单体是不同的。在一些情况下,将第一单体和第二单体同时添加至引发剂。
在一些情况下,可采用atrp生成引物官能化的颗粒(例如,引物官能化的磁珠)。atrp过程的两个示例(示例a和示例b)在图15中图示。在这两个示例中,带有羧酸的珠子(例如,磁珠,例如,myone珠子)经历活化过程,该活化过程在珠子表面上产生2-溴异丙基基团(–c(ch3)2br)。在一些情况下,该活化过程为3步过程,其包括(1)用dsc将羧酸基团活化成反应性酯基团(例如,nhs酯),(2)使该反应性酯与过量1,3-丙二胺反应以在珠子表面上引入伯胺基团,以及(3)使该伯胺基团与α-溴异丁酰溴反应,产生在其表面上包含能够参与原子转移自由基聚合(atrp)反应的引发剂(例如,图15所示的2-溴异丙基基团(–c(ch3)2br))的活化珠子。
在图15所示的两个示例中,将活化的珠子暴露于包含单体(例如,n,n-二甲基丙烯酰胺(dma),2-羟乙基丙烯酰胺(heaa))、抗坏血酸、催化剂(例如,溴化铜)和三(2-吡啶基甲基)胺(tpma)的溶液中,从而产生接枝在表面上的多个聚合物链(例如,线性聚合物链——(dma-heaa)共聚物)。当聚合物链包含反应性heaa单体时,可用dsc将heaa重复单元的羟基基团活化,并随后使其与胺封端的引物(例如,具有至少2-聚体、5-聚体、10-聚体、15-聚体、20-聚体、25-聚体、30-聚体、35-聚体、40-聚体、45-聚体、50-聚体、55-聚体、60-聚体或更大的引物)反应,以得到引物缀合的珠子。
在图15所示的示例a中,在聚合过程中,可将包含胺反应性基团的单体随机添加至生长中的聚合物链,从而产生包含随机分布在整个链长度上的反应性基团的聚合物链。然后,可将这些反应性基团活化(例如,经由dsc),并使其与带有胺的引物反应以将该引物偶联至珠子,使得该引物在聚合物链的整个长度上被偶联至珠子。这种类型的策略的示例在本文其他各处描述,并且包括图16的示例a、图17所示的示例v、图18所示的示例和图19所示的示例。
在图15所示的示例b中,首先将不包含反应性基团的第一单体添加至珠子,以形成从珠子表面往外延伸的“间隔嵌段”链。通过添加包含胺反应性基团的第二单体继续聚合,以产生更大的聚合物链,其反应性部分在该聚合物链的间隔嵌段的更前方(down)。然后,可将该反应性基团活化,并使其与带有胺的引物反应,以将该引物偶联至珠子。在该策略中,由于聚合物链的胺反应性基团与珠子的表面间隔开,因此经由聚合物链偶联至珠子的引物也是如此。将反应性基团与珠子表面间隔开可降低缀合引物与珠子紧邻时的空间效应,并因此改善引物加载。这种类型的策略的示例在本文其他各处描述,并且包括图16的示例b和图17所示的一个示例。可通过控制两种单体的比例、第二单体的添加时机和氨基引物的浓度来控制聚合物链的链长和引物缀合的程度。
尽管图15示出的示例特别涉及胺封端的引物,但经由图15的任一示例生成的聚合物链的胺反应性基团均可用于将任何合适类型的带有胺的寡核苷酸偶联至珠子。可如图15的各个示例所述生成包含胺反应性基团的聚合物链。然后,可将胺反应性基团活化,并使其与带有胺的寡核苷酸反应,以将该寡核苷酸偶联至珠子。还可以类似的方式将带有胺的肽、蛋白质和其他物质偶联至珠子。
高密度引物涂层的表面化学可能是核酸生物传感器的性能的关键组件,特别是对于依赖于酶催化反应如核酸合成的传感器。如果引物表面密度过低,则所产生的信号可能降至传感器的检测极限以下。因此,较高的引物表面密度可允许捕获更多的靶核酸,从而导致对核酸合成的检测增强。然而,过高的引物密度可导致空间位阻、静电排斥力或引物-引物相互作用,这可能限制可捕获的靶核酸的量。对于依赖于所捕获靶核酸的量的检测系统,捕获有利于传感器性能的量的靶核酸可能是重要的,并且这可能不是最高的可能的引物密度。在酶催化反应如核酸合成中,所产生的信号可取决于酶及其接近核苷酸并将该核苷酸掺入引物-靶标复合物的能力。在这种情况下,生物传感器的最佳输出信号可取决于引物涂层的密度、其吸引靶核酸的能力和酶对引物-靶标复合物进行催化反应的能力的组合。
具有二维(2d)表面涂层的生物传感器的性能可取决于数个因素,包括引物涂层的密度。另一方面,三维表面(3d)涂层可允许在引物之间间隔增加的情况下与2d表面相似的引物密度,或总体更高的引物密度,这二者都可改善生物传感器的性能。
在一个方面,本文描述了具有定制引物密度的表面栓系3d结构的合成。这使得可固定到表面上并且可针对靶标捕获(杂交)、核酸靶序列的扩增和随后的互补核酸链合成(例如,如在核酸测序中)而定制的引物量具有更高的灵活性。通过将2d表面延伸成3d体积,为靶核酸固定创造了更大的表面积。在一些实施方案中,利用3d结构的增大的表面积来增加相邻引物之间的间隔,由此提高靶标杂交和酶促核酸扩增的效率。在一些情况下,利用3d结构的增大的表面积来增加可固定至生物传感器表面的占地面积的核酸的量,从而产生更强的生物传感器输出信号。
本文所述的方法采用远离表面延伸的聚合物刷,并且通过“接枝自(grafting-from)”程序如“表面引发的可控自由基聚合(surface-initiatedcontrolledradicalpolymerization,si-crp)来实现。这允许通过实现三个级别的控制来精确控制可固定在单位体积中的引物的量。第一级控制可通过定制固定在下方2d表面上的引发剂分子的量来实现。惰性表面或功能表面或其混合物可被构建并用于转化成纯的或部分的引发剂表面。存在于这些表面上的引发剂分子随后可用于si-crp反应以合成远离2d引发剂表面延伸的聚合物刷。用于聚合的单体可包括惰性单体(例如,n,n-二甲基丙烯酰胺,惰性水溶性单体)、功能性单体,或惰性单体和功能性单体的组合。所使用的单体的类型及其使用比例可用作第二级控制,其中官能团的密度可以自定义。随后可将所得的聚合物刷用于引物固定,其中功能性单体被活化,随后进行引物固定。这可提供第三级控制,其中可调节聚合物刷上的引物密度。可通过将修饰的功能性引物(例如,胺修饰的引物)经由共价键栓系至聚合物刷而实现引物固定。在一些实施方案中,通过添加胺化稀释剂(例如,2-甲氧基乙胺)来控制聚合物刷上的引物密度。在这些情况下,可将活性功能性单体暴露于引物与稀释剂的混合物,其中引物与稀释剂的比例可以定制,以达到合适的引物密度和间隔。在一些实施方案中,功能性共聚单体可直接用于引物固定而无需活化(例如,五氟苯基丙烯酸酯)。
atrp产生的珠子的其他示例可参见图16至图19。图16示出了从带有羧酸官能团的珠子(例如,dynalmyone羧酸珠子(lifetechnologies))(例如,磁珠“mb”)开始的atrp接枝珠子(ii和iii)的制备示例。在图16所示的两个示例中,在三丁胺(bu3n)的存在下用二琥珀酰亚胺基碳酸酯(dsc)活化羧酸官能团。然后使活化的羧酸基团与带有胺的物质(例如,二胺物质(例如,h2n-a-nh2)或单胺物质(例如,h2n-a-nh2),其中a为—(ch2)m(m=1至10)、—(ch2ch2o)n—ch2ch2—(n=1至100)、—(ch2ch2o)n—ch3(n=1至100))反应,以产生带有胺官能团的珠子。然后,在bu3n的存在下使胺基团与物质(例如,α-溴异丁酰溴(brcoc(ch3)2br))反应,以得到包含含有卤素(例如,图16中所示的溴原子)的引发剂物质的自由基活化的珠子(i)。包含卤素的其他物质(例如,2-氯异丁酰氯)也可用于在珠子表面上生成引发剂。
在图16所示的示例中,(i)与单体物质反应,以经由atrp在珠子表面上生成聚合物链。在图16所示的一个示例(示例a)中,(i)在催化剂(例如,溴化铜(ii)“cu(ii)”)、三(2-吡啶基甲基)胺和抗坏血酸)的存在下与第一单体(例如,包含“w”、“r1”和“r2”基团的单体,其中w、r1和r2中每一个的示例均在图16中示出)和第二单体(例如,包含“r3”和“t”基团的单体,其中r3和t中的每一个的示例均在图16中示出)。所产生的珠子(ii)包含无规共聚物,该无规共聚物包含“x”摩尔百分比的第一单体和“y”摩尔百分比的第二单体,其中(x+y)=100mol%。代表第二单体的x摩尔百分比可具有任何合适的值,剩余的百分比归为y摩尔百分比。例如,x摩尔百分比可在0.01mol%至100mol%的范围内。在一些情况下,x摩尔百分比可为至少0.01mol%、至少约0.1mol%、至少约0.5mol%、至少约1mol%、至少约5mol%、至少约10mol%、至少约25mol%、至少约50mol%、至少约75mol%、至少约90mol%或至少约95mol%。在一些情况下,x摩尔百分比可为至多约95mol%、至多约90mol%、至多约75mol%、至多约50mol%、至多约25mol%、至多约10mol%、至多约5mol%、至多约1mol%、至多约0.5mol%、至多约0.1mol%、至多约0.01mol%或更小。
在图16所示的另一示例(示例b)中,(i)在催化剂(例如,溴化铜(ii)“cu(ii)”)、三(2-吡啶基甲基)胺和抗坏血酸)的存在下与第一单体(例如,包含“r3”和“t”基团的单体,其中r3和t中的每一个的示例均在图16中示出)反应,其中生成包含第一单体的均聚物链。然后,使珠子与该第一单体和第二单体(例如,包含“w”、“r1”和“r2”基团的单体,其中w、r1和r2中每一个的示例均在图16中示出)的混合物反应,以产生包含第一和第二单体的共聚物嵌段,和均聚物。所产生的珠子(iii)包含无规共聚物,该无规共聚物包含在均聚物段中的“y”摩尔百分比的第一单体以及“x”摩尔百分比的包含第一单体和第二单体的共聚物嵌段,其中(x+y)=100mol%。在该示例中,该均聚物链可充当珠子表面与随后添加的单体的反应性基团之间的“间隔嵌段”。例如,这样的间隔嵌段可用于使与聚合物链(以及任何缀合的寡核苷酸)的相对紧密邻近相关联的空间效应最小化并改善随后的寡核苷酸加载。
x摩尔百分比可具有任何合适的值,剩余的百分比归为y摩尔百分比。例如,x摩尔百分比可在0.01mol%至100mol%的范围内。在一些情况下,x摩尔百分比可为至少0.01mol%、至少约0.1mol%、至少约0.5mol%、至少约1mol%、至少约5mol%、至少约10mol%、至少约25mol%、至少约50mol%、至少约75mol%、至少约90mol%、至少约95mol%或更大。在一些情况下,x摩尔百分比可为至多约95mol%、至多约90mol%、至多约75mol%、至多约50mol%、至多约25mol%、至多约10mol%、至多约5mol%、至多约1mol%、至多约0.5mol%、至多约0.1mol%、至多约0.01mol%或更小。此外,在该示例中,x摩尔百分比是组成该共聚物嵌段的第一单体的摩尔百分比(“q”)与第二单体的摩尔百分比(“p”)之和(例如,x=(p+q))。例如,p摩尔百分比可在0.01mol%至100mol%的范围内。在一些情况下,p摩尔百分比可为至少0.01mol%、至少约0.1mol%、至少约0.5mol%、至少约1mol%、至少约5mol%、至少约10mol%、至少约25mol%、至少约50mol%、至少约75mol%、至少约90mol%、至少约95mol%或更大。在一些情况下,p摩尔百分比可为至多约95mol%、至多约90mol%、至多约75mol%、至多约50mol%、至多约25mol%、至多约10mol%、至多约5mol%、至多约1mol%、至多约0.5mol%、至多约0.1mol%、至多约0.01mol%或更小。
在图16所示的示例中,(ii)和(iii)的接枝聚合物的r1基团是胺反应性的,并且随后可与带有胺的引物或其他带有胺的寡核苷酸反应,以将该引物或寡核苷酸偶联至(ii)和(iii)。如本文其他各处所述,例如,可通过与r1基团反应的引物或寡核苷酸分子的数目并且/或者通过r1基团对反应的可用性来控制加载的比例。r1基团的可用性可通过包含在聚合期间添加的r1基团的单体分子的数目来控制。在一些情况下,不同量的单体和/或其他组分可导致不同数目的在聚合期间添加的r1基团。
图17示出了atrp接枝的珠子(例如,磁珠“mb”)的其他示例(iv和v),其包含可与带有胺的引物、其他带有胺的寡核苷酸或其他带有胺的生物分子反应的乙烯基二氢唑酮反应性基团。可经由如上所述的示例a中所示的方法从图16所示的(i)制备(iv),不同之处在于第一单体包含含有r4和r5基团的胺反应性乙烯基二氢唑酮基团(例如,图9c中的含有乙烯基二氢唑酮的单体)。此外,可经由如上所述的示例b中所示的方法从图16所示的(i)制备(v),其中第二单体包含含有r4和r5基团的胺反应性乙烯基二氢唑酮基团(例如,图9c中的含有乙烯基二氢唑酮的单体)。在(iv)和(v)二者中,r4和r5基团可独立地为h或ch3。针对图16中的示例a和示例b描述的摩尔百分比也分别适用于图17所示的(iv)和(v)。
图18示出了超支化atrp接枝的珠子(如,磁珠“mb”)的示例(vi),其包含可与其他物质反应以提供每个单体超过一个胺反应性基团的2-羟乙基丙烯酰胺反应性基团。可经由如上所述的示例a中所示的方法从图16所示的(i)制备(vi),其中第一单体的w基团为单键,并且r1基团为包含末端羟基基团的2-羟乙基丙烯酰胺基团。针对图16中的示例a描述的x和y摩尔百分比也适用于图18所示的(vi)(并因此适用于下文所述的(vii)和(viii))。
可在bu3n的存在下用dsc活化(vi)的末端羟基基团,然后在bu3n的存在下使活化的物质与n-(5-氨基-1-羧基戊基)亚氨基二乙酸(图18中的氨基丁基nta)反应以产生图18所示的(vii)。如图18所示,(vii)的每个最初包含单个2-羟乙基丙烯酰胺反应性基团的单体单元均包含多个羧酸基团(例如,图18所示的三个)。然后,该羧酸基团可在bu3n的存在下经历另一轮dsc活化,随后使活化的羧酸基团与带有胺的引物、其他带有胺的寡核苷酸(例如,“寡核苷酸(oligo)”)或其他带有胺的生物分子(例如,带有胺的蛋白质、带有胺的肽和含有胺的碳水化合物)反应,产生(viii)——与引物或其他类型的寡核苷酸相偶联的珠子。
图19示出了将引物或其他类型的寡核苷酸附接至上文描述且图18中示出的atrp接枝的珠子(vi)的示例,其中没有首先向(vi)添加n-(5-氨基-1-羧基戊基)亚氨基二乙酸。如图19所示,可在bu3n的存在下用dsc活化(vi)的2-羟乙基丙烯酰胺基团的末端羟基基团。然后,可使活化的羟基基团与带有胺的引物、其他类型的带有胺的寡核苷酸或其他带有胺的生物分子(例如,带有胺的蛋白质、带有胺的肽、含有胺的碳水化合物)反应以生成(ix)——与引物或其他类型的寡核苷酸相偶联的珠子。如上文所讨论的,针对图16中的示例a描述的x和y摩尔百分比也适用于(vi),并因此也适用于(ix)。
虽然未在图18和图19的示例中示出,但可根据图16所示的示例b生成具有聚合物链的珠子,其中第二单体上的r1基团为2-羟乙基丙烯酰胺。然后,该珠子可在bu3n的存在下与n-(5-氨基-1-羧基戊基)亚氨基二乙酸反应,以对每个r1反应性基团提供多个羧酸官能团,与图18所示的vii类似。然后,该羧酸官能团可在bu3n的存在下被dsc活化,并随后与带有胺的引物、其他带有胺的寡核苷酸或其他带有胺的生物分子(例如,带有胺的蛋白质、带有胺的肽、带有胺的碳水化合物)反应,以将相关的带有胺的物质偶联至珠子。作为图19所示示例的替代或与之类似,第二单体上的r1基团可在bu3n的存在下被dsc活化,并随后与带有胺的引物、带有胺的寡核苷酸或其他带有胺的生物分子(例如,带有胺的蛋白质、带有胺的碳水化合物、带有胺的肽)反应,以将相关物质偶联至珠子。
采用如本文所述的atrp策略得到的珠子的引物或其他寡核苷酸加载可根据例如珠子上生成的聚合物分子的数目和/或可用于反应的聚合物反应性基团的数目而变化。在一些情况下,附接至包含atrp生成的聚合物的珠子上的引物或其他寡核苷酸的数目可为至少约2个、至少约5个、至少约10个、至少约50个、至少约100个、至少约500个、至少约1000个、至少约5000个、至少约10,000个、至少约25,000个、至少约50,000个、至少约60,000个、至少约70,000个、至少约80,000个、至少约90,000个、至少约100,000个、至少约125,000个、至少约150,000个、至少约200,000个、至少约250,000个、至少约300,000个、至少约350,000个、至少约400,000个、至少约450,000个、至少约500,000、至少约1,000,000个或更多。
在一些情况下,附接至包含atrp生成的聚合物的珠子上的引物或其他寡核苷酸的数目可为至多约1,000,000个、至多约500,000个、至多约450,000个、至多约400,000个、至多约350,000个、至多约300,000个、至多约250,000个、至多约200,000个、至多约150,000个、至多约125,000个、至多约100,000个、至多约90,000个、至多约80,000个、至多约70,000个、至多约60,000个、至多约50,000个、至多约25,000个、至多约10,000个、至多约5,000个、至多约1,000个、至多约500个、至多约100个、至多约50个、至多约10个、至多约5个或更少。
在一些情况下,包括图16-19的示例中所示的那些珠子在内,珠子上聚合物链的分子量可在10千道尔顿(kda)至3000kda、50kda至2500kda、100kda至1,500kda,或500kda至1,000kda的范围内。在一些实施方案中,接枝聚合物的分子量可为约10kda、25kda、50kda、100kda、150kda、200kda、250kda、300kda、350kda、400kda、450kda、500kda、550kda、600kda、650kda、700kda、750kda、800kda、850kda、900kda、950kda、1000kda、1050kda、1100kda、1150kda、1200kda、1250kda、1300kda、1350kda、1400kda、1450kda、1500kda、1550kda、1600kda、1650kda、1700kda、1750kda、1800kda、1850kda、1900kda、1950kda、2000kda、2050kda、2100kda、2150kda、2200kda、2250kda、2300kda、2350kda、2400kda、2450kda、2500kda、2550kda、2600kda、2650kda、2700kda、2750kda、2800kda、2850kda、2900kda、2950kda或3000kda。
实施例
实施例1:15-聚体的四丁基铵盐的制备
15-聚体引物的四丁基铵盐在非水性溶剂(例如,n-甲基吡咯烷酮(nmp),dmso)中可能是相对可溶性的,其中珠子上表面接枝的反应性聚合物溶胀。这样的溶解性可导致15-聚体引物向反应性聚合物的缀合增强。该实施例描述了15-聚体寡核苷酸的水溶性钠盐向可溶于非水性溶剂如nmp的盐的转化。
在转化之前,15-聚体寡核苷酸的一般处理准则可包括在打开具有该15-聚体寡核苷酸的容器之前使该寡核苷酸升温至环境温度,以及在清洁且无尘的环境中处理该寡核苷酸以避免交叉污染。无水无胺的nmp可如下制备:使nmp通过中性氧化铝柱,随后在分子筛下储存。
可用于该制备的仪器和材料可包括表1中示出的以下各项:
表1
为了制备引物(15-聚体)的四丁基铵盐而完成的示例方案包括:
(a)向透析盒(例如,slide-a-
(b)通过将1.390g四丁基氯化铵溶解在1l的18mω水中并通过添加40%四丁基氢氧化铵(约200μl)将ph调节至7来制备5mmtbac缓冲液;
(c)在15mlfalcon管中,将211.0mg引物钠盐(从oligofactory获得,tib15-聚体,mw4674.1,5’-氨基c6-dc-dc-t-da-t-dc-dc-dc-dc-t-dg-t-dg-t-dg-3’)溶解在8mltbac缓冲液中;
(d)用注射器针将引物溶液转移至透析盒中;
(e)用1mltbac缓冲液漂洗该15ml管两次,并将漂洗液转移至透析盒中;
(f)用注射器针除去透析盒内的气泡;
(g)将引物溶液在1ltbac缓冲液中透析,每天更换新鲜tbac缓冲液两次,持续两天;
(h)用18mω水重复步骤(g);
(i)将经透析的溶液分配至十六个2-ml微量离心管中;
(j)将该管的内容物在-20℃下冷冻;
(k)在spin-vap蒸发器或冻干机中将内容物蒸发至干及恒重。
在使用前以1:10或1:5w/v的比例将干燥的引物溶解在无水无胺nmp中。
实施例2:氨基珠子的制备
如本文其他各处所述,带有氨基的磁珠可用于预先制备的反应性聚合物或共聚物的表面接枝,以供寡核苷酸的随后缀合。该实施例提供了用于生成带有氨基的磁珠的方案。在该实施例中,采用二琥珀酰亚胺基碳酸酯(dsc)和二氨基丙烷(例如,1,3-二氨基丙烷)将myonetm带有羧基的珠子(thermoscientific)转化成氨基珠子。该实施例中描述的示例方案还可适用于将带有羧基的珠子(例如,来自bangs的promag-hc)转化成带有氨基的珠子。
一般材料处理准则可包括:在干燥条件下处理二琥珀酰亚胺基碳酸酯,因为其可能是吸湿性且水解不稳定的,并且在通风橱中处理1,3-二氨基丙烷,因为其在暴露于空气时是挥发性的。无水无胺的nmp可如下制备:使nmp通过中性氧化铝柱,随后在分子筛下储存。
可用于该制备的仪器和材料可包括表2中示出的以下各项:
表2
为了在作为溶剂的无水无胺nmp中采用dsc制备带有氨基的磁珠而完成的示例方案包括:
(a)向15-mlfalcon管中添加2ml重悬的myonetm羧酸珠子;
(b)用5ml无水无胺nmp洗涤珠子4次;
(c)添加0.2620g(1.0228毫摩尔(mmol))dsc和0.20ml(0.8395mmol)三丁胺在8ml无水无胺nmp中的溶液,并将所得的混合物在环境温度下翻转18小时;
(d)用5ml无水无胺nmp洗涤珠子4次;
(e)将珠子重悬在5ml无水无胺nmp中,并添加1.50ml(17.971mmol)的1,3-二氨基丙烷;
(f)将所得混合物在环境温度下翻转24小时;
(g)用5ml无水无胺nmp洗涤珠子4次;以及
(h)将珠子重悬在5ml无水无胺nmp中,并储存在4℃的冰箱中。
为了在作为溶剂的乙腈(acn)中采用dsc制备带有氨基的磁珠而完成的示例方案包括:
(a)向15-ml离心管中添加2ml重悬的myonetm羧酸珠子;
(b)添加用5ml无水acn洗涤四次的珠子;
(c)添加0.2601g(1.0153mmol)dsc和0.20ml(0.8395mmol)三丁胺在8ml无水acn中的溶液,并将所得的混合物在环境温度下翻转18小时;
(d)用6ml无水acn洗涤珠子4次;
(e)将珠子重悬在10ml无水acn中,并添加1.50ml(17.971mmol)1,3-二氨基丙烷,随后在环境温度下翻转23小时;以及
(f)将珠子用5ml无水acn洗涤4次,重悬在5ml无水acn中,并储存在4℃的冰箱中。
实施例3:20%活性接枝聚合物的制备
如本文其他各处所述,接枝聚合物可充当将引物共价附接至珠子(例如,磁珠)表面上的连接。通过使反应性酯五氟苯基乙酸酯(pfpa)与水溶性单体n,n-二甲基丙烯酰胺(dma)以20:80的摩尔比聚合而制得的共聚物可使珠子(例如,磁珠)表面上的引物间隔开,并可因此导致扩增后扩增子与引物之比增加。该共聚物(例如,具有20mol%反应性基团)可溶于非水性溶剂,如n-甲基吡咯烷酮(nmp)和乙腈(acn)。这样的共聚物可以是相对亲水性和吸湿性的,并且在这类情况下,应在密封容器中低温(例如,-20℃)储存,并在使用前升温至环境温度。
材料的一般处理准则包括:(a)通过真空分馏对pfpa和dma单体进行纯化以去除抑制剂和其他杂质,并将纯化的单体储存在容器中和-20℃下;(b)在打开容器前使纯化的单体升温至环境温度;(c)处理该单体并在通风橱中进行聚合;以及(d)在对单体进行处理后将保护性手套或任何被单体污染的物品留在通风橱中。这些污染的物品可作为危险废物处置。
可用于该制备的仪器和材料可包括表3中示出的以下各项:
表3
为了pfpa和dma的共聚而完成的示例方案包括:
(a)提供反应器皿,包括三颈500-ml圆底烧瓶,该烧瓶装备有2"teflon搅拌叶片、24/40至14/20磨砂玻璃转接器、14/20水冷冷凝器、用于14/20和24/40接头的橡胶隔片、用于氮气吹扫的一个12"18号ss注射器针和用于排放至矿物油鼓泡器中的一个2"18号ss注射器针;
(b)向500-ml三颈圆底烧瓶中加入30ml无水acn、8.004g(80.741mmol)dma(sigmaaldrich,经真空蒸馏)、4.801g(20.163mmol)pfpa(monomer-polymerdajaclabs,经真空蒸馏)和0.011g(0.044mmol)2,2'-偶氮二(2,4-二甲基戊腈)(vazo-52,tciamerica);
(c)在环境温度下通过在125rpm恒定搅拌下以约60ml/min的超纯氮气温和鼓泡持续30分钟来对反应混合物进行吹扫;
(d)将反应烧瓶浸没在55℃油浴中19小时,伴随25ml/min流速的超纯氮气鼓泡和120rpm恒定搅拌,所得的反应混合物高度粘稠;
(e)在60℃水浴温度下在减压(rota-vap)下去除溶剂60分钟,以产生聚合物的固体块;
(f)将该聚合物产物再溶解于30ml无水thf中;
(g)在恒定搅拌下逐滴添加20ml正己烷。所得溶液是浑浊的;
(h)在使用2"teflon搅拌叶片剧烈搅拌的同时,向连续充满干燥氮气的2-l玻璃锥形瓶中的800-ml正己烷中以细流添加在thf/己烷中的聚合物;
(i)将沉淀的聚合物额外搅拌5分钟并丢弃上清液;
(j)向沉淀的聚合物添加500ml新鲜的正己烷并温和搅拌10分钟;
(k)将(i-j)重复一次以生成再次沉淀的聚合物;以及
(l)将沉淀的聚合物转移至广口500-ml玻璃瓶中,并在60℃真空下干燥24小时,以产生9.2g(pfpa-dma)共聚物。
实施例4:20%活性聚合物的接枝和15-聚体的缀合
可将反应性接枝聚合物(例如,如通过实施例3所述的方法制备的20%反应性接枝聚合物)接枝至珠子,并且可将引物偶联至该接枝的聚合物。该实施例描述了用于聚合物接枝和引物向接枝聚合物偶联的示例方法。反应性接枝聚合物可以是吸湿性的,并且在这类情况下应相应地进行处理。
材料的一般处理准则可包括:(a)制备新鲜的加帽溶液以供当天使用;(b)每次反应使用新的含有无水乙腈acn的100-ml瓶;(c)如下制备无水无胺的nmp:使nmp通过中性氧化铝柱,并将其在分子筛下储存。
可用于该制备的仪器和材料可包括表4中示出的以下各项:
表4
为了制备加帽溶液而完成的示例方案包括:
(a)通过将1.21ml的28%氢氧化铵添加至10ml去离子水中,随后用去离子水将其稀释至20ml,来制备1.0m氢氧化钠溶液;
(b)通过将4ml的1.0m氢氧化铵溶液和0.554ml三乙胺(tea)添加至10ml去离子水中,随后用去离子水将其稀释至40ml,来制备加帽溶液;
为了在nmp中进行胺化磁珠的接枝和15聚体引物的缀合而完成的示例方案包括:
(a)将以nmp作为溶剂用dsc制备的一份悬浮的120亿个胺化珠子在50-mlfalcon管中用20ml无水无胺nmp洗涤2次,并将该珠子在5ml无水无胺nmp中重悬并进行声处理;
(b)将600.8mg20%反应性接枝聚合物溶解在12mlnmp中;
(c)将24μltea添加至聚合物溶液中;
(d)将珠子悬浮液添加至聚合物溶液中,并在环境温度下翻转20小时;
(e)用10ml无水无胺nmp洗涤珠子3次;
(f)将珠子重悬在0.6ml无水无胺nmp中,添加600μl在无水无胺nmp中含有20%w/v15-聚体引物的溶液,并在环境温度下将该混合物翻转20小时;
(g)将珠子用10mlnmp洗涤3次,用10ml50%水性nmp洗涤1次,并用10ml18mω水洗涤1次;
(h)添加含有100mmtea和100mm氨的15ml加帽溶液,并在thermomixer中于60℃下振荡2小时;
(i)用10ml18mω水洗涤珠子3次。如果ph高于7,则可完成额外的洗涤;
(j)向珠子添加12ml含有0.05%triton-100和0.01%叠氮化钠(ph7)的1xte缓冲液(ph8.0),并将该悬浮液储存在4℃的冰箱中。
为了在acn中进行胺化磁珠的接枝并在nmp中缀合15聚体引物而完成的示例方案包括:
(a)将以acn作为溶剂用dsc制备的一份悬浮的120亿个胺化珠子在50-mlfalcon管中用20ml无水acn洗涤2次,并在5ml无水acn中重悬并进行声处理;
(b)将612.4mg20%反应性接枝聚合物溶解在12ml无水acn中;
(c)将24μltea添加至聚合物溶液中;
(d)将珠子悬浮液添加至聚合物溶液中,并在环境温度下翻转20小时;
(e)将珠子用10l无水acn洗涤3次,并用10ml的1:1v/v无水acn洗涤1次,并用10ml无水无胺nmp洗涤2次;
(f)将珠子重悬在0.6ml无水无胺nmp中,添加300μl在无水无胺nmp中含有20%w/v15-聚体引物的溶液,并在环境温度下将该混合物翻转20小时;
(g)将珠子用10mlnmp洗涤3次,用10ml50%水性nmp洗涤1次,并用10ml18mω水洗涤1次;
(h)添加含有100mmtea和100mm氨的15ml加帽溶液,并将混合物在thermomixer中于60℃下振荡2小时;
(i)用10ml18mω水洗涤珠子3次。如果ph高于7,则可完成额外的洗涤;以及
(j)向珠子添加12ml含有0.05%triton-100和0.04%叠氮化钠(ph7)的1xte缓冲液,并将该悬浮液储存在4℃的冰箱中。
实施例5:包含寡核苷酸的peg化珠子的合成
在该实施例中,生成了包含与寡核苷酸相连接的dpeg链的珠子。如图20a(图i)所示,提供了包含重复乙二醇单元和胺及羧酸官能团(例如,氨基-dpeg-12-酸)的异双官能dpeg。图20a(图i)所示的示例dpeg的大小为24,指代该dpeg链中重复单元(—ch2ch2o—)的数目。虽然示出了大小为12的dpeg,但该实施例中所述的方法适用于具有任何合适大小的dpeg。也提供并在图20a(图ii)示出了包含表面羧酸基团的珠子。该羧酸基团可经由烃链偶联至珠子表面。在一些情况下,该珠子为myone珠子,其具有经由包含平均50个重复单元的烃链连接至珠子表面的羧酸基团。还可以以盐,例如图20a(图ii)所示的钠盐形式提供珠子。
如图20b所示,所提供的珠子(i)以在水溶液中的钠盐形式提供。首先在n-甲基-2-吡咯烷酮(nmp)的存在下使(i)与四丁基氢氧化铵n(nbu)4oh接触,以将珠子(i)离子交换成四丁基铵盐形式的珠子(ii),随后用nmp进行洗涤。接下来,在nmp和tba的存在下用dsc将珠子(ii)的羧酸基团活化,以生成在珠子表面上包含胺反应性琥珀酰亚胺基反应性基团的珠子(iii)。然后在二甲基亚砜(dmso)和tba的存在下使珠子(iii)与图20a(图i)所示的氨基-dpeg12-酸物质反应,以生成包含具有末端羧酸基团的dpeg链的珠子(iv)。
如图20c所示,然后在nmp的存在下使珠子(iv)与n(nbu)4oh接触,以将珠子(iv)转化成四丁基铵盐形式,随后用nmp进行洗涤。然后,在nmp和tba的存在下用dsc将dpeg链的羧酸基团活化,以生成包含具有末端琥珀酰亚胺基基团的dpeg链的珠子(v)。然后在四丁基铵盐、dmso和tba的存在下使珠子(v)与胺封端的寡核苷酸(例如,5’-nh2-寡核苷酸)反应,以生成与该寡核苷酸相偶联的珠子(vi)。在一些情况下,偶联至珠子的寡核苷酸为引物。在一些情况下,氨基-dpeg12-酸中的peg可具有至少约2000道尔顿(da)、至少约3000da、至少约3500da、至少约4000da、至少约4500da、至少约5000da、至少约5500da或更高的分子量(mw)。
实施例6:氨基磁珠的制备
将5mldynal羧酸珠子(500亿个珠子)放入15-ml聚丙烯falcon管中,并用5ml1nhcl溶液洗涤一次、用5ml10mmhcl溶液洗涤一次、用5ml蒸馏水洗涤两次并用5ml无水无胺nmp洗涤四次。添加0.512g(2.00mmol)dsc和0.50ml(2.10mmol)三丁胺在5ml无水无胺nmp中的溶液,并在20℃下以750rpm混合2小时。用5ml无水无胺nmp将珠子洗涤两次。将珠子重悬在5ml无水无胺nmp、0.5ml(6.00mmol)1,3-二氨基丙烷和0.50ml(2.10mmol)三丁胺的溶液中。将该混合物在20℃下以750rpm混合14小时。将珠子用5ml无水无胺nmp洗涤两次,重悬在5ml无水无胺nmp中,并储存在4℃的冰箱中。
实施例7:稀释的氨基磁珠的制备
将5mldynal羧酸珠子(500亿个珠子)放入15-ml聚丙烯falcon管中,并用5ml1nhcl溶液洗涤一次、用5ml10mmhcl溶液洗涤一次、用5ml蒸馏水洗涤两次并用5ml无水无胺nmp洗涤四次。添加0.512g(2.00mmol)dsc和0.50ml(2.10mmol)三丁胺在5ml无水无胺nmp中的溶液,并在20℃下以750rpm混合2小时。用5ml无水无胺nmp将珠子洗涤两次。将珠子重悬在5ml无水无胺nmp、0.25ml(3.00mmol)1,3-二氨基丙烷、0.26ml2-甲氧基乙胺(2.99mmol)和0.50ml(2.10mmol)三丁胺的溶液中。将混合物在20℃下以750rpm混合14小时。将珠子用5ml无水无胺nmp洗涤两次,重悬在5ml无水无胺nmp中,并储存在4℃的冰箱中。
实施例8:引发剂包覆的(bib)磁珠的制备
将5ml氨基磁珠(500亿个珠子,如实施例2所述生成)放入15-ml聚丙烯falcon管中,并用5ml无水二氯甲烷洗涤两次。添加0.5ml(4.05mmol)α-溴异丁酰溴和0.50ml(2.10mmol)三丁胺在10ml无水二氯甲烷中的溶液,并在20℃下以750rpm混合2小时。将珠子用10ml无水二氯甲烷洗涤两次,并用5ml无水无胺nmp洗涤两次。将珠子重悬在5ml无水无胺nmp中,并储存在4℃的冰箱中。
实施例9:atrp接枝磁珠的制备
将0.25ml引发剂包覆的bib珠子(25亿个珠子,如实施例8所述生成)用0.5ml甲醇洗涤3次并重悬在0.5ml甲醇中。通过将0.311g羟乙基丙烯酰胺(heaa)(2.70mmol)和0.812g二甲基丙烯酰胺(dma)(8.19mmol)溶解在2.5ml甲醇中来制备单体溶液。通过将4mg溴化铜(ii)(cubr2)(0.02mmol)和25mg三(2-吡啶基甲基)胺(tpma)(0.09mmol)溶解在1ml甲醇中来制备铜配体溶液。在圆底4颈烧瓶中将珠子悬浮液与单体溶液和44μl铜配体溶液合并,并通过将超纯氮气鼓泡通过混合物来将该混合物脱氧30分钟。通过将25mg抗坏血酸(0.14mmol)溶解在1ml蒸馏水中来制备活化剂溶液。将0.46ml活化剂溶液添加至脱气的反应混合物中,将其另外脱气5min,并使其在惰性气氛下聚合额外90min。将该反应混合物转移至15mlfalcon管,在其中将珠子与溶液相分离。将珠子用0.5ml甲醇洗涤四次并重悬在0.5ml甲醇中,并储存在4℃的冰箱中。
实施例10:寡核苷酸缀合的磁珠的制备
用0.1ml无水无胺nmp将0.1mlatrp接枝磁珠洗涤四次。制备71mg(0.28mmol)dsc和0.07ml(0.29mmol)三丁胺在0.64ml无水无胺nmp中的溶液。将0.1mldsc溶液添加至atrp接枝磁珠,并在20℃下以1400rpm混合2小时。用0.1ml无水无胺nmp将珠子洗涤两次。通过将寡核苷酸的钠盐相对于5mm四丁基氯化铵(tbac)(调节至ph7)透析并随后相对于18mω水透析来制备在无水无胺nmp中呈四丁基铵盐形式的胺修饰的寡核苷酸(30聚体)。将透析的寡核苷酸冷冻干燥直至恒重,并将其直接溶解在无水无胺nmp中至10%w/v浓度。向dsc活化的珠子加入氨基封端的寡核苷酸在无水无胺nmp和0.0015ml三丁胺中的0.015ml10%溶液(w/v)。将混合物在60℃下以1400rpm混合14小时。将珠子用0.2ml无水无胺nmp洗涤,随后在0.2ml水、1nnaoh、水和珠子储存缓冲液(含有0.05%tritonx-100和0.01%叠氮化钠的1xte(10mm,ph8.0,1mmedta))中洗涤。将珠子重悬在0.5ml珠子储存缓冲液中并储存在4℃的冰箱中。
实施例11:寡核苷酸缀合磁珠的杂交试验
将0.001ml寡核苷酸缀合磁珠与0.001ml100μmfam标记的互补寡核苷酸和0.018ml退火缓冲液(具有100mm氯化钠(nacl)的1xte(10mmtrisph8.01mmedta))混合。通过加热至95℃持续2min并缓慢冷却至室温来将该混合物变性并再次退火。将珠子从溶液中分离并用0.2mltet缓冲液(具有0.01tritonx-100的1xte)洗涤两次,重悬在0.1ml1xte缓冲液中,并在bdaccuric6流式细胞仪上通过流式细胞术进行分析。
实施例12:寡核苷酸-peg缀合的磁珠的制备
将先前采用来自thermoscientific的myonetm羧酸珠子制备的悬浮在乙腈中的20亿个氨基珠子转移至2-ml微量离心管。用1ml无水二氯甲烷(dcm)洗涤珠子3次。将氨基珠子沉淀物加入至19.5mg双-dpeg21-pfp酯(quantabiodesign)在1ml无水dcm和10μl三丁胺(tba)中的溶液中。将混合物在环境温度下翻转3小时。将珠子用1ml无水dcm洗涤3次,用无水dcm与无水dmso的1ml1:1v/v混合物洗涤1次,并用1ml无水dmso洗涤2次。然后将珠子悬浮在80μl无水dmso中。然后,向珠子悬浮液中加入一份10%15-聚体溶液,该溶液是通过将在15-聚体的四丁基铵盐中的13.4mg15-聚体和13.4μltba溶解在134μl无水dmso中而制备的。将混合物在20℃/1400rpm下于thermomixer上涡旋20小时。将珠子用1mldmso、1ml50%水性dmso和1ml去离子水洗涤两次。将1.5ml含有100mm三乙胺和100mm氢氧化铵的加帽溶液添加至珠子的沉淀物。将混合物在60℃/140rpm下涡旋2小时。将珠子用去离子水洗涤两次,用由含有0.05%triton-x100和0.04%叠氮化钠的1xte缓冲液制备的珠子储存缓冲液洗涤一次。将珠子重悬在1ml珠子储存缓冲液中,并将珠子储存在4℃的冰箱中。
本公开内容的系统和方法可与其他系统和方法组合或被其他系统和方法改进,诸如pct专利申请号pct/us2011/054769、pct专利申请号pct/us2012/039880、pct专利申请号pct/us2012/067645、pct专利申请号pct/us2014/027544和pct专利申请号pct/us2014/069624中描述的那些,这些申请中的每一个均通过引用全文并入于此。
尽管在此已经示出和描述了本发明的优选实施方案,但对于本领域技术人员显而易见的是,这样的实施方案只是以示例的方式提供的。本发明并不旨在仅限于说明书中提供的具体示例。尽管已经参考上述说明书描述了本发明,但本文实施方案的描述和图示并不意味着以限制性意义解释。本领域技术人员将会想到不脱离本发明的许多变化、改变和替换。此外应当理解,本发明的所有方面并不限于本文所述的具体描述、配置或相对比例,而是取决于多种条件和变量。应当理解,在实践本发明的过程中可以采用对本文所述发明的实施方案的各种替代方式。因此可以设想,本发明还应当涵盖任何此类替代、修改、变化或等同物。以下权利要求旨在限定本发明的范围,并从而涵盖这些权利要求范围内的方法和结构及其等同物。
- 还没有人留言评论。精彩留言会获得点赞!