一种1‑吩噻嗪基‑3‑芳基‑4‑乙酰基‑1,5‑己二酮及其制备方法与流程
本发明属于化学合成领域,特别涉及一种1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮及其制备方法。
背景技术:
n-吩噻嗪基查尔酮由于其含有一个a,β-不饱和双键,所以关于n-吩噻嗪基查尔酮的反应多围绕michael加成反应或者合环反应进行。它可与肼类、腈、活泼亚甲基化合物或胺等物质进行michael加成反应,生成一系列含有吩噻嗪基的衍生物,该类衍生物在抗菌,抗病毒等领域有很好的应用。
michael加成反应是一类重要的形成碳—碳键的有机反应,其最直接的应用就是增长碳链,合成含有多个官能团的化合物,这些化合物均具有进一步反应的能力,生成各种类型的有机化合物。但传统的michael反应大多是以强碱作催化剂在有机溶剂中进行,催化剂碱性太强或者反应时间较长,会有很多的副产物产生,从而产率不理想。
技术实现要素:
本发明的目的在于提供一种1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮及其制备方法,采用固相研磨法,合成了一系列未见文献报道的新的michael加成产物,该方法反应时间短、无须溶剂、绿色、环保、经济、且操作简单、反应条件温和,后处理简单、产率高。
为达到上述目的,本发明采用以下技术方案:
一种1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮,其结构通式如下:
其中ar为苯基、取代苯基或杂环基。
所述取代苯基为对氯苯基、对溴苯基、对氟苯基、甲基苯基、甲氧基苯基、对硝基苯基、间硝基苯基、邻硝基苯基、二甲氨基苯基、羟基苯基、苯乙烯基;
所述杂环基为呋喃基、噻吩基或吡啶基。
所述的1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮的制备方法,其具体步骤如下:
向干燥的研钵中加入amol1-吩噻嗪基-3-芳基-丙烯酮,bmol催化剂,cmol乙酰丙酮,研磨使其进行反应,tlc跟踪检测直至反应完全,然后水洗、抽滤,将滤饼干燥后即得到1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮,其中a:b:c=1:(1~1.5):(1~2.0)。
所述1-吩噻嗪基-3-芳基-丙烯酮的结构通式如下:
其中ar为苯基、对氯苯基、对溴苯基、对氟苯基、甲基苯基、甲氧基苯基、对硝基苯基、间硝基苯基、邻硝基苯基、二甲氨基苯基、羟基苯基、苯乙烯基、呋喃基、噻吩基或吡啶基。
所述催化剂为固体naoh或无水k2co3。
所述研磨反应的时间为30~40min。
当1-吩噻嗪基-3-芳基-丙烯酮的原料点消失时表示原料反应完全;tlc检测所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂。
抽滤时,对滤饼进行多次水洗,直到滤液的ph呈中性。
与现有技术相比,本发明具有以下有益效果:
本发明采用固相研磨法,由乙酰丙酮和1-吩噻嗪基-3-芳基-丙烯酮反应,合成了一系列未见文献报道的新的michael加成产物,即1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮,并探索了其制备方法,同时优化了实验条件,缩短了反应时间,为绿色合成做出了贡献。本发明提供的1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮是一系列全新的含有吩噻嗪基的酮类衍生物,具有杀菌、抑菌等功效,在抗菌、抗病毒等领域有很好的应用前景。
本发明提供的1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮的制备方法,将1-吩噻嗪基-3-芳基-丙烯酮、催化剂和乙酰丙酮加入干燥的研钵中迅速研磨进行反应,研磨过程中,原料随着反应的进行开始变成粘稠状而后逐渐变为固体,tlc跟踪检测至反应完全,产物经水洗、抽滤、干燥即得到1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮。与传统合成方法相比,本发明采用固相研磨法,反应过程简单,反应现象明显,反应时间短、无须溶剂、绿色、环保、经济、且操作简单、反应条件温和,设备要求低,且该方法的后处理简单、副产物少,产率高。克服了传统合成方法反应时间长,副产物多,产率低等缺点,具有经济、方便、高效、绿色的优点。
进一步的,本发明在制备过程中,用tlc监测反应过程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚,监测准确,利于控制反应进度和结束。同时本发明所用的催化剂为固体naoh或无水k2co3,廉价易得,催化效果良好,使反应更加迅速和完全,且后处理简单。
附图说明
图1为实施例1制得的产物的红外图谱;
图2为实施例2制得的产物的红外图谱;
图3为实施例3制得的产物的红外图谱;
图4为实施例1制得的产物的1hnmr图谱;
图5为实施例2制得的产物的1hnmr图谱;
图6为实施例3制得的产物的1hnmr图谱。
具体实施方式
本发明提供的1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮的反应方程式如下:
其中ar为苯基、对氯苯基、对溴苯基、对氟苯基、甲基苯基、甲氧基苯基、对硝基苯基、间硝基苯基、邻硝基苯基、二甲氨基苯基、羟基苯基、苯乙烯基、呋喃基、噻吩基或吡啶基。
下面将结合本发明较佳的实施例对本发明做进一步详细说明。
实施例1
称取0.002mol乙酰丙酮和0.0015mol无水k2co3于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-苯基-丙烯酮,研磨35min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得灰绿色粉末,即为1-吩噻嗪基-3-苯基-4-乙酰基-1,5-己二酮。产率为:85.6%,m.p.112℃~114℃。
图1是本发明实施例1制备的1-吩噻嗪基-3-苯基-4-乙酰基-1,5-己二酮的红外图谱,由图1可知:3057cm-1处为ar-h的振动吸收峰,而在2954cm-1、1381cm-1处为-ch3的吸收峰,在2921cm-1、1438cm-1处为-ch2的吸收峰,在1734cm-1、1654cm-1处的峰为c=o的特征吸收峰,1589cm-1和1464cm-1处的峰为苯环的呼吸振动吸收峰,742cm-1为苯环上的邻二取代的吸收峰。综上所述,可以证实合成得到了1-吩噻嗪基-3-苯基-4-乙酰基-1,5-己二酮。
图4是本发明实施例1制备的1-吩噻嗪基-3-苯基-4-乙酰基-1,5-己二酮的1hnmr图谱,由图4可知:1hnmr:6.52-7.16(m,13h,ar-h),2.76-2.82(d,2h,coch2),3.80-3.97(m,1h,ch),2.15(s,3h,coch3).
实施例2
称取0.002mol乙酰丙酮和0.0015mol无水k2co3于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(4-氯苯基)-丙烯酮,研磨37min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得棕色粉末,即为1-吩噻嗪基-3-(4-氯苯基)-4-乙酰基-1,5-己二酮。产率为:87.4%,m.p.108℃~112℃。
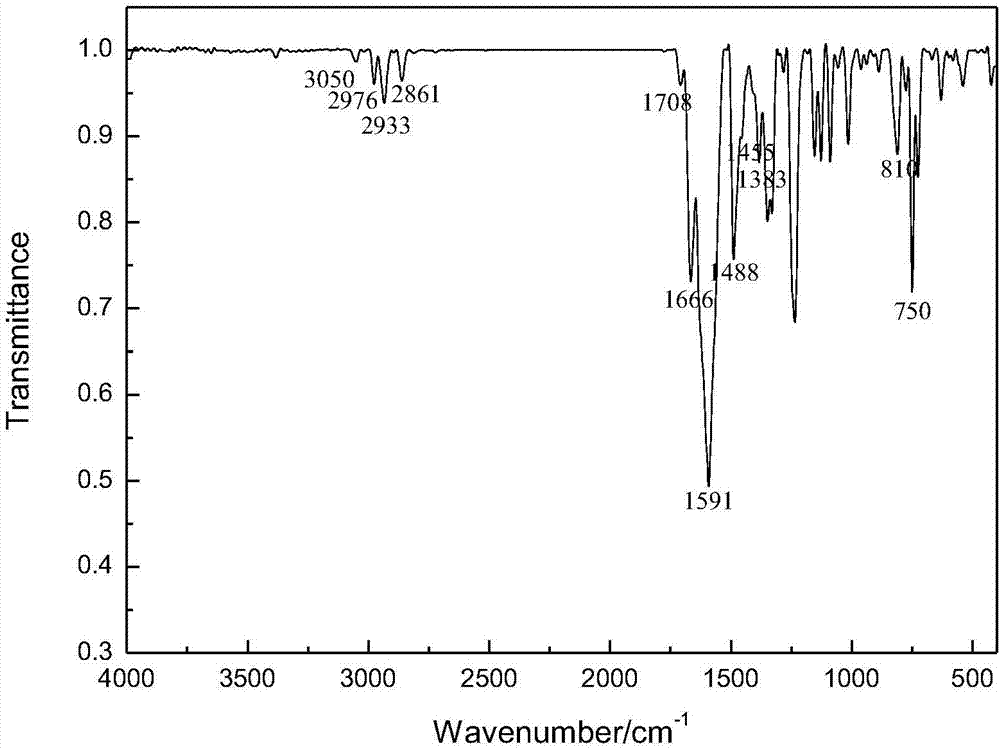
图2是本发明实施例2制备的1-吩噻嗪基-3-(4-氯苯基)-4-乙酰基-1,5-己二酮的红外图谱,由图2可知:3050cm-1处为ar-h的振动吸收峰,而在2976cm-1、1383cm-1处为-ch3的吸收峰,在2933cm-1、1455cm-1处为-ch2的吸收峰,在1708cm-1、1666cm-1处的峰为c=o的特征吸收峰,1591cm-1和1488cm-1处的峰为苯环的呼吸振动吸收峰,750cm-1为苯环上的邻二取代的吸收峰,810cm-1为苯环上对位取代的吸收峰。综上所述,可以证实合成得到了1-吩噻嗪基-3-(4-氯苯基)-4-乙酰基-1,5-己二酮。
图5是本发明实施例2制备的1-吩噻嗪基-3-(4-氯苯基)-4-乙酰基-1,5-己二酮的1hnmr图谱,由图5可知:1hnmr:6.66-7.19(m,12h,ar-h),2.60-2.62(d,2h,coch2),3.62-3.67(m,1h,ch),2.11(s,3h,coch3).
实施例3
称取0.002mol乙酰丙酮和0.0015mol无水k2co3于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(4-溴苯基)-丙烯酮,研磨33min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得灰绿色粉末,即为1-吩噻嗪基-3-(4-溴苯基)-4-乙酰基-1,5-己二酮。产率为:86.5%,m.p.173℃~176℃。
图3是本发明实施例3制备的1-吩噻嗪基-3-(4-溴苯基)-4-乙酰基-1,5-己二酮的红外图谱,由图3可知:3051cm-1处为ar-h的振动吸收峰,而在2976cm-1、1383cm-1处为-ch3的吸收峰,在2934cm-1、1442cm-1处为-ch2的吸收峰,在1716cm-1、1650cm-1处的峰为c=o的特征吸收峰,1558cm-1和1471cm-1处的峰为苯环的呼吸振动吸收峰,736cm-1为苯环上的邻二取代的吸收峰,805cm-1为苯环上对位取代的吸收峰。综上所述,可以证实合成得到了1-吩噻嗪基-3-(4-溴苯基)-4-乙酰基-1,5-己二酮。
图6是本发明实施例3制备的1-吩噻嗪基-3-(4-溴苯基)-4-乙酰基-1,5-己二酮的1hnmr图谱,由图6可知:1hnmr:6.30-7.42(m,12h,ar-h),2.60-2.66(d,2h,coch2),3.54-3.71(m,1h,ch),2.05(s,3h,coch3).
实施例4
称取0.002mol乙酰丙酮和0.0015mol无水k2co3于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(4-二甲氨基苯基)-丙烯酮,研磨36min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得黄色粉末,即为1-吩噻嗪基-3-(4-二甲氨基苯基)-4-乙酰基-1,5-己二酮。产率为:85.3%,m.p.152℃~155℃。
ir(kbr)ν(cm-1):3068(=c-h,ar-h),2981,1385(-ch3),1733,1708(c=o),1595,1468(ar),738(苯环上邻二取代),817(苯环上对位取代).
1hnmr:6.51-7.04(m,12h,ar-h),2.64-2.66(d,2h,coch2),3.50-3.72(m,1h,ch),2.12(s,3h,coch3),2.90(s,3h,nch3).
实施例5
称取0.002mol乙酰丙酮和0.0015mol无水k2co3于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(4-甲氧基苯基)-丙烯酮,研磨34min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得浅黄色粉末,即为1-吩噻嗪基-3-(4-甲氧基苯基)-4-乙酰基-1,5-己二酮。产率为85.7%,m.p.116℃~118℃。
ir(kbr)ν(cm-1):3057(=c-h,ar-h),2975,1395(-ch3),2934,1439(-ch2),1738,1653(c=o),1591,1463(ar),742(苯环上邻二取代),815(苯环上对位取代).
1hnmr:6.47-7.11(m,12h,ar-h),2.62-2.64(d,2h,coch2),3.53-3.82(m,1h,ch),2.11(s,3h,coch3),3.82(s,3h,och3)
实施例6
称取0.002mol乙酰丙酮和0.0015mol无水k2co3于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(4-甲基苯基)-丙烯酮,研磨32min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得棕色粉末,即为1-吩噻嗪基-3-(4-甲基苯基)-4-乙酰基-1,5-己二酮。产率为:85.8%,m.p.114℃~116℃。
ir(kbr)ν(cm-1):3057(=c-h,ar-h),2981,1394(-ch3),1697,1668(c=o),1593,1463(ar),743(苯环上邻二取代),817(苯环上对位取代).
1hnmr:6.63-7.12(m,12h,ar-h),2.63-2.65(d,2h,coch2),3.52-3.76(m,1h,ch),2.08(s,3h,coch3),2.45(s,3h,ch3).
实施例7
称取0.0018mol乙酰丙酮和0.0014mol无水k2co3于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(4-硝基苯基)-丙烯酮,研磨38min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得淡黄色粉末,即为1-吩噻嗪基-3-(4-硝基苯基)-4-乙酰基-1,5-己二酮。产率为89.2%,m.p.108℃~110℃。
ir(kbr)ν(cm-1):3058(=c-h,ar-h),2982,1383(-ch3),1705,1665(c=o),1591,1462(ar),742(苯环上邻二取代),818(苯环上对位取代).
1hnmr:6.56-8.00(m,12h,ar-h),2.65-2.68(d,2h,coch2),3.61-3.76(m,1h,ch),2.14(s,3h,coch3).
实施例8
称取0.0012mol乙酰丙酮和0.0011mol无水k2co3于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(4-氟苯基)-丙烯酮,研磨31min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得淡黄色粉末,即为1-吩噻嗪基-3-(4-氟苯基)-4-乙酰基-1,5-己二酮。产率为:87.8%,m.p.162℃~164℃。
ir(kbr)ν(cm-1):3059(=c-h,ar-h),2972,1380(-ch3),2931,1440(-ch2),1706,1662(c=o),1593,1462(ar),748(苯环上邻二取代),816(苯环上对位取代).
1hnmr:6.57-7.12(m,12h,ar-h),2.58-2.61(d,2h,coch2),3.72-3.80(m,1h,ch),2.12(s,3h,coch3).
实施例9
称取0.002mol乙酰丙酮和0.0015molnaoh于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(2-噻吩基)-丙烯酮,研磨39min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得淡黄色粉末,即为1-吩噻嗪基-3-(2-噻吩基)-4-乙酰基-1,5-己二酮。产率为:86.0%,m.p.120℃~123℃。
ir(kbr)ν(cm-1):3050(=c-h,ar-h),2976,1382(-ch3),2930,1452(-ch2),1702,1650(c=o),1593,1476(ar),750(苯环上邻二取代).
1hnmr:6.57-7.01(m,8h,ar-h),2.65-2.66(d,2h,coch2),3.62-3.76(m,1h,ch),2.08(s,3h,coch3),7.01(d,1h,thy-h),6.73(m,1h,thy-h).
实施例10
称取0.002mol乙酰丙酮和0.0013molnaoh于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(2-吡啶基)-丙烯酮,研磨30min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得棕色粉末,即为1-吩噻嗪基-3-(2-吡啶基)-4-乙酰基-1,5-己二酮。产率为87.5%,m.p.125℃~127℃。
ir(kbr)ν(cm-1):3053(=c-h,ar-h),2976,1385(-ch3),2931,1442(-ch2),1714,1669(c=o),1583,1471(ar),738(苯环上邻二取代).
1hnmr:6.58-6.93(m,8h,ar-h),2.61-2.64(d,2h,coch2),3.57-3.77(m,1h,ch),2.07(s,3h,coch3),7.28-7.54(d,1h,py-h),7.70-7.76(m,2h,py-h),7.92-7.94(d,1h,py-h).
实施例11
称取0.0015mol乙酰丙酮和0.0012molnaoh于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(2-呋喃基)-丙烯酮,研磨40min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得棕色粉末,即为1-吩噻嗪基-3-(2-呋喃基)-4-乙酰基-1,5-己二酮。产率为:86.2%,m.p.122℃~124℃。
ir(kbr)ν(cm-1):3058(=c-h,ar-h),2872,1388(-ch3),2925,1437(-ch2),1714,1680(c=o),1591,1463(ar),1126,1039(c-o-c),743(苯环上邻二取代).
1hnmr:6.58-7.01(m,8h,ar-h),2.58-2.62(d,2h,coch2),3.51-3.76(m,1h,ch),2.09(s,3h,coch3),5.83-5.90(d,1h,fu-h),6.29-6.32(m,1h,fu-h),7.22-7.28(d,1h,fu-h).
实施例12
称取0.001mol乙酰丙酮和0.001molnaoh于干燥的研钵中,迅速将其混合均匀,再加入0.001mol1-吩噻嗪基-3-(3-硝基苯基)-丙烯酮,研磨35min。研磨过程中,混合物会逐渐变黏,继续研磨直至物质不再发生变化,使用tlc跟踪监测反应进程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚的混合溶剂,待反应结束后,用纯净水对产物进行多次水洗抽滤,直到滤液的ph呈中性,然后将滤饼自然风干,得灰色粉末,即为1-吩噻嗪基-3-(3-硝基苯基)-4-乙酰基-1,5-己二酮。产率为88.3%,m.p.114℃~117℃。
ir(kbr)ν(cm-1):3057(=c-h,ar-h),2973,1387(-ch3),2927,1440(-ch2),1708,1648(c=o),1593,1463(ar),743(苯环上邻二取代).
1hnmr:6.56-8.02(m,12h,ar-h),2.65-2.68(d,2h,coch2),3.57-3.89(m,1h,ch),2.08(s,3h,coch3).
除上述实施例外,原料1-吩噻嗪基-3-芳基-丙烯酮还可采用以下物质,其中ar为邻硝基苯基、羟基苯基、苯乙烯基等;在此不一一列举。
另外,本发明中的1-吩噻嗪基-3-芳基-丙烯酮可采用以下方法制备:
向250ml干燥的三口烧瓶中添加10-乙酰基吩噻嗪(1.21g,0.005mol)、naoh颗粒(0.24g,0.006mol)和无水甲醇15ml,室温下搅拌10min,滴加芳香醛(0.006mol)的无水甲醇溶液10ml,回流反应30min(tlc监测所述反应进程)。反应结束后冷却至室温,将所得反应液于40ml冰水中析出全部固体,抽滤,滤饼用冰水洗涤,自然风干,再用无水甲醇对其进行重结晶,即得到得1-吩噻嗪基-3-芳基-丙烯酮。其反应方程式如下:
其中ar为苯基、对氯苯基、对溴苯基、对氟苯基、甲基苯基、甲氧基苯基、对硝基苯基、间硝基苯基、邻硝基苯基、二甲氨基苯基、羟基苯基、苯乙烯基、呋喃基、噻吩基或吡啶基。
本发明采用固相研磨法,由乙酰丙酮和1-吩噻嗪基-3-芳基-丙烯酮反应,合成了一系列未见文献报道的新的michael加成产物,即1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮,并探索了其制备方法,同时优化了实验条件,缩短了反应时间,为绿色合成做出了贡献。本发明提供的1-吩噻嗪基-3-芳基-4-乙酰基-1,5-己二酮是一系列全新的含有吩噻嗪基的酮类衍生物,具有杀菌、抑菌等功效,在抗菌、抗病毒等领域有很好的应用前景。
以上所述,仅是本发明的较佳实施例,并非对本发明作任何限制,凡是根据本发明技术实质对以上实施例所作的任何简单修改、变更以及等效结构变换,均仍属于本发明技术方案的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种具有上转换发光可调的9-乙酰基蒽共晶材料及其制备方法
- N-苯磺酰基-3-乙酰基吲哚酰腙类化合物、制备方法及应用
- N-苯磺酰基-3-(2-基-乙酰基)-6-甲基吲哚类衍生物的用图
- 一种黑霉菌生产(s)-乙酰基噻吩的方法
- 用于治疗皮肤病的甲酰基肽受体2的激动剂的用图
- 1-(1’,3’,4’,6’-四-o-乙酰基-d-葡萄糖)-4-对位取代芳基-[1,2,3]-三唑及制法和应用
- 一种从红豆杉枝叶中分离提纯10-去乙酰基巴卡亭iii的方法
- 一种从红豆杉中提取分离10-去乙酰基巴卡丁ⅲ(10-dab ⅲ)的方法
- 乙酰基澳泽兰素在制备抗肿瘤药物中的应用
- 包含艾地苯醌、n-乙酰基-s-法呢基-l-半胱氨酸和麦角硫因的制剂及其用图