一种喷他佐辛中间体的制备方法与流程
本发明涉及一种喷他佐辛中间体的制备方法,属于化学合成技术领域。
背景技术:
喷他佐辛,化学名为(2r,6r,11r)-顺式-1,2,3,4,5,6-六氢-6,11-二甲基-3-(3-甲基-2-丁烯基)-2,6-甲撑-3-苯并吖辛因-8-醇,其结构是如下:
由1967年由英国斯德林温斯洛伯集团研制成功上市,喷他佐辛是苯并吗啡烷的衍生物,对阿片受体兼有混合物的激动和拮抗作用,主要激动阿片κ受体,较大剂量时可激动σ受体,对μ受体具有部分激动或较弱的拮抗作用。喷他佐辛适用于中至重度疼痛的镇痛,临床应用广泛,如术中辅助镇痛、术后镇痛、慢性疼痛治疗、癌痛治疗等均可适用。用于口服的喷他佐辛片剂,是目前唯一可口服的阿片受体激动拮抗镇痛剂。
近几年,几家国内药业公司研制成功,并逐渐开始使用。国内几家药企制备的方法如下:
1、以3,4-二甲基吡啶为原料,与碘甲烷与对甲氧基苄基氯化镁缩合,再经还原、环合后,进行保护性酰化、脱甲基和水解去保护得到关键中间体,最后与二甲基溴丙烯反应即得。
2、以氰乙酸为原料,与丁酮发生加成,再经过加氢、缩合后,自身在酸的条件下,进行环合反应,得到关键中间体,最后与4-溴-2-甲基-丁烯反应即得喷他佐辛。
目前,国内合成的路线使用易制爆物质以及高压等条件,收率低,难以工业化生产。
随着不对称化学的发展,各种手性催化剂开始应用于喷他佐辛的合成,日本的m.kitamura等人采用催化剂进行不对称氢化反应,生成单一构型的异构体。该工艺路线存在反应压力要求高,催化剂不易制备的缺点,很难应用于工业化生产。
1993年,yvesgenisson等人运用手性吡啶盐与格式试剂进行立体控制烷基化反应,合成出喷他佐辛的关键中间体(+)normetazocine,此路线关键步骤吡啶盐的不对称烷基化收率只有40%,而且ee值为82%(91%:9%),起始原料原料2,4-二硝基苯胺属于易爆物质。
2012年,qiangchen等人运用asa-prins环化和分子内的friedel-crafts反应进行了不对称合成,但此不对称合成的是混合物含有对应异构体,且路线步骤多,收率低,用到了金属钠、正丁基锂等危险品。
技术实现要素:
本发明的主要目的是为了提供一种喷他佐辛中间体的制备方法,解决目前喷他佐辛制备方法存在的收率低及资源浪费高的问题,通过简单的方法得到关键中间体,收率高,工艺简单,适用于工业化生产,节约资源,降低了生产成本。
本发明的目的可以通过采用如下技术方案达到:
一种喷他佐辛中间体的制备方法,制备的喷他佐辛中间体如式(1)所示:
其制备过程的反应方程式如式(2)所示:
其制备过程包括如下步骤:
步骤1:甲基化反应
化合物1在丙酮介质中,反应得到化合物2;
步骤2:开环反应
化合物2中加入浓盐酸、氯化钠溶液,反应得到化合物3;
步骤3:还原反应
化合物3在乙醇介质中,反应得到化合物4;
步骤4:保护反应
化合物4在二氯甲烷介质中,反应得到化合物5;
步骤5:取代-还原反应
化合物5在n,n-二甲基甲酰胺介质中,调酸得到化合物6;
步骤6:酯化反应
化合物6在二氯甲烷介质中,反应得到化合物7;
步骤7:消去反应
化合物7在n,n-二甲基甲酰胺介质中,反应得到化合物8;
步骤8:肼解反应
化合物8在乙醇介质中,氮气保护,反应得到化合物9;
步骤9:关环反应
化合物9加入水,调节ph反应得到化合物10;
步骤10:缩合-脱甲基反应
化合物10和48%hbr,在140℃左右,反应20h,得到化合物11。
进一步的,步骤1中,化合物1在丙酮介质中,加入碳酸钾、碘甲烷,在50℃下,反应得到化合物2,化合物1与碘甲烷的摩尔比为1:1.3-1.5,其中,碘甲烷也可以用硫酸二甲酯替代。
进一步的,步骤2中,化合物2中加入浓盐酸、氯化钠溶液,在50℃下,反应得到化合物3,化合物2与盐酸的摩尔比为1:2.0-2.5,其中,浓盐酸可以用磷酸、硫酸和硝酸中的一种替代。
进一步的,步骤3中,化合物3在乙醇介质中,分批次加入硼氢化钠,控制温度在0-5℃,反应得到化合物4,化合物3与硼氢化钠的摩尔比为1:0.5-0.8。
进一步的,步骤4中,化合物4在二氯甲烷介质中,加入三乙胺、三甲基氯硅烷,控制温度在0-5℃,反应得到化合物5,化合物4分别与三甲基氯硅烷和三乙胺的摩尔比为1:1.1-1.3:2.0-2.5;其中,三甲基氯硅烷可以用叔丁基二甲基氯硅烷替代;三乙胺可以用其它吡啶、n,n-二异丙基乙胺等其中一种替代。
进一步的,步骤5中,化合物5、邻苯二甲酰胺钾盐和四丁基溴化铵在n,n-二甲基甲酰胺介质中,控制温度在60℃反应过夜,调酸得到化合物6,化合物5与邻苯二甲酰胺钾盐的摩尔比为1:1-1.05。
进一步的,步骤6中,化合物6在二氯甲烷介质中,加入三乙胺、甲基磺酰氯,控制温度在0℃,反应得到化合物7,化合物6与甲基磺酰氯的摩尔比为1:1.2-1.3。
进一步的,步骤7中,化合物7在n,n-二甲基甲酰胺介质中,加入碳酸钾和溴化锂,控制温度在105℃,反应得到化合物8,化合物7与碳酸钾与溴化锂的摩尔比为1:1.5-2.0:1.0-1.1;碳酸钾可以用碳酸钠替代,溴化锂可以用溴化钠、氯化锂或者氯化钠中的一种替代。
进一步的,步骤8中,化合物8在乙醇介质中,氮气保护,加入水合肼,加热回流,反应得到化合物9,化合物8与水合肼的摩尔比为1:1.0-1.1。
进一步的,步骤9中,化合物9加入水,调节ph6-7,在90-95℃回流反应得到化合物10,化合物9a如式(3)所示:
其中,化合物9与化合物9a的摩尔比为1.0:1.4-1.5;
在步骤10中,化合物10与48%溴化氢的质量比为1:10-12。
本发明的有益技术效果:
1、本发明提供的喷他佐辛中间体的制备方法,为克服现有技术中存在的问题,采用简单的合成方法,合成化合物9,然后经过缩合环合反应得到关键中间体化合物11,成本低,工艺简单,收率高且产品纯度高达98%。
2、本路线共十步,如下列步骤所示,整个工艺路线原料便宜易得,成本低,工艺简单,操作方便,总收率高;本发明避免高压反应,得到的化合物9的纯度达到97%以上,本步骤收率也能达到95%以上;本发明整个工艺路线简洁,原料便宜易得,成本低,反应条件温和,操作简便。
附图说明
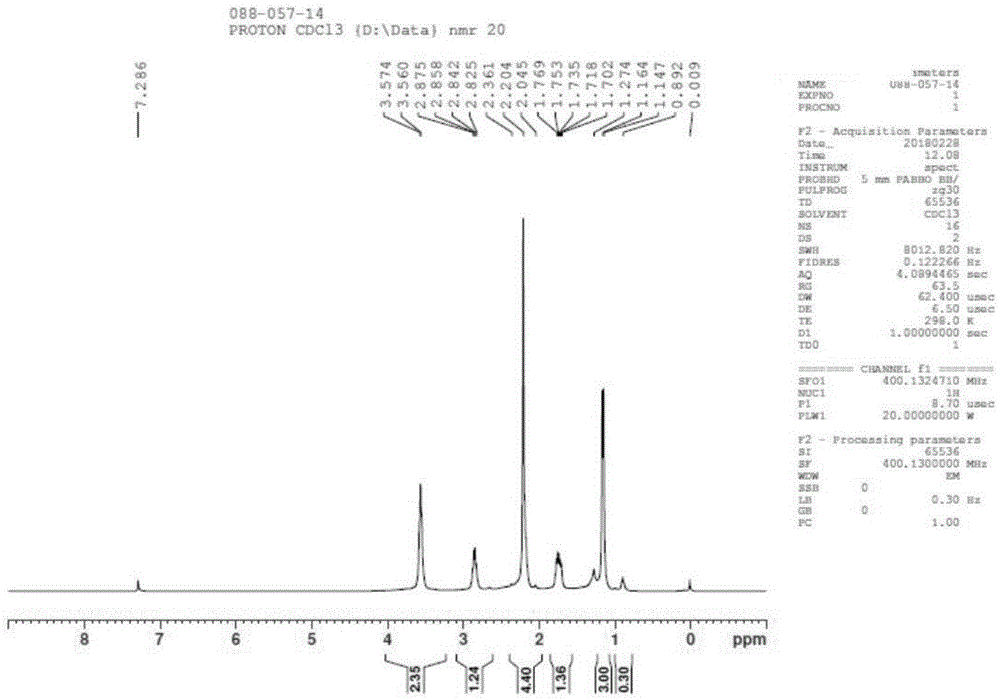
图1为本发明的化合物3的1hnmr图谱;
图2为本发明的化合物5的1hnmr图谱;
图3为本发明的化合物8的1hnmr图谱;
图4为本发明的化合物9纯度的gc图谱;
图5为本发明的化合物10的1hnmr图谱;
图6为本发明的化合物11的1hnmr图谱;
图7为本发明的化合物11纯度的hplc图谱。
具体实施方式
为使本领域技术人员更加清楚和明确本发明的技术方案,下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
本实施例提供的喷他佐辛中间体的制备方法,制备的喷他佐辛中间体如式(1)所示:
其制备过程的反应方程式如式(2)所示:
其制备过程包括如下步骤:
步骤1:甲基化反应
化合物1在丙酮介质中,加入碳酸钾、碘甲烷,在50℃下,反应得到化合物2,化合物1与碘甲烷的摩尔比为1:1.3-1.5,其中,碘甲烷也可以用硫酸二甲酯替代;
步骤2:开环反应
化合物2中加入浓盐酸、氯化钠溶液,在50℃下,反应得到化合物3,化合物2与盐酸的摩尔比为1:2.0-2.5,其中,浓盐酸可以用磷酸、硫酸和硝酸中的一种替代;
步骤3:还原反应
化合物3在乙醇介质中,分批次加入硼氢化钠,控制温度在0-5℃,反应得到化合物4,化合物3与硼氢化钠的摩尔比为1:0.5-0.8;
步骤4:保护反应
化合物4在二氯甲烷介质中,加入三乙胺、三甲基氯硅烷,控制温度在0-5℃,反应得到化合物5,化合物4分别与三甲基氯硅烷和三乙胺的摩尔比为1:1.1-1.3:2.0-2.5;其中,三甲基氯硅烷可以用叔丁基二甲基氯硅烷替代;三乙胺可以用其它吡啶、n,n-二异丙基乙胺等其中一种替代;
步骤5:取代-还原反应
化合物5、邻苯二甲酰胺钾盐和四丁基溴化铵在n,n-二甲基甲酰胺介质中,控制温度在60℃反应过夜,调酸得到化合物6,化合物5与邻苯二甲酰胺钾盐的摩尔比为1:1-1.05;
步骤6:酯化反应
化合物6在二氯甲烷介质中,加入三乙胺、甲基磺酰氯,控制温度在0℃,反应得到化合物7,化合物6与甲基磺酰氯的摩尔比为1:1.2-1.3;
步骤7:消去反应
化合物7在n,n-二甲基甲酰胺介质中,加入碳酸钾和溴化锂,控制温度在105℃,反应得到化合物8,化合物7与碳酸钾与溴化锂的摩尔比为1:1.5-2.0:1.0-1.1;碳酸钾可以用碳酸钠替代,溴化锂可以用溴化钠、氯化锂或者氯化钠中的一种替代;
步骤8:肼解反应
化合物8在乙醇介质中,氮气保护,加入水合肼,加热回流,反应得到化合物9,化合物8与水合肼的摩尔比为1:1.0-1.1;
步骤9:关环反应
化合物9加入水,调节ph6-7,在90-95℃回流反应得到化合物10,化合物9a如式(3)所示:
其中,化合物9与化合物9a的摩尔比为1.0:1.4-1.5;
步骤10:缩合-脱甲基反应
化合物10和48%hbr,在140℃左右,反应20h,得到化合物11,化合物10与48%溴化氢的质量比为1:10-12。
按照上述方法,本发明提供如下实施例:
实施例1:
步骤1:向3l四口瓶中,加入化合物1(200g),丙酮(2l),搅拌,加入碳酸钾(280.1g,1.3eq),搅拌,再加入碘甲烷(288.2g、1.3eq),升温至50℃(微回流),保温16h,gc取样检测:原料<2%;后处理:过滤,固体用少量丙酮(200ml)洗涤两次,旋干丙酮,加入水(800ml)+乙酸乙酯(800ml),搅拌,静置分层,水相再用乙酸乙酯(800ml)萃取一次,有机相合并,有机层用饱和nacl(600ml)洗涤一次,无水硫酸钠干燥,旋干得199g液体化合物2;收率:90%;
步骤2:化合物2(200g,1.0eq),加入浓盐酸(286ml,2.0eq),再加入200ml15%的nacl溶液,加热至50度反应,约4h取样,送样gc,后处理:直接蒸馏反应液,常压蒸水,带出产品,蒸出产品约154g黄绿色油状物化合物3,收率:81.5%;
步骤3:1000ml三口瓶,加入化合物3(50g,1.0eq),500ml95%的乙醇做溶剂,降温至0度左右,分批加入nabh4固体(7.1g,0.5eq),保持0-5度反应;加完后,反应约1-2h;点板检测:pe:ea=10:1,后处理:冰浴下0-5度,2nhcl淬灭反应,调节ph=4-5,加入500mldcm和500ml水,萃取,水相用dcm萃一次,合并有机相,水洗两次,干燥,浓缩,称得油状物化合物4(45g),约90%收率;放置会使颜色变深;
步骤4:化合物4(45g,1.0eq)加入到dcm450ml中,冷却至0度左右,滴加tea(66.6g,2.0eq),控制在0度,滴加完毕后,滴加tmscl(42.98g,1.2eq),滴完后,保温0-5度反应1h,点板检测:pe:ea=10:1,后处理:加入400ml水和200mldcm,0度下搅拌10min,分液,有机相水洗两次,干燥,浓缩,得到57g黄色油状物化合物5,约86.5%收率;
步骤5:2000ml三口瓶,化合物5(150g,1.0eq),邻苯二甲酰胺钾盐(133.1g,1.2eq)和tbab(15g,10%质量比)加入到dmf(750ml)5vol中;加热至内温60度左右反应过夜;送样hplc,后处理,冷却至室温,加入2volmtbe和2vol水,搅拌10min,分液,水相用mtbe萃取一次,合并有机相,水洗一次;半饱和nacl溶液洗两次,再用1n的hcl溶液洗一次;再用mtbe萃一次,合并有机相,干燥,浓缩得到脱完tms的产品,约148g油状物粗品化合物6,收率83%;
步骤6:2000ml三口瓶,氮气保护,化合物6(145g,1.0eq))加入到dcm(900ml)中,冷却至0度,加入tea(118.5g,2.0eq),保持温度0度,滴加mscl(80.6g,1.2eq),滴加完毕后,保持0度左右反应,约3h送样hplc,后处理,加水淬灭反应,分液,水相用dcm萃一次,合并有机相,1n的hcl溶液洗一次,饱和碳酸氢钠溶液洗一次,半饱和nacl溶液洗一次,干燥,浓缩得油状物190g粗品化合物7;
步骤7:2000ml反应瓶,加入化合物7(190g,1.0eq),dmf(1000ml)溶解搅拌,再加入碳酸钾(120.8g,1.5eq)和libr(1.0eq,50.2g),升温至105度反应(反应过程中体系较粘,不太好搅);反应约3h送样有中间态,再延长2h;后处理:加入mtbe1000ml和水1000ml,搅拌10min,分液,水相用mtbe萃一次,有机相合并,水洗一次,半饱和nacl溶液洗两次,干燥,浓缩得油状物120g粗品化合物8,约88%收率;
步骤8:1000ml三口瓶,化合物8(57g,1.0eq),95%乙醇(570ml)搅拌均匀,氮气保护,再滴加80%水合肼(15.6g,1.0eq),加热至回流,内温80度左右反应;后处理,冷却至0度左右,加入20%的naoh溶液300ml,搅拌15min,再加入300mlmtbe一起搅拌10min,再加水300ml,分液,水相用mtbe100ml再萃取一次,有机相合并,用饱和nacl溶液洗两次,有机相干燥,滴加4mol/l的hcl/etoh80ml(0.25mol)成盐,旋干反应液,约得34g成盐产品化合物9,粗品收率接近理论量,收率100%;
步骤9:化合物9盐酸盐(90g,1.0eq),加入水(900ml)作溶剂,搅拌,滴加20%的naoh溶液调节ph=6-7左右,加入193.5g化合物9a(1.4eq),升温至90-95度左右,回流反应;保温过夜反应,送样点板显示,原料存在,继续保温反应,共反应约48h;点板观察原料基本消失,反应完全;后处理,降温至60度左右,加入25%活性炭(约20g),搅拌30min,热过滤,再用10%的活性炭(8g)搅拌30min,热过滤,滤液用20%的naoh溶液调节ph至10左右,500mldcm萃取反应液两次,有机相水洗一次,干燥,浓缩得粗品75g左右;结晶:向粗品中加入异丙醚,室温打浆约2h;抽滤,得到37.4g类白色固体化合物10,约31%收率;
步骤10:将化合物10(100g,1eq)、48%hbr(1000g)依次加入到2l的反应瓶中,升温至外温140℃左右,内温120-125℃;升温结束,在此温度下保温20-24h,hplc监控反应,反应结束,关闭加热,降至室温25℃;加入水1000ml,加入甲苯:正丁醇=2:1混合液700ml,用30%氢氧化钠213g调ph,再用氨水(约300ml)调ph至12;note:氢氧化钠调ph时需控温至15℃以下,氨水调ph时升至室温;分液,水相用700ml*2甲苯:正丁醇=2:1萃取两次,合并有机相;饱和氯化钠700ml洗1次,分层,收集有机相,无水硫酸钠干燥;真空旋干甲苯及正丁醇,得到粗品;note:真空旋干甲苯后期加入适当甲醇帶蒸;加入甲醇50ml,升温至75℃回流0.5h;note:回流期间体系无法溶清;滴入350ml丙酮(约0.5h滴完),滴毕,缓慢将至室温,保温1.0h;抽滤,滤饼用甲醇:丙酮=1:780ml淋洗2次,45℃鼓风干燥,得产品40g,hplc:98.28%,含量:98.24%,收率:45%。
实施例2:
步骤1:向四口瓶中,加入化合物1(2000g),丙酮(20l),搅拌,加入碳酸钾(2801g,1.3eq),搅拌,再加入碘甲烷(2883g、1.3eq),升温至50℃(微回流),保温16h,gc取样检测,;后处理:过滤,固体用少量丙酮(2000ml)洗涤两次,旋干丙酮,加入水(8000ml)+乙酸乙酯(8000ml),搅拌,静置分层,水相再用乙酸乙酯(8000ml)萃取一次,有机相合并,有机层用饱和nacl(6000ml)洗涤一次,无水硫酸钠干燥,旋干得1997g液体化合物2;收率:95%;
步骤2:化合物2(400g,1.0eq),加入浓盐酸(500ml,2.0eq),再加入400ml15%的nacl溶液,加热至50度反应,约4h取样,送样gc,后处理:直接蒸馏反应液,常压蒸水,带出产品,蒸出产品约154g黄绿色油状物化合物3,收率.:90%;
步骤3:向三口瓶中,加入化合物3(200g,1.0eq),2000ml95%的乙醇做溶剂,降温至0度左右,分批加入nabh4固体(28g,0.5eq),保持0-5度反应;加完后,反应约1-2h;点板检测:pe:ea=10:1,后处理:冰浴下0-5度,2nhcl淬灭反应,调节ph=4-5,加入1000mldcm和1000ml水,萃取,水相用dcm萃一次,合并有机相,水洗两次,干燥,浓缩,称得油状物化合物4(184g),95%收率;放置会使颜色变深;
步骤4:化合物4(100g,1.0eq)加入到dcm1000ml中,冷却至0度左右,滴加tea(147.5g,2.0eq),控制在0度,滴加完毕后,滴加tmscl(95.5g,1.2eq),滴完后,保温0-5度反应1h,点板检测:pe:ea=10:1,后处理:加入800ml水和400mldcm,0度下搅拌10min,分液,有机相水洗两次,干燥,浓缩,得到137g黄色油状物化合物5,约90%收率;
步骤5:向三口瓶中,化合物5(500g,1.0eq),邻苯二甲酰胺钾盐(444g,1.0eq)和tbab(50g,10%质量比)加入到dmf(2500ml)中;加热至内温60度左右反应过夜;送样hplc,后处理,冷却至室温,加入mtbe和水,搅拌10min,分液,水相用mtbe萃取一次,合并有机相,水洗一次;半饱和nacl溶液洗两次,再用1n的hcl溶液洗一次;再用mtbe萃一次,合并有机相,干燥,浓缩得到脱完tms的产品,约534g油状物粗品化合物6,收率90%;
步骤6:在三口瓶中,氮气保护,化合物6(500g,1.0eq))加入到dcm(3000ml)中,冷却至0度,加入tea(408g,2.0eq),保持温度0度,滴加mscl(278g,1.2eq),滴加完毕后,保持0度左右反应,约3h送样hplc,后处理,加水淬灭反应,分液,水相用dcm萃一次,合并有机相,1n的hcl溶液洗一次,饱和碳酸氢钠溶液洗一次,半饱和nacl溶液洗一次,干燥,浓缩得油状物658g粗品化合物7,收率100%;
步骤7:在反应瓶中,加入化合物7(500g,1.0eq),dmf(2500ml)溶解搅拌,再加入碳酸钾(318g,1.5eq)和libr(132g,1.0eq),升温至105度反应(反应过程中体系较粘,不太好搅);反应约3h送样有中间态,再延长2h;后处理:加入mtbe2000ml和水2000ml,搅拌10min,分液,水相用mtbe萃一次,有机相合并,水洗一次,半饱和nacl溶液洗两次,干燥,浓缩得油状物317g粗品化合物8,约90%收率;
步骤8:在三口瓶中,化合物8(100g,1.0eq),95%乙醇(1000ml)搅拌均匀,氮气保护,再滴加80%水合肼(27.5g,1.0eq),加热至回流,内温80度左右反应;后处理,冷却至0度左右,加入20%的naoh溶液800ml,搅拌15min,再加入800mlmtbe一起搅拌10min,再加水800ml,分液,水相用mtbe500ml再萃取一次,有机相合并,用饱和nacl溶液洗两次,有机相干燥,滴加4mol/l的hcl/etoh150ml成盐,旋干反应液,约得60g成盐产品化合物9,收率100%;
步骤9:化合物9盐酸盐(90g,1.0eq),加入水(900ml)作溶剂,搅拌,滴加20%的naoh溶液调节ph=6-7左右,加入193.5g化合物9a(1.4eq),升温至90-95度左右,回流反应;保温过夜反应,送样点板显示,原料存在,继续保温反应,共反应约48h;点板观察原料基本消失,反应完全;后处理,降温至60度左右,加入25%活性炭,搅拌30min,热过滤,再用10%的活性炭搅拌30min,热过滤,滤液用20%的naoh溶液调节ph至10左右,500mldcm萃取反应液两次,有机相水洗一次,干燥,浓缩得粗品;结晶:向粗品中加入异丙醚,室温打浆约2h;抽滤,得到37.4g类白色固体化合物10,约45%收率;
步骤10:将化合物10(500g,1eq)、48%hbr(5000g)依次加入到反应瓶中,升温至外温140℃左右,内温120-125℃;升温结束,在此温度下保温20-24h,hplc监控反应,反应结束,关闭加热,降至室温25℃;加入水5000ml,加入甲苯:正丁醇=2:1混合液3500ml,用30%氢氧化钠1000g调ph,再用氨水(约1500ml)调ph至12;note:氢氧化钠调ph时需控温至15℃以下,氨水调ph时升至室温;分液,水相用3500ml*2甲苯:正丁醇=2:1萃取两次,合并有机相;饱和氯化钠3000ml洗1次,分层,收集有机相,无水硫酸钠干燥;真空旋干甲苯及正丁醇,得到粗品;note:真空旋干甲苯后期加入适当甲醇帶蒸;加入甲醇50ml,升温至75℃回流0.5h;note:回流期间体系无法溶清;滴入2000ml丙酮(约0.5h滴完),滴毕,缓慢将至室温,保温1.0h;抽滤,滤饼用甲醇:丙酮=1:780ml淋洗2次,45℃鼓风干燥,得产品217g,hplc:98.28%,含量:98.24%,收率:50%。
实施例3:
步骤1:向四口瓶中,加入化合物1(400g),丙酮(4l),搅拌,加入碳酸钾(560g,1.3eq),搅拌,再加入碘甲烷(576g、1.3eq),升温至50℃(微回流),保温16h,gc取样检测,后处理:过滤,固体用少量丙酮(400ml)洗涤两次,旋干丙酮,加入水(1000ml)+乙酸乙酯(1000ml),搅拌,静置分层,水相再用乙酸乙酯(1000ml)萃取一次,有机相合并,有机层用饱和nacl(1000ml)洗涤一次,无水硫酸钠干燥,旋干得421g液体化合物2;收率:95%;
步骤2:化合物2(1000g,1.0eq),加入浓盐酸(1400ml,2.0eq),再加入1000ml15%的nacl溶液,加热至50度反应,约4h取样,送样gc,后处理:直接蒸馏反应液,常压蒸水,带出产品,蒸出产品约848g黄绿色油状物化合物3,收率:90%;
步骤3:向三口瓶中,加入化合物3(1000g,1.0eq),10l95%的乙醇做溶剂,降温至0度左右,分批加入nabh4固体(3.75g,0.5eq),保持0-5度反应;加完后,反应约1-2h;点板检测:pe:ea=10:1,后处理:冰浴下0-5度,2nhcl淬灭反应,调节ph=4-5,加入5ldcm和5l水,萃取,水相用dcm萃一次,合并有机相,水洗两次,干燥,浓缩,称得油状物化合物4(973g),95%收率;放置会使颜色变深;
步骤4:化合物4(500g,1.0eq)加入到dcm5000ml中,冷却至0度左右,滴加tea(737g,2.0eq),控制在0度,滴加完毕后,滴加tmscl(476g,1.2eq),滴完后,保温0-5度反应1h,点板检测:pe:ea=10:1,后处理:加入4000ml水和2000mldcm,0度下搅拌10min,分液,有机相水洗两次,干燥,浓缩,得到693g黄色油状物化合物5,约91%收率;
步骤5:三口瓶中,化合物5(1000g,1.0eq),邻苯二甲酰胺钾盐(888g,1.0eq)和tbab(100g,10%质量比)加入到dmf(5000ml)中;加热至内温60度左右反应过夜;送样hplc,后处理,冷却至室温,加入mtbe和水,搅拌10min,分液,水相用mtbe萃取一次,合并有机相,水洗一次;半饱和nacl溶液洗两次,再用1n的hcl溶液洗一次;再用mtbe萃一次,合并有机相,干燥,浓缩得到脱完tms的产品,约1067g油状物粗品化合物6,收率90%;
步骤6:在三口瓶中,氮气保护,化合物6(1000g,1.0eq))加入到dcm(6000ml)中,冷却至0度,加入tea(818g,2.0eq),保持温度0度,滴加mscl(556g,1.2eq),滴加完毕后,保持0度左右反应,约3h送样hplc,后处理,加水淬灭反应,分液,水相用dcm萃一次,合并有机相,1n的hcl溶液洗一次,饱和碳酸氢钠溶液洗一次,半饱和nacl溶液洗一次,干燥,浓缩得油状物1319g粗品化合物7,收率100%;
步骤7:在反应瓶中,加入化合物7(1000g,1.0eq),dmf(5000ml)溶解搅拌,再加入碳酸钾(638g,1.5eq)和libr(265g,1.0eq),升温至105度反应(反应过程中体系较粘,不太好搅);反应约3h送样有中间态,再延长2h;后处理:加入mtbe5000ml和水5000ml,搅拌10min,分液,水相用mtbe萃一次,有机相合并,水洗一次,半饱和nacl溶液洗两次,干燥,浓缩得油状物649g粗品化合物8,约92%收率;
步骤8:在三口瓶中,化合物8(500g,1.0eq),95%乙醇(570ml)搅拌均匀,氮气保护,再滴加80%水合肼(15.6g,1.0eq),加热至回流,内温80度左右反应;后处理,冷却至0度左右,加入20%的naoh溶液2000ml,搅拌15min,再加入2000mlmtbe一起搅拌10min,再加水3000ml,分液,水相用mtbe1000ml再萃取一次,有机相合并,用饱和nacl溶液洗两次,有机相干燥,滴加4mol/l的hcl/etoh800ml成盐,旋干反应液,约得294g成盐产品化合物9,收率100%;
步骤9:化合物9盐酸盐(90g,1.0eq),加入水(900ml)作溶剂,搅拌,滴加20%的naoh溶液调节ph=6-7左右,加入193.5g化合物9a(1.4eq),升温至90-95度左右,回流反应;保温过夜反应,送样点板显示,原料存在,继续保温反应,共反应约48h;点板观察原料基本消失,反应完全;后处理,降温至60度左右,加入25%活性炭,搅拌30min,热过滤,再用10%的活性炭搅拌30min,热过滤,滤液用20%的naoh溶液调节ph至10左右,5000mldcm萃取反应液两次,有机相水洗一次,干燥,浓缩得粗品;结晶:向粗品中加入异丙醚,室温打浆约2h;抽滤,得到413gg类白色固体化合物10,约45%收率;
步骤10:将化合物10(1kg)、48%hbr(10kg)依次加入到2l的反应瓶中,升温至外温140℃左右,内温120-125℃;升温结束,在此温度下保温20-24h,hplc监控反应,反应结束,关闭加热,降至室温25℃;加入水10l,加入甲苯:正丁醇=2:1混合液7l,用30%氢氧化钠2000g调ph,再用氨水(约3l)调ph至12;note:氢氧化钠调ph时需控温至15℃以下,氨水调ph时升至室温;分液,水相用7l*2甲苯:正丁醇=2:1萃取两次,合并有机相;饱和氯化钠700ml洗1次,分层,收集有机相,无水硫酸钠干燥;真空旋干甲苯及正丁醇,得到粗品;note:真空旋干甲苯后期加入适当甲醇帶蒸;加入甲醇500ml,升温至75℃回流0.5h;note:回流期间体系无法溶清;滴入4l丙酮(约0.5h滴完),滴毕,缓慢将至室温,保温1.0h;抽滤,滤饼用甲醇:丙酮=1:780ml淋洗2次,45℃鼓风干燥,得产品435g,hplc:98.28%,含量:98.24%,收率:50%。
图1为化合物3的1hnmr图谱;图2为化合物5的1hnmr图谱;图3为化合物8的1hnmr图谱;图4为化合物9纯度的gc图谱;图5为化合物10的1hnmr图谱;图6为化合物11的1hnmr图谱;图7为化合物11纯度的hplc图谱。
目前,市场上制备化合物9方法,纯度低,只能达到25-30%的纯度,将
以上所述,仅为本发明进一步的实施例,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明所公开的范围内,根据本发明的技术方案及其构思加以等同替换或改变,都属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!