一种绝经后骨质疏松的分子标记物的制作方法
本发明属于生物医药领域,涉及一种绝经后骨质疏松的分子标记物。
背景技术:
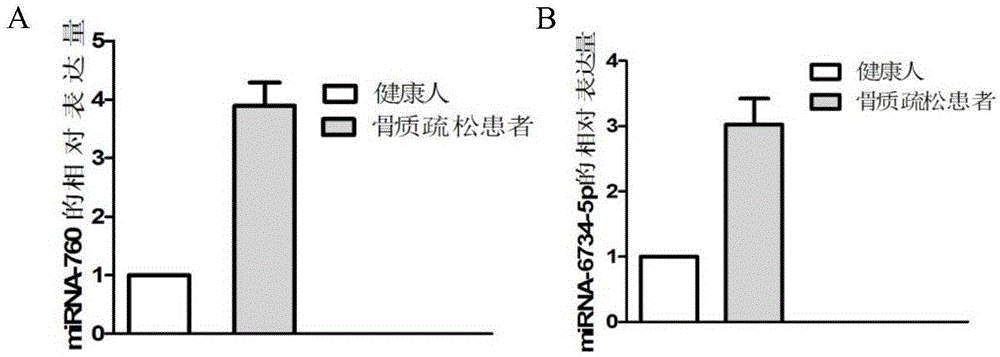
:骨质疏松症是一种以低骨量和骨组织微结构破坏为特征,导致骨质脆性增加和易于骨折的代谢性骨病,可分为原发性和继发性两类,继发性者的原发病因明确,常有内分泌代谢疾病(如甲亢、甲旁亢、性腺功能减退等)或全身性疾病(如器官移植术后、慢性肾功能衰竭、营养不良症等)引起。原发性者又可分为i型和ii型两类,i型即绝经后骨质疏松,发生于绝经后女性;ii型多见于60岁以上的老年人,女性的发病率是男性的2倍以上。随着全世界人口老年化的发展趋势,骨质疏松症患者群体将会愈发庞大,骨痛、骨折甚至丧失生活自理能力等骨质疏松并发症所带来的一些社会经济问题也愈发明显。因此,对于骨质疏松症的发生发展、治疗预防等研究具有重要意义。骨质疏松诊断金标准是双能x线吸收(dma)法测量骨密度(bmd)。dxa检查采用t值进行诊断,其测量的t值是将受试者的骨密度值与一个正常参考人群的平均峰值骨密度和标准差比较,国内骨质疏松诊疗指南推荐使用低于峰值骨量2.5标准差(-2.5sd)作为诊断标准。但是骨强度是由骨质量和bmd两方面决定,bmd仅是骨强度的一个方面,骨密度的变化是一个漫长的过程,需要半年到两年才会由dxa检测出来,而且bmd并不能为骨质疏松鉴别诊断提供更多的临床信息,其临床使用中也有着很大的局限性,因此bmd适合作为诊断而不适合作为治疗观察的指标。骨代谢生化标志物可从血液,尿液中检测出,是一些骨代谢的生化产物或相关的激素,骨代谢生化标志物可用于反映骨代谢平衡状态,是协助诊断、鉴别、治疗以及疗效评价代谢性骨病的重要指标(lingaiahs,morin-papunenl,piltonent,puurunenj,sundstrom-poromaai,stener-victorine,multi-centrestudy.etal.bonemarkersinpolycysticovarysyndrome:aclinicalendocrinology2017)。骨代谢标志物分为三种:①一般的生化标志物如血磷,血钙等等;②与骨代谢调控相关的激素类如甲状旁腺素(pth),维生素d等等;③骨转换标志物,包括骨形成标志物和骨吸收标志物。相对于bmd,骨代谢标志物更具优势(leej,vasikarans.currentrecommendationsforlaboratorytestinganduseofboneturnovermarkersinmanagementofosteoporosis.annalsoflaboratorymedicine2012;32(2):105-112)。microrna作为小型非编码rna族群中的重要一员,在生命活动中发挥着重要的作用。从最早揭示其存在,到现在随着科技领域的不断扩展和深入,人们发现microrna发挥着越来越多、错综复杂的生命调节作用,从生命过程的胚胎发育、生长发育、功能恢复、到疾病的发生演变、个体的衰老死亡均参与一系列调控机制。mirna与骨组织细胞关系密切,主要涉及四类细胞,成骨细胞、破骨细胞、骨细胞、软骨细胞,这些细胞正常运行时,维持骨形成和骨吸收之间的功能水平,从而保持正常的骨形态和功能。而由于各种原因导致的失衡,使得各种骨科疾病得以发生。因此,研究mirna与是骨骼组织细胞的关系能够为骨骼疾病研究提供新的思路,以及潜在的新的诊断标记物和药物靶标,这为骨骼疾病的治疗也提供了新的方向。技术实现要素:为了弥补现有技术的不足,本发明的目的之一在于提供一种可用于诊断绝经后骨质疏松的mirna标记物。相比传统的绝经后骨质疏松的诊断方法,使用mirna标记物来诊断绝经后骨质疏松更方便、快速、安全、经济。本发明的目的之二在于提供一种绝经后骨质疏松的分子靶标,为绝经后骨质疏松的个性化治疗提供了新的手段。为了实现上述目的,本发明采用了如下技术方案:本发明提供了检测mirna的试剂在制备诊断绝经后骨质疏松的产品中的应用,所述mirna为mirna-760。进一步,所述mirna还包括mirna-6734-5p。进一步,所述产品包括通过使用定量或数字pcr、测序、微阵列、luminex核酸测定法或其他基于杂交的技术来检测mirna的水平的试剂。进一步,与健康个体相比,所述mirna在骨质疏松患者中的水平上调。本发明提供了一种诊断绝经后骨质疏松的产品,所述产品包括检测mirna-760和/或mirna-6734-5p水平的试剂。进一步,所述产品包括芯片、阵列或试剂盒。本发明提供了mirna-760和/或mirna-6734-5p在制备治疗绝经后骨质疏松药物中的应用。进一步,所述药物包含mirna-760和/或mirna-6734-5p的抑制剂,所述抑制剂可以降低所述mirna的水平,和/或抑制或下调编码所述mirna的序列的表达或降解或切割所述mirna。进一步,所述抑制剂是所述mirna的反义寡核苷酸或拮抗剂。本发明提供了一种治疗绝经后骨质疏松的药物,所述药物包括mirna-760和/或mirna-6734-5p的抑制剂。所述抑制剂可以降低所述mirna的水平,和/或抑制或下调编码所述mirna的序列的表达或降解或切割所述mirna。本发明的优点和有益效果:本发明首次发现了mirna-760和mirna-6734-5p表达水平与绝经后骨质疏松的发生发展相关,通过检测受试者mirna-760和mirna-6734-5p的表达水平,可以判断受试者是否患有绝经后骨质疏松,或者是否存在患绝经后骨质疏松的风险。本发明发现了mirna-760和mirna-6734-5p与成骨分化相关,通过改变mirna-760和mirna-6734-5p的水平,可以改变骨髓间充质干细胞向成骨分化,提示mirna-760和mirna-6734-5p可作为分子靶标应用于绝经后骨质疏松的治疗。附图说明图1是利用qpcr检测mirna-760和mirna-6734-5p在绝经后骨质疏松患者中的表达情况图;其中,图a是mirna-760,图b是mirna-6734-5p;图2是检测mirna-760和mirna-6734-5p对hmscs成骨能力的影响图。具体实施方式本发明经过广泛而深入的研究,通过高通量测序方法,检测mirna在绝经后骨质疏松患者和正常人血液中的表达水平,通过生物信息学分析,发现其中呈现显著性差异表达的mirna,探讨其与骨质疏松发生发展之间的关系,从而为骨质疏松的早期诊断和治疗寻找更好的途径和方法。通过筛选,本发明首次发现了mirna-760和mirna-6734-5p在骨质疏松患者血液中的表达量显著高于正常人中,进一步细胞实验证明mirna-760和mirna-6734-5p与成骨分化相关。本发明为绝经后骨质疏松的研究以及绝经后骨质疏松的早期诊断和治疗提供了新的分子靶标和治疗靶点。在本发明中,“对照”、“对照样品”或“参考值”是可以在本文中互换使用的术语,并且应理解为用于与实验样品比较的样品或标准。对照可以包括从健康受试者或受试者获得的样品,其不具有发生骨质疏松的风险或患有骨质疏松。此外,对照也可以是标准参考值或值的范围,即比如样品中稳定表达的mirna,例如内源对照cel-mir-39。如本文所用,术语“microrna”或“mirna”或“mir”是指长度为约17至25个核苷酸的非编码rna分子,具体地具有17、18、19、20、21、22、23、24或25个核苷酸的长度,其与编码信使rna杂交并调节其表达。术语“mirna分子”是指代表mirna的任何核酸分子,包括天然mirna分子,即成熟mirna、pre-mirna、pri-mirna。“mir前体”、“pre-mirna”或“pre-mir”指具有发夹结构的非编码rna,其含有mirna。pre-mirna是通过称为drosha的双链rna特异性核糖核酸酶切割初级mi-rna转录物或“pri-mir”的产物。前体可以是相应多核苷酸的形式,因为它们在相应多核苷酸成熟期间出现。作为一种优选的实施方式,一种代表性的mirna的序列分别如seqidno.1(mirna-760)和seqidno.2(mirna-6734-5p)所示。在本发明的上下文中待检测或抑制的多核苷酸的上下文中使用的本文所用的同一的多核苷酸可以具有与包含或组成为seqidno.1或seqidno.2中任一个的核苷酸序列的多核苷酸至少90%、95%、97%、98%或99%同一性的核酸序列。血清或血浆等无细胞血液中循环的microrna是最小或非侵入性的生物标志物来源,允许进行微创检测,因此在诊所和研究库中具有广泛的适用性。这对于影响组织的疾病是特别有利的,所述组织对于活检不容易接近。在本发明中,可以由本领域技术人员选择合适的mirna检测条件。在优选的实施方案中,目标mirna的水平通过聚合酶链式反应(pcr)确定。pcr方法在本领域中是公知的并且广泛使用,它们包括实时定量pcr、半定量pcr、多重pcr、数字pcr,或其任何组合。在特别优选的实施方案中,通过定量实时pcr(qrt-pcr)确定mirna的水平。使用qrt-pcr确定mirna水平的方法是本领域已知的,并且通常在将mirna逆转录成cdna之前进行。在可用于本发明的pcr方法中,引物通常基于成熟mirna分子,但可包括化学修饰以优化杂交行为。qrt-pcr方法可以确定mirna的绝对表达水平。或者,qrt-pcr方法可以确定mirna的相对量。可以通过将mirna的水平标准化(normalize)至一个或多个内部标准核酸序列的水平来确定mirna的相对数量。通常,这种内部标准核酸序列应该在分析的血液或血清样品中具有恒定水平。例如,内部标准核酸序列可以是组成型转录的rna核酸序列,比如mrna如甘油醛-3-磷酸-脱氢酶(gapdh)、β-肌动蛋白(actb),或非编码rna比如5s和18s核糖体rna、rnu48、rnu44和rnu6。此外,可以将血清或血浆中具有恒定和高水平的mirna比如mirna-760或mirna-6734-5p用作相对定量的参照。此外,在rna分离或cdna合成期间以等摩尔量添加的合成rna序列可以用作相对定量特定mirna的参照。由于mirna是相对较短的分子,它可通过在逆转录和扩增之前向链中加入腺苷单体(称为聚腺苷酸化的技术)来延长它们。简而言之,rna可以通过合适的试剂(例如,trizol试剂)从样品中提取,在atp和聚(a)聚合酶存在下聚腺苷酸化,使用聚(t)接头和5'race序列反转录成cdna,并使用衍生自mirna3'端的正向引物和反向race引物扩增。mirna的检测也可以通过本领域已知的其它方法来实现,例如通过深度测序方法,基于微珠的定量,例如illumina珠阵列,基于水凝胶颗粒的定量,例如fireflytm,通过微阵列技术,例如可从invitrogen获得的ncodetm人类mirna阵列,可从affymetrix、agilent获得的芯片阵列,或采用例如来自exiqon的lna主链捕获探针(mircurylnatm阵列)的微阵列。mirna水平的差异还可以使用基于多重化学发光的核酸测定法比如panomics或包含具有microrna-互补调节位点的报告蛋白的报告质粒测定法(“生物传感器”)或本领域已知的其它基于杂交的技术来确定。本发明提供了一种治疗骨质疏松的药物,所述药物包括mirna-760和mirna-6734-5p的抑制剂。在本发明中,mirna本身或其抑制剂/拮抗剂是否作为治疗组合物中的活性成分掺入,不仅取决于这些mirna是否在具有骨质疏松性的患者中上调或下调,还取决于其在成骨分化或破骨细胞生成激活中的特定功能。mirna治疗剂(即mirna的抑制剂)通常基于目标成熟mirna的序列。mirna替代疗法的治疗剂需要共享经取代的成熟mirna的大部分序列。在mirna的5'种子区域中需要准确的序列同源性。旨在特异性抑制mirna功能的治疗剂(抗microrna寡核苷酸,amo)需要与目标序列互补,从而实现mirna的稳定杂交并因此实现mirna的螯合(sequestration)。amo可以分别含有引起稳定的rna双链体形成的化学修饰,比如硫代磷酸酯主链,或lna和糖残基的2'ome修饰。mirna的抑制剂在本领域中是众所周知的,并且定制的mirna抑制剂是可商购的。例如,在本发明的上下文中的抑制剂可以是核酸分子,比如拮抗mirna或任何其它具有硫代磷酸酯键和胆固醇尾的t-o-甲基-rna寡核苷酸、mircurylnatmmicrorna抑制剂(exiqon)、体内lnatmmirna抑制剂(exiqon)、微小lna、mir-诱饵或mir-海绵等。抑制剂也可以是或来源于mirna降解酶,如tedeschi,drugdiscovtoday(2009),14:776-783中所述的锤头状核酶,或如jadhav,angewchemintedengl(2009),48(14:2557-2560)中所述的抗谷氨酰转肽酶(antogomirzyme)。在本发明的上下文中,所述抑制剂包括(但不限于)拮抗mir、micurylnatmmicrorna抑制剂、体内lnatmmir抑制剂、微小lna、mir诱饵或mir海绵。在一种可选择的实施方案中,药物组合物的活性成分根据称为“个性化医疗”的原则来选择,即与本发明的诊断方法的结果相关,在这种情况下,将其称为“伴随”诊断。这意味着,为了替代或抑制特定mirna而对mirna进行治疗性给药的决定,与在个体中分析特定mirna的水平的伴随诊断过程密切相关。本发明的任何mirna治疗剂,都可以与一种或多种其它试剂例如特立帕肽,狄诺塞麦,布鲁宗津单抗(blosozumab)、romosozumab、双膦酸盐如阿仑膦酸盐、唑来膦酸盐,或一种或多种骨生长因子或相应的编码核酸分子,例如bmp-2和/或bmp-7之类的bmp,或例如rna拮抗mir-760或mirna-6734-5p之类的rna,进行组合。本发明的mirna-760和mirna-6734-5p可以是天然的或是人工合成的,或者使用可以表达mirna-760和mirna-6734-5p的dna片段的载体转染细胞获得。本发明的可药用载体可包括但不限于:病毒、脂质体、纳米颗粒或聚合物及其任意组合。相关的递送载剂可包括但不限于:脂质体、生物相容性聚合物(包括天然聚合物和合成聚合物)、脂蛋白、多肽、多糖、脂多糖、人工病毒包膜、无机(包括金属)颗粒、以及细菌或病毒(例如杆状病毒、腺病毒和逆转录病毒)、噬菌体、黏粒或质粒载体。病毒载体可以是能够接受mirna基因产物的编码序列的任何病毒载体;,包括但不限于逆转录病毒载体、腺病毒载体、腺病毒相关病毒载体、疱疹病毒(例如单纯疱疹病毒、痘苗病毒及eb病毒)载体、甲病毒载体。可通过用来自其他病毒的包膜蛋白或其他表面抗原假型化载体或通过置换不同的病毒衣壳蛋白(如果合适)来改变病毒载体的趋向性。真核表达载体可以是任何适当的表达载体,包括但不限于pcmv-myc表达载体、pcdna3.0表达载体、pcdna3.1表达载体、pegfp表达载体、pefbos表达载体、ptet表达载体、ptre表达载体、或者在公知表达载体的基础上经改造的载体,比如pbin438、pcambia1301等。可以表达mirna-760和mirna-6734-5p的dna片段可以通过如下方式获取:从mirna数据库中(http://microrna.sanger.ac.uk/sequences/)寻找mirna-760和mirna-6734-5p在基因组上的位置及具体序列信息,根据基因组序列确定mirna-760和mirna-6734-5p初始mirna的位置,在mirna-760和mirna-6734-5p初始mirna位置的上下游500-800bp区间内设计特异性引物,扩增引物中间的序列即可获得表达mirna-760和mirna-6734-5p的dna片段。在本发明中,术语“血液样品”是指血清、血浆、全血及其组分、血液衍生产品或制剂。在本发明中,术语“治疗”涉及改善健康状况,减少或抑制不想要的体重减轻和/或延长和/或增加个体寿命的任何治疗。所述治疗可以消除个体中的病症、阻止或减缓个体中疾病的发展、抑制或减缓个体中疾病的发展、降低个体中症状的频率或严重程度,和/或减少目前患有或曾患过疾病的个体的复发。术语“预防性治疗”或“预防治疗”可以互换使用,并涉及旨在预防受试者发生疾病的任何治疗。如本文所用,疾病、障碍或病症的“预防”是指相对于未治疗的对照受试者,治疗的受试者中障碍或病症的发生减少,或相对于未治疗的对照受试者,延迟发作或减轻障碍或病症的一种或多种症状的严重程度。术语“保护”、“预防”、“预防性”、“预防的”或“保护的”涉及预防和/或治疗疾病的发生和/或传播。术语“绝经后”女性是指至少有一年没有经期的女性。实施例下面结合具体的实施例进一步说明本发明,本发明的实施例仅用于解释本发明,并不意味着限制本发明的保护范围。下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。实施例1与绝经后骨质疏松相关的mirna的筛选1、样本收集各收集30例健康人和绝经后骨质疏松患者的血液样本。edta抗凝管静置10min,离心分离血清,-20℃保存备用。上述所有标本的取得均通过组织伦理委员会的同意。取5例样本进行mirna表达谱的检测分析,进行差异表达基因的筛选,并在全部30例样本中进行大样本验证实验。排除标准:过早绝经者;如内分泌病、血液病、结缔组织病、药物和营养性疾病等引起的继发性骨质疏松症患者;代谢性骨病、慢性肝肾疾病等干扰骨代谢疾病者;近期服用雌激素、钙剂、二磷酸盐和维生素d等药物的患者;糖尿病患者;高血压患者;合并严重的心脑血管疾病者。2、样本总rna的提取使用invitrogen公司的血液rna提取试剂盒提取总rna。3、rna样品的质量分析(nanodrop1000分光光度计)nanodrop1000分光光度计检测rna样品,rna-seq测序的样品要求:od260/od280为1.8-2.2。将上述提取的rna进行琼脂糖凝胶电泳,agilenttechnologies2100bioanalyzer检测rna样品质量,在凝胶成像仪上观测、拍照,保存图像,一般认为28s:18s≥2可以初步判定总rna质量较好。4、mirna文库的构建1)富集smallrna使用5μg-10μgrna样品,然后用聚丙烯酰胺凝胶分离不同片段大小的rna,选择18-30nt(14-30ssrnaladdermarker,takara)条带回收。2)加接头5’连接接头反应体系:反应条件:20℃,6h;聚丙烯酰胺凝胶分离不同片段大小的rna;选择40-60nt条带回收。3’连接接头反应体系:反应条件:20℃,6h;用聚丙烯酰胺凝胶分离不同片段大小的rna;选择60-80ntnt条带回收。3)反转录反应条件:65℃,10min;48℃,3min;42℃,1h;70℃,15min。4)pcr扩增反应条件:98℃,30s;12-15循环(98℃,10s,72℃,15s);72℃,10min;4℃保存。5)纯化pcr产物用聚丙烯酰胺凝胶进行纯化,分离110bp左右的条带eb溶解,胶回收产物即为最终文库。6)文库质检使用agilent2100bioanalyzer和qpcr对文库质量进行检测。5、上机测序使用hiseq4000测序仪进行上机检测,具体操作按说明书进行。6、高通量转录组测序数据分析1)用cutadapt对reads的5’和3’段进行trim,trim掉质量<20的碱基,并且删掉n大于10%的reads;2)用bowtie把readsmap到基因组上。成熟mirna和mirna前体序列下载自mirbase,参考基因组为grch38;3)用mirdeep2定量已知mirna的表达;4)在r环境下用deseq2包比较两组的表达差异,当p值<0.05,|log2fc|>1时,认为基因显著差异表达。7、结果:测序结果显示,与健康人相比,绝经后骨质疏松患者中mirna-760和mirna-6734-5p的表达量显著升高,提示mirna-760和mirna-6734-5p可能作为检测靶标应用于骨质疏松的诊断。实施例2qpcr验证差异表达的mirna-760和mirna-6734-5p1、对差异表达的mirna-760和mirna-6734-5p进行大样本qpcr验证。2、rna提取利用qiagen血液rna提取试剂盒提取血清中的rna,具体步骤参考说明书。3、逆转录:1)将10pg-1μg的总rna模板与2μl10×缓冲液、2μldatp(10mm)、0.5μlpolya多聚酶、0.5μl核糖核酸酶(rnase)抑制剂和无核糖核酸酶水(rnasefreewater)混合,体积最后为20μl,37℃孵育1h。2)反应管中加入1μl0.5μg/μloligo(dt)特异性rt引物,70℃孵育5min。3)立即冰上孵育至少2min,打断rna和引物的二级结构。4)将上述20μl反应混合物与4μl5×缓冲液、1μldntp(10mm),0.5μlm-mlv逆转录酶,0.5μl核糖核酸酶(rnase)抑制剂,10μlpolya反应混合液和4μl无核糖核酸酶水(rnasefreewater)混合,42℃孵育1h。4、qpcr反应:1)引物设计扩增mirna-760的引物正向引物:cggctctgggtctgtgggga(seqidno.3)反向引物:gtgcagggtccgaggt(seqidno.4)扩增mirna-6734-5p的引物正向引物:ttgaggggagaatgaggtggaga(seqidno.5)反向引物:gtgcagggtccgaggt(seqidno.6)扩增u6snrna的引物正向引物:ctcgcttcggcagcaca(seqidno.7)反向引物:aacgcttcacgaatttgcgt(seqidno.8)2)按照表1配制pcr反应体系:其中,sybrgreen聚合酶链式反应体系购自invitrogen公司。表1pcr反应体系体积sybrgreen聚合酶链式反应体系12.5μl正向引物1μl反向引物1μlcdna模板2μlddh2o8.5μl总体积25μl3)pcr反应条件:95℃10min,(95℃15s,60℃60s)×45个循环。以sybrgreen作为荧光标记物,在lightcycler荧光定量pcr仪上进行pcr反应,以t6snrna作为参照基因,通过融解曲线分析和电泳确定目的条带,δδct法进行相对定量。5、结果如图1所示,与健康人样本相比,绝经后骨质疏松中mirna-760和mirna-6734-5p的表达水平显著升高,差异具有统计学意义p<0.05,提示mirna-760和mirna-6734-5p可作为分子标志物应用于骨质疏松的早期诊断。实施例3mirna-760和mirna-6734-5p对成骨分化的影响培养人的骨髓间充质干细胞(hmscs),将mirna-760的抑制物has-mir-760mirvanatmmirnainhibit(美国lifetechnologies)、模拟物has-mir-760mirvanatmmirnamimic(美国lifetechnologies),mirna-6734-5p的抑制物has-mir-6734-5pmirvanatmmirnainhibit(美国lifetechnologies)、模拟物has-mir-6734-5pmirvanatmmirnamimic(美国lifetechnologies),借助载体lipofectaminernaimaxreagent转染hmscs,观察mirna-760和mirna-6734-5p对hmscs诱导分化为成骨样细胞的影响。1、细胞的培养人的骨髓间充质干细胞(hmscs)以含以含10%胎牛血清和1%p/s的专用培养基在37℃、5%co2、相对湿度为90%的培养箱中培养。2-3天换液1次,使用含edta的0.25%胰蛋白酶常规消化传代,取处于对数生长期的细胞用于实验。2、细胞转染将细胞浓度按3×105/孔接种到6孔细胞培养板中,在37℃、5%co2培养箱中细胞培养24h,待细胞密度在70%时更换培养基,按照转染说明书进行转染培养,3天换液一次,成骨诱导14天后进行ars(茜素红)染色。将实验分成三组,每组设三个平行实验孔,具体分组情况如下:a.对照组(con):含10%胎牛血清的专用培养基+成骨诱导剂;b.模拟物组1(m1):含10%胎牛血清的专用培养基+成骨诱导剂+mirna-760mimic;c.模拟物组2(m2):含10%胎牛血清的专用培养基+成骨诱导剂+mirna-6734-5pmimic;d.抑制物组1(i1):含10%胎牛血清的专用培养基+成骨诱导剂+mirna-760的抑制物;e.抑制物组2(i2):含10%胎牛血清的专用培养基+成骨诱导剂+mirna-6734-5p的抑制物。3、ars染色细胞弃掉培养液,4%多聚甲醛固定15~20min,pbs液冲洗3遍。加入茜素红染液,于染色时加入培养板中,培养箱内放置15分钟,弃染色液,pbs液冲洗3遍,沥干,置于差像显微镜下拍照。在染色后的6孔板加入氯化十六烷基毗淀溶液(100mmol/l),每孔500μl,等其充分溶解后按照一定比例取等量的溶解液,使用分光光度计测量各吸光度数值用于定量。4、结果结果如图2所示,加入mirna-760或mirna-6734-5p的抑制物组能够促进ars阳性标记,加入mirna-760或mirna-6734-5p模拟物组则减少ars阳性标记,说明mirna-760和mirna-6734-5p可以影响成骨能力,提示mirna-760和mirna-6734-5p可以应用于骨质疏松疾病的治疗。上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1