具有Y182T突变的T细胞-抗原偶联物及其方法和用途与流程
交叉引用
本申请要求于2017年10月12日提交的第62/571,354号美国临时申请的权益,该临时申请通过引用并入本文。
序列表
本申请含有序列表,该序列表已经以ascii格式电子提交,并且通过引用整体并入本文。创建于2018年10月11日的所述ascii副本被命名为0034923-00006_sl.txt,大小为40,435个字节。
本公开涉及通过具有针对特定靶细胞的高细胞毒性和降低的脱靶毒性的工程化t细胞来治疗癌症的方法。具体地,本公开涉及表达触发自然t细胞活化过程的新型生物剂的工程化t细胞。
技术实现要素:
在一些实施方案中,本文公开了编码三功能t细胞-抗原偶联物(tri-tac)的核酸序列,其包含:(a)编码选择性结合靶抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的ucht1配体的第二多核苷酸序列,该ucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:26。在一些实施方案中,所述配体特异性结合靶抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述靶抗原是肿瘤抗原。在一些实施方案中,所述肿瘤抗原是her-2抗原。在一些实施方案中,所述肿瘤抗原是bcma抗原。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。
在一些实施方案中,本文公开了编码t细胞-抗原偶联物(tri-tac)的核酸序列,其包含:(a)编码选择性结合靶抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:29。在一些实施方案中,所述配体特异性结合靶抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述靶抗原是肿瘤抗原。在一些实施方案中,所述肿瘤抗原是her-2抗原。在一些实施方案中,所述肿瘤抗原是bcma抗原。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。
在一些实施方案中,本文公开了编码t细胞-抗原偶联物(tri-tac)的核酸序列,其包含:(a)编码选择性结合靶抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合靶抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述靶抗原是肿瘤抗原。在一些实施方案中,所述肿瘤抗原是her-2抗原。在一些实施方案中,所述肿瘤抗原是bcma抗原。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。
在一些实施方案中,本文公开了编码抗-her-2三功能t细胞-抗原偶联物(抗-her-2tri-tac)的核酸序列,其包含:(a)编码选择性结合her-2抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的ucht1配体的第二多核苷酸序列,该ucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,该氨基酸序列包含seqidno:26。在一些实施方案中,该氨基酸序列包含seqidno:29。在一些实施方案中,该氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合her-2抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述her-2抗原在癌细胞上表达。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。
在一些实施方案中,本文公开了编码抗-her-2三功能t细胞-抗原偶联物(抗-her-2tri-tac)的核酸序列,其包含:(a)编码选择性结合her-2抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,该氨基酸序列包含seqidno:26。在一些实施方案中,该氨基酸序列包含seqidno:29。在一些实施方案中,该氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合her-2抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述her-2抗原在癌细胞上表达。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。
在一些实施方案中,本文公开了编码抗-her-2三功能t细胞-抗原偶联物(抗-her-2tri-tac)的核酸序列,其包含:(a)编码选择性结合her-2抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,该氨基酸序列包含seqidno:26。在一些实施方案中,该氨基酸序列包含seqidno:29。在一些实施方案中,该氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合her-2抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述her-2抗原在癌细胞上表达。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。
在一些实施方案中,本文公开了编码抗-bcma三功能t细胞-抗原偶联物(抗-bcmatri-tac)的核酸序列,其包含:(a)编码选择性结合bcma抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的ucht1配体的第二多核苷酸序列,该ucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,该氨基酸序列包含seqidno:26。在一些实施方案中,该氨基酸序列包含seqidno:29。在一些实施方案中,该氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合bcma抗原。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述bcma抗原在癌细胞上表达。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。
在一些实施方案中,本文公开了编码抗-bcma三功能t细胞-抗原偶联物(抗-bcmatri-tac)的核酸序列,其包含:(a)编码选择性结合bcma抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,该氨基酸序列包含seqidno:26。在一些实施方案中,该氨基酸序列包含seqidno:29。在一些实施方案中,该氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合bcma抗原。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述bcma抗原在癌细胞上表达。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。
在一些实施方案中,本文公开了编码抗-bcma三功能t细胞-抗原偶联物(抗-bcmatri-tac)的核酸序列,其包含:(a)编码选择性结合bcma抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,该氨基酸序列包含seqidno:26。在一些实施方案中,该氨基酸序列包含seqidno:29。在一些实施方案中,该氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合bcma抗原。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述bcma抗原在癌细胞上表达。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。
在一些实施方案中,本文公开了包含本文公开的核酸序列的载体。在一些实施方案中,所述载体进一步包含启动子,优选在哺乳动物细胞中具有功能的启动子。
在一些实施方案中,本文公开了用本文公开的载体转染的t细胞。
在一些实施方案中,本文公开了工程化t细胞,其包含本文公开的核酸序列或本文公开的载体。
在一些实施方案中,本文公开了药物组合物,其包含本文公开的工程化t细胞和药学上可接受的载剂(carrier)。
在一些实施方案中,本文公开了治疗有需要的个体中表达靶抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码三功能t细胞-抗原偶联物(tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合所述靶抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的ucht1配体的第二多核苷酸序列,该ucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:26。在一些实施方案中,所述配体特异性结合靶抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述靶抗原是肿瘤抗原。在一些实施方案中,所述抗原是her-2抗原。在一些实施方案中,所述抗原是bcma抗原。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。在一些实施方案中,所述癌症是实体癌或液体癌。在一些实施方案中,所述癌症是肺癌、乳腺癌、结肠癌、多发性骨髓瘤、胶质母细胞瘤、胃癌、卵巢癌、胃癌、结直肠癌、尿路上皮癌、子宫内膜癌或黑素瘤。
在一些实施方案中,本文公开了治疗有需要的个体中表达靶抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码三功能t细胞-抗原偶联物(tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合所述靶抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:29。在一些实施方案中,所述配体特异性结合靶抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述靶抗原是肿瘤抗原。在一些实施方案中,所述抗原是her-2抗原。在一些实施方案中,所述抗原是bcma抗原。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。在一些实施方案中,所述癌症是实体癌或液体癌。在一些实施方案中,所述癌症是肺癌、乳腺癌、结肠癌、多发性骨髓瘤、胶质母细胞瘤、胃癌、卵巢癌、胃癌、结直肠癌、尿路上皮癌、子宫内膜癌或黑素瘤。
在一些实施方案中,本文公开了治疗有需要的个体中表达靶抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码t细胞-抗原偶联物(tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合所述靶抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化变异ucht1(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合靶抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述靶抗原是肿瘤抗原。在一些实施方案中,所述抗原是her-2抗原。在一些实施方案中,所述抗原是bcma抗原。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。在一些实施方案中,所述癌症是实体癌或液体癌。在一些实施方案中,所述癌症是肺癌、乳腺癌、结肠癌、多发性骨髓瘤、胶质母细胞瘤、胃癌、卵巢癌、胃癌、结直肠癌、尿路上皮癌、子宫内膜癌或黑素瘤。
在一些实施方案中,本文公开了治疗有需要的个体中表达her-2抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-her-2三功能t细胞-抗原偶联物(抗-her-2tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合所述her-2抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的ucht1配体的第二多核苷酸序列,该ucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:26。在一些实施方案中,所述配体特异性结合her-2抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。在一些实施方案中,所述癌症是实体癌或液体癌。在一些实施方案中,所述癌症是肺癌、乳腺癌、多发性骨髓瘤、胶质母细胞瘤、胃癌、卵巢癌、胃癌、结直肠癌、尿路上皮癌、子宫内膜癌或结肠癌。
在一些实施方案中,本文公开了治疗有需要的个体中表达her-2抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-her-2三功能t细胞-抗原偶联物(抗-her-2tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合所述her-2抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:29。在一些实施方案中,所述配体特异性结合her-2抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。在一些实施方案中,所述癌症是实体癌或液体癌。在一些实施方案中,所述癌症是肺癌、乳腺癌、多发性骨髓瘤、胶质母细胞瘤、胃癌、卵巢癌、胃癌、结直肠癌、尿路上皮癌、子宫内膜癌或结肠癌。
在一些实施方案中,本文公开了治疗有需要的个体中表达her-2抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-her-2三功能t细胞-抗原偶联物(抗-her-2tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合所述her-2抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合her-2抗原。在一些实施方案中,所述配体是锚蛋白重复序列(darpin)多肽。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。在一些实施方案中,所述癌症是实体癌或液体癌。在一些实施方案中,所述癌症是肺癌、乳腺癌、多发性骨髓瘤、胶质母细胞瘤、胃癌、卵巢癌、胃癌、结直肠癌、尿路上皮癌、子宫内膜癌或结肠癌。
在一些实施方案中,本文公开了治疗有需要的个体中表达bcma抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-bcma三功能t细胞-抗原偶联物(抗-bcmatri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合所述bcma抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的ucht1配体的第二多核苷酸序列,该ucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:26。在一些实施方案中,所述配体特异性结合bcma抗原。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。在一些实施方案中,所述癌症是实体癌或液体癌。在一些实施方案中,所述癌症是多发性骨髓瘤。
在一些实施方案中,本文公开了治疗有需要的个体中表达bcma抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-bcma三功能t细胞-抗原偶联物(抗-bcmatri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合所述bcma抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:29。在一些实施方案中,所述配体特异性结合bcma抗原。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。在一些实施方案中,所述癌症是实体癌或液体癌。在一些实施方案中,所述癌症是多发性骨髓瘤。
在一些实施方案中,本文公开了治疗有需要的个体中表达bcma抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-bcma三功能t细胞-抗原偶联物(抗-bcmatri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合所述bcma抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化ucht1变体(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少80%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些实施方案中,所述氨基酸序列包含seqidno:28。在一些实施方案中,所述配体特异性结合bcma抗原。在一些实施方案中,所述配体是单链可变片段(scfv)。在一些实施方案中,所述与tcr复合物缔合的蛋白质是cd3,优选cd3ε。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体的跨膜域和胞质域。在一些实施方案中,所述tcr共受体是cd4。在一些实施方案中,所述tcr共受体是cd8,优选cd8α。在一些实施方案中,所述第一多肽、所述第二多肽和所述第三多肽直接融合。在一些实施方案中,所述第一多肽和所述第二多肽直接融合,并且通过连接体与所述第三多肽连接。在一些实施方案中,所述第二多肽和所述第三多肽直接融合,并且通过连接体与所述第一多肽连接。在一些实施方案中,所述连接体是肽连接体,优选包含5至30个氨基酸、更优选5个氨基酸、10个氨基酸或15个氨基酸的肽连接体。在一些实施方案中,该肽连接体包括g4s3连接体。在一些实施方案中,所述癌症是实体癌或液体癌。在一些实施方案中,所述癌症是多发性骨髓瘤。
附图说明
本发明的新颖特征在所附权利要求书中具体阐述。通过参考以下对利用本发明原理的说明性实施方案加以阐述的详细描述以及附图,将会对本发明的特征和优点获得更好的理解,在这些附图中:
图1a是自然t细胞活化的示意图。图1b是基于car的t细胞活化的示意图。图1c是基于三功能t细胞-抗原偶联物(tri-tac)的t细胞活化的示意图。
图2a是具有通用抗原结合域的tri-tac分子的示意图。图2b是具有抗-her-2darpin抗原结合域的tri-tac分子的示意图。图2c是具有抗-bcmascfv抗原结合域的tri-tac分子的示意图。
图3a-图3b例示了使用darpin用针对her-2的tri-tac或基于cd28的car工程改造的t细胞。图3a例示了与不表达嵌合受体的t细胞相比,tri-tac和car的表面表达。图3b例示了3个细胞群体的生长。
图4a-图4b例示了各种抗-her-2darpintri-tac对照的受体表面表达和活化。用缺少靶向元件(-darpin)的tri-tac变体或缺少ucht1的tri-tac变体或全长tri-tac对t细胞进行工程改造。图4a例示了细胞表面表达(左侧)、脱粒(中间)和细胞因子产生(右侧),而图4b表明,仅全长抗-her-2darpintri-tac能够引发细胞毒性应答。
图5a-图5b示出了lck与抗-her-2darpintri-tac变体的相互作用。图5a例示了全长tac和胞质缺失将lck拉下的能力,而图5b示出了在图5a的沉淀物中检测到的lck的密度测定法分析。
图6a-图6b示出了用抗-her-2darpintri-tac或基于cd28的抗-her-2darpincar工程改造的t细胞的抗肿瘤活性和毒性。用经抗-her-2darpintri-tac或抗-her-2darpincar工程改造的t细胞治疗荷有已建立的ovcar-3肿瘤的小鼠。图6a例示了相对于t细胞输注日(第35天)的肿瘤生长变化,而图6b例示了在相同小鼠中体重的变化,这是毒性的量度。
图7a-图7c示出了与tri-tac变体文库相比的野生型抗-her-2darpintri-tac,在这些变体中,ucht1序列在预测与cd3结合的位点处随机诱变。图7a是突变体的示例性图示,图7b示出了显示该文库的表面表达的直方图,而图7c示出了该文库激活t细胞并产生细胞因子的能力。
图8a-图8c示出了在筛选图7b中公开的诱变文库之后选择的携带野生型ucht1(ucht1wt)或突变ucht1(ucht1a85v/t161p)的抗-her-2darpintri-tac的比较。图8a示出了在制备过程结束时cd8/cd4t细胞的分布。图8b示出了转导的水平。图8c例示了用表达her-2的细胞刺激后的细胞因子产生。
图9a-图9c示出了具有ucht1点突变体的多种抗-her-2darpintri-tac的表型分析和功能分析,所述ucht1点突变体是从图7b的筛选中分离的。图9a例示了抗-her-2darpintri-tac变体在cd4和cd8细胞中的表面表达。图9b示出了用表达her-2的skov3细胞刺激后,tri-tac变体诱导t细胞功能指示物表达的能力。图9c示出了tri-tac变体表达针对skov3细胞的细胞毒性的能力。
图10例示了在选择随机诱变的文库之后富集特定氨基酸的分析结果。通过将选择后的ucht1文库的序列与(i)图8中所述的原始文库和(ii)包装在慢病毒中的相同文库进行比较来定义富集。
图11a-图11c示出了各种ucht1变体的序列比对。图11a是野生型ucht1与通过富集分析鉴定的ucht1y182t的比对。图11b是野生型ucht1与人源化ucht1(huucht1)的比对。图11c是huucht1与携带来自ucht1y182t的相应突变的huucht1变体(被命名为huucht1y177t)的比对。
图12示出了y182t/y177t突变体相对于未突变的ucht1/huucht1的表面表达。
图13示出了用对照慢病毒(ngfr)或编码携带野生型ucht1、ucht1(y182t)、huucht1或huucht1(y177t)的tri-tac的慢病毒工程改造的t细胞培养物的生长。
图14示出了细胞毒性测定,其比较了用对照慢病毒(ngfr)或编码携带野生型ucht1、ucht1(y182t)、huucht1或huucht1(y177t)的tri-tac的慢病毒工程改造的t细胞培养物。所有tri-tac都是her-2特异性的。skov和a549是her-2阳性靶标。raji是her-2阴性靶标。
图15a-图15c示出了用携带野生型ucht1的tri-tac和携带ucht1(y182t)的tri-tac工程改造的t细胞的功能性。这两种tri-tac均带有针对骨髓瘤靶标bcma的scfv。图15a例证了tri-tac表达的表型分析。图15b示出了与kms-11骨髓瘤细胞(bcma阳性)或skov-3卵巢癌细胞(bmca阴性)共培养后的细胞因子产生。图15c示出了与kms-11或skov-3共培养后,由这2种tri-tac触发的细胞毒性。
图16示出了用携带野生型ucht1或ucht1(y182t)的bcma特异性tri-tac工程改造的t细胞的抗骨髓瘤活性。用工程改造为表达ngfr、具有野生型ucht1的tri-tac或具有ucht1(y182t)的tri-tac的t细胞处理荷有kms-11骨髓瘤的小鼠。通过在图中报告的生物发光监测肿瘤生长。对照t细胞用没有嵌合受体的慢病毒进行工程改造。
图17示出了用携带huucht1或huucht1(y177t)的抗-her-2darpintri-tac工程改造的t细胞的抗肿瘤活性。用经没有肿瘤结合域的对照tri-tac(图a和d)、具有huucht1的抗-her-2darpintri-tac(图b和e)或具有huucht1(y177t)的抗-her-2darpintri-tac(图c和f)工程改造的t细胞处理荷有已建立的ovcar-3肿瘤的小鼠。y轴代表相对于t细胞输注日的肿瘤生长变化。x轴代表相对于t细胞输注日的时间。t细胞产物由两个不同的供体产生。
图18是huucht1的核苷酸序列(seqidno:31)。
具体实施方式
癌症是主要的健康挑战,仅在2013年,在加拿大预计诊断出超过150,000例癌症。虽然患有早期疾病的患者可以通过常规疗法(外科手术、放射、化疗)有效地治疗,但患有晚期疾病的患者可用的选择很少,并且这些选择在本质上一般是姑息性的。
主动免疫疗法寻求采用患者的免疫系统来清除肿瘤种植,并且为常规疗法失效的患者提供令人激动的选择。通常,这种治疗涉及向患者输注大量肿瘤特异性t细胞。在包括黑素瘤、骨髓瘤、白血病、淋巴瘤和滑膜肉瘤等许多疾病的早期临床试验中,这种方法已被证明是成功的。作为具体实例,若干临床研究已经证明,采用t细胞的免疫疗法在晚期黑素瘤患者中可能是治愈性的,从而证实了该方法的效用。另外,罹患慢性淋巴细胞白血病(cll)和急性淋巴母细胞白血病(all)的患者也用t细胞免疫疗法得到有效治疗和治愈。
过继性t细胞疗法的临床应用所面临的关键挑战是t细胞的来源。通常,使从荷瘤患者中分离的t细胞离体生长至大量,然后施用回患者中,以诱导稳健的抗肿瘤免疫应答。肿瘤特异性可以通过以下两种方法之一实现:(i)从患者中分离出天然存在的肿瘤特异性t细胞;或(ii)工程改造来自外周血的批量t细胞以表达肿瘤特异性受体。天然存在的肿瘤特异性t细胞非常少见,从癌症患者中分离出治疗量的这类细胞是辛苦且昂贵的过程。相反,通过遗传操作用肿瘤特异性受体工程改造容易获得的外周t细胞则变得更加有效。已经为该工程化过程开发了在临床上可行的技术,并且若干临床试验已经证明了遗传工程化的t细胞对于癌症治疗的可行性和功效。
就此而言,大多数涉及t细胞遗传修饰的工程化t细胞疗法产生:(i)t细胞受体(tcr)的强制表达;或(ii)对肿瘤上的抗原靶标具有特异性的嵌合抗原受体(car)。迄今为止,用于工程改造t细胞的嵌合抗原受体由以下部分组成:(i)靶向结构域,通常是单链片段可变域(scfv);(ii)跨膜域;和(iii)胞质域,其含有来自t细胞受体和缔合的蛋白质的信号传导元件。此类嵌合抗原受体也被称为“t体(t-body)”或“嵌合免疫受体”(cir),但目前大多数研究人员使用术语“car”。car方法的一个优点是,它允许任何患者的免疫细胞以独立于主要组织相容性复合体(mhc)的方式靶向任何所需靶标。这是具有吸引力的,因为mhc呈递通常在肿瘤细胞中存在缺陷。
car以模块化的方式来考虑,并且科学家已经花费了相当长的时间来研究不同的胞质信号传导域对car功能的影响。常规car通常共有两个主要组分:(i)cd3zeta胞质域,其含有对t细胞活化至关重要的免疫酪氨酸活化基序;和(ii)触发重要存活途径如akt途径的共刺激受体的组分。第一代car采用来自cd3ζ或fcεriγ的单个信号传导域。
第二代car组合了cd3ζ的信号传导域与来自cd28或tnfr受体家族的共刺激受体的胞质域。当前在临床上测试的大多数car-工程化t细胞采用第二代car,其中cd3ζ与cd28或cd137的胞质域偶联。这些第二代car已在cd19阳性肿瘤中显示出抗肿瘤活性。第三代car组合了多个共刺激结构域,但存在第三代car可能失去抗原特异性的担忧。
虽然car-工程化t细胞已经在临床应用方面显示出相当大的希望,但是它们依赖合成方法来替代由t细胞受体(tcr)提供的天然激活信号。由于该合成受体不递送所有与tcr关联的信号传导组分(例如cd3γ、cd3δ、cd3ε上的itam),所以仍然不清楚t细胞是否被car以最佳方式激活或者car活化如何影响t细胞分化(例如进展至记忆t细胞)。而且,由于car信号传导域通过car结构的特有性质从它们的天然调节配偶体上分离,所以还存在以下固有风险:car可导致低水平的组成型活化,这可产生脱靶毒性。因此,原型car的合成性质可破坏规范机制从而限制tcr作用,并可加剧通常与常规cart细胞的治疗剂量相关的严重毒性。
考虑到这些局限性,优选重定向t细胞以经由其天然tcr攻击肿瘤。为此,创建了一类被称为“双特异性t细胞接合物”(bite)的重组蛋白。这些蛋白质采用双特异性抗体片段来将t细胞tcr受体与靶抗原交联。这导致有效的t细胞活化,从而触发细胞毒性。类似地,已产生了实现该目的的双特异性抗体,并且一些科学家已采用化学连接将抗cd3抗体与肿瘤特异性抗体简单地连接。虽然这些双特异性蛋白质已在体外显示出一定的活性,但是gmp生产、短生物半衰期和生物利用度都是这些分子在癌症治疗中成功使用所面临的重大挑战。另外,这些分子也不能正确地重现自然tcr信号传导,因为它们不接合tcr共受体(cd8和cd4)。
最近,已经开发出一种替代的嵌合受体,被称为三功能t细胞抗原偶联物(tri-tac或tac)受体,该受体采用独特的生物学来引导t细胞攻击肿瘤。car是将t细胞受体(tcr)信号传导复合物的组分缝合在一起的完全合成的受体,而tac受体则将tcr重定向至肿瘤靶标,并重现自然tcr信号传导结构。
有鉴于此,仍然需要与传统car和第一代tac受体相比具有增强的活性和安全性的嵌合受体。
某些术语
如本文所用的术语“一个细胞”包括单一细胞以及多个细胞。
如本文所用的术语“t细胞”是指在细胞介导的免疫中起关键作用的一种类型的淋巴细胞。t细胞,也被称为t淋巴细胞,可以通过在细胞表面上存在t细胞受体(tcr)而区别于其他淋巴细胞,如b细胞和自然杀伤细胞。存在几种具有不同功能的t细胞亚群,包括但不限于t辅助细胞、细胞毒性t细胞、记忆性t细胞、调节性t细胞和自然杀伤t细胞。
术语“t细胞抗原偶联物”或tac与“三功能t细胞抗原偶联物”或tri-tac可互换使用,并且是指当在t细胞上表达时,帮助促进t细胞靶向至特定抗原的工程化核酸构建体或多肽。
如本文所用的术语“多核苷酸”和/或“核酸序列”和/或“核酸”是指由碱基、糖和糖间(骨架)连接组成的核苷或核苷酸单体的序列。该术语还包括包含非天然存在的单体或其部分的修饰的或取代的序列。本申请的核酸序列可以是脱氧核糖核酸序列(dna)或核糖核酸序列(rna),并且可以包括天然存在的碱基,所述碱基包括腺嘌呤、鸟嘌呤、胞嘧啶、胸腺嘧啶和尿嘧啶。所述序列还可以包含修饰的碱基。此类修饰的碱基的实例包括氮杂和脱氮腺嘌呤、鸟嘌呤、胞嘧啶、胸腺嘧啶和尿嘧啶;以及黄嘌呤和次黄嘌呤。本公开的核酸可以分离自生物有机体,通过实验室基因重组方法形成,或者通过化学合成或用于产生核酸的其他已知方案获得。
如本文所用的术语“分离的多核苷酸”或“分离的核酸序列”是指当通过重组dna技术产生时,基本上无细胞物质或培养基的核酸,或者当化学合成时,基本上无化学前体或其他化学物质的核酸。分离的核酸也基本上没有天然位于该核酸所源自的核酸侧翼的序列(即,位于该核酸的5’端和3’端的序列)。术语“核酸”旨在包括dna和rna,可以是双链或单链的,并且代表有义链或反义链。此外,术语“核酸”包括互补的核酸序列。
如本文所用的术语“重组核酸”或“工程化核酸”是指在生物有机体中不存在的核酸或多核苷酸。例如,重组核酸可以通过实验室基因重组方法(如分子克隆)形成,以创建不存在于自然界的序列。重组核酸也可以通过化学合成或用于产生核酸的其他已知方案来创建。
如本文所用的术语“多肽”或“蛋白质”描述对应于由核酸编码的那些氨基酸的氨基酸链。本公开的多肽或蛋白质可以是肽,其通常描述2个至约30个氨基酸的氨基酸链。如本文所用的术语蛋白质也描述具有超过30个氨基酸的氨基酸链,并且可以是蛋白质的片段或结构域或者全长蛋白质。而且,如本文所用的,术语蛋白质可指氨基酸的线性链,或者可指已经被加工并且折叠为功能性蛋白质的氨基酸链。然而,应当理解,对于区分肽和蛋白质而言,30是一个任意的数字,并且对于氨基酸链来说,这些术语可互换使用。本公开的蛋白质可以通过从天然产生这些蛋白质的细胞中分离并纯化这些蛋白质而获得,通过酶促(例如蛋白水解)切割而获得,并且/或者通过表达编码本公开的蛋白质或片段的核酸而重组获得。本公开的蛋白质和/或片段也可以通过化学合成或用于产生蛋白质和片段的其他已知方案而获得。
术语“分离的多肽”是指当通过重组dna技术产生时,基本上无细胞物质或培养基的多肽,或者当化学合成时,基本上无化学前体或其他化学物质的多肽。
如本文所用的术语“抗体”旨在包括单克隆抗体、多克隆抗体、单链抗体、嵌合抗体和抗体融合物。该抗体可以来自重组来源和/或在转基因动物中产生。如本文所用的术语“抗体片段”旨在包括但不限于fab、fab'、f(ab')2、scfv、dsfv、ds-scfv、二聚体、微抗体、双抗体以及它们的多聚体、多特异性抗体片段和结构域抗体。
如本文所用的术语“载体”是指可以用来将核酸递送至细胞内的多核苷酸。在一个实施方案中,载体是表达载体,其包含与将在细胞中表达的核酸可操作地连接的表达控制序列(例如,启动子)。本领域已知的载体包括但不限于质粒、噬菌体、粘粒和病毒。
如本文所用的术语“肿瘤抗原”或“肿瘤相关抗原”是指在触发宿主免疫应答的肿瘤细胞中产生的抗原物质(例如,其可以由mhc复合体表示)。
如本文所用的术语“t细胞受体”或tcr是指整合膜蛋白的复合物,其响应于抗原的结合而参与t细胞的激活。tcr是二硫键连接的、膜锚定的异二聚体,该异二聚体通常由被表示为具有不变cd3(分化簇3)链分子的复合物的一部分的高度可变alpha(α)链和beta(β)链组成。表达该受体的t细胞被称为α:β(或αβ)t细胞,虽然少数t细胞表达由可变gamma(γ)和delta(δ)链形成的替代受体,后者被称为γδt细胞。cd3是由四条不同的链组成的蛋白质复合物。在哺乳动物中,该复合物包含cd3γ链、cd3δ链、两条cd3ε链和两条cd3ζ链。
如本文所用的,术语“跨膜域和胞质域”是指可以包括但不限于(a)与脂质筏缔合的和/或(b)结合lck的蛋白质结构域的多肽。如本文所用的,“蛋白质结构域”是指独立于该蛋白质链的其余部分而发挥作用和存在的给定蛋白质序列结构的保守部分。
如本文所用的“tcr共受体”是指帮助t细胞受体(tcr)与抗原呈递细胞进行通信的分子。tcr共受体的实例包括但不限于cd4、cd8、cd5、cd9和cd22。
如本文所用的“tcr共刺激物”是指增强t细胞对抗原的应答的分子。tcr共刺激物的实例包括但不限于icos、cd27、cd28、4-1bb(cd137)、ox40(cd134)、cd30、cd40、淋巴细胞功能相关抗原1(lfa-1)、cd2、cd7、light、nkg2c、b7-h3以及特异性结合cd83的配体。
如本文所用的“tcr共抑制物”是指抑制t细胞对抗原的应答的分子(也称为检查点受体)。tcr共刺激物的实例包括但不限于pd-1、tim3、lag-3、tigit、btla、cd160和cd37。
术语“接受者”、“个体”、“受试者”、“宿主”和“患者”在本文中可互换使用,并且在一些情况下是指需要诊断、治疗或疗法的任何哺乳动物受试者,特别是人。用于治疗目的的“哺乳动物”是指被归类为哺乳动物的任何动物,包括人、家畜和农场动物,以及实验室动物、动物园动物、竞技动物或宠物,如狗、马、猫、牛、绵羊、山羊、猪、小鼠、大鼠、兔、豚鼠、猴等。在一些实施方案中,该哺乳动物是人。
如本文所用的,术语“治疗”、“处理”等在一些情况下是指出于获得效果的目的,施用药剂或实施程序。就完全或部分预防疾病或其症状而言,该效果可以是预防性的,并且/或者就部分或完全治愈疾病和/或疾病症状而言,该效果可以是治疗性的。如本文所用的,“治疗”可包括治疗哺乳动物、特别是人的疾病或病症(例如癌症),并且包括:(a)预防可能易患疾病但尚未被诊断为患有该疾病(例如,包括可能与原发性疾病相关或由原发性疾病引起的疾病)的受试者发生该疾病或疾病症状;(b)抑制该疾病,即,阻止其发展;和(c)缓解该疾病,即,引起该疾病的消退。治疗可指成功治疗或改善或预防癌症的任何标志,包括任何客观或主观的参数,如症状减轻、缓解、减少,或使患者更耐受疾病病况;减缓退化或衰退的速率;或者使退化的终点变得不那么使人虚弱。症状的治疗或改善基于一个或多个客观或主观的参数;包括医师的检查结果。因此,术语“治疗”包括施用本发明的化合物或药剂,以预防或延缓、缓和或阻止或抑制与疾病(例如癌症)相关的症状或病况的发展。术语“治疗效果”是指减少、消除或阻止受试者的疾病、疾病症状或疾病副作用。
除非上下文另外明确指出,否则如本文所用的,单数形式“一种”、“一个”和“该”包括复数指示物。因此,例如,提及“一个抗体”包括多个抗体,而在一些实施方案中,提及“一种抗体”包括多种抗体,依此类推。
除非上下文另外明确指出,否则如本文所用的,所有数值或数值范围包括这类范围内的或包含这类范围的所有整数,以及在范围内的或包含范围的数值或整数的分数。因此,例如,提及90-100%的范围包括91%、92%、93%、94%、95%、95%、97%等,以及91.1%、91.2%、91.3%、91.4%、91.5%等,92.1%、92.2%、92.3%、92.4%、92.5%等,诸如此类。在另一个实例中,提及1-5,000倍的范围包括1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20倍等,以及1.1、1.2、1.3、1.4、1.5倍等,2.1、2.2、2.3、2.4、2.5倍等,诸如此类。
如本文所用的,“约”某一数字是指包括该数字并且范围为该数字以下10%至该数字以上10%的范围。“约”某一范围是指该范围下限以下10%直到该范围上限以上10%。
“同一性百分比(%)”是指两个序列(核苷酸或氨基酸)在比对中在相同位置处具有相同残基的程度。例如,“氨基酸序列与seqidno:y为x%相同”是指该氨基酸序列与seqidno:y的%同一性,并且被阐述为该氨基酸序列中x%的残基与seqidno:y中公开的序列的残基相同。通常,计算机程序用于这类计算。比较和比对序列对的示例性程序包括align(myers和miller,1988)、fasta(pearson和lipman,1988;pearson,1990)和带空位的blast(altschul等人,1997)、blastp、blastn或gcg(devereux等人,1984)。
如本文所用的,术语“选择性结合”是指蛋白质(例如tac的靶标结合配体)结合其靶抗原(例如,her-2或bcma)而非其他抗原的程度。
t细胞-抗原偶联物(tac)
在一些实施方案中,本文公开了编码三功能t细胞-抗原偶联物(tri-tac)的核酸,其通过t细胞受体(tcr)激活自然信号传导,同时保留没有mhc限制的靶向。
在一些实施方案中,本文公开了编码三功能t细胞-抗原偶联物(tri-tac或tac)的核酸,其包含:(a)编码选择性结合靶抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的鼠ucht1(muucht1)配体的第二多核苷酸序列,该muucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合靶抗原。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少75%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少80%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少85%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少90%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少95%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含seqidno:26的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多肽序列与seqidno:26的序列同一性百分比是指除y182t突变外的氨基酸。
在一些实施方案中,本文公开了编码三功能t细胞-抗原偶联物(tri-tac或tac)的核酸,其包含:(a)编码选择性结合靶抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合靶抗原。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少75%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少80%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少85%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少90%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少95%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含seqidno:29的氨基酸序列。
在一些实施方案中,本文公开了编码三功能t细胞-抗原偶联物(tri-tac或tac)的核酸,其包含:(a)编码选择性结合靶抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化ucht1(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合靶抗原。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少75%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少80%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少85%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少90%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少95%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含seqidno:28的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多肽序列与seqidno:28的序列同一性百分比是指除y177t突变外的氨基酸。
在一些实施方案中,选择性结合靶抗原的配体(或靶标特异性配体)将t细胞-抗原偶联物(tac)引导至靶细胞。在一些情况下,靶标特异性配体被称为抗原结合域。在一些情况下,靶标特异性配体是指直接或间接结合靶细胞的任何物质。在一些实施方案中,靶标特异性配体结合靶细胞上的抗原(由可以引发免疫应答的细胞产生的蛋白质)。在一些情况下,靶标特异性配体包括但不限于抗体及其片段,例如单链抗体,如单链抗体(scfv)、单结构域抗体、肽、拟肽、蛋白质、糖蛋白或与靶细胞和/或抗原结合的蛋白聚糖。在一些情况下,靶标特异性配体包括但不限于设计的锚蛋白重复序列蛋白质(darpin)、凝集素、knottin、centryrin、anticalin或肿瘤抗原的天然存在的配体,如生长因子、酶底物、受体或结合蛋白。在一些情况下,靶标特异性配体包括与靶细胞和/或抗原结合的非蛋白质化合物,包括但不限于碳水化合物、脂质、核酸或小分子。在一些情况下,靶标特异性配体是靶向特定细胞和/或抗原的经设计的锚蛋白重复序列(darpin)。在一些情况下,靶标特异性配体是选择性结合her2(erbb-2)抗原的darpin。在一些情况下,靶标特异性配体是特异性结合her2(erbb-2)抗原的darpin。在一些情况下,靶向her-2(erb-2)的darpin包含seqidno:7和seqidno:8。在一些情况下,靶标特异性配体是靶向特定细胞和/或抗原的单链抗体(scfv)。在一些情况下,靶标特异性配体是选择性结合bcma的scfv。在一些情况下,靶标特异性配体是特异性结合bcma的scfv。在一些情况下,结合bcma的scfv包含seqidno:21和seqidno:22。
在一些情况下,靶细胞是与包括但不限于癌症的疾病状态相关的细胞。在一些实施方案中,靶细胞是肿瘤细胞。在一些情况下,靶标特异性配体可以结合肿瘤细胞上的肿瘤抗原或肿瘤相关抗原。在一些情况下,靶抗原是肿瘤抗原。在一些情况下,蛋白质肿瘤抗原是8个或更多个氨基酸直至完整蛋白质的序列。在一些情况下,肿瘤抗原是8个氨基酸至全长蛋白质之间的任何数目的氨基酸,其包含在mhc复合体中代表的全长蛋白质的至少一个抗原性片段。肿瘤抗原的实例包括但不限于her-2(erbb-2)、b细胞成熟抗原(bcma)、甲胎蛋白(afp)、癌胚抗原(cea)、ca-125、muc-1、上皮肿瘤抗原(eta)、酪氨酸酶、黑素瘤相关抗原(mage)、前列腺特异性抗原(psa)、神经胶质瘤相关抗原、β-人绒毛膜促性腺激素、甲状腺球蛋白、rage-1、mn-caix、人端粒酶逆转录酶、ru1、ru2(as)、肠羧基酯酶、muthsp70-2、m-csf、prostase、pap、ny-eso-1、lage-1a、p53、prostein、psma、存活蛋白和端粒酶、前列腺癌肿瘤抗原-1(pcta-1)、elf2m、嗜中性粒细胞弹性蛋白酶、cd22、胰岛素生长因子(igf)-i、igf-ii、igf-i受体和间皮素。在一些情况下,该肿瘤抗原是her-2抗原。在一些情况下,her-2特异性配体包含选自曲妥珠单抗、帕妥珠单抗、拉帕替尼、奈拉替尼、ado-trastuzmabemtansine、gancotamab、margetuximab、timigutuzumab和厄马索单抗(ertumaxomab)的抗体的抗原结合域。在一些情况下,该肿瘤抗原是bcma抗原。在一些情况下,bcma特异性配体包含选自belantamabmafodotin和gsk2857916的抗体的抗原结合域。
在一些实施方案中,tac与共受体刺激相组合地募集t细胞受体(tcr)。在一些情况下,tac包含结合与tcr复合物缔合的蛋白质的配体。在一些情况下,结合与tcr复合物缔合的蛋白质的配体包括直接或间接地与tcr的蛋白质结合的物质。与tcr缔合的蛋白质包括但不限于tcralpha(α)链、tcrbeta(β)链、tcrgamma(γ)链、tcrdelta(δ)链、cd3γ链、cd3δ链和cd3ε链。在一些实施方案中,结合与tcr复合物缔合的蛋白质的配体是tcralpha(α)链、tcrbeta(β)链、tcrgamma(γ)链、tcrdelta(δ)链、cd3γ链、cd3δ链和/或cd3ε链的抗体。在一些情况下,与tcr复合物缔合的蛋白质是cd3。在一些情况下,与tcr复合物缔合的蛋白质是cd3ε。在一些实施方案中,该配体是结合cd3的抗体或其片段。cd3抗体的实例包括但不限于莫罗单抗(muromonab)、奥昔珠单抗(otelixizumab)、替利珠单抗(teplizumab)和维西珠单抗(visilizumab)。在一些实施方案中,结合cd3的抗体是单链抗体,例如单链抗体(scfv)。在一些情况下,与cd3结合的配体是ucht1。在一些情况下,该ucht1配体结合cd3ε。在一些情况下,该ucht1配体是鼠配体。在一些情况下,该鼠ucht1配体包含seqidno:13和14。在一些情况下,该鼠ucht1配体结合cd3ε。在一些情况下,具有y182t突变的鼠ucht1配体结合cd3ε。在一些情况下,人源化ucht1变体配体结合cd3ε。在一些情况下,具有y177t突变的人源化ucht1配体结合cd3ε。
在一些实施方案中,所述tcr信号传导域多肽包含跨膜域。在一些实施方案中,所述tcr信号传导域多肽包含胞质域。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些情况下,所述tcr信号传导域多肽包含tcr共受体的跨膜域和/或胞质域。在一些情况下,该tcr共受体是cd4。在一些情况下,所述tcr信号传导域多肽包含cd4共受体的跨膜域和胞质域,它们包含seqidno:17和18。在一些情况下,该tcr共受体是cd8。在一些情况下,该tcr共受体是cd8α。在一些情况下,该tcr共受体是cd5。在一些情况下,该tcr共受体是cd9。在一些情况下,该tcr共受体是cd5。在一些情况下,该tcr共受体是cd22。在一些情况下,所述tcr信号传导域多肽包含tcr共刺激物的跨膜域和/或胞质域。在一些情况下,该tcr共刺激物是icos。在一些情况下,该tcr共刺激物是cd27。在一些情况下,该tcr共刺激物是cd28。在一些情况下,该tcr共刺激物是4-1bb(cd137)。在一些情况下,该tcr共刺激物是ox40(cd134)。在一些情况下,该tcr共刺激物是cd30。在一些情况下,该tcr共刺激物是cd40。在一些情况下,该tcr共刺激物是淋巴细胞功能相关抗原1(lfa-1)。在一些情况下,该tcr共刺激物是cd2。在一些情况下,该tcr共刺激物是cd7。在一些情况下,该tcr共刺激物是light。在一些情况下,该tcr共刺激物是nkg2c。在一些情况下,该tcr共刺激物是b7-h3。在一些情况下,该tcr共刺激物是特异性结合cd83的配体。在一些情况下,所述tcr信号传导域多肽包含tcr共抑制物的跨膜域和/或胞质域。在一些情况下,该tcr共抑制物是pd-1。在一些情况下,该tcr共抑制物是tim3。在一些情况下,该tcr共抑制物是lag-3。在一些情况下,该tcr共抑制物是tigit。在一些情况下,该tcr共抑制物是btla。在一些情况下,该tcr共抑制物是cd160。在一些情况下,该tcr共抑制物是cd37。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体或共刺激物蛋白质的胞质域和跨膜域。在一些情况下,该胞质域和跨膜域来自相同的共受体或共刺激物或者来自不同的共受体或共刺激物。在一些情况下,该胞质域和跨膜域任选地通过连接体连接。在一些实施方案中,所述tac进一步包含直接或间接作用以靶向或激活t细胞的其他多肽。
在一些实施方案中,第一多肽、第二多肽和第三多肽直接融合。在一些实施方案中,第一多肽、第二多肽和第三多肽通过至少一个连接体连接。在一些实施方案中,第一多肽和第二多肽直接融合,并且通过连接体与第三多肽连接。在一些实施方案中,第二多肽和第三多肽直接融合,并且通过连接体与第一多肽连接。在一些实施方案中,该连接体是肽连接体。在一些实施方案中,该肽连接体包含1至40个氨基酸。在一些实施方案中,该肽连接体包含1至30个氨基酸。在一些实施方案中,该肽连接体包含1至15个氨基酸。在一些实施方案中,该肽连接体包含1至10个氨基酸。在一些实施方案中,该肽连接体包含1至6个氨基酸。在一些实施方案中,该肽连接体包含30至40个氨基酸。在一些实施方案中,该肽连接体包含32至36个氨基酸。在一些实施方案中,该肽连接体包含5至30个氨基酸。在一些实施方案中,该肽连接体包含5个氨基酸。在一些实施方案中,该肽连接体包含10个氨基酸。在一些实施方案中,该肽连接体包含15个氨基酸。在一些实施方案中,该肽连接体包含20个氨基酸。在一些实施方案中,该肽连接体包含25个氨基酸。在一些实施方案中,该肽连接体包含30个氨基酸。在一些实施方案中,该肽连接体包括g4s3连接体。在一些情况下,在tac中使用的连接体的其他实例是对应于seqidno:11、12、15、16、19和20的肽及其变体和片段。
在一些实施方案中,cd4共受体的跨膜域和胞质域与结合cd3的单链抗体融合。在一些情况下,将设计的锚蛋白重复序列(darpin)与cd4-ucht1嵌合体连接,以生成三功能t细胞-抗原偶联物(tri-tac)。在一些情况下,该tri-tac将cd3分子和tcr引入脂质筏区域中,并且使lck接近tcr,这类似于自然的mhc结合。
在一些情况下,用tri-tac工程改造的t细胞在体外显示出等同于常规car的功能性。在一些情况下,用tri-tac工程改造的t细胞在体外显示出优于常规car的功能性。在一些情况下,与传统的car相比,tri-tac提供增强的安全性,这是因为激活结构域都不是该蛋白质的一部分。
在一些实施方案中,所述核酸是重组的或工程化的核酸。在一些实施方案中,第一、第二和/或第三多核苷酸是重组的或工程化的多核苷酸。在一些实施方案中,可以对本文所述的多核苷酸进行修饰或突变,以优化编码的多肽的功能和/或t细胞抗原偶联物的功能、活性和/或表达。
在一些实施方案中,生成具有增强的tac的表面表达的ucht1突变体(图8、9、10、12)。在一些情况下,该tac包含结合tcr复合物的修饰的或突变的配体,其中相比于包含结合tcr复合物的野生型或未修饰的或未突变的配体的tac,包含修饰的或突变的抗体的tac具有增加的表面表达和/或活性。结合cd3的突变的或修饰的抗体的实例是本文公开的ucht1(y182t)突变体(seqidno:25和26)。
预期tri-tac以各种构型存在。在一些实施方案中,靶标特异性配体和t细胞受体信号传导域多肽均与结合tcr复合物的配体融合。例如,本文公开的抗-her-2darpintri-tac(也被称为构型1;seqidno:1和2)按顺序包括:
i)抗-her-2tri-tac前导序列(分泌信号)(seqidno:5和6)
ii)her-2抗原特异darpin(seqidno:7和8)
iii)myc标签(seqidno:9和10)
iv)连接体1(seqidno:11和12)
v)ucht1(seqidno:13和14)
vi)连接体2(seqidno:15和16)
vii)cd4(seqidno:17和18)。
在一些实施方案中,darpin被bcma抗原特异性scfv(seqidno:21和22)替换。
多肽和载体构建体
在一些实施方案中,本文公开了由本文公开的核酸序列编码的多肽。本文还公开了包含本文公开的核酸序列的载体。在一些情况下,该载体进一步包含启动子。在一些情况下,该启动子在哺乳动物细胞中具有功能。采用多种递送载体和表达介质将本文所述的核酸导入细胞中。
启动子是启动特定核酸序列转录的dna区域,是本领域公知的。“在哺乳动物细胞中具有功能的启动子”是指驱使相关核酸序列在哺乳动物细胞中表达的启动子。驱使核酸序列表达的启动子可以被称为与该核酸序列“可操作地连接”。
在一些实施方案中,第一多核苷酸和第三多核苷酸与第二多核苷酸融合,以提供tri-tac融合物,并且该tri-tac融合物的编码序列与启动子可操作地连接。在一些实施方案中,第二多核苷酸和第三多核苷酸与第一多核苷酸融合,以提供tri-tac融合物,并且该tri-tac融合物的编码序列与启动子可操作地连接。在一些实施方案中,载体被设计用于在哺乳动物细胞如t细胞中表达。在一些实施方案中,该载体是病毒载体。在一些情况下,该病毒载体是逆转录病毒载体。
有用的载体包括来源于慢病毒、鼠干细胞病毒(mscv)、痘病毒、致癌逆转录病毒(oncoretroviruses)、腺病毒和腺相关病毒的载体。其他有用的递送载体包括来源于单纯疱疹病毒、转座子、痘苗病毒、人乳头瘤病毒、猿猴免疫缺陷病毒、htlv、人泡沫病毒及其变体的载体。其他有用的载体包括来源于泡沫病毒、哺乳动物b型逆转录病毒、哺乳动物c型逆转录病毒、禽c型逆转录病毒、哺乳动物d型逆转录病毒和htlv/blv型逆转录病毒的载体。在公开的组合物和方法中有用的慢病毒载体的一个实例是pccl载体。
可以对多核苷酸序列(包括本文公开的载体序列和多肽序列)进行许多修饰。修饰包括核苷酸或氨基酸的置换、插入或缺失,或者改变核苷酸或氨基酸的相对位置或顺序。
序列同一性
本文公开的多核苷酸还包括与公开的核酸分子具有至少约70%同一性、至少80%同一性、至少90%同一性、至少95%同一性、至少96%同一性、至少97%同一性、至少98%同一性或至少99%或99.5%同一性的核酸分子(或其片段)。所述多肽还包括与公开的多肽具有至少约70%同一性、至少80%同一性、至少90%同一性、至少95%同一性、至少96%同一性、至少97%同一性、至少98%同一性或至少99%或99.5%同一性的多肽(或其片段)。
序列同一性优选地被设置为与本文提供的核苷酸序列和/或其互补序列具有至少约70%的同一性、至少80%的同一性、至少90%的同一性、至少95%的同一性、至少96%的同一性、至少97%的同一性、至少98%的同一性,或者最优选地至少99%或99.5%的同一性。序列同一性还优选地被设置为与本文提供的多肽序列具有至少约70%的同一性、至少80%的同一性、至少90%的同一性、至少95%的同一性、至少96%的同一性、至少97%的同一性、至少98%的同一性,或者最优选地至少99%或99.5%的同一性。
杂交
在一些情况下,本文公开了这样的dna,其具有的序列与本文描述的核酸分子具有足以在严格杂交条件下杂交的同一性。本文还公开了与本文所述的一个或多个序列和/或其互补序列杂交的核酸分子。此类核酸分子优选地在高严格条件下杂交。高严格性洗涤优选地具有低盐(优选约0.2%ssc)和约50-65℃的温度,并且任选地进行约15分钟。
在t细胞中的表达
三功能t细胞抗原偶联物被设计用于在t细胞中表达。在一些实施方案中,本文公开了工程化t细胞,其包含本文公开的核酸序列或本文公开的载体。在一些情况下,该t细胞表达本文公开的三功能t细胞抗原偶联物(tri-tac)。本文进一步公开了用t细胞抗原偶联物或包含tri-tac的载体转导或转染的t细胞。在一些情况下,该t细胞是分离的t细胞。
t细胞可以获自许多来源,包括但不限于血液(例如,外周血单核细胞)、骨髓、胸腺组织、淋巴结组织、脐带血、胸腺组织、来自感染部位的组织、脾脏组织和肿瘤。在一些实施方案中,该t细胞是自体t细胞。在一些实施方案中,该t细胞从t细胞的细胞系获得。在一些实施方案中,该t细胞从供体获得(同种异体t细胞)。在一些实施方案中,通过分化胚胎或成体干细胞或从诱导的多能干细胞获得t细胞。在一些实施方案中,不管t细胞的来源如何,都已经修饰了t细胞,使得它们缺乏内源tcr的表达和/或永久或暂时缺乏mhc/hla分子的表达(通用供体t细胞)。在一些实施方案中,t细胞对于受试者而言可以是自体的。在一些实施方案中,所述细胞对于受试者而言是同种异体的、同基因的或异种的。
一旦获得,就任选地在体外富集t细胞。在一些情况下,通过阳性选择或阴性选择来富集细胞群体。此外,优选地将t细胞冷冻或低温保存,然后在以后的日期解冻。
在将tri-tac引入t细胞之前或之后,在一些情况下,激活和/或扩增t细胞。在一些情况下,通过与表面接触来扩增t细胞,该表面上附着有刺激cd3/tcr复合物相关信号的试剂以及刺激t细胞表面上的共刺激物分子的配体。
在一些实施方案中,用核酸序列转导或转染t细胞。在一些情况下,表达所转导或转染的t细胞。在一些情况下,可以通过物理、化学或生物学手段将核酸导入细胞内。物理手段包括但不限于显微注射、电穿孔、粒子轰击、脂质转染和磷酸钙沉淀。生物学手段包括使用dna和rna载体。
在一些实施方案中,使用包括逆转录病毒载体在内的病毒载体将核酸导入t细胞中并且在其中表达。病毒载体包括来源于慢病毒、鼠干细胞病毒(mscv)、痘病毒、单纯疱疹病毒i、腺病毒和腺相关病毒的载体。该载体任选地包含驱使转导的核酸分子在t细胞中表达的启动子。
使用多种测定来确认转导的核酸序列和/或由该核酸编码的多肽在t细胞中的存在和/或表达。测定包括但不限于southern印迹法和northern印迹法、rt-pcr和pcr、elisa和western印迹法。
在一些实施方案中,与不表达t细胞抗原偶联物的t细胞相比,和/或与表达传统car的t细胞相比,表达t细胞抗原偶联物的t细胞在抗原的存在下具有增加的t细胞活化。增加的t细胞活化可以通过许多方法来确定,包括但不限于增加的肿瘤细胞系杀伤、增加的细胞因子产生、增加的细胞溶解、增加的脱粒和/或增加的活化标志物如cd107α、ifnγ、il2或tnfα的表达。增加可以在单个细胞或细胞群体中测量。
如本文所用的术语“增加的”或“增加”是指与不表达t细胞抗原偶联物的t细胞或t细胞群体相比,和/或与表达传统car的t细胞或t细胞群体相比,表达t细胞抗原偶联物的t细胞或t细胞群体增加至少1%、2%、5%、10%、25%、50%、100%或200%。
药物组合物
在一些实施方案中,本文公开了药物组合物,其包含(用t细胞抗原偶联物转导的和/或表达t细胞抗原偶联物的)本文公开的工程化t细胞和药学上可接受的载剂。这类组合物可以包含缓冲液,如中性缓冲盐水、磷酸盐缓冲盐水等;碳水化合物,如葡萄糖、甘露糖、蔗糖或葡聚糖、甘露醇;蛋白质;多肽或氨基酸,如甘氨酸;抗氧化剂;螯合剂,如edta或谷胱甘肽;佐剂(例如氢氧化铝);和防腐剂。在一些情况下,将工程化t细胞配制用于静脉内给药。
药物组合物以适合于待治疗(或预防)的疾病的方式施用。给药量和给药频率取决于诸如患者的状况以及患者疾病的类型和严重程度等因素,尽管适当的剂量取决于临床试验。当指示“免疫学有效量”、“抗肿瘤有效量”、“肿瘤抑制有效量”或“治疗量”时,待施用的本发明组合物的精确量可以由医生考虑年龄、体重、肿瘤大小、感染或转移的程度以及患者(受试者)的状况的个体差异来确定。例如,本文所述的修饰的t细胞和/或药物组合物以每kg体重104至109个细胞,任选地每kg体重105至108个细胞、每kg体重106至107个细胞或每kg体重105至106个细胞的剂量施用,包括这些范围内的所有整数值。t细胞组合物也可以以这些剂量多次施用。该剂量可以一次或多次施用,例如每天、每周、每两周或每月一次施用,或者可以在所治疗的癌症复发、重现或进展时施用。可以通过使用免疫疗法中公知的输注技术来施用所述细胞(参见,例如,rosenberg等人,neweng.j.ofmed.319:1676,1988)。
在一些实施方案中,所述药物组合物基本上不含,例如,没有可检测水平的污染物,例如选自内毒素、支原体、具有复制能力的慢病毒(rcl)、p24、vsv-g核酸、hivgag、残余抗-cd3/抗-cd28包被的珠子、小鼠抗体、合并的人血清、牛血清白蛋白、牛血清、培养基组分、载体包装细胞或质粒组分、细菌和真菌的污染物。在一个实施方案中,该细菌是选自粪产碱菌(alcaligenesfaecalis)、白色念珠菌(candidaalbicans)、大肠杆菌(escherichiacoli)、流感嗜血杆菌(haemophilusinfluenza)、脑膜炎奈瑟球菌(neisseriameningitides)、铜绿假单胞菌(pseudomonasaeruginosa)、金黄色葡萄球菌(staphylococcusaureus)、肺炎链球菌(streptococcuspneumonia)和酿脓链球菌(streptococcuspyogenes)a组的至少一种。
在一些实施方案中,可能希望向受试者施用工程化t细胞,随后抽血(或进行单采血液成分术),从中激活t细胞,并向该患者重新输注这些活化并扩增的t细胞。该过程可以每数周进行多次。在一些方面,可以从10cc至400cc的抽取血液激活t细胞。在某些方面,从20cc、30cc、40cc、50cc、60cc、70cc、80cc、90cc或100cc的抽取血液激活t细胞。
修饰的t细胞和/或药物组合物可以通过包括但不限于气雾剂吸入、注射、摄入、输注、植入或移植的方法施用。修饰的t细胞和/或药物组合物可以经动脉、皮下、皮内、瘤内、结内(intranodally)、髓内(intrameduliary)、肌肉内、通过静脉内(i.v.)注射或腹膜内施用于受试者。一方面,通过皮内或皮下注射将修饰的t细胞和/或其药物组合物施用至患者。在一些方面,通过静脉内注射施用修饰的t细胞和/或其药物组合物。修饰的t细胞和/或其药物组合物可以直接注入肿瘤、淋巴结或感染部位。
药物组合物可以通过用于制备可施用于受试者的药学上可接受的组合物的本身已知的方法来制备,使得有效量的t细胞与药学上可接受的载剂组合在混合物中。合适的载剂描述在,例如,remington'spharmaceuticalsciences(remington'spharmaceuticalsciences,第20版,mackpublishingcompany,easton,pa.,usa,2000)中。在此基础上,所述组合物并非排他性地包括与一种或多种药学上可接受的载剂或稀释剂组合,并且包含在具有适当ph并与生理流体等渗的缓冲溶液中的物质溶液。
合适的药学上可接受的载剂包括基本上化学惰性且无毒的组合物,所述组合物不干扰药物组合物的生物活性的有效性。合适的药物载剂的实例包括但不限于水、盐水溶液、甘油溶液、乙醇、n-(1(2,3-二油烯基氧基)丙基)n,n,n-三甲基氯化铵(dotma)、二油酰基磷脂酰基-乙醇胺(dope)和脂质体。此类组合物应含有治疗有效量的化合物以及适量的载剂,以便提供用于直接施用于患者的形式。
药物组合物还可以包括但不限于冻干粉末或水性或非水性无菌可注射溶液或悬浮液,其可以进一步包含抗氧化剂、缓冲液、抑菌剂和使组合物与预期接受者的组织或血液基本上相容的溶质。可以在此类组合物中存在的其他组分包括,例如,水、表面活性剂(如吐温)、醇、多元醇、甘油和植物油。临时注射溶液和悬浮液可由无菌粉末、颗粒、片剂或浓溶液或浓悬浮液制备。
治疗和使用方法
在一些实施方案中,本文公开了治疗有需要的个体中表达靶抗原的癌症的方法,其包括向该个体施用本文公开的工程化t细胞。本文进一步公开了本文公开的工程化t细胞在制备在有需要的个体中治疗癌症的药物中的用途。本文还公开了用于在有需要的个体中治疗癌症的本文公开的工程化t细胞。本文还公开了包含修饰的和未修饰的细胞,或包含具有或不具有未修饰的细胞的不同修饰细胞群体的t细胞混合物的用途。本领域普通技术人员将会理解,治疗量的修饰的t细胞本质上不必是同质的。
在一些实施方案中,本文公开了治疗有需要的个体中表达靶抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码t细胞-抗原偶联物(tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合靶抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的鼠ucht1(muucht1)配体的第二多核苷酸序列,该muucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合靶抗原。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少75%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少80%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少85%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少90%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少95%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含seqidno:26的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多肽序列与seqidno:26的序列同一性百分比是指除y182t突变外的氨基酸。
在一些实施方案中,本文公开了治疗有需要的个体中表达靶抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码t细胞-抗原偶联物(tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合靶抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合靶抗原。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少75%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少80%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少85%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少90%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少95%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含seqidno:29的氨基酸序列。
在一些实施方案中,本文公开了治疗有需要的个体中表达靶抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码t细胞-抗原偶联物(tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合靶抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化ucht1(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合靶抗原。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少75%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少80%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少85%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少90%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少95%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含seqidno:28的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多肽序列与seqidno:28的序列同一性百分比是指除y177t突变外的氨基酸。
在一些实施方案中,选择性结合靶抗原的配体(或靶标特异性配体)将t细胞-抗原偶联物(tri-tac)引导至靶细胞。在一些情况下,靶标特异性配体被称为抗原结合域。在一些情况下,靶标特异性配体是指直接或间接结合靶细胞的任何物质。在一些实施方案中,靶标特异性配体结合靶细胞上的抗原(由可以引发免疫应答的细胞产生的蛋白质)。在一些情况下,靶标特异性配体包括但不限于抗体及其片段,例如单链抗体,如单链抗体(scfv)、单结构域抗体、肽、拟肽、蛋白质、糖蛋白或与靶细胞和/或抗原结合的蛋白聚糖。在一些情况下,靶标特异性配体包括但不限于设计的锚蛋白重复序列蛋白质(darpin)、凝集素、knottin、centryrin、anticalin或肿瘤抗原的天然存在的配体,如生长因子、酶底物、受体或结合蛋白。在一些情况下,靶标特异性配体包括与靶细胞和/或抗原结合的非蛋白质化合物,包括但不限于碳水化合物、脂质、核酸或小分子。在一些情况下,靶标特异性配体是靶向特定细胞和/或抗原的经设计的锚蛋白重复序列(darpin)。在一些情况下,该靶标特异性配体是选择性结合her2(erbb-2)抗原的darpin。在一些情况下,该靶标特异性配体是特异性结合her2(erbb-2)抗原的darpin。在一些情况下,靶向her-2(erb-2)的darpin包含seqidno:7和seqidno:8。在一些情况下,靶标特异性配体是靶向特定细胞和/或抗原的单链抗体(scfv)。在一些情况下,靶标特异性配体是选择性结合bcma的scfv。在一些情况下,靶标特异性配体是特异性结合bcma的scfv。在一些情况下,结合bcma的scfv包含seqidno:21和seqidno:22。
在一些情况下,靶细胞是与包括但不限于癌症的疾病状态相关的细胞。在一些实施方案中,靶细胞是肿瘤细胞。在一些情况下,靶标特异性配体可以结合肿瘤细胞上的肿瘤抗原或肿瘤相关抗原。在一些情况下,靶抗原是肿瘤抗原。在一些情况下,蛋白质肿瘤抗原是8个或更多个氨基酸直至完整蛋白质的序列。在一些情况下,肿瘤抗原是8个氨基酸至全长蛋白质之间的任何数目的氨基酸,其包含在mhc复合体中代表的全长蛋白质的至少一个抗原性片段。肿瘤抗原的实例包括但不限于her-2(erbb-2)、b细胞成熟抗原(bcma)、甲胎蛋白(afp)、癌胚抗原(cea)、ca-125、muc-1、上皮肿瘤抗原(eta)、酪氨酸酶、黑素瘤相关抗原(mage)、前列腺特异性抗原(psa)、神经胶质瘤相关抗原、β-人绒毛膜促性腺激素、甲状腺球蛋白、rage-1、mn-caix、人端粒酶逆转录酶、ru1、ru2(as)、肠羧基酯酶、muthsp70-2、m-csf、prostase、pap、ny-eso-1、lage-1a、p53、prostein、psma、存活蛋白和端粒酶、前列腺癌肿瘤抗原-1(pcta-1)、elf2m、嗜中性粒细胞弹性蛋白酶、cd22、胰岛素生长因子(igf)-i、igf-ii、igf-i受体和间皮素。在一些情况下,该肿瘤抗原是her-2抗原。在一些情况下,her-2特异性配体包含选自曲妥珠单抗、帕妥珠单抗、拉帕替尼、奈拉替尼、ado-trastuzmabemtansine、gancotamab、margetuximab、timigutuzumab和厄马索单抗(ertumaxomab)的抗体的抗原结合域。在一些情况下,该肿瘤抗原是bcma抗原。在一些情况下,bcma特异性配体包含选自belantamabmafodotin和gsk2857916的抗体的抗原结合域。
在一些实施方案中,tri-tac与共受体刺激相组合地募集t细胞受体(tcr)。在一些情况下,tac包含结合与tcr复合物缔合的蛋白质的配体。在一些情况下,结合与tcr复合物缔合的蛋白质的配体包括直接或间接地与tcr的蛋白质结合的物质。与tcr缔合的蛋白质包括但不限于tcralpha(α)链、tcrbeta(β)链、tcrgamma(γ)链、tcrdelta(δ)链、cd3γ链、cd3δ链和cd3ε链。在一些实施方案中,结合与tcr复合物缔合的蛋白质的配体是tcralpha(α)链、tcrbeta(β)链、tcrgamma(γ)链、tcrdelta(δ)链、cd3γ链、cd3δ链和/或cd3ε链的抗体。在一些情况下,与tcr复合物缔合的蛋白质是cd3。在一些情况下,与tcr复合物缔合的蛋白质是cd3ε。在一些实施方案中,该配体是结合cd3的抗体或其片段。cd3抗体的实例包括但不限于莫罗单抗(muromonab)、奥昔珠单抗(otelixizumab)、替利珠单抗(teplizumab)和维西珠单抗(visilizumab)。在一些实施方案中,结合cd3的抗体是单链抗体,例如单链抗体(scfv)。在一些情况下,与cd3结合的配体是ucht1。在一些情况下,该ucht1配体结合cd3ε。在一些情况下,该ucht1配体是鼠配体。在一些情况下,该鼠ucht1配体包含seqidno:13和14。在一些情况下,该鼠ucht1配体结合cd3ε。在一些情况下,具有y182t突变的鼠ucht1配体结合cd3ε。在一些情况下,该人源化ucht1配体结合cd3ε。在一些情况下,具有y177t突变的人源化ucht1配体结合cd3ε。
在一些实施方案中,所述tcr信号传导域多肽包含跨膜域。在一些实施方案中,所述tcr信号传导域多肽包含胞质域。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些情况下,所述tcr信号传导域多肽包含tcr共受体的跨膜域和/或胞质域。在一些情况下,所述tcr共受体是cd4。在一些情况下,所述tcr信号传导域多肽包含cd4共受体的跨膜域和胞质域,它们包含seqidno:17和18。在一些情况下,该tcr共受体是cd8。在一些情况下,该tcr共受体是cd8α。在一些情况下,该tcr共受体是cd5。在一些情况下,该tcr共受体是cd9。在一些情况下,该tcr共受体是cd5。在一些情况下,该tcr共受体是cd22。在一些情况下,所述tcr信号传导域多肽包含tcr共刺激物的跨膜域和/或胞质域。在一些情况下,该tcr共刺激物是icos。在一些情况下,该tcr共刺激物是cd27。在一些情况下,该tcr共刺激物是cd28。在一些情况下,该tcr共刺激物是4-1bb(cd137)。在一些情况下,该tcr共刺激物是ox40(cd134)。在一些情况下,该tcr共刺激物是cd30。在一些情况下,该tcr共刺激物是cd40。在一些情况下,该tcr共刺激物是淋巴细胞功能相关抗原1(lfa-1)。在一些情况下,该tcr共刺激物是cd2。在一些情况下,该tcr共刺激物是cd7。在一些情况下,该tcr共刺激物是light。在一些情况下,该tcr共刺激物是nkg2c。在一些情况下,该tcr共刺激物是b7-h3。在一些情况下,该tcr共刺激物是特异性结合cd83的配体。在一些情况下,所述tcr信号传导域多肽包含tcr共抑制物的跨膜域和/或胞质域。在一些情况下,该tcr共抑制物是pd-1。在一些情况下,该tcr共抑制物是tim3。在一些情况下,该tcr共抑制物是lag-3。在一些情况下,该tcr共抑制物是tigit。在一些情况下,该tcr共抑制物是btla。在一些情况下,该tcr共抑制物是cd160。在一些情况下,该tcr共抑制物是cd37。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体或共刺激物蛋白质的胞质域和跨膜域。在一些情况下,该胞质域和跨膜域来自相同的共受体或共刺激物或者来自不同的共受体或共刺激物。在一些情况下,该胞质域和跨膜域任选地通过连接体连接。在一些实施方案中,所述tac进一步包含直接或间接作用以靶向或激活t细胞的其他多肽。
在一些实施方案中,第一多肽、第二多肽和第三多肽直接融合。在一些实施方案中,第一多肽、第二多肽和第三多肽通过至少一个连接体连接。在一些实施方案中,第一多肽和第二多肽直接融合,并且通过连接体与第三多肽连接。在一些实施方案中,第二多肽和第三多肽直接融合,并且通过连接体与第一多肽连接。在一些实施方案中,该连接体是肽连接体。在一些实施方案中,该肽连接体包含1至40个氨基酸。在一些实施方案中,该肽连接体包含1至30个氨基酸。在一些实施方案中,该肽连接体包含1至15个氨基酸。在一些实施方案中,该肽连接体包含1至10个氨基酸。在一些实施方案中,该肽连接体包含1至6个氨基酸。在一些实施方案中,该肽连接体包含30至40个氨基酸。在一些实施方案中,该肽连接体包含32至36个氨基酸。在一些实施方案中,该肽连接体包含5至30个氨基酸。在一些实施方案中,该肽连接体包含5个氨基酸。在一些实施方案中,该肽连接体包含10个氨基酸。在一些实施方案中,该肽连接体包含15个氨基酸。在一些实施方案中,该肽连接体包含20个氨基酸。在一些实施方案中,该肽连接体包含25个氨基酸。在一些实施方案中,该肽连接体包含30个氨基酸。在一些实施方案中,该肽连接体包括g4s3连接体。在一些情况下,在tri-tac中使用的连接体的其他实例是对应于seqidno:11、12、15、16、19和20的肽及其变体和片段。
在一些实施方案中,cd4共受体的跨膜域和胞质域与结合cd3的单链抗体融合。在一些情况下,将设计的锚蛋白重复序列(darpin)与cd4-ucht1嵌合体连接,以生成三功能t细胞-抗原偶联物(tri-tac)。在一些情况下,该tac将cd3分子和tcr引入脂质筏区域中,并且使lck接近tcr,这类似于自然的mhc结合。
可以治疗的癌症包括任何形式的赘生性疾病。可以治疗的癌症的实例包括但不限于乳腺癌、肺癌和白血病,例如混合谱系白血病(mll)、慢性淋巴细胞白血病(cll)或急性淋巴母细胞白血病(all)。其他癌症包括癌、母细胞瘤、黑素瘤、肉瘤、血液系统癌症、淋巴样恶性肿瘤、良性和恶性的肿瘤以及恶性肿瘤。该癌症可以包括非实体瘤或实体瘤。可以治疗的癌症包括未血管化的肿瘤,或者基本上尚未血管化的肿瘤,以及血管化的肿瘤。在一些情况下,该癌症是实体癌或包含实体肿瘤。在一些情况下,该癌症是液体癌或包含液体肿瘤。在一些情况下,该癌症是肺癌、乳腺癌、结肠癌、多发性骨髓瘤、胶质母细胞瘤、胃癌、卵巢癌、胃癌、结直肠癌、尿路上皮癌、子宫内膜癌或黑素瘤。在一些情况下,该癌症是肺癌。在一些情况下,该癌症是乳腺癌。在一些情况下,该癌症是结肠癌。在一些情况下,该癌症是多发性骨髓瘤。在一些情况下,该癌症是胶质母细胞瘤。在一些情况下,该癌症是胃癌。在一些情况下,该癌症是卵巢癌。在一些情况下,该癌症是胃癌。在一些情况下,该癌症是结直肠癌。在一些情况下,该癌症是尿路上皮癌。在一些情况下,该癌症是子宫内膜癌。在一些情况下,该癌症是黑素瘤。
在一些实施方案中,本文公开了治疗有需要的个体中表达her-2抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-her-2三功能t细胞-抗原偶联物(抗-her-2tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合her-2抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的鼠ucht1(muucht1)配体的第二多核苷酸序列,该muucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合her-2抗原。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少75%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少80%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少85%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少90%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少95%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含seqidno:26的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多肽序列与seqidno:26的序列同一性百分比是指除y182t突变外的氨基酸。
在一些实施方案中,本文还公开了治疗有需要的个体中表达her-2抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-her-2t细胞-抗原偶联物(抗-her-2tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合her-2抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合her-2抗原。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少75%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少80%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少85%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少90%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少95%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含seqidno:29的氨基酸序列。
在一些实施方案中,本文进一步公开了治疗有需要的个体中表达her-2抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-her-2t细胞-抗原偶联物(抗-her-2tri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合her-2抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化ucht1(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合her-2抗原。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少75%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少80%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少85%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少90%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少95%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含seqidno:28的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多肽序列与seqidno:28的序列同一性百分比是指除y177t突变外的氨基酸。
在一些实施方案中,选择性结合靶抗原的配体(或靶标特异性配体)将三功能t细胞-抗原偶联物(tri-tac)引导至靶细胞。在一些情况下,靶标特异性配体被称为抗原结合域。在一些情况下,靶标特异性配体是指直接或间接结合靶细胞的任何物质。在一些实施方案中,靶标特异性配体结合靶细胞上的抗原(由可以引发免疫应答的细胞产生的蛋白质)。在一些情况下,靶标特异性配体包括但不限于抗体及其片段,例如单链抗体,如单链抗体(scfv)、单结构域抗体、肽、拟肽、蛋白质、糖蛋白或与靶细胞和/或抗原结合的蛋白聚糖。在一些情况下,靶标特异性配体包括但不限于设计的锚蛋白重复序列蛋白质(darpin)、凝集素、knottin、centryrin、anticalin或肿瘤抗原的天然存在的配体,如生长因子、酶底物、受体或结合蛋白。在一些情况下,靶标特异性配体包括与靶细胞和/或抗原结合的非蛋白质化合物,包括但不限于碳水化合物、脂质、核酸或小分子。在一些情况下,靶标特异性配体是靶向特定细胞和/或抗原的经设计的锚蛋白重复序列(darpin)。在一些情况下,靶标特异性配体是选择性结合her2(erbb-2)抗原的darpin。在一些情况下,靶标特异性配体是特异性结合her2(erbb-2)抗原的darpin。在一些情况下,靶向her-2(erb-2)的darpin包含seqidno:7和seqidno:8。
在一些情况下,靶细胞是与包括但不限于癌症的疾病状态相关的细胞。在一些实施方案中,靶细胞是肿瘤细胞。在一些情况下,靶标特异性配体可以结合肿瘤细胞上的肿瘤抗原或肿瘤相关抗原。在一些情况下,靶抗原是肿瘤抗原。在一些情况下,蛋白质肿瘤抗原是8个或更多个氨基酸直至完整蛋白质的序列。在一些情况下,肿瘤抗原是8个氨基酸至全长蛋白质之间的任何数目的氨基酸,其包含在mhc复合体中代表的全长蛋白质的至少一个抗原性片段。肿瘤抗原的实例包括但不限于her-2(erbb-2)、b细胞成熟抗原(bcma)、甲胎蛋白(afp)、癌胚抗原(cea)、ca-125、muc-1、上皮肿瘤抗原(eta)、酪氨酸酶、黑素瘤相关抗原(mage)、前列腺特异性抗原(psa)、神经胶质瘤相关抗原、β-人绒毛膜促性腺激素、甲状腺球蛋白、rage-1、mn-caix、人端粒酶逆转录酶、ru1、ru2(as)、肠羧基酯酶、muthsp70-2、m-csf、prostase、pap、ny-eso-1、lage-1a、p53、prostein、psma、存活蛋白和端粒酶、前列腺癌肿瘤抗原-1(pcta-1)、elf2m、嗜中性粒细胞弹性蛋白酶、cd22、胰岛素生长因子(igf)-i、igf-ii、igf-i受体和间皮素。在一些情况下,该肿瘤抗原是her-2抗原。在一些情况下,her-2特异性配体包含选自曲妥珠单抗、帕妥珠单抗、拉帕替尼、奈拉替尼、ado-trastuzmabemtansine、gancotamab、margetuximab、timigutuzumab和厄马索单抗(ertumaxomab)的抗体的抗原结合域。
在一些实施方案中,tri-tac与共受体刺激相组合地募集t细胞受体(tcr)。在一些情况下,tac包含结合与tcr复合物缔合的蛋白质的配体。在一些情况下,结合与tcr复合物缔合的蛋白质的配体包括直接或间接地与tcr的蛋白质结合的物质。与tcr缔合的蛋白质包括但不限于tcralpha(α)链、tcrbeta(β)链、tcrgamma(γ)链、tcrdelta(δ)链、cd3γ链、cd3δ链和cd3ε链。在一些实施方案中,结合与tcr复合物缔合的蛋白质的配体是tcralpha(α)链、tcrbeta(β)链、tcrgamma(γ)链、tcrdelta(δ)链、cd3γ链、cd3δ链和/或cd3ε链的抗体。在一些情况下,与tcr复合物缔合的蛋白质是cd3。在一些情况下,与tcr复合物缔合的蛋白质是cd3ε。在一些实施方案中,该配体是结合cd3的抗体或其片段。cd3抗体的实例包括但不限于莫罗单抗(muromonab)、奥昔珠单抗(otelixizumab)、替利珠单抗(teplizumab)和维西珠单抗(visilizumab)。在一些实施方案中,结合cd3的抗体是单链抗体,例如单链抗体(scfv)。在一些情况下,与cd3结合的配体是ucht1。在一些情况下,该ucht1配体结合cd3ε。在一些情况下,该ucht1配体是鼠配体。在一些情况下,该鼠ucht1配体包含seqidno:13和14。在一些情况下,该鼠ucht1配体结合cd3ε。在一些情况下,具有y182t突变的鼠ucht1配体结合cd3ε。在一些情况下,该人源化ucht1配体结合cd3ε。在一些情况下,具有y177t突变的人源化ucht1配体结合cd3ε。
在一些实施方案中,所述tcr信号传导域多肽包含跨膜域。在一些实施方案中,所述tcr信号传导域多肽包含胞质域。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些情况下,所述tcr信号传导域多肽包含tcr共受体的跨膜域和/或胞质域。在一些情况下,所述tcr共受体是cd4。在一些情况下,所述tcr信号传导域多肽包含cd4共受体的跨膜域和胞质域,它们包含seqidno:17和18。在一些情况下,该tcr共受体是cd8。在一些情况下,该tcr共受体是cd8α。在一些情况下,该tcr共受体是cd5。在一些情况下,该tcr共受体是cd9。在一些情况下,该tcr共受体是cd5。在一些情况下,该tcr共受体是cd22。在一些情况下,所述tcr信号传导域多肽包含tcr共刺激物的跨膜域和/或胞质域。在一些情况下,该tcr共刺激物是icos。在一些情况下,该tcr共刺激物是cd27。在一些情况下,该tcr共刺激物是cd28。在一些情况下,该tcr共刺激物是4-1bb(cd137)。在一些情况下,该tcr共刺激物是ox40(cd134)。在一些情况下,该tcr共刺激物是cd30。在一些情况下,该tcr共刺激物是cd40。在一些情况下,该tcr共刺激物是淋巴细胞功能相关抗原1(lfa-1)。在一些情况下,该tcr共刺激物是cd2。在一些情况下,该tcr共刺激物是cd7。在一些情况下,该tcr共刺激物是light。在一些情况下,该tcr共刺激物是nkg2c。在一些情况下,该tcr共刺激物是b7-h3。在一些情况下,该tcr共刺激物是特异性结合cd83的配体。在一些情况下,所述tcr信号传导域多肽包含tcr共抑制物的跨膜域和/或胞质域。在一些情况下,该tcr共抑制物是pd-1。在一些情况下,该tcr共抑制物是tim3。在一些情况下,该tcr共抑制物是lag-3。在一些情况下,该tcr共抑制物是tigit。在一些情况下,该tcr共抑制物是btla。在一些情况下,该tcr共抑制物是cd160。在一些情况下,该tcr共抑制物是cd37。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体或共刺激物蛋白质的胞质域和跨膜域。在一些情况下,该胞质域和跨膜域来自相同的共受体或共刺激物或者来自不同的共受体或共刺激物。在一些情况下,该胞质域和跨膜域任选地通过连接体连接。在一些实施方案中,所述tac进一步包含直接或间接作用以靶向或激活t细胞的其他多肽。
在一些实施方案中,第一多肽、第二多肽和第三多肽直接融合。在一些实施方案中,第一多肽、第二多肽和第三多肽通过至少一个连接体连接。在一些实施方案中,第一多肽和第二多肽直接融合,并且通过连接体与第三多肽连接。在一些实施方案中,第二多肽和第三多肽直接融合,并且通过连接体与第一多肽连接。在一些实施方案中,该连接体是肽连接体。在一些实施方案中,该肽连接体包含1至40个氨基酸。在一些实施方案中,该肽连接体包含1至30个氨基酸。在一些实施方案中,该肽连接体包含1至15个氨基酸。在一些实施方案中,该肽连接体包含1至10个氨基酸。在一些实施方案中,该肽连接体包含1至6个氨基酸。在一些实施方案中,该肽连接体包含30至40个氨基酸。在一些实施方案中,该肽连接体包含32至36个氨基酸。在一些实施方案中,该肽连接体包含5至30个氨基酸。在一些实施方案中,该肽连接体包含5个氨基酸。在一些实施方案中,该肽连接体包含10个氨基酸。在一些实施方案中,该肽连接体包含15个氨基酸。在一些实施方案中,该肽连接体包含20个氨基酸。在一些实施方案中,该肽连接体包含25个氨基酸。在一些实施方案中,该肽连接体包含30个氨基酸。在一些实施方案中,该肽连接体包括g4s3连接体。在一些情况下,在tac中使用的连接体的其他实例是对应于seqidno:11、12、15、16、19和20的肽及其变体和片段。
在一些实施方案中,cd4共受体的跨膜域和胞质域与结合cd3的单链抗体融合。在一些情况下,该tac将cd3分子和tcr引入脂质筏区域中,并且使lck接近tcr,这类似于自然的mhc结合。在一些情况下,将设计的锚蛋白重复序列(darpin)与cd4-ucht1嵌合体连接,以生成三功能t细胞-抗原偶联物(tri-tac)。
可以治疗的癌症包括任何形式的赘生性疾病。可以治疗的癌症的实例包括但不限于乳腺癌、肺癌和白血病,例如混合谱系白血病(mll)、慢性淋巴细胞白血病(cll)或急性淋巴母细胞白血病(all)。其他癌症包括癌、母细胞瘤、黑素瘤、肉瘤、血液系统癌症、淋巴样恶性肿瘤、良性和恶性的肿瘤以及恶性肿瘤。该癌症可以包括非实体瘤或实体瘤。可以治疗的癌症包括未血管化的肿瘤,或者基本上尚未血管化的肿瘤,以及血管化的肿瘤。在一些情况下,该癌症是实体癌或包含实体肿瘤。在一些情况下,该癌症是液体癌或包含液体肿瘤。在一些情况下,该癌症是肺癌、乳腺癌、结肠癌、多发性骨髓瘤、胶质母细胞瘤、胃癌、卵巢癌、胃癌、结直肠癌、尿路上皮癌或子宫内膜癌。在一些情况下,该癌症是肺癌。在一些情况下,该癌症是乳腺癌。在一些情况下,该癌症是结肠癌。在一些情况下,该癌症是多发性骨髓瘤。在一些情况下,该癌症是胶质母细胞瘤。在一些情况下,该癌症是胃癌。在一些情况下,该癌症是卵巢癌。在一些情况下,该癌症是胃癌。在一些情况下,该癌症是结直肠癌。在一些情况下,该癌症是尿路上皮癌。在一些情况下,该癌症是子宫内膜癌。
在一些实施方案中,本文公开了治疗有需要的个体中表达bcma抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-bcmat细胞-抗原偶联物(抗-bcmatri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合bcma抗原的配体的第一多核苷酸序列;(b)编码具有y182t突变的鼠ucht1(muucht1)配体的第二多核苷酸序列,该muucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:26具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合bcma抗原。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少75%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少80%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少85%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少90%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含与seqidno:26具有至少95%序列同一性的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多核苷酸序列包含seqidno:26的氨基酸序列。在一些情况下,编码具有y182t突变的muucht1配体的第二多肽序列与seqidno:26的序列同一性百分比是指除y182t突变外的氨基酸。
在一些实施方案中,本文还公开了治疗有需要的个体中表达bcma抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-bcmat细胞-抗原偶联物(抗-bcmatri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合bcma抗原的配体的第一多核苷酸序列;(b)编码人源化ucht1(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:29具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合bcma抗原。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少75%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少80%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少85%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少90%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含与seqidno:29具有至少95%序列同一性的氨基酸序列。在一些情况下,编码huucht1配体的第二多核苷酸序列包含seqidno:29的氨基酸序列。
在一些实施方案中,本文进一步公开了治疗有需要的个体中表达bcma抗原的癌症的方法,其包括向该个体施用工程化t细胞,该工程化t细胞包含编码抗-bcmat细胞-抗原偶联物(抗-bcmatri-tac)的核酸序列,该核酸序列包含:(a)编码选择性结合bcma抗原的配体的第一多核苷酸序列;(b)编码具有y177t突变的人源化ucht1(huucht1)配体的第二多核苷酸序列,该huucht1配体包含的氨基酸序列与结合与t细胞受体(tcr)复合物缔合的蛋白质的seqidno:28具有至少70%的序列同一性;以及(c)编码tcr信号传导域多肽的第三多核苷酸序列。在一些情况下,该配体特异性结合bcma抗原。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少75%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少80%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少85%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少90%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含与seqidno:28具有至少95%序列同一性的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多核苷酸序列包含seqidno:28的氨基酸序列。在一些情况下,编码具有y177t突变的huucht1配体的第二多肽序列与seqidno:28的序列同一性百分比是指除y177t突变外的氨基酸。
在一些实施方案中,选择性结合靶抗原的配体(或靶标特异性配体)将t细胞-抗原偶联物(tac)引导至靶细胞。在一些情况下,靶标特异性配体被称为抗原结合域。在一些情况下,靶标特异性配体是指直接或间接结合靶细胞的任何物质。在一些实施方案中,靶标特异性配体结合靶细胞上的抗原(由可以引发免疫应答的细胞产生的蛋白质)。在一些情况下,靶标特异性配体包括但不限于抗体及其片段,例如单链抗体,如单链抗体(scfv)、单结构域抗体、肽、拟肽、蛋白质、糖蛋白或与靶细胞和/或抗原结合的蛋白聚糖。在一些情况下,靶标特异性配体包括但不限于设计的锚蛋白重复序列蛋白质(darpin)、凝集素、knottin、centryrin、anticalin或肿瘤抗原的天然存在的配体,如生长因子、酶底物、受体或结合蛋白。在一些情况下,靶标特异性配体包括与靶细胞和/或抗原结合的非蛋白质化合物,包括但不限于碳水化合物、脂质、核酸或小分子。在一些情况下,靶标特异性配体是靶向特定细胞和/或抗原的经设计的锚蛋白重复序列(darpin)。在一些情况下,靶标特异性配体是靶向特定细胞和/或抗原的单链抗体(scfv)。在一些情况下,靶标特异性配体是选择性结合bcma的scfv。在一些情况下,靶标特异性配体是特异性结合bcma的scfv。在一些情况下,结合bcma的scfv包含seqidno:21和seqidno:22。
在一些情况下,靶细胞是与包括但不限于癌症的疾病状态相关的细胞。在一些实施方案中,靶细胞是肿瘤细胞。在一些情况下,靶标特异性配体可以结合肿瘤细胞上的肿瘤抗原或肿瘤相关抗原。在一些情况下,靶抗原是肿瘤抗原。在一些情况下,蛋白质肿瘤抗原是8个或更多个氨基酸直至完整蛋白质的序列。在一些情况下,肿瘤抗原是8个氨基酸至全长蛋白质之间的任何数目的氨基酸,其包含在mhc复合体中代表的全长蛋白质的至少一个抗原性片段。肿瘤抗原的实例包括但不限于her-2(erbb-2)、b细胞成熟抗原(bcma)、甲胎蛋白(afp)、癌胚抗原(cea)、ca-125、muc-1、上皮肿瘤抗原(eta)、酪氨酸酶、黑素瘤相关抗原(mage)、前列腺特异性抗原(psa)、神经胶质瘤相关抗原、β-人绒毛膜促性腺激素、甲状腺球蛋白、rage-1、mn-caix、人端粒酶逆转录酶、ru1、ru2(as)、肠羧基酯酶、muthsp70-2、m-csf、prostase、pap、ny-eso-1、lage-1a、p53、prostein、psma、存活蛋白和端粒酶、前列腺癌肿瘤抗原-1(pcta-1)、elf2m、嗜中性粒细胞弹性蛋白酶、cd22、胰岛素生长因子(igf)-i、igf-ii、igf-i受体和间皮素。在一些情况下,该肿瘤抗原是bcma抗原。在一些情况下,bcma特异性配体包含选自belantamabmafodotin和gsk2857916的抗体的抗原结合域。
在一些实施方案中,tac与共受体刺激相组合地募集t细胞受体(tcr)。在一些情况下,tac包含结合与tcr复合物缔合的蛋白质的配体。在一些情况下,结合与tcr复合物缔合的蛋白质的配体包括直接或间接地与tcr的蛋白质结合的物质。与tcr缔合的蛋白质包括但不限于tcralpha(α)链、tcrbeta(β)链、tcrgamma(γ)链、tcrdelta(δ)链、cd3γ链、cd3δ链和cd3ε链。在一些实施方案中,结合与tcr复合物缔合的蛋白质的配体是tcralpha(α)链、tcrbeta(β)链、tcrgamma(γ)链、tcrdelta(δ)链、cd3γ链、cd3δ链和/或cd3ε链的抗体。在一些情况下,与tcr复合物缔合的蛋白质是cd3。在一些情况下,与tcr复合物缔合的蛋白质是cd3ε。在一些实施方案中,该配体是结合cd3的抗体或其片段。cd3抗体的实例包括但不限于莫罗单抗(muromonab)、奥昔珠单抗(otelixizumab)、替利珠单抗(teplizumab)和维西珠单抗(visilizumab)。在一些实施方案中,结合cd3的抗体是单链抗体,例如单链抗体(scfv)。在一些情况下,与cd3结合的配体是ucht1。在一些情况下,该ucht1配体结合cd3ε。在一些情况下,该ucht1配体是鼠配体。在一些情况下,该鼠ucht1配体包含seqidno:13和14。在一些情况下,该鼠ucht1配体结合cd3ε。在一些情况下,具有y182t突变的鼠ucht1配体结合cd3ε。在一些情况下,该人源化ucht1配体结合cd3ε。在一些情况下,具有y177t突变的人源化ucht1配体结合cd3ε。
在一些实施方案中,所述tcr信号传导域多肽包含跨膜域。在一些实施方案中,所述tcr信号传导域多肽包含胞质域。在一些实施方案中,所述tcr信号传导域多肽包含跨膜域和胞质域。在一些情况下,所述tcr信号传导域多肽包含tcr共受体的跨膜域和/或胞质域。在一些情况下,所述tcr共受体是cd4。在一些情况下,所述tcr信号传导域多肽包含cd4共受体的跨膜域和胞质域,它们包含seqidno:17和18。在一些情况下,该tcr共受体是cd8。在一些情况下,该tcr共受体是cd8α。在一些情况下,该tcr共受体是cd5。在一些情况下,该tcr共受体是cd9。在一些情况下,该tcr共受体是cd5。在一些情况下,该tcr共受体是cd22。在一些情况下,所述tcr信号传导域多肽包含tcr共刺激物的跨膜域和/或胞质域。在一些情况下,该tcr共刺激物是icos。在一些情况下,该tcr共刺激物是cd27。在一些情况下,该tcr共刺激物是cd28。在一些情况下,该tcr共刺激物是4-1bb(cd137)。在一些情况下,该tcr共刺激物是ox40(cd134)。在一些情况下,该tcr共刺激物是cd30。在一些情况下,该tcr共刺激物是cd40。在一些情况下,该tcr共刺激物是淋巴细胞功能相关抗原1(lfa-1)。在一些情况下,该tcr共刺激物是cd2。在一些情况下,该tcr共刺激物是cd7。在一些情况下,该tcr共刺激物是light。在一些情况下,该tcr共刺激物是nkg2c。在一些情况下,该tcr共刺激物是b7-h3。在一些情况下,该tcr共刺激物是特异性结合cd83的配体。在一些情况下,所述tcr信号传导域多肽包含tcr共抑制物的跨膜域和/或胞质域。在一些情况下,该tcr共抑制物是pd-1。在一些情况下,该tcr共抑制物是tim3。在一些情况下,该tcr共抑制物是lag-3。在一些情况下,该tcr共抑制物是tigit。在一些情况下,该tcr共抑制物是btla。在一些情况下,该tcr共抑制物是cd160。在一些情况下,该tcr共抑制物是cd37。在一些实施方案中,所述tcr信号传导域多肽包含tcr共受体或共刺激物蛋白质的胞质域和跨膜域。在一些情况下,该胞质域和跨膜域来自相同的共受体或共刺激物或者来自不同的共受体或共刺激物。在一些情况下,该胞质域和跨膜域任选地通过连接体连接。在一些实施方案中,所述tac进一步包含直接或间接作用以靶向或激活t细胞的其他多肽。
在一些实施方案中,第一多肽、第二多肽和第三多肽直接融合。在一些实施方案中,第一多肽、第二多肽和第三多肽通过至少一个连接体连接。在一些实施方案中,第一多肽和第二多肽直接融合,并且通过连接体与第三多肽连接。在一些实施方案中,第二多肽和第三多肽直接融合,并且通过连接体与第一多肽连接。在一些实施方案中,该连接体是肽连接体。在一些实施方案中,该肽连接体包含1至40个氨基酸。在一些实施方案中,该肽连接体包含1至30个氨基酸。在一些实施方案中,该肽连接体包含1至15个氨基酸。在一些实施方案中,该肽连接体包含1至10个氨基酸。在一些实施方案中,该肽连接体包含1至6个氨基酸。在一些实施方案中,该肽连接体包含30至40个氨基酸。在一些实施方案中,该肽连接体包含32至36个氨基酸。在一些实施方案中,该肽连接体包含5至30个氨基酸。在一些实施方案中,该肽连接体包含5个氨基酸。在一些实施方案中,该肽连接体包含10个氨基酸。在一些实施方案中,该肽连接体包含15个氨基酸。在一些实施方案中,该肽连接体包含20个氨基酸。在一些实施方案中,该肽连接体包含25个氨基酸。在一些实施方案中,该肽连接体包含30个氨基酸。在一些实施方案中,该肽连接体包括g4s3连接体。在一些情况下,在tac中使用的连接体的其他实例是对应于seqidno:11、12、15、16、19和20的肽及其变体和片段。
在一些实施方案中,cd4共受体的跨膜域和胞质域与结合cd3的单链抗体融合。在一些情况下,将设计的锚蛋白重复序列(darpin)与cd4-ucht1嵌合体连接,以生成三功能t细胞-抗原偶联物(tri-tac)。在一些情况下,该tri-tac将cd3分子和tcr引入脂质筏区域中,并且使lck接近tcr,这类似于自然的mhc结合。
可以治疗的癌症包括任何形式的赘生性疾病。可以治疗的癌症的实例包括但不限于乳腺癌、肺癌和白血病,例如混合谱系白血病(mll)、慢性淋巴细胞白血病(cll)或急性淋巴母细胞白血病(all)。其他癌症包括癌、母细胞瘤、黑素瘤、肉瘤、血液系统癌症、淋巴样恶性肿瘤、良性和恶性的肿瘤以及恶性肿瘤。该癌症可以包括非实体瘤或实体瘤。可以治疗的癌症包括未血管化的肿瘤,或者基本上尚未血管化的肿瘤,以及血管化的肿瘤。在一些情况下,该癌症是实体癌或包含实体肿瘤。在一些情况下,该癌症是液体癌或包含液体肿瘤。在一些情况下,该癌症是黑素瘤。
表1.序列表
1轻链,核苷酸1-324;连接体,核苷酸325-387;重链,核苷酸388-750
2轻链,氨基酸1-108;连接体,氨基酸109-128;重链,氨基酸129-250
3胞外连接体,核苷酸1-66;跨膜域,核苷酸67-132;胞质域,核苷酸133-254
4胞外连接体,氨基酸1-22;跨膜域,氨基酸23-44;胞质域,氨基酸45-84
实施例
给出以下实施例是为了说明本发明的各个实施方案的目的,而并非意味着以任何方式限制本发明。这些实施例以及目前代表优选实施方案的本文所述方法是示例性的,而非旨在限制本发明的范围。本领域技术人员将会想到包含在由权利要求范围所限定的本发明精神之内的其变化以及其他用途。
实施例1.tri-tac技术的表征
tri-tac技术的概述在图1a-图1c中提供。
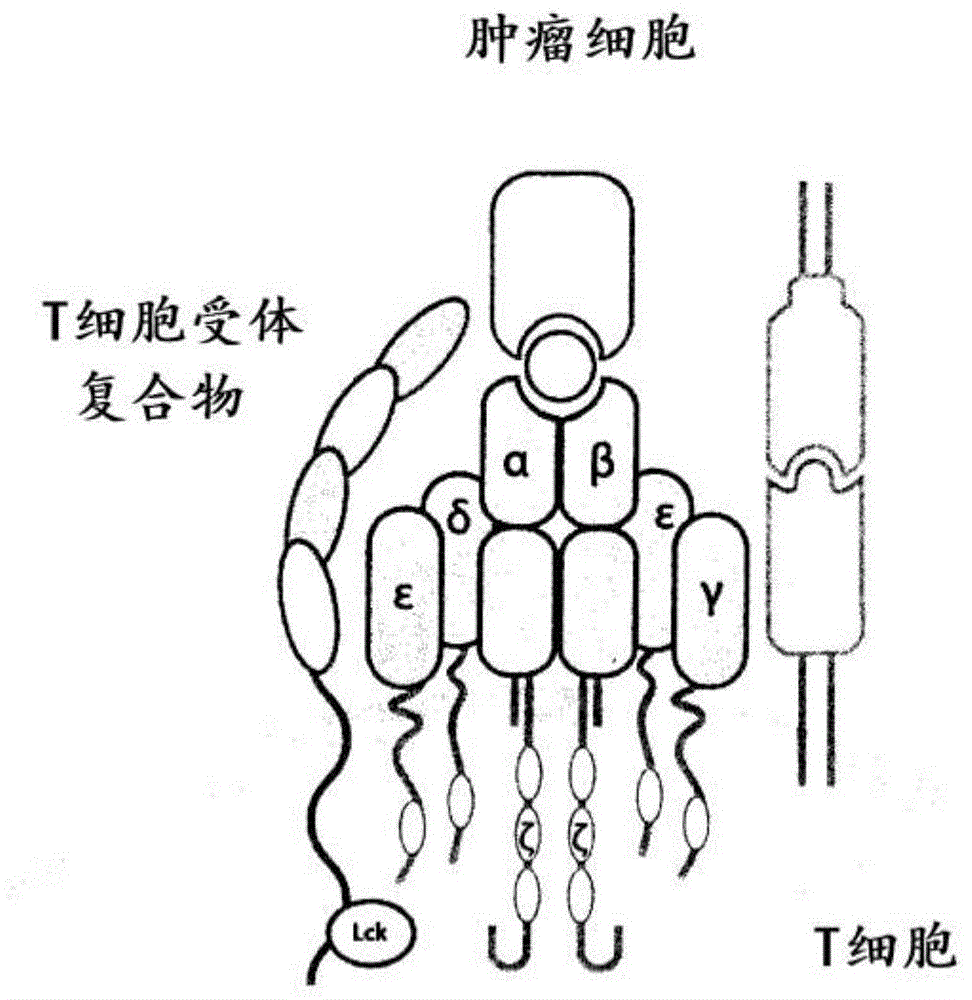
图1a显示了基于不同受体及其缔合的蛋白质配偶体的共装配,cd8t细胞活化的实例。最初,主要组织相容性复合体i呈递抗原(螺旋)。这被能够结合该抗原的t细胞受体(tcr)复合物识别。tcr复合物包含若干单独的亚单位。α/β结构域能够与在mhc-i上呈递的抗原直接相互作用。然后,α/β结构域与若干其他结构域(ε、γ、δ和ζ)相互作用,所有这些结构域都经由各种细胞内激活结构域参与t细胞活化。tcr复合物与cd8共受体同时地与mhc-i相互作用。cd8共受体以独立于抗原的方式结合mhc-i。cd8与lck直接相互作用,lck是对于激活tcr受体复合物至关重要的蛋白激酶。cd8与lck的相互作用还确保了它们与脂质筏(膜部分)微结构域的缔合,假设所述微结构域组织化并包封其他相关信号传导部分(深色球形)。然后,激活的后期阶段导致cd28募集。如果该相互作用级联平行发生若干次,则t细胞变为活化的,并且能够发挥其细胞毒性作用。
图1b提供了嵌合抗原受体(car)的概述。car试图通过将若干关键的激活结构域如ζ和cd28组合在单一合成工程化分子中来重现t细胞活化的复杂机制。然后,使用特异性结合域,car与选择的抗原直接相互作用。此处描绘了锚蛋白重复序列蛋白质(darpin)。据认为,平行发生的若干此类相互作用导致t细胞活化。
图1c是模拟自然激活过程的tri-tac技术的概述。开发了tri-tac,其通过tcr更好地重现自然信号传导,同时保留没有mhc限制的靶向。t细胞活化在tcr连接mhc之后发生,并且t细胞上的共受体(cd4或cd8)同时结合mhc分子内的保守区。共受体具体定位在“脂质筏”内,脂质筏是对于tcr信号复合物的形成特别重要的膜微结构域。除了确保tcr激活复合物的正确微结构域定位之外,这些共受体还直接结合lck——对t细胞活化至关重要的蛋白激酶。如先前所述,传统的嵌合受体或双功能蛋白质均不接合共受体分子或lck。创建了这样的分子,其中cd4共受体的跨膜区和胞内区(其分别定位于脂质筏并结合lck)与结合cd3的单链抗体(ucht1;seqidno:13和14)融合。该构建体被设计用于将cd3分子和tcr引入脂质筏区域中,并且使lck接近tcr,这类似于自然的mhc结合。为了靶向该受体,将设计的锚蛋白重复序列(darpin)与cd4-ucht1嵌合体连接,以生成三功能t细胞-抗原偶联物(tri-tac)。在该实例中,darpin对于原癌基因her-2(erbb-2)是特异性的。
可以将多种类别的配体结合域并入该tri-tac分子中(图2a)。本文中的实例示出了携带her-2特异性darpin(图2b)或bcma特异性scfv(图2c)的tri-tac。
图3示出了携带her-2特异性darpin的tri-tac的功能性。将人t细胞工程改造为表达本文公开的tri-tac或具有相同darpin的常规car。已确定,在所有方面,用tri-tac工程改造的t细胞显示出至少等同于常规car的功能性。有趣的是,对于2个参数(tnf-α产生和cd107a动员),在一些情况下观察到tri-tac比常规car更具活性。
图3a显示了与抗-her-2darpincar和对照t细胞相比,抗-her-2darpintri-tac的表面表达。通过与重组her-2一起孵育来检测嵌合受体。抗-her-2darpintri-tac在工程化t细胞表面上表达良好。然而,其最大表面表达低于抗-her-2darpincar构建体。图3b显示了工程化t细胞培养物的生长。用抗-cd3/抗-cd28dynabeads激活t细胞,并用编码tri-tac、car或无受体(对照)的慢病毒对该t细胞进行工程改造。2周后,car和对照培养物生长到相似的数量,而tri-tac培养物生长略微缓慢。
图4提供的数据证实了配体结合域和ucht1cd3结合域两者对tri-tac功能性的重要性。用携带her-2darpin的全长tri-tac(图4a,底部一行)、缺少darpin的tri-tac变体(图4a,最上一行),或缺少ucht1的tri-tac变体(图4a,中间一行)对t细胞进行工程改造。用her-2阳性肿瘤细胞刺激所有3个工程化的t细胞群体。用全长tri-tac工程改造的t细胞在刺激后可以产生ifn-γ、tnf-α和il-2,而这些变体在刺激后不能产生任何细胞因子。还将这3个t细胞群体与d2f2/e2细胞(表达her-2的细胞)或d2f2细胞(her-2阴性细胞)以4:1的效靶比共培养(图4b)。用全长tri-tac工程改造的t细胞表现出对d2f2/e2细胞的稳健杀伤,但不杀伤d2f2细胞。缺少darpin或ucht1的其他tri-tac变体没有展示出杀伤。
图5示出了lck与tri-tac的相互作用。在图5a中,将293tm细胞工程改造为与全长tri-tac或缺少与lck相互作用的胞质域的tri-tac变体组合地表达lck。用携带重组her-2蛋白的珠子对tri-tac受体进行免疫沉淀。用针对myc标签的抗体,通过western印迹法测量沉淀的tri-tac。用针对lck的抗体,通过western印迹法鉴定共沉淀的lck。β-肌动蛋白未被拉下,并且仅在上清液(s)中检测到。全长tri-tac和缺少胞质域的tri-tac均被有效地拉下,并在结合部分(b)中检测到。载体对照和无胞质域的tac显示出相当的背景lck信号水平。相对于对照,更大量的lck与全长tri-tac共免疫沉淀。图5b显示了以结合分数检测到的lck的密度测定法分析。相对于阴性对照校正信号。该数据支持lck能够与全长tri-tac相互作用。
图6显示了用载体对照(ngfr)、抗-her-2darpincar或抗-her-2darpintri-tac处理的小鼠的结果。使用异种移植小鼠模型。将ovcar-3肿瘤细胞皮下施用至小鼠,并使其生长直至肿瘤达到100-200mm3的大小。然后,静脉内施用工程化的t细胞。图6a显示了相对于治疗日的肿瘤大小归一化的相对肿瘤进展。抗-her-2darpintri-tac工程化的t细胞导致肿瘤体积迅速减小,对照没有效果,而car细胞减缓肿瘤的生长并显示出延迟的肿瘤大小减小。图6b示出了使用t细胞输注后体重的相对变化来监测动物的相对健康。对照和抗-her-2darpintri-tac工程化细胞在治疗后的小鼠体重方面均未显示显著变化。相反,抗-her-2darpincar处理的小鼠显示出显著的体重减轻,表明存在严重毒性。
讨论
使用嵌合受体将t细胞以独立于mhc的方式重定向至特定靶标是治疗癌症的新型方法,并且可以适用于其中来自病原体的抗原存在于质膜中的传染病。嵌合受体将导致:(1)针对靶细胞的特定细胞毒性,和(2)最小的脱靶毒性。常规car在这方面存在局限性,因为它们依赖于这样的合成结构:信号传导域位于非天然位置,在其中它们可能无法接收到适当的调节,因此对特定活性的细胞控制降低。
将tri-tac设计为重定向自然tcr的信号传导组分,而不采用信号传导域的异位定位。用以下原则设计tri-tac:(1)嵌合受体应与关键的激活蛋白质复合物相互作用并促进其有序装配,(2)嵌合受体应利用预先存在的细胞适应,如微结构域环境,以及(3)嵌合受体不应具有任何激活结构域。tri-tac能够有效地实现这一点,并且如数据所证明的,其激活速率等于(如果不是好于)第二代car的激活速率。
所述tri-tac适合用于与另外设计的共受体进一步整合,以进一步微调t细胞活化。tri-tac似乎表现出比现有car更低的毒性。抗-her-2darpincar在高的细胞与靶标之比下显示出轻微的脱靶杀伤,当用于治疗时,这可能会成为问题。然而,抗-her-2darpintri-tac——其功能与传统car一样——不显示脱靶效应。由于darpin以高亲和力结合靶标,因此脱靶效应可能在表达高水平的采用darpin的嵌合受体的细胞上更常见。因此,不受理论的约束,tri-tac的低表面表达可能是有利的,因为它降低了此类脱靶效应的可能性。
tri-tac技术的模块化性质允许微调t细胞活化过程。例如,tcr复合物的募集被具有较低cd3亲和力的工程化tri-tac分子调节。这模拟天然的低tcr亲和力,同时保留了高亲和力靶向结构域以检测癌症靶标。与经典car不同,tri-tac技术被工程改造为更密切地类似于这种情形。
提出的tri-tac技术是高度有效的分子工具,其能够(1)有效触发t细胞活化和细胞毒性,(2)能够通过模拟自然t细胞活化来实现这一点,并且(3)不需要其自身具有激活结构域。
实施例2.ucht1的突变影响tri-tac功能
图7a显示了与tri-tac变体文库相比的野生型抗-her-2darpintri-tac,在这些变体中,ucht1序列在预测与cd3结合的位点处随机诱变。为了建立该文库,将在ucht1和cd3ε的结合表面上发现的ucht1内的24个氨基酸进行随机诱变,产生理论数目为480个的独特克隆。图7a显示了突变体文库的示意图。表面表达的分析揭示,突变tri-tac的表达水平高于原始tri-tac(图7b)。测试了用原始tri-tac或突变体文库工程改造的t细胞的功能性。用突变体文库工程改造的t细胞保留了功能性,表明存在保留tri-tac功能的ucht1突变体(图7c)。
图8显示了携带选自所述文库的ucht1突变体的tri-tac的增强的表面表达。对用tri-tac文库工程改造的t细胞进行筛选,以针对tri-tac刺激t细胞的能力进行选择。从选择的文库中随机选择序列产生了突变体,其中在ucht中,a85被v代替,而t161被p代替(seqidno:23和24)。用原始抗-her-2darpintri-tac或携带具有a85v和t161p突变的ucht1的变体工程改造t细胞。已经注意到,相对于对照t细胞,用原始tri-tac工程改造的t细胞培养物偏向于cd8+t细胞的扩增。用a85v、t161p突变体tri-tac工程改造的t细胞未显示出偏向于cd8+t细胞扩增(图8a)。对表面表达的比较揭示,与原始tri-tac相比,携带a85v、t161p突变体的tri-tac以更高的水平在t细胞表面上表达(图8b)。关于功能性,用a85v、t161p突变体tri-tac工程改造的t细胞在用her-2刺激后产生较低水平的细胞因子,并且脱粒减少。这些结果表明,ucht1的突变可以影响tri-tac功能的多个方面。
在图9中,测试了另外七个点突变。其中四个突变体(t161r、t178r、n180r和n180g)导致tri-tac的表面表达增强(图9a)。在用a549或skov-3细胞刺激后,测试了各个突变体的功能性。除t178p以外,所有突变体均表现出细胞因子产生大大受损(图9b),并且没有一个突变体表现出针对her-2阳性靶细胞的细胞毒性(图9c)。这些结果表明,单个突变可以完全消除tri-tac功能。
图10显示了在选择随机诱变的文库之后富集特定氨基酸的分析结果。通过将选择后的ucht1文库的序列与(i)图7中描述的原始文库和(ii)包装在慢病毒中的相同文库进行比较来定义富集。通过比较以下的频率来确定在选择后富集的突变:(i)图8中描述的原始文库(黑线);(ii)包装到慢病毒中的文库(灰线);和(iii)选择后的文库(圆圈)。如实心圆圈所示,显示出独特富集的突变被认为是候选物(图10)。空心圆圈表示低数目的读取。发现的最明显的单个突变是在位置88-90处酪氨酸(y)被替换为苏氨酸(t)。
图11显示了ucht1和ucht1变体的序列比对。ucht1和ucht1(y182t)(seqidno:26)的序列显示在图11a中。ucht1和人源化ucht1(huucht1)(seqidno:29)的序列显示在图11b中。将y->t突变插入huucht1中的相应位点,以产生huucht1(y177t)(图11c)(seqidno:28)。
基于y182t和y177t突变体的表面表达表型和其他功能性质(即,细胞生长和细胞毒性)在体外对其进行分析。
图12说明,与携带ucht1和huucht1的tri-tac相比,携带y->t突变ucht1(y182t)或huucht1(y177t)的tri-tac在工程化t细胞的表面上分别以更高的水平表达。将人pbmc用抗-cd3/抗-cd28激活,用慢病毒(moi=10)转导,该慢病毒仅表达:(i)ngfr,(ii)原型tri-tac分子,(iii)携带ucht1(y182t)的tri-tac,(iv)携带huucht1的tri-tac,以及(v)携带huucht1(y177t)的tri-tac。14天后,将细胞用针对ngfr(转导标志物)、tac受体和t细胞标志物cd8和cd4的抗体染色。将细胞在cd8(上图)和cd4(下图)上门控。在每种情况下,y182t/y177t突变的存在都会改善tac受体的表面表达。这在多个供体中都观察到,并且显示了代表性的图示。
图12还揭示了与携带ucht1的原始tri-tac相比,携带huucht1的tri-tac的表面表达增强,表明在人源化过程中并入ucht1中的突变引入了影响表面表达的属性。
图13证明了用携带huucht1、muucht1(y182t)或huucht1(y177t)的tri-tac工程改造的t细胞比用携带ucht1的原始tri-tac工程改造的t细胞更大程度地扩增。将人pbmc用抗-cd3/抗-cd28激活,用慢病毒(moi=10)转导,该慢病毒仅表达:(i)ngfr,(ii)原型tri-tac分子,(iii)携带ucht1(y182t)的tri-tac,(iv)携带huucht1的tri-tac,以及(v)携带huucht1(y177t)的tri-tac。生长14天后,对细胞进行计数,以确定相对于基线的扩增倍数。将扩增倍数相对于仅用ngfr慢病毒工程改造的对照细胞的扩增进行归一化。两个不同供体的平均值在图13中示出。用具有ucht1(y182t)的tri-tac工程改造的t细胞比用携带ucht1的原始tri-tac工程改造的t细胞更大程度地扩增。用具有huucht1和huucht1(y177t)的tri-tac工程改造的t细胞扩增到相同程度;两者均表现出比携带ucht1的原始tri-tac更高的扩增。
再次,应当指出,相对于对照t细胞,携带ucht1的tri-tac显示出受损的扩增,而相对于对照,携带huucht1的tri-tac显示出扩增没有受损。
图14描述了tri-tac变体的细胞毒性。用原始tri-tac、携带huucht1的tri-tac和携带具有y->t突变的ucht1变体的tri-tac对t细胞进行工程改造。所有tri-tac均被抗-her-2darpin靶向。通过将工程化t细胞与her-2阳性靶标(skov-3和a549)或her-2阴性靶标loximvi一起孵育来评估细胞毒性。示出了两个不同供体的平均值。所有t细胞群体均显示出相当的细胞毒性。
如图14所示,用携带huucht1的tri-tac或携带具有y->t突变的huucht1变体[huucht1(y177t)]的tri-tac对t细胞进行工程改造。这两种tri-tac均被抗-her-2darpin靶向。用携带huucht1(y177t)但不携带肿瘤结合域的tri-tac工程改造对照t细胞。使用t细胞治疗图6中描述的ovcar-3异种移植小鼠模型。静脉内施用工程化t细胞,肿瘤达到100-200mm3的大小。该数据显示了相对于治疗日的肿瘤大小归一化的相对肿瘤进展。图17(图a-c)示出了由供体a产生的t细胞的结果。图17(图d-f)示出了由供体b产生的t细胞的结果。
图15显示了用携带对骨髓瘤靶标bcma具有特异性的scfv的tri-tac工程改造的t细胞的体外表征。用原始tri-tac或具有ucht1(y182t)的tri-tac对t细胞进行工程改造。用对照慢病毒、表达原始tri-tac的慢病毒或表达具有ucht1(y182t)的tri-tac的慢病毒以moi为5对t细胞进行工程改造。通过将工程化细胞与重组bcma-fc一起孵育,随后通过流式细胞术进行测量,来评估tri-tac的细胞表面表达。通过将工程化细胞或对照细胞与bcma阳性(kms-11)或bcma阴性(skov-3)细胞系共培养来评估细胞因子产生。共培养4h后,处理细胞以进行细胞因子的细胞内染色,并通过流式细胞术测量细胞因子产生。通过将工程化细胞或对照细胞与bcma阳性(kms-11)或bcma阴性(skov-3)细胞系共培养并在共培养6h后评估活力来评估细胞毒性。如前所述,与原始tri-tac相比,用tri-tacucht1(y182t)工程改造了更高比例的t细胞;tri-tacucht1(y182t)的表达水平也高于原始tri-tac(图15a)。尽管表达水平较高,但用原始tri-tac和tri-tacucht1(y182t)工程改造的t细胞在细胞因子产生(图15b)和对表达bcma的靶标(kms-11;图15c)的细胞毒性方面表现出相似的功能性。
图16示出了用携带ucht1(y182t)的tri-tac工程改造的t细胞的增强的抗肿瘤功效。如图15所示,用对照慢病毒、表达原始tri-tac的慢病毒或表达具有ucht1(y182t)的tri-tac的慢病毒以moi为5对t细胞进行工程改造。通过接种已经用增强萤火虫萤光素酶工程改造的kms-11细胞系(kms-11eff),在免疫缺陷的nrg小鼠中建立了多发性骨髓瘤肿瘤。在骨髓瘤肿瘤建立后7天,用间隔48h施用的分剂量的工程化t细胞治疗小鼠。小鼠接受等剂量的对照t细胞或用2种bcma特异性tri-tac(具有ucht1的原始tri-tac和具有ucht1(y182t)的变异tri-tac)工程改造的t细胞。定期通过体内生物发光成像来监测小鼠肿瘤负荷。图中的数据反映了通过生物发光增加而评估的,随着时间推移的肿瘤生长。在未接受治疗的小鼠和接受对照t细胞的小鼠中,肿瘤生长相当。在开始时,用经原始tri-tac工程改造的t细胞治疗的小鼠中的肿瘤生长减慢,但在治疗后约2周,这些小鼠中的肿瘤控制丧失。相反,用携带ucht1(y182t)的tri-tac工程改造的t细胞表现出肿瘤消退和长期肿瘤控制。
讨论
tri-tac是基于改变各种组分可以调节受体功能这一理念设计的。在此,通过突变ucht1中的单个氨基酸来研究对ucht1与cd3之间的接触区的修饰。首先,证明了ucht1中的点突变影响受体的表面表达。虽然大多数突变会增加表面表达,但某些突变会降低表面表达(例如,t161w、t178p)。其次,注意到对ucht1的突变也提高了制备过程中t细胞的总产量。最后,发现对ucht1的突变可以逆转所制备的产物向cd8+t细胞的偏向,这种偏向是原始tri-tac受体的共同特征。
在许多情况下,突变会损害细胞因子ifn-γ、tnf-α和il-2的产生,并且还损害细胞毒性。我们发现了一个特定的突变(y182t),其产生的tri-tac所具有的性质对制备而言是高度具有吸引力的(不损害t细胞扩增,不抑制cd4+t细胞扩增),而不会损害受体的功能性。此外,用tri-tac(ucht1y182t)工程改造的t细胞比用原始tri-tac工程改造的t细胞表现出更高的抗肿瘤活性。
携带人源化ucht1变体(huucht1)的tri-tac相对于原始tri-tac也显示出增强的制备性质。这些增强的特征是由于与人源化相关的huucht1中的突变。
综合起来,这些数据证明,ucht1的细微突变会极大地影响tri-tac的功能。尽管迄今为止这些研究都集中在肿瘤学应用上,但该知识还适用于tri-tac受体的其他应用(例如,自身免疫、变态反应),其中的突变,除本文所述的之外,对这些特定应用可能具有价值。
虽然本文已经示出并描述了本发明的优选实施方案,但对于本领域技术人员明显的是,这些实施方案仅以示例的方式提供。本领域技术人员在不脱离本发明的情况下现将想到许多变化、改变和替代。应当理解,在实施本发明的过程中可以采用本文所述的本发明实施方案的各种替代方案。旨在以所附权利要求书限定本发明的范围,并由此涵盖这些权利要求范围内的方法和结构及其等同物。
序列表
<110>麦克马斯特大学
<120>具有y182t突变的t细胞-抗原偶联物及其方法和用途
<130>27109-p57378pc00
<150>us62/571,354
<151>2017-10-12
<160>30
<170>patentinversion3.5
<210>1
<211>1575
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成多核苷酸
<400>1
atggatttccaggtccagattttctccttcctgctgatttccgcaagcgtcattatgtca60
cggggctccgacctgggcaaaaagctgctggaggccgctagggccgggcaggacgatgaa120
gtgagaatcctgatggccaacggggctgacgtgaatgctaaggatgagtacggcctgacc180
cccctgtatctggctacagcacacggccatctggagatcgtggaagtcctgctgaaaaac240
ggagccgacgtgaatgcagtcgatgccattgggttcactcctctgcacctggcagccttt300
atcggacatctggagattgcagaagtgctgctgaagcacggcgctgacgtgaacgcacag360
gataagttcggaaaaaccgcttttgacatcagcattggcaacggaaatgaagacctggct420
gaaatcctgcagaaactgaatgaacagaaactgattagcgaagaagacctgaaccccggg480
ggaggaggagggagcgggggaggaggcagcggcgggggaggctctggaggaggagggagc540
ggatccatggacatccagatgactcagaccacaagctccctgtctgcaagtctgggcgac600
cgggtgacaatctcctgcagagcctctcaggatattaggaactacctgaattggtatcag660
cagaaacctgatggcacagtcaagctgctgatctactataccagccggctgcactcaggc720
gtgccaagcaaattctcaggaagcggctccgggactgactactccctgaccatctctaac780
ctggagcaggaagatattgctacctatttctgccagcagggcaatacactgccctggact840
tttgccggaggcaccaaactggagatcaaggggggaggcgggagtggaggcgggggatca900
ggaggaggaggcagcggaggaggagggtccgaggtccagctgcagcagagcggaccagaa960
ctggtgaagcccggagcaagtatgaaaatctcctgtaaggcctcaggatacagcttcacc1020
ggctatacaatgaactgggtgaaacagtcccatggcaagaacctggaatggatggggctg1080
attaatccttacaaaggcgtcagcacctataatcagaagtttaaagacaaggccacactg1140
actgtggataagtctagttcaaccgcttacatggagctgctgtccctgacatctgaagac1200
agtgccgtgtactattgtgctcggtctggctactatggggacagtgattggtacttcgat1260
gtctggggacagggcactaccctgaccgtgttttctactagtggcggaggaggatcactc1320
gagagcggacaggtgctgctggaatccaatatcaaagtcctgcccacttggtctaccccc1380
gtgcagcctatggctctgattgtgctgggaggagtcgcaggactgctgctgtttatcggg1440
ctgggaattttcttttgcgtgcgctgccggcaccggagaaggcaggccgagcgcatgagc1500
cagatcaagcgactgctgagcgagaagaaaacctgtcagtgtccccatagattccagaag1560
acctgttcacccatt1575
<210>2
<211>525
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>2
metasppheglnvalglnilepheserpheleuleuileseralaser
151015
valilemetserargglyseraspleuglylyslysleuleugluala
202530
alaargalaglyglnaspaspgluvalargileleumetalaasngly
354045
alaaspvalasnalalysaspglutyrglyleuthrproleutyrleu
505560
alathralahisglyhisleugluilevalgluvalleuleulysasn
65707580
glyalaaspvalasnalavalaspalaileglyphethrproleuhis
859095
leualaalapheileglyhisleugluilealagluvalleuleulys
100105110
hisglyalaaspvalasnalaglnasplyspheglylysthralaphe
115120125
aspileserileglyasnglyasngluaspleualagluileleugln
130135140
lysleuasngluglnlysleuileserglugluaspleuasnprogly
145150155160
glyglyglyglyserglyglyglyglyserglyglyglyglysergly
165170175
glyglyglyserglysermetaspileglnmetthrglnthrthrser
180185190
serleuseralaserleuglyaspargvalthrilesercysargala
195200205
serglnaspileargasntyrleuasntrptyrglnglnlysproasp
210215220
glythrvallysleuleuiletyrtyrthrserargleuhissergly
225230235240
valproserlyspheserglyserglyserglythrasptyrserleu
245250255
thrileserasnleugluglngluaspilealathrtyrphecysgln
260265270
glnglyasnthrleuprotrpthrphealaglyglythrlysleuglu
275280285
ilelysglyglyglyglyserglyglyglyglyserglyglyglygly
290295300
serglyglyglyglysergluvalglnleuglnglnserglyproglu
305310315320
leuvallysproglyalasermetlysilesercyslysalasergly
325330335
tyrserphethrglytyrthrmetasntrpvallysglnserhisgly
340345350
lysasnleuglutrpmetglyleuileasnprotyrlysglyvalser
355360365
thrtyrasnglnlysphelysasplysalathrleuthrvalasplys
370375380
serserserthralatyrmetgluleuleuserleuthrsergluasp
385390395400
seralavaltyrtyrcysalaargserglytyrtyrglyaspserasp
405410415
trptyrpheaspvaltrpglyglnglythrthrleuthrvalpheser
420425430
thrserglyglyglyglyserleugluserglyglnvalleuleuglu
435440445
serasnilelysvalleuprothrtrpserthrprovalglnpromet
450455460
alaleuilevalleuglyglyvalalaglyleuleuleupheilegly
465470475480
leuglyilephephecysvalargcysarghisargargargglnala
485490495
gluargmetserglnilelysargleuleuserglulyslysthrcys
500505510
glncysprohisargpheglnlysthrcysserproile
515520525
<210>3
<211>1647
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成多核苷酸
<400>3
atggactttcaggtgcagattttctcttttctgctgatttccgcaagcgtcatcgagctc60
ggggggggggggtcaggatccatggacatccagatgactcagaccacaagctccctgagc120
gcatccctgggcgaccgagtgacaatctcatgcagagccagccaggatattaggaactac180
ctgaattggtatcagcagaaacctgacggcacagtcaagctgctgatctactatacttcc240
cggctgcactctggcgtgccaagtaaattctctgggagtggatcaggcactgactactca300
ctgaccatcagcaacctggagcaggaagatattgctacctatttctgccagcagggcaat360
acactgccctggacttttgcaggcgggaccaaactggagatcaagggcggcggcggaagt420
ggaggaggaggctcaggcggaggagggagcggcggaggaggcagcgaggtccagctgcag480
cagagcggaccagaactggtgaagcctggcgcatccatgaaaatctcttgtaaggcctct540
gggtacagtttcaccggatatacaatgaactgggtgaaacagtctcatggcaagaacctg600
gaatggatgggcctgattaatccttacaaaggcgtcagcacctataatcagaagtttaaa660
gacaaggccacactgactgtggataagtctagttcaaccgcttacatggagctgctgtca720
ctgacaagcgaagactccgccgtgtactattgcgctaggagcggatactatggcgactcc780
gattggtacttcgatgtctgggggcagggaactaccctgaccgtgtttagcactagtgga840
ggaggaggctctggaggaggagggagtggaggcgggggatcaggaggaggaggcagcgat900
atcatgtcacggggctccgacctgggcaaaaagctgctggaggccgctagggccgggcag960
gacgatgaagtgagaatcctgatggccaacggggctgacgtgaatgctaaggatgagtac1020
ggcctgacccccctgtatctggctacagcacacggccatctggagatcgtggaagtcctg1080
ctgaaaaacggagccgacgtgaatgcagtcgatgccattgggttcactcctctgcacctg1140
gcagcctttatcggacatctggagattgcagaagtgctgctgaagcacggcgctgacgtg1200
aacgcacaggataagttcggaaaaaccgcttttgacatcagcattggcaacggaaatgaa1260
gacctggctgaaatcctgcagaaactgaatgaacagaaactgattagcgaagaagacctg1320
aacgtcgacggaggaggagggtctggaggagggggaagtggcgggggaggcagcggggga1380
ggcgggtctctcgagagtggccaggtgctgctggaaagcaatatcaaggtcctgccaact1440
tggtccaccccagtgcagcctatggctctgattgtgctgggaggagtcgcaggactgctg1500
ctgtttatcggcctggggattttcttttgcgtgcgctgccggcaccggagaaggcaggct1560
gagcgcatgtctcagattaagcgactgctgagcgagaagaagacctgtcagtgcccccat1620
agattccagaaaacctgttcacccatt1647
<210>4
<211>547
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>4
metasppheglnvalglnilepheserpheleuleuileseralaser
151015
valilegluleuglyglyglyglyserglysermetaspileglnmet
202530
thrglnthrthrserserleuseralaserleuglyaspargvalthr
354045
ilesercysargalaserglnaspileargasntyrleuasntrptyr
505560
glnglnlysproaspglythrvallysleuleuiletyrtyrthrser
65707580
argleuhisserglyvalproserlyspheserglyserglysergly
859095
thrasptyrserleuthrileserasnleugluglngluaspileala
100105110
thrtyrphecysglnasnthrleuprotrpthrphealaglyglythr
115120125
lysleugluilelysglyglyglyglyserglyglyglyglysergly
130135140
glyglyglyserglyglyglyglysergluvalglnleuglnglnser
145150155160
glyprogluleuvallysproglyalasermetlysilesercyslys
165170175
alaserglytyrserphethrglytyrthrmetasntrpvallysgln
180185190
serhisglylysasnleuglutrpmetglyleuileasnprotyrlys
195200205
glyvalserthrtyrasnglnlysphelysasplysalathrleuthr
210215220
valasplysserserserthralatyrmetgluleuleuserleuthr
225230235240
sergluaspseralavaltyrtyrcysalaargserglytyrtyrgly
245250255
aspserasptrptyrpheaspvaltrpglyglnglythrthrleuthr
260265270
valpheserthrserglyglyglyglyserglyglyglyglysergly
275280285
glyglyglyserglyglyglyglyseraspilemetserargglyser
290295300
aspleuglylyslysleuleuglualaalaargalaglyglnaspasp
305310315320
gluvalargileleumetalaasnglyalaaspvalasnalalysasp
325330335
glutyrglyleuthrproleutyrleualathralahisglyhisleu
340345350
gluilevalgluvalleuleulysasnglyalaaspvalasnalaval
355360365
aspalaileglyphethrproleuhisleualaalapheileglyhis
370375380
leugluilealagluvalleuleulyshisglyalaaspvalasnala
385390395400
glnasplyspheglylysthralapheaspileserileglyasngly
405410415
asngluaspleualagluileleuglnlysleuasngluglnlysleu
420425430
ileserglugluaspleuasnvalaspglyglyglyglyserglygly
435440445
glyglyserglyglyglyglyserglyglyglyglyserleugluser
450455460
glyglnvalleuleugluserasnilelysvalleuprothrtrpser
465470475480
thrprovalglnprometalaleuilevalleuglyglyvalalagly
485490495
leuleuleupheileglyleuglyilephephecysvalargcysarg
500505510
hisargargargglnalagluargmetserglnilelysargleuleu
515520525
serglulyslysthrcysglncysprohisargpheglnlysthrcys
530535540
serproile
545
<210>5
<211>54
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成寡核苷酸
<400>5
atggatttccaggtccagattttctccttcctgctgatttccgcaagcgtcatt54
<210>6
<211>18
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成肽
<400>6
metasppheglnvalglnilepheserpheleuleuileseralaser
151015
valile
<210>7
<211>387
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成多核苷酸
<400>7
atgtcacggggctccgacctgggcaaaaagctgctggaggccgctagggccgggcaggac60
gatgaagtgagaatcctgatggccaacggggctgacgtgaatgctaaggatgagtacggc120
ctgacccccctgtatctggctacagcacacggccatctggagatcgtggaagtcctgctg180
aaaaacggagccgacgtgaatgcagtcgatgccattgggttcactcctctgcacctggca240
gcctttatcggacatctggagattgcagaagtgctgctgaagcacggcgctgacgtgaac300
gcacaggataagttcggaaaaaccgcttttgacatcagcattggcaacggaaatgaagac360
ctggctgaaatcctgcagaaactgaat387
<210>8
<211>129
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>8
metserargglyseraspleuglylyslysleuleuglualaalaarg
151015
alaglyglnaspaspgluvalargileleumetalaasnglyalaasp
202530
valasnalalysaspglutyrglyleuthrproleutyrleualathr
354045
alahisglyhisleugluilevalgluvalleuleulysasnglyala
505560
aspvalasnalavalaspalaileglyphethrproleuhisleuala
65707580
alapheileglyhisleugluilealagluvalleuleulyshisgly
859095
alaaspvalasnalaglnasplyspheglylysthralapheaspile
100105110
serileglyasnglyasngluaspleualagluileleuglnlysleu
115120125
asn
<210>9
<211>30
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成寡核苷酸
<400>9
gaacagaaactgattagcgaagaagacctg30
<210>10
<211>10
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成肽
<400>10
gluglnlysleuileserglugluaspleu
1510
<210>11
<211>75
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成寡核苷酸
<400>11
aaccccgggggaggaggagggagcgggggaggaggcagcggcgggggaggctctggagga60
ggagggagcggatcc75
<210>12
<211>25
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成肽
<400>12
asnproglyglyglyglyglyserglyglyglyglyserglyglygly
151015
glyserglyglyglyglyserglyser
2025
<210>13
<211>750
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成多核苷酸
<400>13
atggacatccagatgactcagaccacaagctccctgtctgcaagtctgggcgaccgggtg60
acaatctcctgcagagcctctcaggatattaggaactacctgaattggtatcagcagaaa120
cctgatggcacagtcaagctgctgatctactataccagccggctgcactcaggcgtgcca180
agcaaattctcaggaagcggctccgggactgactactccctgaccatctctaacctggag240
caggaagatattgctacctatttctgccagcagggcaatacactgccctggacttttgcc300
ggaggcaccaaactggagatcaaggggggaggcgggagtggaggcgggggatcaggagga360
ggaggcagcggaggaggagggtccgaggtccagctgcagcagagcggaccagaactggtg420
aagcccggagcaagtatgaaaatctcctgtaaggcctcaggatacagcttcaccggctat480
acaatgaactgggtgaaacagtcccatggcaagaacctggaatggatggggctgattaat540
ccttacaaaggcgtcagcacctataatcagaagtttaaagacaaggccacactgactgtg600
gataagtctagttcaaccgcttacatggagctgctgtccctgacatctgaagacagtgcc660
gtgtactattgtgctcggtctggctactatggggacagtgattggtacttcgatgtctgg720
ggacagggcactaccctgaccgtgttttct750
<210>14
<211>250
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>14
metaspileglnmetthrglnthrthrserserleuseralaserleu
151015
glyaspargvalthrilesercysargalaserglnaspileargasn
202530
tyrleuasntrptyrglnglnlysproaspglythrvallysleuleu
354045
iletyrtyrthrserargleuhisserglyvalproserlyspheser
505560
glyserglyserglythrasptyrserleuthrileserasnleuglu
65707580
glngluaspilealathrtyrphecysglnglnglyasnthrleupro
859095
trpthrphealaglyglythrlysleugluilelysglyglyglygly
100105110
serglyglyglyglyserglyglyglyglyserglyglyglyglyser
115120125
gluvalglnleuglnglnserglyprogluleuvallysproglyala
130135140
sermetlysilesercyslysalaserglytyrserphethrglytyr
145150155160
thrmetasntrpvallysglnserhisglylysasnleuglutrpmet
165170175
glyleuileasnprotyrlysglyvalserthrtyrasnglnlysphe
180185190
lysasplysalathrleuthrvalasplysserserserthralatyr
195200205
metgluleuleuserleuthrsergluaspseralavaltyrtyrcys
210215220
alaargserglytyrtyrglyaspserasptrptyrpheaspvaltrp
225230235240
glyglnglythrthrleuthrvalpheser
245250
<210>15
<211>27
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成寡核苷酸
<400>15
actagtggcggaggaggatcactcgag27
<210>16
<211>9
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成肽
<400>16
thrserglyglyglyglyserleuglu
15
<210>17
<211>252
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成多核苷酸
<400>17
agcggacaggtgctgctggaatccaatatcaaagtcctgcccacttggtctacccccgtg60
cagcctatggctctgattgtgctgggaggagtcgcaggactgctgctgtttatcgggctg120
ggaattttcttttgcgtgcgctgccggcaccggagaaggcaggccgagcgcatgagccag180
atcaagcgactgctgagcgagaagaaaacctgtcagtgtccccatagattccagaagacc240
tgttcacccatt252
<210>18
<211>84
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>18
serglyglnvalleuleugluserasnilelysvalleuprothrtrp
151015
serthrprovalglnprometalaleuilevalleuglyglyvalala
202530
glyleuleuleupheileglyleuglyilephephecysvalargcys
354045
arghisargargargglnalagluargmetserglnilelysargleu
505560
leuserglulyslysthrcysglncysprohisargpheglnlysthr
65707580
cysserproile
<210>19
<211>66
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成寡核苷酸
<400>19
agcggacaggtgctgctggaatccaatatcaaagtcctgcccacttggtctacccccgtg60
cagcct66
<210>20
<211>22
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成肽
<400>20
serglyglnvalleuleugluserasnilelysvalleuprothrtrp
151015
serthrprovalglnpro
20
<210>21
<211>801
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成多核苷酸
<400>21
atggattttcaggtgcagattttcagcttcctgctaatcagtgcctcagtcataatgtct60
agagacatcgtgctgacccagagcccccccagcctggccatgtctctgggcaagagagcc120
accatcagctgccgggccagcgagagcgtgaccatcctgggcagccacctgatccactgg180
tatcagcagaagcccggccagccccccaccctgctgatccagctcgccagcaatgtgcag240
accggcgtgcccgccagattcagcggcagcggcagcagaaccgacttcaccctgaccatc300
gaccccgtggaagaggacgacgtggccgtgtactactgcctgcagagccggaccatcccc360
cggacctttggcggaggcaccaaactggaaatcaagggcagcaccagcggctccggcaag420
cctggctctggcgagggcagcacaaagggacagattcagctggtgcagagcggccctgag480
ctgaagaaacccggcgagacagtgaagatcagctgcaaggcctccggctacaccttcacc540
gactacagcatcaactgggtgaaaagagcccctggcaagggcctgaagtggatgggctgg600
atcaacaccgagacaagagagcccgcctacgcctacgacttccggggcagattcgccttc660
agcctggaaaccagcgccagcaccgcctacctgcagatcaacaacctgaagtacgaggac720
accgccacctacttttgcgccctggactacagctacgccatggactactggggccagggc780
accagcgtgaccgtgtccagc801
<210>22
<211>267
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>22
metasppheglnvalglnilepheserpheleuleuileseralaser
151015
valilemetserargaspilevalleuthrglnserproproserleu
202530
alametserleuglylysargalathrilesercysargalaserglu
354045
servalthrileleuglyserhisleuilehistrptyrglnglnlys
505560
proglyglnproprothrleuleuileglnleualaserasnvalgln
65707580
thrglyvalproalaargpheserglyserglyserargthraspphe
859095
thrleuthrileaspprovalglugluaspaspvalalavaltyrtyr
100105110
cysleuglnserargthrileproargthrpheglyglyglythrlys
115120125
leugluilelysglyserthrserglyserglylysproglysergly
130135140
gluglyserthrlysglyglnileglnleuvalglnserglyproglu
145150155160
leulyslysproglygluthrvallysilesercyslysalasergly
165170175
tyrthrphethrasptyrserileasntrpvallysargalaprogly
180185190
lysglyleulystrpmetglytrpileasnthrgluthrargglupro
195200205
alatyralatyrasppheargglyargphealapheserleugluthr
210215220
seralaserthralatyrleuglnileasnasnleulystyrgluasp
225230235240
thralathrtyrphecysalaleuasptyrsertyralametasptyr
245250255
trpglyglnglythrservalthrvalserser
260265
<210>23
<211>750
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成多核苷酸
<400>23
atggacatccagatgactcagaccacaagctccctgtctgcaagtctgggcgaccgggtg60
acaatctcctgcagagcctctcaggatattaggaactacctgaattggtatcagcagaaa120
cctgatggcacagtcaagctgctgatctactataccagccggctgcactcaggcgtgcca180
agcaaattctcaggaagcggctccgggactgactactccctgaccatctctaacctggag240
caggaagatattgttacctatttctgccagcagggcaatacactgccctggacttttgcc300
ggaggcaccaaactggagatcaaggggggaggcgggagtggaggcgggggatcaggagga360
ggaggcagcggaggaggagggtccgaggtccagctgcagcagagcggaccagaactggtg420
aagcccggagcaagtatgaaaatctcctgtaaggcctcaggatacagcttcaccggctat480
ccgatgaactgggtgaaacagtcccatggcaagaacctggaatggatggggctgattaat540
ccttacaaaggcgtcagcacctataatcagaagtttaaagacaaggccacactgactgtg600
gataagtctagttcaaccgcttacatggagctgctgtccctgacatctgaagacagtgcc660
gtgtactattgtgctcggtctggctactatggggacagtgattggtacttcgatgtctgg720
ggacagggcactaccctgaccgtgttttct750
<210>24
<211>250
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>24
metaspileglnmetthrglnthrthrserserleuseralaserleu
151015
glyaspargvalthrilesercysargalaserglnaspileargasn
202530
tyrleuasntrptyrglnglnlysproaspglythrvallysleuleu
354045
iletyrtyrthrserargleuhisserglyvalproserlyspheser
505560
glyserglyserglythrasptyrserleuthrileserasnleuglu
65707580
glngluaspilevalthrtyrphecysglnglnglyasnthrleupro
859095
trpthrphealaglyglythrlysleugluilelysglyglyglygly
100105110
serglyglyglyglyserglyglyglyglyserglyglyglyglyser
115120125
gluvalglnleuglnglnserglyprogluleuvallysproglyala
130135140
sermetlysilesercyslysalaserglytyrserphethrglytyr
145150155160
prometasntrpvallysglnserhisglylysasnleuglutrpmet
165170175
glyleuileasnprotyrlysglyvalserthrtyrasnglnlysphe
180185190
lysasplysalathrleuthrvalasplysserserserthralatyr
195200205
metgluleuleuserleuthrsergluaspseralavaltyrtyrcys
210215220
alaargserglytyrtyrglyaspserasptrptyrpheaspvaltrp
225230235240
glyglnglythrthrleuthrvalpheser
245250
<210>25
<211>750
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成多核苷酸
<400>25
atggacatccagatgactcagaccacaagctccctgtctgcaagtctgggcgaccgggtg60
acaatctcctgcagagcctctcaggatattaggaactacctgaattggtatcagcagaaa120
cctgatggcacagtcaagctgctgatctactataccagccggctgcactcaggcgtgcca180
agcaaattctcaggaagcggctccgggactgactactccctgaccatctctaacctggag240
caggaagatattgctacctatttctgccagcagggcaatacactgccctggacttttgcc300
ggaggcaccaaactggagatcaaggggggaggcgggagtggaggcgggggatcaggagga360
ggaggcagcggaggaggagggtccgaggtccagctgcagcagagcggaccagaactggtg420
aagcccggagcaagtatgaaaatctcctgtaaggcctcaggatacagcttcaccggctat480
acaatgaactgggtgaaacagtcccatggcaagaacctggaatggatggggctgattaat540
cctaccaaaggcgtcagcacctataatcagaagtttaaagacaaggccacactgactgtg600
gataagtctagttcaaccgcttacatggagctgctgtccctgacatctgaagacagtgcc660
gtgtactattgtgctcggtctggctactatggggacagtgattggtacttcgatgtctgg720
ggacagggcactaccctgaccgtgttttct750
<210>26
<211>250
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>26
metaspileglnmetthrglnthrthrserserleuseralaserleu
151015
glyaspargvalthrilesercysargalaserglnaspileargasn
202530
tyrleuasntrptyrglnglnlysproaspglythrvallysleuleu
354045
iletyrtyrthrserargleuhisserglyvalproserlyspheser
505560
glyserglyserglythrasptyrserleuthrileserasnleuglu
65707580
glngluaspilealathrtyrphecysglnglnglyasnthrleupro
859095
trpthrphealaglyglythrlysleugluilelysglyglyglygly
100105110
serglyglyglyglyserglyglyglyglyserglyglyglyglyser
115120125
gluvalglnleuglnglnserglyprogluleuvallysproglyala
130135140
sermetlysilesercyslysalaserglytyrserphethrglytyr
145150155160
thrmetasntrpvallysglnserhisglylysasnleuglutrpmet
165170175
glyleuileasnprothrlysglyvalserthrtyrasnglnlysphe
180185190
lysasplysalathrleuthrvalasplysserserserthralatyr
195200205
metgluleuleuserleuthrsergluaspseralavaltyrtyrcys
210215220
alaargserglytyrtyrglyaspserasptrptyrpheaspvaltrp
225230235240
glyglnglythrthrleuthrvalpheser
245250
<210>27
<211>735
<212>dna
<213>人工序列
<220>
<223>人工序列的描述:合成多核苷酸
<400>27
atggatatccagatgacccagtccccgagctccctgtccgcctctgtgggcgatagggtc60
accatcacctgccgtgccagtcaggacatccgtaattatctgaactggtatcaacagaaa120
ccaggaaaagctccgaaactactgatttactatacctcccgcctggagtctggagtccct180
tctcgcttctctggttctggttctgggacggattacactctgaccatcagcagtctgcaa240
ccggaagacttcgcaacttattactgtcagcaaggtaatactctgccgtggacgttcgga300
cagggcaccaaggtggagatcaaaggcggcggcggaagtggaggaggaggctcaggcgga360
ggagggagcgaggttcagctggtggagtctggcggtggcctggtgcagccagggggctca420
ctccgtttgtcctgtgcagcttctggctactcctttaccggctacactatgaactgggtg480
cgtcaggccccaggtaagggcctggaatgggttgcactgattaatcctaccaaaggtgtt540
agtacctacaaccagaagttcaaggaccgtttcactataagcgtagataaatccaaaaac600
acagcctacctgcaaatgaacagcctgcgtgctgaggacactgccgtctattattgtgct660
agaagcggatactacggcgatagtgactggtattttgacgtgtggggtcaaggaaccctg720
gtcaccgtctcctcg735
<210>28
<211>245
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>28
metaspileglnmetthrglnserproserserleuseralaserval
151015
glyaspargvalthrilethrcysargalaserglnaspileargasn
202530
tyrleuasntrptyrglnglnlysproglylysalaprolysleuleu
354045
iletyrtyrthrserargleugluserglyvalproserargpheser
505560
glyserglyserglythrasptyrthrleuthrileserserleugln
65707580
progluaspphealathrtyrtyrcysglnglnglyasnthrleupro
859095
trpthrpheglyglnglythrlysvalgluilelysglyglyglygly
100105110
serglyglyglyglyserglyglyglyglysergluvalglnleuval
115120125
gluserglyglyglyleuvalglnproglyglyserleuargleuser
130135140
cysalaalaserglytyrserphethrglytyrthrmetasntrpval
145150155160
argglnalaproglylysglyleuglutrpvalalaleuileasnpro
165170175
thrlysglyvalserthrtyrasnglnlysphelysaspargphethr
180185190
ileservalasplysserlysasnthralatyrleuglnmetasnser
195200205
leuargalagluaspthralavaltyrtyrcysalaargserglytyr
210215220
tyrglyaspserasptrptyrpheaspvaltrpglyglnglythrleu
225230235240
valthrvalserser
245
<210>29
<211>245
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成多肽
<400>29
metaspileglnmetthrglnserproserserleuseralaserval
151015
glyaspargvalthrilethrcysargalaserglnaspileargasn
202530
tyrleuasntrptyrglnglnlysproglylysalaprolysleuleu
354045
iletyrtyrthrserargleugluserglyvalproserargpheser
505560
glyserglyserglythrasptyrthrleuthrileserserleugln
65707580
progluaspphealathrtyrtyrcysglnglnglyasnthrleupro
859095
trpthrpheglyglnglythrlysvalgluilelysglyglyglygly
100105110
serglyglyglyglyserglyglyglyglysergluvalglnleuval
115120125
gluserglyglyglyleuvalglnproglyglyserleuargleuser
130135140
cysalaalaserglytyrserphethrglytyrthrmetasntrpval
145150155160
argglnalaproglylysglyleuglutrpvalalaleuileasnpro
165170175
tyrlysglyvalserthrtyrasnglnlysphelysaspargphethr
180185190
ileservalasplysserlysasnthralatyrleuglnmetasnser
195200205
leuargalagluaspthralavaltyrtyrcysalaargserglytyr
210215220
tyrglyaspserasptrptyrpheaspvaltrpglyglnglythrleu
225230235240
valthrvalserser
245
<210>30
<211>15
<212>prt
<213>人工序列
<220>
<223>人工序列的描述:合成肽
<400>30
glyglyglyglyserglyglyglyglyserglyglyglyglyser
151015
- 还没有人留言评论。精彩留言会获得点赞!