一种阿司匹林药物相关基因基因多态性检测的引物组、试剂盒及检测方法与流程
本发明涉及生物技术及医学领域,更具体地,涉及一种阿司匹林药物相关基因基因多态性检测的引物组、试剂盒及检测方法。
背景技术:
:阿司匹林是治疗急性冠状动脉综合征和经皮冠状动脉介入术后抗栓的基础药物,广泛应用于心脑血管疾病一级和二级预防。临床发现部分患者尽管长期低剂量服用阿司匹林仍不能有效抑制血小板的活性,即阿司匹林抵抗,其发生率约50%~60%,且存在明显种族差异性。研究表明,基因多态性在阿司匹林抵抗中起着重要作用,主要集中在gpiiiap1a1/a2、pear1基因多态性。gpiiiap1a2是阿司匹林抵抗主要基因,该基因突变使gpiib/iiia受体结构发生改变,使血小板之间发生交叉连接,导致血小板聚集。研究发现,发生阿司匹林抵抗患者携带p1a2等位基因的频率明显高于阿司匹林敏感患者,且p1a2/a2纯合突变型患者服用阿司匹林后疗效均不理想。携带突变型p1a2等位基因患者行支架术后,其亚急性血栓事件发生率是p1a1纯合野生型患者的5倍,需要更高剂量的阿司匹林才能达到抗凝效果。pear1是参与血小板激活途径的一种横跨细胞膜的分子,它的磷酸化作用可以促进血小板的聚集。研究发现,pear1的rs12041331基因多态性变化与患者的抗血小板治疗反应性密切相关,其中,pear1gg等位基因型患者对阿司匹林应答效果好,aa或ag基因型患者支架植入术后服用阿司匹林,其发生心肌梗死和死亡率高。因此,建议在使用阿司匹林前,检测gpiiiap1a1/a2和pear1,临床药师将针对患者基因型对患者进行疗效预测,并对高风险患者提前干预,以降低患者用药风险,保障临床用药安全、有效。关于基因突变检测方法有很多,各国学者对此都进行了大量研究。己经报道的方法包括直接测序法、dhplc(denaturinghighperformanceliquidchromatography,变性高效液相色谱分析)、pcr(聚合酶链式反应)-sscp(单链构象多态性)/rflp(限制性片段长度多态性)、scorpionsarms(蝎形探针扩增阻滞突变系统)、taqmanpcr法、me-pcr法等。这些方法各有优缺点,其中在临床和科研中较为常用的方法为直接测序法以及arms(amplificationrefractorymutationsystem,扩增阻滞突变系统)法。直接测序法检测能力有限,其检测灵敏度约20%左右,而且步骤复杂,整个检测过程涉及pcr-电泳-测序-测序结果的解读等一系列的步骤,费时费力,但是该方法的优点是能够发现一些新的未知突变。arms方法是将分子信标(探针)与特异性的arms引物相结合创造出来的,arms引物3’端设计在突变位点,最后一个碱基与突变碱基配对,釆用无3’→5’外切酶活性的taqdna聚合酶,特异性的识别引物的3’末端,只有引物3’末端完全配对时,才能正常扩增,当引物3’末端发生错配时,不能有效的扩增。当引物与突变模板结合并延伸出相应的产物后,探针两端的荧光基团和淬灭基团分离而产生荧光。目前,市场上相关试剂盒包括qiagen公司和厦门艾德公司,价格昂贵。技术实现要素:本发明的目的在于克服现有技术存在的上述缺陷,提供一种阿司匹林药物相关基因基因多态性检测的引物组、试剂盒及检测方法,釆用arms技术与sybr染料相结合的方法,该方法灵敏度高,特异性强,方法简单,结果准确,且检测成本大大降低。为实现上述目的,本发明的技术方案如下:一种阿司匹林药物相关基因基因多态性检测的引物组,其特征在于,包括,gpiiia(176)基因多态性的检测引物5′-tcttacaggccctgcctgt-3′seqidno:15′-ttacaggccctgcctac-3′seqidno:25′-cagagcccttgtcgctga-3′seqidno:3pear1(1568697)基因多态性的检测引物5′-tctgctgtctcacttcaa-3′seqidno:45′-cttctgctgtctcacttctg-3′seqidno:55′-ctaaactccagctcagct-3′seqidno:6内控的检测引物5′-agcaagcaggagtatgacg-3'seqidno:75′-gaaagggtgtaacgcaact-3'seqidno:8。一种阿司匹林药物相关基因基因多态性检测的试剂盒,其特征在于,包括如权利要求1所述的引物组、pcr缓冲液、阳性对照液和阴性对照液。优选地,所述pcr缓冲液包括3’→5’外切酶活性高保真taq酶、1.0-5.0mm的mgcl2、1.0-5.0mm的datp、1.0-5.0mm的dttp、1.0-5.0mm的dgtp、1.0-5.0mm的dctp以及sybrgreeni。优选地,所述阳性对照液为gpiiia质粒混合液以及pear1质粒混合液,gpiiia质粒混合液含有带有待检测突变位点gpiiia的等位基因,pear1质粒混合液含有带有待检测突变位点pear1的等位基因。优选地,所述阴性对照液为tris-hcl缓冲液,所述的tris-hcl缓冲液的浓度为7-13mm,ph为7.5-8.5。一种阿司匹林药物相关基因基因多态性的检测方法,其特征在于,包括以下步骤步骤s1:对待检测样本抽提dna样本;步骤s2:取出适量pcr缓冲液,与各基因多态性的检测引物形成的野生型和突变型引物组、内参的检测引物组分别混匀形成各反应液,分装至反应管涡旋振荡10秒,2000rpm离心15秒,之后,分装至各pcr反应管;步骤s3:取出适量pcr缓冲液,与各基因多态性的检测引物形成的突变型引物组分别混匀形成各阳性对照反应液,涡旋振荡10秒,2000rpm离心15秒,之后,分装至各pcr反应管;步骤s4:取出适量pcr缓冲液,与各基因多态性的检测引物形成的野生型引物组分别混匀形成各阴性对照反应液,涡旋振荡10秒,2000rpm离心15秒,之后,分装至各pcr反应管;步骤s5:加dna样本,将dna样本分别加入到步骤s2形成的各反应液的pcr反应管中,将各阳性对照液加入到步骤s3形成的对应的各阳性对照反应液的pcr反应管,将阴性对照液分别加入到步骤s4形成的各阴性对照反应液的pcr反应管中,将所有pcr反应管放入荧光定量pcr仪,设定反应条件,进行扩增反应,得到各扩增产物;步骤s6:检测步骤s5形成的各产物的sybr信号荧光强度,以sybr信号荧光强度达到设定的阈值所需的循环次数ct值作为相关突变基因存在的判断标准。优选地,所述步骤s1中,所述的待检测样本包括手术切除的新鲜病理组织、甲醛固定石蜡包埋的病理组织、石蜡切片、全血、血浆、血清、胸腔积液、或口腔黏膜脱落细胞。从上述技术方案可以看出,本发明经过大量试验,研究和分析成功筛选出用于快速、灵敏、有效的检测(gpiiia、pear1)基因多态性的引物组,并利用这些引物开发出具有这样的优点的用于检测阿司匹林用药基因(gpiiia、pear1)基因多态性的方法和试剂盒。因此,本发明的检测试剂盒及检测方法具有灵敏度高,特异性强,方法简单,结果准确等显著特点。附图说明图1为本发明具体实施例中使用试剂盒检测gpiiia(176)样品的扩增曲线图。图2为本发明具体实施例中使用试剂盒检测pear1(1568697)样品的扩增曲线图。具体实施方式下面结合附图,对本发明的具体实施方式作进一步的详细说明。本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。在进一步描述本发明具体实施方式之前,应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围;在本发明说明书和权利要求书中,除非文中另外明确指出,单数形式“一个”、“一”和“这个”包括复数形式。当实施例给出数值范围时,应理解,除非本发明另有说明,每个数值范围的两个端点以及两个端点之间任何一个数值均可选用。除非另外定义,本发明中使用的所有技术和科学术语与本
技术领域:
技术人员通常理解的意义相同。除实施例中使用的具体方法、设备、材料外,根据本
技术领域:
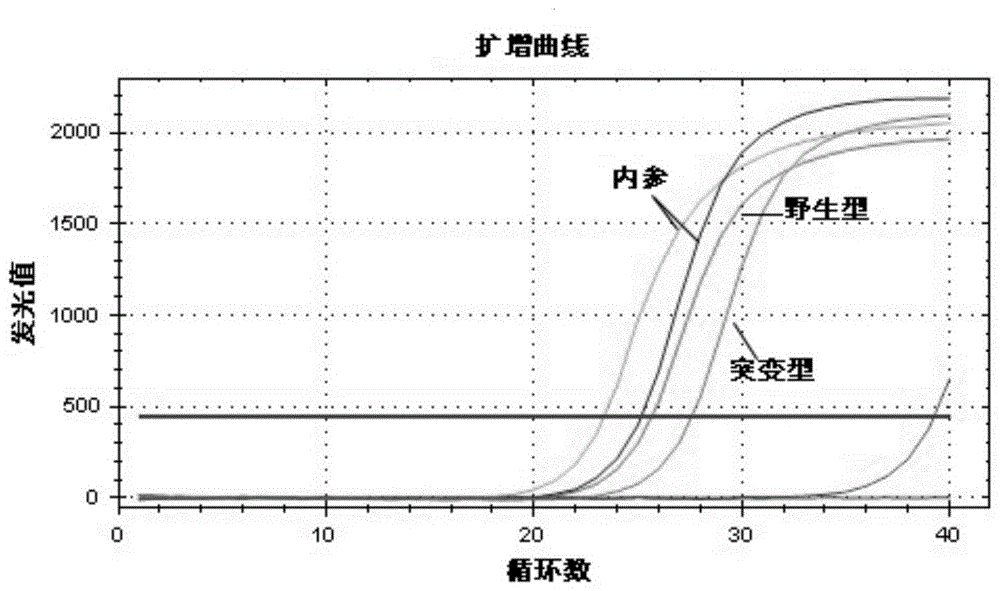
的技术人员对现有技术的掌握及本发明的记载,还可以使用与本发明实施例中所述的方法、设备、材料相似或等同的现有技术的任何方法、设备和材料来实现本发明。试剂盒的制备,包括引物组的设计与合成、对照液的设计、pcr缓冲液设计三部分,分述如下。1引物组的设计与合成本发明采用sybr染料法,建立了针对人类相关基因(gpiiia、pear1)基因多态性(如表1所示)的多重实时pcr检测方法。经过大量试验、研究和分析成功筛选出能够用于快速、灵敏、有效的检测(gpiiia、pear1)基因多态性的引物组合,如表2~4所示。表1:(gpiiia、pear1)基因多态性形式表2:gpiiia(176)基因多态性的检测引物表3:pear1(1568697)基因多态性的检测引物表4:内控的检测引物2对照液的设计本实施例中,试剂盒内包括阳性对照液和阴性对照液。阳性对照液为gpiiia质粒混合液以及pear1质粒混合液,gpiiia质粒混合液含有带有待检测突变位点gpiiia的等位基因,pear1质粒混合液含有带有待检测突变位点pear1的等位基因;所述两种质粒混合液的质粒浓度均为1000copies/μl。阴性对照液为tris-hcl缓冲液,所述的tris-hcl缓冲液的浓度为7-13mm,ph为7.5-8.5。3pcr缓冲液设计本具体实施例中,pcr缓冲液包括3’→5’外切酶活性高保真taq酶、1.0-5.0mm的mgcl2、1.0-5.0mm的datp、1.0-5.0mm的dttp、1.0-5.0mm的dgtp、1.0-5.0mm的dctp以及sybrgreeni。pcr缓冲液的成分终浓度及含量为:pcr缓冲液12.5μl,各对引物0.2μm-1μm。使用试剂盒进行阿司匹林药物相关基因基因多态性检测,包括以下步骤1样本处理和核酸提取本具体实施例中,样品可以为手术切除的新鲜病理组织、甲醛固定石蜡包埋的病理组织、石蜡切片、全血、血浆、血清、胸腔积液或口腔黏膜脱落细胞等。利用商品化的dna提取试剂盒处理样本。具体操作参见试剂盒说明书,所提dna需用紫外分光光度计测定浓度和纯度,其dnaod260/od280的值应在1.8~2.0,浓度应在5~50ng/μl之间,样本dna质量不合格者不得用于检测,建议低于5ng/μl者重新进行核酸提取,高于50ng/μl者予以适当稀释至规定的浓度范围。提取完得到的pcr模板建议立即进行检测,否则请于-20℃以下保存,保存时间不要超过6个月。2试剂配置提前30分钟将前述的试剂盒中所有试剂取出,室温融化,涡旋振荡10秒,2000rpm离心15秒待用。取出适量pcr缓冲液,与各基因多态性的检测引物形成的野生型和突变型引物组、内参的检测引物组分别混匀形成各反应液,用纯化水调节浓度,参考表5,涡旋振荡10秒,2000rpm离心15秒,然后将上述混合液23μl/管分装至pcr反应管中(无菌和rnase-free)。表5:pcr反应体系混合液配置表。试剂检测位点pcr缓冲液p引物混合液纯化水反应液1(μl)gpiiia(176)-t(野生)12.5*n2.0*n8.5*n反应液2(μl)gpiiia(176)-c(突变)12.5*n2.0*n8.5*n反应液3(μl)pear1(1568697)-a(野生)12.5*n2.0*n8.5*n反应液4(μl)pear1(1568697)-g(突变)12.5*n2.0*n8.5*n反应液5(μl)内控12.5*m2.0*m8.5*m取出适量pcr缓冲液,与各基因多态性的检测引物形成的突变型引物组分别混匀形成各阳性对照反应液,参考表6,涡旋振荡10秒,2000rpm离心15秒,然后将上述混合液23μl/管分装至pcr反应管中(无菌和rnase-free)。表6:pcr反应体系混合液配置表。试剂检测位点pcr缓冲液p引物混合液纯化水反应液2(μl)gpiiia(176)-c(突变)12.5*n2.0*n8.5*n反应液4(μl)pear1(1568697)-g(突变)12.5*n2.0*n8.5*n取出适量pcr缓冲液,与各基因多态性的检测引物形成的野生型引物组分别混匀形成各阴性对照反应液,参考表7,涡旋振荡10秒,2000rpm离心15秒,然后将上述混合液23μl/管分装至pcr反应管中(无菌和rnase-free)。表7:pcr反应体系混合液配置表。试剂检测位点pcr缓冲液p引物混合液纯化水反应液1(μl)gpiiia(176)-t(野生)12.5*n2.0*n8.5*n反应液3(μl)pear1(1568697)-a(野生)12.5*n2.0*n8.5*n3加dna样本根据下表8提示的加样量,将dna样本分别加入到表5所示的各反应液的pcr反应管中,将各阳性对照液加入到表6所示的对应的各阳性对照反应液的pcr反应管,将阴性对照液分别加入到表7形成的各阴性对照反应液的pcr反应管中。盖紧管盖(避免气泡产生),2000rpm离心15秒将管壁上的液体全部甩至管底,然后立即进行pcr扩增反应。表8:样品及对照液上样表。表中std代表阳性对照液;ntc代表阴性对照液。4pcr扩增程序设置根据下表9所示的阶段顺序,进行pcr扩增表9:pcr反应程序的设定检测gpiiia(176)样品和pear1(1568697)样品的扩增曲线图如图1~2所示。5检测检测各反应管的sybr信号荧光强度,以sybr信号荧光强度达到设定的阈值所需的循环次数ct值作为相关突变基因存在的判断标准,ct值小于32为阳性,ct值大于35为阴性,ct值介于32到35之间为弱阳性。如果结果为阳性,则基因为突变型,如果结果为阴性,则基因为野生型。使用试剂盒及上述检测方法,可在50ng野生型基因组dna背景下准确检出1%的突变dna,且针对性设计不同突变位点的特异性引物,使用荧光定量pcr进行检测,检测过程均为闭管反应,大大降低污染。以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本
技术领域:
的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1