用于检测艾滋病治疗药物D4T和AZT耐药突变位点的引物对和探针及其应用的制作方法
本发明属于生物医药领域,特别涉及一种用于检测艾滋病治疗药物d4t和azt耐药突变位点的引物对和探针及其应用。
背景技术:
人类免疫缺陷病毒(hiv-1),属于逆转录病毒慢性病毒,是艾滋病的病原体。艾滋病即获得性免疫缺陷综合症(aids),是一种由人类免疫缺陷病毒引起的,以全身免疫系统严重损伤为特征的传染性人体免疫系统疾病。临床表现为不常见的感染、恶性肿瘤以及不明原因的免疫缺陷综合症。
hiv-1的病毒结构、生活周期及复制过程:
hiv-1是rna逆转录病毒,它的生活周期类似于rna肿瘤病毒。病毒颗粒外包被磷脂双分子层包膜,内有圆柱状核心蛋白,有rna逆转录酶、整合酶和结构蛋白等组成。有三个蛋白基因:gag基因编码核心蛋白、pol基因编码逆转录酶与整合酶、env基因编码包膜蛋白;6个非结构蛋白基因。hiv-1病毒颗粒从亲代到子代的复制过程,构成了它的生活周期,包括了病毒的衣服、侵入和脱壳、反转录、整合、病毒rna和蛋白质的合成、装配、释放和成熟等阶段。首先hiv-1通过与宿主细胞上的受体结合,与宿主细胞膜融合后侵入靶细胞。一旦hiv-1外壳和靶细胞质膜相融合,病毒的核心蛋白就进入细胞。在hiv-1的核心蛋白中包埋着rna基因组合逆转录酶。病毒的rna基因组复制需要经过dna中间产物,后在逆转录酶的作用下将病毒rna基因组转变成双链dna,再整合进入宿主细胞的染色体中,最后以原病毒的形式成为宿主基因组的永久成分,并在宿主细胞分裂时随宿主dna的复制而复制。
科学家发现了的hiv-1的治疗药物司他夫定(d4t)和齐多夫定(azt)是目前常用的两种hiv-1核苷酸逆转录酶抑制剂(nrtis),但是由于耐药突变的产生大大降低了这两种药物的有效性。过去的研究一证明可引起d4t和azt耐药产生的突变是pol结构基因m41l、d67n、k70r、l210w、t215y和q151m六中突变。
目前应用于检测hiv-1耐药突变的方法主要是pcr产物直接测序法。然而该方法却存在着检测周期长、灵敏度低、非闭管操作、易造成交叉污染、杂合突变等等缺陷,使得很难适应于临床检测。因此,开发出一种快速、准确、操作简便和避免交叉污染的hiv-1耐药突变检测方法是对临床检测hiv-1耐药检测具有重要意义。
技术实现要素:
本发明目的在于克服现有技术检测艾滋病治疗药物d4t和azt耐药突变位点的方法存在的灵敏度低、特异性差、操作繁琐、检测成本高、花费时间长等问题,本发明提供了一种灵敏度高、特异性好、检测成本低、快速、简单的艾滋病治疗药物d4t和azt耐药突变位点的引物对和探针,还提供了一种包括上述引物对和探针的检测试剂盒以及使用方法。
为实现上述目的,本发明提供如下技术方案,如下:
本发明提供了一种艾滋病治疗药物d4t和azt耐药突变位点的引物对和探针,包括检测hiv-1病毒rna的pol基因的第41位、67位、70位、210位、215位和151位突变位点m41l、d67n、k70r、l210w、t215y和q151m的arms引物和taqman探针。
m41l的arms引物对的上游引物和下游引物分别为seqidno.1和seqidno.4所示的核苷酸序列,taqman探针为seqidno.5所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
d67n的arms引物对的上游引物和下游引物分别为seqidno.2和seqidno.4所示的核苷酸序列,taqman探针为seqidno.5所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
k70r的arms引物对的上游引物和下游引物分别为seqidno.3和seqidno.4所示的核苷酸序列,taqman探针为seqidno.5所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
l210w的arms引物对的上游引物和下游引物分别为seqidno.6和seqidno.9所示的核苷酸序列,taqman探针为seqidno.10所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
t215y的arms引物对的上游引物和下游引物分别为seqidno.7和seqidno.9所示的核苷酸序列,taqman探针为seqidno.10所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
q151m的aarms引物对的上游引物和下游引物分别为seqidno.8和seqidno.9所示的核苷酸序列,taqman探针为seqidno.10所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
本发明还提供了一种用于检测艾滋病治疗药物d4t和azt耐药突变位点中的试剂盒,包括权利要求上述arms引物对和探针。
优选地,所述试剂盒还包括rt-pcr混合液、混合酶液、阳性对照品混合液、阴性对照品混合液;所述rt-pcr混合液包括:rt-pcr缓冲液、dntps、mgcl2、6对上下游引物及2条探针;所述混合酶液包括:m-mlv逆转录酶和tapdna聚合酶。
更优选地,所述试剂盒中各组分含量分别为:
更优选地,所述试剂盒中:
rt-pcr混合液包括
rt-pcr缓冲液(20mmtris-hcl,50mmkclph8.3)终浓度1×;
dntps终浓度2mm;
mgcl2终浓度2mm;
arms引物对的上、下游引物以及试剂盒质控品引物对的上、下游引物的终浓度均为200nm;
各arms上下游引物以及试剂盒质控品上下游引物所对应的taqman探针终浓度为175nm;
mlv逆转录酶终浓度1.6u/μl;taqdna聚合酶终浓度0.05u/μl;
阳性对照混合液中模板cdna终浓度0.1~10ng/μl;
本发明还提供了上述试剂盒在检测艾滋病治疗药物d4t和azt耐药突变位点中的应用,包括以下步骤:
总rna提取:提取待测样本的rna,提到模板rna溶液;
反应组分配制:分别配制检测混合物、阳性对照品混合物和阴性对照品混合物;其中,检测混合物按pcr混合液14ul、混合酶液2.5ul、引物探针3.5ul、模板rna溶液5ul配制一人份;阳性对照品混合物按pcr混合液14ul、混合酶液2.5ul、引物探针3.5ul、阳性对照品混合液5ul配制一人份;阴性对照品混合物按pcr混合液17.5ul、混合酶液2.5ul、引物探针3.5ul、阴性对照品混合液5ul配制一人份;
扩增:分别将检测混合物、阳性质控品混合物、阳性对照品混合物和阴性对照品混合物放入荧光定量pcr仪扩增,反应条件为42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果判定:根据荧光信号到达设定阈值所经历的循环数ct值判定结果:当阳性质控品和阳性对照品的ct值小于等于35,或者检测混合物为阳性时,试剂盒有效;当阳性质控品或阳性对照品的ct值大于35,或者检测混合物无ct值时,试剂盒无效或需重复检测。
其中,根据检测混合物的ct值定性判定,依据为:ct>40时,待测样本中无hiv-1治疗药物d4t和azt耐药突变;35≤ct≤40时,待测样本可疑,需重检一次,重检结果如ct>40或无扩增曲线,则为待测样本中无hiv-1治疗药物d4t和azt耐药突变,反之则为待测样本中有hiv-1治疗药物d4t和azt耐药突变;ct﹤35时,待测样本中有hiv-1治疗药物d4t和azt耐药突变产生。
所述的检测艾滋病治疗药物d4t和azt耐药突变位点的方法是:rt-arms-taqmanqpcr,该技术基于rt-real-timepcr平台,结合arms突变富集技术。利用arms引物对突变靶序列进行特异性pcr扩增,taqman探针对扩增产物进行特异性位点检测,在real-timepcr基础上鉴定特定突变。
有益效果:本发明公开的基于rt-arms-taqmanqpcr技术检测hiv-1耐药突变的方法,具有特异性强、灵敏度高、操作简便、快速、成本低等优点。设计的arms引物只针对基因突变序列,能特异性扩增突变模板rna,在arms引物的3’向5’端1-2位设计两个错配碱基,可以增加arms引物的特异性,本发明设计的taqman探针针对目的基因正义连的突变位点设计,特异地结合突变模板rna,设计的arms引物只针对基因特异突变序列,能特异性扩增突变模板rna,从而达到对微量突变模板的富集作用,提高检测灵敏度,本发明公开的方法检测基因突变灵敏度可以达到1%(即目的基因的突变基因rna模板数占野生型rna模板数的1%),而直接测序法检测基因突变的灵敏度为10%(即目的基因的突变基因rna模板数占野生型rna模板数的10%),检测过程为闭管反应,减少污染的可能性,操作简单快速,整个pcr反应过程只有80分钟,结果判读明确客观,只需根据pcr仪器上的数据即可完成对样本基因类型的判读,同时本发明还具有安全性高,整个体系不包含有毒有害物质,无需pcr产物的开管,对试验人员以及环境都无危害。
附图说明
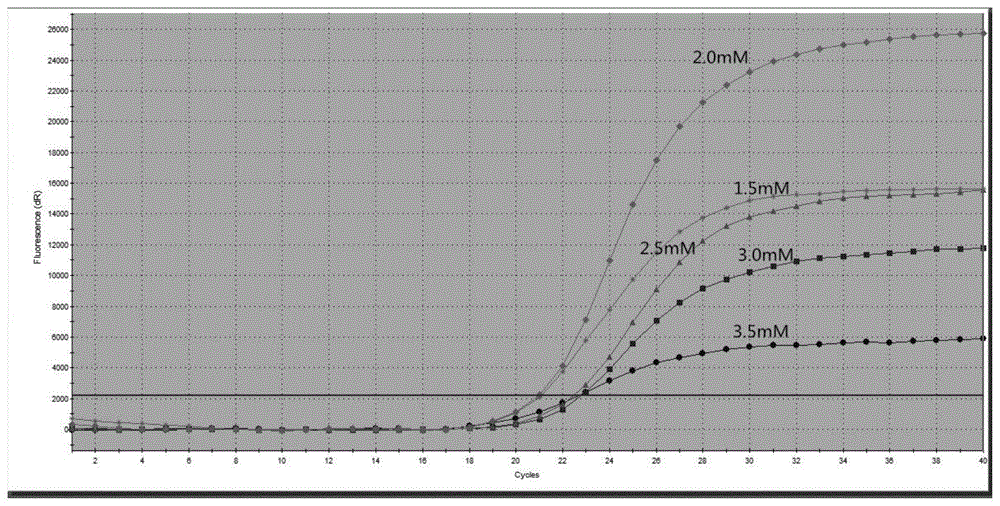
图1为不同mgcl2浓度rt-arms-taqmanqpcr检测结果图(1.5、2.0、2.5、3.0和3.5分别表示mgcl2浓度1.5mm、2.0mm、2.5mm、3.0mm与3.5mm)。
图2为不同dntps浓度rt-arms-taqmanqpcr检测结果图(0.6、0.8、1.0和1.2分别表示0.6mm、0.8mm、1.0mm与1.2mm)。
图3为不同rt-pcr缓冲液浓度rt-arms-taqmanqpcr检测结果图(0.5×、1.0×、1.5×、2×分别为0.5倍、1倍、1.5倍与2倍)。
图4为不同探针浓度rt-arms-taqmanqpcr检测结果图(100、175、250、325、400、475分别表示100nm、175nm、250nm、325nm、400nm与475nm)。
图5为以含有m41l点突变的合成突变型polrt基因为模板,用不同稀释比例进行pcr进行扩增,检测d4t和azt主要耐药突变位点m41l、d67n、k70r、l210w、t215y和q151m突变型的rt-arms-taqmanqpcr检测结果图。
图6为以含有d67n点突变的合成突变型polrt基因为模板,用不同稀释比例进行pcr进行扩增,检测d4t和azt主要耐药突变位点m41l、d67n、k70r、l210w、t215y和q151m突变型的rt-arms-taqmanqpcr检测结果图。
图7为以含有k70r点突变的合成突变型polrt基因为模板,用不同稀释比例进行pcr进行扩增,检测d4t和azt主要耐药突变位点m41l、d67n、k70r、l210w、t215y和q151m突变型的rt-arms-taqmanqpcr检测结果图。
图8为以含有l210w点突变的合成突变型polrt基因为模板,用不同稀释比例进行pcr进行扩增,检测d4t和azt主要耐药突变位点m41l、d67n、k70r、l210w、t215y和q151m突变型的rt-arms-taqmanqpcr检测结果图。
图9为以含有t215y点突变的合成突变型polrt基因为模板,用不同稀释比例进行pcr进行扩增,检测d4t和azt主要耐药突变位点m41l、d67n、k70r、l210w、t215y和q151m突变型的rt-arms-taqmanqpcr检测结果图。
图10为以含有q151m点突变的合成突变型polrt基因为模板,用不同稀释比例进行pcr进行扩增,检测d4t和azt主要耐药突变位点m41l、d67n、k70r、l210w、t215y和q151m突变型的rt-arms-taqmanqpcr检测结果图。
图11为以阳性对照品为模板进行扩增得到的qpcr检测结果图。
图12为以阳性质控品为模板进行扩增得到的qpcr检测结果图。
图13为以阴性对照品为模板进行扩增得到的qpcr检测结果图。
具体实施方式
以下结合附图和具体实施例对上述方案做进一步说明。应理解,这些实施例是用于说明本发明而不限于限制本发明的范围。实施例中采用的实施条件可以根据具体厂家的条件做进一步调整,未注明的实施条件通常为常规实验中的条件。
本发明使用的试剂及其来源:人工合成的引物探针核苷酸序列及人工合成的hiv-1病毒rna序列由上海基康生物技术有限公司负责合成;rt-pcr缓冲液、dntps、m-mlv逆转录酶、taqdna聚合酶终浓度、mgcl2等试剂均是从宝生物工程(大连)有限公司采购获得。
实施例1
用于检测艾滋病治疗药物d4t和azt耐药突变位点的试剂盒,包括:
1、rt-pcr混合液700μl
rt-pcr混合液包括
rt-pcr缓冲液(20mmtris-hcl,50mmkclph8.3)终浓度1×
dntps终浓度2mm;
mgcl2终浓度2mm;
arms引物对的上、下游引物以及试剂盒质控品引物对的上、下游引物的终浓度均为200nm;各arms上下游引物以及试剂盒质控品上下游引物所对应的taqman探针终浓度为175nm;
具体而言,所述rt-pcr混合液中包含:引物序列seqidno.1,seqidno.2,seqidno.3,seqidno.4,seqidno.6,seqidno.7,seqidno.8,seqidno.9其各自浓度分别为0.2,0.4,0.2,0.2,0.4,0.4,0.2,0.2mmol/μl,taqman探针序列为seqidno.5和seqidno.10,终浓度分别为0.2,0.2mmol/μl。
seqidno:1
f1(m41l):5’-gcattagtagaaatttgtacagtct-3’(tm53.3,length25)
seqidno:2
f4(d67n):5’-cagtatttgccataaagaaattta-3’(tm54.8,length24)
seqidno:3
f7(k70r):5’-cataaagaaaaaagacagtacatg-3’(tm53,length24)
seqidno:4
r1:5’-ctaggtatggtaaatgcagtatac-3’(tm52.1,length24)
seqidno:5
a1:fam-5’-ctgaagtcttcatctaagggaactgaa-3’-bhq(tm62.4,length27)
seqidno:6
f16(l210w):5’-gagctgagacaacatctacg-3’(tm53.3,length20)
seqidno:7
f17(t215y):5’-ctgttgaggtggggacaata-3’(tm58.4,length20)
seqidno:8
f15(q151m):5’-tatcagtacaatgtgcttcgtat-3’
seqidno:9
r2:5’-tactgtccatttatcaggatg-3’(tm52.7,length21)
seqidno:10
a2:fam-5’-cataacccatccaaaggaatgg-3’-bhq(tm62.4,length22)
其中,用于检测艾滋病治疗治疗药物d4t和azt耐药突变位点的引物对和探针,包括检测hiv-1病毒rna的pol基因的第41位、67位、70位、210位、215位和151位突变位点m41l、d67n、k70r、l210w、t215y和q151m的arms引物和taqman探针。
m41l的arms引物对的上游引物和下游引物分别为seqidno.1和seqidno.4所示的核苷酸序列,taqman探针为seqidno.5所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
d67n的arms引物对的上游引物和下游引物分别为seqidno.2和seqidno.4所示的核苷酸序列,taqman探针为seqidno.5所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
k70r的arms引物对的上游引物和下游引物分别为seqidno.3和seqidno.4所示的核苷酸序列,taqman探针为seqidno.5所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
l210w的arms引物对的上游引物和下游引物分别为seqidno.6和seqidno.9所示的核苷酸序列,taqman探针为seqidno.10所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
t215y的arms引物对的上游引物和下游引物分别为seqidno.7和seqidno.9所示的核苷酸序列,taqman探针为seqidno.10所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
q151m的aarms引物对的上游引物和下游引物分别为seqidno.8和seqidno.9所示的核苷酸序列,taqman探针为seqidno.10所示的核苷酸序列,分别用fam和bhq1标记5’端和3’端;
2、混合酶液
m-mlv逆转录酶终浓度1.6u/μl;
taqdna聚合酶终浓度0.05u/μl;
3、阳性对照100μl
4、阳性质控品40μl
阳性对照混合液中模板cdna终浓度为0.1~10ng/μl
所述阳性对照品混合物是六种阳性对照品的混合物,包括阳性对照品溶液1,通过人工合成的方法将m41l点突变引入hiv-1polrt基因而得到;阳性对照品溶液2,通过人工合成的方法将d67n点突变引入hiv-1polrt基因而得到;阳性对照品溶液3,通过人工合成的方法将k70r点突变hiv-1polrt基因而得到;阳性对照品溶液4,通过人工合成的方法将l210w点突变hiv-1polrt基因而得到;阳性对照品溶液5,通过人工合成的方法将t215y点突变hiv-1polrt基因而得到;阳性对照品溶液6,通过人工合成的方法将q151m点突变hiv-1polrt基因而得到;其制备方法,具体如下:
hiv-1polrt基因cdna序列如seqidno.11所示。
通过人工合成的方法将m41l点突变引入到hiv-1polrt基因,得到突变型阳性对照品1。将合成的含m41l点突变的hiv-1polrt突变型阳性对照品1克隆到pgm-t载体中,构建成重组质粒,然后将重组质粒转化dh5α大肠杆菌,经测序鉴定正确后,提取重组质粒稀释后,制得阳性对照品1。
通过人工合成的方法将d67n点突变引入到hiv-1polrt基因,得到突变型阳性对照品2。将合成的含d67n点突变的hiv-1polrt突变型阳性对照品2克隆到pgm-t载体中,构建成重组质粒,然后将重组质粒转化dh5α大肠杆菌,经测序鉴定正确后,提取重组质粒稀释后,制得阳性对照品2。
通过人工合成的方法将k70r点突变引入到hiv-1polrt基因,得到突变型阳性对照品3。将合成的含k70r点突变的hiv-1polrt突变型阳性对照品3克隆到pgm-t载体中,构建成重组质粒,然后将重组质粒转化dh5α大肠杆菌,经测序鉴定正确后,提取重组质粒稀释后,制得阳性对照品3。
通过人工合成的方法将l210w点突变引入到hiv-1polrt基因,得到突变型阳性对照品4。将合成的含l210w点突变的hiv-1polrt突变型阳性对照品4克隆到pgm-t载体中,构建成重组质粒,然后将重组质粒转化dh5α大肠杆菌,经测序鉴定正确后,提取重组质粒稀释后,制得阳性对照品4。
通过人工合成的方法将t215y点突变引入到hiv-1polrt基因,得到突变型阳性对照品5。将合成的含t215y点突变的hiv-1polrt突变型阳性对照品5克隆到pgm-t载体中,构建成重组质粒,然后将重组质粒转化dh5α大肠杆菌,经测序鉴定正确后,提取重组质粒稀释后,制得阳性对照品5。
通过人工合成的方法将q151m点突变引入到hiv-1polrt基因,得到突变型阳性对照品6。将合成的含q151m点突变的hiv-1polrt突变型阳性对照品6克隆到pgm-t载体中,构建成重组质粒,然后将重组质粒转化dh5α大肠杆菌,经测序鉴定正确后,提取重组质粒稀释后,制得阳性对照品6。
将制得的阳性对照品1、阳性对照品2、阳性对照品3、阳性对照品4、阳性对照品5和阳性对照品6各稀释至1%浓度,混合均匀成阳性对照品混合液,备用。
5、阴性对照混合液100μl
所述阴性对照混合液是提取的健康人体基因组dna。
实验例2
以试剂盒质控品的引物探针seqidno.5、seqidno.10、作为引物探针对,以上面制备的阴性对照稀释后为模板进行rt-arms-taqmanqpcr,pcr反应中mgcl2浓度分别为1.5mm、2.0mm、2.5mm、3.0mm与3.5mm,其余成分浓度相同(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、0.8mmdntps、1.65u/μl混合酶、200nm引物、175nmtaqman探针、0.1~10ng/μl的阳性对照品)。pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。结果如图1所示,由图1可知,在mgcl2浓度为1.5mm~3.5mm范围内均有扩增曲线,当mgcl2浓度为2.0mm时其结果最佳。
实验例3
以试剂盒质控品的引物探针seqidno.5、seqidno.10、作为引物探针对,以上面制备的阴性对照稀释后为模板进行rt-arms-taqmanqpcr,pcr反应中dntps浓度分别为0.6mm、0.8mm、1.0mm与1.2mm,其余成分浓度相同(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、2mmmgcl2、1.65u/μl混合酶、200nm引物、175nmtaqman探针、0.1~10ng/μl的阳性对照品)。pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。结果如图2所示,由图2可知,在dntps浓度为1.5mm~3.5mm范围内均有扩增曲线,当dntps浓度为0.8mm时其结果最佳。
实验例4
以试剂盒质控品的引物探针seqidno.5、seqidno.10、作为引物探针对,以上面制备的阴性对照稀释后为模板进行rt-arms-taqmanqpcr,pcr反应中探针浓度分别为100nm、175nm、250nm、325nm、400nm与475nm,其余成分浓度相同(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、0.8mmdntps、2mmmgcl2、1.65u/μl混合酶、200nm引物、0.1~10ng/μl的阳性对照品)。pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。结果如图3所示,由图3可知,在探针浓度为100nm~475nm范围内均有扩增曲线,当探针浓度为175nm时其结果最佳。
实验例5
以试剂盒质控品的引物探针seqidno.5、seqidno.10、作为引物探针对,以上面制备的阴性对照稀释后为模板进行rt-arms-taqmanqpcr,pcr反应中引物浓度分别为100nm、200nm、300nm、400nm、500nm与600nm,其余成分浓度相同(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、0.8mmdntps、2mmmgcl2、1.65u/μl混合酶、175nm探针、0.1~10ng/μl的阳性对照品)。pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。结果如图4所示,由图4可知,在探针浓度为100nm~600nm范围内均有扩增曲线,当探针浓度为200nm时其结果最佳。
实施例6
对实施例1中艾滋病治疗药物d4t和azt耐药突变位点rt-pcr检测试剂盒对m41l的检测灵敏度
按每个样本rt-pcr反应液14μl,混合酶液2.5μl配制,引物探针3.5μl,将实施例1中阳性对照品1的1%、阳性对照品的0.01%、阳性对照品的0.0001%、阳性对照品的0.000001%进行稀释后作为模版进行pcr反应,每个稀释样本上样量为5ul,以确定本发明中检测试剂盒对m41l的检测灵敏度(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、3mmdntps、1.6mmmgcl2、1.65u/μl混合酶、200nm引物、175nmtaqman探针),pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果如图5所示,本发明公开的检测方法对m41l点突变的检测灵敏度可以达到0.000001%突变样本。
实施例7
对实施例1中艾滋病治疗药物d4t和azt耐药突变位点rt-pcr检测试剂盒对d67n的检测灵敏度
按每个样本rt-pcr反应液14μl,混合酶液2.5μl配制,引物探针3.5μl,将实施例1中阳性对照品1的1%、阳性对照品的0.01%、阳性对照品的0.0001%、阳性对照品的0.000001%进行稀释后作为模版进行pcr反应,每个稀释样本上样量为5ul,以确定本发明中检测试剂盒对d67n的检测灵敏度(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、3mmdntps、1.6mmmgcl2、1.65u/μl混合酶、200nm引物、175nmtaqman探针),pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果如图6所示,本发明公开的检测方法对d67n点突变的检测灵敏度可以达到0.000001%突变样本。
实施例8
对实施例1中艾滋病治疗药物d4t和azt耐药突变位点rt-pcr检测试剂盒对k70r的检测灵敏度
按每个样本rt-pcr反应液14μl,混合酶液2.5μl配制,引物探针3.5μl,将实施例1中阳性对照品1的1%、阳性对照品的0.01%、阳性对照品的0.0001%、阳性对照品的0.000001%进行稀释后作为模版进行pcr反应,每个稀释样本上样量为5ul,以确定本发明中检测试剂盒对k70r的检测灵敏度(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、3mmdntps、1.6mmmgcl2、1.65u/μl混合酶、200nm引物、175nmtaqman探针),pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果如图7所示,本发明公开的检测方法对k70r点突变的检测灵敏度可以达到0.000001%突变样本。
实施例9
对实施例1中艾滋病治疗药物d4t和azt耐药突变位点rt-pcr检测试剂盒对l210w的检测灵敏度
按每个样本rt-pcr反应液14μl,混合酶液2.5μl配制,引物探针3.5μl,将实施例1中阳性对照品1的1%、阳性对照品的0.01%、阳性对照品的0.0001%、阳性对照品的0.000001%进行稀释后作为模版进行pcr反应,每个稀释样本上样量为5ul,以确定本发明中检测试剂盒对l210w的检测灵敏度(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、3mmdntps、1.6mmmgcl2、1.65u/μl混合酶、200nm引物、175nmtaqman探针),pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果如图8所示,本发明公开的检测方法对l210w点突变的检测灵敏度可以达到0.000001%突变样本。
实施例10
对实施例1中艾滋病治疗药物d4t和azt耐药突变位点rt-pcr检测试剂盒对t215y的检测灵敏度
按每个样本rt-pcr反应液14μl,混合酶液2.5μl配制,引物探针3.5μl,将实施例1中阳性对照品1的1%、阳性对照品的0.01%、阳性对照品的0.0001%、阳性对照品的0.000001%进行稀释后作为模版进行pcr反应,每个稀释样本上样量为5ul,以确定本发明中检测试剂盒对t215y的检测灵敏度(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、3mmdntps、1.6mmmgcl2、1.65u/μl混合酶、200nm引物、175nmtaqman探针),pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果如图9所示,本发明公开的检测方法对t215y点突变的检测灵敏度可以达到0.000001%突变样本。
实施例11
对实施例1中艾滋病治疗药物d4t和azt耐药突变位点rt-pcr检测试剂盒对q151m的检测灵敏度
按每个样本rt-pcr反应液14μl,混合酶液2.5μl配制,引物探针3.5μl,将实施例1中阳性对照品1的1%、阳性对照品的0.01%、阳性对照品的0.0001%、阳性对照品的0.000001%进行稀释后作为模版进行pcr反应,每个稀释样本上样量为5ul,以确定本发明中检测试剂盒对q151m的检测灵敏度(在20μl体系中各组分的终浓度分别为1×rt-pcr缓冲液、3mmdntps、1.6mmmgcl2、1.65u/μl混合酶、200nm引物、175nmtaqman探针),pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果如图10所示,本发明公开的检测方法对q151m点突变的检测灵敏度可以达到0.000001%突变样本。
实施例12
利用实施例1的艾滋病治疗药物d4t和azt耐药突变位点rt-pcr检测试剂盒检测。
rt-pcr反应液及混合酶液,按每个样本rt-pcr反应液14μl,混合酶液2.5μl,引物探针3.5μl配制,对阳性对照品混合液进行pcr扩增,pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果如图11所示,检测试剂盒中配备的阳性对照品的ct值均在35以下。
实施例13
利用实施例1的艾滋病治疗药物d4t和azt耐药突变位点rt-pcr检测试剂盒检测。
rt-pcr反应液及混合酶液,按每个样本rt-pcr反应液14μl,混合酶液2.5μl,引物探针3.5μl配制,对阳性对照质控品混合液进行pcr扩增,pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果如图12所示,检测试剂盒中配备的阳性质控品的ct值均在35以下。
实施例14
利用实施例1的艾滋病治疗药物d4t和azt耐药突变位点rt-pcr检测试剂盒检测。
rt-pcr反应液及混合酶液,按每个样本rt-pcr反应液14μl,混合酶液2.5μl,引物探针3.5μl配制,对阴性性对照品混合液进行pcr扩增,pcr反应条件为:42℃逆转录10min,一个循环;95℃预变性3min,一个循环;95℃变形10s,55℃退火并延伸30s,40个扩增循环。
结果如图13所示,本发明公开的检测方法对正常人基因组不进行扩增。
序列表
<110>江苏发士达生物科技有限公司
<120>用于检测艾滋病治疗药物d4t和azt耐药突变位点的引物对和探针及其应用
<141>2019-04-30
<160>11
<170>siposequencelisting1.0
<210>1
<211>25
<212>dna
<213>m41l的arms引物对的上游引物(2ambystomalateralexambystomajeffersonianum)
<400>1
gcattagtagaaatttgtacagtct25
<210>2
<211>24
<212>dna
<213>d67n的arms引物对的上游引物(2ambystomalateralexambystomajeffersonianum)
<400>2
cagtatttgccataaagaaattta24
<210>3
<211>24
<212>dna
<213>k70r的arms引物对的上游引物(2ambystomalateralexambystomajeffersonianum)
<400>3
cataaagaaaaaagacagtacatg24
<210>4
<211>24
<212>dna
<213>m41l、d67n和k70r的arms引物对的下游引物(2ambystomalateralexambystomajeffersonianum)
<400>4
ctaggtatggtaaatgcagtatac24
<210>5
<211>27
<212>dna
<213>m41l、d67n和k70r的taqman探针(2ambystomalateralexambystomajeffersonianum)
<400>5
ctgaagtcttcatctaagggaactgaa27
<210>6
<211>20
<212>dna
<213>l210w的arms引物对的上游引物(2ambystomalateralexambystomajeffersonianum)
<400>6
gagctgagacaacatctacg20
<210>7
<211>20
<212>dna
<213>l215y的arms引物对的上游引物(2ambystomalateralexambystomajeffersonianum)
<400>7
ctgttgaggtggggacaata20
<210>8
<211>23
<212>dna
<213>q151m的arms引物对的上游引物(2ambystomalateralexambystomajeffersonianum)
<400>8
tatcagtacaatgtgcttcgtat23
<210>9
<211>21
<212>dna
<213>l210w、t215y和q151m的下游引物(2ambystomalateralexambystomajeffersonianum)
<400>9
tactgtccatttatcaggatg21
<210>10
<211>22
<212>dna
<213>l210w、t215y和q151m的taqman探针(2ambystomalateralexambystomajeffersonianum)
<400>10
cataacccatccaaaggaatgg22
<210>11
<211>1680
<212>dna
<213>hiv-1polrt基因cdna序列(2ambystomalateralexambystomajeffersonianum)
<400>11
cccattagccctattgagactgtaccagtaaaattaaagccaggaatggatggcccaaaa60
gttaaacaatggccattgacagaagaaaaaataaaagcattagtagaaatttgtacagag120
atggaaaaggaagggaaaatttcaaaaattgggcctgaaaatccatacaatactccagta180
tttgccataaagaaaaaagacagtactaaatggagaaaattagtagatttcagagaactt240
aataagagaactcaagacttctgggaagttcaattaggaataccacatcccgcagggtta300
aaaaagaaaaaatcagtaacagtactggatgtgggtgatgcatatttttcagttccctta360
gatgaagacttcaggaagtatactgcatttaccatacctagtataaacaatgagacacca420
gggattagatatcagtacaatgtgcttccacagggatggaaaggatcaccagcaatattc480
caaagtagcatgacaaaaatcttagagccttttagaaaacaaaatccagacatagttatc540
tatcaatacatggatgatttgtatgtaggatctgacttagaaatagggcagcatagaaca600
aaaatagaggagctgagacaacatctgttgaggtggggacttaccacaccagacaaaaaa660
catcagaaagaacctccattcctttggatgggttatgaactccatcctgataaatggaca720
gtacagcctatagtgctgccagaaaaagacagctggactgtcaatgacatacagaagtta780
gtggggaaattgaattgggcaagtcagatttacccagggattaaagtaaggcaattatgt840
aaactccttagaggaaccaaagcactaacagaagtaataccactaacagaagaagcagag900
ctagaactggcagaaaacagagagattctaaaagaaccagtacatggagtgtattatgac960
ccatcaaaagacttaatagcagaaatacagaagcaggggcaaggccaatggacatatcaa1020
atttatcaagagccatttaaaaatctgaaaacaggaaaatatgcaagaatgaggggtgcc1080
cacactaatgatgtaaaacaattaacagaggcagtgcaaaaaataaccacagaaagcata1140
gtaatatggggaaagactcctaaatttaaactgcccatacaaaaggaaacatgggaaaca1200
tggtggacagagtattggcaagccacctggattcctgagtgggagtttgttaatacccct1260
cccttagtgaaattatggtaccagttagagaaagaacccatagtaggagcagaaaccttc1320
tatgtagatggggcagctaacagggagactaaattaggaaaagcaggatatgttactaat1380
agaggaagacaaaaagttgtcaccctaactgacacaacaaatcagaagactgagttacaa1440
gcaatttatctagctttgcaggattcgggattagaagtaaacatagtaacagactcacaa1500
tatgcattaggaatcattcaagcacaaccagatcaaagtgaatcagagttagtcaatcaa1560
ataatagagcagttaataaaaaaggaaaaggtctatctggcatgggtaccagcacacaaa1620
ggaattggaggaaatgaacaagtagataaattagtcagtgctggaatcaggaaagtacta1680
- 还没有人留言评论。精彩留言会获得点赞!