一种普兰林肽的二硫类似物及其制备方法与流程
本发明涉及一种普兰林肽的二硫类似物及其制备方法。
背景技术:
糖尿病是一种常见的内分泌疾病,在中国就有超过1亿的人患糖尿病。糖尿病是一种慢性疾病,以高血糖为特征,具有包括疲劳、视力模糊、口渴和尿频等令人痛苦的日常症状。如果高血糖不能得到及时控制和治疗,就会引起糖尿病酮症酸中毒和高渗性高血糖,这是糖尿病2种最严重的急性代谢并发症。
普兰林肽是一种胰淀粉素类似物,是一种有效的治疗方法,与胰岛素协同调节患者血糖平衡。普兰林肽含37个氨基酸以及一对二硫键,半衰期在38分钟左右。研究表明,二硫键在维持普兰林肽三维空间结构中发挥着重要的作用。然而,二硫键在体内还原条件下是不稳定的,容易被硫醇还原,导致多肽结构重排和生物活性的丧失。因此,寻找一种稳定的二硫键的替代键具有重要的意义。
技术实现要素:
针对普兰林肽的二硫键在体内还原环境中应用潜在的缺陷,本发明旨在提供一种普兰林肽的二硫类似物及其制备方法。本发明利用二氨基二酸fmoc-a2(ally/alloy)-oh把普兰林肽中对还原体系不稳定的二硫键替换成稳定的硫醚键。还原稳定性实验表明本发明普兰林肽的二硫类似物具有良好的还原稳定性。
本发明普兰林肽的二硫类似物,是通过使用二氨基二酸实现普兰林肽二硫键的替换后获得的。
所述二氨基二酸为fmoc-a2(ally/alloy)-oh,其结构式如下:
本发明普兰林肽的二硫类似物,具有如下结构:
本发明普兰林肽的二硫类似物的制备方法,包括如下步骤:
步骤1:合成酰肼树脂
将37.5mg2-ci-trt树脂(载量0.40mmol/g,15umol)用375uldmf溶胀,在冰盐浴和搅拌的条件下滴加50uldiea(300umol)、15uln2h4·h2o(300umol)和150uldmf的混合液反应20分钟,随后将反应体系置于室温条件下继续反应70分钟后,加入7.5ulmeoh(185umol)反应20分钟,所得树脂依次用dmf、meoh、乙醚洗涤5次,55℃真空干燥1h后即可得到合成多肽酰肼的酰肼树脂。
步骤2:fmoc固相合成法合成酰肼多肽
2a、将步骤1获得的酰肼树脂转移到固相合成管中,用dmf溶胀15分钟,加入现配制的dic、oxyma、酰肼多肽c端第1个氨基酸的dmf混合液(4.5倍当量dic:4.5倍当量oxyma:4.5倍当量保护的目标c肽端第1个氨基酸,500uldmf),于55℃反应40分钟,将树脂用dmf洗涤,随后用封闭试剂(醋酸酐:2,6-二甲基吡啶:dmf=5:6:89,v%)浸泡树脂2分钟,再一次用dmf洗涤树脂。外加20%哌啶的dmf溶液分别浸泡树脂8分钟和6分钟。用大量dmf洗涤后,依肽序采用fmoc固相合成法缩合氨基酸fmoc-arg(pbf)-oh,fmoc-gln(trt)-oh,fmoc-thr(tbu)-oh,fmoc-ala-oh,fmoc-a2(ally/alloy)-oh,fmoc-thr(tbu)-oh,fmoc-ala-oh,fmoc-thr(tbu)-oh,fmoc-asn(trt)-oh和fmoc-lys(boc)-oh。对于特殊氨基酸fmoc-a2(ally/alloy)-oh的缩合,配置混合液(2倍当量pybop:2倍当量oxyma:500uldmf:1.5倍当量fmoc-a2(ally/alloy)-oh)加入树脂常温过夜反应。当酰肼多肽c端第10个氨基酸fmoc-asn(trt)-oh缩合完成之后,配制pd(pph3)4和n-甲基苯胺的thf混合液(1倍当量pd(pph3)4:28倍当量的n-甲基苯胺:500ulthf),加入树脂中避光常温反应2小时;所得树脂依次用dmf、dmf配制的0.5%nas2cn(c2h5)2溶液、dcm、dmf洗涤。外加20%哌啶的dmf溶液分别浸泡树脂8分钟和6分钟,dmf洗涤树脂。配制pyaop、hoat和nmm的dmf混合液(5倍当量pyaop:5倍当量hoat:10倍当量nmm:500uldmf),加入树脂中反应4小时,反应结束后所得树脂用大量dmf洗涤。依肽序采用fmoc固相合成法继续缩合氨基酸fmoc-lys(boc)-oh。
2b、当酰肼多肽最后一个氨基酸fmoc-lys(boc)-oh缩合结束后,将树脂用大量dmf、dcm洗涤,自然干燥后,外加切割试剂(tfa:苯酚:水:tips=88:5:5:2,v%)0.5ml-0.8ml处理2小时。收集切割试剂,加入15倍体积当量的冰乙醚沉淀,离心粉末状初肽,半制备hplc纯化酰肼多肽。分析hplc和质谱确认产物(图3a,3b),真空冷冻干燥得到纯化的酰肼多肽h-lys-cys-asn-thr-ala-thr-ala-ala-thr-gln-arg-leu-nhnh2(cys2-ala7,硫醚键)。
步骤3:fmoc固相合成法合成半胱氨酸多肽
3a、将45.5mgrinkamide-am树脂(载量0.33mmol/g,15umol)转移到固相合成管中并用dmf溶胀15分钟,外加20%哌啶的dmf溶液浸泡树脂8分钟和6分钟,用大量dmf洗涤树脂。配制dic、oxyma和半胱氨酸多肽c端第一个氨基酸的dmf混合液(4.5倍当量dic:4.5倍当量oxyma:500uldmf:4.5倍当量保护的目标肽端第一个氨基酸),加入树脂中于55℃反应40分钟,用大量dmf洗涤树脂。封闭试剂(醋酸酐:2,6-二甲基吡啶:dmf=5:6:89,v%)浸泡树脂2分钟,再次用大量dmf洗涤树脂。外加20%哌啶的dmf溶液分别浸泡树脂8分钟和6分钟,用大量dmf洗涤树脂后,依肽序采用fmoc固相合成法缩合氨基酸fmoc-thr(tbu)-oh,fmoc-asn(trt)-oh,fmoc-ser(tbu)-oh,fmoc-gly-oh,fmoc-val-oh,fmoc-asn(trt)-oh,fmoc-thr(tbu)-oh,fmoc-pro-oh,fmoc-pro-oh,fmoc-leu-oh,fmoc-ile-oh,fmoc-pro-oh,fmoc-gly-oh,fmoc-phe-oh,fmoc-asn(trt)-oh,fmoc-asn(trt)-oh,fmoc-ser(tbu)-oh,fmoc-ser(tbu)-oh,fmoc-his(trt)-oh,fmoc-val-oh,fmoc-leu-oh,fmoc-phe-oh,fmoc-asn(trt)-oh,fmoc-cys(trt)-oh。
3b、待半胱氨酸多肽最后一个氨基酸fmoc-cys(trt)-oh缩合结束后,将树脂用大量dmf、dcm洗涤,自然干燥后,外加切割试剂(tfa:苯酚:水:tips=88:5:5:2,v%)0.5ml-0.8ml处理2小时;收集切割试剂,外加15倍体积当量的冰乙醚沉淀,离心粉末状初肽;半制备hplc纯化目标肽。分析hplc和质谱确认产物(图4b,4c),真空冷冻干燥得到纯化的半胱氨酸多肽h-cys-asn-phe-leu-val-his-ser-ser-asn-asn-phe-gly-pro-ile-leu-pro-pro-thr-asn-val-gly-ser-asn-thr-tyr-nh2。
步骤4:酰肼多肽和半胱氨酸多肽自然拼接
称取1.6mg步骤2获得的酰肼多肽h-lys-cys-asn-thr-ala-thr-ala-ala-thr-gln-arg-leu-nhnh2(cys2-ala7,硫醚键)溶于0.5mlpbs(6.0m盐酸胍,0.2m磷酸盐,ph3.0),加入磁子,在冰盐浴(约-10℃左右)搅拌的条件下滴加120ulnano2(0.1m)水溶液,低温反应20分钟;反应结束后,向体系中滴加200ulmesna盐酸胍溶液(0.6mmesna,6.0m盐酸胍,0.2m磷酸盐,ph7.0),加入3.8mg步骤3获得的半胱氨酸多肽h-cys-asn-phe-leu-val-his-ser-ser-asn-asn-phe-gly-pro-ile-leu-pro-pro-thr-asn-val-gly-ser-asn-thr-tyr-nh2,撤去冰盐浴,取naoh(2.0m)溶液小心调节反应液ph至中性,反应2天后,hplc检测,分离出新峰,分析hplc和质谱确定连接产物(图6a,6b)。
步骤5:自然拼接产物脱硫
称取1mg步骤4获得的自然拼接肽h-lys-cys-asn-thr-ala-thr-ala-ala-thr-gln-arg-leu-cys-asn-phe-leu-val-his-ser-ser-asn-asn-phe-gly-pro-ile-leu-pro-pro-thr-asn-val-gly-ser-asn-thr-tyr-nh2(cys2-ala7,硫醚键)溶于1mlpbs(6.0m盐酸胍,0.2m磷酸盐,ph7.0)中,加入磁子,于37℃搅拌条件下加入143mgtcep·hcl,调节反应液ph至6.9,随后加入50ul2-甲基-2-丙硫醇和500ul自由基引发剂va-044(0.1m水溶液),调节反应液ph至6.9;反应6小时后,hplc检测,分离出新峰,分析hplc和质谱确定脱硫产物,即普兰林肽二硫类似物(图7a,7b)。
本发明的普兰林肽二硫类似物与现有的普兰林肽相比,还原稳定性实验发现提高了还原稳定性,并且在结构上只有一个原子的差别,避免了结构上的较大干扰。
附图说明
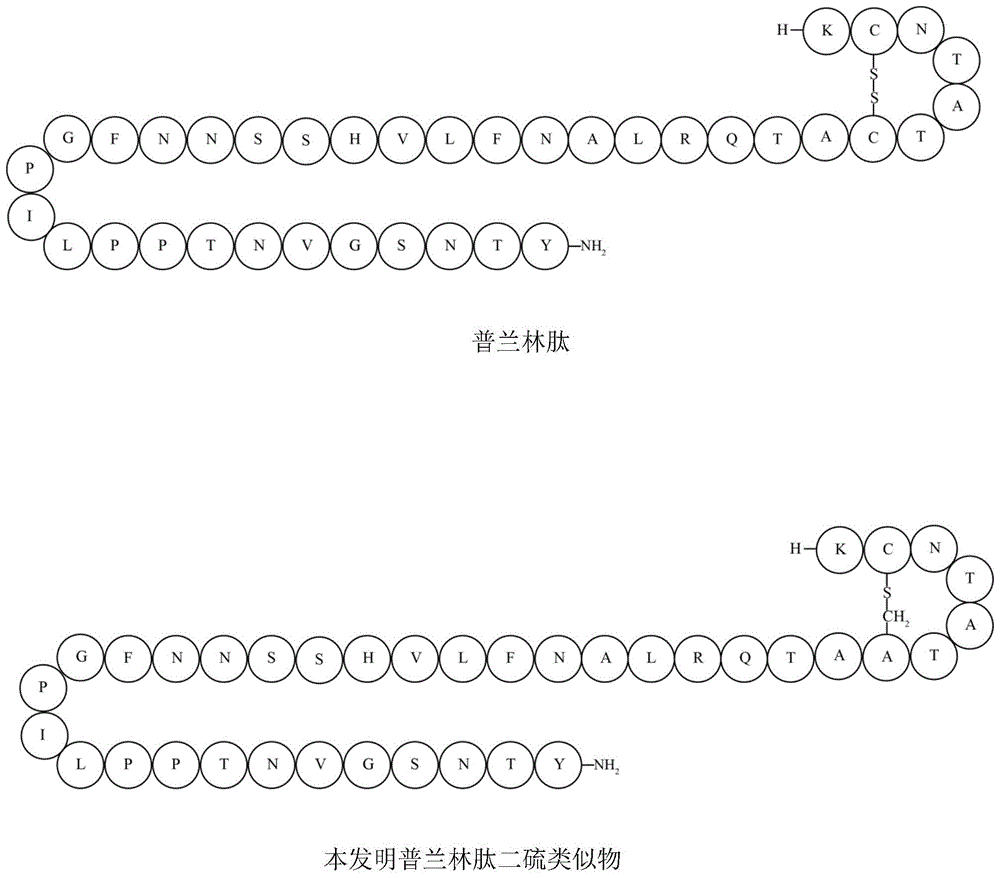
图1是普兰林肽和普兰林肽二硫类似物的结构对比示意图。
图2是本发明酰肼多肽合成示意图。
图3是本发明酰肼多肽hplc图(a)和质谱图(b)。
图4是本发明半胱氨酸多肽结构示意图(a)、hplc图(b)和质谱图(c)。
图5是普兰林肽二硫类似物合成示意图。
图6是酰肼多肽和半胱氨酸多肽自然拼接产物hplc图(a)和质谱图(b)。
图7是普兰林肽二硫类似物hplc图(a)和质谱图(b)。
图8是普兰林肽和普兰林肽二硫类似物还原稳定性测试。
具体实施方法
以下结合实施例做进一步的说明:
本发明所使用的缩写的含义列于下表:
实施例1:合成酰肼树脂
将37.5mg2-ci-trt树脂(载量0.40mmol/g,15umol)用375uldmf溶胀,在冰盐浴和搅拌的条件下滴加50uldiea(300umol)、15uln2h4·h2o(300umol)和150uldmf的混合液反应20分钟,随后将反应体系置于室温条件下继续反应70分钟后,加入7.5ulmeoh(185umol)反应20分钟,所得树脂依次用dmf、meoh、乙醚洗涤5次,55℃真空干燥1h后即可得到合成多肽酰肼的酰肼树脂。
实施例2:fmoc固相合成法合成酰肼多肽
2a、将实施例1获得的酰肼树脂转移到固相合成管中,用dmf溶胀15分钟,加入现配制的dic、oxyma、酰肼多肽c端第1个氨基酸的dmf混合液(4.5倍当量dic:4.5倍当量oxyma:4.5倍当量保护的目标c肽端第1个氨基酸,500uldmf),于55℃反应40分钟,将树脂用dmf洗涤,随后用封闭试剂(醋酸酐:2,6-二甲基吡啶:dmf=5:6:89,v%)浸泡树脂2分钟,再一次用dmf洗涤树脂。外加20%哌啶的dmf溶液分别浸泡树脂8分钟和6分钟。用大量dmf洗涤后,依肽序采用fmoc固相合成法缩合氨基酸fmoc-arg(pbf)-oh,fmoc-gln(trt)-oh,fmoc-thr(tbu)-oh,fmoc-ala-oh,fmoc-a2(ally/alloy)-oh,fmoc-thr(tbu)-oh,fmoc-ala-oh,fmoc-thr(tbu)-oh,fmoc-asn(trt)-oh。对于特殊氨基酸fmoc-a2(ally/alloy)-oh的缩合,配置混合液(2倍当量pybop:2倍当量oxyma:500uldmf:1.5倍当量fmoc-a2(ally/alloy)-oh)加入树脂常温过夜反应。当酰肼多肽c端第10个氨基酸fmoc-asn(trt)-oh缩合完成之后,配制pd(pph3)4和n-甲基苯胺的thf混合液(1倍当量pd(pph3)4:28倍当量的n-甲基苯胺:500ulthf),加入树脂中避光常温反应2小时;所得树脂依次用dmf、dmf配制的0.5%nas2cn(c2h5)2溶液、dcm、dmf洗涤。外加20%哌啶的dmf溶液分别浸泡树脂8分钟和6分钟,dmf洗涤树脂。配制pyaop、hoat和nmm的dmf混合液(5倍当量pyaop:5倍当量hoat:10倍当量nmm:500uldmf),加入树脂中反应4小时,反应结束后所得树脂用大量dmf洗涤。依肽序采用fmoc固相合成法继续缩合氨基酸fmoc-lys(boc)-oh。
2b、当酰肼多肽最后一个氨基酸fmoc-lys(boc)-ohfmoc固相缩合结束后,将树脂用大量dmf、dcm洗涤,自然干燥后,外加切割试剂(tfa:苯酚:水:tips=88:5:5:2,v%)0.5ml-0.8ml处理2小时。收集切割试剂,加入15倍体积当量的冰乙醚沉淀,离心粉末状初肽,半制备hplc纯化酰肼多肽。分析hplc和质谱确认产物(图3a,3b),真空冷冻干燥得到纯化的酰肼多肽h-lys-cys-asn-thr-ala-thr-ala-ala-thr-gln-arg-leu-nhnh2(cys2-ala7,硫醚键)。
实施例3:fmoc固相合成法合成半胱氨酸多肽
3a、将45.5mgrinkamide-am树脂(载量0.33mmol/g,15umol)转移到固相合成管中并用dmf溶胀15分钟,外加20%哌啶的dmf溶液浸泡树脂8分钟和6分钟,用大量dmf洗涤树脂。配制dic、oxyma和半胱氨酸多肽c端第一个氨基酸的dmf混合液(4.5倍当量dic:4.5倍当量oxyma:500uldmf:4.5倍当量半胱氨酸多肽端第一个氨基酸),加入树脂中于55℃反应40分钟,用大量dmf洗涤树脂。封闭试剂(醋酸酐:2,6-二甲基吡啶:dmf=5:6:89,v%)浸泡树脂2分钟,再次用大量dmf洗涤树脂。外加20%哌啶的dmf溶液分别浸泡树脂8分钟和6分钟,用大量dmf洗涤树脂后,依肽序采用fmoc固相合成法缩合氨基酸fmoc-thr(tbu)-oh,fmoc-asn(trt)-oh,fmoc-ser(tbu)-oh,fmoc-gly-oh,fmoc-val-oh,fmoc-asn(trt)-oh,fmoc-thr(tbu)-oh,fmoc-pro-oh,fmoc-pro-oh,fmoc-leu-oh,fmoc-ile-oh,fmoc-pro-oh,fmoc-gly-oh,fmoc-phe-oh,fmoc-asn(trt)-oh,fmoc-asn(trt)-oh,fmoc-ser(tbu)-oh,fmoc-ser(tbu)-oh,fmoc-his(trt)-oh,fmoc-val-oh,fmoc-leu-oh,fmoc-phe-oh,fmoc-asn(trt)-oh,fmoc-cys(trt)-oh。
3b、待半胱氨酸多肽最后一个氨基酸fmoc-cys(trt)-oh缩合结束后,将树脂用大量dmf、dcm洗涤,自然干燥后,外加切割试剂(tfa:苯酚:水:tips=88:5:5:2,v%)0.5ml-0.8ml处理2小时。收集切割试剂,外加15倍体积当量的冰乙醚沉淀,离心粉末状初肽,半制备hplc纯化目标肽。分析hplc和质谱确认产物(图4b,4c),真空冷冻干燥得到纯化的半胱氨酸多肽h-cys-asn-phe-leu-val-his-ser-ser-asn-asn-phe-gly-pro-ile-leu-pro-pro-thr-asn-val-gly-ser-asn-thr-tyr-nh2。
实施例4:酰肼多肽和半胱氨酸多肽自然拼接
1、称取1.6mg实施例2获得的酰肼多肽h-lys-cys-asn-thr-ala-thr-ala-ala-thr-gln-arg-leu-nhnh2(cys2-ala7,硫醚键)溶于0.5mlpbs(6.0m盐酸胍,0.2m磷酸盐,ph3.0)。
2、加入磁子,于冰盐浴中(约-10℃左右)搅拌下滴加120ulnano2(0.1m)水溶液,低温反应20分钟左右。
3、氧化结束后,滴加200ulmesna盐酸胍溶液(0.6mmesna,6.0m盐酸胍,0.2m磷酸盐,ph7.0),加入3.8mg实施例3获得的半胱氨酸多肽h-cys-asn-phe-leu-val-his-ser-ser-asn-asn-phe-gly-pro-ile-leu-pro-pro-thr-asn-val-gly-ser-asn-thr-tyr-nh2,撤去冰盐浴,取naoh(2.0m)溶液小心调节反应液ph至中性。
4、反应2天后,hplc检测,分离出新峰,分析hplc和质谱确定连接产物(图6a,6b)。
实施例5:自然拼接产物脱硫
1、称取1mg实施例4获得的自然拼接肽h-lys-cys-asn-thr-ala-thr-ala-ala-thr-gln-arg-leu-cys-asn-phe-leu-val-his-ser-ser-asn-asn-phe-gly-pro-ile-leu-pro-pro-thr-asn-val-gly-ser-asn-thr-tyr-nh2(cys2-ala7,硫醚键)溶于1mlpbs(6.0m盐酸胍,0.2m磷酸盐,ph7.0)。
2、加入磁子,于油浴锅中(37℃)搅拌条件下加入143mgtcep·hcl,调节反应液ph至6.9。
3、加入50ul2-甲基-2-丙硫醇和500ul自由基引发剂va-044(0.1m水溶液),调节反应液ph至6.9。
4、反应6小时后,hplc检测,分离出新峰,分析hplc和质谱确定脱硫产物h-lys-cys-asn-thr-ala-thr-ala-ala-thr-gln-arg-leu-ala-asn-phe-leu-val-his-ser-ser-asn-asn-phe-gly-pro-ile-leu-pro-pro-thr-asn-val-gly-ser-asn-thr-tyr-nh2(cys2-ala7,硫醚键),即普兰林肽二硫类似物(图7a,7b)。
实施例6:普兰林肽和普兰林肽二硫类似物还原稳定性比较测试
普兰林肽和普兰林肽二硫类似物各称取100ug,溶于100uldtt的缓冲溶液(20mmtris-hcl,ph=7.4,150mmnacl,1mmcacl2,1mmmgcl2,0.1%tritonx-100,3mmdtt)。在25℃孵育条件下,利用hplc在0,0.5,1,2,4,8小时分别监测普兰林肽和普兰林肽二硫类似物的百分比含量变化(图8)。从图8中我们可以看出,在dtt的缓冲溶液中,普兰林肽8小时后大部分已被还原,而普兰林肽二硫类似物基本保持稳定。说明普兰林肽二硫类似物在还原环境下比普兰林肽更稳定。
- 还没有人留言评论。精彩留言会获得点赞!