一种用于检测幽门螺杆菌耐药基因的核酸组合物及其试剂盒和应用的制作方法
本发明涉及生物
技术领域:
,且特别涉及一种用于检测幽门螺杆菌耐药基因的核酸组合物及其试剂盒和应用。
背景技术:
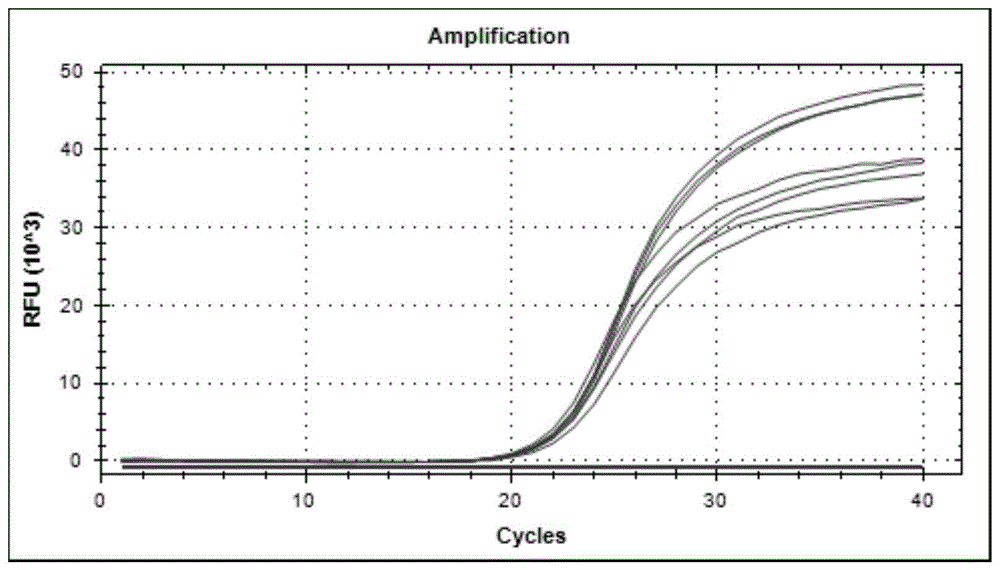
:幽门螺杆菌(helicobacterpylori,h.pylori,hp),是一种微需氧的革兰氏阴性螺旋杆菌,1994年被世界卫生组织列为与胃癌发生相关的i类致癌因子。研究显示幽门螺杆菌感染与胃部炎症、胃黏膜萎缩、胃黏膜肠化、胃黏膜异型增生以及胃癌等的发生发展具有密切相关。目前,用于治疗h.pylori感染的主要药物有:克拉霉素(clarithromycin,cla)、甲硝唑(metronidazole,mtz)、阿莫西林(amoxicillin,amx)和左氧氟沙星(levofloxacin,lev)等。但目前h.pylori耐药现象日趋严峻,严重影响其临床疗效和根除率。研究显示,对克拉霉素耐药的h.pylori菌株50s亚基的23srrna的v区的突变位点如a2143g、a2142g以及a2142c等占所有克拉霉素耐药原因的80%~90%,其他位于hp23srrnav区的突变位点有a2144g、t2115g、g2141a、t2190c、c2195t、a2223g、c2694a、g2254t、ga2172t,以及位于23srrnav区以外的t2617c、t2289c、g2224a、c2245t、t2115g、g2141a、2717.2182.2289.2223.2694少见。h.pylori对喹诺酮类如左氧氟沙星的高度耐药有gyra氨基酸序列的突变引起,gyra氨基酸序列有4种突变(asn-87-lys,ala88-val,aso91-gly,asn或tyr取代ala97-val)。其中,第91位氨基酸的突变占左氧氟沙星耐药原因的30%-50%左右。鉴于此,怎样快速、准确的对h.pylori耐药基因进行检测分析是本领域技术人员需解决的问题。技术实现要素:本发明的目的在于提供一种用于检测幽门螺杆菌耐药基因的核酸组合物及其试剂盒和应用。本发明解决其技术问题是采用以下技术方案来实现的。第一方面,本发明实施例提供了一种用于检测幽门螺杆菌耐药基因的核酸组合物,其包括其包括引物对1和/或引物对2;所述引物对1的上游引物的碱基序列如seqidno.1所示,下游引物的碱基序列如seqidno.2所示;所述引物对2的上游引物的碱基序列如seqidno.3所示,下游引物的碱基序列如seqidno.4所示。第二方面,本发明实施例提供一种用于检测幽门螺杆菌耐药基因的试剂盒,其包括如前述实施例所述的用于检测幽门螺杆菌耐药基因的核酸组合物。第三方面,本发明实施例提供了前述实施例所述的用于检测幽门螺杆菌耐药基因的核酸组合物在幽门螺杆菌的抗生素耐药性检测和/或分析中的应用。第四方面,本发明实施例提供了如前述实施例所述的用于检测幽门螺杆菌耐药基因的核酸组合物在制备用于检测和/或诊断幽门螺杆菌相关疾病的产品中的应用。本发明实施例的核酸组合物的有益效果为:本发明实施例提供了一种用于检测幽门螺杆菌耐药基因的核酸组合物,其包括引物对1和/或引物对2,该核酸组合物解决了现有幽门螺杆菌耐药基因耐药基因的突变位点检测单一且昂贵的缺陷,提供了一种新的能快速且高效地检测幽门螺杆菌耐药基因的途径。附图说明为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。图1为本发明验证例1中引物对1对幽门螺杆菌进行实时荧光定量pcr在不同退火温度(50~60℃)下的扩增图;图2为本发明验证例1中引物对2对幽门螺杆菌进行实时荧光定量pcr在不同退火温度(50~60℃)下的扩增图;图3本发明验证例2中引物对1的上游引物和下游引物均为400nm时的荧光定量pcr的扩增图;图4本发明验证例2中引物对2的上游引物和下游引物均为400nm时的荧光定量pcr的扩增图;图5为本发明验证例3中的引物对1的最低检测限图;图6为本发明验证例3中的引物对2的最低检测限图;图7为本发明验证例6中的引物对1的roc曲线图;图8为本发明验证例6中的引物对2的roc曲线图;图9为本发明验证例7中的幽门螺杆菌耐药基因特异性实验结果图;图10为本发明验证例8中的引物对1的差分曲线图;图11为本发明验证例8中的引物对1的溶解曲线图;图12为本发明验证例8中的引物对2的差分曲线图;图13为本发明验证例8中的引物对2的溶解曲线图。具体实施方式为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。有必要在此指出的是以下实施例只用于对本发明进行进一步说明,不能理解为对本发明保护范围的限制,该领域的技术人员可以根据上述本
发明内容对本发明作出一些非本质的改进和调整。文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明中。下面对本申请提供的一种用于检测幽门螺杆菌耐药基因的核酸组合物及其试剂盒和应用进行具体说明。本发明实施例提供了一种用于检测幽门螺杆菌耐药基因的核酸组合物,其包括其包括引物对1和/或引物对2;所述引物对1的上游引物的碱基序列如seqidno.1所示,下游引物的碱基序列如seqidno.2所示;所述引物对2的上游引物的碱基序列如seqidno.3所示,下游引物的碱基序列如seqidno.4所示。具体地,通过采用上述引物对1对待测样品进行pcr检测,能够针对幽门螺杆菌23srrna的2142、2143位点的多态性进行检测和分析,可同时获得该基因上2个突变位点的检测结果。同理,通过采用上述引物对2对待测样品进行pcr检测,能够针对幽门螺杆菌gyra基因的261以及272位点的多态性进行检测和分析,可同时获得该基因上2个突变位点的检测结果。一方面,上述检测引物对不需要合成荧光探针,克服了现在耐药基因检测价格昂贵的缺陷。另一方面,采用上述引物对进行pcr检测时间(从标本处理开始)仅为2-3小时,操作时间远远短于药敏实验,且pcr检测是全封闭操作,加入样本抽提产物之后可以不再打开管盖,减少了污染产生的机会。同时,采用上述引物对针对幽门螺杆菌的耐药基因进行检测,具有灵敏度高、特异性好、可重复性强以及检测结果快速客观等优点。需要说明的是,只要包含上述任一引物对的核酸组合物均在本申请的保护范围内。需要说明的是,上述幽门螺杆菌23srrna的2142位点突变为a2142g。幽门螺杆菌23srrna的2143位点突变为a2143g;上述幽门螺杆菌gyra基因的261位点突变为c261t;和/或幽门螺杆菌gyra基因的261位点突变为c261a,幽门螺杆菌gyra基因的272位点突变为a272g。本发明实施例还提供了一种用于检测幽门螺杆菌耐药基因的试剂盒,其包括如前述任一实施方式所述的用于检测幽门螺杆菌耐药基因的核酸组合物。在可选实施方式中,所述试剂盒还包括以下任意一种或多种试剂的组合:pcr缓冲液、mgcl2溶液、dntps、热启动dna聚合酶以及pcr反应染料;在可选实施方式中,所述pcr反应染料为饱和染料。本发明实施例还提供如前述任一实施方式所述的用于检测幽门螺杆菌耐药基因的核酸组合物在幽门螺杆菌的抗生素耐药性检测和/或分析中的应用,所述应用不以疾病的诊断或治疗为目的。在可选实施方式中,所述幽门螺杆菌的抗生素耐药性检测和/或分析包括采用所述核酸组合物对待测样品进行pcr检测;优选地,在进行pcr检测中,所述核酸组合物中所述引物对1的上游引物与下游引物的浓度均为350~450nm;优选地,在进行pcr检测中,所述核酸组合物中所述引物对2的上游引物与下游引物的浓度均为350~450nm;优选地,在进行pcr检测时,退火温度为50~60℃。在上述引物对的浓度和退火温度下,pcr扩增的效果更好。此外,本发明实施例还提供了如前述任一实施方式所述的用于检测幽门螺杆菌耐药基因的核酸组合物在制备用于检测和/或诊断幽门螺杆菌相关疾病的产品中的应用。在可选实施方式中,所述幽门螺杆菌相关疾病选自:胃部炎症、胃黏膜萎缩、胃黏膜肠化、胃黏膜异型增生和胃癌。在可选实施方式中,所述应用包括采用所述核酸组合物对待测样品进行pcr检测。在可选实施方式中,在进行pcr检测中,所述核酸组合物中所述引物对1的上游引物与下游引物的浓度均为350~450nm。具体地,在一些实施例中,引物对1的上游引物与下游引物的浓度均可以为350nm、380nm、400nm、420nm或450nm。在可选实施方式中,在进行pcr检测中,所述核酸组合物中所述引物对2的上游引物与下游引物的浓度均为350~450nm。具体地,在一些实施例中,引物对2的上游引物与下游引物的浓度均可以为350nm、380nm、400nm、420nm或450nm。在可选实施方式中,在进行pcr检测时,退火温度为50℃~60℃。具体地,在一些实施例中,退火温度可以为50℃、52℃、55℃、58℃或60℃。以下结合实施例对本发明的特征和性能作进一步的详细描述。实施例1本实施例提供一种用于检测幽门螺杆菌耐药基因的试剂盒,其包括引物对1、引物对2、highresolutionmeltingmaster饱和染料、阳性对照物、阴性对照物、mgcl2、pcr缓冲液、mgcl2溶液、dntps、热启动dna聚合酶。阳性对照物:a2142g突变质粒(具有hp23srrna基因a2142g突变的质粒,下同);a2143g突变质粒;c261t突变质粒(具有hpgyra基因c261t突变的质粒);c261a突变质粒;a272g突变质粒。阴性对照物是无核酸酶超纯水。饱和染料购至roche公司(货号04909631001)。引物合成于生工生物工程(上海)股份有限公司,引物对1和2的序列如表1所示。表1序列序列(5’-3’)seqidno.引物对1上游引物acgagatgggagctgtctca1下游引物tagtaaaggtccacggggtct2引物对2上游引物tcgtgggtgatgtgattggt3下游引物gcatggaaaaatcttgcgcc4实施例2采用实施例1提供的试剂盒对幽门螺杆菌的耐药基因进行检测,具体包括以下步骤:1)待测样品利用(江苏硕世生物科技股份有限公司)核酸提取试剂盒提取幽门螺杆菌患者胃组织标本中的hp的dna作为待测样本;2)配置pcr反应混合液:表2反应体系表2中,引物对1和引物对2的上游引物和下游引物的浓度均为400nm。pcr扩增反应的条件请参照表3。表3pcr扩增反应条件3)结果分析待测样本实验结果均需用bio-radprecisionmeltanalysis分析。将待测样本得到的溶解曲线和差分曲线结果,与阳性对照品和阴性对照品的结果对比,判断待测样本是否具有相应突变位点。若待测样本的溶解曲线和差分曲线结果与未突变的质粒一致,则未突变,若与突变质粒的结果一致,则为具有对应的突变位点。验证例1对实施例2中的退火温度进行验证。本试验例采用实施例2中的方法,分别在50℃~60℃的退火温度下进行pcr扩增,比较不同退火温度下的扩增效率,结果如附图1和图2所示。由附图1和2可知,当pcr的退火温度为50-60℃引物的扩增效果均较好,阴性对照没有扩增曲线。验证例2对实施例2中的引物浓度进行验证。待测样本为:耐药基因23srrna的2142及2143位点均未突变菌株26695,a2142g突变菌株,a2143g突变菌株的核酸样本;合成的未突变质粒,a2142g突变质粒,a2143g突变质粒;左氧氟沙星耐药基因gyra的261和272位点均未突变菌株,c261t突变菌株,c261a突变菌株、a272g突变菌株;以及合成的未突变质粒、c261t突变质粒、c261a突变质粒和a272g突变质粒的核酸样本。按照实施例3提供的方法,在不同浓度配比的引物中进行pcr扩增实验。引物浓度配比以及扩增结果如表4和附图3和附图4所示。表4引物配比实验结果由实验结果可知,当反应体系中引物浓度为400nm,ct值小且扩增曲线呈现光滑的s型,且bio-radprecisionmeltanalysis软件分析,差分曲线结果中的突变菌株与合成的相应的突变位点质粒为同一组,与未突变组为不同组。验证例3对实施例2中方法的检测最低限进行验证。在正常胃组织中分别加入不同cfu的幽门螺杆菌菌液(2×105cfu、2×104cfu、2×103cfu、2×102cfu、1×102cfu),采用病毒核酸dna提取试剂盒提取幽门螺杆菌基因组dna,然后用实施例2的方法对核酸样本进行实时荧光定量pcr分析,结果如图5和图6所示。由图5和图6可知,耐药基因23srrna(引物对1)、gyra(引物对2)的最低检测线均为200cfu,且用于检测的幽门螺杆菌最高菌液浓度低于1×106cfu/ml。验证例4对实施例2中方法的检测的准确度。取23srrna2142及2143位点均未突变菌株26695,a2142g突变菌株,a2143g突变菌株弱阳性样本(ct值在30~33间),以及合成的未突变质粒,a2142g突变质粒,a2143g突变质粒,然后取左氧氟沙星gyra,c261t,c261a,a272g,位点均未突变菌株,c261t突变菌株、c261a突变菌株、a272g突变菌株的弱阳性样本(ct值在30~33间),以及合成的未突变质粒,c261t突变质粒,c261a突变质粒,a272g突变质粒,采用实施例2的方法进行实时荧光定量pcr扩增实验,批内重复至少10个样本,至少重复3次实验。实验结果如下表6所示。表6实验结果由表6可知,幽门螺杆菌耐药基因23srrna,gyra基因同一样本复孔ct值的变异系数(cv%)小于5.0%。变异系数无异常,精密度良好,实验的准确度高。验证例5验证实施例2提供的方法的检测灵敏度。在在正常胃组织中加入200cfu的幽门螺杆菌(a2142g突变菌株、a2143g突变菌株、c261t突变菌株、c261a突变菌株、a272g突变菌株的),采用病毒核酸提取试剂盒提取幽门螺杆菌核酸,用实施例2中的方法对核酸样本进行实时荧光定量pcr分析,实验结果如表7所示。表7实验结果由表7可知,克拉霉素耐药基因23srrna,左氧氟沙星耐药基因gyra,最低检测线均为200cfu。最低检测限的ct值小于cutoff值,重复20次实验检出率为100%,故本发明实施例1提供的用于检测幽门螺杆菌耐药基因核酸组合具有很高的灵敏性。验证例6本实施例对实施例1提供的用于检测幽门螺杆菌耐药基因的核酸组合进行roc曲线的验证。样本制备样本1:选取正常人胃组织样本10例,试剂盒提取模板dna;样本2:在正常20例人胃组织样本中加入2×104cfu的幽门螺杆菌菌液,试剂盒提取模板dna;样本3:在正常20例人胃组织样本中加入2×103cfu的幽门螺杆菌菌液,试剂盒提取模板dna;样本4:在正常20例人胃组织样本中加入2×102cfu的幽门螺杆菌菌液,试剂盒提取模板dna;样本4:在正常20例人胃组织样本中加入1×102cfu的幽门螺杆菌菌液,试剂盒提取模板dna;样本5:大肠杆菌菌株,粪链球菌菌株,嗜酸乳杆菌共10例,试剂盒提取模板dna。按照实施例2中的方法进行实时荧光定量pcr检测,分析数据。然后将实时荧光定量分析所得ct值带入spss软件,制备roc曲线,roc曲线如图7和图8所示,阴性对照无实时荧光定量pcr扩增曲线。spss软件分析各样本ct值的结果如表8和附图7和图8所示。表8spss分析结果备注:a.underthenonparametricassumption(假设在非参数性的情况下)b.nullhypothesis:truearea=0.5(b.虚无假设:真区域=0.5)。由表8和附图7和8可知,克拉霉素耐药基因23srrna和左氧氟沙星耐药基因gyra的roc曲线结果auc(areaunderroc)分别为0.993和0.987,尤登指数(正确指数)最大分别为0.91和0.91,最大youden指数对应的ct值分别为33.51和33.5,即为cutoff值(阳性判定临界值)。验证例7验证实施例2提供的方法的检测特异性。以江苏硕世磁珠法病毒核酸提取试剂盒中洗脱液为空白对照,以正常胃组织基因组dna为阴性对照,幽门螺杆菌菌株的核酸为阳性对照,与大肠杆菌、梭杆菌、乙链球菌、金黄色葡萄球菌、胃内常见菌体嗜酸乳杆菌菌株的核酸样本,采用实施例1的引物对,按照实施例2中的方法进行实时定量荧光pcr分析后的扩增曲线和ct值,实验结果如表9和图9所示。表9实验结果由表9和图9可知,空白对照和大肠杆菌、梭杆菌、乙链球菌、金黄色葡萄球菌、胃内常见菌体嗜酸乳杆菌均无特异性扩增和ct值。请参照附图9,阳性对照样品的耐药基因有特异扩增曲线,且ct值在18~35之间,胃内杂菌和其他菌体对测定无干扰,该引物对1和引物对2对幽门螺杆菌耐药基因检测的特异性良好。验证例8取幽门螺杆菌克拉霉素耐药基因23srrna的2142及2143位点均未突变菌株26695,a2142g突变菌株,a2143g突变菌株的核酸样本,以及合成的未突变质粒,a2142g突变质粒,a2143g突变质粒,以及左氧氟沙星耐药基因gyra的c261t,c261a以及a272g位点均未突变菌株,c261t突变菌株,c261a突变菌株、a272g突变菌株、合成的未突变质粒、c261t突变质粒、c261a突变质粒、a272g突变质粒核酸样本,按照实施例2的方法进行实时荧光定量pcr扩增实验,至少重复3次实验,结果请参照附图10~13。备注:所选突变菌株均为本单位保存的,临床分离菌株,所有菌株突变位点均经过测序鉴定。由附图10,图11可知,耐药基因23srrna的差分曲线和溶解曲线分别分为3个组,分别为26695未突变组,a2142g突变组,a2143g突变组且未突变菌株组与未突变质粒组分为一组,突变菌株与对应的突变质粒组分为一组,结果符合预期。由附图12,图13可知耐药基因gyra的差分曲线和溶解曲线分别分为4个组,分别为未突变组,c261t突变组,c261a突变组和a272g突变组,且未突变菌株组与未突变质粒组分为一组,突变菌株与对应的突变质粒组分为一组,结果符合预期。以上所描述的实施例是本发明一部分实施例,而不是全部的实施例。本发明的实施例的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。sequencelisting<110>重庆博利达医学科技有限公司<120>一种用于检测幽门螺杆菌耐药基因的核酸组合物及其试剂盒和应用<160>4<170>patentinversion3.5<210>1<211>20<212>dna<213>人工序列<400>1acgagatgggagctgtctca20<210>2<211>21<212>dna<213>人工序列<400>2tagtaaaggtccacggggtct21<210>3<211>20<212>dna<213>人工序列<400>3tcgtgggtgatgtgattggt20<210>4<211>20<212>dna<213>人工序列<400>4gcatggaaaaatcttgcgcc20当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1