HIV-2重组抗原及其制备方法、用途与流程
本发明涉及hiv检测领域,具体涉及用于hiv-2免疫检测的重组抗原。
背景技术:
艾滋病(获得性免疫系统缺陷症,aids)是当今世界瞩目的严重危害人类健康的病毒性疾病。引起艾滋病的主要病原是人i型和ii型免疫缺陷病毒(hiv-1和hiv-2)。hiv感染者因免疫缺陷程度加深,从无症状携带者发展至严重免疫功能衰竭,导致多种致死性疾病的发展而死亡。根据who统计,截止到2018年底全球hiv感染者估计为3790万例,仅2018年全球新hiv感染者达170万例。在发展中国家,由于经济、文化和教育等多方面的原因,hiv的流行越演越烈,部分国家已失去对疾病流行的控制,而我国也趋于爆发性流行的前期阶段。
hiv基因全长约9.8kb,含有3个结构基因(gag、pol、env)、2个调节基因(tat反式激活因子、rev毒粒蛋白表达调节子)和4个辅助基因(nef负调控因子、vpr病毒r蛋白、vpu病毒u蛋白和vif毒粒感染性因子)。hiv是一种变异性很强的病毒,各基因的变异程度不同,env基因变异率最高。
根据hiv基因差异,分为hiv-1型和hiv-2型。在hiv-1和hiv-2两型之间,其核苷酸序列有40%-60%的同源性。
根据编码包膜蛋白的env基因和编码壳蛋白的gag基因序列的同源性,hiv-1型又进一步分为3个组,m亚型组(main即主要组)、o亚型组(outline即外围组)和n亚型组(new、non-m、non-o新组或非m非o组),其中m组有a、b、c、d、e、f、g、h、i、j、k11个亚型。此外,近年来发现多个流行重组型。o组是1990年从喀麦隆和加蓬分离到的,与m组其他亚型的氨基酸序列只有50%的同源性。n组是最近才从两名喀麦隆病人分离到的,在系统树上,既不属于m组,也不属于o组的一组新病毒,故称n组。
hiv-2的生物学特性与hiv-1相似,并至少有a、b、c、d、e、f、g7个亚型。
我国以hiv-1为主要流行株。但1999年起在部分地区发现并证实我国有少数hiv-2型感染者。及时发现hiv感染者并鉴定hiv亚型对于追踪流行趋势、及时做出诊断、开发新的诊断试剂和新药研制、疫苗开发均具有重要意义。
艾滋病的防治方向主要为疫苗、诊断和治疗这三个方面,其中,hiv疫苗的研制至今仍未获得成功;hiv的治疗不仅价格昂贵,而且效果极其有限;这使得hiv的诊断成为艾滋病防治的最基础、最有效的手段。
自1985年第一代elisa试剂问世以来,随着医学技术的飞速发展,包被抗原已从第一代的全病毒裂解物发展为目前已基因重组与多肽抗原包被和标记的有着良好敏感性和特异性的第三代双抗原夹心试剂,检测亚型包括hiv-1、hiv-2和hiv-1型的o亚型,窗口期由10周缩短至3~4周。为避免窗口期传染,目前已研制出同时检测抗原抗体的第四代elisa筛查试剂。
抗原的质量是决定hiv检测试剂性能的最关键因素。而hiv检测性能的提升既在于检测的灵敏度和特异性,从而确保检测结果的准确性,同时还在于试剂的稳定性,以实现在较复杂的环境下进行检测并获得准确结果。
据此,在本领域中存在着对hiv抗原进行改善以提高hiv检测试剂性能的强烈需求。
技术实现要素:
为了提高hiv检测试剂性能,本发明人对截短型hiv-2gp36抗原进行研究,通过大量实验,从多种不同的截短型抗原中选取了一种特异性高、稳定性好,且满足免疫诊断试剂开发需求的hiv-2重组gp36抗原,从而完成本发明。
在第一方面,本发明提供一种hiv-2重组抗原,所述重组抗原:
1)包括如seqidno.1所示的氨基酸序列;或者
2)由1)中的氨基酸序列经过取代、缺失或添加一个或者几个(如两个、三个、四个、五个或六个)氨基酸获得的衍生的氨基酸序列,所述衍生的氨基酸序列具有1)中所示的氨基酸序列的活性。
需要说明的是,本发明的重组抗原是一种截短型的hiv-2gp36重组抗原。如下文实施例部分中所证实的,与结构类似的其它截短型gp36重组抗原相比,本发明的重组抗原所制备的试剂盒进行检测时与现有试剂盒具有更高的符合率(100%)。
在第二方面,本发明提供了一种多核苷酸序列,所述多核苷酸序列:
a)编码本发明的重组抗原的氨基酸序列;或者
b)与a)互补。
在一个具体的实施方式中,本发明的多核苷酸序列如seqidno.5所示。
在第三方面,本发明提供了一种多核苷酸构建体,所述多核苷酸构建体含有本发明的多核苷酸。
在第四方面,本发明提供了一种宿主细胞,所述宿主细胞含有本发明的多核苷酸构建体或本发明的多核苷酸。
在第五方面,本发明提供了一种融合蛋白,其包括本发明的重组抗原,以及一个或更多个额外的蛋白。
在一些实施方式中,一个或更多个额外的蛋白可以是用于检测hiv抗体的其它抗原。
在具体的实施方式中,用于检测hiv抗体的其它抗原可以是hiv-2gp41抗原和/或hiv-2gp120抗原。
在一些实施方式中,相邻的重组抗原与额外的蛋白之间,以及相邻的额外的蛋白之间可通过连接子相连。
在第六方面,本发明提供了一种用于检测hiv的组合物,所述组合物包括本发明的重组抗原或本发明的融合蛋白。
在一些实施方式中,本发明的重组抗原可包被在固相载体上。
在一些实施方式中,本发明的融合蛋白可包被在固相载体上。
在一些实施方式中,本发明的重组抗原可带有可检测的标记。
在一些实施方式中,本发明的融合蛋白可带有可检测的标记。
在第七方面,提供了本发明的重组抗原或融合蛋白在制备用于检测hiv抗体的试剂盒中的用途。
在一些实施方式中,本发明的试剂盒用于检测hiv-1抗体和hiv-2抗体。
可以理解,在对hiv-1和hiv-2进行检测的情况下,本发明的试剂盒可额外包括用于检测hiv-1的反应物。
在一些实施方式中,本发明的试剂盒用于检测hiv-2抗体。
在第八方面,本发明提供了一种hiv-2重组抗原的制备方法,包括:
1)将编码本发明的重组抗原的多核苷酸导入宿主细胞中,或者将含所述多核苷酸的多核苷酸构建体转入宿主细胞中;
2)在适合产生重组抗原的条件下培养步骤1)中的所述宿主细胞;以及
3)任选地从步骤2)获得培养物中分离所述重组抗原。
在第九方面,本发明提供了一种重组抗原,其通过本发明的制备方法生产。
本发明获得了以下有益效果:
一方面,通过对hiv-2gp36抗原的截取位置进行优化,本发明最大限度地提高了检测hiv时特异性。
另一方面,通过国家参考品检测,证实本发明重组抗原的灵敏度满足诊断试剂开发的需求。
又一方面,本发明的重组抗原具有优异的热稳定性,在延长了保存周期同时适用于复杂的环境;此外,本发明的重组抗原具有很好的冻融稳定性,增加了重复使用的频次。可以理解,由于这些性质的存在,大大降低了hiv的检测成本及使用限制。
附图说明
图1示出了实施例2中gp36-1重组抗原诱导表达鉴定结果。从左到右,依次为:蛋白marker、gp36-1诱导前菌样、gp36-1诱导后菌样。
图2示出了实施例2中gp36-2重组抗原诱导表达鉴定结果。从左到右,依次为:蛋白marker、gp36-2诱导前菌样、gp36-2诱导后菌样。
图3示出了实施例2中gp36-3重组抗原诱导表达鉴定结果。从左到右,依次为:蛋白marker、gp36-3诱导前菌样、gp36-3诱导后菌样。
图4示出了实施例2中gp36-4重组抗原诱导表达鉴定结果。从左到右,依次为:蛋白marker、gp36-4诱导前菌样、gp36-4诱导后菌样。
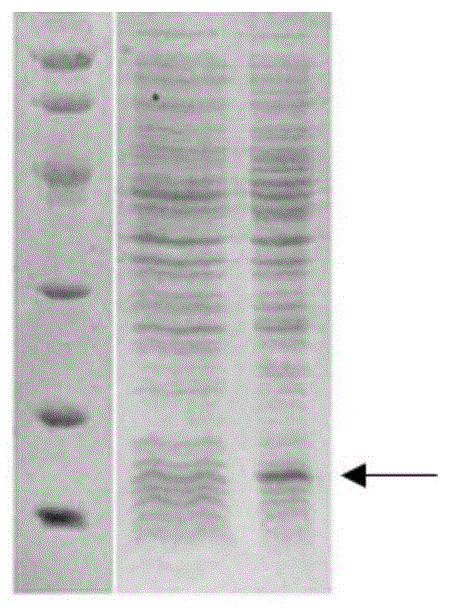
图5示出了实施例3中gp36-1重组抗原电泳图。从左到右,依次为:蛋白marker、目的蛋白gp36-1。
具体实施方式
下文将结合具体实施方式和实施例,具体阐述本发明,本发明的优点和各种效果将由此更加清楚地呈现。本领域技术人员应理解,这些具体实施方式和实施例是用于说明本发明,而非限制本发明。
在整个说明书中,除非另有特别说明,本文使用的术语应理解为如本领域中通常所使用的含义。因此,除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域技术人员的一般理解相同的含义。若存在矛盾,本说明书优先。
如前文所述,抗原的质量是影响hiv免疫检测的最关键因素,故本领域中存在的对抗原的性能不断改进以更好地提升、满足hiv体外检测能力的需求。同时,由于病毒性传染病的抗原往往较大,在体外难以实现完整抗原蛋白的表达,或者即使实现体外表达,分子量比较大的抗原蛋白也往往不能正确折叠,导致后期的复性困难,或者复性获得的抗原活性很差,制约了检测试剂的开发。
为此,本发明提供了一种新的hiv-2gp36重组抗原,其选取了hiv-2抗原全长的553-668aa区域。这样的重组抗原不仅涵盖gp36抗原的优势抗原表位区域,还具有优于与选取区域略有不同的其它抗原的检测能力,同时具有更优的热稳定性、更高的冻融稳定性以及对来自血液中hiv-2型抗体的免疫反应性和灵敏度。
在本发明中衍生的重组抗原可以与如seqidno.1所示的氨基酸序列具有至少约90%、至少约91%、至少约92%、至少约93%、至少约94%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%的一致性。
氨基酸(或核酸)序列之间的一致性百分比可以使用本领域技术人员已知的标准方法来确定。例如,为了确定两条氨基酸序列之间的同源性百分比,将序列进行比对以达到最佳比较目的。然后比较在相应氨基酸位置处的氨基酸残基。可以在一条或两条氨基酸序列中引入空位以实现最佳比对,而且为了比较的目的可以忽略非同源序列。当第一序列中的位置被与第二序列相应位置处的氨基酸残基相同的氨基酸残基占据时,则在该位置处,这两条序列是一致的。考虑进为了最佳比对而引入的空位的数量和每个空位的长度,两条序列之间的一致性百分比是由这两条序列共有的相同位置的数量的函数。两条序列之间的序列比较和一致性百分比及相似性可以使用数学算法来确定。
本发明的试剂盒可采用本领域技术人员熟知的多种形式,例如,试纸、含有各种测试所需试剂的测试盒、微流体芯片等,可以按照已知的标准步骤来制造试剂盒。
在一个具体的实施方式中,本发明的试剂盒可以是胶体金试纸。
本发明的试剂盒根据需要可包括容器、芯片、使用说明书、缓冲剂、免疫助剂和/或用于进行诊断/检测所需的其他材料、结构和/或试剂。
在一些实施方式中,本发明的重组抗原在用于制备试剂盒或组合物的情况下,例如可以溶解或干燥形式存在于容器中,包被在固相支持物上(例如,膜(如nc膜)、板、珠(如磁珠)、微球(诸如羧基微球、氨基微球、氯甲基微球、物理吸附微球等),以溶解或干燥形式存在于芯片的腔室中,但本发明不限于此。
本发明的试剂盒中用于进行诊断/检测所需的其他反应物包括但不限于,除本发明的重组抗原外的其他hiv抗原等。上述其他反应物可以以本领域常规的方式存在,例如,以溶解或干燥形式存在于容器中,包被在固相支持物上,以溶解或干燥形式存在于芯片的腔室中,但本发明不限于此。
本发明的试剂盒中用于进行检测所需的其他材料包括但不限于用于取样材料、用于进行对照材料和/或用于观察检测过程或结果的材料。
本发明的试剂盒中用于进行检测所需的其他试剂包括但不限于缓冲液、洗涤剂、显色剂和/或终止剂。
在一些实施方式中,本发明的重组抗原在用于制备试剂盒或组合物的情况下经可检测地标记。可以使用本领域技术人员已知的任何标记物和标记方法。常用的标记物可包括酶(如辣根过氧化物酶、β-半乳糖苷酶、碱性磷酸酶等)、放射性同位素(如32p或125i)等、生物素、地高辛、胶态金属(如胶体金等)、荧光染料(如荧光素、罗丹明、德克萨斯红等)、化学发光化合物或生物发光化合物(如二氧杂环丁烷、鲁米诺或吖啶鎓等)。可以使用任何本领域众所周知的标记步骤,如酶或生物素基团的共价偶联、碘化、磷酸化、生物素化等。
在一些实施方式中,用于进行检测所需的其他反应物中的一种或更多种也可以为可检测地标记的。
在本发明的试剂盒中,重组抗原可以合适的浓度存在,本领域技术人员能够根据试剂盒的具体类型,例如参考市售试剂盒中gp36抗原的浓度或通过常规实验确定这样的范围。
本发明包括一种检测受试者中hiv的存在的方法。
例如,检测方法包括:使得自受试者的样本与至少包被有本发明的重组抗原的固相支持物接触,所述接触在足以使固相支持物上的包被物与样本中的待测物产生复合体的条件和时间下进行;与此同时或在此之后,加入带有可检测标记的标记组分,其能与待测物结合从而形成固相包被物-待测物-标记组分的复合物;随后,通过测量可检测标记获得检测结果。
例如,检测方法包括:使得自受试者的样本与包被在固相支持物上的固相组分接触,所述接触在足以使固相支持物上的固相组分与样本中的待测物产生复合体的条件和时间下进行;与此同时或在此之后,加入带有可检测标记的标记组分,该标记组分至少包括本发明的重组抗原,该标记组分能与待测物结合从而形成固相组分-待测物-标记组分的复合物;随后,通过测量可检测标记获得检测结果。
可选地,在形成复合物之后还包括洗涤步骤以去除未结合的组分。
在本发明中,样本可选自血清、血浆和血液。
检测方法包括但不限于elisa(酶联免疫吸附测定)、放射自显影、比浊法、荧光显微镜检术、直接和间接的酶促反应、放射性同位素法或非放射性同位素法等。这些方法尤其包括免疫比浊法、乳胶增强透射比浊法、western印迹、重叠测定、ria(放射免疫测定)和irma(免疫放射免疫测定)、gia(胶体金免疫测定)、eia(酶免疫测定)、fia(荧光免疫测定),以及clia(化学发光免疫测定)。
本发明还涉及编码重组抗原的多核苷酸,以例如用于生产本发明的重组抗原的融合蛋白。编码本发明重组抗原的多核苷酸包括但不限于:重组抗原的编码序列本身;重组抗原的编码序列及额外的编码序列;重组抗原的编码序列(和任选的额外的编码序列)及非编码序列,例如可以另外包括但不必限于一种或多种调节性核酸序列,其可以是受调节的或可调节的启动子、增强子、其它转录调节序列、抑制子结合序列、翻译调节序列或任何其它调节性核酸序列。
本发明也包括等效的多核苷酸构建体。本领域技术人员能够理解,多核苷酸构建体用于通过重组表达制备重组抗原,该多核苷酸构建体包含可操作地连接到表达控制序列上的编码重组抗原的核酸分子,另外包含用于在各自宿主细胞中维持和繁殖的遗传元件,如复制起点和/或选择标记基因。
本发明的多核苷酸构建体例如可以是原核宿主细胞例如细菌(例如,大肠杆菌、枯草芽孢杆菌或李斯特菌)中表达的噬菌体、质粒或粘粒载体;用于在酵母(例如,酿酒酵母、粟酒裂殖酵母、巴斯德毕赤酵母)中表达的载体;用于在昆虫细胞系统(例如,sf9细胞)中表达的杆状病毒载体;用于在植物细胞系统中表达的病毒和质粒载体(例如,ti质粒、花椰菜花叶病毒camv;烟草花叶病毒tmv);以及用于在高等真核细胞或生物体中表达的病毒和质粒载体。通常,这样的载体可商购,或者可从保藏机构获得,或者可根据出版物的记载而获得(这些出版物描述这些载体的序列、结构和生成方法),从而使得本领域技术人员能够应用它们。
在本发明中,融合蛋白中的各个蛋白彼此连接子相连,从而保证它们各自的结构以及活性不受影响。示例性的连接子可以是带有甘氨酸的柔性连接子,如gsg、gsggsg、gsggsgg、gsggsggg、ggggsggg、ggggs和sgg等。
实施例1重组gp36抗原的设计和表达载体的构建
利用基因工程技术,以优势表位区成为抗原研究的方向,发明人设计大量hiv-2gp36的抗原片段,以下仅以其中的gp36-1(seqidno.1)、gp36-2(seqidno.2)、gp36-3(seqidno.3)和gp36-4(seqidno.4)作为示例,说明实验筛选的过程。
选取hiv-2抗原全长的553-668aa区域,命名为gp36-1,对密码子进行优化后采用化学合成的方法得到核苷酸序列gp36-1(seqidno.5);选取hiv-2抗原全长的538-668aa区域,命名为gp36-2,对密码子进行优化后采用化学合成的方法得到核苷酸序列gp36-2(seqidno.6);选取hiv-2抗原全长的523-668aa区域,命名为gp36-3,对密码子进行优化后采用化学合成的方法得到核苷酸序列gp36-3(seqidno.7);以及选取hiv-2抗原全长的520-679aa区域,命名为gp36-4,对密码子进行优化后采用化学合成的方法得到核苷酸序列gp36-4(seqidno.8)。
将目的基因片段gp36-1、gp36-2、gp36-3和gp36-4和表达载体ptrchisa分别经限制性内切酶xhoi和ecori双酶切处理。
37℃水浴酶切3h,酶切产物用1%tae琼脂糖凝胶电泳检测。用qiagen小量胶回收试剂盒回收。16℃连接4h,并将连接产物通过热激法转入感受态e.colidh5α细胞,涂布于含100μg/mlamp+的lb琼脂培养基上,在37℃条件下,倒置培养过夜或培养12~14小时至长出单菌落。
利用菌液pcr进行初步筛选。具体地:首先用无菌牙签挑取单菌落于含有1mllb(含100μg/mlamp+)的1.5mleppendorf管中,37℃振荡培养4h后取出菌液备用。菌液pcr鉴定:加好反应体系后,用小枪头吸取1μl菌液,混于混合物中,放入pcr仪后开始扩增。pcr反应条件为:95℃,5min;95℃,30s,56℃,30秒,72℃,1min(扩增30个循环);72℃,10min。扩增产物用1%tae琼脂糖凝胶电泳检测。
用双酶切鉴定进行进一步的鉴定。具体地:吸取10μl经菌液pcr鉴定正确的克隆子菌液,加入到含有5mllb(含100μg/mlamp+)的15ml试管中,37℃振荡培养过夜。用axygen小量质粒试剂盒进行质粒提取。用限制性内切酶xhoi和ecori进行双酶切鉴定。37℃水浴酶切2h。酶切产物用1%tae琼脂糖凝胶电泳检测。
对经菌液pcr和质粒酶切鉴定正确的菌液进行菌种保存后送到生工生物工程(上海)股份有限公司进行测序。测序结果与预期一致,未发生碱基置换、缺失或者添加,说明目的基因成功克隆至表达载体ptrchisa,将其命名为ptrc-gp36-1、ptrc-gp36-2、ptrc-gp36-3、ptrc-gp36-4。
实施例2重组gp36抗原的诱导表达和纯化
将测序正确的酶切鉴定过的阳性重组质粒,用热激的方法转化大肠杆菌e.colibl21(rossett)感受态细胞,涂布于含100μg/mlamp+和25μg/mlchl+的lb琼脂培养基上,在37℃条件下,倒置培养过夜或培养12~14h至长出单菌落。
挑取2个单菌落接种至含100μg/mlamp+和25μg/mlchl+的5mllb液体培养基中,37℃,200rpm培养过夜。次日,取200μl菌液转接于5ml新鲜的含100μg/mlamp+和25μg/mlchl+的lb液体培养基中,37℃,200rpm培养至od600约0.8。取1ml菌液作为诱导前小样,向剩余的菌液中加入iptg至终浓度为1mm,于37℃下继续振荡培养4~5h。诱导结束后进行sds-page电泳(见图1-图4)。将诱导出目的蛋白的克隆子菌液进行菌种保存,并将其命名为rptrc-gp36-1、rptrc-gp36-2、rptrc-gp36-3、rptrc-gp36-4。
选择诱导出目的蛋白的克隆子,按上述确定的诱导条件进行大量发酵培养2000ml。收集菌体,并用20mmpbsph7.4的缓冲液洗涤两次。菌体冻存于-20℃。
用破菌缓冲液(20mmpb,0.5mnacl,ph7.4,)重悬发酵菌体,冰水浴条件下超声破碎(超声破碎条件为:功率为500w,超声5s,间隔9s,超声时间为60min);超声结束后,12000rpm,10℃条件下离心20min;去上清收集沉淀。沉淀用20mmpb,0.5mnacl,8m尿素,ph7.4的溶液溶解,用玻璃棒搅拌沉淀,让其混合均匀,再用超声溶解沉淀(300-400w功率,超声5s,间隔9s,超声20-30min),12000rpm离心20min,收集上清,并用0.22μm滤膜过滤。
上样缓冲液为20mmpb,0.5mnacl,8m尿素,ph7.4;洗杂缓冲液为:20mmpb,0.5mnacl,8m尿素,30mm咪唑,ph7.4;洗脱缓冲液为:20mmpb,0.5mnacl,8m尿素,500mm咪唑,ph7.4。
实施例3重组gp36抗原的蛋白复性
收集洗脱液,装入3000-3500da分子量的透析袋,在2~8℃条件下复性目的蛋白:
buffera:10mmcb,0.05%sds,10%甘油,1mmdtt,4m尿素,ph10.2;
bufferb:10mmcb,0.05%sds,ph10.2。
先用buffera(1l)透析目的蛋白,约2~4h后,向buffera中加入同等体积的bufferb(2l),再透析约2~4h。之后,倒掉1l含2m尿素的透析液,向其中再加入1lbufferb,继续透析2~4h。最后换为新的2lbufferb透析,透析3次,每次透析2~4h。透析完毕后,将蛋白从透析袋中取出。
复性后的目的蛋白用超滤离心管进行浓缩,然后以12000rpm于2-8℃离心20min,收集上清于15ml离心管中,同时用bca蛋白定量试剂盒(pierce)测定抗原蛋白浓度。
取复性后目的蛋白的小样进行sds-page电泳(电泳结果见图5)。目的蛋白大小与预期一致,蛋白纯度大于85%。
实施例4重组gp36抗原的特异性
用本发明的实施例3中制备的gp36-1、gp36-2、gp36-3、gp36-4抗原,分别与hiv-i型抗原(来自菲鹏生物股份有限公司)同时包被nc膜,用hiv-i+ii型抗原(来自菲鹏生物股份有限公司)标记胶体金,制成人类免疫缺陷病毒(hiv1+2)抗体检测试剂盒。
首先,分别使用gp36-2、gp36-3、gp36-4、gp36-1抗原按照常规方法制备的hiv-1和hiv-2联合检测胶体金试剂盒,对确诊的100例阳性样本和500例阴性样本进行检测,以进行本发明抗原的特异性评价。具体步骤为:将试纸条一端的样品垫插入盛有样本的容器中,约10秒见明显上样后,取出平放;随后放置室温,15分钟至20分钟内观察结果。同时,使用参照试剂(迈克生物产品名称:人类免疫缺陷病毒(hiv1+2)抗体检测试剂盒(胶体金法),批号:0917041),按照产品说明书记载的方法对上述100例阳性样本和500例阴性样本进行复测,并计算两次测试结果的符合率,结果如表1-表3所示。
表1gp36-2抗原的临床样本检测
表2gp36-3抗原的临床样本检测
表3gp36-4抗原的临床样本检测
由表1-表3可见,gp36-2、gp36-3、gp36-4抗原制备的抗体检测试剂盒,特异性差,出现假阳性结果。
接下来,使用ptrc-gp36-1抗原制备的抗体检测试剂盒与参照试剂,分别按照上述方法,检测了1580例临床样本,其中107例hiv-i型阳性样本,21例hiv-ii型阳性样本,1452例阴性样本,结果如表4所示。
表4gp36-1抗原的临床样本检测
由表4可见,用gp36-1抗原制成的该试剂的人类免疫缺陷病毒(hiv1+2)抗体检测试剂盒检测特异性为100%,说明本发明的gp36-1抗原的特异性可以满足免疫诊断试剂开发的需求。
实施例5重组gp36抗原的热稳定性检测
用实施例3中制备的gp36-1抗原,分别经37℃热处理7天、14天,经sds-page电泳检测,蛋白未聚集或者降解。用热处理后的抗原,与hiv-1型抗原(来自菲鹏生物股份有限公司)同时包被nc膜,用hiv-1+2型抗原(来自菲鹏生物股份有限公司)标记胶体金,制成人类免疫缺陷病毒(hiv1+2)抗体检测试剂盒,检测人类免疫缺陷病毒抗体快速试剂企业参考品(见表5)。结果表明,与新鲜制备的抗原相比,本发明的重组gp36抗原在经过37℃热处理7天、14天后,在检测企业参考品时无明显差异(见表6)。
表5企业参考品标准
表6热处理后的gp36-1抗原检测企业参考品结果
实施例6重组gp36抗原的冻融稳定性
用实施例3中制备的gp36-1抗原,分别经冻融3次、5次,经sds-page电泳检测,蛋白未聚集或者降解。用冻融后的抗原,与hiv-1型抗原(来自菲鹏生物股份有限公司)同时包被nc膜,用hiv-1+2型(来自菲鹏生物股份有限公司)抗原标记胶体金,制成人类免疫缺陷病毒(hiv1+2)抗体检测试剂盒,检测人类免疫缺陷病毒抗体快速试剂企业参考品(见表5)。结果表明,与新鲜制备的抗原相比,本发明的重组gp36抗原在经冻融3次、5次后,在检测企业参考品时无明显差异(见表7)。
表7冻融后的gp36抗原检测企业参考品结果
实施例7重组gp36抗原的灵敏度
用实施例3中制备的gp36-1抗原,与hiv-1型抗原(来自菲鹏生物股份有限公司)同时包被nc膜,用hiv-1+2型抗原(来自菲鹏生物股份有限公司)标记胶体金,制成人类免疫缺陷病毒(hiv1+2)抗体检测试剂盒,检测人类免疫缺陷病毒抗体快速试剂国家参考品(见表8),进行本发明抗原的灵敏度评价(见表9)。
表8国家参考品标准
表9gp36-1抗原检测国家参考品结果
由表9可知,本发明的重组gp36-1抗原对人类免疫缺陷病毒抗体快速试剂国家参考品检测均能达到要求,说明本发明的抗原的灵敏度可以满足免疫诊断试剂开发的需求。
应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
序列表
<110>四川迈克生物新材料技术有限公司
<120>hiv-2重组抗原及其制备方法、用途
<130>2020
<160>8
<170>patentinversion3.5
<210>1
<211>116
<212>prt
<213>hiv-2
<400>1
glnleuleuaspvalvallysargglnglngluleuleuargleuthr
151015
valtrpglythrlysasnleuglnalaargvalthralaileglulys
202530
tyrleuglnaspglnalaargleuasnsertrpglycysalaphearg
354045
glnvalcyshisthrthrvalprotrpvalasnaspserleualapro
505560
asptrpaspasnmetthrtrpglnglutrpglulysglnvalargtyr
65707580
leuglualaasnileserlysserleugluglnalaglnileglngln
859095
glulysasnmettyrgluleuglnlysleuasnsertrpaspilephe
100105110
glyasntrpphe
115
<210>2
<211>131
<212>prt
<213>hiv-2
<400>2
alaglnserargthrleuleualaglyilevalglnglnglnglngln
151015
leuleuaspvalvallysargglnglngluleuleuargleuthrval
202530
trpglythrlysasnleuglnalaargvalthralaileglulystyr
354045
leuglnaspglnalaargleuasnsertrpglycysalaphearggln
505560
valcyshisthrthrvalprotrpvalasnaspserleualaproasp
65707580
trpaspasnmetthrtrpglnglutrpglulysglnvalargtyrleu
859095
glualaasnileserlysserleugluglnalaglnileglnglnglu
100105110
lysasnmettyrgluleuglnlysleuasnsertrpaspilephegly
115120125
asntrpphe
130
<210>3
<211>146
<212>prt
<213>hiv-2
<400>3
alathralaglyseralametglyalaalaserleuthrvalserala
151015
glnserargthrleuleualaglyilevalglnglnglnglnglnleu
202530
leuaspvalvallysargglnglngluleuleuargleuthrvaltrp
354045
glythrlysasnleuglnalaargvalthralaileglulystyrleu
505560
glnaspglnalaargleuasnsertrpglycysalapheargglnval
65707580
cyshisthrthrvalprotrpvalasnaspserleualaproasptrp
859095
aspasnmetthrtrpglnglutrpglulysglnvalargtyrleuglu
100105110
alaasnileserlysserleugluglnalaglnileglnglnglulys
115120125
asnmettyrgluleuglnlysleuasnsertrpaspilepheglyasn
130135140
trpphe
145
<210>4
<211>160
<212>prt
<213>hiv-2
<400>4
glypheleualathralaglyseralametglyalaalaserleuthr
151015
valseralaglnserargthrleuleualaglyilevalglnglngln
202530
glnglnleuleuaspvalvallysargglnglngluleuleuargleu
354045
thrvaltrpglythrlysasnleuglnalaargvalthralaileglu
505560
lystyrleuglnaspglnalaargleuasnsertrpglycysalaphe
65707580
argglnvalcyshisthrthrvalprotrpvalasnaspserleuala
859095
proasptrpaspasnmetthrtrpglnglutrpglulysglnvalarg
100105110
tyrleuglualaasnileserlysserleugluglnalaglnilegln
115120125
glnglulysasnmettyrgluleuglnlysleuasnsertrpaspile
130135140
pheglyasntrppheaspleuthrsertrpvallystyrileglntyr
145150155160
<210>5
<211>348
<212>dna
<213>人工合成
<400>5
cagctgctggacgttgttaaacgtcagcaggaactgctgcgtctgaccgtttggggtacc60
aaaaacctgcaggctcgtgttaccgctatcgaaaaatacctgcaggaccaggctcgtctg120
aactcttggggttgcgctttccgtcaggtttgccacaccaccgttccgtgggttaacgac180
tctctggctccggactgggacaacatgacctggcaggaatgggaaaaacaggttcgttac240
ctggaagctaacatctctaaatctctggaacaggctcagatccagcaggaaaaaaacatg300
tacgaactgcagaaactgaactcttgggacatcttcggtaactggttc348
<210>6
<211>393
<212>dna
<213>人工合成
<400>6
gctcagtctcgtaccctgctggctggtatcgttcagcagcagcagcagctgctggacgtt60
gttaaacgtcagcaggaactgctgcgtctgaccgtttggggtaccaaaaacctgcaggct120
cgtgttaccgctatcgaaaaatacctgcaggaccaggctcgtctgaactcttggggttgc180
gctttccgtcaggtttgccacaccaccgttccgtgggttaacgactctctggctccggac240
tgggacaacatgacctggcaggaatgggaaaaacaggttcgttacctggaagctaacatc300
tctaaatctctggaacaggctcagatccagcaggaaaaaaacatgtacgaactgcagaaa360
ctgaactcttgggacatcttcggtaactggttc393
<210>7
<211>438
<212>dna
<213>人工合成
<400>7
gctaccgctggttctgctatgggtgctgcttctctgaccgtttctgctcagtctcgtacc60
ctgctggctggtatcgttcagcagcagcagcagctgctggacgttgttaaacgtcagcag120
gaactgctgcgtctgaccgtttggggtaccaaaaacctgcaggctcgtgttaccgctatc180
gaaaaatacctgcaggaccaggctcgtctgaactcttggggttgcgctttccgtcaggtt240
tgccacaccaccgttccgtgggttaacgactctctggctccggactgggacaacatgacc300
tggcaggaatgggaaaaacaggttcgttacctggaagctaacatctctaaatctctggaa360
caggctcagatccagcaggaaaaaaacatgtacgaactgcagaaactgaactcttgggac420
atcttcggtaactggttc438
<210>8
<211>480
<212>dna
<213>人工合成
<400>8
ggtttcctggctaccgctggttctgctatgggtgctgcttctctgaccgtttctgctcag60
tctcgtaccctgctggctggtatcgttcagcagcagcagcagctgctggacgttgttaaa120
cgtcagcaggaactgctgcgtctgaccgtttggggtaccaaaaacctgcaggctcgtgtt180
accgctatcgaaaaatacctgcaggaccaggctcgtctgaactcttggggttgcgctttc240
cgtcaggtttgccacaccaccgttccgtgggttaacgactctctggctccggactgggac300
aacatgacctggcaggaatgggaaaaacaggttcgttacctggaagctaacatctctaaa360
tctctggaacaggctcagatccagcaggaaaaaaacatgtacgaactgcagaaactgaac420
tcttgggacatcttcggtaactggttcgacctgacctcttgggttaaatacatccagtac480
- 还没有人留言评论。精彩留言会获得点赞!