用于宫颈癌检测的DNA甲基化qPCR试剂盒及其使用方法与流程
本发明属于生物技术和dna检测技术领域,尤其涉及一种用于宫颈癌检测的dna甲基化qpcr试剂盒及其使用方法、应用,具体而言,涉及一种利用宫颈细胞dna进行甲基化qpcr以确定一个目标基因靶点的甲基化状态来用于宫颈癌检测或筛查的试剂盒及其使用方法,此外,本发明还涉及上述检测试剂盒在生物医学中的应用。
背景技术:
宫颈癌是女性最常见的癌症之一,多发生于宫颈鳞柱交界处(移行带)。在全球范围内,估计2018年有57万例新发病例,占所有癌症死亡妇女的7.5%。而中国的宫颈癌病例占全球的28%以上,高发年龄为50—55岁。近年来,中国宫颈癌的发病率和死亡率一直呈上升趋势。其中85-90%为鳞状细胞癌,余下的10-15%中多数为腺癌。宫颈癌的临床表现多不明显,或仅有类似宫颈炎的症状,容易造成漏诊;一旦出现症状,多已发展到晚期,从而丧失了最佳的治疗窗口。
多项大型研究表明,定期接受宫颈癌筛查是预防宫颈癌的最佳方法。常用的宫颈癌筛检方式主要有两种,一种是常见的宫颈细胞学检查,包括传统的巴氏涂片(paptest)和液基薄层细胞技术(tct)两种方式,通过观察子宫颈部的分泌物而筛查可能发生癌变的非典型细胞,以早期侦测宫颈癌;另一种则为人类乳突病毒检测(hpvtesting),即观察宫颈脱落细胞中是否存在高危hpv亚型的感染。然而巴氏涂片法因取材、制片、阅片过程中存在的问题以及传统的巴氏五级分类法等都是导致它敏感性低的原因,故临床上假阴性者多见;液基薄层细胞技术因相关设备及检查耗材价格昂贵,导致它难以普及;人类乳突病毒检测虽然具有高敏感度,却容易造成高的假阳性,会导致临床上的过度治疗和增加病人的负担。因此,临床上急需能够即时、准确,并且费用低的宫颈癌早期检测技术的出现。
dna甲基化改变是癌症进程中最早发生的分子变化之一,且具有组织特异性,肿瘤抑制基因的高甲基化水平已被确定为抑制基因表达和促进癌细胞生长和扩增的重要机制。在宫颈癌中,一些抑癌基因的cpg(胞嘧啶(c)后接续鸟苷(g))的高甲基化已被认为是癌症的生物标记之一。因此,对这些基因中的一种或多种的甲基化状态进行分析可用于诊断宫颈癌的状态。在宫颈癌筛查中,由于能直接收集到宫颈的上皮细胞,因此通过分析宫颈细胞中的基因甲基化来早期诊断、检测或者筛查宫颈癌,比发生在其他器官上的肿瘤更容易操作。
技术实现要素:
在上述资料的基础上,我们通过更加广泛和深入的研究,发现了可用于早期宫颈癌筛查的更好的甲基化基因靶点,并设计出数套可针对这些靶点进行甲基化检测的引物及探针组合,我们的方案可取得更高的检测特异性和敏感度,利用新发现的基因靶标检测组合制成了早期宫颈癌癌的检测和筛查试剂盒。
本发明的目的在于提供一种用于宫颈癌早期诊断、检测或者筛查的多基因联合检测引物探针组合试剂盒,以解决现有技术中存在的检测方法特异性和敏感性过低的缺陷。
本发明的第一方面在于提供一种用于宫颈癌检测的dna甲基化qpcr试剂盒,通过检测或测量受试样品dna中一种或多种特定基因的甲基化状态或水平来筛查和诊断宫颈癌。
在一些实施方式中,所述试剂盒包括检测或测量受试样品dna中一种或多种特定基因的甲基化状态或水平的特异性引物和探针,所述特定基因包括jam3和actb。
在一些实施方式中,用于检测jam3基因甲基化状态的特异性引物和探针选自下述三种特异性引物和探针组合中的任一种:特异性引物seqidno:1-2和探针seqidno:3、特异性引物seqidno:4-5和探针seqidno:6、特异性引物seqidno:7-8和探针seqidno:9。
在一些实施方式中,用于检测actb基因甲基化状态的特异性引物和探针为特异性引物seqidno:10-11和探针seqidno:12。
在一些实施方式中,所述特异性引物seqidno:1、2、4、5、7、8、10、11均经过硫代磷酸酯修饰,且在严格条件下与甲基化或非甲基化的目标基因区域杂交。
在一些实施方式中,所述探针seqidno:3、6、9、12是基于taqmantm设计的,且在严格条件下与甲基化或非甲基化的目标基因区域杂交。
在一些实施方式中,jam3基因探针seqidno:3、6、9核苷酸序列5’端标记cy5,3’端标记qsy;actb基因探针seqidno:12核苷酸序列5’端标记vic,3’端标记mgbnfq。
在一些实施方式中,所述特异性引物seqidno:1、2、4、5、7、8、10、11和所述探针seqidno:3、6、9、12的长度为10-50nt。
在一些实施方式中,所述试剂盒中还包含下述组成部分:dntp混合溶液、mgcl2溶液、dna聚合酶、pcr反应缓冲液、pcr去离子水。
在一些实施方式中,所述试剂盒中还包含下述组成部分:组织基因组dna提取试剂和dna甲基化转化试剂,优选地,所述宫颈细胞dna甲基化转化试剂为亚硫酸氢盐。
在一些实施方式中,所述受试样品dna为完整基因组、无细胞dna或循环肿瘤dna。
在一些实施方式中,具体的特异性引物和探针序列如下表1所示:
表1本发明试剂盒中包含的特异性引物和探针
本发明的第二方面在于提供一种根据第一方面所述的试剂盒的使用方法,
(1)宫颈细胞中的dna提取:利用组织dna提取试剂从待测样本中提取宫颈细胞中的dna;
(2)dna甲基化转化:利用dna甲基化转化试剂对提取的宫颈细胞中的dna进行亚硫酸氢盐处理并随后进行纯化;
(3)将进行甲基化转化并纯化的血浆游离dna进行荧光定量pcr扩增,pcr反应结束后,将ct阈值设定在线性扩增区间,ct值小于40的扩增认定为阳性;
(4)结果判定:当内部参照位点actb检测结果阳性,靶点jam3的三个重复扩增中至少两个为阳性则确定为该靶点结果阳性;
优选地,所述第(3)步骤中,每个模板的pcr扩增做三个重复;
优选地,所述第(3)步骤中,选用下述方法中的任一种:甲基化特异性定量pcr、实时甲基化特异性pcr、使用甲基化dna特异性结合蛋白的pcr。
在一些实施方式中,每个反应体系10μl,其中含(0.5-1.5μl)1xpcr反应缓冲液、200-400μmdntps、3-6mmmgcl2、1-3uamplitaqgolddna聚合酶、30-60nmrox染料。
在一些实施方式中,jam3基因区域靶点的引物各300-500nm。
在一些实施方式中,jam3基因区域靶点的探针各200-300nm。
在一些实施方式中,actb基因区域靶点的引物150-250nm,actb基因区域靶点的探针50-150nm。
在一些实施方式中,pcr扩增条件为:90-100℃预变性8-12min;90-100℃变性10-20s,60-70℃退火和延伸60-70s,40-50个循环。
本发明的第三方面在于提供根据第一方面所述的试剂盒在在制备宫颈癌检测的试剂或医疗器械中的医用。
本发明的有益效果在于:
经实验测试,本发明的方法具有快速、灵敏度高和特异性高等特点,能够在早期及时对人宫颈癌进行诊断,使得早期准确诊断宫颈癌成为可能,避免了医疗资源的浪费。
经实验测试,本发明试剂盒能够显著提高早期宫颈癌的阳性检出率和特异性(真实阴性率)。
附图说明
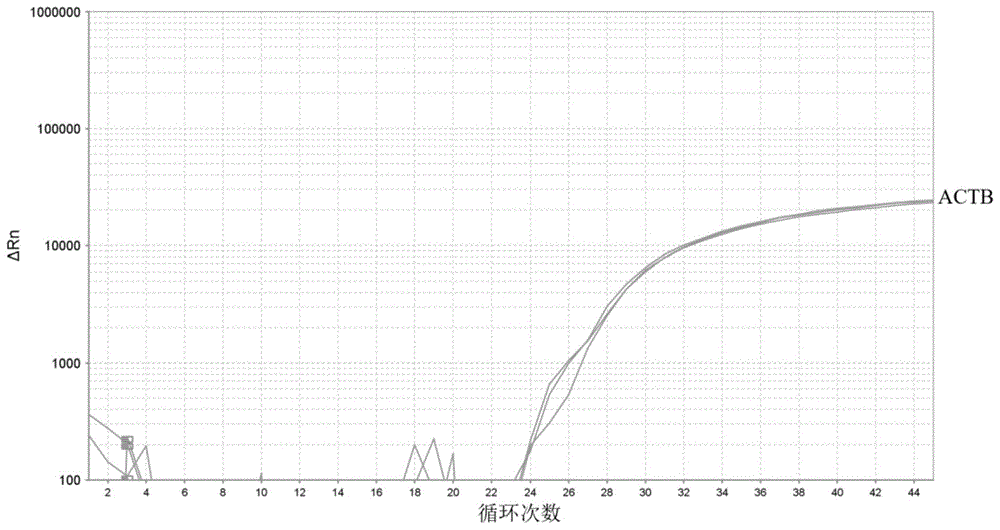
图1为本发明一种实施方式的试剂盒的非宫颈癌对照人群的宫颈刷片样本dna甲基化qpcr扩增曲线图;
图2为本发明一种实施方式的试剂盒的宫颈癌患者的宫颈刷片样本dna的甲基化qpcr扩增曲线图;
图3为本发明实施例1和2中利用试剂盒对宫颈癌癌的诊断价值分析(roc曲线)结果。
具体实施方式
以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
在进一步描述本发明具体实施方式之前,应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围。
下述实施例中所用材料、试剂等,如无特殊说明,均可从商业途径得到。
定义
术语“患者”、“个体”或“受试者”可以在本文中互换使用,可以指哺乳动物,特别是人类。所述受试者可能有轻度、中度或重度疾病。所述患者可能是未治、易治或难治。所述患者可能是基于特定症状或家族病史需要治疗或需要诊断的个体。
术语“样本”、“患者样本”、“生物样本”等包括从患者、个体或受试者获得的各种样本类型,并且可用于诊断或监测检测。所述患者样本可以从健康受试者、患病患者或患有宫颈癌相关症状的患者获得。而且,从患者获得的样本可以被分割,并且只有一部分可以用于诊断。此外,所述样本或其一部分可以在保持样本用于以后分析的条件下储存。该定义具体包括血液和其他生物来源的液体样本(包括但不限于外周血、血清、血浆、尿、唾液、痰、粪便和滑液),固体组织样本(如活检标本或组织培养物或由其衍生的细胞及其后代)。该定义还包括在获取后以任何方式操作的样本,如通过离心、过滤、沉淀、透析、色谱法、试剂处理、洗涤或富集某些细胞群。这些术语还包括临床样本、培养细胞、细胞上清液、组织样本、器官等。所述样本还可以包含新鲜冷冻和/或福尔马林固定的石蜡包埋组织块,例如由临床或病理活组织检查制备的块,其被制备用于病理分析或通过免疫组织化学研究。
术语“测量”、“确定”、“检测”或“检查”在全文中可互换使用,并且可以指包括获得患者样本和/或检测患者样本中的生物标志物甲基化状态或水平的方法。在一个实施方式中,这些术语是指获得患者样本并检测样本中一种或多种生物标志物的甲基化状态或水平。在另一个实施方式中,术语“测量”、“确定”或“检测”是指检测患者样本中一种或多种生物标志物的甲基化状态或水平。测量可以通过本领域已知的方法和本文进一步描述的方法完成,包括但不限于甲基化特异性定量聚合酶链式反应(qpcr)。
术语“甲基化”是指在胞嘧啶的c5或n4位置、腺嘌呤的n6位置的胞嘧啶甲基化或其他类型的核酸甲基化。体外扩增的dna是未甲基化的,因为体外dna扩增方法不保留扩增模板的甲基化模式。然而,“未甲基化的dna”或“甲基化的dna”也可以分别指其原始模板是未甲基化或甲基化的扩增dna。
术语“cpg岛”是指具有高密度cpg的基因组dna的连续区域。
术语“甲基化状态”或“甲基化水平”是指特定核苷酸或部分dna中的核苷酸处的甲基化的存在、不存在和/或量。
应该理解的是,无论在何处使用语言“包括”描述实施例,还提供了以“由…组成”和/或“基本上由…组成”描述的其他类似实施例。
实施例1:利用本发明试剂盒对非宫颈癌对照人群的样本进行宫颈癌甲基化多重qpcr检测
(一)实验材料
1.非宫颈癌对照人群的宫颈刷片10例;
2.组织基因组dna提取试剂盒(北京天根生化科技有限公司);
3.ezdnamethylation-lightning试剂盒(购自zymoresearch公司);
4.本发明试剂盒(其中包含检测靶点jam3的组合1引物及探针组合、actb扩增引物及探针);
5.amplitaqgoldtmdna聚合酶及缓冲试剂(购自thermofisher公司)。
(二)实验方法
1.宫颈组织,和宫颈细胞刷片dna提取
取1.0ml临床上经病理已经确认的非宫颈癌对照人群的宫颈刷片样本到1.5ml离心管,12000rmp离心3-5min,去掉上清,收集宫颈细胞;然后用北京天根生化科技有限公司的组织基因组dna提取试剂盒提取dna。
2.dna甲基化转化
使用zymoresearch公司的ezdnamethylation-lightning试剂盒对提取的10份dna进行亚硫酸氢盐处理并随后进行纯化。
3.qpcr扩增
对亚硫酸氢盐处理过的dna使用thermofisher公司quantstudio3仪器进行qpcr扩增,每个模板的pcr扩增做三个重复。每个反应体系10μl,其中含1xpcr反应缓冲液、400μmdntps、4mmmgcl2、2uamplitaqgolddna聚合酶、30nmrox染料;jam3基因区域靶点的引物各800nm(每个靶点只选择一对引物),jam3基因区域靶点的探针各500nm(每个靶点选择一条与所选引物相对应的探针);actb基因区域靶点的引物200nm,actb基因区域靶点的探针100nm。
pcr扩增条件为:95℃预变性10min;
95℃变性15s,65℃退火和延伸30s,45个循环;
pcr反应结束后,将ct阈值设定在线性扩增区间(本实验中,设定δrn为0.1),ct值小于40的扩增认定为阳性。
(三)实验结果
对于结果的判定标准是,内部参照位点(actb)检测结果阳性,jam3检测位/靶点的三个重复扩增中至少两个为阳性则确定为结果阳性。
下表2显示的是使用本发明的多重测定(jam3)对从5个非宫颈癌对照个体获得的5份宫颈刷片样品进行检测的结果(图1)。由表2可见,本方案检测特异性非常高。
表2利用本发明试剂盒对非宫颈癌对照人群的宫颈刷片样品的检测结果
实施例2:利用本发明试剂盒对宫颈癌患者dna样本进行宫颈癌甲基化多重qpcr检测
(一)实验材料
1.宫颈癌患者的宫颈刷片10例;
2.组织基因组dna提取试剂盒(北京天根生化科技有限公司);
3.ezdnamethylation-lightning试剂盒(购自zymoresearch公司);
4.本发明试剂盒(其中包含检测靶点jam3的其中组合1引物及探针组合、actb扩增引物及探针);
5.amplitaqgoldtmdna聚合酶及缓冲试剂(购自thermofisher公司)。
(二)实验方法
1.宫颈组织,和宫颈细胞刷片dna提取
取1.0ml临床上经病理已经确认的宫颈癌患者的宫颈刷片样本到1.5ml离心管,12000rmp离心3-5min,去掉上清,收集宫颈细胞;然后用北京天根生化科技有限公司的组织基因组dna提取试剂盒提取dna。
2.dna甲基化转化
使用zymoresearch公司的ezdnamethylation-lightning试剂盒对提取的10份dna进行亚硫酸氢盐处理并随后进行纯化。
3.qpcr扩增
对亚硫酸氢盐处理过的dna使用thermofisher公司quantstudio3仪器进行qpcr扩增,每个模板的pcr扩增做三个重复。每个反应体系10μl,其中含1xpcr反应缓冲液、400μmdntps、4mmmgcl2、2uamplitaqgolddna聚合酶、30nmrox染料;jam3基因区域靶点的引物各800nm(每个靶点只选择一对引物),jam3基因区域靶点的探针各500nm(每个靶点选择一条与所选引物相对应的探针);actb基因区域靶点的引物200nm,actb基因区域靶点的探针100nm。
pcr扩增条件为:95℃预变性10min;
95℃变性15s,65℃退火和延伸30s,45个循环;
pcr反应结束后,将ct阈值设定在线性扩增区间(本实验中,设定δrn为0.1),ct值小于40的扩增认定为阳性。
(三)实验结果
对于结果的判定标准是,内部参照位点(actb)检测结果阳性,jam3检测位/靶点的三个重复扩增中至少两个为阳性则确定为结果阳性。
下表3显示的是使用本发明的多重测定(jam3)对从10个宫颈癌患者获得的10份宫颈刷片样品进行检测的结果(图2)。由表3可见,本方案阳性检出率非常高。
表3利用本发明试剂盒对宫颈癌患者的宫颈刷片样本的检测结果
综合实施例1和实施例2,可以看出,利用本发明试剂盒进行宫颈癌筛查,其阳性检出率为86.3%,特异性(真实阴性率)为100%,其诊断价值分析值(roc曲线)为0.90(图3)。
与实施例1不同的,采用包含检测靶jam3的组合2引物及探针组合、包含检测靶点jam3的组合3引物及探针组合的试剂盒,对非宫颈癌对照人群的样本和宫颈癌患者的宫颈刷片样本检测取得了与实施例1、实施例2类似的结果。
以上对本发明优选的具体实施方式和实施例作了详细说明,但是本发明并不限于上述实施方式和实施例,在本领域技术人员所具备的知识范围内,还可以在不脱离本发明构思的前提下作出各种变化。
序列表
<110>深圳市新合生物医疗科技有限公司
<120>用于宫颈癌检测的dna甲基化qpcr试剂盒及其使用方法
<160>12
<170>siposequencelisting1.0
<210>1
<211>22
<212>dna
<213>人工序列
<400>1
aaacgttgtgttgagttcggta22
<210>2
<211>20
<212>dna
<213>人工序列
<400>2
ctcgccaacgtttttcgtta20
<210>3
<211>22
<212>dna
<213>人工序列
<400>3
gaatcgtcgtaaatgtgtaacg22
<210>4
<211>20
<212>dna
<213>人工序列
<400>4
cggtcggtgtgtttaggagt20
<210>5
<211>22
<212>dna
<213>人工序列
<400>5
caaacttctaccgaactcaaca22
<210>6
<211>22
<212>dna
<213>人工序列
<400>6
aagtttgttagcgaaaacgttg22
<210>7
<211>20
<212>dna
<213>人工序列
<400>7
tcgatcgtgtcgtcgttatc20
<210>8
<211>21
<212>dna
<213>人工序列
<400>8
cacaaccatctcttccttcca21
<210>9
<211>23
<212>dna
<213>人工序列
<400>9
tcgttgtacgggtagttaaaagt23
<210>10
<211>26
<212>dna
<213>人工序列
<400>10
tagggagtatataggttggggaagtt26
<210>11
<211>27
<212>dna
<213>人工序列
<400>11
aacacacaataacaaacacaaattcac27
<210>12
<211>25
<212>dna
<213>人工序列
<400>12
tggtgatggaggaggtttaggcagt25
- 还没有人留言评论。精彩留言会获得点赞!