一种结直肠癌筛查标志组合物及其选取方法、结直肠癌筛查试剂盒与流程
1.本发明涉及体外诊断技术领域,特别涉及一种结直肠癌筛查标志组合物及其选取方法、结直肠癌筛查试剂盒。
背景技术:
2.结直肠癌(colorectal cancer, crc) 是全球第四大男性常见癌症,是全球第二大女性常见癌症,在发达国家的发病率最高。近年来,随着我国人民生活水平的提高,生活习惯与饮食结构的改变,环境污染日益严重,我国结直肠癌的发病率不断增加。国家癌症早诊早治项目专家委员会2013年的研究报告指出,我国40岁以上的高危人群患进展期腺瘤和早期肠癌的比率为6% 。据2015年《中国肿瘤登记年报》统计,结直肠癌的发病率近年来仍在增长,每年死亡患者多达23万人。
3.结直肠癌主要包括结肠癌与直肠癌两大类,其发展是一个渐进过程:增生>小腺瘤>大腺瘤>重度非典型增生>早期腺癌>晚期腺瘤。大多数肠癌形成之前以息肉(异常突起)或腺瘤(腺上皮良性肿瘤)的形式在发病部位缓慢发展多年,在此期间患者无任何不适。随着时间的推移,部分腺瘤可转变为癌症。在癌变过程中,肿瘤细胞侵入肠壁,与血管或淋巴管融合,通过吸收患者养分迅速扩增。后期,癌细胞通过淋巴管侵入附近的淋巴结或身体的其它器官,形成癌扩散。结直肠癌在早期并没有明显症状,通常发展至晚期才有明显症状显现,如腹痛,便血等。
4.我国大多数患者缺乏癌症早期筛查的意识,由于疾病早期症状不明显,发现明显症状后才到医院进行检查,至被确诊为结直肠癌时,癌细胞已经扩散,错失最佳的治疗时间。中晚期患者所需治疗费用高、疗效差、五年生存率低。如果能够在早期发现结直肠癌,不仅治疗费用降低,还能早期筛查甚至治愈,因此亟待开发更好的结直肠癌筛查方法。
5.结直肠癌的筛查方法主要包括粪便隐血检测与肠镜检查。其中,粪便隐血检测敏感性与特异性较低;肠镜检查虽然准确度高,但属于侵入性检测,患者依从性低。随着人类基因组计划的完成以及高通最测序技术的发展,基因筛查技术已成为一种新的结直肠癌诊断方法,在结直肠癌的早期诊断中有显著的优势。
技术实现要素:
6.本发明的主要目的是提供一种结直肠癌筛查标志组合物,旨在解决现有结直肠癌诊断方法对于早期病变检测灵敏度低,肠镜检查难以接受的问题。
7.为实现上述目的,本发明提出一种结直肠癌筛查标志组合物,其特征在于,包括:第一靶标:所述第一靶标的位置包括chr5:100,238,835
‑
100,239,200;第二靶标:所述第二靶标的位置包括chr15:79,383,462
‑
79,383,827;第三靶标:所述第三靶标的位置包括chr5:100,238,840
‑
100,239,205;第四靶标:所述第四靶标的位置包括chr7:45,018,729
‑
45,018,908;
第五靶标:所述第五靶标的位置包括chr11:60,738,950
‑
60,739,349;第六靶标:所述第六靶标的位置包括chr17:75,369,779
‑
75,370,053。
8.本技术还提出一种结直肠癌筛查标志组合物的选取方法,包括:筛选结直肠癌人群早期基因组超甲基化区域,并与白细胞基因组对应区域进行比对;选取在白细胞中低甲基化,结直肠癌中高甲基化,且含有ccgc,ccgg,gcgc,acgt,gcgg中至少一个位点的区域作为靶标。
9.优选地,选取在白细胞中低甲基化,结直肠癌中高甲基化,且含有ccgc,ccgg,gcgc,acgt,gcgg中至少两个位点的区域作为靶标。
10.优选地,所述标志组合物包括:第一靶标:所述第一靶标的位置包括chr5:100,238,835
‑
100,239,200;第二靶标:所述第二靶标的位置包括chr15:79,383,462
‑
79,383,827;第三靶标:所述第三靶标的位置包括chr5:100,238,840
‑
100,239,205;第四靶标:所述第四靶标的位置包括chr7:45,018,729
‑
45,018,908;第五靶标:所述第五靶标的位置包括chr11:60,738,950
‑
60,739,349;第六靶标:所述第六靶标的位置包括chr17:75,369,779
‑
75,370,053。
11.本发明还提出一种结直肠癌筛查试剂盒,包括用于检测上述的结直肠癌筛查标志组合物的引物和探针。
12.优选地,所述结直肠癌筛查试剂盒包括:用于检测所述第一靶标的上游引物序列为seq id no.1,下游引物序列为seq id no.2,探针序列为seq id no.3;用于检测所述第二靶标的上游引物序列为seq id no.4,下游引物序列为seq id no.5,探针序列为seq id no.6;用于检测所述第三靶标的上游引物序列为seq id no.7,下游引物序列为seq id no.8,探针序列为seq id no.9;用于检测所述第四靶标的上游引物序列为seq id no.10,下游引物序列为seq id no.11,探针序列为seq id no.12;用于检测所述第五靶标的上游引物序列为seq id no.13,下游引物序列为seq id no.14,探针序列为seq id no.15;用于检测所述第六靶标的上游引物序列为seq id no.16,下游引物序列为seq id no.17,探针序列为seq id no.18。
13.优选地,所述结直肠癌筛查试剂盒使用的内参基因为β
‑
actin。
14.可选地,用于检测所述β
‑
actin的上游引物序列为seq id no.19,下游引物序列为seq id no.20,探针序列为seq id no.21。
15.可选地,所述结直肠癌筛查试剂盒还包括甲基化敏感内切酶,所述甲基化敏感内切酶包括hinp1i、hpaii、acii和hpych4iv。
16.本发明还提出上述的引物和探针在制备结直肠癌筛查试剂盒的应用。
17.本发明技术方案的结直肠癌筛查标志组合物在结直肠癌中高甲基化,白细胞中低甲基化,且具有甲基化敏感内切酶酶切位点,利用甲基化敏感内切酶不能切割甲基化位点
的特性,降解非肿瘤来源cfdna,特异扩增肿瘤来源ctdna,极大提升检查灵敏度。并且ctdna的检测是非侵入性的,具有迅速,便捷,无创的特点,可以提高患者对于结直肠癌筛选的接受度。通过更精准有效的检测排查早期结直肠癌,进而降低结直肠癌的死亡率,减少结直肠癌的伤害。
附图说明
18.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图示出的结构获得其他的附图。
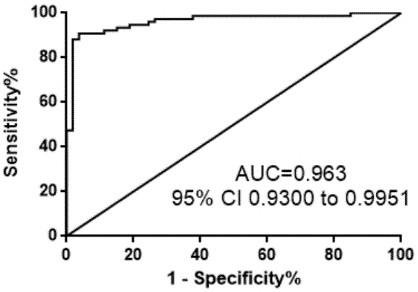
19.图1为健康者和结直肠癌患者结直肠癌风险性能测试结果图;图2为结直肠癌高风险判读结果图;图3为早期结直肠癌风险分类器性能验证图。
20.本发明目的的实现、功能特点及优点将结合实施例,参照附图做进一步说明。
具体实施方式
21.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
22.循环肿瘤dna(circulating tumor dna,ctdna)来源于肿瘤细胞的凋亡、坏死或分泌产生的dna片段,是循环游离dna(circulatingcell
‑
free dna,cfdna)的一部分。健康人群中大部分cfdna的长度在167 bp左右,但肿瘤患者的ctdna长度有所缩短。ctdna含有与其来源肿瘤dna同样的基因缺陷,如点突变、重排、扩增、微卫星改变、表观遗传修饰等。当肿瘤dna进入血液时,这些基因缺陷模式在血浆和血清中也可被检测到。
23.本发明提出一种结直肠癌筛查标志组合物,其特征在于,包括:第一靶标:所述第一靶标的位置包括chr5:100,238,835
‑
100,239,200;第二靶标:所述第二靶标的位置包括chr15:79,383,462
‑
79,383,827;第三靶标:所述第三靶标的位置包括chr5:100,238,840
‑
100,239,205;第四靶标:所述第四靶标的位置包括chr7:45,018,729
‑
45,018,908;第五靶标:所述第五靶标的位置包括chr11:60,738,950
‑
60,739,349;第六靶标:所述第六靶标的位置包括chr17:75,369,779
‑
75,370,053。
24.上述结直肠癌筛查标志组合物的选取方法,包括:筛选结直肠癌人群早期基因组超甲基化区域,并与白细胞基因组对应区域进行比对;选取在白细胞中低甲基化,结直肠癌中高甲基化,且含有ccgc,ccgg,gcgc,acgt,gcgg中至少一个位点的区域作为靶标。
25.通过选取结直肠癌肿瘤高甲基化,白细胞低甲基化的区域,更方便检出结直肠癌。由于血浆里面大部分是白细胞碎片化dna,需要去掉这部分dna的背景干扰,所以靶标区域
在白细胞基因组中不能高甲基化,否则无法检出真正特异化的肿瘤来源的核酸。因此,筛选靶标位点的标准:1、白细胞中位点的甲基化程度低;2、肿瘤位点的甲基化程度高。
26.其中,ccgc,ccgg,gcgc,acgt和gcgg均为甲基化敏感内切酶的酶切位点,c/cgc和g/cgg均为acii的酶切位点,c/cgg为hpaii的酶切位点,g/cgc为hinp1i的酶切位点,a/cgt为hpych4iv的酶切位点,斜线为切割位点。
27.本发明技术方案的结直肠癌筛查标志组合物在结直肠癌中高甲基化,白细胞中低甲基化,且具有甲基化敏感内切酶酶切位点,利用甲基化敏感内切酶不能切割甲基化位点的特性,降解非肿瘤来源cfdna,特异扩增肿瘤来源ctdna,极大提升检查灵敏度。并且ctdna的检测是非侵入性的,具有迅速,便捷,无创的特点,可以提高患者对于结直肠癌筛选的接受度。通过更精准有效的检测排查早期结直肠癌,进而降低结直肠癌的死亡率,减少结直肠癌的伤害。
28.优选地,选取在白细胞中低甲基化,结直肠癌中高甲基化,且含有ccgc,ccgg,gcgc,acgt,gcgg中至少两个位点的区域作为靶标。
29.具体的,靶标内可以包含其中2
‑
5个酶切位点,选择包含至少两个酶切位点,可以防止甲基化敏感内切酶酶切的时候有些酶没有工作,从而出现假阳性的情况,至少两个位点可以保证背景dna有更高的概率被切掉,提高检测准确性。
30.本发明还提出一种结直肠癌筛查试剂盒,包括用于检测上述的结直肠癌筛查标志组合物的引物和探针。
31.优选地,所述标志组合物包括:第一靶标:所述第一靶标的位置包括chr5:100,238,835
‑
100,239,200;第二靶标:所述第二靶标的位置包括chr15:79,383,462
‑
79,383,827;第三靶标:所述第三靶标的位置包括chr5:100,238,840
‑
100,239,205;第四靶标:所述第四靶标的位置包括chr7:45,018,729
‑
45,018,908;第五靶标:所述第五靶标的位置包括chr11:60,738,950
‑
60,739,349;第六靶标:所述第六靶标的位置包括chr17:75,369,779
‑
75,370,053。
32.针对上述标志组合物可以设计不同的引物和探针来检测,例如本技术人设计100余对引物,从中筛选pcr效率高,特异性强,稳定性好的引物,最终得到6对可用于判别早期结直肠癌风险的特异性引物及对应探针序列,如表1所示。
33.优选地,所述结直肠癌筛查试剂盒包括:用于检测所述第一靶标的上游引物序列为seq id no.1,下游引物序列为seq id no.2,探针序列为seq id no.3;扩增序列为seq id no.22。
34.用于检测所述第二靶标的上游引物序列为seq id no.4,下游引物序列为seq id no.5,探针序列为seq id no.6;扩增序列为seq id no.23。
35.用于检测所述第三靶标的上游引物序列为seq id no.7,下游引物序列为seq id no.8,探针序列为seq id no.9;扩增序列为seq id no.24。
36.用于检测所述第四靶标的上游引物序列为seq id no.10,下游引物序列为seq id no.11,探针序列为seq id no.12;扩增序列为seq id no.25。
37.用于检测所述第五靶标的上游引物序列为seq id no.13,下游引物序列为seq id no.14,探针序列为seq id no.15;扩增序列为seq id no.26。
38.用于检测所述第六靶标的上游引物序列为seq id no.16,下游引物序列为seq id no.17,探针序列为seq id no.18;扩增序列为seq id no.27。
39.表1 靶标特异性引物和探针序列和扩增序列
优选地,所述结直肠癌筛查试剂盒使用的内参基因为β
‑
actin。内参基因可以是在cfdna存在的管家基因即可,不同的内参基因,阳性检出值不同,最后的肿瘤判断阈值不同。
40.可选地,用于检测所述β
‑
actin的上游引物序列为seq id no.19,下游引物序列为seq id no.20,探针序列为seq id no.21,如表2所示。
41.可选地,所述结直肠癌筛查试剂盒还包括甲基化敏感内切酶,所述甲基化敏感内切酶包括hinp1i、hpaii、acii和hpych4iv。
42.表2 内参基因特异性引物和探针序列本发明还提出上述的引物和探针在制备结直肠癌筛查试剂盒的应用。
43.下面将结合具体实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
44.实施例1.取5 ml血浆,使用qiagen血浆游离dna提取试剂盒(cat: 55204)提取cfdna。
45.2. 取20 ng 提取的cfdna与hinp1i(cat:r0124, neb), hpaii(cat:r0171, neb), acii(cat:r0551, neb), hpych4iv(cat: r0619, neb)四种甲基化敏感内切酶(终浓度10 u/μl),20 μl体系,37℃孵育16 h,80℃酶失活20 min,酶切体系如表3所示,切割白
细胞来源的cfdna。
46.表3 甲基化敏感内切酶酶切体系3. 将孵育完成的全部产物作为模板,加入上述6对靶标特异引物(每种50 nm)和1对内参引物(10 nm),配置体系进行多重pcr,反应体系如表4所示,多重pcr反应程序为:98℃/45 s;8cycles (98℃/15 s, 55℃/30 s, 72℃/30 s);72℃/1 min;4℃/hold,反应得到多重pcr产物,扩增肿瘤来源的cfdna。
47.表4 多重pcr反应体系4. 取上步3中1μl多重pcr产物做为模板,加入6对靶标特异引物(每种0.25 μm),以及对应的6个特异性引物探针(每种0.1μm),再加1对内参引物(0.05 μm),及内参引物探针(0.02 μm),20 μl体系在abi 7500荧光pcr仪中进行qpcr反应。qpcr反应体系如表5所示,qpcr反应程序为:95℃/3 min;40cycles (98℃/15 s,60℃/60 s);每轮循环结束前采集fam及vic通道信号。
48.表5 qpcr反应体系5. 根据6对靶标特异引物与1个内参引物ct值之差,评估结直肠癌风险。
49.其中,δct= 内参引物扩增ct值
‑
6对引物特异扩增ct值,如图2所示,提示结直肠癌高风险。
50.对53例健康者和76例
ⅰ‑ⅲ
期结直肠癌患者的血液样本同时采用本发明方案评估结直肠癌风险性能,样本信息和测试结果如表6所示,并根据表6的数据制备得到图1所示的结果图。
51.表6 健康者和结直肠癌患者结直肠癌风险性能测试结果健康者和结直肠癌患者结直肠癌风险性能测试结果
将表6中的数据导入到graphpad prism 6.0软件中,自动生成roc曲线,并统计曲线下面积auc值,如图3所示,图3中横坐标为1
‑
特异度,纵坐标为敏感度,软件统计结果以δct>
‑
1.65为阈值,分类器敏感度90.79%,特异度96.23%。
52.因此,本发明方案的结直肠癌评估方式为:δct>
‑
1.65 结直肠癌高风险,建议定期ct检测;δct≤
‑
1.65 结直肠癌低风险。
53.以上所述仅为本发明的可选实施例,并非因此限制本发明的专利范围,凡是在本发明的发明构思下,利用本发明说明书及附图内容所作的等效结构变换,或直接/间接运用在其他相关的技术领域均包括在本发明的专利保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1