用于校准分析物测量值的方法以及系统与流程
本发明涉及医学检测领域,具体而言,涉及一种确定应用于待校准测量系统的校准系数的方法,以及一种用于校准待测样本中的分析物的测量值的方法和系统,以用于临床检验中。
背景技术:
在临床医学检验中,通常需要对生化分析仪进行定期校准或者对在每次测量前或测量时对标准品进行测量从而控制仪器状态、不同批次的试剂、室内环境因素或人员操作造成的误差。在质控过程中,需要确定校准曲线,并且根据确定的校准曲线对分析物的测量值进行校准。
而在传统的医学检验中使用的样本通常是病人到医院现场采集的新鲜样本,这样的样本采集方法存在受时间空间限制、样本运输不便或保存时间短暂等问题,因此现阶段开发了一些新型的不需要到医院去采样的方法,例如,在家或其他任意场所随时根据需要进行干血斑片采样或者干尿斑片采样方法等。这些采样方法提供了方便廉价的样品采集,可以很容易地通过邮件、包裹等方式被运到分析实验室,并且可以稳定地进行长期贮存。
然而由于上述采样方法不同于传统的采样方法,并且存储时间较长,所以迫切地需要建立一种校准对新型采样方法得到的样品进行测量的系统的方法。同时也迫切需要确定存储时间的长短对于通过新型采样方法获得的样品中分析物的测量值的影响。
技术实现要素:
本申请提供了一种确定使用了不同的样本处理方法并经一定存储时间的待校准测量系统的校准系数的方法以及校准上述使用了不同的样本处理方法并经一定存储时间的待测样本中的分析物的测量值的方法。
在本申请的一个方面中,提供了一种一种确定应用于待校准测量系统的校准系数的方法,包括:获取N1个校准用样本对,其中每个校准用样本对包括方法一样本以及方法二样本,且所述每个校准用样本对中的方法一样本和方法二样本是基于同一来源的样本;将所述N1个校准用样本对存储时间T1,对每个所述存储时间T1后的方法一样本MT1以及相应的方法二样本ST1中的分析物的含量进行检测,其中N1个所述方法一样本中的分析物的测量值分别为Y1,T1,Y2,T1…YN1,T1,并且对应的N1个所述方法二样本中的分析物的测量值分别为X1,T1,X2,T1…XN1,T1,N1为大于等于2的整数;以及通过对上述测量值Y1,T1,Y2,T1…YN1,T1以及X1,T1,X2,T1…XN1,T1进行数据处理,确定反映在存储时间T1时方法一样本与方法二样本中的分析物的测量值之间映射关系的校准方程的校准系数。在某些实施方式中,所述数据处理是通过鲁棒的估计方法进行的。在某些实施方式中,所述校准方程为线性方程。在某些实施方式中,所述校准系数包括斜率AT1及轴截距BT1。
在某些实施方式中,所述确定校准系数的步骤包括:以所述X1,T1,X2,T1…XN1,T1中的每一个为横坐标和所述Y1,T1,Y2,T1…YN1,T1中的相应一个为纵坐标获得N1个校准点;确定所述N1个校准点之间的一个或多个可能斜率,其中借助至少一个鲁棒的估计方法,确定概率斜率AT1,其中所述鲁棒的估计方法是在出现异常值或分布假设仅近似有效的情况下也仍提供稳定的统计估计量的统计估计方法;并且通过所述N1个校准点确定多条具有概率斜率AT1的直线,确定每条所述具有概率斜率AT1的直线的轴截距,借助至少一个所述鲁棒的估计方法,由多个轴截距确定概率及轴截距BT1。在某些实施方式中,所述确定校准系数的步骤进一步包括:执行似然性观察,其中在似然性观察时丢弃不现实的校准点和/或不现实的斜率和/或不现实的轴截距。
在某些实施方式中,所述确定应用于待校准测量系统的校准系数的方法进一步包括:获取Ni个校准用样本对,将其存储时间Ti,其中所述Ti不等于T1;对 每个所述存储时间Ti后的方法一样本MTi以及相应的方法二样本STi中的分析物的含量进行检测,其中Ni个所述方法一样本中的分析物的测量值分别为Y1,Ti,Y2,Ti…YNi,Ti,并且对应的Ni个所述方法二样本中的分析物的测量值分别为X1,Ti,X2,Ti…XNi,Ti,Ni为大于等于2的整数;以及通过对上述测量值Y1,Ti,Y2,Ti…YNi,Ti以及X1,Ti,X2,Ti…XNi,Ti进行数据处理,确定反映在存储时间Ti时方法一样本与方法二样本中的分析物的测量值之间映射关系的校准方程的校准系数。在某些实施方式中,所述数据处理是通过鲁棒的估计方法进行的。在某些实施方式中,所述校准方程为线性方程。在某些实施方式中,所述校准系数包括斜率ATi及轴截距BTi。
在某些实施方式中,所述确定应用于待校准测量系统的校准系数的方法进一步包括:获取Z对斜率ATi及轴截距BTi,其中所述Z为大于等于2的整数;分别确定斜率ATi以及轴截距BTi随存储时间Ti变化的回归曲线;基于所述斜率随时间变化的回归曲线确定所述斜率随时间变化的回归方程A(t);以及基于所述轴截距随时间变化的回归曲线确定所述轴截距随存储时间变化的回归方程B(t)。
在某些实施方式中,所述方程A(t)和B(t)均为指数方程。在某些实施方式中,所述校准方程为:y=A(t)*x+B(t)。
在某些实施方式中,所述确定应用于待校准测量系统的校准系数的方法进一步包括:根据所述回归方程A(t)和所述回归方程B(t),对于任意存储时间Tβ,获得ATβ及BTβ的值;将所述ATβ及BTβ的值代入所述校准方程中,从而根据所述方法一样本中的分析物的测量值YNj,Tβ推得与其对应的所述方法二样本中的分析物的测量值XNj,Tβ。
在某些实施方式中,所述A(t)=(A1-A2)e-k(t-T0)+A2,其中t为样本的存储时间,所述t的范围为T0-T∞,单位为小时,A1为t=T0时获得的所述校准方程的斜率,A2为t=T∞时后获得的所述校准方程的斜率。并且,在某些实施方式中,所述T∞的值随着所述测量值y的不同而具有不同的值。在某些实施方式中,所述T0的范围为1-2小时。在某些实施方式中,T∞的范围为120-240小时。在某些实施方式中,k的范围为0.010-0.100。在某些实施方式中,A1的范围为0.5-5.0,优选地为0.85-0.90,A2的范围为0.5-5.0,优选地为0.65-0.80,A的范围为0.5-5.0, 优选地为0.65-0.90。
在某些实施方式中,所述B(t)=(B2-B1)(1-e-p(t-T0))+B1,其中t为样品存储的时间,所述t的范围为T0-T∞,单位为小时,B1为t=T0时获得的所述校准方程的轴截距,B2为t=T∞时后获得的所述校准方程的轴截距。并且,在某些实施方式中,所述T∞的值随着所述测量值y的不同而具有不同的值。在某些实施方式中,所述T0的范围为1-2小时。在某些实施方式中,T∞的范围为120-240小时。在某些实施方式中,p的范围为0.010-0.100。在某些实施方式中,B1大于等于0,优选地为0.0040-0.0050,B2大于等于0,优选地为0.0085-0.0170,B大于等于0,优选地为0.0040-0.0101。
本申请的另外一方面提供了一种用于校准经方法一处理的待测样本中的分析物的测量值的方法,包括:对所述待测样本中的分析物的含量进行检测,以确定测量值y,其中所述待测样本是经方法一处理后存储了时间t后所得到的;确定与所述存储时间t相对应的校准方程的校准系数,其中所述校准系数随着存储时间t的不同而变化;以及基于所述校准方程,将所述分析物的测量值y换算为其所对应的经方法二处理的样本中的分析物的测量值x,其中,所述测量值x代表与所述待测样本同一来源的经方法二处理的样本中将检测到的所述分析物的含量值。在某些实施方式中,每个经方法二处理的样本中所述分析物的测量值x不随存储时间的变化而变化。
在某些实施方式中,所述校准方程为:y=A(t)*x+B(t)。
在某些实施方式中,所述方程A(t)和B(t)均为指数方程。
在某些实施方式中,所述其中t为样本的存储时间,所述t的范围为T0-T∞,单位为小时,A1为t=T0时获得的所述校准方程的斜率,A2为t=T∞时后获得的所述校准方程的斜率。在某些实施方式中,所述T0的范围为1-2小时。在某些实施方式中,T∞的范围为120-240小时。在某些实施方式中,k的范围为0.010-0.100。在某些实施方式中,A1的范围为0.5-5.0,优选地为0.85-0.90。在某些实施方式中,A2的范围为0.5-5.0,优选地为0.65-0.80。在某些实施方式中,A的范围为0.5-5.0,优选地为0.65-1.0,更优选地为0.65-0.90。 在某些实施方式中,所述其中t为样品存储时间,所述t的范围为T0-T∞,单位为小时,B1为t=T0时获得的所述校准方程的轴截距,B2为t=T∞时后获得的所述校准方程的轴截距。在某些实施方式中,所述T0的范围为1-2小时。在某些实施方式中,T∞的范围为120-240小时。在某些实施方式中,p的范围为0.010-0.100。在某些实施方式中,B1大于等于0,优选地为0.0040-0.0050。在某些实施方式中,B2大于等于0,优选地为0.0085-0.0170。在某些实施方式中,B大于等于0,优选地为0.0020-0.0200,更优选地为0.0040-0.0101。
在某些实施方式中,所述待测样本为体液样本。在某些实施方式中,所述待测样本是经干燥处理后存储时间t后的体液干燥样本。在某些实施方式中,所述待测样本为干血样本,所述与待测样本同一来源的经方法二处理的样本为与所述待测样本同一来源的全血样本。在一些实施方式中,所述干血样本被采集和存储在干血斑片上。在某些实施方式中,所述待测样本为干尿样本,所述与待测样本同一来源的经方法二处理的样本为与所述待测样本同一来源的新鲜尿液样本。在一些实施方式中,所述干尿样本被采集和存储在干尿斑片上。
在某些实施方式中,所述分析物为蛋白,所述测量值x和y为蛋白含量百分比或蛋白重量。在某些实施方式中,所述蛋白是糖化血红蛋白、丙氨酸氨基转移酶、天冬氨酸氨基转移酶、碱性磷酸酶、r-谷氨酰转移酶、胆碱酯酶、谷氨酸脱氢酶、异柠檬酸脱氢酶、亮氨酸氨基肽酶、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇、肌酸激酶、肌酸激酶同工酶、乳酸脱氢酶、a-羟丁酸脱氢酶、补体C3、补体C4、免疫球蛋白A、免疫球蛋白M、免疫球蛋白G、抗链球菌溶血素、类风湿因子、前白蛋白、a-L-岩藻糖苷酶、转铁蛋白、脂蛋白a、尿微量白蛋白、5’核苷酸酶、载脂蛋白B、β2-微球蛋白、载脂蛋白A、糖化血红蛋白、腺苷脱氨酶、C-反应蛋白、胱抑素C、总蛋白、白蛋白、淀粉酶中的至少一种。在某些实施方式中,所述蛋白是糖化血红蛋白。
在某些实施方式中,所述待测样本的校准得到的标准测量值与其实际值的差异不超过20%,优选的不超过10%,更优选的在5%-10%之间,或在2%-5%之间,或不超过2%。
本申请的再一个方面提供了一种用于检测经方法一处理的待测样本中的分析物的测量值的系统,包括:样本收集器,其用于采集并储存待测样本;检测设备,其用于对所述待测样本中的分析物的含量进行检测,以确定测量值y,其中所述待测样本是经方法一处理后存储了时间t后所得到的;以及校准装置,其用于确定与所述存储时间t相对应的校准方程的校准系数,其中所述校准系数随着存储时间t的不同而变化,并用于基于所述校准方程,将所述分析物的测量值y换算为其所对应的经方法二处理的样本中的分析物的测量值x,其中,所述测量值x代表与所述待测样本同一来源的经方法二处理的样本中将检测到的所述分析物的含量值。
并且,在某些实施方式中,所述样本收集器为干血斑片。所述检测设备为高效液相色谱仪。
以上为本申请的概述,可能有简化、概括和省略细节的情况,因此本领域的技术人员应该认识到,该部分仅是示例说明性的,而不旨在以任何方式限定本申请范围。本概述部分既非旨在确定所要求保护主题的关键特征或必要特征,也非旨在用作为确定所要求保护主题的范围的辅助手段。
附图说明
通过下面说明书和所附的权利要求书并与附图结合,将会更加充分地描述本申请内容的上述和其他特征。可以理解,这些附图仅描绘了本申请内容的若干实施方式,因此不应认为是对本申请内容范围的限定。通过采用附图,本申请内容将会得到更加明确和详细的说明。
图1示出了根据本发明的一种具体实施方式的用于确定应用于待校准测量系统的校准系数的方法100的示例性流程图。
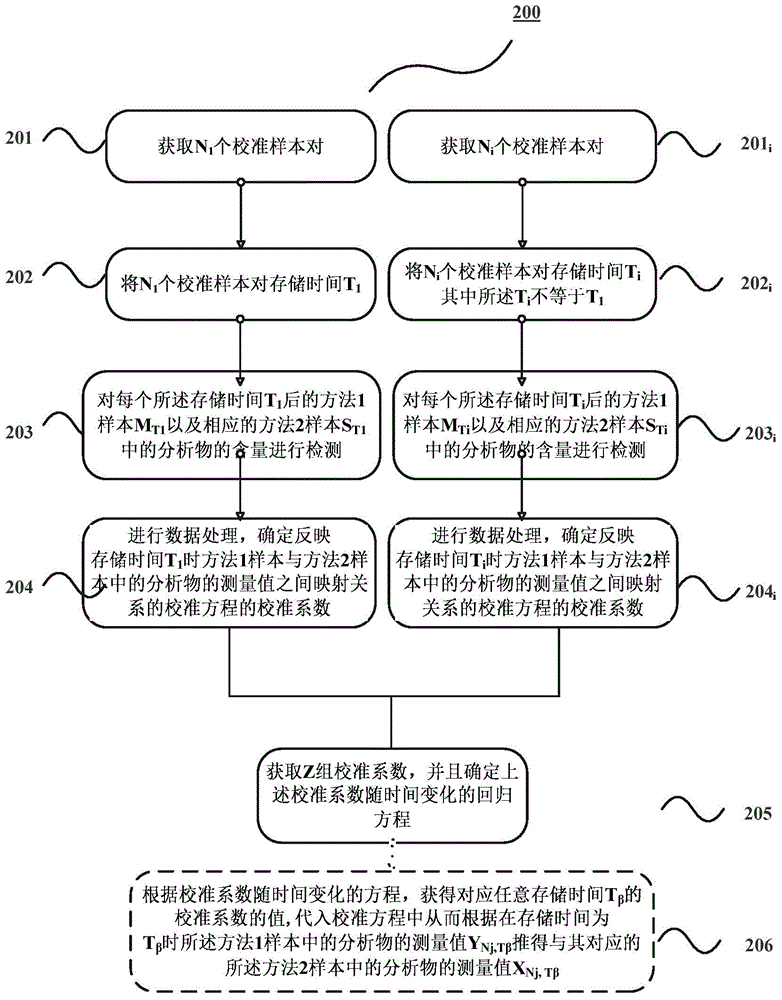
图2示出了根据本发明的另一种具体实施方式的用于确定应用于待校准测量系统的校准系数的方法200的示例性流程图。
图3示出了根据本发明的一种具体实施方式的用于校准经方法一处理的待测样本中的分析物的测量值的方法300的示例性流程图。
图4示出了将DBS(干血斑片)样本与WB(全血)样本均存储2小时,与其相对应的DBS(干血斑片)样本中HbA1c(糖化血红蛋白)的测量值y与WB(全血)样本中HbA1c的测量值x的关系。其中待测样本对数量为62对,以DBS样本中HbA1c的测量值为横坐标,以WB样本中HbA1c的测量值为纵坐标,获得62个校准点,借助鲁棒的线性回归方法确定概率斜率A为0.8713,概率轴截距B为0.0052,线性回归相关系数的平方R2=0.9923。
图5示出了将DBS样本存储2小时,WB样本存储时间19小时,与其相对应的DBS样本中HbA1c的测量值y与WB样本中HbA1c的测量值x的关系。其中待测样本对数量为62对,以DBS样本中HbA1c的测量值为横坐标,以WB样本中HbA1c的测量值为纵坐标,获得62个校准点,借助鲁棒的线性回归方法确定概率斜率A为0.8788,概率轴截距B为0.0053,线性回归相关系数的平方R2=0.9951。
图6示出了在3个不同的存储时间(分别为T0=2小时(图6a),T2=19小时(图6b),T3=38小时(图6c))的条件下DBS样本中HbA1c的测量值y与WB样本中HbA1c的测量值x的关系。其中待测样本对数量为62对,以相同存储时间条件下获得的DBS样本中HbA1c的测量值为横坐标,WB样本中HbA1c的测量值为纵坐标,相对应每个存储时间均获得62个校准点。在图6a中借助鲁棒的线性回归方法确定概率斜率A2为0.8699,概率轴截距B2为0.0058,线性回归相关系数的平方R2=0.996。在图6b中借助鲁棒的线性回归方法确定概率斜率A19为0.8191,概率轴截距B19为0.0075,线性回归相关系数的平方R2=0.9956。在图6c中借助鲁棒的线性回归方法确定概率斜率A38为0.8109,概率轴截距B38为0.0079,线性回归相关系数的平方R2=0.9956。
图7示出了在3个不同的存储时间(分别为T0=2小时(图7a),T2=70小时(图7b),T3=93小时(图7c))的条件下DBS样本中HbA1c的测量值y 与WB样本中HbA1c的测量值x的关系。其中待测样本对数量为72对,以相同存储时间条件下获得的DBS样本中HbA1c的测量值为横坐标,WB(全血)样本中HbA1c的测量值为纵坐标,相对应每个存储时间均获得72个校准点。在图7a中借助鲁棒的线性回归方法确定概率斜率A2为0.917,概率轴截距B2为0.0031,线性回归相关系数的平方R2=0.9969。在图7b中借助鲁棒的线性回归方法确定概率斜率A70为0.7812,概率轴截距B70为0.0096,线性回归相关系数的平方R2=0.994。在图7c中借助鲁棒的线性回归方法确定概率斜率A93为0.7654,概率轴截距B93为0.0106,线性回归相关系数的平方R2=0.9931。
图8示出了斜率A以及轴截距和存储关系的关系图,图中以存储时间t为横坐标,以在各个存储时间分别确定的斜率A以及轴截距B分别作为纵坐标,将各个数据点用平滑的线相连,并且借助鲁棒的回归估算方法得到模拟的回归曲线。
图9示出了校准系数A与B之间的关系,图中以斜率A为横坐标以及轴截距B为纵坐标,将每个存储时间下确定的A与B一一对应获得数据点,并且借助鲁棒的估算方法得到A与B之间近线性的关系。
图10示出了根据本发明的一种具体实施方式的用于校准经方法一处理的待测样本中的分析物的测量值的系统400的示例框图。
具体实施方式
在下面的详细描述中,参考了构成其一部分的附图。在附图中,类似的符号通常表示类似的组成部分,除非上下文另有说明。详细描述、附图和权利要求书中描述的示例性实施方式并非旨在限定。在不偏离本申请的主题的精神或范围的情况下,可以采用其他实施方式,并且可以做出其他变化。可以理解,可以对本文中一般性描述的、在附图中图解说明的本申请内容的各个方面进行多种不同构成的配置、替换、组合、设计,而所有这些都明确地构成本申请内容的一部分。
在下文中,为了对具体实施例进行清楚的描述,将采用一些特定的术语。然而采用这些术语的本意并非限制本申请的保护范围,这些术语的范围应该扩展至 任何以大致相同的手段达到大致相同的目的的等同替换。
首先参考图1和图2来具体说明根据本发明中所提供的确定应用于待校准测量系统的校准系数的方法的具体实施方式。
图1示出了根据本发明的一种具体实施方式的用于确定应用于待校准测量系统的校准系数的方法100的示例性流程图,所述方法100包括以下步骤:获取N1个校准用样本对(101),其中每个校准用样本对包括方法一样本以及方法二样本,且所述每个校准用样本对中的方法一样本和方法二样本是基于同一来源的样本;将所述N1个校准用样本对存储时间T1(102);对每个所述存储时间T1后的方法一样本MT1以及相应的方法二样本ST1中的分析物的含量进行检测,其中N1个所述方法一样本中的分析物的测量值分别为Y1,T1,Y2,T1…YN1,T1,并且对应的N1个所述方法二样本中的分析物的测量值分别为X1,T1,X2,T1…XN1,T1,N1为大于等于2的整数(103);以及通过对上述测量值Y1,T1,Y2,T1…YN1,T1以及X1,T1,X2,T1…XN1,T1进行数据处理,确定反映在存储时间T1时方法一样本与方法二样本中的分析物的测量值之间映射关系的校准方程的校准系数(104)。
在本申请中使用的术语“校准用样本对”涉及基于同一来源但经不同方法处理的一对用于确定待校准测量系统的校准系数的样本,其包括方法一样本以及方法二样本。
在本申请中涉及的“样本”可以是本领域技术人员公知的能够用于医学检验的任意类型的样本。在某些实施方式中,所述样本可以是体液样本,包括但不限于,血液、尿液、唾液、脓液、痰液、精液、胸膜积水、羊水等。在某些具体的实施方式中,所述样本为血液。而本申请中涉及的对样本的不同处理方法也可以包括任何本领域技术人员公知的处理方法,例如:对于血液的肝素抗凝、冷藏处理、离心分离血清、抗体孵育、点样干燥以获得干血斑片等,或者对于尿液的冷藏处理、离心分离、过滤、抗体孵育、点样干燥以获得干尿斑片等。
本申请中述及的“存储时间T”是指以取样的时间点为0,至测量发生时样本经历的时间。在某些具体的实施方式中,由于取样后对样本进行的不同处理需要一定时间,从而导致了即使经处理后的样本即刻进行了分析物的测量,该样本此刻的存储时间T0仍大于0,但本领域技术人员应当理解这种样本实际上是“未经 存储”的。在一些实施方式中,上述T0的值在不超过48小时、不超过24小时、0-24小时、0-12小时、0-6小时、0-3小时、0-2小时、0-1小时、或者0-0.5小时的范围内。
本申请中涉及的术语“分析物”是指本领域技术人员公知的可以在医学检验中被检测的任意物质,包括但不限于,蛋白、核酸、细胞、化合物、金属、重金属、离子等。在某些实施方式中,分析物可以是蛋白,其包括糖化血红蛋白、丙氨酸氨基转移酶、天冬氨酸氨基转移酶、碱性磷酸酶、r-谷氨酰转移酶、胆碱酯酶、谷氨酸脱氢酶、异柠檬酸脱氢酶、亮氨酸氨基肽酶、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇、肌酸激酶、肌酸激酶同工酶、乳酸脱氢酶、a-羟丁酸脱氢酶、补体C3、补体C4、免疫球蛋白A、免疫球蛋白M、免疫球蛋白G、抗链球菌溶血素、类风湿因子、前白蛋白、a-L-岩藻糖苷酶、转铁蛋白、脂蛋白a、尿微量白蛋白、5’核苷酸酶、载脂蛋白B、β2-微球蛋白、载脂蛋白A、糖化血红蛋白、腺苷脱氨酶、C-反应蛋白、胱抑素C、总蛋白、白蛋白、淀粉酶中的至少一种。在某些特定的实施方式中,分析物是糖化血红蛋白。分析物的“含量”通常指分析物的质量百分比、体积百分比、数量百分比、质量或数量等。“测量值”通常指在医学检验中通过仪器测量获得的信号在经过某种内置的数据处理或者程序转化后得到的分析物的含量的测定值。
以下将以分析物为糖化血红蛋白为例进行举例说明方法100。
在步骤101中,获取来源于同一供体的N1个校准用血液样品对,其中的方法一样本是干血斑片样本,而其相对应的方法二样本则是与上述方法一样本来源于同一供体的新鲜采集的静脉血样本。
在步骤102中,将N1个校准用样本对存储时间T1。本申请中的“存储时间”可以是任意长的时间。在一些实施方式中存储时间在0-3年范围内。在一些实施方式中存储时间在0-180天范围内。在某些特定的实施方式中,存储时间在0-240小时范围内。就新鲜采集的静脉血样本来说,本领域技术人员可以根据需要测定的分析物的稳定性、静脉血样本是否经过抗凝处理、使用的抗凝剂种类以及存储环境条件等来选取适当的存储时间范围,例如:针对在4℃环境下存储的经肝素抗凝的静脉血样本,当其中分析物为糖化血红蛋白时存储时间可以在0-240小时 的范围内,优选地在0-120小时的范围内。就干血斑片样本来说,本领域技术人员也可以根据需要测定的分析物的稳定性以及存储环境条件等来选取适当的存储时间范围,例如:针对在室温环境下存储的干血斑片,当其中分析物为糖化血红蛋白时存储时间可以在0-240小时的范围内,优选地在0-120小时的范围内,而当存储的环境变为-80℃超低温存储时,存储时间可以在0-180天范围内。
在步骤103中,对每个所述存储时间T1后的方法一样本MT1以及相应的方法二样本ST1中的分析物的含量进行检测,假设N1=5,5个所述存储时间T1后的方法一样本MT1中的分析物的测量值分别为Y1,T1,Y2,T1,Y3,T1,Y4,T1,Y5,T1,并且对应的5个存储时间T1后的方法二样本ST1中的分析物的测量值分别为X1,T1,X2,T1,X3,T1,X4,T1,X5,T1。在某些实施方式中,每个所述方法二中的分析物的测量值是随存储时间变化的。在另一些实施方式中,每个所述方法二样本中的分析物的测量值是基本不随存储时间变化的。在一些实施方式中,上述测量值X1,T1,X2,T1,X3,T1,X4,T1,X5,T1是对应的5个标准样本经存储时间T1后所测得的。在另一些实施方式中,方法二样本中的分析物的测量值是基本不随存储时间变化而变化的,因此所述测量值X1,T1,X2,T1,X3,T1,X4,T1,X5,T1可以是对应的5个方法二样本未经存储所测得的。
在步骤104中,通过对上述测量值Y1,T1,Y2,T1,Y3,T1,Y4,T1,Y5,T1以及X1,T1,X2,T1,X3,T1,X4,T1,X5,T1进行数据处理,确定反映在存储时间T1时方法一样本与方法二样本中的分析物的测量值之间映射关系的校准方程的校准系数。具体地,确定校准系数的步骤104包括以测量值X1,T1,X2,T1,X3,T1,X4,T1,X5,T1中的每一个为横坐标和以测量值Y1,T1,Y2,T1,Y3,T1,Y4,T1,Y5,T1中的与之相应的一个为纵坐标获得5(N1)个校准点,用平滑的曲线将各个校准点相连,基本估计反映待测样本与标准样本中的分析物的测量值之间映射关系的校准方程的种类。常用的校准方程可以是任意形式的方程,包括但不限于,线性方程、指数方程、对数方程、抛物线方程等。H.Passing和W.Bablok发表在Journal of Clinical Chemistry Clinical Biochemistry,Vol.21,1983,709-720页上的文章“A New Biometrical Procedure for Testing the Equality of Measurements from Two Different Analytical Methods:Application of linear regression procedures for method comparison studies in Clinical Chemistry,part I”中详细地描述了线性回归的方法在临床化学的方法比较研究中 的使用。在本申请的一些实施方式中,反映在存储时间T1时方法一样本与方法二样本中的分析物的测量值之间映射关系的校准方程为线性方程,因此相应的待确定的校准系数包括斜率AT1和轴截距BT1。对于线性方程校准系数的确定,可以通过在上述获得的校准点中任选两个校准点定义一条直线,即确定该直线的斜率AT1和轴截距BT1。在N1个校准点的情况下,可以得到N1*(N1-1)/2个可能的斜率,即当N1=5时可以得到10个可能的斜率。在此可以考虑所有的校准点,从而确定校准点之间的所有可能的斜率。但是替换地,也可以在所述校准方法中忽略可能的斜率中的一个或多个斜率,从而确定少于所有可能斜率的最大数量个的斜率。但是在任何情况下都应当确定校准点之间的至少两个可能斜率,优选至少三个可能斜率,和特别优选地多于三个可能斜率。由通过上述方式确定的在校准点之间的多个可能的斜率,借助至少一种鲁棒的估计方法确定校准直线的斜率的至少一个估计量,该斜率称为概率斜率AT1。之后通过上述5个校准点确定多条(最多5条)具有概率斜率AT1的直线,确定每条所述具有概率斜率AT1的直线的轴截距,并且借助至少一个鲁棒的估计方法,由多个轴截距确定概率轴截距BT1。本申请所述的鲁棒的估计方法是指在出现异常值或分布假设仅近似有效的情况下也仍提供稳定的统计估计量的统计估计方法。在一些实施方式中,本申请所用的鲁棒的估计方法是鲁棒的回归估计方法。鲁棒的估计方法的一种实施方式可以是,首先对获得的系列数字(例如:上文中确定的多个可能的斜率或多个可能的轴截距)取中值,而后根据所述中值对随机参量的预期值的概率分布进行估计。通常来说,中值的选取应当使得所述系列数字中的至少一半小于或等于该中值并且所述系列数字中的至少一半大于或等于中值。具体地,中值的选取可以通过将所有获得的可能的斜率(假设为m个)按照其数值大小排列为集合{A1,A2,...Am}中,当m为奇数时,通常可以选择上述集合中的A(m+1)/2作为中值,而当m为偶数时,中值则可以为上述集合中各数值的算术平均值。本领域技术人员应当理解,中值的选取可以是基于剔除了异常值的系列数字集合的,例如:当将上述m个可能的斜率按照其数值大小排列为集合时,若A1或者Am明显偏离集合中其他数值较大程度时,将该偏离的数值剔除之后再选取中值。替换地或附加于生成中值的鲁棒的估计方法,原则上还可以采用其它鲁棒的估计方法,尤其是基于一个或多个置换算法和/或一个或多个分类算法的其它鲁棒的估计方 法和/或其它类型的鲁棒的估计方法。也可以采用多个不同的鲁棒的估计方法的组合。
在一些实施方式中,步骤104进一步包括:执行似然性观察,其中在似然性观察时丢弃不现实的校准点和/或不现实的斜率和/或不现实的轴截距。在本申请中所述的似然性观察是一种统计学上估计分布概率的方法,其可以通过本领域技术人员公知的任意方法实施。在本申请的一些实施方式中,所述似然性观察可以通过迭代地用校准点/斜率/轴截距的多个子集合来实施。举例来说,对于每个校准点CN,可以以所有除其以外的校准点为子集合,根据子集合中的校准点确定概率斜率及概率轴截距,检查该校准点CN对概率斜率或概率轴截距是否产生影响。将那些对于根据其余的校准点所确定的概率斜率或概率轴截距具有超出预定偏移影响的,或者处于根据其余的校准点所预期的分布图或值域之外的校准点被称为具有“异常值”或者“不现实”的校准点。在本申请的另一些实施方式中,上述似然性观察可以通过如上文描述鲁棒的估计方法时涉及的中值确定的方法实施。
图2示出了根据本发明的另一种具体实施方式的用于确定应用于待校准测量系统的校准系数的方法200的示例性流程图。图1所示的方法公开了对于存储时间T1,计算其相应的校准方程的校准系数AT1和BT1的具体步骤,而方法200则公开了对于不同的时间存储时间Ti,计算其相应的校准方程的校准系数ATi和BTi,并基于所计算的Z组ATi和BTi,确定ATi和BTi的时间回归曲线,从而确定回归方程A(t)以及B(t),具体如下文所述。
所述方法200包括以下步骤:获取N1个校准用样本对(201);将所述N1个校准用样本对存储时间T1(202);对每个所述存储时间T1后的方法一样本MT1以及相应的方法二样本ST1中的分析物的含量进行检测(203);以及通过对上述测量值进行数据处理,确定反映在存储时间T1时方法一样本与方法二样本中的分析物的测量值之间映射关系的校准方程的校准系数(204);。获取Ni个校准用样本对(201i);将其存储时间Ti,其中所述Ti不等于T1(202i);对每个所述存储时间Ti后的方法一样本MTi以及相应的方法二样本STi中的分析物的含量进行检测(203i);以及通过对上述测量值进行数据处理,确定反映在存储时间Ti时方法一样本与方法二样本中的分析物的测量值之间映射关系的校准 方程的校准系数(204i);获取Z组校准系数,并且确定上述校准系数随时间变化的回归方程(205)。
其中方法200中的步骤201、201i对应于方法100中的步骤101;步骤202、202i对应于步骤102;步骤203、203i对应于步骤103;步骤204、204i对应于步骤104;具体操作细节参见方法100中对相应的步骤的描述。并且步骤201中的N1个校准用样本对与步骤201i中的Ni个校准用样本对可以是相同的,也可以是不同的;步骤201-204及步骤201i-204i可以是同时进行的,也可以是先后进行的;但存储时间Ti不等于T1。在本申请的一些实施方式中,反映在存储时间T1或Ti时方法一样本与方法二样本中的分析物的测量值之间映射关系的校准方程为线性方程,因此相应的待确定的校准系数包括斜率和轴截距,即步骤201-204中确定的校准系数为AT1和BT1,而步骤201i-204i中确定的校准系数为ATi和BTi。
在步骤205中,获取Z组校准系数,并且确定上述校准系数随时间变化的回归方程。以校准方程为线性方程为例,步骤205具体包括获取Z对斜率{AT1…ATi…ATz}及轴截距{BT1…BTi…BTz},其中所述Z为大于等于2的整数;并且基于斜率随时间变化的回归曲线确定所述斜率随时间变化的回归方程A(t);以及基于所述轴截距随时间变化的回归曲线确定所述轴截距随存储时间变化的回归方程B(t)。例如,以存储时间为横坐标,斜率和轴截距分别作为纵坐标,获得Z个数据点,用平滑的曲线将各个数据点相连,基本估计斜率或轴截距随存储时间变化的回归方程的种类,其中所述回归方程可以是任意形式的方程,包括但不限于,线性方程、指数方程、对数方程、抛物线方程等。类似地,在本申请的一些实施方式中,校准系数A及B随时间t变化的方程可以均为指数方程、均为对数方程、或者一个为指数方程另一个为对数方程。
在某些实施方式中,所述方程A(t)和B(t)均为指数方程。在某些实施方式中,所述校准方程为:y=A(t)*x+B(t)。在某些实施方式中,可以借助至少一个鲁棒的估计方法确定校准系数A及B随时间t变化的指数方程。本领域技术人员应当理解,根据不同的样本处理方式、不同的存储环境条件(例如不同的存储温度或湿度等)上述校准系数A及B随时间t变化的方程可能是不同类型的,或者同是指数方程但各相关参数、系数等是不同的。在某些特定的实施例中上述估计方 法包括:首先借助上述各数据点相连后所得到曲线的趋势(例如:校准系数随存储时间的增加而升高或降低的趋势,存储时间及校准系数各自的取值极限等)确定所述方程中应当包含的各种参数,并且建立包含上述各种未知参数的方程,而后通过将至少三个数据点(包括但不限于,所述方程中指数趋向于0时的数据点以及所述方程中指数趋向于负无穷时的数据点等)代入上述方程中推导出所述指数方程的各参数的估计方式。在某些实施方式中,样本在取样并且经处理后即刻进行了分析物的测量(即未经存储),此时存储时间为T0,根据测量值x和y获得的斜率A及轴截距B分别为A1和B1。同时应当理解,为了保证样本中的分析物能够被有效检测出,针对不同的待测量分析物的性质、样本的处理方法、存储环境等因素,经处理的样本的最大存储时间T∞实际上是受限制的,例如:在0-3年范围内、0-180天范围内或0-120小时范围内等。对经最大存储时间T∞的经处理的样本进行测量,获得A2和B2。据此设定所述指数方程的指数系数为负,此时所述指数方程中A与B的值随时间增长最终分别无限接近A2和B2。
以分析物为糖化血红蛋白、待测样品为经干燥处理的存储在室温环境下的干血斑片、标准样本为经肝素抗凝的4℃环境下存储的静脉血样为例,设指数方程的底数为自然常数e(其值约为2.71828)。由于干血斑片在指尖采血后通常需要经室温条件下1-2小时的干燥处理,即T0为1-2小时。在本申请的某些实施方式中T0为2小时,获得斜率A1及轴截距B1。同时,由于若需在上述静脉血样中有效的检测出糖化血红蛋白,样本的存储时间T∞一般不能超过120-240小时,否则检测结果将失去其可靠性,即本申请的某些实施方式中T∞在120-240小时之间,获得斜率A2及轴截距B2。另外通过实验得到至少一个存储时间介于T0与T∞之间的数据点,并根据各数据点相连后所得到曲线的趋势建立包含各种未知参数的方程,例如设,其中g、i、k、j均为未知参数,当将t=T0=2小时、A=A1;t=T∞=120-240小时、A=A2;以及t趋向于正无穷时、A=A2这三个数据点分布代入上述含有未知参数g、i、k、j的指数方程,可以推导出i=T0,在此处i=2,并且j=A2,g=(A1-A2),即由此得到斜率A随时间t变化的指数方程为:虽然根据上述数据点不能推出k值,但是可以根 据上述的至少一个存储时间介于T1与T2之间的数据点进一步对k值进行推导。在本申请的一些具体实施方式中得到的A1的范围为0.5-5.0,优选地为0.85-0.90,A2的范围为0.5-5.0,优选地为0.65-0.80,A的范围为0.5-5.0,优选地为0.65-0.90。同理,设B(t)=o*e-p(t-r)+q,其中o、p、r、q均为未知参数,当将t=T0=2小时、B=B1;t=T∞=120-240小时、B=B2;以及t趋向于正无穷时、B=B2这三个数据点分布代入上述含有未知参数o、p、r、q的指数方程,可以推导出r=T0,在此处r=2,并且q=B2,g=(B1-B2),即由此得到轴截距B随时间t变化的指数方程为:由于B值随着时间的增长而升高,即B1-B2为负值,为了方便理解,将上述方程转换为B(t)=(B2-B1)(1-e-p(t-2))+B1。在本申请的一些具体实施方式中得到的B1大于等于0,优选地为0.0040-0.0050,B2大于等于0,优选地为0.0085-0.0170,B大于等于0,优选地为0.0040-0.0101。
并且,需要注意的是,T∞的值随着所述测量值y的不同而具有不同的值。T∞可以等于也可以不等于存储时间值。具体而言,随着测量值y(例如实施例中的干血纸片DBS的HbA1c测量值)的不同,T∞可以具有不同的最大值Tmax。如果实际存储时间<=Tmax,T∞=实际存储时间;但是如果实际存储时间〉Tmax,T∞=Tmax。以下为示例性的对于干血纸片的HbA1c测量值的Tmax的值。
当HbA1c值<=5.5%时,Tmax=30小时;而当5.5%<HbA1c值<=6.5%时,Tmax=60小时;而当HbA1c>6.5%时,Tmax=200小时。在某些实施方式中,方法200还进一步包括步骤206:根据校准系数随时间变化的方程,获得对应任意存储时间Tβ的校准系数的值,代入校准方程中从而根据在存储时间为Tβ时所述方法一样本中的分析物的测量值YNj,Tβ推得与其对应的所述方法二样本中的分析物的测量值XNj,Tβ。以校准方程为线性方程为例,根据所述回归方程A(t)和所述回归方程B(t),对于任意存储时间Tβ,获得ATβ及BTβ的值;将所述ATβ及BTβ的值代入所述校准方程y=A(t)*x+B(t)中,从而根据在存储时间为Tβ时所述方法一样本中的分析物的测量值YNj,Tβ推得与其对应的所述方法二样本中的分析物的测量值XNj,Tβ。
以下将参考图3来具体说明根据本发明中所提供的用于校准待测样本中的分析物的测量值的方法的具体实施方式。
图3示出了根据本发明的一种具体实施方式的用于校准经方法一处理的待测样本中的分析物的测量值的方法300的示例性流程图,所述方法300包括以下步骤:确定经方法一处理并且存储时间t后所得的待测样本中的分析物的测量值y(301);确定与存储时间t相对应的校准方程的校准系数(302),其中所述校准系数随着存储时间t的不同而变化;以及,基于校准方程将分析物的测量值y换算为与所述待测样本同一来源的经方法二处理的样本中将检测到的所述分析物的含量值x(303)。其中步骤301与步骤302可以同时或任意先后地进行,两者的顺序并不对方法300的实施产生任何影响。
在步骤302中,确定与存储时间t相对应的校准方程的校准系数的详细方法和步骤可以参照上文中对方法100及方法200的详细描述。
在步骤303中,通过将在步骤302中确定的与存储时间t相对应的校准方程的校准系数代入所述校准方程中,并且将步骤301中的存储时间t的实际值以及待测样本中分析物的测量值y的值代入上述校准方程中,得到一个x的一元一次方程,从而可以反推出x的值。在一些实施方式中,方法二样本中的分析物的测量值x是基本不随存储时间变化而变化的,因此x又被称为标准测量值。
例如,在某些实施方式中,所述方法一为干血收集法,而方法二则为测量新鲜全血收集法,所以所述待测样本为干血样本,而与待测样本同一来源的经方法二处理的样本为与所述待测样本同一来源的全血样本,通过对干血样本所对应的测量值利用与所述存储时间t相对应的校准方程进行换算,从而得到全血样本中的分析物的含量值,从而有利于借鉴标准测量方法的指标来评价分析物含量,从而实现考虑时间因素的两个方法学间的校准。
并且,上述方法可以通过如图10的系统来实现:如图10所示,根据本发明的一种具体实施方式的用于校准经方法一处理的待测样本中的分析物的测量值的系统400包括样本收集器410,其用于采集并储存待测样本;检测设备420,其用于对所述待测样本中的分析物的含量进行检测,以确定测量值y,其中所述待测样本是经方法一处理后存储了时间t后所得到的;以及校准装置430,其用于确定与所述存储时间t相对应的校准方程的校准系数,其中所述校准系数随着存储时间t的不同而变化,并用于基于所述校准方程,将所述分析物的测量值y 换算为其所对应的经方法二处理的样本中的分析物的测量值x,其中,所述测量值x代表与所述待测样本同一来源的经方法二处理的样本中将检测到的所述分析物的含量值。
在某些实施方式中,所述样本收集器410为干血斑片,所述待测样本即为干血样本,所述方法一为干血样本的采集和处理。对于待采血的人群来说,通过使用包括干血基质的样本收集器410,比如干血纸片、干血高分子塑料片、干血海绵以及干血棉等,方便人群自己采血,无需到医药采血,节省了时间和精力,而且只需要少量的指尖血量,也便于收集大量样本。而且血液样品即干血样本的运输也非常便捷,为病人和实验室节省了成本。而所述方法二为测量新鲜全血收集法,而与待测样本同一来源的经方法二处理的样本为与所述待测样本同一来源的全血样本。
并且在某些实施方式中,所述检测设备420为高效液相色谱仪,其用于检测样本收集器410所收集的待测样本,以确定测量值y。而所述校准装置430则可以是任何形式的数字平台,包括台式计算机、笔记本、便携式掌上电脑、数字平台、计算机集群、网络工作站等。例如,其可以包括:一个或多个输入组件;一个或多个输出组件;一个或多个中央处理器(CPU);以及一个或多个存储组件,所述存储组件在其中存储一个或多个计算机程序、一个或多个操作系统、以及可选的一个或多个数据库。
其中,输入组件使得可以向系统提供数据输入。常用的输入组件包括数据输入接口、网络传输接口,或者其它类型的输入部件。在本申请中,输入组件用于获取由检测设备420所检测的分析物含量值。
并且,输出组件用于向用户提供计算结果,常见的输出组件包括用户图形界面(GUI)、三维显示界面、输出数据接口、网络传输接口,或者其它类型的输出部件等。在本申请中,输出组件用于输出分析物的测量值y所对应的经方法二处理的样本中的分析物的测量值x。
中央处理器(CPU)通常控制系统的整体操作,诸如与显示、数据处理、数据存储、数据通信以及记录操作相关联的操作等。中央处理器(CPU)可以包括一个或多个处理器来执行指令,以完成上述的方法的全部或部分步骤。此外,中 央处理器(CPU)可以包括一个或多个模块,便于处理中央处理器(CPU)和其他组件之间的交互。例如,中央处理器(CPU)可以包括输入/输出模块,以方便输入组件、输出组件和中央处理器(CPU)之间的交互。
存储器可以由任何类型的随机存取存储设备RAM或只读存储设备ROM或者它们的组合实现,如静态随机存取存储器(SRAM)、电可擦除可编程只读存储器(EEPROM)、可擦除可编程只读存储器(EPROM)、可编程只读存储器(PROM)、只读存储器(ROM)、CD-ROM、磁带、软盘和光数据存储设备等。存储器可以被配置为存储各种类型的数据以支持在系统的操作。
其中,本申请的方法可以用例如计算机软件、硬件或者其组合来在计算机可读介质中实现。对于硬件实现而言,这里所述的实施例可以通过专用集成电路(ASIC)、数字信号处理器(DSP)、数字信号处理设备(DSPD)、可编程逻辑器件(PLD)、现场可编程门阵列(FPGA)、处理器、控制器、微控制器、微处理器、设计成执行这里所述功能的其它电子单元或者其选择性组合内的一个或多个来实现。
对于软件实现而言,这里所述的实施例可以用单独的软件模块,诸如过程模块和功能模块来实现,其每一个都执行一个或多个这里所述的功能和操作。软件代码可以用任何适当的编程语言编写的软件应用来实现,并且可以存储在专用的计算机系统的存储器或者其他计算机可读介质中,并且由计算机系统的处理器来执行,也可以安装在具备数据存储和处理功能的其他电子设备中,如平板电脑、服务器等。
在一些实施方式中,可以通过校准装置430实现:确定与所述存储时间t相对应的校准方程的校准系数,其中所述校准系数随着存储时间t的不同而变化,并用于基于所述校准方程,将所述分析物的测量值y换算为其所对应的经方法二处理的样本中的分析物的测量值x,其中,所述测量值x代表与所述待测样本同一来源的经方法二处理的样本中将检测到的所述分析物的含量值。
并且,在其他实施例中,校准装置430还可以为包含于检测设备420中的一个内置单元。例如,所述校准装置430则可以为包含于检测设备420中的一个内置中央处理器、微处理器、单片机等。
综上所述,利用系统400,通过对干血样本所对应的测量值利用与所述存储 时间t相对应的校准方程进行换算,从而得到全血样本中的分析物的含量值,从而有利于借鉴标准测量方法的指标来评价分析物含量,从而实现考虑时间因素的两个方法学间的校准。
以下将通过实验例具体描述本发明。
实验例
通过下述非限制性实验例进一步描述本发明。需要说明的是举出这些实验例只是用于进一步说明本发明的技术特征,并非旨在也不能够被解释为对本发明的限制。所述实验例不包含本领域一般技术人员所公知的传统方法的详细描述。
以下实施例中,通用的分析物为糖化血红蛋白,其测量值反映糖化血红蛋白占总血红蛋白的数量百分比。
在现有的临床实验室中,对于糖尿病等的检测所使用的标准方法是基于全血(例如新鲜的静脉血)的糖化血红蛋白实验。对于基于全血的糖化血红蛋白实验,可以使用多种分析仪器和方法,比如使用美国伯乐公司Varriant II高效液相色谱仪(Bio-Rad Variant II),或者使用另一种HPLC仪器(比如日本东商HLC-723G8),或使用免疫比浊仪(比如罗氏自动生化分析仪)等等。在这些分析仪中,美国伯乐公司Varriant II高效液相色谱仪是金标准仪器,因为它被用于糖尿病控制和并发试验(DCCT)项目中,该项目设定了糖化血红蛋白的临床诊断标准。美国伯乐公司Varriant II高效液相色谱仪也被美国国家糖化血红蛋白标准化计划(NGSP)认证。本发明使用的仪器是美国伯乐公司Varriant II高效液相色谱仪,其基于HPLC技术,可用于精确检测糖化血红蛋白,高效液相色谱仪的操作流程是糖化血红蛋白HbA1c检测试剂盒(HPLC法)说明书(VRIANTTM II Hemoglobin A1c program)中的标准操作流程。
以下基于糖化血红蛋白含量检测的实施例中,待校准样本对中的待测样本为干血斑片样本,待校准样本对中的标准样本为静脉采集的全血样本。
实施例1:
样本的采集及制备
对照实验的采血方法:对于每一位受试者采集新鲜的静脉血液样品,将其血液样品分成两份,第一份是全血血液,存储在含有抗凝剂的采血管中置于4℃冷藏备用,用于测定基于全血样本的糖化血红蛋白含量;第二份涂布在样本收集器例如一系列的干血纸片上,进一步室温干燥约1个小时,得到存储在干血纸片上的干血样本,用于测定基于干血样本的糖化血红蛋白含量。
样本中糖化血红蛋白的检测
对于在全血样本中进行糖化血红蛋白检测前的样本处理步骤采用HbA1c检测试剂盒(HPLC法)说明书(VRIANTTM II Hemoglobin A1c program)中的标准操作流程进行。
对于在干血样本中进行糖化血红蛋白检测前的样本处理主要包括如下步骤:1)取出干血纸片,用3毫米打孔仪(GE Micro-Punch WB100038)与打孔垫(GE打孔垫)在干血纸片上打孔,得到直径3毫米的干血样本。尽可能在左侧的样品圆圈处打两个孔(忽略样品五个样品圆圈中最左侧的样品圆圈),并将得到的两个圆纸片置于试管中。必要时,可用酒精试纸擦拭3毫米打孔仪的打孔机头。2)将得到的圆形干血样本放入试管后,用瑞宁移液器和枪头(Rainin XLS+LTS)将1.3毫升的0.01%NaN3水溶液作为溶血试剂加入每个试管中,以得到干血样本和溶血试剂的混合液。所述干血样本面积和所述溶血试剂体积的比例是1mm2:92ul。3)将试管置于大龙旋转混匀仪(Dragonlab MX-RL-Pro)上,在室温下以每分钟30转的转速旋转30分钟,充分混合干血样本和溶血试剂,完成检测前样本处理,其中经处理的样本可以在没有去除干血样本的情况下直接进行后续检测。
对于经过处理后的全血样本及经过处理后的干血纸片样本,之后均可使用美国伯乐公司Varriant II高效液相色谱仪(Bio-Rad Variant II)根据是糖化血红蛋白检测试剂盒(HPLC法)说明书(VRIANTTM II Hemoglobin A1c program)中的操作流程进行糖化血红蛋白含量的检测。对于N个校准用样本对来说,将每个成对的方法一样本(干血样本)以及方法二样本(全血样本)交替上样检测,以保证在每对校准用样本的检测中维持最小的由于仪器状态、环境因素、上样时间等引起的误差。
实施例2
采用实施例1中所述的样本采集、处理及对糖化血红蛋白进行检测的方法,其中校准用样本对的数量为62对。样本采集后经处理并且进行检测前的样本处理后,开始检测,此时距离取样大约在1.5小时-2小时之间。考虑到由于样本量较大(共124个样本)上样时间也延续较长,各个样本从取样到检测相距的时间平均值大约为2小时,即T0为2小时。
如图4所示,以干血样本(DBS)中HbA1c的测量值为横坐标,以全血样本(WB)中HbA1c的测量值为纵坐标,获得62个校准点,借助鲁棒的线性回归方法确定概率斜率A为0.8713,概率轴截距B为0.0052,线性回归相关系数的平方R2=0.9923。
实施例3
先根据实施例1中所述的方法采集全血样本,两天后对全血样本来源一致的受试者对应获取干血样本、处理及对糖化血红蛋白进行检测的方法,其中校准用样本对的数量为62对。干血样本在被采集后经处理干燥并且进行检测前的样本处理后,开始检测,此时与干血样本的取样点相距大约1.5小时-2小时之间。同样考虑到由于样本量较大(共124个样本)上样时间也延续较长,各个干血样本从取样到检测相距的时间平均值大约为2小时,即T0为2小时。而与其相对应的全血样本距离其相应的取样时间已经历了大约两天时间。
如图5所示,以干血样本(DBS)中HbA1c的测量值为横坐标,以全血样本(WB)中HbA1c的测量值为纵坐标,获得62个校准点,借助鲁棒的线性回归方法确定概率斜率A为0.8788,概率轴截距B为0.0053,线性回归相关系数的平方R2=0.9951。
比较实施例2与实施例3中获得的斜率A及轴截距B,发现两者并未发生明显变化。由此可以推断,全血样本中糖化血红蛋白的测量值x相对稳定,基本不随时间发生改变,其对于反映上述两种经不同处理方法的血液样本中糖化血红蛋白的测量值之间映射关系的校准方程中的校准系数基本不产生随时间改变的影响。
实施例4
采用实施例1中所述的样本采集、处理及对糖化血红蛋白进行检测的方法,其中校准用样本对的数量为62对。样本采集后经处理并且取出部分进行检测前的样本处理后,开始检测,此时距离取样大约在1.5小时-2小时之间。考虑到由于样本量较大(共124个样本)上样时间也延续较长,各个样本从取样到检测相距的时间平均值大约为2小时,即T0为2小时。之后剩余的样本被分别保存在4℃(全血样本)或者封装后保存在室温下(干血样本),经约18小时及37小时后分别取出所有样本的部分进行检测前的处理并开始检测,考虑到样本的处理及平均上样时间的因素,上述的两个数据采集点t分别记为19小时和38小时。
图6示出了在3个不同的存储时间(分别为T0=2小时(图6a),T2=19小时(图6b),T3=38小时(图6c))的条件下DBS样本中HbA1c的测量值y与WB样本中HbA1c的测量值x的关系。其中以相同存储时间条件下获得的DBS样本中HbA1c的测量值为横坐标,WB样本中HbA1c的测量值为纵坐标,相对应每个存储时间均获得62个校准点。在图6a中借助鲁棒的线性回归方法确定概率斜率A2为0.8699,概率轴截距B2为0.0058,线性回归相关系数的平方R2=0.996。在图6b中借助鲁棒的线性回归方法确定概率斜率A19为0.8191,概率轴截距B19为0.0075,线性回归相关系数的平方R2=0.9956。在图6c中借助鲁棒的线性回归方法确定概率斜率A38为0.8109,概率轴截距B38为0.0079,线性回归相关系数的平方R2=0.9956。
由此可见干血样本的存储时间对于斜率A及轴截距B均有影响,A与B的值随存储时间的增加分别减少和增加。为了进一步验证这个发现,以下进一步验证了更长的存储时间对斜率A及轴截距B的影响。
实施例5
采用实施例4中所述的样本采集、处理、存储及对糖化血红蛋白进行检测的方法,其中校准用样本对的数量增加至72对,各数据点的采集时间则分别为2小时、70小时和93小时。
图7示出了在3个不同的存储时间(分别为T0=2小时(图7a),T2=70小时(图7b),T3=93小时(图7c))的条件下DBS样本中HbA1c的测量值y与WB样本中HbA1c的测量值x的关系。以相同存储时间条件下获得的DBS样 本中HbA1c的测量值为横坐标,WB(全血)样本中HbA1c的测量值为纵坐标,相对应每个存储时间均获得72个校准点。在图7a中借助鲁棒的线性回归方法确定概率斜率A2为0.917,概率轴截距B2为0.0031,线性回归相关系数的平方R2=0.9969。在图7b中借助鲁棒的线性回归方法确定概率斜率A70为0.7812,概率轴截距B70为0.0096,线性回归相关系数的平方R2=0.994。在图7c中借助鲁棒的线性回归方法确定概率斜率A93为0.7654,概率轴截距B93为0.0106,线性回归相关系数的平方R2=0.9931。
该实施例的结果进一步证明了干血样本的存储时间对于斜率A及轴截距B具有影响,且A与B的值在较长的存储时间条件下与2小时存储时间条件下或的相应值相比分别减少和增加。但同时该实施例的结果也发现了在70小时后,A与B的值都趋于稳定,70小时与93小时确定的A与B的值均变化不大。
实施例6
采用实施例1中所述的样本采集、处理及对糖化血红蛋白进行检测的方法,其中校准用样本对的数量为59对。为了确定斜率A及轴截距B分别随时间t变化的方程,将该14对校准用样本对分别存储10个不同的存储时间:T0=2小时,T1=29小时,T2=46小时,T3=70小时,T4=93小时,T5=117小时,T6=144小时,T7=169小时,T8=190小时,T9=217小时。获得不同存储时间条件下校准用样本对中分析物测量值x和y的数据。
如实施例3中所述全血样本中糖化血红蛋白的测量值x相对稳定,基本不随时间发生改变。并且在本实验中也再次证明全血样本中糖化血红蛋白测量值x在不同的存储时间0-215小时范围内基本不随时间变化而变化(数据未显示),因此本实验中x值为不同存储时间下各全血样本中糖化血红蛋白测量值的平均值,且该平均值基本等于T0时全血样本中的糖化血红蛋白测量值。由此可以推断,对于针对全血样本和干血样本的方法学测量值校准来说,全血样本并不必须存储与干血样本相同的存储时间之后再对其中的糖化血红蛋白进行测量,代入校准方程的Ti存储时间条件下的x或者根据Ti存储时间条件下的y由校准方程推出的Ti存储时间条件下的x的值可以等同于T0下的测量值x。
根据不同存储时间条件下校准用样本对中分析物测量值x和y的数据,按照如实施例2-实施例5中所述的数据处理方法,获得10组不同存储时间条件下的校准方程,从而确定10组不同存储时间下的校准系数A与B。
表1:不同存储时间条件下获得的校准系数A与B的值
根据表1中所列的数据,如图8A及图8B所示,分别以存储时间t为横坐标,以在各个存储时间条件下确定的斜率A以及轴截距B的值作为纵坐标,获得两组数据点,根据数据点的连线确定反映斜率A以及轴截距B和存储时间t关系的方程的类型,之后设定参数并代入数据点确定方程A(t)和方程B(t)。此处,根据图8A及图8B所示的模拟趋势线,判定方程A(t)和方程B(t)均为指数方程,并且根据数据点的代入得到斜率A随时间t变化的指数方程为:A(t)=(A1-A2)轴截距B随时间t变化的指数方程为:B(t)=(B2-B1)(1-e-p(t-2))+B1。此处A1为t=T0时获得的A值,A2为t=T9时获得的A值;B1为t=T0时获得的B值,B2为t=T9时获得的B值。根据上述确定的方程A(t)和方程B(t),相应的校准方程为y=A(t)*x+B(t),当将前文所述的每个样本对中基本不变的x值代入,则可推出各存储时间条件下,y的相应值。而实际操作中,在不方便获取病人的全血样本的情况下,根据干血样本中的糖化血红蛋白测量值y,该样本的存储时间t,也可以从上述校准方程中推出其对应的全血样本中糖化血红蛋白的测量值x。另外,以不同存储时间条件下获得的A值与相应的B值分别为x、y轴,获得不同存储时间条件下斜率A与相应的轴截距B之间的关系,由图9中所示可以看出,斜率A与其相应的轴截距B之间具有负相关的线性关系。
上述示意图仅仅为了示例的目的而示出的,并非是对本发明的限制。在一些情况下,可以根据需要添加或者减少其中的一些模块或装置。
应当注意,尽管在上文详细描述中提及了检测设备的若干装置或子装置,但是这种划分仅仅是示例性的而并非强制性的。实际上,根据本发明的实验例,上 文描述的两个或更多装置的特征和功能可以在一个装置中具体化。反之,上文描述的一个装置的特征和功能可以进一步划分为由多个装置来具体化。
那些本技术领域的一般技术人员可以通过研究说明书、公开的内容及附图和所附的权利要求书,理解和实施对披露的实施方式的其他改变。在权利要求中,措词“包括”不排除其他的元素和步骤,并且措辞“一”、“一个”不排除复数。在发明的实际应用中,一个零件可能执行权利要求中所引用的多个技术特征的功能。权利要求中的任何附图标记不应理解为对权利要求的范围的限制。
- 还没有人留言评论。精彩留言会获得点赞!