一种肺癌诊断模型的构建方法与流程
本发明涉及分子生物学分析及可视化仪器研制领域。更具体地,涉及一种肺癌诊断模型的构建方法。
背景技术:
质谱成像是一种新的分子成像技术,它可获得分子在组织切片中的空间分布,相比现有技术,它不需要特异性的标记,通过一次成像扫描分析,可以获得上百种不同分子的分布图。通过多分析物分布图与组织病理或临床信息相互关联,使得质谱成像技术有望成为一种理想的组织病理检查方法。如maldi-msi成像技术可以对多肽、蛋白质、糖类、脂质等化合物进行检测,其检测限在atto摩尔水平的范围内。maldi-msi的质谱成像的空间分辨率通常约为50-200μm。虽然低至几个微米的分辨率的成像也可以实现,但质谱检测需要依赖更高灵敏度的质谱分析器。desi-msi是一种常压敞开式质谱成像技术,不需要在高真空和封闭条件下进行试验,样品前处理简单,因此在组织样本的成像分析研究中得到迅速发展。desi更适用于研究小分子代谢物在生物组织中的空间分布,对于生物组织中脂类化合物的成像效果很好,但对于低丰度和低分子量的内源性代谢物的成像分析却鲜有报道。尽管近些年关于内源性代谢物的质谱成像研究日益受到重视,报道逐年增多,但在所能检测的分子种类的范围、检测灵敏度和成像质量等方面尚存在诸多问题需要解决。目前临床上用于肺癌诊断的检查手段主要有ct、pet-ct、支气管镜检查、脱落细胞学检查、组织穿刺活检等,但是存在费用较高,穿刺活检成功率不高,病情随访时间内必须接受多次大剂量射线辐射的劣势,诊断准确率和敏感性也有待提高,且不能判断肿瘤预后,因而探索与肺癌诊断、治疗效果随访、预后相关的标记物显得尤为必要。
技术实现要素:
本发明的目的在于提供一种肺癌诊断模型的构建方法,能够更快捷、更灵敏、更特异地筛查肺癌,进而更有效地指导肺癌治疗。
为达到上述目的,本发明采用下述技术方案:
一种肺癌诊断模型的构建方法,包括以下步骤:(1)获取3组组织标本切片,(2)利用afai-ms获得3组肺癌组织标本切片的代谢脂质分子分布图,寻找组内不同组织的脂质分子表达差异,建立快速区分癌与正常组织的肺癌快速诊断模型、肺癌分子病理诊断模型和肺癌基因诊断模型;其中,3组组织标本切片包括1)肺癌组织、正常组织、癌旁组织,2)腺癌组织、鳞癌组织、小细胞癌组织,3)egfr基因突变与egfr野生型肺癌组织。
本发明的有益效果如下:
基于afai-msi技术的构建肺癌诊断模型的方法具有以下优势:
1)无需特异性标记,能对已知目标和未知内源性代谢物进行成像分析;
2)灵敏度高,对各类代谢物的检测覆盖范围宽;
3)基于多代谢物相图的直观方式,可客观呈现组织的各种生理、病理状态和类型;
4)可提供丰富的生物化学信息,可为生物医药、分子生物学等方面的研究从代谢物水平提供新的视角;
5)成像速度快,1cm2的组织切片成像可在半小时内完成
附图说明
下面结合附图对本发明的具体实施方式作进一步详细的说明。
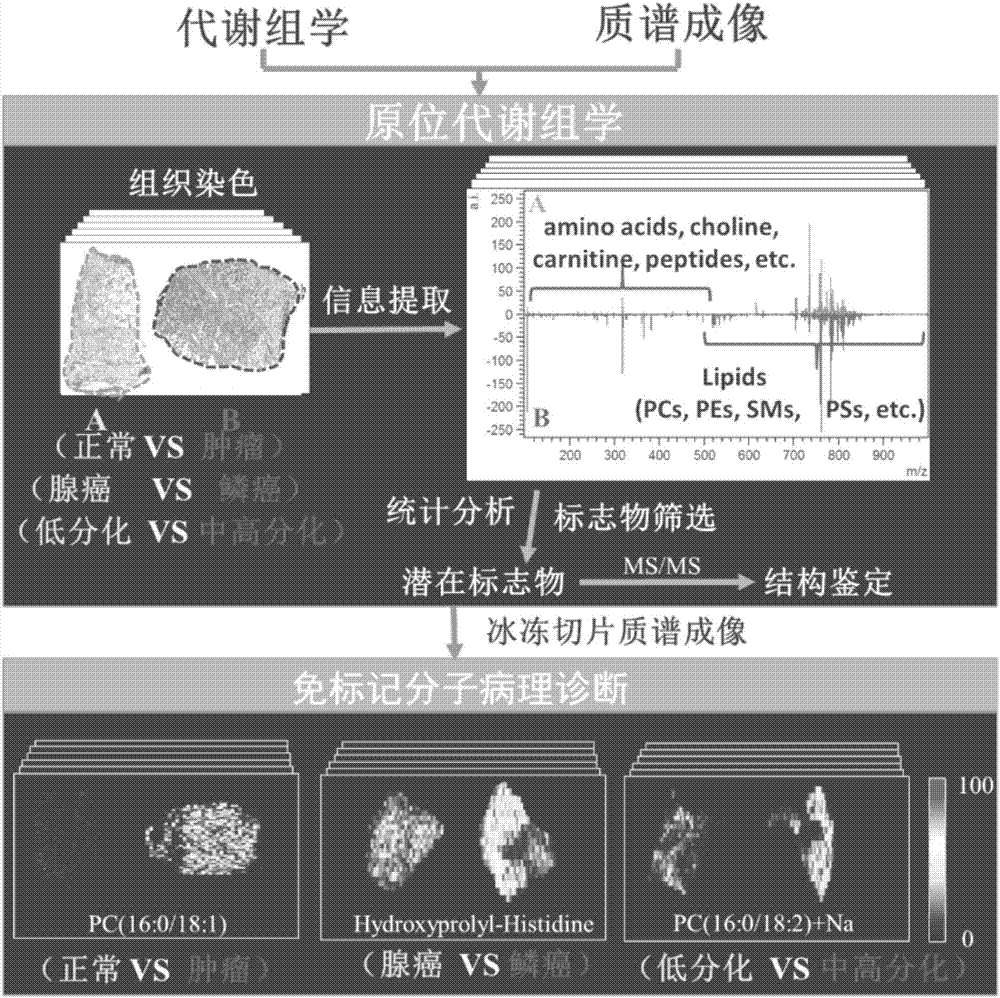
图1示出afai-msi生物组织成像分析原理。
图2示出afai生物组织成像分析步骤图。
图3示出代表性肺癌组织与正常组织提取的质谱峰。
图4示出肺癌快速诊断模型、肺癌分子病理诊断模型和肺癌基因诊断模型。
图5示出(a)肺正常组织和(b)肺癌组织的afai-ms图像。
图6示出(a)腺癌组织和(b)鳞癌组织的afai-ms图像。
图7示出egfr(wild)和egfr(mut)的afai-ms图像。
具体实施方式
为了更清楚地说明本发明,下面结合优选实施例和附图对本发明做进一步的说明。附图中相似的部件以相同的附图标记进行表示。本领域技术人员应当理解,下面所具体描述的内容是说明性的而非限制性的,不应以此限制本发明的保护范围。
1、样品及试剂
(1)组织样本:人体术后肺癌组织切片按临床规范及伦理要求收集。
(2)试剂:甲醇、乙腈、异丙醇(ipa)和甲酸(hplc级,购自德国merck公司)、纯净水(购于杭州娃哈哈集团有限公司)。
2、实验仪器与装置
(1)实验仪器
自制的afai-msi成像系统平台;超高压液相色谱仪(dionexultimate3000,thermofisher)配有高压二元梯度泵。q-orbitrap(qexactive,thermofisher)质谱仪,配备自制的afai离子源。数据采集和分析采用xcalibur3.0数据系统和自制的质谱成像控制软件,成像数据分析采用自制的质谱成像数据处理软件。
(2)afai-msi成像技术平台
自制的空气动力辅助离子化(afai)离子源,主要由以下部分组成:喷雾系统由电喷雾毛细管(od150μm,id100μm)、雾化气管路、喷雾液流路组成,并安装于多维手动精密调节装置上;不锈钢离子传输管(od4mm,id3mm)、与商用质谱仪分析器的接口、真空泵管路和抽气泵(0~60l/min,本单位真空抽气系统或me4nt,vacuumbrand公司)。气体流量计采用玻璃转子流量计(0~45l/min,lzb-10wb,天津流量仪表有限公司),接于抽气泵和afai离子源出口。两路高压电源(-10000~10000v可调,东文高压)分别施加在喷雾毛细管和离子传输管上。
质谱成像控制平台:自组装的3d(x、y、z)样品移动台,精度控制在微米量级,三维样品台分别由步进平移台sc100和步进电机控制器组装而成(北光世纪光学仪器厂,北京,中国),xyz三维电动平移台控制箱(mts225,北光世纪光学仪器厂)、电喷雾喷嘴(od150μm,id100μm)、4d(x、y、z、旋转)精密手动喷雾系统调节装置。自制的afai与q-orbitrap质谱接口,自制的数据采集自动同步装置。
(3)afai-msi平台相关参数及数据采集条件
实验过程中,设置好q-orbitrap质谱仪及afai离子源的基本参数,冷冻保存的组织切片经真空干燥后,直接进行质谱成像分析。组织切片的质谱成像数据的采集采用逐行扫描方式。采用自编的质谱成像数据处理软件(massimager1.0)进行质谱成像数据处理和分析,在“质谱图像生成参数”项下设置成像离子的质量数,精确到小数点第4位。“质荷比容差”设置为0.005da,“强度归一化值”设置为“全局图像”或某一数值大小;“图像质量”设置为中,“预设色彩图”点选为“光谱”。在色彩图坐标上将0值设为黑色。在eic通道前的复选框中选中某一离子,在图像窗口中显示该离子的成像图。
实施例1肺癌诊断模型的构建
1、获取组织标本切片
经手术切除新鲜冰冻的3组组织标本,包括:1)肺癌组织、正常组织、癌旁组织,2)腺癌组织、鳞癌组织、小细胞癌组织,3)egfr基因突变与egfr野生型肺癌组织。
制备3组组织标本的切片,使其厚度为8um,用h&e染色。
2、组织切片的afai-msi(原理如图1所示)扫描及数据处理
在配备有定制的afai离子源的qexactive混合四极orbitrap质谱仪(thermofisherscientific,usa)上进行3组组织标本的切片的afai-msi分析,在正离子和负离子模式中获得数据。在正离子扫描模式中,通过将甲醇和水(8:2,v/v)与0.1%甲酸混合,而甲醇:水(8:2,v/v)用作负离子扫描模式中的喷雾溶剂。溶剂流速为5μl/min,萃取流量为45l/min。所有数据采集都使用xcalibur2.3软件进行操作。质谱数据记录在m/z100-1000的质量范围内。喷射电压为±8.5kv,管电压为±3.0kv。毛细管温度设定在450℃。orbitrap的分辨率设置为70000。
将样本分为训练和验证集进行统计分析,按2:1比例随机分配样本。对所有组织样品进行afai-msi分析(具体步骤如图2所示)。基于肺癌组织相应h&e染色光学图像,分别多次多处提取感兴趣区域(roi)中肺癌组织及相邻癌旁组织、腺癌及鳞癌、egfr基因突变与egfr野生型肺癌组织的质谱数据。然后将多个提取的roi区域的矩阵数据文件导入markerview1.2.1软件(absciex)进行背景扣除,峰值采集和峰值对齐后,然后对处理后的数据导入simca-p12.0软件(umetricsab,
通过以上方法获得能建立快速区分癌与正常组织的肺癌快速诊断模型、肺癌分子诊断模型和肺癌基因诊断模型(见图4),其中癌与正常组织的肺癌快速诊断模型的差异的m/z为760.6、246.9和329.3(见图5),腺癌和鳞癌的差异的m/z为282.1、276.1和637.6(见图6),egfr基因突变与egfr野生型肺癌组织的差异的m/z为307.3、732.6和746.6(见图7)。
显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定,对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动,这里无法对所有的实施方式予以穷举,凡是属于本发明的技术方案所引伸出的显而易见的变化或变动仍处于本发明的保护范围之列。
- 还没有人留言评论。精彩留言会获得点赞!