一种他达那非及其类似物的乳胶微球免疫检测试剂盒及其制备和应用
本发明涉及食品药品安全检测
技术领域:
,具体地,涉及一种他达那非及其类似物的乳胶微球免疫检测试剂盒及其制备和应用。
背景技术:
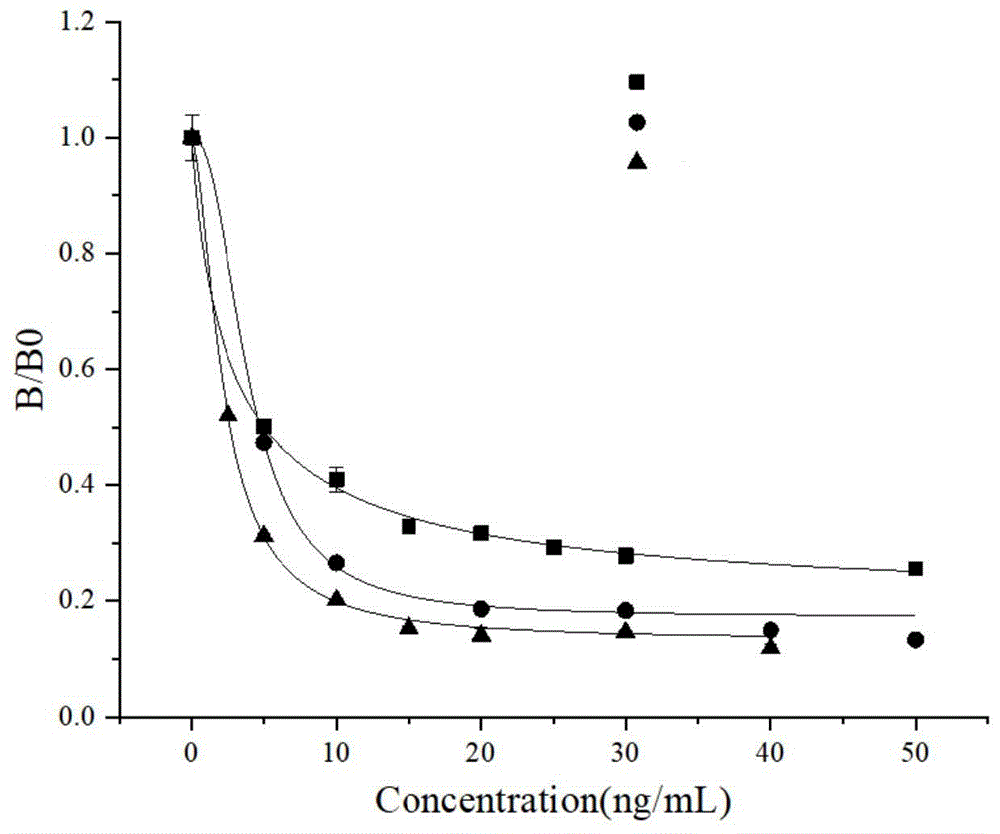
:他达那非,又名西力士,最早由icos礼来公司研发,因其与体内环pb鸟苷(cgmp)的结构相似,能有效抑制体内cgmp的特异性水解酶—5型pb二酯酶的(pde5)的活性,减少cgmp的降解,增强阴茎勃起,可达到治疗男性阴茎勃起功能障碍(ed)的作用。因此,2003年11月经美国fda批准,他达那非成为西地那非和伐地那非之后的第三种用于治疗男性勃起功能障碍(ed)的处方药,目前已在中国、美国、欧洲等100多个国家上市。目前,国内外针对他达那非及其类似物的检测方法有多种,包括含高效液相色谱(hplc)、液相色谱-质谱法(lc-ms/ms)在内的仪器分析方法、光谱法、免疫分析法、电化学方法等等。仪器方法灵敏度高,特异性强,但需要昂贵的设备、专业的操作人员和繁琐的样品前处理,不适合大量样本的快速筛查;而免疫分析方法以其快速简单、成本低、灵敏度高、适合在实际生产中现场监控及大规模样本筛查等优势,在食品中药物残留检测领域发展迅速。其中,免疫检测法目前应用最广泛的包括有酶联免疫检测法(elisa)以及免疫层析法(lfias)等。免疫层析法是将免疫和色谱层析技术相结合的检测方法,以标记物标记的抗体与目标待测物特异性结合为基础并通过标记物信号实现定性或定量的目的。该方法检测时间短,使用方便,前处理简单,且不需要专业培训过的人员即可简单的操作,成本低、携带十分方便,检测效果能满足需求,适合用于食品样品的现场检测。现有针对他达那非及其类似物在食品样品中残留的免疫层析检测方法主要为胶体金、荧光微球免疫层析法,同时大多数只针对见检测单一对象,检测限较高,并且前处理步骤较复杂。比如专利cn110133259a公开了一种他达那非及其类似物的胶体金微孔法检测试剂盒,其对他达那非的最低检测限为0.2ng/ml,而且样品的前处理步骤复杂,检测时间较长。目前,针对他达那非类药物具有多样性的现状,执法部门非常有必要建立起保健食品中中他达那非类药物残留的免疫层析检测方法,以满足市场的需求。因此,建立一种快速、灵敏、准确、可靠的他达那非及其类似物的多残留免疫层析检测方法,对保健品中他达那非类药物的安全检测和初筛具有重要的意义。技术实现要素:本发明旨在针对现有技术中对他达那非的检测灵敏度不高、检测耗时长的缺陷,提供一种他达那非及其类似物的乳胶微球免疫检测试剂盒及其制备和应用。本发明的乳胶微球免疫检测试剂盒通过优化乳胶微球抗体探针的制备,有效提高其检测实际样品的灵敏度;通过调节样品垫配方以适应不同样品的检测要求,精简样品前处理步骤,一步处理即可完成样品前处理的操作。本发明的首要目的是提供一种他达那非抗体-乳胶微球标记物。本发明的另一目的是提供所述他达那非抗体-乳胶微球标记物在非诊断目的检测他达那非或制备检测他达那非的试剂盒中的应用。本发明的另一目的是提供一种他达那非和/或其类似物的乳胶微球免疫检测试剂盒。本发明的另一目的是提供所述的乳胶微球免疫检测试剂盒在非诊断目的检测他达那非和/或他达那非类似物中的应用。本发明的再一目的是提供一种非诊断目的检测他达那非和/或他达那非类似物的方法。本发明的上述目的是通过以下技术方案给予实现的:一种他达那非抗体-乳胶微球标记物,其特征在于,其制备方法包括如下步骤:s1.对mes缓冲溶液中的乳胶微球进行羧基活化,离心去除上清;所述mes缓冲溶液的ph为6.0~7.4,浓度为0.04~0.06m;s2.重悬步骤s1中的产物,再加入经0.5~1%w/vbsa溶液稀释为0.08~0.10mg/ml的他达那非单克隆抗体溶液进行标记;乳胶微球和他达那非单克隆抗体的用量比为(100~120μg):(8~9.6μg);s3.用15~30%w/vbsa溶液对步骤s2中标记后的溶液进行封闭,封闭时间为30~60min,离心去除上清;s4.重悬步骤s3中的产物,即得到他达那非抗体-乳胶微球标记物。优选地,所述乳胶微球为红色乳胶微球。优选地,步骤s1所述mes缓冲溶液的ph为6.5,浓度为0.05m。优选地,步骤s1中,所述采用edc和nhs对mes缓冲溶液中的乳胶微球进行羧基活化。步骤s1中,红色乳胶微球:edc:nhs的用量比为(100~120μg):(10~12μg):(12~15μg)。更优选地,步骤s1中,红色乳胶微球:edc:nhs的用量比为100μg:10μg:12μg。进一步更优选地,步骤s1中,在1mlph为6.5、0.05m的mes缓冲溶液中加入20μl5mg/ml的红色乳胶微球溶液,配制红色乳胶微球溶液;随后加入20μl0.5mg/ml的edc溶液、24μl0.5mg/ml的nhs溶液;200rpm反应15min,随后在4℃下14000rpm,离心20min。优选地,步骤s2中,用ph为7.5~8.5,浓度为0.01~0.03m的bb缓冲液重悬。更优选地,步骤s2中,用ph为8.0,浓度为0.02m的bb缓冲液重悬。优选地,步骤s2所述bsa溶液的浓度为0.5%w/v。所述bsa溶液为bsa水溶液。优选地,步骤s2所述乳胶微球和他达那非单克隆抗体的用量比为100μg:8μg。优选地,步骤s3所述封闭时间为30min。优选地,步骤s3所述bsa溶液的浓度为20%w/vbsa.优选地,步骤s4中用ph为7.4,浓度为0.02m的pb缓冲液重悬;所述pb缓冲液还含有0.5~1%v/vtween-20、3~5%w/v蔗糖、0.5~1%bsa、0.3~0.5%w/vpvp和0.03~0.05%w/vprocline-300。更优选地,所述pb缓冲液还含有0.5%v/vtween-20、5%w/v蔗糖、0.5%bsa、0.3%w/vpvp和0.03%w/vprocline-300。以上任一所述他达那非抗体-乳胶微球标记物在非诊断目的检测他达那非或制备检测他达那非的试剂盒中的应用,也应在本发明的保护范围之内。本发明还要求保护一种他达那非和/或其类似物的乳胶微球免疫检测试剂盒,其特征在于,包括微孔板和免疫层析试纸条;所述微孔板含有乳胶微球标记探针样品孔,所述乳胶微球标记探针样品孔中含有所述的他达那非抗体-乳胶微球标记物;所述免疫层析试纸条包括样品垫、反应膜、吸水垫和底板;样品垫、反应膜、吸水垫依次相互交错固定在底板上;反应膜上设有平行的质控线和检测线,所述质控线靠近吸水垫端,并包被有羊抗鼠igg,所述检测线靠近样品垫端,并包被有结构如式(ⅱ)所示的他达那非抗原:优选地,所述微孔板为酶标微孔板。优选地,所述乳胶微球标记探针样品孔为酶标孔。优选地,所述结合垫为玻璃纤维膜。优选地,所述反应膜为nc膜。优选地,所述吸水垫为吸水纸,所述底板为pvc底板。优选地,所述样品垫采用样品垫缓冲液浸泡处理,所述样品垫处理缓冲液为含有0.25%~1%v/vtween-20、ph为7.0~8.0的0.01~0.03m的pbs溶液。更优选地,所述样品垫处理缓冲液为含有1%v/vtween-20、ph为7.4的0.02m的pbs溶液。本发明的乳胶微球免疫检测试剂盒在他达那非抗体-乳胶微球标记物和试纸条的制备过程中,通过对活化、标记的ph值、抗体稀释液的选择、抗体用量、封闭时间以及样品垫处理缓冲液的配方进行优化,有效提高乳胶微球与他达那非单克隆抗体的结合效率,影提高标记的乳胶微球抗体探针在试纸条上的释放,通过对特定的样品垫处理缓冲液配方,提高了标记效率和释放,使抗体探针可以有效与包被原或药物发生反应以提高灵敏度,保证效果的同时减少抗体原材料的使用。样品稀释液离子浓度的不同在较大程度上影响着抗体探针与包被原的反应,因此选择合适的离子浓度能够使反应过程中显色更快、并且使其更加灵敏。本发明通过调整样品稀释液浓度、包被原浓度,对层析条件进行优化,可有效减少检测耗时以及增强灵敏度。样品垫处理工艺中,缓冲液的选择可以影响样品液跑样时的ph值及其离子浓度,使液体处于一个合适抗体与药物或包被原反应的条件;表面活性剂的选择很大程度的影响了样品液的流动速度,本发明通过对缓冲溶液的种类、浓度、ph值,表面活性剂浓度的控制,使其可达到对样品液的二次前处理,调节了样品垫配方以适应液体和固体样品的检测要求,可以降低样品液的基质效应,使样品前处理要求相对降低,不必通过更复杂的步骤来降低基质效应,从而减少检测耗时。本发明通过对样品垫工艺进行优化,以适应不同实际样品的检测需求,通过缓冲溶液调整对样品液的ph值起到调节作用,使其处于合适的ph值及离子浓度条件以达到更好的检测效果;并通过一定浓度的表面活性剂,使样品液的检测流动速度在保证检测效果的同时能够使检测过程更加省时。因此,本发明要求保护以上任一所述的乳胶微球免疫检测试剂盒在检测他达那非和/或他达那非类似物中的应用。优选地,所述他达那非类似物包括乙酰氨基他达那非、去甲基他达那非。本发明还要求保护一种非诊断目的检测他达那非和/或他达那非类似物的方法,利用所述的乳胶微球免疫检测试剂盒进行检测:将样品加入到乳胶微球标记探针样品孔中,孵育,再将免疫层析试纸条的样品垫置于乳胶微球样品孔中进行反应,通过t线、c线的显色情况,检测样品中的他达那非和/或其类似物。优选地,所述他达那非类似物包括乙酰氨基他达那非、去甲基他达那非。优选地,样品的前处理方法为:将样品用有机试剂萃取,得到样品检测液,用pb缓冲液稀释后,混匀后备用。更优选地,所述pb缓冲液的浓度为0.2~0.3m,ph为7~7.5。更优选地,所述pb缓冲液的浓度为0.3m,ph为7.4。优选地,所述孵育的温度为20℃~25℃。优选地,所述孵育的时间为3~4min。优选地,所述反应的时间为5~8min。优选地,用吸取经前处理后的样品加入到乳胶微球标记探针样品孔中,孵育3min,再将检测试纸条样品垫端插入乳胶微球标记探针样品孔中,计时6min后将试纸条取出,通过t线、c线显色判断检测结果;并结合胶体金/荧光免疫层析读数仪,进行样品中他达那非和/或其类药物的定性和定量检测结果判定。更优选地,所述检测结果的判定方法如下:(1)定性检测结果的判定方法1)若t线和c线均显红色,两线显色程度相当,则判断为阴性结果,即样品中不含有他达那非和/或其类似物;2)若t线和c线均显红色,但t线显色程度浅于c线,则判断为弱阳性结果,即样品中含有一定量的他达那非和/或其类似物;3)若c线显红色,t线不显色,则判断为强阳性结果,即样品中含有他达那非和/或其类似物;4)若c线不显红色,无论t线显或不显红色,则判断为试纸条失效。(2)定量检测结果的判定方法根据定性检测结果判定为弱阳性或者强阳性结果的吸光度值,绘制标准曲线计算样品中他达那非和/或其类似物的含量。与现有技术相比,本发明具有以下有益效果:本发明公开了一种他达那非及其类似物的乳胶微球免疫检测试剂盒及其制备和应用。本发明的乳胶微球免疫检测试剂盒通过优化他达那非抗体-乳胶微球标记物的制备,有效提高其检测实际样品的灵敏度;通过调节免疫试纸条的样品垫配方以适应液体和固体类样品的检测要求,精简样品前处理步骤,一步处理后即可完成样品前处理操作。本发明的乳胶微球免疫检测试剂盒对他达那非的最低检测限为0.12ng/ml,检测灵敏度高、特异性强、稳定性好且制备方法简单。本发明制备的检测他达那非及其类似物的乳胶微球免疫检测试剂盒具有简便、快速、直观、准确等优点,能够实现对样品的现场快速检测,符合市场需求,对保健食品中他达那非类药物的安全检测和初筛具有重要的意义。附图说明图1是实施例2得到的免疫层析试纸条的剖面示意图;其中,1代表pvc底板,2代表硝酸纤维素膜,3代表样品垫,4代表检测t线,5代表质控c线,6代表吸水垫。图2是免疫检测试剂盒对他达那非的检测cut-off值。图3是免疫检测试剂盒检测实际样品的标准曲线。图4是不同ph的mes缓冲溶液对试纸条检测效果的影响。图5是不同抗体稀释液对试纸条检测效果的影响。图6是不同抗体用量对试纸条检测效果的影响。图7是不同封闭时间对试纸条检测效果的影响。图8是不同样品垫缓冲体系对试纸条样品垫跑样效果的影响。图9是不同浓度的表面活性剂对试纸条样品垫跑样效果的影响。具体实施方式以下结合说明书附图和具体实施例来进一步说明本发明,但实施例并不对本发明做任何形式的限定。除非特别说明,本发明采用的试剂、方法和设备为本
技术领域:
常规试剂、方法和设备。除非特别说明,以下实施例所用试剂和材料均为市购。抗原tada-ova由本实验室自制;他达那非单克隆抗体由本实验室自制;红色乳胶微球溶液于bangs公司购买。实施例1标记有红色乳胶微球的他达那非单克隆抗体的制备1、在1.5ml离心管加入1mlmes溶液(0.05m,ph=6.5),随后加20μl5mg/ml的红色乳胶微球溶液;2、在上述溶液中加入20μl0.5mg/mledc溶液、24μl0.5mg/mlnhs溶液;200rpm反应15min,随后在4℃下14000rpm,离心20min;3、去除上清液,加入1mlbb溶液(0.02m,ph=8.0)后加入100μl经0.5%bsa稀释为0.08mg/ml的他达那非单克隆抗体溶液200rpm反应40min;4、在上述溶液中加入20μl20%bsa溶液,200rpm反应1h,随后在4℃下14000rpm离心20min;5、去除上清液,加入200μl复溶液,即得到标记有红色乳胶微球的他达那非单克隆抗体,4℃保存待用;其中复溶液为0.02mpb溶液(ph=7.4),其中含有0.5%v/vtween-20、5%w/v蔗糖、0.5%bsa、0.3%w/vpvp和0.03%w/vprocline-300。实施例2他达那非及其类似物乳胶微球免疫检测试剂盒的制备1、人工抗原tada-ova及tada-klh的制备(1)在他达那非的原分子结构上延伸出丁酸手臂合成得到tada半抗原,利用活泼酯法将半抗原与载体蛋白ova、klh进行偶联。经活化、偶联、透析后得到免疫原tada-klh与包被原tada-ova。(2)通过紫外分光光度计对载体蛋白、半抗原、人工抗原进行扫描鉴定得到人工抗原tada-klh和tada-ova,其结构式分别如式(ⅰ)和(ⅱ)所示:2、他达那非单克隆抗体的制备(1)动物免疫:将人工抗原tada-klh与佐剂进行乳化后,免疫雌性balb/c小鼠,免疫后三周对小鼠抗血清进行质量评价;(2)抗血清质量评价:采用同源包被的形式,用icelisa方法对抗血清进行效价与抑制率的评价。评价不同抗血清的效价与抑制率,选出抗血清效果好的小鼠准备进行细胞融合实验,在进行细胞融合实验的前三天,往小鼠的腹腔直接注射免疫原进行冲击免疫;(3)细胞融合:对小鼠进行冲击免疫完成三天后,取出小鼠脾脏放入装有基础培养基的培养皿中,冲洗筛选得到脾细胞。将复苏好的骨髓瘤细胞与小鼠的脾细胞一同孵育融合2周后,用elisa检测上清液,选出效价高、抑制率高的阳性孔,借助有限稀释法进行亚克隆实验,直至整版每孔为阳性且效价、抑制相近时,挑单选克隆细胞进行建株。(4)腹水的制备及抗体纯化:提前一周时间,向雌性balb/c小鼠腹腔注射液体石蜡。再向小鼠体内注射筛选出的杂交瘤细胞,注射一周后取出小鼠腹水,离心去除上层脂肪及多余的石蜡,中间呈淡黄色的澄清液体即为腹水。小鼠腹水采用proteing蛋白柱层析方法纯化,经装柱、平衡、清洗、洗脱、冲洗、离心浓缩后得到单克隆抗体。(5)抗体质量及特异性评价:采用同源包被的形式,用icelisa方法对抗体进行效价与抑制率的评价。利用拟合得到的曲线计算出抗体对tada的半抑制浓度。将其他功能结构类似物用缓冲溶液进行梯度稀释,将筛选出的抗体对此类药物进行icelisa检测,拟合出标准曲线得到半抑制浓度,并根据交叉反应率,选择最佳的单克隆抗体。3、他达那非及其类似物乳胶微球免疫检测试剂盒的制备(1)划膜:抗原tada-ova和羊抗鼠igg通过cb溶液(0.02m,ph=9.6)稀释,使抗原tada-ova浓度为0.5mg/ml,羊抗鼠igg浓度为0.175mg/ml,通过喷金划膜仪将抗原tada-ova、羊抗鼠igg划到nc膜上,用量为0.8μl/cm,划好后37℃烘箱干燥过夜,并于阴凉干燥处密封保存备用。(2)样品垫处理:将型号为sb08的玻纤膜浸泡于样品垫处理液中,充分浸泡后取出至垂直放置无液体滴落,并将其水平放置与37℃的烘箱中烘干过夜,并将其密封保存于干燥阴凉处。其中,样品垫处理液配方为1%v/vtween-20、0.5%bsa、0.3%w/vpvp和0.03%w/vprocline-300溶于ph为7.4的0.02mpbs中。(3)试纸条组装:在pvc背板上贴上步骤(1)制备的nc膜,pvc板的一端与样品垫重叠1~2mm相连,另一端与吸水纸重叠1~2mm相连,组装好后用裁条机裁剪成3.05mm,放入干燥剂待用;(4)乳胶微球样品孔的制备:将实施例1制备的标记他达那非单克隆抗体的红色乳胶微球溶液以8μl/孔的用量加入酶标微孔板中的酶标孔中,37℃烘箱干燥30min,密封备用。(5)试纸盒的组装:将划有检测线和质控线的nc膜(2.5cm)、样品垫(1.6cm)、吸水垫(1.8cm)依次衔接在pvc底板上,样品垫与硝酸纤维素膜重叠2mm,吸水垫与硝酸纤维素膜重叠4mm,重叠部位样品垫和吸水垫均在nc膜的上方;用切条机将其切成宽度为3.05mm的试纸条,密封干燥保存;将得到的试纸条与步骤(4)得到的酶标微孔板组装成乳胶微球免疫检测试剂盒。其中,本实施例2的免疫层析试纸条的剖面示意图如图1所示。实施例3乳胶微球免疫检测试剂盒对实际样品的检测以上实施例2得到的乳胶微球免疫检测试剂盒的使用方法包括以下步骤:1、样品前处理(1)液体类样品前处理:量取0.5ml试样于10ml离心管中,加入1.5ml0.3mpb缓冲液,充分混匀,备用;(2)固体类样品前处理:将被测样品碾成粉末状后,准确称取0.5g试样于10ml离心管中,加入2ml甲醇,涡旋30s,4000r/min离心2min或者静置2min;量取1ml上清液后加入1ml0.3mpb缓冲液,充分混匀,备用。2、实际样品的检测用胶头滴管吸取2滴经前处理后的样品加入实施例2制备的乳胶微球样品孔中,孵育3min,再将检测试纸条样品垫端插入乳胶微球样品孔中,计时6min后将试纸条取出,通过t线、c线显色判断检测结果。并结合胶体金/荧光免疫层析读数仪,进行样品中他达那非类药物的定性和定量检测结果判定;其中,所述定性和定量检测的结果判定方法如下:(1)定性检测结果的判定方法1)若t线和c线均显红色,两线显色程度相当,则判断为阴性结果,即样品中不含有他达那非和/或其类似物;2)若t线和c线均显红色,但t线显色程度浅于c线,则判断为弱阳性结果,即样品中含有一定量的他达那非和/或其类似物;3)若c线显红色,t线不显色,则判断为强阳性结果,即样品中含有他达那非和/或其类似物;4)若c线不显红色,无论t线显或不显红色,则判断为试纸条失效。(2)定量检测结果的判定方法根据定性检测结果判定为弱阳性或者强阳性结果的吸光度值,标准曲线计算样品中他达那非类药物的含量。实施例4乳胶微球免疫检测试剂盒的灵敏性和特异性检测1、试剂盒的灵敏性和特异性检测实验采用实施例2制备的乳胶微球免疫检测试剂盒,按实施例3的检测方法对他达那非类药物及其功能类似物(如表1所示)进行检测,利用实施例3中前处理得到的阴性基质溶液对表中的药物进行稀释,分别配制成0、5、10、20、30、40、50ng/ml的标准溶液。2、灵敏性和特异性检测结果本发明实施例2制备得到的免疫检测试剂盒的检测灵敏度、特异性和标准曲线如表1、图2和图3所示;结果表明,该试剂盒对他达那非、去甲基他达那非、乙酰氨基他达那非的检测结果呈阳性,且最低检测限分别为0.12ng/ml、0.62ng/ml、1.66ng/ml;对三者的裸眼消线(cut-off)值分别20ng/ml、50ng/ml、20ng/ml,检测灵敏度高。而且该试剂盒对其他功能类似物西地那非类药物的检测结果均呈阴性。以上结果说明:本发明的免疫检测试剂盒可实现对他达那非类及其类似药物进行多残留免疫分析检测,检测特异性强,灵敏度高,具有简便、快速、直观、准确等优点,能够实现对样品的现场快速检测,符合市场需求,对食品药品中他达那非类药物的安全检测和初筛具有重要的意义。表1.试剂盒的检测灵敏性和特异性结果药物检测结果检测限(ng/ml)他达那非阳性0.12乙酰氨基他达那非阳性1.66去甲基他达那非阳性0.62西地那非阴性-豪莫西地那非阴性-硫代西地那非阴性-硫代豪莫西地那非阴性-去甲基西地那非阴性-巯基西地那非阴性-巯基豪莫西地那非阴性-注:“-”代表未检测到药物。实施例5乳胶微球的最适活化ph值优化实施例1的标记过程中,活化过程中的ph值及时间会影响乳胶微球的结合效率,合适的条件则可以使其与抗体有效结合,因此,本发明对活化的ph值进行优化。1、实验方法分别选择表2所示的不同ph值的mes缓冲溶液,其他步骤均按实施例1~2的方法制备乳胶微球免疫检测试剂盒的免疫层析试纸条,并按实施例3的方法对实际样品进行检测,根据检测得到的显色效果、检测限选择合适ph值的mes溶液。表22、实验结果结果如图4所示,随着mes缓冲液ph值升高,ph值为6.5时阴性样本的t线显色最深且阳性样本抑制完全,但当ph值继续增大时,抑制效果变差。因此在保证显色效果并兼顾灵敏度的情况下,选择ph值为6.5的mes溶液作为活化缓冲液,此条件下阳性样本t线完全消除。实施例6乳胶微球标记抗体稀释液的优化实施例1的标记过程中,抗体稀释液的选择会影响乳胶微球的结合效率,合适的抗体稀释液则可以使其与抗体有效结合,因此,本发明对抗体稀释液的选择进行优化。1、实验方法分别选择表3所示的抗体稀释液,其他步骤均按实施例1~2的方法制备乳胶微球免疫检测试剂盒的免疫层析试纸条,并按实施例3的方法对实际样品进行检测,根据检测得到的显色效果、检测限选择合适的抗体稀释液。表32、实验结果结果如图5所示,选用h2o,bb溶液进行稀释以及抗体原液进行标记时,t线、c线显色较浅,灵敏度比较差;相对而言其他三种稀释液显色均较强,同时使用bsa作为稀释液的灵敏度略好且消线完全;因此选用灵敏度较高的条件,即0.5%bsa为抗体稀释液。实验也充分证明了,适当的稀释抗体可以有效地提高其灵敏度,这一点从原液的结果与其他条件的结果对比就可以明显得出,而适当的抗体稀释液也能起到很好的作用,但不同抗体以及不同标记物情况各有不同。实施例7乳胶微球标记抗体用量的优化实施例1的标记过程中,抗体用量对试纸条的性能也有较大的影响,抗体的用量越多,t线的颜色越深,但当抗体超过一定量时,会使试纸条的灵敏度变差;过多的抗体用量不仅造成抗体浪费,还会引起拖带现象,使得显色过深;过少的抗体用量标记不完全,容易出现假阳性现象。因此,本发明对抗体用量进行优化。1、实验方法用乳胶微球标记分别标记表4所示的不同用量的抗体,其他步骤均按实施例1~2的方法制备乳胶微球免疫检测试剂盒的免疫层析试纸条,并按实施例3的方法对实际样品进行检测,根据检测得到的显色效果、检测限选择合适的抗体用量。表42、实验结果结果如图6所示,将抗体用实施例6优化的条件0.5%bsa稀释100倍后添加不同抗体用量与微球偶联,随着用量的增加,阴性样品的t线逐渐变深;添加体积为8.0μg与9.6μg时,t线显色相近,从节省抗体用量的角度考虑,实验选择抗体用量为8.0μg。实施例8乳胶微球标记抗体过程中封闭时间的优化实施例1的标记过程中,封闭时间不宜太短,如果封闭不完全,会出现非特异性吸附,降低灵敏度;延长封闭时间,虽可以减少非特异性吸附,但是对试纸条灵敏度的提升程度有限,为了合理地控制标记过程的时间。因此,本发明对封闭时间进行了优化。1、实验方法用表5所示的不同封闭时间进行封闭,其他步骤均按实施例1~2的方法制备乳胶微球免疫检测试剂盒的免疫层析试纸条,并按实施例3的方法对实际样品进行检测,根据检测得到的显色效果、检测限选择合适的封闭时间。表52、实验结果结果如图7所示,当封闭时间为30min和60min时,阴性样品t线显色最深,封闭时间为45min时虽然抑制效果最好,但t线显色较浅。可以看到延长封闭时间可以提高抑制效果但不明显,综合考虑灵敏度与节省时间的角度考虑,封闭时间选择30min。实施例9样品垫缓冲体系的优化实施例2的样品垫处理工艺中,样品稀释液离子浓度的不同在较大程度影响着抗体探针与包被原的反应,选择合适的离子浓度能够使反应过程中显色更快、并且使其更加灵敏;缓冲液的选择可以影响样品液跑样时的ph值,使液体处于一个合适于抗体与药物或包被原反应的条件。因此,本发明对样品垫缓冲体系中缓冲溶液的种类、浓度及ph值进行优化,使试纸条能够适应不同实际样品的检测,通过特定的缓冲溶液的调节对样品液的ph值起到调节作用,使其处于合适的ph值及离子浓度条件以达到更好的检测效果。1、实验方法分别采用表6所示的不同种类的缓冲体系、浓度及不同的ph值配制成不同的样品垫处理液配方,其他步骤均按实施例1~2的方法制备乳胶微球免疫检测试剂盒的免疫层析试纸条,并按实施例3的方法对实际样品进行检测,根据实际的检测结果、样品流动速度等确定合适种类、浓度及ph值的缓冲溶液处理样品垫。表62、实验结果结果如图8所示,在实际样品检测中,ph值较高的bb溶液与tris-hcl溶液在跑样过程中会在样品垫与nc膜的连接处有明显的探针滞留,显色效果差且灵敏度低;而含有nacl的pbs溶液相对于pb溶液其t线显色基本相同,但抑制更完全。综合考虑选择0.02mpbs溶液作为样品垫处理缓冲液。实施例10样品垫处理液中表面活性剂优化实施例2的样品垫处理工艺中,样品垫处理液的配方会影响标记的乳胶微球抗体探针在试纸条上的释放,主要通过其表面活性剂与盐离子的含量进行调节,表面活性剂的选择在很大程度上影响了样品液的流动速度。因此,本发明通过对样品垫处理液中的表面活性剂的浓度进行优化,使样品液的检测流动速度在保证检测效果的同时能够有一定的提高,并降低样品液的基质效应,使样品前处理的要求相对降低,不必通过更复杂的步骤降低基质效应,使检测过程更加省时,减少检测耗时。1、实验方法分别采用表7所示的不同体积百分比的tween-20配制成不同的样品垫处理液配方,其他步骤均按实施例1~2的方法制备乳胶微球免疫检测试剂盒的免疫层析试纸条,并按实施例3的方法对实际样品进行检测,根据显色效果、样品液流动速度等确定合适的表面活性剂浓度来配制样品垫处理缓冲液。表72、实验结果结果如图9所示,随着tween-20浓度的逐渐升高,阴性样本的t线显色明显增强。当其浓度较低为0.25%时纸条上有明显的探针滞留,考虑到其他三个浓度的抑制效果接近因此选择浓度为1%tween-20作为样品垫处理液的表面活性剂。表面活性剂的含量变化明显改变了样品液流动的速度,因此检测速度也是本实验的考虑因素之一。最后应当说明的是,以上具体实施方式为便于理解本发明而说明的较佳实施例,但本发明并不局限于上述实施例,即不意味着本发明必须依赖上述实施例才能实施。所属
技术领域:
的技术人员应该明了,对本发明的任何改进,对本发明所选用原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1