一种治疗方法与流程
提交数据
本申请与2014年10月21日提交的题为“治疗方法”的美国临时专利申请no.62/066,808相关并要求其优先权,其全部内容通过引用并入本文。
本公开涉及对人和动物中覆盖背部和末端趾骨的角状包膜(horn-likeenvelopes)、和动物中有关的脑部突出物(cerebralprotrusions)以及人和动物表面含角蛋白的材料的真菌感染的控制。用于控制这些包膜和有关突出物以及含角蛋白的材料的真菌感染的试剂以及天然的和合成的制剂与提取物也包括在本公开中。在一个实施方案中,本公开教导了甲的真菌感染特别是人的甲真菌病的治疗。
背景技术:
本说明书中作者提及的出版物的书目细节在说明书的最后按字母顺序收集。
本说明书中对任何现有技术的提及,不是并且不应被视为承认、或者任何形式的暗示,即在任何国家这种现有技术构成普通常识的一部分。
包括侵染(infestation)的真菌感染可导致人和动物的重大健康问题。
虽然化学杀真菌剂在人和兽医药物中已经得以成功,但是持续使用化学试剂来控制真菌感染存在一系列的环境和监管问题。这些试剂的使用越来越多也为真菌物种抵抗力的出现提供了选择性的压力。显然需要开发替代机制来控制真菌病原体对人和动物的感染。
特别麻烦的疾病是甲真菌病,也称为皮肤癣菌性甲真菌病和甲癣(tineaungium)(rapini等人(2007)dermatology:第2卷组,st.louis:mosby)。这是甲和其他覆盖人和动物中背部和末端趾骨的角状包膜的真菌感染。特别是涉及甲单元中任何成分(包括基质、床或板)的趾甲或指甲的感染。人中的这种疾病并不罕见,但由于感染性的真菌嵌入甲内和甲底,而难以治疗。虽然不会危及生命,但甲真菌病可引起疼痛、不适、毁容,并产生身心伤害。甲真菌病的作用广泛,对生活质量有重大影响。
引起甲真菌病的主要病原体是皮肤癣菌红色毛癣菌(trichophytonrubrum)和须癣毛癣菌(trichophytonmentagrophytes),其中红色毛癣菌占病例的90%(sotiriou等人(2010)actaderm-venereol9(2):216-217)。
甲真菌病的治疗取决于临床亚型,受影响的甲的数目以及甲受累的严重程度。虽然口服药物是最有效的,但有一些阻碍其使用的因素。副作用,包括与全身暴露于大多数口服抗真菌药物相关的肝毒性,使口服药物不受关注。此外,老年人占主要群体,他们患有甲真菌病,并且由于经常使用伴随药物而产生不必要的药物相互作用,这排除了对口服药物的使用。这突出了开发局部疗法来治疗甲真菌病的重要性。大多数治疗涉及局部或者口服抗真菌制剂(westerberg等人(2013)americanfamilyphysician88(11):762-770)。口服药物包括特比萘芬、伊曲康唑和氟康唑(westerberg等人(2013)同上)。这些治疗只能治愈14-38%病例中的感染,并且具有很高的肝损伤风险。局部药物包括环吡酮、克霉唑、阿莫罗芬、依芬康唑、tavaborole和布替那芬。这些治疗方法的治愈率在5%至17%之间,必须每天施用,持续至少48周。这种低治愈率是因为活性成分穿透甲的渗透性很差,以及仅抑制真菌生长而不是杀死真菌细胞的真菌抑制作用模式,从而允许真菌储存池持续并再感染甲。此外,长期治疗方案导致许多患者难以遵守。这些治疗方法并非完全有效,疾病可持续多年。
为了使局部甲真菌病治疗达到感染部位,抗真菌剂必须能够渗透甲。通过几种模型抗真菌药物对人甲板和来自牛蹄的角蛋白膜的渗透研究显示,甲渗透性随着分子量的增加而降低(mertin和lippold(1997)jpharmpharmacol49:866-872;kobayashi等人(2004)eurjpharmsci21:471-477)。测试的每种模型药物的分子量小于1000。这些研究表明,mw>5000的分子将不能渗透甲。
另一麻烦的疾病是毛发和其他含角蛋白的材料的真菌感染,包括毛发和毛发毛囊之间的界面。这种疾病有时被称为头癣或头皮癣。治疗可以是口服药物的形式,包括灰黄霉素、特比萘芬和伊曲康唑。局部治疗包括含有抗真菌剂如酮康唑、环吡酮、吡罗克酮和吡硫锌的洗发剂。头皮和皮肤的真菌感染也可引起皮肤刺激和剥落,导致比如脂溢性皮炎和头皮屑等疾病。含有抗真菌剂的洗发剂可用于治疗由真菌感染引起的头皮屑。
植物防御素是小的(45-54个氨基酸)、具有四至五个二硫键的碱性蛋白质(janssen等人(2003)biochemistry42(27):8214-8222)。它们具有共同的二硫键结构和共同的结构折叠,其中三链的反平行β-折叠片通过三个二硫键附着至α-螺旋,形成半胱氨酸稳定的αβ基序。第四个二硫键还连接n-和c-末端,产生非常稳定的结构。植物防御素可以具有许多生物功能,包括抗菌活性、蛋白质合成抑制、α淀粉酶和蛋白酶抑制,在花的发育和花粉传感和抗真菌活性中发挥作用(colilla等人(1990)febslett270(1-2):191-194;bloch和richardson(1991)febslett279(1):101-104;vanderweerden等人(2013)fungalbiolrev26:121-131)。
防御素的结构由七个“环”组成,定义为半胱氨酸残基之间的区域。环1包括第一个β链(1a)、以及前两个不变半胱氨酸残基之间的连接该β链与α螺旋的大部分柔性区(1b)。环2、3,以及4的开始部分(4a)构成α螺旋,而剩余的环(4b-7)构成β链2和3、以及连接它们的柔性区(β发夹区域)(vanderweerden等人(2013)cellmollifesci70(19):3545-3570]。已知植物防御素的环5对抗真菌活性至关重要,是这些蛋白质作用机制的重要决定因素(sagaram等人,(2011)plosone6.4:e18550)。
植物防御素通常共享八个完全保守的半胱氨酸残基。这些残基通常被称为“不变半胱氨酸残基”,因为它们的存在、位置和连通性在防御素中是保守的。基于序列相似性,植物防御素可以分为不同的组。在每组中,序列同源性相对较高,而组间氨基酸相似性较低(vanderweerden等人(2013)fungalbiolrev26:121-131)。对于相同的生物活性,属于不同组的植物防御素通常具有不同的生物活性或不同的作用机制。例如,属于萝卜肽rsafp2组的植物防御素通过与细胞壁中的鞘脂结合来抑制真菌生长(thevissen等人(2012)molmicrobiol84(1):166-180)。相反,属于烟草(nicotiana)防御素nad1组的植物防御素通过进入真菌细胞并诱导产生导致细胞裂解的活性氧(ros)来抑制真菌生长(hayes等人(2013)antimicrobagentsch57(8)3667-3675)。
植物防御素有两大类。i类防御素由内质网(er)信号序列组成,其中内质网信号序列后为成熟的防御结构域。ii类防御素作为较大的前体而产生,所述前体带有约33个氨基酸的c末端前结构域或前肽(ctpp)。迄今为止鉴定的大多数ii类防御素都发现于茄属(solanaceous)植物的物种。
需要开发更有效地管理人和动物特别是人中甲真菌病的真菌感染的方案,为此,直到本发明发现以前,没有安全有效的治疗可用。虽然一些防御素具有抗真菌性质,但是它们在不同真菌病原体之间的活性显著不同,并且大部分被证明的活性是针对植物真菌病原体的。此外,它们的尺寸(mw>5000da)似乎将限制其在甲中的渗透性。
技术实现要素:
氨基酸序列由序列标识符号(seqidno)表示。seqidno与序列标识符<400>1(seqidno:1)、<400>2(seqidno:2)等数字对应。序列标识符的概要在表1中提供。在权利要求之后提供序列列表。
本公开部分地基于令人惊奇的确定,即不管大小如何,一些防御素能够有效地渗透甲并治疗真菌感染。另外,尽管开发用于靶向植物真菌病原体,一些植物防御素对引起甲真菌病的真菌病原体如红色毛癣菌具有强力的活性,而对哺乳动物细胞没有脱靶活性。更令人惊讶的是,一些植物防御素具有杀真菌作用的模式,使其能够在接触时杀死真菌细胞。因此,本公开教导了一种抑制真菌病原体感染的方法,所述感染在受试者的覆盖背部和末端趾骨的角状包膜、或者有关的脑部突出物、或者受试者上含角蛋白的材料之中或之上,所述方法包括用有效量的植物防御素或其功能性天然或者合成衍生物或变体接触所述包膜或突出物或含角蛋白的材料,所述植物防御素、衍生物或变体具有seqidno:24所示的一致性氨基酸序列。在一个实施方案中,防御素选自hxl008(seqidno:1)、hxl035(seqidno:2)和hxl036(seqidno:3)。本文考虑的其他防御素选自hxl001(seqidno:4)、hxl002(seqidno:5)、hxl003(seqidno:6)、hxl004(seqidno:7)、hxl005(seqidno:8)、hxl009(seqidno:9)、hxl012(seqidno:10)、hxl013(seqidno:11)、hxl015(seqidno:12)、hxl032(seqidno:13)、hxl033(seqidno:14)、hxl034(seqidno:15)、nsd1(seqidno:16)、nsd2(seqidno:17)、nad1(seqidno:18)、nod173(seqidno:19)dmamp1(seqidno:20)、hxp4(seqidno:21);hxp34(seqidno:22)、hxp35(seqidno:23),以及添加有n末端丙氨酸残基的上述任一种(分别为seqidno:25至47),以及最佳比对后与seqidno:1至47中的任一个具有至少约80%的氨基酸序列相似性的植物防御素。防御素通常通过局部应用在足以根除或控制真菌生长的条件下和角状包膜或含角蛋白的材料接触一段时间。包膜包括手指和脚趾的甲以及爪、蹄和角。在一个实施方案中,本公开实现在受试者中治疗甲真菌病或相关疾病的方法,所述方法包括向受试者施用有效量的植物防御素或者其功能性天然或合成衍生物或变体,植物防御素或者变体具有seqidno:24所示的一致性氨基酸序列。在一个实施方案中,防御素选自seqidno:1至3或seqidno:4至47中的任一个或与seqidno:1至47中任一个具有至少约80%相似性的防御素。在一个具体实施方案中,防御素是hxl008(seqidno:1)、hxl035(seqidno:2)或者hxl036(seqidno:3)或其功能性天然或合成变体中的任一个,包括含n末端丙氨酸残基的防御素(分别为seqidno:25至27)。
在另一个实施方案中,含角蛋白的材料是毛发或皮毛。在此实施方案中,本公开实现了一种用于治疗受试者中毛发或皮毛真菌感染的方法,所述方法包括向受试者施用有效量的植物防御素或其功能性天然或合成衍生物或变体,所选的植物防御素或变体具有seqidno:24所示的一致性氨基酸序列。在一个实施方案中,防御素选自seqidno:1至3或seqidno:4至47中任一个或与seqidno:1至47中任一个具有至少约80%相似性的防御素。在一个具体的实施方案中,防御素选自seqidno:1、seqidno:2或seqidno:3或其功能性天然或合成变体,其包括含n末端丙氨酸残基的防御素(分别为seqid25至27)。在另一个实施方案中,含角蛋白的材料是皮肤。在这个实施方案中,本公开实现了一种用于治疗受试者中皮肤真菌感染的方法,所述方法包括向受试者施用有效量的植物防御素或其功能性天然或合成衍生物或变体,所选的植物防御素或变体具有seqidno:24所示的一致性氨基酸序列。在一个实施方案中,防御素选自seqidno:1至3或seqidno:4至47中任一个或与seqidno:1至47中任一个具有至少约80%相似性的防御素。在一个具体的实施方案中,防御素限定为seqidno:1、seqidno:2或seqidno:3或其功能性天然或合成衍生物或变体,其包括含n末端丙氨酸残基的防御素(分别为seqid25至27)。
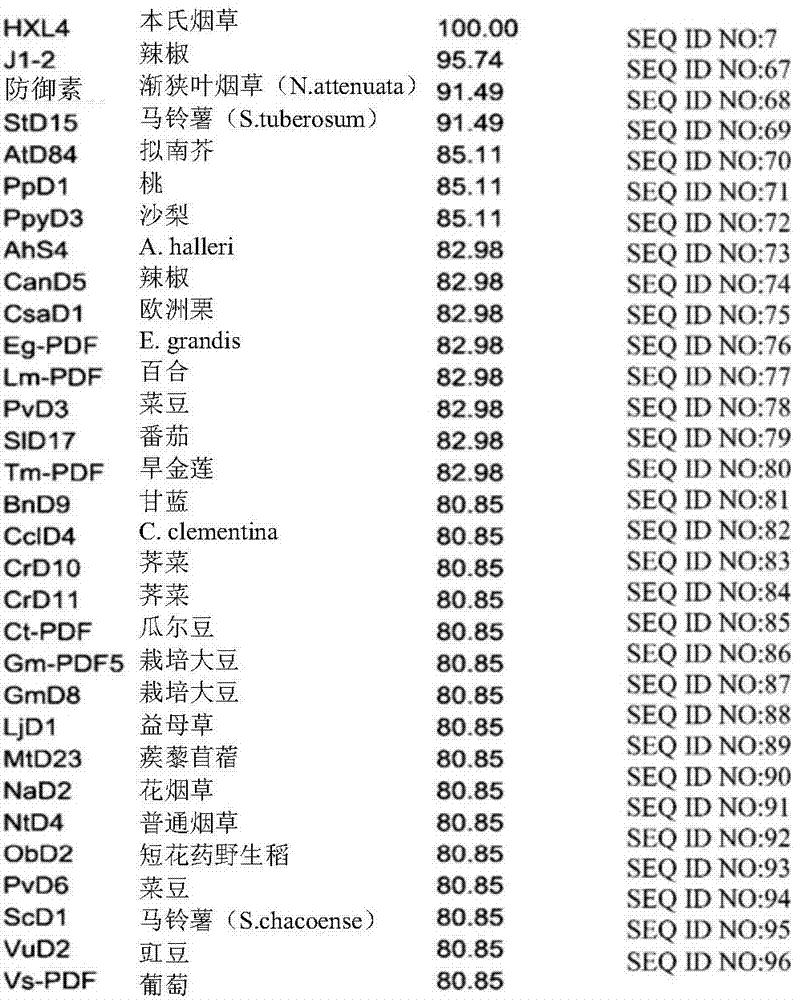
预期用于治疗方案的防御素列于表2中,以及是最佳比对后与表2所列防御素中的任一个具有至少80%相似性的防御素。为了简洁起见,此后提及“seqidno:1至47”包括与seqidno:1至47中的任一个具有至少80%相似性的防御素。在一个实施方案中,防御素是渗透性防御素或者其功能性天然或者合成衍生物或变体。合成变体的实例包括在其中,来自i类防御素的环1b取代来自茄属(solanaceous)ii类防御素的环1b。这些是hxp4、hxp34和hxp35。其他变体或衍生物包括表2中列出的防御素或与表2中列出的防御素具有至少80%相似性,其中防御素在其n末端包含丙氨酸残基(即seqidno:25至47)。在防御素的n末端添加丙氨酸允许在巴斯德毕赤酵母(pichiapastoris)表达系统中重组产生肽,而不需要ste13蛋白酶位点。ste13位点通常允许通过kex2有效地加工α交配因子(matingfactor)分泌信号。然而,在高表达负载下,ste13蛋白酶切割可能是低效的,而导致残留在肽的n末端的glu-ala重复。这些重复赋予的额外负电荷可能对植物防御素的活性不利。可以用丙氨酸取代ste13蛋白酶位点以防止不完全的加工(cabral等人(2003)proteinexprespurif31(1):115-122)。n末端丙氨酸的存在也可以降低防御素裂解血红细胞的能力(wo2011/16074)。
在一个实施方案中,修饰表2中列出的防御素(seqidno:1至47)以增强肽的稳定性。在另一个实施方案中,这是通过以下而实现的,即通过将脱酰胺易感的氨基酸如天冬酰胺和谷氨酰胺、或者将异构化易感的氨基酸如天冬氨酸,取代为对修饰不易感的氨基酸。在一个具体的实施方案中,防御素hxl008、hxl035或者hxl036在位置18、36或42有修饰。
在一个实施方案中,修饰表2中列出的防御素(seqidno:1至47)以增加肽的正电荷。已知正电荷对抗菌肽包括植物防御素的活性很重要(sagaram等人,(2011)plosone6.4:e18550)。在一个实施方案中,通过用中性氨基酸取代带负电荷的残基例如谷氨酸或天冬氨酸来实现正电荷的增加。在一个实施方案中,中性氨基酸是丙氨酸或甘氨酸。在另一个实施方案中,通过用带正电荷的残基如赖氨酸或精氨酸取代中性氨基酸来实现正电荷的增加。
在本文中也考虑保守氨基酸的改变。
在一个实施方案中,治疗包括防御素与非防御素肽、蛋白酶抑制剂、另一种防御素、或者蛋白或非蛋白的(即化学的)杀真菌剂组合。
真菌病原体是指在受试者的手指或者脚趾的甲、爪、蹄或者角中导致甲真菌病或者相关疾病的病原体。
提及“甲”包括覆盖人和动物中背部和末端趾骨的任何角状包膜、以及动物中相关的脑部突出物(即角)。“甲真菌病相关的疾病”是人、非人灵长类动物或者动物中甲的周围角质层中的感染,或者动物中爪、蹄或者角状突出物之中或之上的感染。相关疾病的实例是癣。
真菌病原体包括皮肤癣菌、酵母菌和非皮肤癣菌霉菌。皮肤癣菌包括毛癣菌属(trichophyton)的物种,包括红色毛癣菌(trichophytonrubrum)、须癣毛癣菌(trichophytonmentagrophytes)、指(趾)间毛癣菌(trichophytoninterdigitale)、紫色毛癣菌(trichophytonviolaceum)、断发癣菌(trichophytontonsurans)和苏丹毛癣菌(trichophytonsoudanense)、粉小孢子菌(microsporumfulvum)、絮状表皮癣菌(epidermophytonfloccosum)和石膏样小孢子菌(microsporumgypseum)。酵母包括假丝酵母属(candida)的物种,包括白色念珠菌(candidaalbicans)和光滑念珠菌(candidaglabrata)。
在一个实施方案中,防御素被局部应用于感染区域并穿透甲或者角状结构以在感染部位积聚。惊奇地确定,一些防御素例如但不限于hxl008(seqidno:1)、hxl035(seqidno:2)和hxl036(seqidno:3)具有高程度的甲渗透性,并且是皮肤癣菌病原体和非皮肤癣菌霉菌的强效杀真菌抑制剂,因此使其在治疗比如甲真菌病的疾病方面非常有效。在一个实施方案中,防御素对哺乳动物或细菌细胞没有脱靶作用。对哺乳动物细胞的活性会增加皮肤刺激和其他副作用的可能性。对细菌细胞的活性可能会破坏该区域中天然的有益微生物群落。众所周知,原生的(native)微生物群落在预防真菌感染中起重要作用(reid等人(2011)naturereviewsmicrobiology9:27-38)。
本文进一步教导的是包含植物提取物或酵母提取物(例如,经遗传修饰以产生防御素的毕赤酵母提取物)的制剂或者提取物,其包含选自seqidno:1至47的植物防御素。制剂或者提取物可以进一步包含另一种活性剂或者制剂或者提取物的组合,其中至少一种制剂或者提取物包含本文所限定的防御素,其在使用前进行混合或者以任一顺序依次使用。可以按照例如草药制剂和天然身体或甲的洗涤剂和洗发剂的形式(包括浸液)来使用植物防御素或提取物,其包含本文所限定的植物防御素或提取物。防御素通常配制成以允许穿透到目标部位(例如甲或者皮肤或毛发或皮毛的束(strand))。
本文实现的是,seqidno:1至47限定的植物防御素在制备用于治疗或预防受试者中角状包膜的真菌感染的药物中的用途,所述角状包膜覆盖背部和末端趾骨或相关脑部突出物。本文还教导了,seqidno:1至47限定的植物防御素用于在受试者中治疗或预防覆盖背部和末端趾骨的角状包膜或相关脑部突出物的真菌感染。本文实现的是,seqidno:1至47限定的植物防御素在制备用于治疗或预防受试者上含角蛋白的材料的真菌感染的药物中的用途。本文还教导了seqidno:1至47限定的植物防御素。在一个具体的实施方案中,防御素由一致性序列seqidno:24或其功能性天然或合成变体所限定。实例包括由seqidno:1、seqidno:2和seqidno:3限定的防御素以及包含n末端丙氨酸残基的防御素(分别为seqid25至27)。
在一个实施方案中,真菌感染导致甲真菌病或相关疾病。
一般来说,受治疗的受试者是患有甲真菌病或者患有指甲或趾甲的相关疾病的人。然而,本发明还涉及治疗动物的手指和脚趾的甲、爪、以及适当时角,例如在非人灵长类动物、农场动物和有角的动物中。
本文进一步考虑的是,分离的微生物,其经过工程化以表达本文限定的防御素,其用于制造包含微生物的组合物。微生物的一个实例是毕赤酵母(pichia)。这样的组合物可用于人和动物的治疗。或者,防御素作为包含植物提取物或微生物提取物的细胞提取物而提供。
本文还教导了一种用于治疗真菌感染的分区(compartmental)形式的试剂盒,其包含植物防御素或其功能性天然或合成衍生物或变体,所述植物防御素或变体选自seqidno:1至47。在一个任选的实施方案中,另一个区室(compartment)包含第二活性剂,以及任选在另一区室中单独地、或者和现有区室一起,药学上或者兽医学上可接受的稀释剂、载体或赋形剂。在一个实施方案中,防御素是由seqidno:24所示的一致性氨基酸序列限定的。实例包括hxl008(seqidno:1)、hxl035(seqidno:2)和hxl036(seqidno:3)。
在一个实施方案中,预期用于本文的防御素可以或者可不包括n末端丙氨酸残基。对于一些含有n末端丙氨酸残基的重组防御素而言,尤其如此。本文中“防御素”的定义包括带有n末端丙氨酸的seqidno:1至23中的任一个,即seqidno:25至47。一致性氨基酸序列seqidno:24具有任选的末端丙氨酸残基。
表1
序列标示符汇总
hxl蛋白的氨基酸序列引用于us专利号6,911,577和相关的专利家族成员。
表2
植物防御素的实例
附图说明
图1(a)至(e)是本文包含的各种防御素的氨基酸比对的示意图。
图2(a)至(d)是显示植物防御素nad1(虚线)和hxl008(实线)对红色毛癣菌的四种临床分离株体外生长的影响的照片图示。通过在接种生长介质后72小时获得的595nm处的光密度(a595)的增加来测量真菌生长,并且相对于蛋白的浓度(μg/ml,水平轴)而言,绘制为相对于无蛋白质对照的生长百分比(垂直轴)。
图3(a)至(e)是用100μm的hxl008处理72小时后在琼脂平板上生长的红色毛癣菌存活菌落的照片图示。图板(a)至(d)分别代表临床分离株14-01、14-02、14-03和13-04。存活的菌落用黑色矩形标记。图板(e)代表尚未用hxl008处理的红色毛癣菌的生长。
图4(a)至(c)是每天给予hxl008后的红色毛癣菌存活菌落的示意图。图4a是在1/2沙氏葡萄糖琼脂(sabourauddextroseagar,sda)上经过每天0μg/ml(左图板)、10μg/ml(中图板)或50μg/ml(右图板)hxl008处理后存活的菌落的照片。平板来自处理24小时(上图板)、14d(中图板)或25d(下图板)的培养物。图4b是用hxl008每日处理(50μg/ml/天)之后在100μl培养物中存活的菌落数的照片图示。图4c是在不存在(左)或存在10μg/ml(中间)或50μg/ml(右)hxl008时的培养物的照片。
图5是使用甲的接合系统(adaptersystem)进行的hxl008(黑色三角形,实黑线)、nad1(黑星,实黑线)、hxl004(虚线圈,虚黑线)、hxl012(灰色方形,虚灰线)、tavaborole(黑色菱形,黑色虚线)、环吡酮(虚线方形,实黑线)和依芬康唑(灰色圈,实灰线)对甲的渗透性的示意图,其中用湿的棉签作为甲底的接收溶液(receptorsolution)。
图6是在不同浓度的植物防御素nad1(◆虚线)、hxl004(●虚线)和hxl008(▲虚线)存在时,大肠杆菌(escherichiacoli)生长的示意图。人抗菌肽ll37(■虚线)用作对照。
图7是rnad1、hxp4、hxl001、hxl002、hxl004、hxl005、hxl008、hxl009、hxl012和hxl013(10μm)对人u937细胞的透化(permeabilization)的示意图。通过监测荧光染料碘化丙啶(pi)的摄取来测量透化。
图8是相对于水对照测量的,由hxl008、hxl004和nad1诱导的血红细胞裂解的示意图。
图9是随着时间hxl008在不同制剂中甲渗透性的示意图,水(黑条)、50mm柠檬酸缓冲液ph4.0(条纹条)和50mm柠檬酸缓冲液ph4.0、20%v/v乙醇、0.5mmedta(灰色条)。
图10(a)至(c)是纯化的hxl008+丙氨酸的sds-page、rp-hplc和质谱分析的示意图。图10(a)是纯化的hxl008+丙氨酸的sds-page凝胶。泳道1、2和14是分子量标记(
图11是hxl008、hxl035和hxl036的氨基酸比对、以及通过比对产生的一致性序列的示意图。相同的氨基酸以黑色突出显示。保守的氨基酸以灰色突出显示。
具体实施方式
贯穿本说明书,除非上下文另有要求,词语“包含”或者如“包括”或“含有”之类的变化,将被理解为暗示包含所述元素或整数或方法步骤、或者元素或整数或方法步骤的组,但不排除任何元素或整数或方法步骤、或者元素或整数或方法步骤的组。
如本说明书所使用的,单数形式“一”、“一个”和“该”包括复数的方面,除非上下文另有明确规定。因此,例如,提及“防御素”包括单一的防御素,以及两种或更多的防御素;提及“试剂”包括单一的试剂,以及两个或更多试剂;提及“公开”包括本公开教导的单个和多个方面;等。本文教导的且实现的方面包含在术语“发明”之内。所有这些方面都在本发明范围内实现。所有变体和衍生物或者各方面都包括在本发明的术语“形式”中。
提及“防御素”是指保留抗真菌活性的以下植物防御素之一:
(i)具有seqidno:24所示的一致性氨基酸序列的防御素;
(ii)选自hxl008(seqidno:1)、hxl035(seqidno:2)和hxl036(seqidno:3)的防御素;
(iii)选自hxl001(seqidno:4)、hxl002(seqidno:5)、hxp35(seqidno:3)、hxl003(seqidno:6)、hxl004(seqidno:7)、hxl005(seqidno:8)、hxl009(seqidno:9)、hxl012(seqidno:10)、hxl013(seqidno:11)、hxl015(seqidno:12)、hxl032(seqidno:13)、hxl033(seqidno:14)、hxl034(seqidno:15)、nsd1(seqidno:16)、nsd2(seqidno:17)、nad1(seqidno:18)、nod173(seqidno:19)、dmamp1(seqidno:20)、hxp4(seqidno:21)、hxp34(seqidno:22)和hxp35(seqidno:23)的防御素;
(iv)seqidno:1至47中任一个的功能性天然存在或合成衍生物或变体;
(v)在最佳比对后与seqidno:1至47中任一个具有至少80%相似性的防御素;
(vi)包含n末端丙氨酸残基的seqidno:1至47中的任一个(即,seqidno:25至47);和/或
(vii)与seqidno:1至3中任一个具有或最佳比对后具有至少80%相似性的防御素。为了方便起见,这些防御素包括在seqidno:24所示的一致性氨基酸序列中。
在一个实施方案中,防御素是由seqidno:1、seqidno:2或者seqidno:3限定的,或者是其功能性天然或合成衍生物或变体,其包括具有抗真菌活性的、氨基酸序列在最佳比对后与seqidno:1、seqidno:2或seqidno:3中的任一个具有至少80%相似性的多肽。
当第二防御素与第一防御素组合使用时,第二防御素可以是任何防御素。
本文描述了一种方案,其用于促进真菌感染的管理,包括在人和动物受试者中的特定解剖部位的侵染。该方案包含植物防御素或者其功能性天然或合成衍生物或变体来抑制或控制真菌病原体的生长的用途,其中所述真菌病原体在人和动物中覆盖背部或末端趾骨的角状包膜以及有角动物中相关脑部突出物之上或之中。在一个实施方案中,包膜是手指或者脚趾的甲、爪或者蹄,以及脑部突出物是角。在一个实施方案中,真菌感染导致甲真菌病。在一个实施方案中,防御素对红色毛癣菌具有强的杀真菌活性,对哺乳动物或细菌细胞无活性或者医学上可接受的最小活性。在一个实施方案中,防御素对甲具有良好的渗透性,例如具有seqidno:24所示的一致性氨基酸序列的防御素。实例包括hxl008(seqidno:1)、hxl035(seqidno:2)和hxl036(seqidno:3)或具有n末端丙氨酸残基的这些防御素(分别为seqidno:25、seqidno:26和seqidno:27)。在一个任选的实施方案中,防御素与另一抗真菌剂协同组合使用。后者试剂包括非防御素肽、蛋白酶抑制剂、另一防御素和具有抗真菌性质的蛋白或非蛋白(化学)试剂。该方案还延伸到治疗含角蛋白的材料的真菌感染,如皮肤、毛发和皮毛以及毛发和皮毛毛囊。
本文实现的是一种抑制受试者上真菌病原体感染的方法,所述真菌病原体在覆盖背部或末端趾骨的角状包膜或相关脑部突出物之上或之中,所述方法包括使包膜接触有效量的植物防御素或者其功能性天然或合成衍生物或变体。在一个实施方案中,包膜是甲、爪或者蹄。因此,本文中教导的是一种抑制真菌病原体生长的方法,所述真菌病原体在指甲或趾甲之上或之中、或者在动物的爪或蹄之上,所述方法包括使甲或爪或蹄接触有效量的植物防御素或者其功能性天然或合成变体或衍生物。通常,在足以抑制真菌病原体生长的条件下接触一段时间。
本文教导的是一种用于在受试者上含角蛋白的材料之上或之中抑制真菌病原体感染的方法,所述方法包括使材料接触有效量的植物防御素或其功能性天然或合成衍生物或者变体。在一个实施方案中,含角蛋白的材料是毛发或者皮毛。因此,本文中教导的是一种用于在毛发或皮毛或者毛发或皮毛毛囊之上或之中抑制真菌病原体生长的方法,所述方法包括使毛发或皮毛或者毛发或皮毛毛囊接触有效量的植物防御素或其功能性天然或合成变体或衍生物。通常,在足以抑制真菌病原体生长的条件下接触一段时间。
在一个实施方案中,含角蛋白的材料是皮肤。因此,本文中教导的是一种在皮肤之上或之中抑制真皮病原体生长的方法,该方法包括使皮肤接触有效量的植物防御素或者其功能性天然或合成变体或衍生物。通常,在足以抑制真菌病原体生长的条件下接触一段时间。
“真菌抑制”包括杀真菌和抑制真菌的活性,其是通过与对照相比真菌生长的减少(或活力丧失)而测量的。根据真菌,可以通过本领域已知的许多不同的方法来测量真菌生长。例如,通常使用的测量丝状真菌生长的方法需要在合适的生长介质中萌发孢子、孵育足以实现可测量的生长的时间、以及在指定的孵育时间后测量培养物中光密度的增加。光密度随着生长的增加而增加。通常,真菌生长对于发病机制是必需的。因此,抑制病原体生长提供了保护免受真菌性疾病的适当指标,即抑制越强,保护越有效。此外,杀真菌或抑制真菌活性的有效性可以通过目视检查甲、爪、蹄或角或者毛发或皮毛或者毛发或皮毛毛囊来确定。
对于甲真菌病的成功治疗没有明确的定义。真菌学治愈通常定义为koh和培养测试中都是阴性结果(elewski等人(2012)fungaldiseasesin:bolognia,jorizzo,schaffereds,dermatology第三版,费城,pa;elseviersaunders;第77章)。
治疗方案包括预防(即防止)有风险的受试者免于感染。“有风险”的受试者可能是热带气候的受试者。因此,在本文中“预防感染”是指人或动物宿主用防御素进行治疗,以避免真菌感染或与其相关的疾病症状,或者显示出减少的或者最小化的或者较不频繁的真菌感染或与其相关的疾病症状,与未暴露于防御素的宿主相比,这是宿主-真菌相互作用的天然结果。也就是说,真菌病原体感染得以免于或减少引起疾病和/或相关疾病症状(即甲真菌病)。与没有经过本文所教导的方案治疗的宿主相比,感染和/或症状减少至少约10%、20%、30%、40%、50%、60%、70%或80%或更多。可以通过适合宿主和真菌病原体的任何方便的手段来确定减少百分比。
因此,防御素的作用是抑制真菌病原体的生长、复制、感染和/或维持、以及其他抑制活性和/或诱导真菌感染或侵染症状的改善。
在一个实施方案中,真菌感染导致或者与甲真菌病或相关疾病有关。
因此,本文实现的是在受试者中治疗或者预防甲真菌病或者相关疾病的方法,所述方法包括在足以改善甲真菌病症状的条件下使受试者的感染部位与植物防御素或其功能性天然或合成衍生物或变体接触一段时间。
提及“甲真菌病”包括远端甲下甲真菌病、白色表浅甲真菌病、近端甲下甲真菌病和念珠菌甲真菌病。提及“甲真菌病相关疾病”包括包围甲、爪、蹄或角的角质层组织的癣和感染。
在一个实施方案中,真菌感染是头癣、头皮屑或脂溢性皮炎。
因此,本文实现的是在受试者中治疗或预防头癣、头皮屑、脂溢性皮炎或相关疾病的方法,所述方法包括在足以改善真菌感染症状的条件下使受试者的材料与植物防御素或其功能性天然或合成衍生物或变体接触一段时间。
在一个实施方案中,真菌感染是含角蛋白的材料的感染。
因此,本文实现的是一种用于治疗或预防受试者中含有角蛋白的材料的真菌感染的方法,所述方法包括在足以改善真菌感染症状的条件下使受试者的材料与植物防御素或其功能性天然或合成衍生物或变体接触一段时间。
关于后者的实施方案,含角蛋白的材料包括皮肤、毛发或皮毛,或者是毛发或皮毛毛囊。
因此,本文所教导的是一种用于在人上治疗或预防毛发或皮毛或毛发或皮毛毛囊真菌感染的方法,该方法包括在足以改善真菌感染症状的条件下使受试者上的毛发或皮毛或毛发或皮毛毛囊与植物防御素或其功能性天然或合成衍生物或变体接触一段时间。
“接触”包括局部施用或者应用至人或动物受试者之后,将真菌病原体暴露于防御素。可能接触纯化的植物防御素或含有植物防御素的制剂、或天然含有防御素的植物提取物或经工程化而产生防御素的植物提取物。制剂包括草药制剂和提取物,如甲油(polish)和甲洗涤剂。提取物可以衍生自植物或微生物如酵母(例如毕赤酵母)。因此,防御素被局部应用于人或动物受试者的表面区域。提及“接触”包括向受试者或受试者上感染的部位施用的步骤。
在一个实施方案中,防御素被制剂成局部制剂、甲、爪、蹄或角制剂或者身体或毛发洗涤液。也可以应用包含防御素的微生物或细胞提取物。一个实例是来自毕赤酵母的提取物。局部制剂包括水溶液、液体制剂、溶液、浸液、补剂(tonic)、洗涤剂、喷雾剂、涂层剂、粉末、分散剂、雾化制剂、霜剂、软膏、唇膏、凝胶、泥浆剂(sludge)、糊剂、贴剂、浸渍绷带等。本文还考虑包含防御素的植物提取物,包括含有防御素的植物提取物。通常,防御素被配制成允许渗透进入目标部位(例如,甲、爪、蹄、角或毛发或皮毛颗粒)。在一个实施方案中,根据其渗透性选择防御素。
本文实现的是含有植物防御素或者其功能性天然或合成衍生物或变体的制剂,其用于在人或动物受试者上抑制真菌病原体感染,所述真菌病原体感染在覆盖背部或末端趾骨的角状包膜或者相关脑部突出物之中或之上。
本文进一步实现的是包含植物防御素或者其功能性天然或合成衍生物或变体的制剂,其用于抑制人或动物受试者甲、爪、蹄或角上的真菌病原体感染。
本文进一步实现的是包含植物防御素或者其功能性天然或合成衍生物或变体的制剂,其用于抑制人受试者中与甲真菌病相关的真菌病原体的感染。
本文实现的是包含植物防御素或者其功能性天然或合成衍生物或变体的制剂,其用于抑制人或动物受试者上含角蛋白的材料的真菌病原体的感染。
本文进一步实现的是包含植物防御素或者其功能性天然或合成衍生物或变体的制剂,其用于抑制人或动物受试者上毛发或皮毛或者毛发或皮毛毛囊的真菌病原体的感染。
本文实现的是包含植物防御素或者其功能性天然或合成衍生物或变体的制剂,其用于抑制人或动物受试者上与头癣、头皮屑或脂溢性皮炎相关的真菌病原体的感染。
在一个实施方案中,本文教导的是包含区室或者分区形式的治疗试剂盒,其中区室包含植物防御素或其功能性天然或合成衍生物或变体。第二或其他区室可以包括含有其他抗真菌剂的其他试剂或赋形剂。每个区室的内容物可在使用之前混合,或以任何顺序依次使用。其他抗真菌剂包括非防御素肽、蛋白酶抑制剂、另一种防御素或蛋白或化学(非蛋白的)抗真菌剂。可以与植物防御素组合使用的其他抗真菌剂的实例包括灰黄霉素、特比萘芬、阿莫罗芬、环吡酮、依芬康唑、tavaborole和三唑。
提及“植物防御素”是指参考表2在本文限定的那些。基于甲、爪、蹄或者角的渗透性,也可以选择表2的防御素。基于其对红色毛藓菌的强效杀真菌活性以及对哺乳动物和细菌细胞缺乏活性或者具有医学上可接受的最小活性,也可以选择表2的防御素。如本文中所限定的,防御素包括与seqidno:24具有至少约80%相似性的防御素,包括seqidno:1、seqidno:2或seqidno:3中的任一个或seqidno:4至47中的任一个。在最佳比对后确定80%相似性,并且在必要时,在使用适当的间隔(space)用以优化比对之后确定。“至少80%”或“至少约80%”包括80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99和100%。在本发明的实践中有用的防御素是容易穿透入甲中的防御素。具体实例包括带有n末端丙氨酸残基的hxl008(seqidno:1)、hxl035(seqidno:2)和hxl036(seqidno:3)及其变体(分别为seqidno:25、seqidno:26和seqidno:27)。
因此,本文中教导的是一种用于在受试者上抑制真菌病原体感染的方法,所述真菌病原体在覆盖背部或末端趾骨的角状包膜或相关脑部突出物或者含角蛋白的材料或含角蛋白的材料的毛囊上,所述方法包括用有效量的选自seqidno:1至47的植物防御素、或其功能性天然或合成衍生物或变体、或者最佳比对之后与seqidno:1至47中任一个具有至少80%相似性的防御素、或者带有n末端丙氨酸残基的选自seqidno:25至47的防御素,在足以改善感染症状的条件下与所述包膜或突出物或含角蛋白的材料接触一段时间。
本文还实现的是一种用于在受试者上抑制真菌病原体感染的方法,所述真菌病原体在覆盖背部或末端趾骨的角状包膜或相关脑部突出物或者含角蛋白的材料或含角蛋白的材料的毛囊上,所述方法包括用有效量的具有seqidno:24所示的一致性氨基酸序列的防御素、或其功能性天然或合成衍生物或变体、或者与seqidno:24具有至少80%相似性的防御素,任选地带有n末端丙氨酸残基,在足以改善感染症状的条件下与所述包膜或突出物或含角蛋白的材料接触一段时间。
本文进一步教导的是hxl008(seqidno:1)、hxl035(seqidno:2)或者hxl036(seqidno:3)治疗甲真菌病的用途。还教导了seqidno:25、seqidno:26或者seqidno:27所限定的防御素治疗甲真菌病的用途。
本文所用的术语“相似性”包括在氨基酸水平上在待比较序列之间的精确同一性。如果在氨基酸水平存在非同一性,“相似性”包括无论如何在结构、功能、生化和/或构象水平上彼此相关的氨基酸。在一个实施方案中,在同一性而非相似性水平上进行氨基酸序列比较。
用于描述两个或更多多肽之间序列关系的术语包括“参考序列”、“比较窗口”、“序列相似性”、“序列同一性”、“百分比序列相似性”、“百分比序列同一性”、“基本相似”和“基本同一”。“参考序列”长度至少为12,但通常为15至18,通常至少为25或以上,例如30个氨基酸残基。因为两个多肽可以各自包含(1)在两个多肽之间相似的序列(即仅完整氨基酸序列的一部分),和(2)两个多肽之间区别的序列,通常通过在“比较窗口”上比较两个多肽的序列来进行两个(或更多)多肽之间的序列比较,以鉴定和比较序列相似性的局部区域。“比较窗口”是指与参考序列进行比较的通常为12个连续残基的概念段。对于两个序列的最佳比对,比较窗口可以包括,与参考序列(其不包含添加或者缺失)相比,约20%或更少的添加或者缺失(即,缺口)。用于比对比较窗口的最佳序列比对,可以通过计算机化的算法应用(gap、bestfit、fasta、clustalw2和wisconsingeneticssoftwarepackagerelease7.0中的tfasta,遗传学计算机小组,575sciencedrivemadison,wi,usa)或者通过检查和任何所选择的各种方法产生的最佳比对(即比较窗口之间产生最高的百分比同源性)而进行。也可以参考blast程序家族,例如altschul等人(1997)nucl.acids.res.25(17):3389-3402所公开的。序列分析的详细讨论可见于ausubel等人(1994-1998)in:currentprotocolsinmolecularbiology,johnwiley&sonsinc的单元19.3。其他比对软件包括bwa(li和durbin(2010)bioinformatics26:589-595)以及bowtie(langmead等人(2009)genomebiol10:r25和blat(kent(2002)genomeres12:656-664)。
本文所用的术语“序列相似性”和“序列同一性”是指在氨基酸-氨基酸的基础上在比较窗口中序列相同或在功能上或在结构上相似的程度。因此,例如通过在比较窗口上比较两个最佳比对的序列,确定在两个序列中存在的相同氨基酸残基(例如,ala、pro、ser、thr、gly、val、leu、ile、phe、tyr、trp、lys、arg、his、asp、glu、asn、gln、cys和met)的位置数而产生匹配的位置数,将匹配的位置数除以比较窗口中的位置总数(即,窗口大小),并将结果乘以100以产生序列同一性百分比,来计算“序列同一性百分比”。为了本发明的目的,“序列同一性”将被理解为意指通过任何合适的方法或者使用软件随附参考手册中使用的标准默认值的计算机算法所计算的“匹配百分比”。类似的评论适用于序列相似性。
本文使用的一些防御素,取决于它的来源在本文中可以称为“天然存在的”防御素、“修饰的”防御素、“变体”防御素、“突变的”防御素、“合成衍生物或者变体”或者“嵌合的”防御素。对于本发明的实践,这种防御素保留抗真菌活性。
在一个实施方案中,防御素是ii类茄属(solanaceous)防御素。在一个实施方案中,防御素在防御素n末端部分的第一β链(β链1)和α螺旋之间的环区被修饰。在一个实施方案中,环区包含第二不变半胱氨酸残基n末端的6个氨基酸或其等同物。这个区被定义为“环1b”。对于成熟结构域的相对保守c末端部分而言,ii类茄属(solanaceous)防御素区别于其他防御素。
本文包括包含修饰的ii类茄属(solanaceous)防御素骨架的人工产生的防御素用于产生具有抗病原体活性的变体防御素的用途,其中通过单个或更多氨基酸的取代、添加和/或缺失来修饰n末端部分的β链1和α螺旋之间的环区。在一个实施方案中,环区为第二不变半胱氨酸残基n末端的6个氨基酸残基所限定的环1b。在本文中考虑任何防御素中的等同区域。在一个实施方案中,人工产生的防御素包含修饰的ii类防御素。本方案不延及含有天然氨基酸序列的nad1的用途。
合适的防御素的实例包括表1中列出的那些。这些包括合成防御素变体,比如hxp4(seqidno:21)、hxp34(seqidno:22)和hxp35(seqidno:23)。本文还包括带有n末端丙氨酸残基的后三种防御素(即,分别为seqidno:45至47)。有用的防御素是hxl008(seqidno:1)、hxl035(seqidno:2)和hxl036(seqidno:3)或者其功能性天然或合成衍生物或变体,包括seqidno:25、seqidno:26和seqidno:27。
本文教导的是一种用于在甲、爪、蹄或角之上或之中抑制真菌病原体感染的方法,所述方法包括使甲、爪、蹄或者角接触有效量的选自本文表1中列出的植物防御素或者其衍生物或变体。一般来说,防御素在足以改善感染症状的条件下应用一段时间。在一个实施方案中,症状与甲真菌病或相关疾病有关。
本文教导的是一种用于在甲、爪、蹄或角之上或之中抑制真菌病原体感染的方法,所述方法包括使甲、爪、蹄或者角接触有效量的选自本文表2中列出的植物防御素或者其衍生物或变体。防御素可以按照0.1%至10%w/v的浓度,每天一次、每天两次、每两天一次、每周一次、每两周一次或每月一次的频率,为期四周、两周、一周、三周、一个月、两个月、三个月或直至十二个月进行应用。在一个实施方案中,症状与甲真菌病或相关疾病有关。
本文教导的是一种用于在皮肤、毛发或皮毛之上或之中抑制真菌病原体感染的方法,所述方法包括使皮肤、毛发或皮毛或者毛发或皮毛毛囊接触有效量的选自本文表1中列出的植物防御素或者其衍生物或变体。防御素在足以改善感染症状的条件下应用一段时间。在一个实施方案中,症状与真菌感染有关。
本文教导的是一种用于在皮肤、毛发或皮毛之上或之中抑制真菌病原体感染的方法,所述方法包括使皮肤、毛发或皮毛或者毛发或皮毛毛囊接触有效量的选自本文表1中列出的植物防御素或者其衍生物或变体。防御素可以按照0.1%至10%w/v的浓度,每天一次、每天两次、每两天一次、每周一次、每两周一次或每月一次的频率,为期一周、两周、三周、一个月、两个月、三个月或直至十二个月进行应用。在一个实施方案中,症状与真菌感染有关。
在一个任选的实施方案中,防御素或者其衍生物或者变体与另一种试剂如抗真菌剂组合使用。建议防御素和肽协同作用。其他试剂的实例包括非防御素抗微生物肽、蛋白酶抑制剂、另一种防御素或者蛋白或非蛋白质化学杀真菌剂。
与受试防御素组合使用的化学抗真菌剂包括特比萘芬、伊曲康唑、氟康唑、环吡酮、克霉唑、阿莫罗芬、布替那芬、tavaborole、依芬康唑、an2718和np213。
提及协同作用意味着,给定的防御素或其他试剂单独的抑制作用,当两者一起使用时比单独使用时更强。greco等人(1995)pharmacolrev.47:331-385定义了一类协同作用,其基础在于组合使用两种试剂时,比各自单独测试时的加成作用具有更强的活性。因此,本文采用的定义包括所有这些情况,只要两种试剂一起发挥的组合作用大于各试剂单独发挥作用时的总和。此外,如本文术语所期望的,如果存在一组条件,包括但不限于浓度,当试剂一起发挥作用时的组合作用大于各组分单独发挥作用时的总和,则试剂的组合被认为是协同的。richer(1987)pesticsci19:309-315描述了建立协同作用验证的数学方法。这种方法使用limpel公式来比较两种抑制剂x和y组合存在时观察到的抑制水平(io),以及在和测量其组合作用时所用的相同浓度下各x或y分别发挥作用所产生的预期加成作用(ee)。加成百分比抑制ee计算为x+y-xy/100,其中x和y表示为抑制百分比。当io>ee时,存在协同作用。
协同作用可以表示为协同作用尺度。在一个实施方案中,高达14的值代表着没有显著的协同作用,例如0、1、2、3、4、5、6、7、8、9、10、11、12、13或14;从15到29的值代表低协同作用,如15、16、17、18、19、20、21、22、23、24、25、26、27、28或29;30至60的值代表中等的协同作用,如30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59或者60;大于60的值代表高度的协同作用。“大于60”包括61至100,包括61、70、80、90和100以及之间的任意值。
本方法可用于治疗或预防覆盖背部或末端趾骨的角状包膜或相关脑部突出物或含角蛋白的材料(例如皮肤、毛发或者皮毛)的真菌病原体感染或侵染受试者。术语“受试者”包括任何年龄的人或动物,如农场动物(例如羊、猪、马、牛、驴、骆驼、美洲鸵、羊驼)或禽鸟(例如鸡、鸭、火鸡、雉鸡、孔雀)、伴侣动物(如狗或猫)、实验室检验动物(如小鼠、大鼠、兔、豚鼠或仓鼠)或捕获的野生动物(如野山羊)。“人”或者“动物”包括其部分,如脚趾甲、手指甲、爪、蹄、角、皮肤、毛发或皮毛。
提及“真菌”包括皮肤癣菌、酵母和非皮肤癣菌霉菌(非皮肤癣菌)。皮肤癣菌包括毛癣菌属(trichophyton)的物种,包括红色毛癣菌(trichophytonrubrum)、指(趾)间毛癣菌(trichophytoninterdigitale)、紫色毛癣菌(trichophytonviolaceum)、断发癣菌(trichophytontonsurans)、苏丹毛癣菌(trichophytonsoudanense)和须癣毛癣菌(trichophytonmentagrophytes)、粉小孢子菌(microsporumfulvum)、絮状表皮癣菌(epidermophytonfloccosum)和石膏样小孢子菌(microsporumgypseum)。酵母包括假丝酵母属(candida)的物种,包括白色念珠菌(candidaalbicans)和光滑念珠菌(candidaglabrata)。真菌可引起癣,如足癣、头皮屑或皮炎。
本文教导的另一方面是一种组合物,其包含植物防御素或其功能性天然或合成衍生物或变体、以及一种或更多药学上或兽医学上可接受的载体、稀释剂或赋形剂,其用于治疗或者预防甲真菌病或者相关疾病。一个任选的实施方案中,植物防御素与防御素和另一种抗真菌剂组合使用。在一个实施方案中,组合物为喷雾剂、雾剂、微米或纳米颗粒、水溶液、浸液、洗涤剂、补剂、分散剂、雾化制剂、唇膏、泥浆剂、粉剂、霜剂、软膏剂、凝胶、贴剂、浸渍绷带、液体、制剂、涂层剂或其他合适的分散介质的形式,包括局部组合物的形式。防御素可以特别配制成用以促进甲、爪、蹄或者角或毛发或皮毛颗粒的渗透性。
有用的应用包括用于甲、爪、蹄或者角或毛发或皮毛真菌感染的溶液、涂层剂、霜剂、粉剂、滴剂、软膏剂、洗发剂和浸液。
包含本文所述的防御素和任选另一种抗真菌剂的组合物,通常包括载体、赋形剂、稀释剂、防腐剂、稳定剂和/或固体或液体添加剂。含有防御素的植物提取物也可以使用。制剂包括身体沐浴露或洗发剂或浸液。
根据预期的施用方法,组合物可以采用多种形式。通常但非唯一地,局部组合物用于人或动物受试者。在制备组合物时,可以使用通常的介质,例如水,有机酸如柠檬酸或乙酸,二醇如乙二醇、丙二醇、1,3-丁二醇和聚乙二醇,油,醇如乙醇、甲醇或异丙醇,防腐剂和/或着色剂。组合物可以采取液体制剂的形式,比如例如悬浮液、酏剂和溶液。还可以使用载体如淀粉、糖、微晶纤维素、稀释剂、造粒剂、润滑剂、粘合剂、崩解剂等。组合物也可以是涂层剂、粉剂、分散剂、软膏剂、霜剂或洗涤剂的形式。
组合物可以包括一种或更多种可接受的赋形剂,例如乙二胺四乙酸、环甲基硅氧烷、羟丙基纤维素、羧甲基纤维素、羟丙基壳聚糖、聚乙烯吡咯烷酮、乙酸乙酯、二异丙基己二酸酯、肉豆蔻酸异丙酯和乳酸肉豆蔻酯。
通常在足以改善感染症状的条件下持续一段时间将防御素直接施用于感染部位。这包括改善甲真菌病或者相关疾病的症状。
在一个实施方案中,防御素以0.1%至10%w/v的浓度,每天一次、每天两次、每两天一次、每周一次、每两周一次或每月一次的频率,为期一周、两周、三周、一个月、两个月、三个月或直至十二个月,直接施用于感染部位。
当通过气雾剂或喷雾剂施用时,根据药物制剂领域众所周知的技术制备组合物,并且可以制备成盐溶液,使用苄醇或其他合适的防腐剂、吸收促进剂以提高生物利用度、碳氟化合物和/或本领域已知的其他增溶剂或分散剂。
根据是单独使用还是特定组合使用、施用方式、待治疗的真菌病原体和真菌病原体侵染的严重程度,防御素的有效剂量可以改变。因此,根据包括受试者的种类、物种、年龄、体重、性别和医疗处置;待治疗疾病的严重程度;施用方式;以及所用的具体防御素等多种因素,来选择利用防御素的剂量方案。医生、临床医师或兽医普通技术人员可以很容易地确定并规定预防、抵制或者阻止真菌病原体侵染进展所需的防御素有效量。缓释制剂也在本文中考虑。在一个实施方案中,组合物包含渗透剂以便于防御素进入感染部位。
在一个实施方案中,组合物含有增加甲的渗透的分子。增加甲渗透性的分子包括无机盐、硫醇、甘氨酸、半胱氨酸、脲、过氧化物、酸如磷酸或巯基乙酸、碱如氢氧化钠或钾、还原剂(硫醇、亚硫酸盐/酯)、二甲基亚砜、聚二醇、甘油、c2-5醇、c2-8多元醇、c6-24脂肪酸甘油三酸酯、c6-24脂肪醇、c6-24烷基硫酸酯、c6-24脂肪酸;非离子表面活性剂或其混合物(murthy等人(2009)jpharmsci98(11):4264-4271;nair等人(2009)jpharmpharmacol61(4):413-417;malhotra和zatz(2002)jpharmsci91(2):312-323;khengar等人(2007)pharmres24(12):2207-2212;murdan(2008)expertopindrugdeliv5(11):1267-1282;reevesus专利号6,391,879;willers等人,欧洲专利号2664327)。
另一方面提供了一种用于治疗或预防动物(包括哺乳动物,例如被真菌病原体感染或侵染的人受试者)的方案或者方法,所述方案或者方法包含在一个部位对受试者施用抗真菌病原体有效量的包含植物防御素的组合物,所述部位是覆盖背部或末端趾骨的角状包膜或相关脑部突出物或者是含角蛋白的材料。
另一方面提供了一种用于治疗或者预防甲真菌病或皮肤、毛发或皮毛真菌感染的方案或方法,所述方案或方法包括将抗真菌病原体有效量的组合物施用至甲、爪、蹄、角或者毛发或皮毛颗粒或者毛发或皮毛毛囊,所述组合物含有植物防御素和任选另一种抗真菌剂。所述另一种抗真菌剂包括非防御素抗微生物肽、蛋白酶抑制剂、另一种防御素和蛋白或非蛋白质化学抗真菌剂。
术语“应用(applying)”包括接触和暴露以及施用于部位。在一个实施方案中,应用包括渗透甲、爪、蹄或角的作用或者渗透毛发或皮毛颗粒或毛发或皮毛毛囊的作用。
防御素可用于对抗真菌疾病或角状包膜以及相关脑部突出物(如甲、爪、蹄和角)或含角蛋白的材料(如皮肤、毛发或皮毛)的感染。在一个实施方案中,本说明书教导了用于治疗或者预防甲真菌病或相关疾病的方案。在一个实施方案中,本说明书教导了一种用于治疗或预防头癣、头皮屑和脂溢性皮炎或者相关疾病的方案。该方案具有人和兽医学应用。
例如使用肽或蛋白质合成仪,使用标准的逐步添加一个或更多氨基酸残基,基于其氨基酸序列制备本发明的防御素。或者,通过重组方法制备防御素。重组防御素在其n-末端可以包括额外的丙氨酸残基。因此,本文考虑的防御素可含有n末端丙氨酸残基。
本文中教导的另一个方面是重组生产植物防御素的方法。在一个实施方案中,使用微生物表达系统生产植物防御素。在又一个实施方案中,表达系统是基于酵母的表达系统,如巴斯德毕赤酵母(pichiapastoris)。在一个优选的实施方案中,植物防御素被表达为具有靶向细胞外蛋白的分泌信号的融合蛋白。然后酶促去除分泌信号以将成熟的植物防御素释放到表达介质中。然后通过离子交换色谱纯化植物防御素。在一个优选的实施方案中,通过使用树脂(如sp-sepharose)的阳离子交换色谱纯化植物防御素。然后,通过使用适合小蛋白的介质(如superdex30)的尺寸排阻色谱法进一步纯化植物防御素。
此外,防御素可以进行化学修饰以使防御素成为化学类似物。这种防御素类似物可能表现出更强的稳定性,或者在与组织接触的位置具有更长的半衰期。
本文考虑的类似物包括但不限于侧链的修饰,在肽、多肽或蛋白合成期间掺入非天然氨基酸和/或其衍生物,以及使用交联剂和对防御素分子赋予构象限制的其他方法。该术语也不排除防御素的修饰,例如糖基化、乙酰化、磷酸化等。在定义中包括例如含有一个或更多氨基酸类似物(包括例如非天然氨基酸)的防御素或具有取代键的防御素。这种类似物可具有增强的稳定性和/或渗透性。
本发明考虑的侧链修饰的实例包括氨基的修饰,例如通过与醛反应然后用nabh4还原的还原烷基化;与亚氨酰乙酸甲酯进行的酰胺化;用乙酸酐进行的酰化;氨基与氰酸酯进行的甲酰化;氨基与2,4,6-三硝基苯磺酸(tnbs)进行的三硝基苯甲酰化;氨基与琥珀酸酐和四氢邻苯二甲酸酐进行的酰化;以及赖氨酸和吡哆醛-5-磷酸进行的吡哆酰化,随后用nabh4还原。
可以通过用例如2,3-丁二酮、苯甲酰甲醛和乙二醛的试剂形成杂环缩合产物来修饰精氨酸残基的胍基。
可以通过形成o-酰基异脲,随后衍生成为例如相应的酰胺,通过碳酰亚胺的活化来修饰羧基。
可以通过诸如用碘乙酸或碘乙酰胺进行羧甲基化;过甲酸氧化成半胱氨酸;与其他硫醇化合物形成混合的二硫化物;与马来酰亚胺、马来酸酐或其他取代的马来酰亚胺反应;使用4-氯代苯甲酸汞、4-氯代苯磺酸汞、苯基氯化汞、2-氯汞-4-硝基苯酚以及其他汞形成汞衍生物;在碱性ph下用氰酸酯进行氨甲酰化的方法修饰硫基。
可以通过例如用n-溴代琥珀酰亚胺进行氧化、或用2-羟基-5-硝基苄基溴或者磺酰卤将吲哚环烷基化,来修饰色氨酸残基。另一方面,酪氨酸残基可以通过用四硝基甲烷形成3-硝基酪氨酸衍生物进行的硝化得以修饰。
可以通过用碘乙酸衍生物进行的烷基化或焦碳酸二乙酯进行n-乙酯基化来实现组氨酸残基咪唑环的修饰。
在肽合成过程中并入非天然氨基酸和衍生物的实例包括但不限于使用正亮氨酸、4-氨基丁酸、4-氨基-3-羟基-5-苯基戊酸、6-氨基己酸、叔丁基甘氨酸、正缬氨酸、苯基甘氨酸、鸟氨酸、肌氨酸、4-氨基-3-羟基-6-甲基庚酸、氨基酸的2-噻吩丙氨酸和/或d-异构体。双官能交联剂,例如具有(ch2)n间隔基团的双官能亚胺酯,其中n=1至n=6,戊二醛,n-羟基琥珀酰亚胺酯以及通常含有氨基反应性部分(如n-羟基琥珀酰亚胺)和另一基团特异性反应性部分(例如马来酰亚胺或二硫代部分(sh)或碳二亚胺(cooh))的异双官能试剂。此外,例如通过引入cα和nα-甲基氨基酸、氨基酸的cα和cβ原子之间引入双键、以及通过引入共价键形成环肽或类似物(例如在n和c末端之间、在两条侧链之间或侧链与n或c末端之间形成酰胺键)使得肽在构象上受限制。
模拟物是另一类有用的防御素类似物组。该术语旨在指与防御素具有一些化学相似性并模仿其抗真菌活性的物质。肽模拟物可以是模仿蛋白二级结构元件的含肽分子(johnson等人,peptideturnmimeticsinbiotechnologyandpharmacy,pezzuto等人编辑,chapmanandhall,newyork,1993)。使用肽模拟物的基本原理是蛋白的肽骨架主要以定向氨基酸侧链的方式存在以促进活性作用。
另一方面提供了一种用于减少或控制人甲上的真菌感染或侵染的方法,所述方法包括,将植物防御素或其功能性天然或合成衍生物或变体以及任选地另一种抗真菌剂局部应用到人潜在感染的区域。在一个实施方案中,药物为溶液、粉剂、喷雾剂、雾化剂、纳米颗粒、凝胶、糊剂、浸渍绷带、涂层剂、气雾剂、浸液或其他液体的形式。抗真菌制剂也可以是缓释组合物。
另一方面提供了一种用于减少或控制人毛发上真菌感染或侵染的方法,所述方法包括,将植物防御素或其功能性天然或合成衍生物或变体以及任选地另一种抗真菌剂局部应用到人潜在感染的区域。在一个实施方案中,药物为溶液、粉剂、喷雾剂、雾化剂、纳米颗粒、凝胶、糊剂、浸渍绷带、涂层剂、气雾剂、浸液或其他液体的形式。抗真菌制剂也可以是缓释组合物。
如本文所使用的,“包含”是“包括”、“含有”或“特征在于”的同义词,并且是包容性的或者是开放式的,并且不排除额外的未被引用的元素或者方法步骤。如本文所用,“由...组成”不包括在权利要求要素中未指定的任何元素、步骤或者成分。如本文所使用的,“基本上由...组成”不排除不重大影响权利要求中基本的和新颖性特征的材料或步骤。本文中术语“包含”的任何引述,特别是在组合物组分或者描述装置元件的描述中,被理解为包括基本上由以及由所述组分或元素组成的那些组合物和方法。适当地,可以缺失本文没有具体公开的任何一个或更多元素、一个或更多限定,来实施本文中所说明性描述的公开。
当本文使用马库什组或者其他分组时,该组的所有个体成员以及该组可能的所有组合和子组合旨在单独包含在本公开中。
当在本文中提及范围时,意图包括在所述范围内的所有子范围以及在所述范围内的所有整数值,就好像每个子范围和整数值都被提及一样。
实施例
现在,在以下非限定性实施例中描述本文所公开的和实施的方面。
方法
从巴斯德毕赤酵母中纯化防御素
在250ml烧瓶中,用单一ppink-防御素巴斯德毕赤酵母pichiapink(商标)株1菌落接种25mlbmg介质(invitrogen毕赤酵母表达手册中描述),在30℃振荡培养箱(140rpm)中孵育2-3天。在1l带有挡板的(baffled)烧瓶中,培养物用于接种200mlbmg,将烧瓶置于30℃振荡培养箱(140rpm)过夜。通过离心(1,500×g,10分钟,4℃)收集细胞,并在5l带有挡板的烧瓶中重新悬浮于1lbmm介质中,并在28℃振荡培养箱中孵育3天(对于nad1是2天)。培养物诱导t=24和48h。通过离心(6000rpm,20分钟,4℃)将表达介质与细胞分离。将介质调节至ph3.0,然后将其施用于用ph6.0的100mm磷酸钾缓冲液预平衡的spsepharose柱(1cm×1cm,amershambiosciences)上。然后用100ml100mm磷酸钾缓冲液ph6.0洗涤柱(对于hxl004,洗涤×2)。结合的蛋白在10x10ml含有500mmnacl的100mm磷酸钾缓冲液中洗脱。进行斑点印迹以鉴定具有最高浓度的洗脱蛋白的馏分,并且使用离心柱将这些馏分浓缩至1ml,并使用无菌milliq超纯水洗涤5次。用二辛可宁酸(bca)蛋白分析(piercechemicalco.),使用牛血清白蛋白(bsa)作为蛋白标准,确定毕赤酵母表达的防御素的蛋白浓度。
本文考虑使用的防御素列于表1和表2中,包括最佳比对之后与所列防御素中的任何一个具有至少为80%相似性的防御素。
图1(a)至(e)提供了显示氨基酸序列之间相似性的比对(参见表1的定义)。图11提供了hxl008(seqidno:1)、hxl035(seqidno:2)和hxl036(seqidno:3)的氨基酸序列的比对。这种比对用于产生seqidno:24所示的一致性氨基酸序列。任何这些序列可以包含任选的n末端丙氨酸残基。
实施例1
在植物防御素存在时抑制红色毛癣菌和粉小孢子菌的生长
植物防御素包括茄属(solanaceous)ii类防御素(nad1)和i类防御素(hxl001、hxl002、hxl004、hxl005、hxl008、hxl009、hxl012、hxl013、hxl015、nad2)。有关序列标识符,请参见表1和表2。
植物防御素对红色毛癣菌、指(趾)间毛癣菌、粉小孢子菌和白色念珠菌的生长的抑制作用(获自国立真菌学参考中心、澳大利亚阿德莱德,妇女儿童医院的南澳大利亚病理科),是基本上按照broekaert等人(1990)femsmicrobiollett69:55-59的描述进行测量。
从生长在1/2强度沙氏葡萄糖琼脂(sda)上产生孢子的真菌中分离红色毛藓菌、指(趾)间毛癣菌和粉小孢子菌的孢子。通过加入1/2强度马铃薯葡萄糖肉汤(pdb)从板上除去孢子。将白色念珠菌细胞在酵母蛋白胨肉汤(ypd)中培养16小时。使用血细胞计数器测量孢子和细胞浓度。
基本上如本文所述,在96孔微量滴定板中进行抗真菌分析。孔中加载20μl过滤灭菌的(0.22μm注射器过滤器,millipore)防御素(各终浓度为10×储备液)或水和80μl5×104孢子/ml(红色毛藓菌、指(趾)间毛癣菌、粉小孢子菌)或5,000细胞/ml(白色念珠菌)在1/2强度的pdb中。在30℃孵育板。通过使用微量滴定板读板器(spectramaxprom2;moleculardevices)测量595nm(a595)的光密度测定真菌生长。允许生长进行,直到不存在任何测试防御素时真菌的光密度(od)达到0.2的od。各测试进行两次。
孵育72小时后,将来自孔中的介质接种到新鲜的沙氏葡萄糖琼脂上,所述孔含有用100g/mlhxl008孵育的红色毛藓菌的临床分离株。板在30℃孵育5天,以允许菌落在拍照之前得以发育。
抑制分析的结果示于表3中。hxl005、hxl008和hxl035对于各种真菌病原体是最有效的植物防御素。hxl001和hxl009在测试浓度下没有显示任何活性。hxl002和nad2是粉小孢子菌和白色念珠菌非常差的抑制剂。hxl004、hxl012、hxl013和hxl015对于各种病原体显示中等活性。
hxl008(实线)和nad1(虚线)对红色毛藓菌临床分离株的抑制结果显示于图2(a)至图2(d)。在低浓度时,两种肽都抑制了真菌生长,其中对四种临床分离株的ic50低于20μg/ml。然而,在所有情况下,hxl008以比nad1更低的浓度抑制生长。
红色毛藓菌临床分离株的细胞存活分析结果如图3(a)至3(e)所示。接种有未用植物防御素孵育过的细胞的板,几乎完全被生长所覆盖。相比之下,接种有在hxl008存在时孵育72小时的细胞的板只有1-3个菌落,表明几乎所有细胞死亡。
表3
实施例2
在hxl008存在时红色毛癣菌的生长抑制持续28天
在28天内监测hxl008对红色毛癣菌(获自国立真菌学参考中心、澳大利亚阿德莱德,妇女儿童医院的南澳大利亚病理科)生长的抑制作用。
红色毛藓菌的孢子从生长在1/2强度沙氏葡萄糖琼脂上产生孢子的真菌中分离出来。通过加入1/2强度的马铃薯葡萄糖肉汤(pdb),从板上除去孢子。使用血细胞计数器测量孢子和细胞浓度。
在含有0、10或50μg/mlhxl008的1/2pbd(2ml)中将孢子稀释至5×104个孢子/ml的浓度。在30℃下不振摇地孵育培养物。24小时后,每个培养物提取100μl并涂布在1/2sda板上。然后加入另外100μl的1/2pdb,其中含有0、20或100μg的hxl008。然后将sda板在30℃下孵育5天。该过程每24小时重复一次,持续28天。15天后,不含hxl008的培养物变得太稠而无法用移液管吸取,不再用于测定。
抑制分析的结果如图4所示。用10μg/ml或50μg/ml处理的培养物在分析期间没有显示任何可见的红色毛藓菌的生长。在24小时内,50μg/ml的hxl008已经杀死了超过80%的红色毛藓菌细胞,当在没有hxl008的情况下接种到1/2sda上时可见。在接下来的19天,存活的菌落数继续减少。治疗20天后,板具有0或者只有1个菌落,表明超过99.5%的细胞死亡。
实施例3
植物防御素对人甲的渗透性
根据hui等人(2002)jpharmsci91(1):189-195的方法测量nad1对人甲的渗透性。人脚趾甲获自sciencecare(usa),并用磷酸盐缓冲盐水(细节,pbs)洗涤,然后置于已经浸泡在pbs中3小时的kimwipe中,以使得甲再水化。然后将甲放置在塑料的甲接合器(permagear,usa)中,剂量面积为0.5×0.5cm,并将用75微升pbs润湿的棉签放置在接收室中与甲底侧接触。
持续4天将蛋白(10-30μl的5-10mg/ml溶液)每24小时施用至甲的顶部。24小时后、以及随后的每24小时后,将接触甲底侧的棉签除去。通过用500μl的0.1%v/v三氟乙酸洗涤两次,从棉签中回收穿透甲的蛋白。使用rp-hplc定量回收的蛋白。
甲渗透性分析的结果表示在表4和图5中。当每天施用至甲的表面时,相较于目前的局部甲真菌病治疗活性成分(tavaborole、依芬康唑和环吡酮),植物防御素hxl008、nad1和hxl004能够更快更有效地渗透甲。相较于nad1或者hxl004,检测出更多穿透甲的hxl008。植物防御素hxl012没有渗透甲。
表4
实施例4
在植物防御素的存在时抑制大肠杆菌(escherichiacoli)的生长
使用单个大肠杆菌菌落接种5mlluria-bertani介质,并在37℃下生长过夜。第二天,测量培养物的光密度,在mueller-hinton肉汤中将大肠杆菌稀释至0.01的600nm光密度(od600)。稀释的大肠杆菌以10μm、5μm、2.5μm、1.25μm、0.625μm、0.3125μm或0.1625μm的浓度加入具有防御素的96孔板中。在od595时读取板以获得时间零数据点。板在37℃下孵育18小时,然后再次在od595读取以评估大肠杆菌生长的量。
大肠杆菌的抑制结果示于图7中。hxl004以浓度依赖性方式抑制大肠杆菌的生长,这类似于ll37对照。在测试浓度下,nad1和hxl008不抑制大肠杆菌的生长。
实施例5
在植物防御素存在时哺乳动物细胞的存活
将人单核细胞淋巴瘤(u937)细胞在rpmi-1640介质中培养。所有培养介质均补充5-10%v/v胎牛血清、100u/ml青霉素和100μg/ml链霉素。细胞系在37℃,含有5%v/vco2的潮湿气氛中培养。通过加入含有0.25%v/v胰蛋白酶和0.5μm的edta的混合物将贴壁细胞系与烧瓶分离。
进行基于流式细胞仪的碘化丙啶(pi)吸收分析,以分析植物防御素渗透u937细胞的能力(基本上如poon等,2014所述)。简言之,在0.1%v/vbsa/rpmi-1640中将细胞悬浮至1×106个细胞/ml,并在37℃下用植物防御素(10μm)孵育30分钟。将样品加入到含有终浓度为1μg/mlpi的pbs中并置于冰上。然后使用bdfacscantoii流式细胞仪和bdfacsdiva软件v6.1.1对样品立即进行分析。使用flowjo软件v8.8.6分析得到的流式细胞术数据。基于正向散射和侧向散射适当地对细胞进行门控(gated),通过pi阳性染色鉴定细胞渗透性。
pi吸收分析的结果如图7所示。植物防御素nad1和hxl005在测试条件下对哺乳动物细胞有毒性。nad1渗透33%的细胞,而hxl005渗透接近25%。植物防御素hxp4、hxl004和hxl013对哺乳动物细胞毒性较小,仅渗透13%(hxp4和hxl004)或5%(hxl013)的细胞。相比之下,hxl001、hxl002、hxl008、hxl009和hxl012在测试条件下对哺乳动物细胞无显著毒性,渗透小于2%的细胞。
实施例6
植物防御素存在时的人血红细胞裂解
从全血收集人血红细胞(rbc),并用1×pbs洗涤,以1000×g沉淀10分钟。rbc按照1对10进行稀释,以便用植物防御素(100μm)进行处理,在5%v/vco2/95%v/v空气的湿润氛围下孵育过夜。孵育24小时后,以2000rpm离心细胞10分钟,上清液用1×pbs按照1对100进行稀释。然后,通过测量412nm处的吸光度确定rbc裂解的指示物释放的血红蛋白。结果已经比对着用水处理的rbc进行归一化(指定为100%裂解)。
血红细胞裂解分析的结果如图8所示。在100μm时,植物防御素nad1和hxl004分别裂解1.47和1.09%的rbc,而hxl008仅裂解0.42%。误差条表示标准偏差。
实施例7
制剂成分对hxl008人甲渗透性的影响
在水、50mm柠檬酸缓冲液ph4.0、或者含20%v/v乙醇和0.5mmedta的50mm柠檬酸缓冲液ph4.0中,将hxl008溶解至浓度为10mg/ml。根据同上hui等人(2002)的方法,测量各制剂中hxl008对人甲的渗透性。人的趾甲获自sciencecare(usa),并用磷酸缓冲盐水(pbs)洗涤,之后放置在于pbs中浸泡了3小时的kimwipe上,以使得甲再水化。然后将甲放置在塑料的甲接合器(permagear,usa)中,剂量面积为0.5×0.5cm,并将用75微升pbs润湿的棉签放置在接收室中与甲底侧接触。
持续2或3天将制剂中的蛋白(10μl的10mg/ml溶液)每24小时施用至甲的顶部。24小时后、以及随后的每24小时后,将接触甲底侧的棉签除去。通过用500μl的0.1%v/v三氟乙酸洗涤两次,从棉签中回收穿透甲的蛋白。使用rp-hplc定量回收的蛋白。
渗透性分析的结果表示在表6和图9中。当每天施用至甲的表面时,hxl008穿透甲的渗透性,当50mm柠檬酸缓冲液ph4.0存在时,有或没有乙醇和edta,得以增强。
表6
在三种不同的制剂中hxl008对甲的渗透性
实施例8
使用巴斯德毕赤酵母进行的植物防御素的重组表达
在方法中,描述了植物防御素hxl008、hxl008+丙氨酸、hxl004和nad1在巴斯德毕赤酵母中的表达。
来自巴斯德毕赤酵母中重组表达的各种植物防御素的产量如表7所示。hxl008+丙氨酸是最高度表达的蛋白,产量为7.5mg/l。
表7
蛋白表达和纯化之后的防御素产量
实施例9
hxl008+丙氨酸的大规模表达和纯化
将hxl008+丙氨酸的开放阅读框(orf)克隆到毕赤酵母表达载体ppic9中。orf和α因子分泌信号插入框内,直接位于kex2切割位点的下游。然后,使用限制性酶sali将质粒在his4选择盒中线性化,并转化到电感受态的gs115巴斯德毕赤酵母细胞中。使用缺乏组氨酸的介质选择阳性菌落。阳性菌落用于接种5mlypd,并在振荡培养箱中在30℃下孵育25小时。将培养物中的细胞与20%甘油混合,速冻并储存在-80℃。
将来自甘油储液的细胞划线于ypd板上,并使其在30℃下生长48小时。然后,将板在4℃下储存达2周。
在2.5l烧瓶中使用来自ypd板的细胞(ppic9-防御素,gs115)接种500mlbmg介质(在invitrogen毕赤酵母表达手册中描述),并将培养物在28℃振荡培养箱(120rpm)中孵育2天。48小时后,在30lbbraun发酵罐中培养物用于接种20l发酵基础盐介质。在发酵期间温度保持在28℃。通过加入25%v/v氨溶液,在发酵期间将ph保持在5.0,以响应ph的任何降低。在发酵期间,通过增加搅拌(最小500rpm)或增加流量或者氧气,将溶解氧(do)保持在30%。
20l培养物以3.6ml/min的速率喂以无菌的100%v/v甘油,直到细胞密度达到250-300g/l。此时,停止甘油进料,并允许培养直到所有甘油消耗,如do中的峰所证明的。然后,培养物喂以含有12ml/l痕量金属的无菌100%v/v甲醇。持续8小时,进料速率从0.2加速至2.18ml/min。然后,将2.18ml/min的进料速率再维持48小时。
通过离心(6000rpm,20分钟,4℃)收获表达介质并与细胞分离。介质通过0.22μm的膜进行过滤,得以澄清。介质在50mm乙酸盐缓冲液ph5.3中以1对5进行稀释。然后,将稀释的介质应用于已经用ph5.3的50mm乙酸盐缓冲液预平衡的sp-sepharose柱(高效)。然后,将柱用20个柱体积的50mm乙酸盐缓冲液ph5.3洗涤。使用含有1mnacl的0至100%v/v50mm乙酸盐缓冲液ph5.3的线性梯度洗脱结合的hxl008。将含有蛋白的馏分(通过280nm处的吸光度鉴定)合并,并浓缩至200ml,然后进行尺寸排阻色谱法。将蛋白质加载到1800mlsuperdex30柱(5cm×92cmxk50/100柱)上,以15ml/min用50mm磷酸钠缓冲液、150mmnacl、ph7.2进行洗脱。弃去空(void)体积洗脱的蛋白,并使用质谱鉴定含有hxl008+丙氨酸的馏分。合并含有hxl008的馏分,然后在无菌milliq水中脱盐,并使用3000mwco旋转柱浓缩。
通过sds-page、rp-hplc和质谱分析所得肽溶液。通过使用bca分析测量肽浓度,来确定最终产量。产生总共1.436g的hxl008+丙氨酸,并纯化至大于99%的纯度。
纯化的结果示于图10中。图10a是纯化的hxl008+丙氨酸的sds-page凝胶。泳道1、2和14是分子量标记(seeblue[注册商标]plus2)。泳道3和4是hxl008+丙氨酸标准(5μg)。泳道5至12是来自合并的尺寸排阻馏分的样品。图10b是合并的洗脱液的rp-hplc痕。在约7.1分钟处,观察到单峰,这与hxl008+丙氨酸的预期保留时间一致。图xc是从4kda到20kda的maldi-tof质谱曲线。观察到的质量(5477da)对应于所有四个二硫键形成的hxl008+丙氨酸的预期值。
本领域技术人员将理解,除了具体描述的那些之外,本文所述的公开易于进行变化和修改。应当理解,本公开考虑所有这些变化和修改。本公开还实现了本说明书中提及的或指明的所有步骤、特征、组合物和化合物,单独地或组合地,以及任何两个或更多步骤或特征或组合物或化合物的任意组合和所有组合。
文献
altschul等人(1997)nucl.acids.res.25:3389
ausubel等人(1994-1998)in:currentprotocolsinmolecularbiology,johnwiley&sonsinc
bloch和richardson(1991)febslett279(1):101-104
broekaert等人(1990)femsmicrobiollett69:55-59
cabral等人(2003)proteinexpresspurif31(1):115-122
colilla等人(1990)febslett270(1-2):191-194
elewski等人(2012)fungaldiseasesin:bolognia,jorizzo,schaffereds,dermatology第三版philadelphia,pa;elseviersaunders;77章
greco等人(1995)pharmacolrew47:331-385
hayes等人(2013)antimicrobagentsch57(8)3667-3675
hui等人(2002)j.pharmsci9(11):189-195
janssen等人(2003)biochemistry42(27):8214-8222
johnson等人,peptideturnmimeticsinbiotechnologyandpharmacy,pezzuto等人编辑chapmanandhall,newyork,1993
kent(2002)genomeres12:656-664
khengar等人(2007)pharmres24(12):2207-2212
kobayashi等人(2004)eurojpharmsci21:471-477
langmead等人(2009)genomebiol10:r25
li和durbin(2010)bionformatics26:589-595
malhotra和zatz(2002)jpharmsci91(2):312-323
merten和lippold(1997)jpharmpharmacol49:866-872
murdan(2008)expertopindrugdeliv5(11):1267-1282
murthy等人(2009)jpharmsci98(11):4264-4271
nair等人(2009)jpharmpharmacol61(4):431-437
rapini等人(2007)dermatology:2-volumeset,st.louis:mosby
reevesus专利号6,391,879
reid等人(2011)naturereviewµbiol9:27-38
richer(1987)pesticsci19:309-315
sagaram等人,(2011)plosone6.4:e18550
sotiriou等人(2010)actaderm-venereol9(2):216-217
thevissen等人(2012)molmicrobiol84(1):166-180
- 还没有人留言评论。精彩留言会获得点赞!