一种地榆苷元注射剂及其制备方法和用途与流程
本发明涉及一种地榆苷元注射剂及其制备方法和用途,属药物领域。
背景技术:
骨髓抑制是临床上常见的造血系统疾病,它可发生于各系统肿瘤性疾病的放射治疗及(或)化学治疗、电离辐射引起的放射损伤、病毒性肝炎、微小病毒感染或药物(氯霉素、苯、磺胺、抗癫痈药、镇静剂、抗甲状腺药、抗糖尿病药、抗疟疾、安眠药)等因素。骨髓抑制可引起骨髓微环境、造血干细胞、造血细胞生长因子等的损伤,粒、红、巨核细胞系统一系、二系或三系细胞受抑制。粒细胞缺乏会引起严重感染;红细胞明显减少会引起严重贫血;血小板明显下降引起严重出血,甚至导致死亡。
目前,临床上对于骨髓抑制,尤其是放化疗引起的骨髓抑制,尚缺乏有效的治疗手段。因此,寻找到有效的药物来缓解骨髓抑制,成为了一个亟待解决的问题。
地榆苷元是从蔷薇科地榆属植物地榆(Sanguisorba officinalis L.)或长叶地榆[S.officinalis L.var.longifolia(Bertol.)Yu et Li]的根中提取得到的一种活性成分,是地榆皂苷I和地榆皂苷II的苷元,化学名:3β,19α-羟基乌索-12烯-28-羧酸,其结构式如下所示:
然而,迄今尚未见以地榆苷元为活性成分制备注射剂,用于治疗和/或预防骨髓抑制的公开报道。
技术实现要素:
为解决上述问题,本发明提供了一种地榆苷元注射剂,其特征在于:它是包含下述原料制备而成的制剂:
地榆苷元、增溶剂。
进一步地,它是包含下述重量配比的原料制备而成的制剂:
地榆苷元0.5-10份、增溶剂0.001-60份。
进一步地,所述地榆苷元与增溶剂的重量配比为1:0.005~300。
进一步地,所述的增溶剂为吐温80、聚氧乙烯蓖麻油EL或泊洛沙姆188;所述的pH调节剂为氢氧化钠。
进一步地,所述注射剂中地榆苷元的浓度为0.2mg/mL。
进一步地,所述的注射剂是注射液、粉针剂、水针剂或大输液。
进一步地,包括下述步骤:
按配比称取地榆苷元分散于注射用水中,加入相应配比的增溶剂、pH调节剂,调节pH至10,搅拌溶解,再加入注射用水,过滤、灭菌,即得本发明注射剂。
本发明还提供了所述注射剂用于制备治疗和/或预防骨髓抑制的药物的用途。
进一步地,所述的药物是治疗和/或预防化学物质导致的骨髓抑制的药物。
进一步地,所述的药物是升高血细胞和/或骨髓造血干细胞的药物。
进一步地,所述的药物是升高外周血白细胞、中性粒细胞、红细胞、血小板和/或血红蛋白的药物。
发明人前期研究发现,地榆苷元存在溶解度低、口服胃肠吸收率小等问题,造成该成分口服生物利用度低,限制了该成分升高血细胞效果的发挥。
发明人经过对剂型及其配方的研究,通过本发明制备的地榆苷元注射剂解决了地榆苷元溶解度低的问题,提高了地榆苷元生物利用度,进而提高其升高血细胞的疗效,对地榆苷元的新剂型开发及更好的临床应用具有十分重要的意义。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
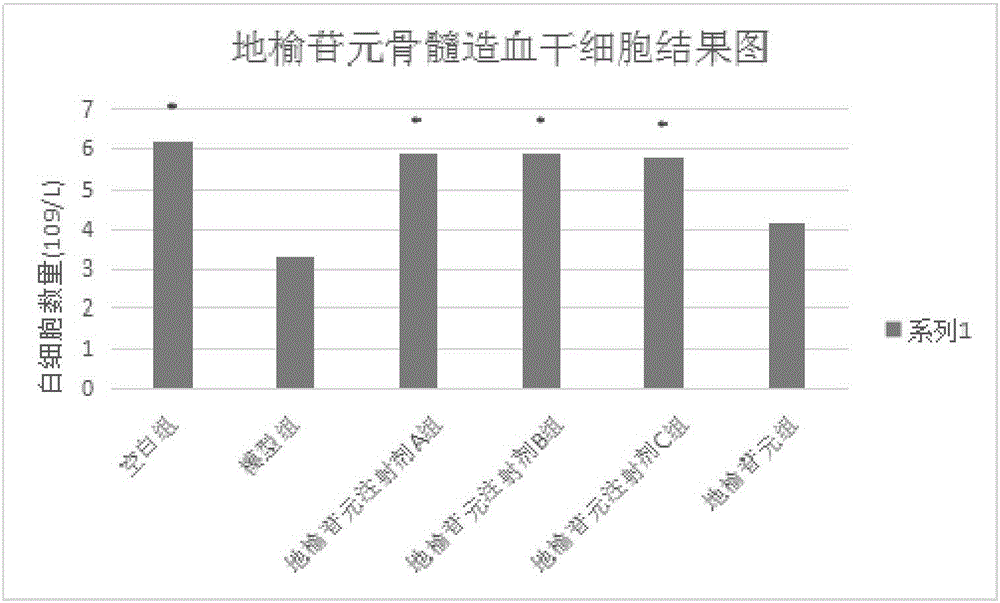
图1为各实验组小鼠骨髓造血干细胞计数比较。
具体实施方式
实施例1本发明注射剂的制备
按下述配比称取原料:
地榆苷元1.5g、吐温80 10g、pH调节剂适量。
制备方法如下:
取地榆苷元分散于10mL注射用水中,加入吐温80、氢氧化钠,调节pH至10,搅拌溶解,再加入注射用水至7500mL使溶液中地榆苷元的浓度为0.2mg/mL,用0.22um微孔滤膜过滤、灭菌,即得本发明注射剂。
实施例2本发明注射剂的制备
按下述配比称取原料:
地榆苷元2.5g、聚氧乙烯蓖麻油EL 60g、pH调节剂适量。
制备方法如下:
取地榆苷元分散于10mL注射用水中,加入聚氧乙烯蓖麻油EL、氢氧化钠,调节pH至10,搅拌溶解,再加入注射用水至12500mL使溶液中地榆苷元的浓度为0.2mg/mL,用0.22um微孔滤膜过滤、灭菌,即得本发明注射剂。
实施例3本发明注射剂的制备
按下述配比称取原料:
地榆苷元10g、泊洛沙姆188 60g、pH调节剂适量。
制备方法如下:
取地榆苷元分散于10mL注射用水中,加入泊洛沙姆188、氢氧化钠,调节pH至10,搅拌溶解,再加入注射用水至50000mL使溶液中地榆苷元的浓度为0.2mg/mL,用0.22um微孔滤膜过滤、灭菌,即得本发明注射剂。
以下通过具体实验证明本发明的有益效果。
实验例1采用不同辅料制备的地榆苷元注射剂的质量评价
本研究根据地榆苷元的性质,选用吐温80、聚氧乙烯蓖麻油EL、泊洛沙姆188、丙二醇、维生素C为辅料,制成地榆苷元注射剂。
制备方法如下:取地榆苷元0.2g分散于100mL注射用水中,分别加入不同的辅料(吐温80、聚氧乙烯蓖麻油EL、泊洛沙姆188、丙二醇、维生素C)、氢氧化钠,调节pH至10,搅拌溶解,再加入注射用水至1000mL使溶液中地榆苷元的浓度为0.2mg/mL,用0.22um微孔滤膜过滤、灭菌,即得本发明注射剂,结果见表1。
热原按《中国药典》(2010年版)热原检查法测定。
澄明度按《中国药典》(2010年版)可见异物检查法项下的灯检法检查。
地榆苷元含量,采用HPLC法测定,色谱条件:Agilent extend-C18色谱柱(250×4.6mm,5μm);流动相:乙腈-0.5%磷酸(70:30)。流速:0.8mL·min-1,柱温:40℃,检测波长:205nm,进样量:10μL。
表1 采用不同辅料制备的地榆苷元注射剂的质量评价
注:与吐温80组比较,*P<0.05。
实验结果:采用本发明辅料吐温80、聚氧乙烯蓖麻油EL、泊洛沙姆188制备的地榆苷元注射剂,热源检查合格,澄明度检查合格,地榆苷元含量测定显示含量较高,表明采用本发明辅料吐温80、聚氧乙烯蓖麻油EL、泊洛沙姆188制备的地榆苷元注射剂符合制剂要求,且最大程度保留地榆苷元成分。其它二种辅料丙二醇、维生素C制备的地榆苷元注射剂,热源检查合格,澄明度检查不合格,地榆苷元含量测定显示含量较低。
实验例2采用不同量辅料制备的地榆苷元注射剂的质量评价
制备方法如下:取地榆苷元0.2g分散于100mL注射用水中,分别加入不同量的增溶剂(吐温80)、氢氧化钠,调节pH至10,搅拌溶解,再加入注射用水至1000mL使溶液中地榆苷元的浓度为0.2mg/mL,用0.22um微孔滤膜过滤、灭菌,即得本发明注射剂,结果见表2。
表2 采用不同量增溶剂制备的地榆苷元注射剂的质量评价
注:与1.0mg组比较,*P<0.05。
实验结果:仅在本发明地榆苷元0.2g和增溶剂用量为1.0mg-60g比例下制备的地榆苷元注射剂热源合格,澄明度符合要求,含量高,制剂最佳,可制备符合要求的地榆苷元注射剂。
实验例3本发明地榆苷元注射剂药效学研究
1实验材料
1.1受试药物本发明地榆苷元注射剂A组(按照实施例1制备)、B组(按照实施例2制备)、C组(按照实施例3制备)、地榆苷元10%DMSO-生理盐水组、环磷酰胺。
1.2实验动物KM-小鼠:18.5~22.5g。
1.3实验仪器:全自动血球分析仪;BS-600L电子天平:规格:600g/0.1g,
上海友声衡器有限公司。
1.4统计方法
用SPSS 17.0软件进行统计分析。数据以均数±标准差表示,组间采用单因素方差分析,方差齐者组间进行LSD检验,方差不齐者进行Tamhane’s T2检验。
2实验方法
2.1实验动物分组及模型制备
所有动物适应性喂养1周后按体重随机分为:空白组;模型组;地榆苷元注射剂A、B、C组,制成2.5mg·kg-1混悬液,临用前配制;地榆苷元组:地榆苷元粉末,用10%DMSO-生理盐水溶解,配制成2.5mg·kg-1混悬液,临用前配制。实验第1天,除空白组外,其余各组小鼠按50mg·kg-1剂量腹腔注射环磷酰胺生理盐水溶液,连续3天,空白组小鼠尾静脉注射等体积生理盐水。
2.2给药
各实验组自实验第1天开始按剂量、给药方式给予相应药物,空白组和模型组小鼠尾静脉注射等体积生理盐水,连续7天。
2.3标本采集
实验第8天,各实验组小鼠眼眶取血,用装有EDTA抗凝剂的0.5mlEP管收集待测。
2.4检测指标及方法
外周血象检测:采用全自动血球计数仪对各实验组小鼠外周血白细胞(WBC)、中性粒细胞(NEUT)红细胞(RBC)、血小板(PLT)、血红蛋白(HGB)进行计数。
骨髓造血干细胞计数(以骨髓细胞CD34+抗原表达量计)用含牛血清白蛋白浓度为0.2%的PBS缓冲液冲出小鼠右侧股骨骨髓细胞,取出106个细胞离心,弃上清,加入30μL正常小鼠血清以封闭非特异结合位点,再加入10μL FITC标记的大鼠抗小鼠CD34+抗体,对照管加入10μL相应对照抗体,4℃避光反应30min。加入2mL红细胞裂解液,作用5min,洗细胞2次,加入终浓度为3μg/mL的PI染液,采用流式细胞仪检测骨髓细胞CD34+抗原表达。
3实验结果
3.1外周血主要血细胞计数比较,见表3、表4。
表3 各实验组小鼠外周血血细胞数量
注:与模型组比较,*P<0.05,**P<0.01;注:与地榆苷元组比较,△P<0.05,△△P<0.01。
结果显示,与模型组比较,地榆苷元注射剂A组、地榆苷元注射剂B组、地榆苷元注射剂C组小鼠造血干细胞数量均有显著升高(P<0.05),地榆苷元组无显著性差异;与地榆苷元组比较,地榆苷元注射剂A组、地榆苷元注射剂B组、地榆苷元注射剂C组小鼠外周血WBC、RBC、PLT数量均有显著升高(P<0.05)。
表4 各实验组小鼠外周血血细胞数量
注:与模型组比较,*P<0.05,**P<0.01;注:与地榆苷元组比较,△P<0.05,△△P<0.01。
结果显示,与模型组比较,地榆苷元注射剂A组、地榆苷元注射剂B组、地榆苷元注射剂C组小鼠外周血NEUT和HGB数量均有显著升高(P<0.05),地榆苷元组无显著性差异;与地榆苷元组比较,地榆苷元注射剂A组、地榆苷元注射剂B组、地榆苷元注射剂C组组小鼠外周血NEUT和HGB数量均有显著升高(P<0.05)
3.2、骨髓造血干细胞计数比较
从图1可知,与模型组比较,本发明地榆苷元注射剂组小鼠造血干细胞数量均有显著升高(P<0.05),地榆苷元组无显著性差异;与地榆苷元组比较,本发明地榆苷元注射剂组小鼠造血干细胞数量均有显著升高(P<0.05)。
以上实验结果表明,本发明地榆苷元注射剂可以有效升高血细胞,药效明显优于直接用地榆苷元原药给药。
综上所述,本发明制备的地榆苷元注射剂解决了地榆苷元溶解度低的问题,提高了地榆苷元生物利用度,进而提高其升高血细胞的疗效,对地榆苷元更好的临床应用具有十分重要的意义。
- 还没有人留言评论。精彩留言会获得点赞!