用于预防宫腔粘连及子宫内膜损伤修复的细胞制剂及其制备方法与流程
本发明属于妇产科学领域,其涉及用于预防宫腔粘连及修复子宫内膜损伤的细胞制剂及其制备方法。
背景技术:
宫腔粘连(intrauterine adhesions,IUA)又称Asherman综合征,是指由创伤、感染等因素造成的子宫内膜基底层细胞的损伤导致子宫腔内粘连组织形成,引起宫腔变形甚至宫腔完全消失,使患者出现月经异常(闭经或月经量减少等)、不孕、流产、早产及周期性腹痛等异常情况。近年来由于频繁的宫腔操作及宫腔镜手术的普及,子宫粘连的发病率和检出率逐渐上升,而且发病年龄呈年轻化趋势,已成为女性继发不孕的第二大病因。尽管临床医生不断寻求新的治疗方案,子宫粘连的治愈率和妊娠率仍无明显改善,且复发率较高(轻度IUA患者治疗后复发率为33.3%,重度IUA患者治疗后复发率更是高达66.7%),由此引起的不孕以及反复流产、早产、前置胎盘、胎盘粘连或植入等产科并发症严重威胁着女性的生殖健康。目前临床上针对IUA的治疗主要是采用宫腔镜下宫腔粘连分离术、术后放置宫内节育器或防粘连材料(主要为透明质酸钠凝胶)以及术后应用雌孕激素治疗,但是以上方法存在着治疗周期长、治愈率低下、粘连易复发、妊娠率低、大剂量雌激素应用会增加患者乳腺和子宫内膜肿瘤风险等问题。此外,对于严重的子宫内膜损伤,该治疗方法并不能解决内膜疤痕问题,且无法实现子宫内膜功能性修复及生育功能的恢复。研究报道采用人羊膜植入治疗IUA可促进子宫内膜生长,抑制纤维化瘢痕的形成,可同样对于重度子宫内膜损伤患者来说,该方法也无法实现子宫内膜功能性修复。子宫腔灌注粒细胞集落刺激因子可使部分内膜薄患者内膜厚度增加,但该方法存在作用时间短,局部疗效差,且无法促进疤痕内膜生长等缺陷。骨髓间充质干细胞治疗宫腔粘连,可以促进子宫内膜组织再生,实现子宫内膜功能性修复,但是单一应用骨髓间充质干细胞存在难于局部定位以及修复不稳定、不彻底等问题。胶原支架复合骨髓或脐带间充质干细胞可以治疗严重子宫内膜损伤,促进疤痕子宫内膜修复,恢复患者生育功能,但是此法也存在的一定的局限性,比如细胞制剂制备方法复杂,细胞获取不方便,细胞获取或细胞制剂应用时对患者造成的痛苦大及创伤大等。
技术实现要素:
本发明所要解决的技术问题是,针对现有技术中细胞获取不便、对患者造成的痛苦大、创伤大及采用单一干细胞存在难于局部定位、修复不稳定、不彻底以及传统宫腔粘连及子宫内膜损伤修复方法无法实现严重子宫内膜再生修复、子宫内膜功能性恢复或作用时间短,局部疗效差等问题,提供一种能够高效预防宫腔粘连及修复严重子宫内膜损伤的混合干细胞制剂及其制备方法。
为了实现上述目的,本发明采用的技术方案是:
一种用于预防宫腔粘连及修复子宫内膜损伤的细胞制剂,所述的细胞制剂由间充质干细胞、人重组基质细胞衍生因子-1α(rhSDF-1α)和用于承载间充质干细胞及rhSDF-1α的透明质酸钠凝胶组成,所述的间充质干细胞为脐带间充质干细胞或胎盘间充质干细胞。
所述的间充质干细胞的来源为人脐带或胎盘;
所述的细胞制剂中,间充质干细胞的浓度为5×106~2×108个/mL;
所述的间充质干细胞为原代-第10代的间充质干细胞;优选地,所述的间充质干细胞为原代-第3代的间充质干细胞。
所述的细胞制剂中,rhSDF-1α的质量浓度为10-150ng/mL;
所述的细胞制剂中,透明质酸钠凝胶的质量浓度为10-100mg/mL;
所述的透明质酸钠凝胶的分子量为400000-1000000;
所述的透明质酸钠凝胶为医用透明质酸钠凝胶。
所述的细胞制剂为混悬液。
所述的细胞制剂的制备方法,其特征在于,包括如下步骤:
1)制备脐带或胎盘间充质干细胞;
2)将所述脐带或胎盘间充质干细胞与rhSDF-1α和透明质酸钠凝胶按比例混合,制得。
所述的脐带间充质干细胞的制备方法,包括如下步骤:
1)取志愿、健康合格孕妇的足月剖宫产的新生儿脐带,充分洗涤去除脐动静脉中的血管;
2)将脐带组织剪成块状,加入胶原酶消化液,37℃恒温摇床中振荡消化,完全培养基(DMEM)和10%胎牛血清(FBS)终止消化;
3)50目筛网过滤人脐带组织消化后的产物;
4)将收集的过滤液离心、分离获得单个核细胞;
5)将离心后获得单个核细胞重悬于完全培养基(DMEM+10%FBS),接种于培养皿中,在37℃,体积分数为5%CO2培养箱中培养;
6)待细胞生长至80-90%融合度时,用胰酶消化进行传代培养,即得脐带间充质干细胞;必要时进行冻存待用。
所述的胎盘间充质干细胞的制备方法,包括如下步骤:
1)取志愿、健康合格孕妇的足月剖宫产胎儿的胎盘,PBS反复冲洗去除胎盘血;
2)将胎盘组织剪成块状,加入胶原酶消化液,37℃恒温摇床中振荡消化,完全培养基(DMEM+10%FBS)终止消化;
3)50目筛网过滤人胎盘组织消化后的产物;
4)将收集的过滤液离心、分离获得单个核细胞;
5)将离心后获得单个核细胞重悬于完全培养基(DMEM+10%FBS),接种于培养皿中,在37℃,体积分数为5%CO2培养箱中培养;
6)待细胞生长至80-90%融合度时,用胰酶消化进行传代培养,即得胎盘间充质干细胞;必要时进行冻存待用。
本发明提供的用于预防宫腔粘连及子宫内膜损伤修复的细胞制剂中,所述细胞制剂中,透明质酸钠凝胶为医用透明质酸钠凝胶,是经CFDA批准可应用于临床妇科及骨科等手术中预防肌腱或宫腔粘连的明质酸钠凝胶。
本发明提供的细胞制剂可局部注射,制剂经注射至病灶部位后,透明质酸钠凝胶可为间充质干细胞提供定植点,且具有缓释作用,联合rhSDF-1α的趋化作用,间充质干细胞制剂可在宫腔内或病灶区缓释、定植和生长,利用三者的协同作用可以发挥更好的疗效。
本发明提供的细胞制剂可局部注射,局部注射部位可为子宫宫底、宫腔内、盘腔内及子宫肌瘤剥除术、剖腹产术以及输卵管复通等术后的吻合口部位。
本发明提供的细胞制剂可用于修复由于各种原因造成的子宫内膜过度损伤,可用于子宫内膜功能性修复和解决内膜疤痕问题以及可用于人流手术、宫腹腔联合手术、剖宫产术及刮宫手术等术后宫腔粘连的预防。
本发明具有如下技术优势:
1)透明质酸钠凝胶是由N-乙酰葡萄糖醛酸反复交替而形成的一种高分子多糖体生物材料,具有高度的黏弹性、可塑性、可降解性以及良好的生物相容性,在预防粘连及修复软组织方面具有明显的作用,其作为间充质干细胞及rhSDF-1α延时缓释载体,不仅为干细胞提供定植点,同时可为干细胞的生长提供合适的三维空间结构及适宜的维环境,在一定程度上可促进干细胞的生长和分泌。此外,透明质酸钠凝胶还具有抗炎、防粘连作用,而且能抑制纤维细胞的渗出,术后宫腔内注入透明质酸钠凝胶,可以起到润滑作用及生物屏障功能,促进组织生理性修复,抑制疤痕形成,从而防止术后再次粘连。
2)rhSDF-1α,其具有趋化作用,可通过其受体CXCR4发挥细胞募集作用。研究表明rhSDF-1α可以动员组织自身干细胞以及外源干细胞归巢,提高损伤部位干细胞浓度,延长干细胞的作用时间,从而达到促进受损子宫内膜再生修复,提高局部疗效。此外,rhSDF-1α可诱导损伤部位血管内皮细胞生长因子(vascular endothelial growth factor,VEGF)表达促进新生血管生成,而新生的血管可使局部血液灌流增加,改善移植细胞的生存环境,提高干细胞的存活,干细胞的存活又能提高其旁分泌作用。
3)脐带或胎盘间充质干细胞作为预防宫腔粘连及修复严重子宫内膜损伤的活性成分,其不仅获取方便,且具有组织再生修复能力及强大的免疫调节功能,能分泌多种生长因子改善局部微环境,促进疤痕子宫内膜再生修复,增加内膜厚度以及局部血管密度等。
4)因此,利用脐带或胎盘间充质干细胞、rhSDF-1α及透明质酸钠凝胶三者的协同作用,可以更好的使干细胞定植在子宫内膜损伤部位,提高干细胞的在损伤部位的浓度,延长干细胞的作用时间,提高局部疗效。三者的协同作用可有效促进疤痕子宫内膜损伤修复,防止术后宫腔再次粘连。
附图说明
图1(a1)为脐带间充质干细胞的形态图;
图1(a2)为脐带间充质干细胞培养至第三代形态图;
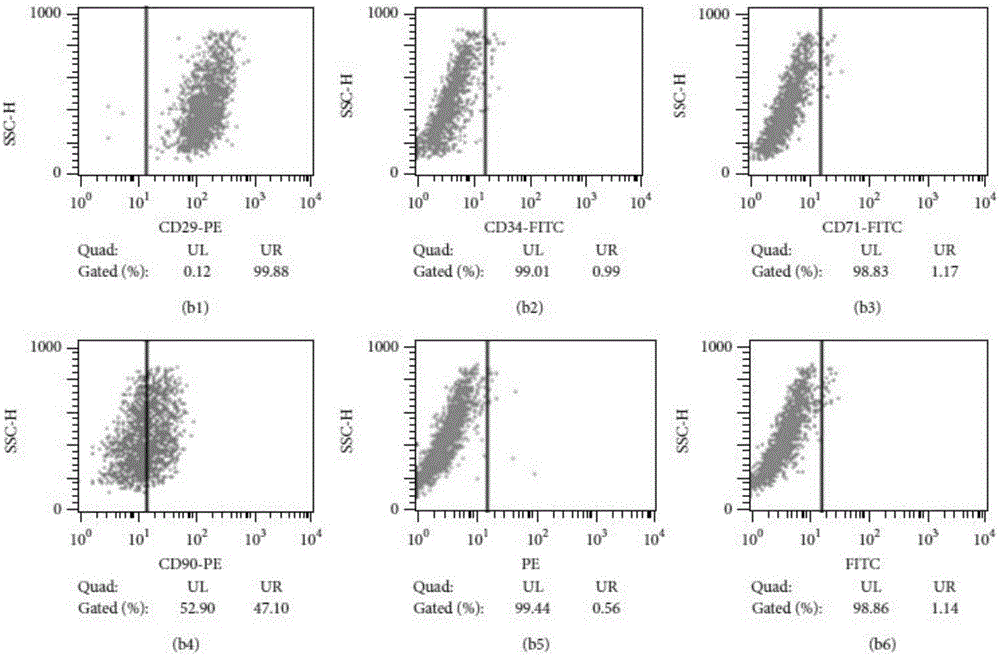
图2(b1-b6)为第三代脐带间充质干细胞的流式细胞分析结果;
图3(c1)为胎盘间充质干细胞的形态图;
图3(c2)为胎盘间充质干细胞培养至第三代形态图;
图4(d1-d6)为第三代胎盘间充质干细胞的流式细胞分析结果;
图5为脐带和胎盘间充质干细胞体外定向诱导分化结果;其中a1为(脐带间充质干细胞成骨细胞诱导前茜素红染色图),a2为(脐带间充质干细胞成骨细胞诱导分化后茜素红染色图),b1为(脐带间充质干细胞成脂肪细胞诱导前油红O染色图),b2为(脐带间充质干细胞成脂肪细胞诱导分化后油红O染色图),c1为(脐带间充质干细胞成软骨细胞诱导前番红O染色图),c2为(脐带间充质干细胞成软骨细胞诱导分化后番红O染色图)),d1为(胎盘间充质干细胞成骨细胞诱导前茜素红染色图),d2为(胎盘间充质干细胞成骨细胞诱导分化后茜素红染色图),e1为(胎盘间充质干细胞成脂肪细胞诱导前油红O染色图),e2为(胎盘间充质干细胞成脂肪细胞诱导分化后油红O染色图),f1为(胎盘间充质干细胞成软骨细胞诱导前番红O染色图),f2为(胎盘间充质干细胞成软骨细胞诱导分化后番红O染色图);
图6A为脐带来源间充质干细胞制剂用于小鼠子宫内膜损伤修复后子宫内膜纤维化面积比变化分析结果;
图6B为胎盘来源间充质干细胞制剂用于小鼠子宫内膜损伤修复后子宫内膜纤维化面积比变化分析结果;
图7A为脐带来源间充质干细胞制剂用于小鼠子宫内膜损伤修复后子宫内膜腺体数量变化分析结果。
图7B为胎盘来源间充质干细胞制剂用于小鼠子宫内膜损伤修复后子宫内膜腺体数量变化分析结果。
具体实施方式
以下结合附图对本发明的优选实施例进行说明,应当理解,此处所描述的优选实施例仅用于说明和解释本发明,并不用于限定本发明。
实施例1制备用于预防宫腔粘连及子宫内膜损伤修复的细胞制剂
本实施例的用于预防宫腔粘连及子宫内膜损伤修复的细胞制剂是由第三代脐带或胎盘间充质干细胞与rhSDF-1α及医用透明质酸钠凝胶所组成的混悬液,且该混悬液中各成分的浓度为脐带或胎盘间充质干细胞的终浓度为5×106个/mL,rhSDF-1α的质量浓度为10ng/mL,透明质酸钠凝胶的质量浓度为10mg/mL,透明质酸钠凝胶的分子量为400000。
其中,上述脐带间充质干细胞是由以下方法制备得到:
取志愿、健康合格孕妇的足月剖宫产的新生儿脐带,PBS反复洗涤后去除脐动静脉中的血管,将脐带组织剪成块状,加入胶原酶消化液,37℃恒温摇床中振荡消化60min后,加入完全培养基(DMEM+10%胎牛血清)终止消化,采用50目筛网过滤人脐带组织消化后的产物,收集过滤液离心、分离获得单个核细胞,将获得的单个核细胞重悬于完全培养基(DMEM+10%胎牛血清),接种于培养皿中,置于37℃,体积分数为5%CO2培养箱中培养,待细胞生长至80-90%融合度时,用胰酶消化进行传代培养,即得脐带间充质干细胞,冻存待用。
其中,上述胎盘间充质干细胞是由以下方法制备得到:
取志愿、健康合格孕妇的足月剖宫产胎儿的胎盘,PBS反复冲洗去除胎盘血,剔除底蜕膜及松散绒毛组织后,将胎盘组织剪成块状,加入胶原酶消化液,37℃恒温摇床中振荡消化60min后,加入完全培养基(DMEM+10%胎牛血清)终止消化,采用50目筛网过滤人胎盘组织消化后的产物,收集过滤液离心、分离获得单个核细胞,将获得的单个核细胞重悬于完全培养基(DMEM+10%胎牛血清),接种于培养皿中,置于37℃,体积分数为5%CO2培养箱中培养,待细胞生长至80-90%融合度时,用胰酶消化进行传代培养,即得胎盘间充质干细胞,冻存待用。
实施例2制备用于预防宫腔粘连及子宫内膜损伤修复的细胞制剂
本实施例的用于预防宫腔粘连及子宫内膜损伤修复的细胞制剂是由第三代脐带或胎盘间充质干细胞与rhSDF-1α及医用透明质酸钠凝胶所组成的混悬液,且该混悬液中各成分的浓度为脐带或胎盘间充质干细胞的终浓度1×107个/mL,rhSDF-1α的质量浓度为80ng/mL,透明质酸钠凝胶的质量浓度为55mg/mL,透明质酸钠凝胶的分子量为700000。
其中,上述脐带间充质干细胞制备方法与实施例1相同。
其中,上述胎盘间充质干细胞制备方法与实施例1相同。
实施例3制备用于预防宫腔粘连及子宫内膜损伤修复的细胞制剂
本实施例的用于预防宫腔粘连及子宫内膜损伤修复的细胞制剂是由第三代脐带或胎盘间充质干细胞与rhSDF-1α及医用透明质酸钠凝胶所组成的混悬液,且该混悬液中各成分的浓度为脐带或胎盘间充质干细胞的终浓度为2×108个/mL,rhSDF-1α的质量浓度为150ng/mL,透明质酸钠凝胶的质量浓度为100mg/mL,透明质酸钠凝胶的分子量为1000000。
其中,上述脐带间充质干细胞制备方法与实施例1相同。
其中,上述胎盘间充质干细胞制备方法与实施例1相同。
实施例4脐带间充质干细胞、胎盘间充质干细胞的细胞表面标志鉴定及体外诱导分化
1)采用倒置显微镜分别观察上述实施例提取培养的脐带间充质干细胞、胎盘间充质干细胞的形态和培养至第三代的脐带间充质干细胞、胎盘间充质干细胞的形态,结果见附图,其中,图1(a1)为脐带间充质干细胞的形态图,图1(a2)为脐带间充质干细胞培养至第三代形态图,图3(c1)为胎盘间充质干细胞的形态图,图3(c2)为胎盘间充质干细胞培养至第三代形态图。
2)将培养至第三代的脐带来源间充质干细胞、胎盘来源间充质干细胞分别进行表面标志检测,脐带来源间充质干细胞的检测结果如图2(b1-b6)所示,胎盘来源间充质干细胞的检测结果如图4(d1-d6)所示。
对于脐带来源间充质干细胞,其表面抗原CD29(99.88%,见图2(b1)),CD34(0.99%,见图2(b2)),CD71(1.17%,见图2(b3)),CD90(47.10%,见图2(b4)),阴性对照PE(0.56%,见图2(b5)),FITC(1.14%,见图2(b6))。
对于胎盘来源间充质干细胞,其表面抗原CD29(99.90%,见图4(d1)),CD34(1.29%,见图4(d2)),CD71(1.21%,见图4(d3)),CD90(80.45%,见图4(d4)),阴性对照PE(0.97%,见图4(d5)),FITC(0.71%,见图4(d6))。
3)脐带、胎盘来源间充质干细胞的体外定向诱导分化结果如图5所示,结果表明脐带或胎盘来源间充质干细胞可以向成骨细胞(a2,d2),成脂肪细胞(b2,e2),成软骨细胞(c2,f2)分化。
实施例5
为了进一步证明本发明提供的用于预防宫腔粘连及子宫内膜损伤修复的细胞制剂的显著效果,将通过以下实验及实验数据进行具体说明。
(1)动物子宫内膜损伤模型的构建
取120只8周龄大的雌性小鼠分为10组,采用双重(感染+机械)损伤法构建子宫内膜损伤模型,即小鼠麻醉后,取下腹部正中长约2cm纵切口进腹,于子宫中下1/3处作0.5cm纵行切口,采用子宫内膜刮勺搔刮中上段子宫腔,当刮勺进出子宫凹凸感消失,四壁感觉粗糙时,停止刮宫,刮宫后宫腔留置脂多糖棉线,缝合腹部切口,48h后取出脂多糖棉线。建模完成后,分别将2mL本发明实施例1-实施例3制备的细胞制剂注射至子宫宫腔内。设置空白对照组(假手术组),仅注射生理盐水(模型)组;仅注射透明质酸钠凝胶组以及仅注射rhSDF-1α组。在小鼠动情3个周期后将小鼠与雄性小鼠进行交配。1个月后取材行HE染色和Masson染色进行子宫内膜组织功能学评估,3个月后行小鼠妊娠结果评估。
结果:术后1个月组织功能学评估显示,与各对照组相比,脐带或胎盘来源间充质干细胞联合rhSDF-1α和透明质酸钠凝胶治疗组的纤维化程度明显减少(图6(A)和(B));与各对照组相比,实施例1-3的实施例中的细胞制剂,脐带或胎盘来源间充质干细胞联合rhSDF-1α和透明质酸钠凝胶治疗组的腺体数量均高于各对照组(图7(A)和(B))。妊娠结果评估显示,脐带或胎盘来源间充质干细胞联合rhSDF-1α和透明质酸钠凝胶组的妊娠率高于各对照组,结果如表1所示。
表1各组小鼠妊娠结果分析
- 还没有人留言评论。精彩留言会获得点赞!