制备环糊精复合物的方法与流程
依据35u.s.c.§119(e),本申请要求2016年1月5日提交的美国临时申请第62/274,962号和2016年12月30日提交的美国非临时申请序号15/395,138的优先权,其内容以全文引用的方式并入本文中。
本申请一般涉及环糊精复合物,更具体地说,涉及制备环糊精复合物的方法,以及相关的系统和产品。
背景技术:
环糊精(例如,环状糊精,环状低聚糖,本文缩写为cd)是由通过α-1,4糖苷键在环中连接的d-吡喃葡萄糖基残基构成的环状结构。在环中结合在一起的葡萄糖分子形成具有疏水内部和亲水外部的中空圆形截头圆锥。这一结构使cd能够在其空腔(例如孔)内容纳客体分子(复合剂)。与各种化学物质形成包合物(复合物)的能力促进cd充当载体以包封、稳定和/或改变客体分子的化学和物理性质(例如,挥发性和溶解性),cd已广泛用于农业、食品、制药和化学行业。通常,αcd、βcd和γcd分别在其环中包括六个、七个和八个吡喃葡萄糖单元。
技术实现要素:
本公开的方法实施例包含制备试剂-环糊精复合物。制备试剂-环糊精复合物包括使包含试剂的第一组合物与多孔环糊精-金属有机骨架接触以形成包含试剂-环糊精-金属有机骨架复合物的第二组合物,所述环糊精-金属有机骨架包括多个环糊精分子和至少一个金属阳离子。制备试剂-环糊精复合物还包括将试剂-环糊精-金属有机骨架复合物溶解在水性溶剂中以形成包括试剂-环糊精复合物的第三组合物。
在一些实施例中,多孔环糊精-金属有机骨架的环糊精分子包括一或多个α环糊精分子、β环糊精分子、γ环糊精分子或其混合物。在一些实施例中,试剂包括一或多种药物、芳香剂、着色剂、调味剂或维生素。在一些实施例中,试剂在25℃下的水溶解度为至多约10mg/ml。在一些实施例中,试剂的平均直径为约10埃或更小、约7埃或更小或约5埃或更小。在一些实施例中,试剂的pka比多孔环糊精-金属有机骨架中存在的碱抗衡离子的pka低至少约10个单位、至少约5个单位或至少约2个单位。
在任何此类实施例中,水性溶剂包括水、水混溶性溶剂或其混合物。任何此类实施例可进一步包括提供含有试剂的第一组合物。在一些此类实施例中,提供第一组合物包括制备试剂的盐。在一些此类实施例中,提供第一组合物包括将试剂溶解于溶剂中。任何此类实施例可进一步包括提供多孔环糊精-金属有机骨架。在一些此类实施例中,提供多孔环糊精-金属有机骨架包括提供固体形式的多孔环糊精-金属有机骨架。在一些此类实施例中,提供多孔环糊精-金属有机骨架包括将多孔环糊精-金属有机骨架溶解在含有金属阳离子或碱的水性溶剂中。
任何此类实施例可进一步包括在溶解试剂-环糊精-金属有机骨架复合物之前干燥第二组合物以形成固体试剂-环糊精-金属有机骨架复合物。在一些实施例中,溶解试剂-环糊精-金属有机骨架复合物包括在试剂和多孔环糊精-金属有机骨架所具有的金属阳离子之间形成盐。任何此类实施例可进一步包括将试剂-环糊精复合物与第三组合物的其它组分分离和/或将金属盐形式的试剂与第三组合物的其它组分分离。
附图说明
当结合附图阅读时,从以下详细描述中最好地理解本公开的实施例。现在参考以下结合附图的描述,其中:
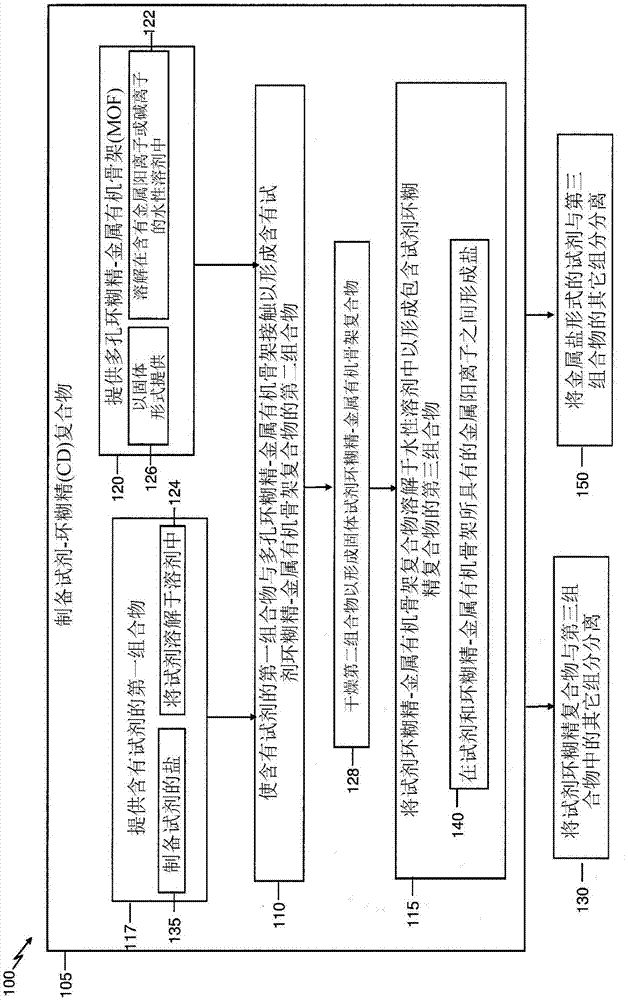
图1显示了本公开的示例性方法的流程图,其包含制备环糊精复合物;
图2显示了含有曲线的图表,其显示:(1)在100mgγcd-mof中10ml水中溶解的水杨酸的百分比与水杨酸的负载百分比(曲线10),和(2)在不存在任何添加剂(如cd-mof)的情况下,基于100mg水杨酸计算的溶解的水杨酸的百分比与加入10ml水中的水杨酸的百分比(曲线11);
图3显示了含有曲线的图表,其显示:(1)在500mgγcd-mof中10ml水中溶解的水杨酸的百分比与水杨酸的负载百分比(曲线20),(2)在不存在任何添加剂(如cd-mof)的情况下,基于500mg水杨酸计算的溶解的水杨酸的百分比与加入10ml水中的水杨酸的百分比(曲线21),和(3)在含有等量γcd和koh的500mg样品中10ml水中溶解的水杨酸的百分比与水杨酸的负载百分比(曲线22);
图4显示了含有曲线的图表,其显示:(1)在100mgγcd-mof中10ml水中溶解的水杨酸的量与水杨酸的负载量(曲线30),(2)在500mgγcd-mof中10ml水中溶解的水杨酸的量与水杨酸的负载量(曲线31),(3)在含有等量γcd和koh的500mg样品中10ml水中溶解的水杨酸的量与水杨酸的负载量(曲线32),和(4)在不存在任何添加剂(如cd-mof)的情况下,10ml水中溶解的水杨酸的量与加入10ml水中的水杨酸的量(曲线33)。
具体实施方式
本公开的实施例得益于意外的发现,即环糊精-金属有机骨架(cd-mof)可用作制备cd复合物(例如,药物cd复合物)的中间体,使得效率显著提高(例如,产率更高),从而显著减少废产物的量并降低生产这种cd复合物的制造成本。
具体来说,本公开得益于我们的发现,即中间试剂-cd-mof复合物可以比通过将试剂和cd一起直接混合形成的试剂-cd复合物的浓度更高的浓度制备。另外,我们发现中间试剂-cd-mof复合物随后可以在水性溶剂中分解,以形成高产量的所需试剂-cd复合物。令人惊讶或反直觉的是,通过将额外的步骤,即形成中间试剂-cd-mof复合物,然后将这一中间复合物分解引入制备方法,可以制备更高产率的试剂cd复合物。
图1显示了本公开的示例性方法100的流程图,其包含制备试剂-环糊精复合物(步骤105)。如图1所示,根据步骤105制备试剂环糊精复合物包括使含有试剂的第一组合物与多孔cd-mof接触以形成含有试剂cd-mof复合物的第二组合物(步骤110)。根据步骤105制备环糊精复合物还包括将试剂cd-mof复合物溶解于水性溶剂中以形成包含试剂cd复合物的第三组合物(步骤115)。即,第三组合物的试剂cd复合物不包括cd-mof的mof组分。
cd-mof可包括一或多个环糊精分子和至少一个金属阳离子。如本文所用,术语环糊精包括α-、β-和γ-环糊精及其衍生物,例如本文式(i)中所描述的那些或其cd混合物。
方法100的实施例可进一步包括提供含有试剂的第一组合物(步骤117)。
如本文所用,例如在本文所述的制备方法中使用的术语试剂可以是任何合适的物质,例如,受益于改善的水溶解度、生物利用度或其它性质的物质,例如具有可适合cd-mof的孔的尺寸的物质。例如,试剂的实施例可以具有约5、7或10埃的平均直径(例如,通过x射线晶体学、尺寸排阻色谱法或相关领域的技术人员熟悉的其它技术确定),使得试剂可分别适合α-、β-和γ-cd-mof的孔。
试剂的合适实施例的实例包括药物、芳香剂、着色剂、调味剂、维生素或其组合。在一些实施例中,试剂可以基本上由这类试剂实施例之一组成,例如99重量%(或在一些实施例中99.9或99.99重量%)的单一药物、芳香剂、着色剂、香料或维生素,除了与试剂形成盐的任选抗衡离子外,仅含有痕量的其它分子或原子。
在一些实施例中,试剂(例如,药物)在室温(25℃)下可以具有低水溶解度。例如,药物的实施例在25℃下的水溶解度可以是至多约10mg/ml(例如,至多约5mg/ml、至多约1mg/ml、至多约0.5mg/ml或至多约0.1mg/ml)和/或至少约0.1μg/ml(例如,至少约0.5μg/ml、至少约1μg/ml、至少约5μg/ml、至少约10μg/ml、至少约50μg/ml、至少约0.1mg/ml、至少约0.5mg/ml或至少约1mg/ml)。
在一些实施例中,试剂(例如,药物)可以是弱酸性的。例如,试剂(例如,药物)的pka可以是至少约1(例如,至少约1.5、至少约2、至少约2.5、至少约3、至少约3.5、至少约4、至少约4.5或至少约5)和/或至多约10(例如,至多约9.5、至多约9、至多约8.5、至多约8、至多约7.5、至多约7、至多约6.5、至多约6、至多约5.5或至多约5)。
在一些实施例中,为了促进形成试剂(例如,药物)的盐形式,可以选择cd-mof的试剂和碱,使得试剂的pka比cd-mof中存在的碱抗衡离子的pka低至少约2个单位(并且在一些实施例中,至少约5个单位或至少约10个单位,例如log10单位)。例如,在一些实施例中,cd-mof可包括pka为约13至14的碱金属碱(例如koh、naoh)。当试剂cd-mof复合物溶解在水性溶剂中时(例如,步骤115),cd-mof被认为分解成其各别组分(例如碱和环糊精),且从而使碱脱离形成试剂的盐形式。例如,碱naoh和对应于乙酰水杨酸(例如,pka约为3.5)或水杨酸(例如,pka约为3)的试剂的药物实施例可分别形成乙酰水杨酸钠和水杨酸钠的离子盐。
可用于本文所述制备方法的试剂的合适药物实施例的非限制性实例包括水杨酸、乙酰水杨酸、布洛芬(ibuprofen)、萘普生(naproxen)、地西泮(diazepam)、氢化可的松(hydrocortisone)、苯妥英(phenytoin)、腺苷和氢氯噻嗪。
可用于本文所述制备方法的试剂的合适芳香剂实施例的非限制性实例包括芳樟醇(linalool)、乙酸苄酯、薄荷醇(menthol)、邻氨基苯甲酸甲酯、柠檬烯(limonene)或其组合。
可用于本文所述制备方法的试剂的合适着色剂实施例的非限制性实例包括花色素苷、类胡萝卜素、姜黄素或其组合。
可用于本文所述制备方法的试剂的合适调味剂实施例的非限制性实例包括乙基麦芽酚(ethylmaltol)、苯甲醛、丁子香酚(eugenol)、乙基香草醛(ethylvanillin)、肉桂醛(cinnamaldehyde)、双乙酰或其组合。
可用于本文所述制备方法的试剂的合适维生素实施例的非限制性实例包括生育酚、抗坏血酸、视黄醇或其组合。
方法100的实施例可以进一步包括提供cd-mof(步骤120)。可用于本文所述制备方法的所提供的cd-mof可包括美国专利第9,085,460号(本文中称为460'专利)中描述的cd-mof,其以全文引用的方式併入本文中。
本文所述制备方法中使用的cd-mof可包括至少一个金属阳离子(例如,多个金属阳离子)和多个环糊精组分(例如本文式(i)中所示的那些)。至少一个金属阳离子一般可与多个环糊精分子或环糊精衍生物配位。cd-mof具有至少一个孔。
可用于cd-mof的合适金属阳离子包括第i族金属阳离子(例如,na+、k+、rb+或cs+)、第ii族金属阳离子(例如,mg2+、ca2+、sr2+或ba2+)和过渡金属阳离子(例如,mn4+、fe3+、co2+、ni2+、cu2+或zn2+)。通过使用盐或碱作为起始物质,可以将金属阳离子包括在cd-mof中。合适的盐的实例包括kf、kcl、kbr、k2co3、k2(偶氮苯-4,4'-二甲酸酯)、na2co3和nabph4。合适的碱的实例包括koh、naoh、rboh和csoh。
本文所述制备方法中使用的cd-mof包括环糊精,即包括以圆环连接的单糖残基的环状寡糖。可用于cd-mof的合适的环糊精包括例如α-、β-和γ-环糊精及其衍生物。在460'专利中公开了可用于在环糊精中形成结构单元的α-1,4-连接的d-吡喃葡萄糖基残基的实例结构和γ-环糊精环的结构。如相关领域的技术人员所理解的,环糊精可以通过可再生来源(例如淀粉)的酶促降解来大量生产。
本文所述制备方法中使用的cd-mof可以通过将环糊精组分(例如,γ-环糊精)和含金属的组分(例如,金属盐如kcl)或含有金属阳离子的碱(例如koh)溶解(步骤122)在其中两者都具有良好溶解性(例如,在水中10mg/ml或更大)的水性溶剂(例如水)中来制备(例如,作为步骤120的一部分)。例如,α-、β-和γ-cd的一些实施例可以分别在水中具有约145、18和232mg/ml的溶解度。cd-mof复合物的分离(例如,作为步骤120的一部分)可以通过添加不良溶剂来实现,其中上述组分中的任一种具有差的溶解度(例如,在水中小于10mg/ml)。合适的不良溶剂实例包括c1-c18醇(例如甲醇)、丙酮、四氢呋喃、二噁烷、乙腈或其混合物。
在一些实施例中,本文所述制备方法中使用的cd-mof可如下制备(例如,作为步骤120的一部分提供)。在环境温度和压力下,γ-cd可以溶解在含有碱金属阳离子(例如k+)的水溶液中,然后蒸汽扩散水混溶性溶剂(例如甲醇)以形成毫米大小体心的立方晶体结构。
在不通过理论考虑限制本公开的范围的情况下,认为γ-cd环可以采用立方体的面,其一级(1°)面(例如,c6羟基(oh)基团)指向立方体内部并且其二级(2°)面(例如,c2和c3oh基团)向外指向。此外,据信γ-cd环通过碱金属阳离子与一级c6oh基团和糖苷环氧原子的配位而连接在一起。通过使更多的碱金属阳离子与γ-cd环的二级面的c2和c3oh基团配位,各个立方体可以包装以形成体心立方晶体。这种cd-mof几何结构的非限制性实例公开在460'专利中。
cd-mof的实施例包括cd组分和含金属的组分。含金属的组分可具有式mn,其中m可为第i族、第ii族金属或过渡金属,n可为有机或无机、单价或多价阴离子。非限制性合适的无机阴离子包括氯离子、氟离子、氢氧根、硫离子、亚磺酸根、碳酸根、铬酸根以及氰离子。合适的有机阴离子包括例如苯甲酸根、偶氮苯-4,4'-二甲酸根、乙酸根和草酸根。cd-mof的cd组分可以是式(i)的化合物:
其中n=0-10;r选自由以下组成的组:-oh;-nr'r";任选地经一个、两个、三个、四个或五个r1基团取代的c1-c18烷基;任选地经一个、两个、三个、四个或五个r1基团取代的c2-c18烯基;任选地经一个、两个、三个、四个或五个r1基团取代的c2-c18炔基;任选地经一个、两个、三个、四个或五个r1基团取代的c1-c18烷氧基;-s(=o)2r';-s(=o)or';-s(=o)r';-c(=o)or';-cn;-c(=o)r';-sr'、-n=n+=n-;-no2、-oso2r';-c(=o)or';-o(=s)sr';-p(=o)(or')2;-op(=o)(or')2;-p(=o)(or')r";-n=r'r";-nr'p(or")(or”');-oc(=o)nr'r";任选地经一个、两个、三个、四个或五个r2基团取代的芳基;任选地经一个、两个、三个、四个或五个独立地选自r2基团的基团取代的杂芳基;和任选地经一个、两个、三个、四个或五个独立地选自r2基团的基团取代的环烷基;每个r1基团独立地选自由以下组成的组:羟基、卤基、c1-c6烷氧基、-nr'r";-s(=o)2r';-s(=o)or';-s(=o)r';-c(=o)or';-cn;-c(=o)r';-sr'、-n=n+=n-;-no2、-oso2r';-c(=o)or';-o(=s)sr';-p(=o)(or')2;-op(=o)(or')2;-p(=o)(or')r";-n=r'r";-nr'p(or")(or”');-oc(=o)nr'r";任选地经一个、两个、三个、四个或五个r'基团取代的芳基;任选地经一个、两个、三个、四个或五个独立地选自r'基团的基团取代的杂芳基;和任选地经一个、两个、三个、四个或五个独立地选自r'基团的基团取代的环烷基;每个r2基团独立地选自由以下组成的组:c1-c6烷基、c2-c6烯基、c2-c6炔基、羟基、卤基、c1-c6烷氧基、-nr'r";-s(=o)2r';-s(=o)or';-s(=o)r';-c(=o)or';-cn;-c(=o)r';-sr'、-n=n+=n-;-no2、-oso2r';-c(=o)or';-o(=s)sr';-p(=o)(or')2;-op(=o)(or')2;-p(=o)(or')r";-n=r'r";-nr'p(or")(or”');-oc(=o)nr'r";任选地经一个、两个、三个、四个或五个r'基团取代的芳基;任选地经一个、两个、三个、四个或五个独立地选自r'基团的基团取代的杂芳基;和任选地经一个、两个、三个、四个或五个独立地选自r'基团的基团取代的环烷基;;并且其中每个r'、r"和r”'独立地选自由h、c1-c6烷基和芳基组成的组。式(i)化合物的实例包括α-、β-和γ-环糊精。
如本文所用,术语“烷基”是指直链或支链烷基。实例包括但不限于甲基、乙基、丙基、异丙基、正丁基、仲丁基、叔丁基、戊基、2-戊基、异戊基、新戊基、己基、2-己基、3-己基和3-甲基戊基。每个烷基可任选地经一个、两个或三个取代基取代,如卤素、环烷基、芳基、烯基或烷氧基。
如本文所用,术语“低碳烯基”是指具有一个或两个双键的直链或支链烃基,包括例如乙烯基、丙烯基、1-丁-3-烯基、1-戊-3-烯基以及1-己-5-烯基。烯基还可以任选地经例如卤基、芳基、环烷基或烷氧基单取代、二取代或三取代。
如本文所用,术语“炔基”是指具有一个或两个三键的直链或支链烃基,包括例如丙炔基和1-丁-3-炔基。炔基还可以任选地经例如卤基、芳基、环烷基或烷氧基单取代、二取代或三取代。
如本文所用,术语“烷氧基”是指-o-烷基,其中烷基如上文所定义。
如本文所用,术语“卤基”或“卤素”是指氟、氯、溴或碘的卤素基团。
如本文所用,术语“芳基”是指具有单环(例如苯基)、多环(例如联苯)或其中至少一个是芳族的多个稠合环(例如1,2,3,4-四氢萘基)的芳族碳环基团。
如本文所用,术语“杂芳基”是指含有至少一个和至多四个杂原子(例如,氮、氧或硫)的5、6或7元环的一个芳环或多个稠合芳环系统。实例包括但不限于呋喃基、噻吩基、吡啶基、嘧啶基、苯并咪唑基和苯并噁唑基。
如本文所用,术语“环烷基”是指具有单环(例如环己基)、多环(例如双环己基)或多个稠合环(例如十氢萘基)的碳环基团。另外,环烷基可以具有一或多个双键。
在一些实施例中,本文所述制备方法中使用的第一组合物可包括其中溶解有试剂的溶剂(例如,步骤124)。溶剂可以是有机溶剂,如烷烃(例如己烷和矿物油)、醇(例如,c1-c18醇,如甲醇、乙醇、异丙醇或丙二醇)、酮(例如丙酮)、酯(例如乙酸乙酯)、醚(例如乙醚、二醇醚、四氢呋喃或二噁烷)、腈(例如乙腈)及其混合物。
在一些实施例中,本文所述制备方法中使用的cd-mof(例如,作为步骤120的一部分提供)可以固体形式(步骤126)提供,例如晶体或粉末。在此类实施例中,尽管不通过理论考虑限制本公开的范围,但据信使含有试剂的第一组合物与cd-mof接触(例如,步骤110)可将试剂分子负载到cd-mof的孔中,从而形成含有试剂cd-mof复合物的第二组合物。在一些此类实施例中,试剂cd-mof复合物中的试剂可以与cd-mof形成配位键(例如,共享电子对的共价键,其中两个电子都来自cd-mof的相同原子)。在一些此类实施例中,试剂cd-mof复合物的试剂可以通过其它分子间相互作用(例如,氢键、疏水相互作用或范德华力)固定在cd-mof的孔中,而不与cd-mof形成任何配位键。
在一些实施例中,可以通过任何合适的方法(例如,通过空气、真空或加热)干燥(步骤128)如本文所述形成的第二组合物(例如步骤110),以形成固体试剂cd-mof复合物并除去第二组合物的其它组分(例如,用于在步骤122中溶解试剂和/或作为步骤120的一部分溶解cd-mof的溶剂。
如上所述,形成含有试剂cd复合物的第三组合物(例如,作为步骤115的一部分)包括将试剂cd-mof复合物溶解在水性溶剂中。在一些实施例中,水性溶剂可包括水、水混溶性溶剂(例如乙醇,或水乙醇混合物)。
虽然本公开的范围不受理论考虑因素限制,但相信当试剂cd-mof复合物溶解在水性溶剂(例如水)中时,cd-mof分解并产生游离的环糊精和金属阳离子以及相应的阴离子。此外,相信当试剂cd-mof在水性溶剂中分解时,通过使用cd-mof作为形成第三组合物的中间体促进试剂分子紧邻游离环糊精和/或金属阳离子,例如,借助于位于cd-mof的孔中。例如,cd-mof孔中的试剂分子可以在环糊精环和/或cd-mof的金属阳离子的约10埃内。进一步相信,试剂与游离环糊精和/或金属阳离子的这种紧密接近可促进试剂cd复合物和/或盐形式的试剂的形成,从而显著提高制备试剂cd复合物(例如,药物cd复合物)和/或试剂的盐形式的效率(例如,产率)。
尽管本公开的范围不受理论考虑因素限制,但相信对于所述方法的一些实施例,与在不使用cd-mof作为中间体的情况下直接在水性溶剂中混合试剂和相应的cd相比,可以更有效地以较高产率制备试剂cd复合物。例如,相信,与以cd-mof形式使用相同量的成分(例如,相同量的试剂和cd)时相比,第三组合物中的试剂cd复合物的量可以比通过在水性溶剂中直接混合试剂和相应的cd制备的组合物中试剂cd复合物的量显著更高的量制造。
在一些实施例中,制备方法100可以进一步包括将试剂cd复合物与第三组合物中的其它组分分离(例如,步骤130)。在一些实施例中,例如,可以通过使用柱色谱、过滤和/或离心分离试剂cd复合物。
在一些实施例中,所述方法可以进一步包括制备盐形式的试剂(例如药物)(步骤135)。例如,在步骤110中,方法100可包括使含有药物的第一组合物与多孔环糊精-金属有机骨架(cd-mof)接触以形成含有药物cd-mof复合物的第二组合物。cd-mof可包括多个环糊精分子和至少一个金属阳离子。药物可为酸性并且pka为至少约1。在此类实施例中,药物和cd-mof可以具有上述性质和/或特征。例如,第一组合物可以固体形式(例如,晶体或粉末,如在步骤120中提供的)接触cd-mof以形成第二组合物。
在一些实施例中,含有试剂(例如药物)的第一组合物可以进一步包括溶剂(例如上文在步骤124的上下文中描述的有机溶剂),例如,其中药物可以在负载到cd-mof上之前溶解以形成药物cd-mof复合物。
在一些实施例中,作为步骤128的一部分的方法100可以进一步包括干燥第二组合物(例如,通过从第二组合物中除去溶剂)以形成固体试剂(例如药物)cd-mof复合物。干燥可通过任何合适的手段进行。
在一些实施例中,作为步骤115的一部分的方法100可以进一步包括将固体试剂cd-mof复合物(例如,在干燥步骤128之后)溶解在水性溶剂中以形成(例如,步骤140)含有盐形式的试剂(例如,盐形式的药物)的第三组合物,其中在试剂和多孔cd-mof所具有的金属阳离子之间形成盐(例如,作为步骤120的一部分)。
在一些实施例中,方法100可以进一步包括将盐形式的药物与第三组合物的其它组分(例如cd和mof组分)分离(步骤150)。在一些实施例中,可以通过使用结晶、溶剂萃取和/或柱色谱分离盐。
制备上述试剂(例如药物)盐形式的方法可用于制备某些试剂的盐形式(例如,具有相对低水溶解度的那些),并且其盐以其它方式难以以高产率制备。例如,某些药物的盐形式可能比与相应的游离酸或碱结合形成盐具有更大的吸水倾向。在这种情况下,这些药物的盐形式比药物本身更不稳定且更具吸湿性,使得它们不易处理并且保质期短。作为另一实例,某些化合物如氢氧化钾是如此吸湿,以至于它们可以溶解在潮湿空气中。
例如,用氢氧化钾形成某些试剂(例如阿司匹林等药物)的盐形式可能是困难的。然而,使用cd-mof作为中间体可以促进形成稳定的药物cd-mof复合物,其可以储存相对长的时间段(例如,数周或数月)。例如,药物cd-mof复合物可用于促进在使用盐形式的药物(例如,施用给患者)之前立即制造药物的盐形式(例如,通过在水性溶剂中添加药物cd-mof复合物)。例如,当药物cd-mof复合物(例如,负载阿司匹林的cd-mof)在水中溶解时,复合物可以分解形成药物、cd和用于形成cd-mof的金属阳离子,使得药物可以与金属阳离子(例如,氢氧化钾中的钾阳离子)反应形成药物的盐,因为药物和药物cd-mof复合物中的金属阳离子非常接近(例如,在cd-mof的孔中)。据信这种方法可以通过将这类化合物储存在药物cd-mof复合物中来帮助克服与某些化合物(例如氢氧化钾)相关的吸湿问题。
在一些实施例中,本文所述的制备方法可用于提高试剂负载于cd中的效率。当试剂是药物时,本文所述的制备方法也可用于提高药物的生物利用度。在一些实施例中,本文所述的制备方法可用于在使用试剂之前立即制备试剂cd复合物或试剂的盐形式。在此类实施例中,可以显著改善试剂的保质期。
在下面的实例中说明了本发明的一些非限制性方面,以证明第三组合物中试剂cd复合物的量可以比当使用相同量的成分时但不使用多孔cd-mof作为中间体,通过在水性溶剂中混合试剂和cd制备的组合物中试剂cd复合物的量高多少。
cd-mof的实例制备
按照如美国专利第9,085,460号中所描述的类似程序制备cd-mof晶体。具体地,cd-mof晶体通过甲醇蒸汽扩散到γ-环糊精和氢氧化钾的水溶液中而生长。使晶体生长约1至2周的时间,然后收集晶体,过滤,用甲醇洗涤,接着在真空室中在室温下抽真空至约10-3托,持续24小时。随后cd-mof晶体不经进一步纯化即用于以下实验中。
试剂cd-mof复合物的实例制备
为了通过使用cd-mof测量药物水溶解度的增加,使用水杨酸(弱酸性药物)作为实例并以特定的负载重量百分比负载到上面制备的cd-mof中。具体地,首先将水杨酸以1g/10ml乙醇溶解在乙醇中。以下不同样品中使用的水杨酸溶液的量基于目标负载重量百分比。例如,为了达到10%重量的负载,将10mg水杨酸负载到100mgcd-mof样品中。在用水杨酸乙醇溶液负载cd-mof样品后,干燥样品以蒸发乙醇,留下负载有水杨酸的干燥γcd-mof粉末。
随后将干燥的负载cd-mof样品溶解于10ml水中并搅拌。测量从溶液中取出的等分试样的uv-vis光谱,以确定溶解在水溶液中的水杨酸的量。
我们相信当水杨酸负载到cd-mof样品中时,药物分子扩散并位于cd-mof晶体的内部孔隙空间内。当负载的cd-mof晶体溶解在水中时,cd-mof断裂并产生游离的环糊精、钾离子和氢氧根离子。据信,通过使用cd-mof作为中间体,水杨酸分子可以在水中紧邻环糊精和氢氧化钾分子。
因此,我们认为,与不使用cd-mof的常规方法相比,通过这种方法形成的水杨酸可以更易溶于水,原因至少有两个:1)水杨酸分子可以更容易与环糊精分子形成包合物,因为它们非常接近,和2)水杨酸可以更容易与氢氧化钾反应形成更易溶的盐形式(即水杨酸钾),因为它们非常接近。对于低负载百分比,认为溶解在水中的水杨酸的量可以相对较高,因为存在足够多的环糊精和氢氧化钾分子以形成复合物或与水杨酸反应。然而,据信,随着负载百分比的增加,水杨酸分子的量最终可超过可用的环糊精和/或氢氧化钾的量,从而留下未复合和未反应的水杨酸。据信,由于这种未复合和未反应的水杨酸在水中的溶解性较小,因此溶解的水杨酸的总量将达到最大值。
下面图2-4中所示的所有水溶解度都是在室温下测量的。作为参考,在通过在水中加入适量的水杨酸而没有任何添加剂制备的样品中和在通过在含有γcd和koh的水溶液中加入适量的水杨酸制备的样品中,比较水杨酸的水溶解度。
图2显示了含有曲线的图表,其显示(1)在100mgγcd-mof中10ml水中溶解的水杨酸的百分比与水杨酸的负载百分比(曲线10),和(2)在不存在任何添加剂(如cd-mof)的情况下,基于100mg水杨酸计算的溶解的水杨酸的百分比与加入10ml水中的水杨酸的百分比(曲线11)。例如,在x轴中,曲线10中的500%表示负载在100mgcd-mof样品中的500mg水杨酸。对于曲线11,x轴上的500%表示在没有任何cd-mof的情况下添加到10ml水中的500mg水杨酸。
如图2中的曲线10和11所示,当使用100mgcd-mof样品时,10ml水中溶解的水杨酸的百分比在约25-500%(特别是约25-300%)的负载百分比范围内高于在不存在任何添加剂(例如cd-mof)的情况下10ml水中溶解的水杨酸的百分比。
图3显示了含有曲线的图表,其显示(1)在500mgγcd-mof中10ml水中溶解的水杨酸的百分比与水杨酸的负载百分比(曲线20),(2)在不存在任何添加剂(如cd-mof)的情况下,基于500mg水杨酸计算的溶解的水杨酸的百分比与加入10ml水中的水杨酸的百分比(曲线21),和(3)在含有等量γcd和koh的500mg样品中10ml水中溶解的水杨酸的百分比与水杨酸的负载百分比(曲线22)。用于获得曲线22的γcd和koh的量与用于制备曲线20中的γcd-mof的γcd和koh的量相同。例如,在x轴中,曲线20或曲线22中的100%表示500mgcd-mof样品或含有γcd和koh的500mg样品中负载的500mg水杨酸。对于曲线21,x轴上的100%表示在没有任何cd-mof的情况下添加到水中的100mg水杨酸。
如图3所示,当使用500mgcd-mof样品时,10ml水中溶解的水杨酸的百分比(曲线20)在10-100%的整个测试负载百分比中显著高于在不存在任何添加剂的情况下10ml水中溶解的水杨酸的百分比(曲线21)和在存在含有等量γcd和koh的500mg样品的情况下10ml水中溶解的水杨酸的百分比(曲线22)。例如,如图3所示,当将30%水杨酸负载到500mgcd-mof样品中时,150mg水杨酸负载到cd-mof粉末中,约69%(或约103mg)水杨酸溶解于10ml水中。此溶解度远高于:(1)在不存在cd-mof的情况下未复合的水杨酸在水中的溶解度,其在室温下在10ml水中约为13%(或约20mg)和(2)将水杨酸直接加入含有等量γcd和koh的溶液中的溶解读,其在室温下在10ml水中约为39%(或约58.5mg)。也就是说,图3显示使用cd-mof作为中间体可以形成水杨酸cd复合物,其效率远高于通过将水杨酸直接加入含有等量cd和koh的溶液中形成水杨酸cd复合物,并且与在无任何添加剂的情况下在水中加入水杨酸或在含有γ等量cd和koh的水溶液中加入水杨酸相比,可以显著提高水杨酸在水中的溶解度。
图4显示了含有曲线的图表,其显示:(1)在100mgγcd-mof中10ml水中溶解的水杨酸的量与水杨酸的负载量(曲线30),(2)在500mgγcd-mof中10ml水中溶解的水杨酸的量与水杨酸的负载量(曲线31),(3)在含有等量γcd和koh的500mg样品中10ml水中溶解的水杨酸的量与水杨酸的负载量(曲线32),和(4)在不存在任何添加剂(如cd-mof)的情况下,10ml水中溶解的水杨酸的量与加入10ml水中的水杨酸的量(曲线33)。
如图4中的曲线33所示,在不存在任何添加剂的情况下溶解在10ml水中的水杨酸的量达到约20mg的最大值。相反,曲线30和31表明,使用cd-mof作为中间体可显著增加水杨酸在水中的溶解度(例如,当使用500mgcd-mof样品时,高达约110mg)。此外,曲线31和曲线32表明,与将水杨酸直接加入含有等量cd和koh的水溶液相比,使用cd-mof作为中间体可显著增加水杨酸在水中的溶解度,这表明前一种方法可以高得多的效率形成水杨酸cd复合物。
本申请所涉及领域的技术人员将理解,可以对所描述的实施例进行其它和进一步的添加、删除、替换和修改。
- 还没有人留言评论。精彩留言会获得点赞!