一种用于气管软组织修复的纤维膜及其制备方法与流程
本发明属于生物医学工程
技术领域:
,特别是气管软组织修复材料制备
技术领域:
,公开了一种用于气管软组织修复的纤维膜及其制备方法。
背景技术:
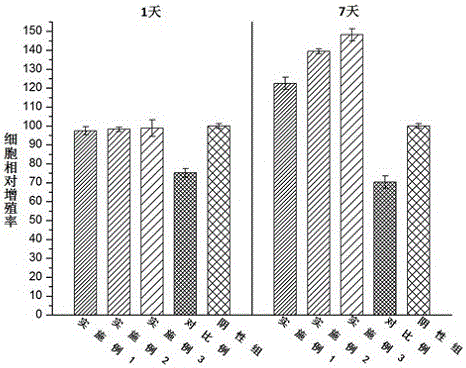
:临床上若遇气管肿瘤、甲状腺及其他部位肿瘤侵袭气管,以及气管的先天性或创伤性原因导致气管严重狭窄时,均需行气管的切除与重建。由于气管特殊的生理结构,决定气管移植成功的关键因素包括移植物的血管化,免疫排斥以及组织细胞的再生等问题。理想的气管替代物应具备以下特征:为了保证颈部活动性不受限制,气管必须容易弯曲但不致塌陷;为了满足通气功能和防止纵隔感染,管腔必须密闭不漏气;内壁光滑,防止成纤维细胞和细菌的侵入;其次,要有利于气管黏膜上皮生长,使其具有清洁气道的功能;更重要的一点是,要有良好的组织相容性。组织工程气管能够修补因创伤、肿瘤、炎症等引起的气管缺损。由于软骨缺乏再生能力,病损后难以自身修复,必须利用其他组织或替代材料进行修复与重建。在近20年中,组织工程领域已旨在恢复或更换损坏或丢失组织和器官。组织工程化气管需要对于结构,机械和功能的组织。气管的良性或恶性病变往往需要广泛的气管重建。用于气管置换方式已经被报道,包括使用自体的组织、自体移植同种异体移植物、假体材料或这些方法的组合。但是这些方法中,往往会出现气管狭窄、纤维化、细菌感染及免疫排斥、材料失效,导致气管替代物进行移植失败。再者一些的组织工程气管的生物相容性低,降解性能差也是限制组织工程气管在临床上的进一步应用。重组转化生长因子-β3(rhTGF-β3),是胚胎无瘢痕愈合反应中重要的细胞因子。有人很早就发现了早期胚胎的无瘢痕愈合现象并比较了无瘢痕愈合和瘢痕形成的细胞和分子机制。重组转化生长因子-β3(rhTGF-β3)在伤后修复过程中最初的形态发生,随后的细胞增殖及最终的组织重建中起着重要的作用。重组转化生长因子-β3(rhTGF-β3)经过了大量的多中心的对照和前瞻性临床试验,证实其在多种外科手术中能有效地减少瘢痕,临床试验证实了重组人TGFβ3的安全性、有效性以及改善瘢痕外观方面的作用。技术实现要素:本发明的目的在于针对现有的气管组织修复材料应用后会出现气管狭窄、纤维化、免疫排斥、材料失效,导致气管替代物进行移植失败,和其生物相容性和可降解性能低等不足,提供一种用于气管软组织修复的纤维膜及其制备方法,该气管软组织修复纤维膜免疫原性低,材料来源丰富,具有良好的生物相容性和可降解性能,且具有诱导软组织修复能力和能抑制受损气管纤维化的出现。为实现上述目的,本发明的技术方案为:所述一种用于气管软组织修复的纤维膜为核-壳多孔网状结构,由聚己内酯、Ⅰ型胶原、重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)组成。进一步的,所述一种用于气管软组织修复的纤维膜按重量份数计由以下成分组成:聚己内酯10份;Ⅰ型胶原10份;重组转化生长因子-β3(rhTGF-β3)0.01-0.05份;牛血清蛋白(BSA)0.05-0.1份。优选的,所述的聚己内酯的分子量为8×105Da,所述的Ⅰ型胶原的分子量为1×105Da,所述的重组转化生长因子-β3(rhTGF-β3)其分子量为25kDa。进一步的,所述一种用于气管软组织修复的制备方法,其制备方法通过以下步骤实现:一、纤维膜材料的制备、二、气管软组织修复纤维膜的纺丝。进一步的,所述纤维膜材料的制备具体步骤为:(1)壳层材料制备:将聚己内酯和Ⅰ型胶原按质量比4:1溶于六氟异丙醇搅拌12小时,配制成质量浓度为12%的聚己内酯/Ⅰ型胶原的混合溶液,然后超声处理30min去除搅拌时产生的气泡,制得壳层材料混合溶液;(2)核层材料制备:S1:将重组转化生长因子-β3(rhTGF-β3)加入到磷酸盐缓冲液中轻柔搅拌1h配置成浓度为40μg/mL的rhTGF-β3溶液;S2:将牛血清蛋白(BSA)加入到磷酸盐缓冲液中轻柔搅拌1h配置成浓度为200μg/mL的BSA溶液;S3:然后将S1制得的浓度为40μg/mL的rhTGF-β3溶液和S2制得的浓度为200μg/mL的BSA溶液等体积混合,配制成rhTGF-β3/BSA的混合溶液;S4:将Ⅰ型胶原溶于去离子水配成质量浓度为20%的Ⅰ型胶原溶液;S5:将S4制得的质量浓度为20%的Ⅰ型胶原溶液和S3中制得的rhTGF-β3/BSA的混合溶液等体积混合,制得核层材料混合溶液。更进一步的,所述气管软组织修复纤维膜的纺丝具体步骤如下:S1:将所述壳层材料混合溶液和所述核层材料混合溶液分别加到同轴静电纺丝设备中的壳层材料注射器和核层材料注射器中,静置30-60min至排尽所述壳层材料注射器和核层材料注射器的空气;S2:调节辊筒接收器和同轴喷头间的距离为15-20cm,调节高压电源至15~20kV,调节载有壳层材料注射器的微量注射泵的输出速度调节至1mL/h,调节载有核层材料注射器的微量注射泵的输出速度至0.2mL/h,辊筒接收器的转速控制在200~350rpm;S3:待核层材料完全输出后,结束纺丝,从收集装置上取下纺丝膜,即得一种用于气管软组织修复的纤维膜。优选的,所述的同轴静电纺丝装置由高压电源,壳层材料注射器,核层材料注射器,微量注射泵,收集装置,喷射头和辊筒接收器。更进一步的,所述同轴喷射头内孔径为0.5mm,所述同轴喷射头外孔径为0.8mm。本发明通过以聚己内酯和Ⅰ型胶原为基质,以重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)为生物活性成分,通过同轴静电纺丝技术,制备出一种具用核-壳多孔网状结构的纤维膜,该种修复纤维膜具有良好的三维网状结构和生物相容性有利于细胞的在其表面黏附和生长,而且由于其具有核-壳结构,能有效解决重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)制备时容易失效的问题,且能使该种修复纤维膜具有缓释功能,可以缓慢持续释放出重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)至受损部位,能有效地促进损伤部位的愈合和抑制纤维化的出现。而该种修复纤维膜所采用的基质为生物可降解材料,可以在组织修复完成后降解成对人体无害的小分子随人体循环排除体外。本发明的有益效果为:(1)本发明通过同轴静电纺丝技术,制备出一种具用核-壳多孔网状结构的纤维膜,该种修复纤维膜具有良好的三维网状结构利于细胞的在其表面黏附和生长,从而加快新生组织的生长。而且由于其具有核-壳结构,能有效解决重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)在制备时容易失效和负载率低的问题,且能使该种修复纤维膜具有缓释功能,可以缓慢持续释放出重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)至受损部位,能有效地促进损伤部位的愈合和抑制纤维化的出现;(2)本发明通过以重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)为核层材料,赋予所制得的修复纤维膜具有促进受损部位愈合的作用。重组转化生长因子-β3(rhTGF-β3)可以通过减少炎症细胞聚集和结缔组织沉积减少瘢痕,拮抗TGFβ1和TGFβ2的作用,使伤口修复过程中的胶原合成与分解处于平衡状态,既能保证伤口的愈合,又不致瘢痕过度。此外,重组转化生长因子-β3(rhTGF-β3)能促进间充质干细胞的分化,而牛血清蛋白(BSA)在能为间充质干细胞的生长和分化提高营养外,还能作为保护剂保护重组转化生长因子-β3(rhTGF-β3)延长其在人体内的半衰期。附图说明图1为实施例4中的rhTGF-β3体外释放评价实验结果图;图2为实施例5中的与间充质干细胞(MSCS)培养1天和7天后细胞毒性评价结果图。具体实施方式下面结合实施例对本发明的技术方案做进一步的说明。实施例1一种用于气管软组织修复的纤维膜,所述用于气管软组织修复的纤维膜为核-壳多孔网状结构,由聚己内酯、Ⅰ型胶原、重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)组成组成;所述用于气管软组织修复的纤维膜按重量份数计由聚己内酯10份、Ⅰ型胶原10份、重组转化生长因子-β3(rhTGF-β3)0.01份和牛血清蛋白(BSA)0.05份组成;所述的聚己内酯的分子量为8×105Da,所述的Ⅰ型胶原的分子量为1×105Da,所述的重组转化生长因子-β3(rhTGF-β3)的分子量为25kDa。上述用于气管软组织修复的纤维膜,其制备方法的具体步骤如下:一、纤维膜材料的制备:(1)壳层材料制备:将聚己内酯和Ⅰ型胶原按质量比4:1溶于六氟异丙醇搅拌12小时,配制成质量浓度为12%的聚己内酯/Ⅰ型胶原的混合溶液,然后超声处理30min去除搅拌时产生的气泡,制得壳层材料混合溶液;(2)核层材料制备:S1:将重组转化生长因子-β3(rhTGF-β3)加入到磷酸盐缓冲液中轻柔搅拌1h配置成浓度为40μg/mL的rhTGF-β3溶液;S2:将牛血清蛋白(BSA)加入到磷酸盐缓冲液中轻柔搅拌1h配置成浓度为200μg/mL的BSA溶液;S3:然后将S1制得的浓度为40μg/mL的rhTGF-β3溶液和S2制得的浓度为200μg/mL的BSA溶液等体积混合,配制成rhTGF-β3/BSA的混合溶液;S4:将Ⅰ型胶原溶于去离子水配成质量浓度为20%的Ⅰ型胶原溶液;S5:将S4制得的质量浓度为20%的Ⅰ型胶原溶液和S3中制得的rhTGF-β3/BSA的混合溶液等体积混合,制得核层材料混合溶液。二、气管软组织修复纤维膜的纺丝:S1:将所述壳层材料混合溶液和所述核层材料混合溶液分别加到同轴静电纺丝设备中的壳层材料注射器和核层材料注射器中,静置30-60min至排尽所述壳层材料注射器和核层材料注射器的空气;S2:连接辊筒接收器和同轴喷头间的电线,调节辊筒接收器和同轴喷头间的距离为15cm;接通高压电源,调节高压电源至15kV,启动微量注射泵,调节载有壳层材料注射器的微量注射泵的输出速度调节至1mL/h,调节载有核层材料注射器的微量注射泵的输出速度调节至0.2mL/h,启动辊筒接收器接收纺丝,辊筒接收器的转速控制在200rpm;S3:待核层材料完全输出后,结束纺丝,关闭高压电源,从收集装置上取下纺丝膜,即得一种用于气管软组织修复的纤维膜。所述的同轴静电纺丝装置包括高压电源,壳层材料注射器,核层材料注射器,微量注射泵,收集装置,同轴喷头和辊筒接收器。所述同轴喷射头内孔径为0.5mm,所述同轴喷射头外孔径为0.8mm。实施例2一种用于气管软组织修复的纤维膜,所述用于气管软组织修复的纤维膜为核-壳多孔网状结构,由聚己内酯、Ⅰ型胶原、重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)组成组成;所述用于气管软组织修复的纤维膜按重量份数计由聚己内酯10份、Ⅰ型胶原10份、重组转化生长因子-β3(rhTGF-β3)0.025份和牛血清蛋白(BSA)0.075份组成;所述的聚己内酯的分子量为8×105Da,所述的Ⅰ型胶原的分子量为1×105Da,所述的重组转化生长因子-β3(rhTGF-β3)的分子量为25kDa。上述用于气管软组织修复的纤维膜,其制备方法的具体步骤如下:一、纤维膜材料的制备:(1)壳层材料制备:将聚己内酯和Ⅰ型胶原按质量比4:1溶于六氟异丙醇搅拌12小时,配制成质量浓度为12%的聚己内酯/Ⅰ型胶原的混合溶液,然后超声处理30min去除搅拌时产生的气泡,制得壳层材料混合溶液;(2)核层材料制备:S1:将重组转化生长因子-β3(rhTGF-β3)加入到磷酸盐缓冲液中轻柔搅拌1h配置成浓度为40μg/mL的rhTGF-β3溶液;S2:将牛血清蛋白(BSA)加入到磷酸盐缓冲液中轻柔搅拌1h配置成浓度为200μg/mL的BSA溶液;S3:然后将S1制得的浓度为40μg/mL的rhTGF-β3溶液和S2制得的浓度为200μg/mL的BSA溶液等体积混合,配制成rhTGF-β3/BSA的混合溶液;S4:将Ⅰ型胶原溶于去离子水配成质量浓度为20%的Ⅰ型胶原溶液;S5:将S4制得的质量浓度为20%的Ⅰ型胶原溶液和S3中制得的rhTGF-β3/BSA的混合溶液等体积混合,制得核层材料混合溶液。二、气管软组织修复纤维膜的纺丝:S1:将所述壳层材料混合溶液和所述核层材料混合溶液分别加到同轴静电纺丝设备中的壳层材料注射器和核层材料注射器中,静置30-60min至排尽所述壳层材料注射器和核层材料注射器的空气;S2:连接辊筒接收器和同轴喷头间的电线,调节辊筒接收器和同轴喷头间的距离为17cm;接通高压电源,调节高压电源至17kV,启动微量注射泵,调节载有壳层材料注射器的微量注射泵的输出速度调节至1mL/h,调节载有核层材料注射器的微量注射泵的输出速度调节至0.2mL/h,启动辊筒接收器接收纺丝,辊筒接收器的转速控制在300rpm;S3:待核层材料完全输出后,结束纺丝,关闭高压电源,从收集装置上取下纺丝膜,即得一种用于气管软组织修复的纤维膜。所述的同轴静电纺丝装置包括高压电源,壳层材料注射器,核层材料注射器,微量注射泵,收集装置,同轴喷头和辊筒接收器。所述同轴喷射头内孔径为0.5mm,所述同轴喷射头外孔径为0.8mm。实施例3一种用于气管软组织修复的纤维膜,所述用于气管软组织修复的纤维膜为核-壳多孔网状结构,由聚己内酯、Ⅰ型胶原、重组转化生长因子-β3(rhTGF-β3)和牛血清蛋白(BSA)组成组成;所述用于气管软组织修复的纤维膜按重量份数计由聚己内酯10份、Ⅰ型胶原10份、重组转化生长因子-β3(rhTGF-β3)0.05份和牛血清蛋白(BSA)0.1份组成;所述的聚己内酯的分子量为8×105Da,所述的Ⅰ型胶原的分子量为1×105Da,所述的重组转化生长因子-β3(rhTGF-β3)的分子量为25kDa。上述用于气管软组织修复的纤维膜,其制备方法的具体步骤如下:一、纤维膜材料的制备:(1)壳层材料制备:将聚己内酯和Ⅰ型胶原按质量比4:1溶于六氟异丙醇搅拌12小时,配制成质量浓度为12%的聚己内酯/Ⅰ型胶原的混合溶液,然后超声处理30min去除搅拌时产生的气泡,制得壳层材料混合溶液;(2)核层材料制备:S1:将重组转化生长因子-β3(rhTGF-β3)加入到磷酸盐缓冲液中轻柔搅拌1h配置成浓度为40μg/mL的rhTGF-β3溶液;S2:将牛血清蛋白(BSA)加入到磷酸盐缓冲液中轻柔搅拌1h配置成浓度为200μg/mL的BSA溶液;S3:然后将S1制得的浓度为40μg/mL的rhTGF-β3溶液和S2制得的浓度为200μg/mL的BSA溶液等体积混合,配制成rhTGF-β3/BSA的混合溶液;S4:将Ⅰ型胶原溶于去离子水配成质量浓度为20%的Ⅰ型胶原溶液;S5:将S4制得的质量浓度为20%的Ⅰ型胶原溶液和S3中制得的rhTGF-β3/BSA的混合溶液等体积混合,制得核层材料混合溶液。二、气管软组织修复纤维膜的纺丝:S1:将所述壳层材料混合溶液和所述核层材料混合溶液分别加到同轴静电纺丝设备中的壳层材料注射器和核层材料注射器中,静置30-60min至排尽所述壳层材料注射器和核层材料注射器的空气;S2:连接辊筒接收器和同轴喷头间的电线,调节辊筒接收器和同轴喷头间的距离为20cm;接通高压电源,调节高压电源至20kV,启动微量注射泵,调节载有壳层材料注射器的微量注射泵的输出速度调节至1mL/h,调节载有核层材料注射器的微量注射泵的输出速度调节至0.2mL/h,启动辊筒接收器接收纺丝,辊筒接收器的转速控制在350rpm;S3:待核层材料完全输出后,结束纺丝,关闭高压电源,从收集装置上取下纺丝膜,即得一种用于气管软组织修复的纤维膜。所述的同轴静电纺丝装置包括高压电源,壳层材料注射器,核层材料注射器,微量注射泵,收集装置,同轴喷头和辊筒接收器。所述同轴喷射头内孔径为0.5mm,所述同轴喷射头外孔径为0.8mm。实施例4对比例:为负载了rhTGF-β3的异种脱细胞真皮基质。异种脱细胞真皮基质参考CN201510549616.9所公开的一种生物相容性良好的异种脱细胞真皮基的制备方法。负载rhTGF-β3的具体步骤为:将rhTGF-β3溶于去离子水中,配成浓度为40μg/mL的rhTGF-β3溶液,然后将异种脱细胞真皮基质浸泡rhTGF-β3溶液中静置12h,然后置于冷冻干燥机中-80℃冷冻干燥,即得负载了rhTGF-β3的异种脱细胞真皮基质。实验组1~3:为实施例1~3所得的用于气管软组织修复纤维膜。将上述实施例1~3所制备的一种用于气管软组织修复的纤维膜与对比例制得的负载了rhTGF-β3的异种脱细胞真皮基质进行rhTGF-β3体外释放评价实验,对比实施例1~3和对比例的rhTGF-β3释放效果。实验结果如图1示。通过上述释放评价实验,从图1可以看出,通过本发明制备方法得到的一种用于气管软组织修复的纤维膜具有缓释功能,能够缓慢持续地释放重组转化生长因子-β3(rhTGF-β3)。实施例5对比例:异种脱细胞真皮基质(参考CN201510549616.9所公开的一种生物相容性良好的异种脱细胞真皮基的制备方法所制得)实验组1~3:为实施例1~3制得的用于气管软组织修复的纤维膜。将上述实施例1~3所制备的用于气管软组织修复的纤维膜与对比例进行细胞毒性评价实验(按国标GB/T16886.5-2003进行实验)。实验结果如图2所示。细胞毒性检测结果显示实施例1~3在与间充质干细胞(MSCS)共培养1天和7天后其对应的细胞相对增殖率均在95%以上,细胞毒性评级为0级,证明其具有良好的细胞形容性,而对比例与间充质干细胞(MSCS)共培养1天和7天后其对应细胞相对增殖率均小于80%,细胞毒性评级为3级,具有较高的细胞毒性。此外,共培养时间的延长实施例1~3的相对增殖率均有明显提高,实施例1~3在共培养7天后其细胞相对增殖率均明显较阴性组要高(均高于110%),证明采用本发明所公开的制备方法所制得的用于气管软组织修复的纤维膜具有促进间充质干细胞(MSCS)的生长的作用,有利于受损部位的修复。实施例6实验组1~3:为实施例1~3所制得的用于气管软组织修复的纤维膜。将上述实施例1~3所制备的用于气管软组织修复的纤维膜进行急性毒性评价和体外溶血评价以评价其生物安全性。测试方法:急性毒性评价方法:按GB/T16886.11-2011《医疗器械生物学评价第11部分:全身毒性试验》中的急性毒性检测方法进行检测。体外溶血评价方法:将2mL血液于1000×g离心5min,去除上层清液,加入适量PBS溶液(pH=7.4),缓慢摇匀,将红细胞清洗三次后再以1000×g离心5min,取下层红细胞悬液用PBS溶液配制成16%的红细胞悬浮液。取50μL上述红细胞悬浮液,分别加入1mL蒸馏水、PBS溶液和1mg/mL的样品浸提液溶液中,分别设为阳性对照组、阴性对照组和试验组,轻轻混匀后在37℃下孵育1h,将各组样品于1000×g离心5min,取上清液200μL加入96孔板中,每组3个平行样,在540nm波长下测试其吸光度,重复试验3次。根据测得的吸光度,由公式(1)计算各试验的溶血率(Y)。Y(%)=(A-A0)/(A100-A0)×100皮肤刺激评价方法:按GB/T16886.10-2005《医疗器械生物学评价第10部分:刺激与迟发型超敏反应试验》中皮内刺激检测方法进行检测。评价结果如表1所示:表1急性毒性评价和体外溶血评价结果实施例1实施例2实施例3急性毒性评价正常,无症状正常,无症状正常,无症状体外溶血评价2.33%1.25%3.11%从上表结果可知,实施例1~3所制得的具有生物活性的皮肤修复材料均无急性毒性,体外溶血均符合溶血率合格标准,证明本发明所制备的用于气管软组织修复的纤维膜具有良好的生物安全性。显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定;对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动,这里无需也无法对所有的实施方式予以穷举;凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1