可控释放白藜芦醇和/或白藜芦醇衍生物的载体及其制备方法与应用与流程
本发明涉及生物医用材料技术领域,具体涉及一种可控释放白藜芦醇和/或白藜芦醇衍生物的载体及其制备方法与应用。
背景技术:
冠心病、外周动脉阻塞性疾病等缺血性疾病严重威胁着人类的健康,尤其是以终末端小血管弥漫性受损为主的病变,目前临床治疗仍旧无法取得满意的疗效,临床上存在大量患有心肌缺血、下肢缺血等缺血性疾病的病人。近十年来,根据促血管生成的机制,开展了如促血管生成因子、转基因治疗和细胞治疗等多种治疗手段,取得了一些进展。血管搭桥术可用于治疗缺血性疾病,血管搭桥术中所需要的人工血管替代物,在冠状动脉搭桥、肾透析病人以及新生儿先天性疾病中有很大的需求,然而至今没有令人满意的替代物产品,主要是因为人工血管植入后会形成急性血栓,植入后中长期会发生内膜增生或钙化等。利用VEGF、HGF、NGF等因子可以促进血管快速内皮化;在人工血管上预先种植细胞包括内皮细胞(ECs)、间充质干细胞(MSCs)以及iPS-ECs等构建组织工程血管;将相关基因(eNOs)负载到支架材料中实现局部转染周边细胞,使其释放促血管新生的活性分子如NO,最终促进内皮细胞再生,这些方法可以在一定程度上改善上述不良后果,然而制备过程复杂,重复性差,活性物质稳定性差,并且生产成本高,支架载体植入后的综合效果也有待提高。
技术实现要素:
针对现有技术中的缺陷,首先,本发明提供了一种可控释放白藜芦醇和/或白藜芦醇衍生物的载体的制备方法,包括如下步骤:S1:将可降解聚合物加入到氯仿甲醇溶液中,混合均匀,可降解聚合物的质量和氯仿甲醇溶液的体积比为1g:(3~10)mL;S2:将白藜芦醇和/或白藜芦醇衍生物加入到甲醇溶液中,混合均匀,白藜芦醇和/或白藜芦醇衍生物的质量和甲醇溶液的体积比为(6.25~25)g:1mL;S3:将步骤S1和步骤S2得到的溶液混合均匀并装入微量注射器中,其中白藜芦醇和/或白藜芦醇衍生物与可降解聚合物的质量比为0.25~1:100;S4:将高压直流电源与微量注射器的针头相连,高压直流电源的电压为10~12kV,微量注射器中的溶液流速为6~10mL/h,将电纺丝仪的圆柱形接收器与地线相连,将微量注射器的针头正对电纺丝仪的圆柱形接收器的中央进行电纺,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为10~22cm,电纺的时间为6~35min;S5:将电纺得到的材料真空干燥,得到的产品即为可控释放白藜芦醇和/或白藜芦醇衍生物的载体成品;其中,步骤S1和步骤S2无先后顺序。需要说明的是,上述制备过程均优选在室温20~30℃下进行,将电纺丝仪的圆柱形接收器与地线相连,是为了达到静电的目的。
在本发明的进一步实施方式中,在步骤S1中,可降解聚合物为聚己内酯、聚丙交酯、聚乙醇酸、聚(丙交酯-乙醇酸)共聚物、聚(丙交酯-己内酯)共聚物、聚羟基脂肪酸酯、聚对二氧六环己酮中的一种或几种;可降解聚合物的平均相对分子质量为75000~85000。
在本发明的进一步实施方式中,在步骤S1中,氯仿甲醇溶液中氯仿和甲醇的体积比为10:1。
在本发明的进一步实施方式中,在步骤S3中,白藜芦醇和/或白藜芦醇衍生物与可降解聚合物的质量比为0.4~0.6:100。
在本发明的进一步实施方式中,在步骤S4中,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为20~22cm,电纺的时间为25~35min。需要说明的是,在上述参数范围内,制备得到的可控释放白藜芦醇和/或白藜芦醇衍生物的载体成品为纤维膜状支架材料,纤维膜状支架材料的厚度为300~400μm。
在本发明的进一步实施方式中,在步骤S4中,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为10~12cm,电纺的时间为6~10min。需要说明的是,在上述参数范围内,制备得到的可控释放白藜芦醇和/或白藜芦醇衍生物的载体成品为管状人工血管,血管壁厚度为400~500μm。
在本发明的进一步实施方式中,在步骤S1中,可降解聚合物的质量和氯仿甲醇溶液的体积比为1g:(3~5)mL。
本发明提供的可控释放白藜芦醇和/或白藜芦醇衍生物的载体的制备方法,可以简化制备方法流程,提高可重复性、可操作性和稳定性,降低生产成本。
其次,本发明提供了根据上述的可控释放白藜芦醇和/或白藜芦醇衍生物的载体的制备方法制备得到的可控释放白藜芦醇和/或白藜芦醇衍生物的载体。
本发明提供的可控释放白藜芦醇和/或白藜芦醇衍生物的载体材料,可以实现长时间缓慢释放白藜芦醇的效果,可以提高内皮细胞的功能,包括内皮细胞形成管的能力、内皮细胞迁移能力以及内皮细胞合成和释放NO的能力;并且,可控释放白藜芦醇和/或白藜芦醇衍生物的载体材料可以抑制巨噬细胞所释放的炎症因子TNFa,可以上调M2型巨噬细胞相关基因的表达,提高材料植入体内后的组织修复型CD206+巨噬细胞的数量;再者,可控释放白藜芦醇和/或白藜芦醇衍生物的载体材料可以制备成小口径人工血管,可以显著性的改善支架植入后的血管化以及内皮化程度,改善了人工血管的体内表现。
另外,本发明还提供了上述可控释放白藜芦醇和/或白藜芦醇衍生物的载体在制备下述产品中的应用:1)治疗缺血性疾病的产品;2)治疗心血管疾病的产品;3)治疗皮肤病的产品。
本发明还提供了上述可控释放白藜芦醇和/或白藜芦醇衍生物的载体在制备促进组织再生产品中的应用。
本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
图1为本发明实施例五制备得到的可控释放白藜芦醇物的载体纤维膜状支架材料的形貌图。
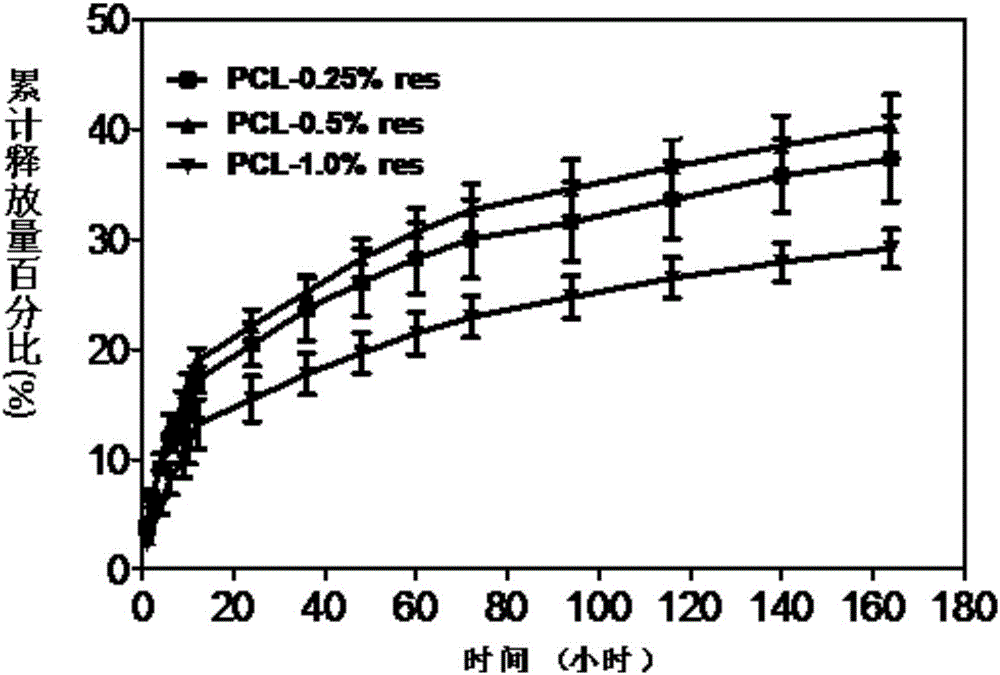
图2为本发明实施例一、实施例三和实施例五制备得到的可控释放白藜芦醇物的载体纤维膜状支架材料不同时间点的累计释放量百分比曲线图。
图3为本发明实施例一、实施例三和实施例五制备得到的可控释放白藜芦醇物的载体纤维膜状支架材料不同时间点的累计释放量曲线图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
下述实施例中的实验方法,如无特殊说明,均为常规方法。
下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。
以下实施例中的定量试验,均设置三次重复实验,数据为三次重复实验的平均值或平均值±标准差。
本发明提供一种可控释放白藜芦醇和/或白藜芦醇衍生物的载体的制备方法,包括如下步骤:
S1:将可降解聚合物加入到氯仿甲醇溶液中,混合均匀,可降解聚合物的质量和氯仿甲醇溶液的体积比为1g:(3~10)mL,优选为1g:(3~5)mL;可降解聚合物优选为聚己内酯、聚丙交酯、聚乙醇酸、聚(丙交酯-乙醇酸)共聚物、聚(丙交酯-己内酯)共聚物、聚羟基脂肪酸酯、聚对二氧六环己酮中的一种或几种;可降解聚合物的平均相对分子质量优选为75000~85000;氯仿甲醇溶液中氯仿和甲醇的体积比优选为10:1。
S2:将白藜芦醇和/或白藜芦醇衍生物加入到甲醇溶液中,混合均匀,白藜芦醇和/或白藜芦醇衍生物的质量和甲醇溶液的体积比为(6.25~25)g:1mL。
S3:将步骤S1和步骤S2得到的溶液混合均匀并装入微量注射器中,其中白藜芦醇和/或白藜芦醇衍生物与可降解聚合物的质量比为0.25~1:100,优选为0.4~0.6:100。
S4:将高压直流电源与微量注射器的针头相连,高压直流电源的电压为10~12kV,微量注射器中的溶液流速为6~10mL/h,将电纺丝仪的圆柱形接收器与地线相连,将微量注射器的针头正对电纺丝仪的圆柱形接收器的中央进行电纺,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为10~22cm,电纺的时间为6~35min;
其中,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为20~22cm,电纺的时间为25~35min,制备得到的可控释放白藜芦醇和/或白藜芦醇衍生物的载体成品为膜状支架,支架厚度为300~400μm;
微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为10~12cm,电纺的时间为6~10min,制备得到的可控释放白藜芦醇和/或白藜芦醇衍生物的载体成品为管状人工血管,血管壁厚度为400~500μm。
S5:将电纺得到的材料真空干燥,得到的产品即为可控释放白藜芦醇和/或白藜芦醇衍生物的载体成品。
其中,步骤S1和步骤S2无先后顺序。
下面结合具体实施例对本发明提供的本发明提供的可控释放白藜芦醇和/或白藜芦醇衍生物的载体及其制备方法作进一步说明。
实施例一
称取2.5g平均相对分子质量为80000的聚己内酯聚合物,加入到10mL的氯仿甲醇溶液中,氯仿甲醇溶液中氯仿和甲醇的体积比为10:1,搅拌混合均匀;称取6.25mg白藜芦醇,加入到1mL的甲醇溶液中,搅拌使白藜芦醇充分溶解;将上述两种溶液混合均匀并装入直径为14.9mm的微量注射器中,将高压直流电源与微量注射器的针头相连,用铝箔包裹在电纺丝仪的圆柱形接收器,将电纺丝仪的圆柱形接收器与地线相连,将微量注射器的针头正对电纺丝仪的圆柱形接收器的中央进行电纺,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为21cm,高压直流电源的电压为11kV,微量注射器中的溶液流速为8mL/h,电纺时间为30min;将得到的材料真空干燥,至溶剂完全挥发,得到可控释放白藜芦醇物的载体纤维膜状支架材料,纤维膜状支架材料的厚度为350μm。
实施例二
称取2.5g平均相对分子质量为80000的聚己内酯聚合物,加入到10mL的氯仿甲醇溶液中,氯仿甲醇溶液中氯仿和甲醇的体积比为10:1,搅拌混合均匀;称取6.25mg白藜芦醇,加入到1mL的甲醇溶液中,搅拌使白藜芦醇充分溶解;将上述两种溶液混合均匀并装入直径为14.9mm的微量注射器中,将高压直流电源与微量注射器的针头相连,将直径为2毫米的不锈钢圆柱安装到电纺丝仪的接收器上,将电纺丝仪的圆柱形接收器与地线相连,将微量注射器的针头正对电纺丝仪的圆柱形接收器的中央进行电纺,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为11cm,高压直流电源的电压为11kV,微量注射器中的溶液流速为8mL/h,电纺时间为8min;将得到的材料真空干燥,至溶剂完全挥发,得到可控释放白藜芦醇的载体管状人工血管,血管壁厚度为450μm。
实施例三
称取2.5g平均相对分子质量为80000的聚己内酯聚合物,加入到10mL的氯仿甲醇溶液中,氯仿甲醇溶液中氯仿和甲醇的体积比为10:1,搅拌混合均匀;称取25mg白藜芦醇,加入到1mL的甲醇溶液中,搅拌使白藜芦醇充分溶解;将上述两种溶液混合均匀并装入直径为14.9mm的微量注射器中,将高压直流电源与微量注射器的针头相连,用铝箔包裹在电纺丝仪的圆柱形接收器,将电纺丝仪的圆柱形接收器与地线相连,将微量注射器的针头正对电纺丝仪的圆柱形接收器的中央进行电纺,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为21cm,高压直流电源的电压为11kV,微量注射器中的溶液流速为8mL/h,电纺时间为30min;将得到的材料真空干燥,至溶剂完全挥发,得到可控释放白藜芦醇物的载体纤维膜状支架材料,纤维膜状支架材料的厚度为350μm。
实施例四
称取2.5g平均相对分子质量为80000的聚己内酯聚合物,加入到10mL的氯仿甲醇溶液中,氯仿甲醇溶液中氯仿和甲醇的体积比为10:1,搅拌混合均匀;称取25mg白藜芦醇,加入到1mL的甲醇溶液中,搅拌使白藜芦醇充分溶解;将上述两种溶液混合均匀并装入直径为14.9mm的微量注射器中,将高压直流电源与微量注射器的针头相连,将直径为2毫米的不锈钢圆柱安装到电纺丝仪的接收器上,将电纺丝仪的圆柱形接收器与地线相连,将微量注射器的针头正对电纺丝仪的圆柱形接收器的中央进行电纺,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为11cm,高压直流电源的电压为11kV,微量注射器中的溶液流速为8mL/h,电纺时间为8min;将得到的材料真空干燥,至溶剂完全挥发,得到可控释放白藜芦醇的载体管状人工血管,血管壁厚度为450μm。
实施例五
称取2.5g平均相对分子质量为80000的聚己内酯聚合物,加入到10mL的氯仿甲醇溶液中,氯仿甲醇溶液中氯仿和甲醇的体积比为10:1,搅拌混合均匀;称取12.5mg白藜芦醇,加入到1mL的甲醇溶液中,搅拌使白藜芦醇充分溶解;将上述两种溶液混合均匀并装入直径为14.9mm的微量注射器中,将高压直流电源与微量注射器的针头相连,用铝箔包裹在电纺丝仪的圆柱形接收器,将电纺丝仪的圆柱形接收器与地线相连,将微量注射器的针头正对电纺丝仪的圆柱形接收器的中央进行电纺,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为21cm,高压直流电源的电压为11kV,微量注射器中的溶液流速为8mL/h,电纺时间为30min;将得到的材料真空干燥,至溶剂完全挥发,得到可控释放白藜芦醇物的载体纤维膜状支架材料,纤维膜状支架材料的厚度为350μm。
实施例六
称取2.5g平均相对分子质量为80000的聚己内酯聚合物,加入到10mL的氯仿甲醇溶液中,氯仿甲醇溶液中氯仿和甲醇的体积比为10:1,搅拌混合均匀;称取12.5mg白藜芦醇,加入到1mL的甲醇溶液中,搅拌使白藜芦醇充分溶解;将上述两种溶液混合均匀并装入直径为14.9mm的微量注射器中,将高压直流电源与微量注射器的针头相连,将直径为2毫米的不锈钢圆柱安装到电纺丝仪的接收器上,将电纺丝仪的圆柱形接收器与地线相连,将微量注射器的针头正对电纺丝仪的圆柱形接收器的中央进行电纺,微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离为11cm,高压直流电源的电压为11kV,微量注射器中的溶液流速为8mL/h,电纺时间为8min;将得到的材料真空干燥,至溶剂完全挥发,得到可控释放白藜芦醇的载体管状人工血管,血管壁厚度为450μm。
本发明制备得到的可控释放白藜芦醇物的载体纤维膜状支架材料的纤维表面光滑,粗细均匀,纤维之间随机排列,具体如图1所示,图1为本发明实施例五制备得到的可控释放白藜芦醇物的载体纤维膜状支架材料的形貌图。
将本发明实施例一至实施例六制备得到的可控释放白藜芦醇的载体的性能进行生物学功能测定。
1、白藜芦醇的释放行为
将实施例一、实施例三和实施例五制备得到的可控释放白藜芦醇物的载体纤维膜状支架材料进行白藜芦醇的释放行为测定,不同实施例负载的白藜芦醇负载浓度不同,将实施例一、实施例三和实施例五制备得到的可控释放白藜芦醇物的载体纤维膜状支架材料分别记为PCL-0.25%res、PCL-1%res和PCL-0.5%res。将上述材料分别剪取20mg,分别浸泡在1ml PBS缓冲液中,收集不同时间点的浸泡液,直至160h,在每个时间点收集后都将纤维膜状支架材料放入新鲜的1ml PBS缓冲液中,通过测试收集的浸泡液的OD303来计算白藜芦醇的释放量,并且将未负载白藜芦醇的聚己内酯纤维膜状支架(空白PCL材料)作为对照。
检测发现,收集的未负载白藜芦醇的聚己内酯纤维膜状支架(空白PCL材料)浸泡液基本未检测到紫外吸收。实施例一、实施例三和实施例五制备得到的可控释放白藜芦醇物的载体纤维膜状支架材料不同时间点的累计释放量百分比曲线和累计释放量曲线分别如图2和图3所示。从图2和图3可以看到,负载不同浓度的白藜芦醇的三种纤维膜状支架材料中,均未观察到突释现象,在最开始的24h,三种维膜状支架材料的白藜芦醇释放速率都相对较快,随后开始缓慢释放,随着起始状态白藜芦醇负载量的增加,白藜芦醇累积释放量增加,也就是说实施例三制备得到的负载25mg白藜芦醇的纤维膜状支架材料(PCL-1%res)的累积释放量最大;然而累计释放量百分比与起始负载量不相关,实施例五制备得到的负载12.5mg白藜芦醇的纤维膜状支架材料(PCL-0.5%res)的累计释放量百分比最高,其次是实施例一制备得到的负载6.25mg白藜芦醇的纤维膜状支架材料(PCL-0.25%res)。
2、对于内皮细胞功能影响的测定
将实施例一、实施例三和实施例五制备得到的可控释放白藜芦醇物的载体纤维膜状支架材料进行对内皮细胞功能影响的测定。分别将上述材料剪取20mg,浸泡在基础培养基中24h,获得材料洗脱液,然后利用成管实验和划痕实验检测三种纤维膜状支架材料对于内皮细胞功能的影响。
成管实验:将Matrigel放于4℃融化,然后取50ul加入到96孔板的孔中,并放置于37度1小时形成凝胶。然后每孔种植1万个细胞,分别加入上述培养基培养,4h后正置显微镜下拍照记录细胞的成管情况。
划痕实验方案:将HUVEC细胞种植到24孔板中,待细胞完全铺满后,用1ml枪头比着直尺做横线划痕,然后用PBS洗细胞3次,去处划下的细胞,分别加入上述抽提液,24h后显微镜下拍照记录细胞迁移情况。
结果:(1)白藜芦醇抽提液对于内皮细胞迁移的影响。划痕损伤24小时后,相比于未负载白藜芦醇的聚己内酯纤维膜状支架(空白PCL材料),三种负载白藜芦醇的纤维膜状支架材料处理的内皮细胞的迁移速率都有所增加,说明负载的白藜芦醇提高了内皮细胞的迁移速率,而三组中,实施例五制备得到的负载12.5mg白藜芦醇的纤维膜状支架材料(PCL-0.5%res)组的效果最好,说明白藜芦醇的功效具有浓度依赖性。
(2)材料抽提取液对于内皮成管的影响。与未负载白藜芦醇的聚己内酯纤维膜状支架(空白PCL材料)相比,三组负载白藜芦醇白藜芦醇的纤维膜状支架材料抽提液处理的内皮细胞形成管的能力显著性提高,其中实施例五制备得到的负载12.5mg白藜芦醇的纤维膜状支架材料(PCL-0.5%res)组的效果最好。
(3)负载白藜芦醇的纤维膜状支架材料对于内皮细胞释放NO的影响。3天之后HUVEC细胞在空白PCL材料表面与培养板表面NO释放量达到最大,5天之后不再升高。而负载白藜芦醇的三组纤维膜状支架材料均可促进内皮细胞持续释放NO,且培养5天后,实施例五制备得到的负载12.5mg白藜芦醇的纤维膜状支架材料(PCL-0.5%res)组和实施例三制备得到的负载25mg白藜芦醇的纤维膜状支架材料(PCL-1%res)组的NO释放量比空白PCL材料组有显著性的提高。
(4)白藜芦醇对于炎症反应的作用。TNFa是巨噬细胞来源促炎因子的主要因子之一,通过实验检测不同组材料对于巨噬细胞分泌TNFa的影响,从而判定白藜芦醇对于炎症反应的作用。实验结果发现,对于空白PCL材料组,培养巨噬细胞一天后,TNFa分泌量为61.60±7.00pg/ml;而负载白藜芦醇的三组纤维膜状支架材料,均未检测到TNFa表达,说明负载白藜芦醇可以抑制TNFa的分泌。
3、动物实验评价
将实施例六制备得到的可控释放白藜芦醇的载体管状人工血管组(A组)进行动物实验评价,同时利用未负载白藜芦醇的聚己内酯管状人工血管(空白PCL材料)组(B组)作为空白对照。利用大鼠腹主动脉人工血管替代模型,将负载白藜芦醇的人工血管移植于大鼠腹主动脉,2周与4周后考察材料的通畅性,并取材做冰冻切片,用免疫染色的方法,来检测内皮、平滑肌细胞以及毛细血管再生情况。
血管吻合手术:腹腔注射10%水合氯醛麻醉大鼠(0.33ml/100g体重),待大鼠彻底麻醉后,按100U.I/kg剂量尾静脉注射肝素对大鼠进行全身肝素化处理,然后将大鼠固定在手术台上,备皮并用碘伏进行消毒。剪开腹部皮肤,用医用纱布将肠道等组织器官覆盖并挪至腹腔的一侧,使腹主动静脉暴露,然后使用钝性分离器将肾动脉与下肢动脉之间的动静脉进行剥离,大致长度为1cm,期间若发现有动脉小分支,则对其进行结扎。用动脉夹夹住动脉的两端,剪断腹主动脉,用8-0带针尼龙缝合线将小口径人工血管原位植入,缝合长度约为10mm。缝合时以米字法缝合,每端缝8~10针。两端均缝好后,缓慢移除动脉夹以恢复血流,该过程总缺血时间不超过50min。用棉花压住缝合处止血,然后用3-0缝合线缝合腹部肌肉层和皮肤,碘伏消毒。将其放置于保温毯上待其苏醒后,放于干净饲养笼饲养。
移植后血管材料的性能评价:在不同的时间点包括2周和四周取材前,利用体式显微镜拍照,记录取材材料的外观形貌,然后将材料分为两部分,一部分做SEM观察其内表面形态,另外一部分做冰冻切片进行组织学分析。
冰冻切片:样品经4%多聚甲醛固定6小时后,用PBS清洗几遍,30%蔗糖脱水至样品沉入底部,用OCT包埋样品,-20℃冰冻切片厚度为6μm,贮存于-80℃备用。
H&E染色:(1)流水冲洗5min;(2)伊红染色30s,流水冲洗5min;(3)苏木素染色2min,流水冲洗5min;(4)HCl-乙醇分化1s,流水冲洗5min;(5)70%、80%、90%乙醇各蘸三次,99%乙醇I、II各5min;(6)二甲苯I、II各5min;(7)中性树胶封片,使用普通光学显微镜镜检。
免疫荧光染色:(1)冷丙酮-20℃固定10min,风干,PBS洗涤5min×2次;(2)进行胞内抗原染色时,需使用0.1%Triton-PBS破膜,PBS洗涤5min×2次;(3)5%羊血清4℃封闭45min;(4)一抗4℃孵育过夜,PBS洗涤5min×8次;(5)二抗避光室温孵育2h,PBS洗涤5min×8次;(6)使用含DAPI的封片剂封片,使用高级正置荧光显微镜镜检。免疫染色的检测指标主要包括:内皮细胞(vWF或CD31)、平滑肌细胞(α-SMA,MYH)等,未加一抗的样品作为阴性对照。
结果:人工血管腹主动脉移植模型评价结果发现,对于实施例六制备得到的可控释放白藜芦醇的载体管状人工血管(A组),植入两周后,相比于未负载白藜芦醇的聚己内酯管状人工血管(空白PCL材料)组(B组),负载白藜芦醇组(A组)的CD206+细胞数量显著提高,而在4周后,两组的CD206+细胞数量相近,没有显著差异。
CD31+染色显示血管壁中的小血管,在植入2周时,相比于未负载白藜芦醇的聚己内酯管状人工血管(空白PCL材料)组(B组),负载白藜芦醇的管状人工血管(A组)材料中的绿色区域,也就是代表的CD31+阳性血管数量显著提高。毛细血管化直接影响支架材料中再生细胞的营养代谢,最终影响支架植入后再生。同样在植入4周时,负载白藜芦醇的支架(A组)材料的CD31+阳性血管数量仍高于空白对照组(B组)。负载白藜芦醇的支架(A组)血管化4周时与2周时相比,血管密度略有下降,然而血管的长度变长,从一定程度上讲,代表支架材料中的血管化程度在向更成熟稳定的方向发展。
内皮化形成是表征人工血管植入后成败的关键指标,人工血管植入后快速内皮化可以抑制植入材料表面血栓形成以及平滑肌增生。利用取材后组织冰冻切片纵切片进行CD31染色观察内皮细胞在材料表面的覆盖率。植入后4周,未负载白藜芦醇的聚己内酯管状人工血管(空白PCL材料)组(B组)覆盖率大约为51.80±4.19%,而负载白藜芦醇的管状人工血管组(A组)的覆盖率将近80.21±3.38%,说明负载白藜芦醇的材料内皮化程度增加了将近30%。
本发明提供的可控释放白藜芦醇和/或白藜芦醇衍生物的载体材料,可以实现长时间缓慢释放白藜芦醇的效果,可以提高内皮细胞的功能,包括内皮细胞形成管的能力、内皮细胞迁移能力以及内皮细胞合成和释放NO的能力。并且,可控释放白藜芦醇和/或白藜芦醇衍生物的载体材料可以抑制巨噬细胞所释放的炎症因子TNFa,可以上调M2型巨噬细胞相关基因的表达,提高材料植入体内后的组织修复型CD206+巨噬细胞的数量。动物实验表明本发明提供的可控释放白藜芦醇和/或白藜芦醇衍生物的载体材料可以制备成小口径人工血管,可以显著性的改善支架植入后的血管化以及内皮化程度,改善了人工血管的体内表现。
需要说明的是,除了上述实施例一至实施例六列举的情况,选用其他可降解聚合物、降解聚合物的质量和氯仿甲醇溶液的体积比、氯仿甲醇溶液中氯仿和甲醇的体积比、白藜芦醇和/或白藜芦醇衍生物的质量和甲醇溶液的体积比、白藜芦醇和/或白藜芦醇衍生物与可降解聚合物的质量比、高压直流电源的电压、溶液流速、微量注射器的针头与电纺丝仪的圆柱形接收器的中央的距离和电纺时间也是可行的,只是在实施例一至实施例六列举的情况下,制备得到的可控释放白藜芦醇和/或白藜芦醇衍生物的载体效果更好。
本发明提供的可控释放白藜芦醇和/或白藜芦醇衍生物的载体的制备方法,可以简化载体材料制备方法流程,提高可重复性、可操作性和稳定性,降低生产成本。
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型,而并不使相应技术方案的本质脱离本发明各实施例技术方案的范围,其均应涵盖在本发明的权利要求和说明书的范围当中。
- 还没有人留言评论。精彩留言会获得点赞!