一种人参皂苷RZ1固体分散体及其制备方法与流程
本发明涉及药物制剂领域,尤其涉及一种人参皂苷rz1固体分散体及其制备方法。
背景技术:
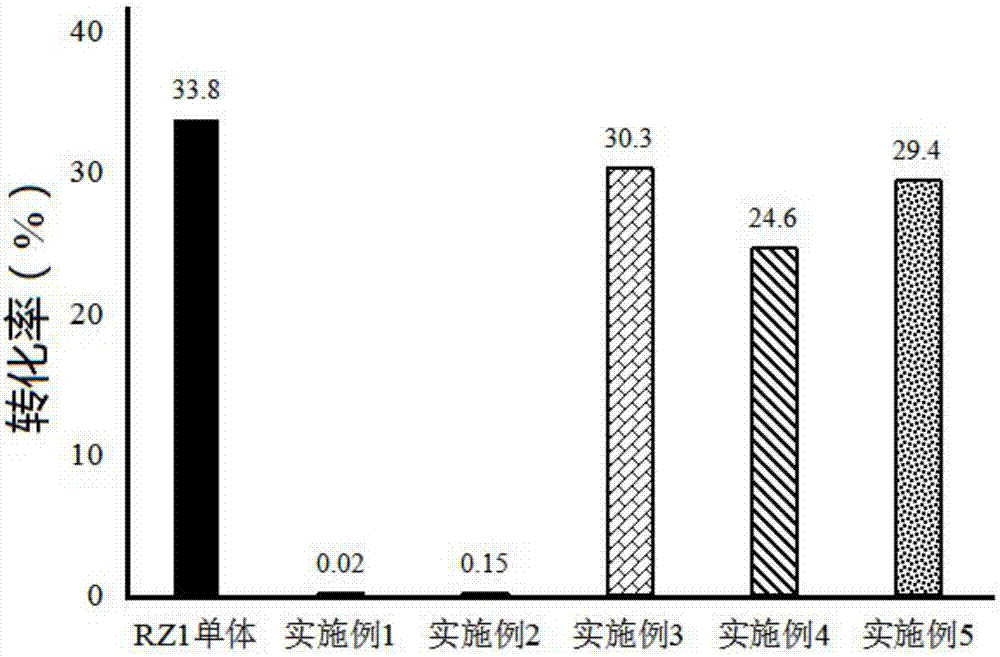
:申请人研究发现人参皂苷rz1可有效促进骨髓间充质干细胞成骨分化。人参皂苷rz1最早由韩国学者sangmyunglee从加热炮制的人参中分离得到(参考文献:ginsenosidesfromheatprocessedginseng,chempharmbull,2009),生源上由人参皂苷rg3脱水而得。人参皂苷rz1有两个同分异构体,即人参皂苷rk1和rg5,三者化学结构式及生源降解途径如下所示:人参皂苷rg3的c20羟基与c21氢发生消除反应得到人参皂苷rk1,人参皂苷rg3的c20羟基与c22氢发生消除反应得到人参皂苷rg5和rz1,人参皂苷rk1与rg5、rz1为双键位置异构,人参皂苷rg5与rz1为双键顺反异构。其中,人参皂苷rz1双键两端的大基团在双键同侧,由于空间位阻原因,相对不稳定,容易向人参皂苷rg5转化。因此,申请人在开发人参皂苷rz1相关制剂时,至少需要克服如下两个问题:第一,人参皂苷rz1水溶性极差,生物利用度低;第二,降低人参皂苷rz1向人参皂苷rg5转化的速度。技术实现要素:本发明目的在于提供一种人参皂苷rz1固体分散体及制备方法,一方面提高人参皂苷rz1的水溶性,另一方面提高人参皂苷rz1的稳定性,抑制人参皂苷rz1向人参皂苷rg5转化。为实现上述目的,本发明提供了以下技术方案:一种人参皂苷rz1固体分散体,固体载体为聚维酮k-30。上述人参皂苷rz1固体分散体的制备方法,采用超临界抗溶剂法制备,包括如下步骤:步骤a,启动装置,待结晶釜的温度达到预定值后,将co2由高压泵压缩并经预热器预热后从釜顶通入结晶釜内至预定压力;待釜内温度和压力稳定后,打开釜底co2出口阀,并调节微调阀至预定的体积流量;步骤b,将一定量的人参皂苷rz1和聚维酮k-30按质量比1:(2-4)溶于等体积比的丙酮与二氯甲烷混合溶剂中配置成所需浓度的溶液,由高压输液泵以设定的体积流量从釜顶泵入结晶釜内,此时含溶剂的co2经微调阀进入分离釜,在分离釜中实现溶剂的回收,co2则经转子流量计排出,待进液完毕后再洗脱20-30分钟;步骤c,关闭co2进口阀,将釜内气体排空后,打开结晶釜取出微粒。在一个具体实施例中,温度为50-60℃,压力为13-15mpa。在一个具体实施例中,co2预定体积流量为2.5-3.5l/min。在一个具体实施例中,人参皂苷rz1质量浓度为14-16mg/ml。在一个具体实施例中,溶液体积流量为0.8-1.0ml/min。上述人参皂苷rz1固体分散体的制备方法:将一定量的人参皂苷rz1和聚维酮k-30按质量比1:(2-4)溶于无水乙醇中配置成所需浓度的溶液,常温搅拌,减压蒸发除去溶剂,干燥,粉碎,得人参皂苷rz1固体分散体。在一个具体实施例中,人参皂苷rz1质量浓度为14-16mg/ml。在一个具体实施例中,常温磁力搅拌3h,于50℃减压旋转蒸发除去溶剂,真空干燥24h,粉碎过5号筛。聚维酮k-30作为制剂辅料在提高人参皂苷rz1水溶性和稳定性方面的应用。本发明提供的人参皂苷rz1固体分散体以聚维酮k-30为固体载体,聚维酮k-30不仅可以提高在水中的溶解度,而且可以提高其稳定性,抑制人参皂苷rz1向人参皂苷rg5转化。附图说明图1是人参皂苷rz1单体及不同载体制成的固体分散体的溶解度(水,25℃)。图2是温度40℃、湿度75%的环境下放置30天人参皂苷rz1单体及不同载体制成的固体分散体的异构化程度。具体实施方式实施例1超临界抗溶剂法制备人参皂苷rz1固体分散体制粒仪器为美国appliedseparations公司生产的helix超临界结晶制粒系统。人参皂苷rz1自制,纯度大于98%。制备工艺流程:启动装置,待结晶釜的温度达到55℃后,将co2由高压泵压缩并经预热器预热后从釜顶通入结晶釜内至14mpa。待釜内温度和压力稳定后,打开釜底co2出口阀,并调节微调阀至预定的体积流量3l/min。将人参皂苷rz1和pvp-k30按质量比1:3溶于丙酮与二氯甲烷的混合溶剂(丙酮与二氯甲烷体积比1:1)中配置成人参皂苷rz1质量浓度为15mg/ml的溶液,由高压输液泵以0.9ml/min从釜顶泵入结晶釜内,此时含溶剂的co2经微调阀进入分离釜,在分离釜中实现溶剂的回收,co2则经转子流量计排出,待进液完毕后再洗脱30分钟。最后关闭co2进口阀,将釜内气体排空后,打开结晶釜取出微粒,置于干燥器内保存备用。实施例2溶剂搅拌法制备人参皂苷rz1固体分散体将一定量的人参皂苷rz1和聚维酮k-30按质量比1:3溶于无水乙醇中配置成人参皂苷rz1质量浓度为15mg/ml的溶液,常温磁力搅拌3h(100r/min),于50℃减压旋转蒸发除去溶剂,真空干燥24h,粉碎过5号筛,置于干燥器内保存备用。实施例3对比实施例将固体载体换成β-环糊精,其他同实施例2。实施例4对比实施例将固体载体换成聚乙烯吡咯烷酮,其他同实施例2。实施例5对比实施例将固体载体换成羟丙基纤维素,其他同实施例2。实施例6效果实施例1、溶解度的测定将过量的人参皂苷rz1、不同实施例制备的人参皂苷rz1固体分散体分别放入盛有10ml水的试管中,超声至不再溶解,放入振动器(100r/min)中,25℃振荡24h,待溶解平衡后,取出饱和溶液,于10000r/min离心10min,吸取上清液测定人参皂苷rz1溶解度。测定结果如表1和图1所示。表1人参皂苷rz1单体及不同载体制成的固体分散体的溶解度(水,25℃)皂苷rz1单体实施例1实施例2实施例3实施例4实施例5溶解度(g/l)0.0250.5350.4530.4200.3850.405结果表明,将人参皂苷rz1制成固体分散体可显著提高其在水中溶解度,水溶性增强。2、稳定性考察将人参皂苷rz1、不同实施例制备的人参皂苷rz1固体分散体分别置于温度为40℃、湿度为75%的环境中进行高温高湿加速试验考察,30天后测定各样品中人参皂苷rg5转化率。人参皂苷rg5转化率(%)=人参皂苷rg5含量/(人参皂苷rz1+人参皂苷rg5含量)测定结果如表2和图2所示。表2人参皂苷rz1单体及不同载体制成的固体分散体的异构化程度皂苷rz1单体实施例1实施例2实施例3实施例4实施例5转化率(%)33.80.020.1530.324.629.4结果表明,聚维酮k-30可以明显提高人参皂苷rz1稳定性,抑制其异构化。本发明提供的人参皂苷rz1固体分散体以聚维酮k-30为固体载体,聚维酮k-30不仅可以提高在水中的溶解度,而且可以提高其稳定性,抑制人参皂苷rz1向人参皂苷rg5转化。本领域技术人员应当知道,上述具体实施方式仅用于解释本发明,本发明的保护范围并不局限于上述具体实施方式。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种对11种人参皂苷类成分同时进行定性及定量的方法
- 含有人参皂苷rh4的皮肤外用剂组合物的制作方法
- 一种三七皂苷R1、人参皂苷Rg1、Re、Rb1和Rd的制备方法
- 含有杂质三七皂苷R<sub>1</sub>的人参皂苷Rg<sub>1</sub>的制作方法
- 人参皂苷Compound K酯类衍生物及其在制备防治动脉粥状硬化的药物中的应用的制作方法
- 一种含有人参皂苷Rh2、麦冬皂苷B的药物组合物的制作方法
- 通过微波辐照产生的具有提高的人参皂苷Rg3、Rg5和Rk1含量比的人参属植物提取物、制 ...的制作方法
- 含有来自水耕栽培人参的人参皂苷f2的皮肤外用剂组合物的制作方法
- 20(R)-人参皂苷Rg3在制备白癜风药物中的应用的制作方法
- 20(R)-人参皂苷Rg3在制备痛经药物中的应用的制作方法