烟叶提取物及其治疗烟瘾的用途的制作方法
本发明涉及烟叶提取物,以及含有该烟叶提取物的药物组合物及其在烟草成瘾治疗中的用途。
现有技术
一般而言,世界卫生组织将依赖或成瘾定义为“一种物质的使用比其他曾经具有更大价值的行为具有更高优先级的综合征”。在其极端形式中,依赖状态的特征是对物质的不可抗拒的需求迫使遭受这种依赖的个人冲动地寻求这种物质。
烟草依赖导致严重的公共卫生问题,大量与吸烟有关的疾病,如癌症(肺癌、咽喉癌、口腔癌、唇癌等)、心血管疾病、慢性支气管炎等。除了疾病本身,吸烟有很多副作用(生育能力下降、表皮改变、口腔和鼻粘膜改变、脑动脉改变、食道和胃损伤、维生素b和c缺乏等)。
有三种类型的烟草依赖同时起作用:身体依赖,主要是由于烟草中存在尼古丁,表现为渴望的感觉(强烈的吸烟欲望,兴奋,紧张,不安,焦虑,睡眠障碍等);与尼古丁的精神作用有关的心理依赖,该作用提供快乐、放松、智力刺激、抗焦虑、抗抑郁和抑制食欲的作用;环境或行为的依赖性,其取决于社会和友好的压力。身体依赖平均在几周内消失。戒断症状在戒烟后三至四天达到高峰,可持续数周。心理依赖需要更长时间才能减少,并且可持续数月。
通过积极和消极的强化来维持对烟草的依赖。尼古丁负责释放多巴胺,即奖励回路中的神经递质。吸烟者吸烟以重现由多巴胺释放引起的愉悦感(这是香烟的正强化)并且当他的多巴胺水平太低时避免戒断症状(这是香烟的负强化)。
烟草依赖的药理学治疗有三种主要方法。第一个目标是在最初设定的目标戒烟日期立即停止,在尼古丁替代品的情况下在此目标戒烟日期之后进行药物治疗,且在安非他酮或伐尼克兰的情况下在一周之前进行药物治疗(为了在目标戒烟日期时达到足够的血浆浓度)。第二种方法在于在尝试停止之前减少其消耗,其中减少阶段对应于施用药理学治疗的预处理。第三种方法是成功停止后预防复发。这三种方法可以减少加入(cuttingdown)而不试图停止。
对于吸烟者,准备阶段加强了这些方法各自的功效,他们必须说服自己戒烟的必要性,并强化他这样做的动机。因此,针对烟草依赖性的药理学治疗的处方信息表明,戒烟治疗更有可能在有动力戒烟的患者中成功。
目前有四种主要类型的烟草依赖治疗方法(更不用说行为心理治疗、针灸和催眠),即尼古丁替代品、安非他酮、伐尼克兰和顺势疗法。这四种方法中的每一种的作用原理都是基于尼古丁是负责烟草依赖机制的分子这一事实。
尼古丁替代品可以多种方式给药:以贴剂的形式透皮,以口香糖、锭剂或舌下片剂的形式口服,或以吸入器形式通过肺部途径。尼古丁替代物的施用主要通过尽可能地防止吸烟者感觉到与戒断相关的戒断症状来减少香烟的负强化,其中由替代物提供尼古丁以补偿香烟的尼古丁。尼古丁替代品的功效根据使用的方法而变化,戒烟率通常为15%至20%。尼古丁替代品在尝试立即戒烟期间使用,并且也在戒烟尝试之前作为预处理以帮助吸烟者减少他们的香烟消耗,作为逐渐戒烟的一部分(减少至戒除)。它们还可以用于减少烟草消费的唯一目的。它们在预防复发方面的功效尚未得到证实。
由glaxosmithklinelaboratories销售的安非他酮(商标名为
伐尼克兰(varenicline)由辉瑞实验室(商品名
第四种戒烟途径是顺势疗法,其基于使用无限小剂量的引起人们希望控制的症状的物质。“烟草”的提取物通常被用于戒烟。爱尔兰专利申请ie960511特别描述了使用顺势疗法的烟草提取物的稀释物来制造用于恢复神经元功能和缓解尼古丁戒断症状的药物产品。像其他非常规戒烟技术一样,其在重度吸烟者中的疗效不足。
尽管在该领域进行了大量研究,但仍需要寻找新的治疗方法或改进现有的烟草依赖治疗方法。
在申请pct/fr2007/000786中,申请人发现,给吸烟者注射烟草叶提取物的水溶液使得可以治疗所述吸烟者的烟草依赖性。这一发现确实出乎意料,因为申请人能够确定所述水性烟叶提取物含有少量尼古丁。因此,使用这种水性烟叶提取物治疗烟草依赖性所涉及的作用机制并不是向吸烟者提供尼古丁。
然而,所述水性烟叶提取物含有少量尼古丁的事实并未提供关于其组成及其制备方法的信息。水性烟草叶提取物的尼古丁含量确实可以根据许多因素而显著变化。
对于主要类型的烟草种植,烟草叶中的尼古丁含量可以为0.5%至8%(davis等,“production,chemistry,andtechnology”,isbn-13:978-0632047918,第8章,第275页)。
白肋烟草含有大约两倍于马里兰烟草的尼古丁和三倍于东方烟草的尼古丁(leffingwell,“chemicalconstituentsoftobaccoleafanddifferencesamongtobaccotypes”,leffingwellreports,vol.1(no.2),2001年2月)。
氮肥的使用影响烟叶的尼古丁含量,且上部叶片的尼古丁含量高于中部叶片,而中部叶片的尼古丁含量则高于下部叶片(xiao-tang等,“yieldandnicotinecontentofflue–curedtobaccoasaffectedbysoilnitrogenmineralization”,pedosphere18(2):227–235,2008,issn1002–0160/cn32–1315/p)。
作物轮作影响烟叶的尼古丁含量(butorac等,“theeffectoftobaccomonocultureandcroprotationsontobaccoleafcomposition”,agriculturaeconspectusscientificus,vol.69(2004)no.4(95-101))。
烟叶的化学组成和尼古丁含量受紫外线辐射和光照强度的影响(andersen等,“chemicalcompositionoftobaccoleavesalteredbynear–ultravioletandintensityofvisiblelight”,plantphysiol.(1973)51,723-726)。
提取物制备方法也会影响尼古丁含量,特别是浸渍时间和条件、灭菌方法以及物理和化学分离。
如申请pct/fr2007/000786中所述的烟草提取物包含低分子量的分子,即小于10kda。这些低分子量分子包括烟草特有的n-亚硝胺(tsna)和n-亚硝基氨基酸,其衍生自非挥发性生物碱、挥发性醛、多核芳烃(如苯并[a]芘)、内酯、尿烷或金属如镉等(参见wagner等人,plantphysiol.1986,82,274–279和iarcmonographsontheevaluationofcarcinogenicriskstohuman,vol.49)。这些化合物可具有致癌性、致突变性或毒性,且可导致癌症以及肾脏和骨骼问题。因此,这些化合物对已经被给予含有所述化合物的组合物的患者的健康有害。
这种烟草提取物包含多种具有所有分子量的蛋白质。例如,swiss-prot数据库识别759种烟草蛋白。仅rubisco蛋白可代表30-50%的可溶性蛋白质。完整的rubisco蛋白通常具有8个亚单元,形成约540kda的蛋白质复合物。以溶液行驶皮下给药的这些蛋白质的毒性是未知的,尽管没有迹象表明它们中的全部或部分可参与到任何治疗效果中。
本发明的目的是提供有效的烟草成瘾治疗。有利地,该治疗是无毒的,患者耐受良好,并且通过尽可能多地减少原则上不具有治疗效果的未知毒性分子的施用而具有有限的风险。
尽管烟草提取物含有数千种化合物,但申请人惊奇地发现来自烟叶提取物的蛋白质诱导特异性igg免疫应答,其促进戒烟。因此,根据本发明的包含高蛋白质含量和特定蛋白质组成的烟叶提取物诱导促进戒烟的特异性igg免疫应答。
这一发现更令人惊讶,因为水性烟叶提取物含有数千种化合物,其中蛋白质仅构成其中一类化合物。并不知道烟草蛋白质在烟草成瘾中起作用,因此没有动机将它们用于戒烟。
申请人特别指出,根据本发明的烟叶提取物具有高蛋白质含量和特定蛋白质组成。当使用经过干燥的烟叶时,可以显著地获得这种特定的蛋白质组成。干燥(curing)促进蛋白质的降解,例如通过水解机制,以及烟叶中游离氨基酸的增加(hamilton&lowe,1978;long&weybrew,1981;burton等人,1983)。
申请人惊奇地发现,根据本发明的来自烟叶提取物的蛋白质诱导促进戒烟的特异性igg抗体的产生。申请人显示,根据本发明的烟叶提取物的施用诱导特异性igg免疫应答并且使得可以获得对烟草成瘾的有效治疗,甚至不须向提取物添加可以促进免疫应答的辅助剂。申请人表明,当使用干燥的烟叶的提取物时,特异性igg免疫应答、烟草成瘾治疗和戒烟特别有效。
该发现更加令人惊讶,因为现有技术中没有任何内容表明对烟叶提取物蛋白质特异的igg抗体可能有助于吸烟者减少或停止吸烟。到目前为止,从未描述过在施用烟草提取物后特异性igg免疫应答的激活和烟草提取物在戒烟中的作用。迄今为止,从未描述过免疫系统(特别是涉及特异性igg抗体的产生)和可以促进戒烟的神经系统(特别是涉及吸烟和行为的感知)之间的这种联系。
有利地,根据本发明的烟草成瘾的治疗仅需要施用几次本发明的药物组合物,有利地仅施用一次,使得患者不再感觉到香烟的强化效果或者感觉显著减少,尤其是吸烟的冲动(正强化)和香烟的适口性降低。
技术实现要素:
在第一方面,本发明涉及烟叶提取物,其基于干燥提取物的总重量包含至少5重量%的分子量大于10kda的蛋白质,且基本上不含分子量小于10kda的分子。优选地,所述蛋白质选自以下蛋白质家族:形成木质素的阴离子过氧化物酶、葡聚糖内切-1,3–β–葡萄糖苷酶、内切几丁质酶、发病机理相关的蛋白质、渗调蛋白(osmotin)和蛋白酶抑制剂及其混合物。
本发明进一步涉及包含所述烟叶提取物的药物组合物及其治疗烟瘾的用途。
本发明还涉及包含所述烟叶提取物的药物组合物及其在戒烟中的用途。
本发明还涉及一种治疗烟瘾的方法,包括将所述烟叶提取物给予患有烟草成瘾或依赖的受试者。
本发明还涉及一种治疗烟瘾的方法,该方法包括将包含所述烟叶提取物的所述药物组合物给予患有烟草成瘾的受试者。
在本发明的上下文中,烟草依赖或成瘾的治疗包括所有形式的烟草消费,即吸烟的烟草,以制造或卷起的香烟、小雪茄或雪茄、烟斗烟草的形式,以及无烟烟草如鼻烟、咀嚼烟草或湿鼻烟(snus)。
本发明还涉及制备所述烟叶提取物的方法,所述烟叶提取物基于干燥提取物的总重量含有至少5重量%的分子量大于10kda的蛋白质,且基本上不含分子量小于10kda的分子,该方法包括以下步骤:
a.将烟叶干燥,
b.研磨干燥的烟叶以获得磨碎的干燥烟叶,
c.在机械搅拌下用溶剂,例如水性溶剂,优选ph为6.0-8.5的水性缓冲溶液,提取研磨的干燥烟叶,
d.通过过滤或离心从研磨的干燥烟叶提取物溶液中分离固体残余物,以获得不含固体残余物的研磨的干燥烟叶提取物溶液,
e.将步骤d中得到的溶液用溶剂,优选水性溶剂,以恒定体积过滤,所述溶剂的量为2至12倍体积,优选3至10倍体积,优选4至8倍体积,优选6倍体积,基于提取物的体积,且使用10kda截留膜,
f.任选地冻干步骤e中获得的蛋白质溶液。
本发明还涉及试剂盒,其包含含所述烟叶提取物的药物组合物,所述烟叶提取物基于干燥提取物的总重量含有至少5重量%的分子量大于10kda的蛋白质,且基本上不含分子量小于10kda的分子。
附图说明
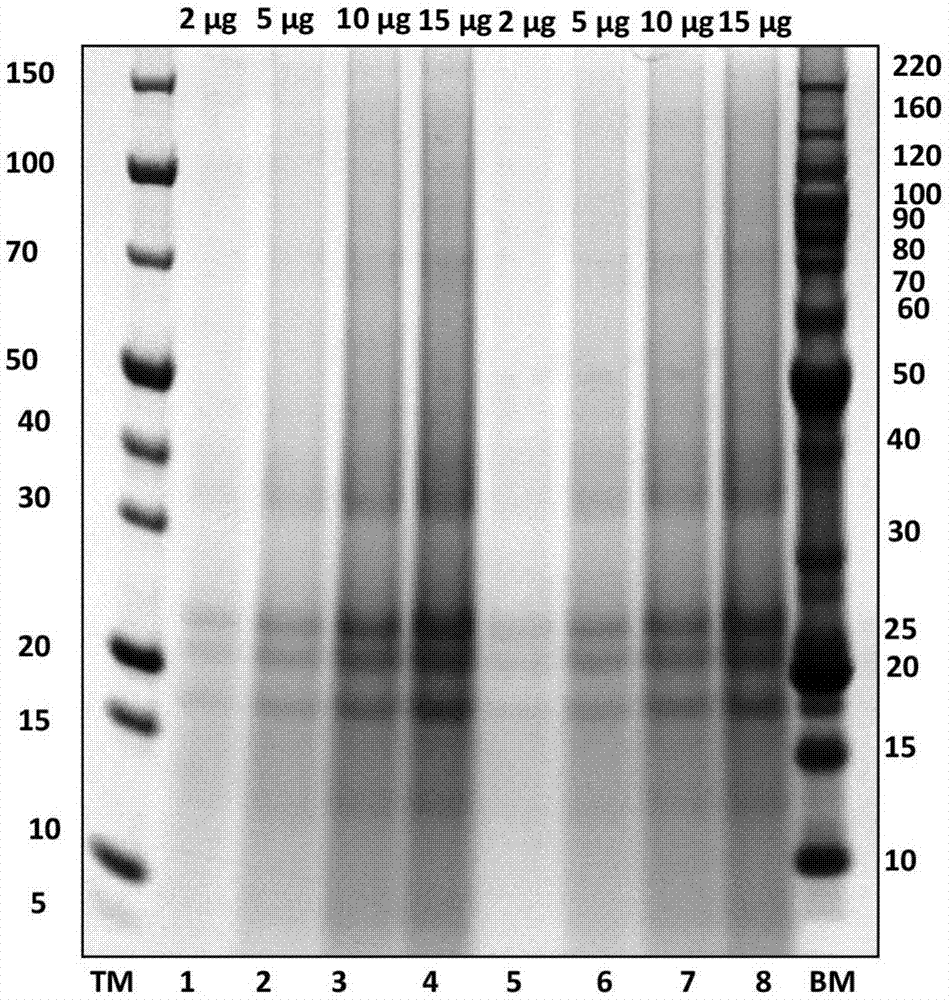
图1.根据实施例1的烟叶提取物的电泳图谱的示例:在mes缓冲液中和在还原剂存在下在4%-12%nupage凝胶上分级分离。
图2.在小鼠中注射根据实施例1的烟叶提取物后的igg诱导。
图3.用于表征活化的免疫细胞的免疫表型分析图示。
图4.根据实施例1的烟叶提取物对自然杀伤细胞的活化。
图5.根据实施例1的烟叶提取物对t和b淋巴细胞的活性。
图6.根据实施例1的烟叶提取物对促炎细胞因子和ifnγ的诱导。
图7.根据实施例1的烟叶提取物对th2细胞因子和趋化因子和造血生长因子的诱导。
图8和9.通过施用根据实施例1的烟叶提取物治疗的患者的烟草消费变化。
发明详述
烟叶提取物
本发明涉及烟叶提取物,其基于干燥提取物的总重量包含至少5重量%、优选至少10重量%、优选至少15重量%、优选约20重量%的分子量大于10kda的蛋白质,且基本上不含分子量小于10kda的分子。
干燥提取物有利地在根据本发明的烟叶提取物被冻干之前获得,然后置于真空钟形罩下,优选在p2o5存在下,直至获得恒定质量的提取物。
有利地,基于提取物的总重量,分子量小于10kda的分子的含量小于5重量%,优选小于2.5重量%,更优选小于1重量%。
出于本发明的目的,由于测量不确定性,“约”意味着加或减1%。
在烟叶提取物中通常测量的分子量大于10kda的蛋白质的含量为约1%。因此根据本发明的烟叶提取物具有的分子量大于10kda的蛋白质的含量远大于之前已知的。
优选地,根据本发明的提取物中存在的蛋白质选自以下蛋白质家族:形成木质素的阴离子过氧化物酶、葡聚糖内切-1,3–β–葡萄糖苷酶、内切几丁质酶、发病机理相关的蛋白质、渗调蛋白和蛋白酶抑制剂及其混合物。
对于根据本发明的提取物中存在的蛋白质所指示的名称对应于swiss-prot数据库中给出的名称,swiss-prot数据库是列出蛋白质序列的生物学数据库。
根据一个实施方案,根据本发明的烟叶提取物包含至少一种属于葡聚糖内切-1,3–β–葡萄糖苷酶家族的蛋白质,且优选选自β–1,3–内切葡聚糖酶酸性亚型pr–q′(根据uniprot数据库的pr36401)、β–1,3–内切葡聚糖酶碱性空泡亚型glb(根据uniprot数据库的p27666),及其混合物。
根据一个实施方案,根据本发明的烟叶提取物包含至少一种属于内切几丁质酶家族的蛋白质,且优选选自酸性内切几丁质酶p(根据uniprot数据库的p17513)、酸性内切几丁质酶q(根据uniprot数据库的p17514)、内切几丁质酶b(根据uniprot数据库的p24091),及其混合物。
根据一个实施方案,根据本发明的烟叶提取物至少包含渗调蛋白(根据uniprot数据库的p14170)。
根据一个实施方案,根据本发明的烟叶提取物包含至少一种形成木质素的阴离子过氧化物酶(根据uniprot数据库的p11965)。
根据一个实施方案,根据本发明的烟叶提取物包含至少一种发病机理相关的蛋白质,且优选选自发病机理相关的蛋白质r(根据uniprot数据库的p13046)、发病机理相关的蛋白质pr–4a(根据uniprot数据库的pr29062)、发病机理相关的蛋白质pr–4b(根据uniprot数据库的pr29063),及其混合物。
根据一个实施方案,根据本发明的烟叶提取物包含至少一种属于蛋白酶抑制剂家族的蛋白质,且优选选自蛋白酶抑制剂i–b(根据uniprot数据库的q03199)、蛋白酶抑制剂i–a(根据uniprot数据库的q03198),及其混合物。
根据一个实施方案,所述烟叶提取物还包含分子量大于10kda且优选为水溶性的多糖。
优选地,根据本发明的烟叶提取物基于干燥提取物的总重量包含至少5重量%,优选至少10重量%,优选至少15重量%,优选约20重量%的选自以下蛋白质家族的蛋白质:形成木质素的阴离子过氧化物酶、葡聚糖内切-1,3–β–葡萄糖苷酶、内切几丁质酶、发病机理相关的蛋白质、渗调蛋白和蛋白酶抑制剂及其混合物。
根据一个实施方案,根据本发明的烟叶提取物基本上不含高分子量蛋白质。
出于本发明的目的,“高分子量蛋白质”是指分子量大于500kda的蛋白质,优选分子量大于400kda的蛋白质,更优选分子量大于300kda的蛋白质,优选分子量大于200kda的蛋白质,还更优选分子量大于150kda的蛋白质,且更优选分子量大于100kda的蛋白质。
根据一个实施方案,根据本发明的烟叶提取物基本上不含分子量大于50kda的蛋白质。
出于本发明的目的,“基本上不含”是指分子含量少于15重量%,基于提取物的总蛋白重量,优选分子含量少于10重量%,基于提取物的总蛋白重量,更优选小于7.5重量%,基于提取物的总蛋白重量,更优选小于5重量%,基于提取物的总蛋白重量,优选小于2.5重量%,基于提取物的总蛋白重量,更优选小于1重量%,基于提取物的总蛋白重量,且还更优选小于0.5重量%,基于提取物的总蛋白重量。
有利地,高分子量蛋白质的含量少于15重量%,基于提取物的总蛋白重量,优选小于10重量%,基于提取物的总蛋白重量,更优选小于7.5重量%,基于提取物的总蛋白重量,更优选小于5重量%,基于提取物的总蛋白重量,优选小于2.5重量%,基于提取物的总蛋白重量,更优选小于1重量%,基于提取物的总蛋白重量,且还更优选小于0.5重量%,基于提取物的总蛋白重量。
根据一个实施方案,根据本发明的烟叶提取物基本上不含rubisco蛋白质。
根据一个实施方案,烟叶是普通烟草(nicotianatabacum)种或黄花烟草(nicotianarustica)种。烟叶可以来自棕色或金色烟草,并且可以选自弗吉尼亚烟草、白肋烟、东方烟草、拉塔基亚(latakia)烟草、百里科(perique)烟草、马里兰烟草、肯塔基烟草、加州烟草、texmex烟草及其混合物。
当然,提取物不一定由烟叶的纯提取物组成,并且添加从大麻中提取的蛋白质以处理烟草和大麻依赖性。
根据一个具体实施方案,烟草叶提取物得自棕色烟草、弗吉尼亚烟草和白肋烟草的1/1/1混合物。
根据一个具体实施方案,该烟叶提取物获自白肋烟草。
根据一个实施方案,该烟叶提取物获自干燥的烟叶。
根据一个具体实施方案,该烟叶提取物获自晾制的(air–cured)烟叶。
根据一个具体实施方案,烟叶提取物是从烟叶中获得的,所述烟叶晾制达适合于当地气候条件的一段时间,优选最少持续一个月。
出于本发明的目的,“晾制”或“自然干燥(naturalcuring)”是指在天然室外或室内空气存在下进行干燥。晾制可以在开放或封闭、覆盖或未覆盖的结构中进行。晾制可以例如在自然干燥室中进行。在这种情况下,新鲜收集或预先干燥的烟叶在露天的作用下自然干燥。烟叶可以例如悬挂在未加热的通风室中。烟叶可以例如自然地干燥直到它们变成棕色。在这个阶段,叶子中几乎没有糖。有利地,干燥进行达适合于当地气候条件的一段时间,优选最少持续一个月。举例来说,可在9月至12月期间对法国中部的收获物进行干燥。在干燥期间,烟叶可以转动或充气一次或多次,以允许均匀的干燥并避免形成凝聚和叶子的腐烂或降解。晾制方法可用于例如白肋烟品种。
根据一个具体实施方案,烟叶提取物获自在自然干燥室中干燥的烟叶。
根据另一具体实施方案,该烟叶提取物获自在加热的干燥室中干燥的烟叶。在该情况下,干燥可在加热至合适的温度的室或结构中进行。
根据另一个具体实施方案,烟叶提取物获自烟熏的烟叶。在这种情况下,干燥可以在加热到合适温度的结构或室中进行。可以通过连接到外部热源的管道将热量引入结构或室中。这种受控的加热产生黄橙色叶子。因此这些叶子含有高糖含量。例如,弗吉尼亚烟草可以根据该方法进行干燥。
根据另一个具体实施方案,烟叶提取物获自晒干的烟叶。在这种情况下,烟叶可以铺在架子上并暴露在阳光下12到30天。在来自太阳的直接光照和热量下,叶子变成黄色或橙色,并保持高糖含量。通常使用这种方法干燥东方烟草。
根据另一个具体实施方案,烟叶提取物获自火烤烟叶。在这种情况下,小块木头可以在烟叶下面燃烧,这种烟叶在吸收“烟熏”香气的同时干燥。
根据本发明的烟叶提取物有利地是水性提取物。
根据本发明的烟叶提取物有利地为棕色的水性提取物。
优选地,烟叶提取物可以通过以下获得:将研磨的干燥烟叶经受溶剂提取方法,例如水性溶剂,然后从研磨的干燥烟叶提取物溶液中分离固体残余物,然后用水性溶剂对不含固体残余物的研磨的干燥烟叶提取物溶液进行恒定体积渗滤,水性溶剂的量为2至12倍体积,优选3至10倍体积,优选4至8倍体积,优选6倍体积,基于提取物的体积,且使用10kda截留膜。
当然,可以使用其他类型的溶剂来进行烟叶提取物的提取过程。步骤c的提取可以用有机或无机溶剂,或用有机和/或无机溶剂的混合物进行。
为了确保良好的提取效率和产率,并获得具有所需纯度性质和组成的优质提取物,本领域技术人员将容易地知道如何根据以下标准选择合适溶剂:
-溶剂或溶剂混合物的极性(极性或非极性);
-溶剂或溶剂混合物的物理状态(例如液体,固体,超临界或气体);
-溶剂或溶剂混合物的化学性质(例如有机或无机);
-溶剂或溶剂混合物的电荷(例如离子或非离子);
-溶剂或溶剂混合物的来源;
-溶剂或溶剂混合物的混溶性;
-溶剂或溶剂混合物的溶解度。
基于所需的提取产率和提取物纯度和组成,本领域技术人员将知道使用哪种技术来选择对应于其标准的溶剂。
有利地,根据本发明的烟叶提取物通过下面描述的烟叶制备方法获得。
药物组合物
在第二方面,本发明涉及包含上述烟叶提取物作为活性成分的药物组合物。
根据本发明的药物组合物进一步包含至少一种药物可接受的赋形剂,如药物可接受的溶剂,且例如水。
有利地,该药物组合物包含的根据本发明的烟叶提取物中存在的蛋白质的含量为1至1000μg/ml,优选10至500μg/ml,优选50至300μg/ml,优选60至200μg/ml,优选80至150μg/ml。
根据本发明的药物组合物优选为水性组合物。
根据一个具体实施方案,药物组合物可进一步包含作用于负强化的活性剂,如例如尼古丁替代物、伐尼克兰或安非他酮。
根据一个实施方案,药物组合物进一步包含辅助剂。辅助剂的实例包括:膨胀剂,例如糖如乳糖、蔗糖、海藻糖、山梨醇、葡萄糖、棉子糖、甘露醇,优选乳糖、蔗糖、海藻糖、葡萄糖或甘露醇,氨基酸如精氨酸、甘氨酸或组氨酸,优选甘氨酸,或葡聚糖或聚乙二醇类型的聚合物,或其混合物。根据该实施方案,药物组合物包含50至99重量%的辅助剂,优选80至97重量%,基于药物组合物的总重量。
根据一个具体实施方案,该药物组合物可进一步包含从大麻提取的蛋白质.
根据一个实施方案,根据本发明的药物组合物以适于皮下施用的形式提供。
根据另一个实施方案,所述药物组合物以适于通过粘附性透皮治疗系统给药的形式提供。有利地,药物组合物以贴剂形式提供。
根据另一个实施方案,药物组合物以适于通过喷雾或通过汽化给药的形式提供。有利地,药物组合物以喷涂器、蒸发器或喷雾器形式提供。
根据本发明的药物组合物优选根据制备包含下述烟叶提取物的药物组合物的方法制备。
药物组合物的用途
在第三方面,本发明涉及该药物组合物用于治疗烟草成瘾的用途。
出于本发明的目的,“治疗烟草成瘾”或“治疗烟草依赖”更准确地意味着减少香烟的成瘾强化。根据本发明的药物组合物的施用显著地减少了香烟的正强化,特别是吸烟的冲动。
本发明还涉及包含如上定义的烟叶提取物的组合物,其用于治疗烟草成瘾。
换句话说,本发明还涉及治疗烟草成瘾或依赖的方法,包括施用包含如上定义的烟叶提取物的组合物。
有利地,根据本发明的组合物的施用使得患者能够通过减弱烟草的正强化并且特别是吸烟的冲动来停止吸烟、减少其消费或防止其复发,从而促进戒烟。有利地,组合物的施用有助于任何类型的吸烟者(即包括重度吸烟者)戒烟并减少或避免戒烟后的复发。
有利地,根据本发明施用还包含从大麻中提取的蛋白质的组合物,使得可以同时治疗对烟草和大麻的依赖性或成瘾性。
根据一个实施方案,根据本发明的组合物通过皮下注射给药。根据该实施方案,该药物组合物以适合皮下给药的形式提供。
根据一个实施方案,该药物组合物以0.03ml至10ml、优选0.1ml至5ml、优选0.5至2ml的剂型提供。因此该药物组合物优选以0.03ml至10ml、优选0.1至5ml、优选0.5ml至2ml的量通过皮下注射给药。
根据一个实施方案,根据本发明的组合物通过包含如上定义的烟叶提取物的粘附透皮治疗系统施用。根据该实施方案,药物组合物以适于通过粘附透皮治疗系统施用的形式提供。有利地,药物组合物以贴剂形式提供。
贴剂可以是具有一个或多个隔室的储库型贴片或基质型贴片的形式。贴片的实际执行将由本领域技术人员基于他对受试者的一般知识来确定,以在贴剂施用的整个期间获得受控制的和延长的烟叶提取物的全身给药,例如持续约2小时至24小时。
储库型贴剂包括一个或多个单独的储库,其在溶液中含有活性成分(包括烟叶提取物),或活性成分悬浮在聚合物基质中,通过半透性聚合物膜与皮肤接触,使得可以调整活性成分的释放率。
基质型贴剂将包含聚合物质,其中活性成分将以适当的比例溶解或分散。这些活性成分通过扩散通过所述基质的聚合物链而释放。
根据这种类型贴剂的特定实施方案,粘合剂覆盖基质的整个释放表面并且是后者的组成部分。因此,本领域技术人员已知这种活性粘合剂型贴片,其制造简化并且允许产生薄的、适当柔性的贴片,从而允许在患者皮肤上舒适地施用。
为了确保以适当的剂量、以适当的扩散速率和适当的持续时间皮下或在血流中良好地输注这些活性成分,本领域技术人员可以容易地设定以下参数:
-贴片的每个隔室的表面积和体积的比率;
-任选加入一种或多种亲水性添加剂;
-任选加入一种或多种扩散活化剂或抑制剂;
-任选加入一种或多种增溶剂;
-任选加入一种或多种稳定剂;
-任选加入一种或多种吸收促进剂,和;
-更一般地,本领域技术人员熟知的所有类型的允许良好地控制烟叶提取物的流动和稳定性的添加剂。
本领域技术人员将基于所需的溶解度和稳定性知道使用哪种技术来设定上面列出的参数。
本领域技术人员可以容易地调整贴剂的各种制造参数以达到所需剂量。
以本身已知的方式,这种贴片包括可移除的保护膜,该保护膜用于在制造贴片之后和整个储存期间保护待施加到皮肤上的粘合剂侧。以本身已知的方式,本领域技术人员将例如使用聚酯薄膜,其一侧可用抗粘附的硅酮处理。
根据另一个实施方案,根据本发明的组合物通过含有如上定义的烟叶提取物的喷雾或蒸发系统施用。根据该实施方案,药物组合物以适于通过喷雾或蒸发施用的形式提供。有利地,药物组合物以喷涂器、蒸发器或喷雾器形式提供。
喷涂器、蒸发器或喷雾器可以是具有带有一个或多个隔室的储库的喷涂器、蒸发器或喷雾器的形式。喷涂器、蒸发器或喷雾器的实际执行将由技术人员基于其对受试者的一般知识来确定,以获得烟叶提取物的受控和延长的全身给药。
喷涂器、蒸发器或喷雾器将具有一个或多个单独的储库,所述储库包含溶液或悬浮液中的活性成分(包括烟叶提取物)。然后通过在待治疗的身体区域上喷雾或蒸发施用活性成分。喷雾或蒸发可以例如在皮肤上进行。活性成分可以通过喷雾或蒸发到粘膜中来施用。
为了确保以适当的剂量、以适当的扩散速率和适当的持续时间皮下或在血流中良好地输注这些活性成分,本领域技术人员可以容易地设定以下参数:
-喷涂器、蒸发器或喷雾器的每个隔室或储库的表面积和体积的比率;
-任选添加一种或多种亲水性添加剂;
-任选添加一种或多种扩散活化剂或抑制剂;
-任选添加一种或多种增溶剂;
-任选添加一种或多种稳定剂;
-任选添加一种或多种吸收促进剂,和;
-更一般地,本领域技术人员熟知的所有类型的允许良好地控制烟叶提取物的流动和稳定性的添加剂。
本领域技术人员将基于所需的溶解度和稳定性知道使用哪种技术来设定上面列出的参数。
本领域技术人员可以容易地调整喷涂器、蒸发器或喷雾器的不同制造参数以达到所需剂量。
根据第一个实施方案,药物组合物以旨在仅施用一次的形式提供。根据该实施方案,药物组合物仅施用一次,因此允许减少或抑制烟草的正强化,特别是吸烟的冲动。
根据另一个实施方案,药物组合物以旨在施用数次、优选两次或三次的形式提供。根据该实施方案,药物组合物优选在第0天和第10天,或第0、10和30天施用,从而允许减少或抑制烟草的正强化,特别是吸烟的冲动。在该实施方案中,第二次注射和任选第三次注射的剂量与第一次注射的剂量相同。
根据一个具体实施方案,根据本发明的药物组合物可以与包含作用于负强化的活性剂的组合物一起施用,所述活性剂例如尼古丁替代品、伐尼克兰、安非他酮或其混合物。根据该实施方案,可以设想几种特定的给药模式:
(i)在尝试戒烟之前,施用根据本发明的药物组合物以减少香烟消费,然后施用作用于负强化的活性剂以限制负强化的作用,特别是戒断感觉;
(ii)在试图戒烟时同时施用本发明的药物组合物和作用于负强化的活性剂,目的是立即戒烟;
(iii)在尝试戒烟时施用作用于负强化的活性剂,例如试图戒烟后持续达12周,然后施用本发明的药物组合物,例如在施用作用于负强化的活性剂结束后持续达2周,目的是防止复发。
烟叶提取物的制备
在第四方面,本发明涉及根据本发明的烟叶提取物的制备。
有利地,制备根据本发明的烟叶提取物的方法包括以下步骤:
a.干燥烟叶,
b.研磨干燥的烟叶以获得研磨的干燥烟叶,
c.在机械搅拌下用溶剂,例如水性溶剂,优选ph为6.0-8.5的水性缓冲溶液,提取研磨的干燥烟叶,
d.通过过滤或离心从研磨的干燥烟叶提取物溶液中分离固体残余物,以获得不含固体残余物的研磨的干燥烟叶提取物溶液,
e.将步骤d中得到的溶液用溶剂,优选水性溶剂,以恒定体积过滤,所述溶剂的量为2至12倍体积,优选3至10倍体积,优选4至8倍体积,优选6倍体积,基于提取物的体积,且使用10kda截留膜,
f.任选地冻干步骤e中获得的蛋白质溶液。
根据一个具体实施方案,步骤a的干燥在露天进行,称为自然干燥。在这种情况下,干燥在室外或室内在自然露天存在下进行。干燥可以在开放或封闭、覆盖或未覆盖的结构中进行。晾制可以例如在自然干燥室中进行。在这种情况下,新鲜收集的或预先干燥的烟叶在露天的作用下自然干燥。烟叶可以例如悬挂在未加热的通风室中。例如,烟叶可以自然干燥,直到它们变成棕色。在这个阶段,叶子中几乎没有糖。有利地,进行干燥达适合于当地气候条件的一段时间,优选最少持续一个月。举例来说,可以在9月至12月期间对法国中部的收获物进行干燥。在干燥期间,烟叶可以翻动一次或多次,以便允许均匀的干燥并避免形成凝聚和叶子的腐烂或降解。晾制方法可用于例如白肋烟品种。根据一个具体实施方案,步骤a的干燥在自然干燥室中进行。
根据另一具体实施方案,步骤a的干燥在加热的干燥室中进行。在该情况下,干燥可在加热至合适的温度的室或结构中进行。
根据另一个具体实施方案,步骤a的干燥通过烟熏进行。在这种情况下,干燥可以在加热到合适温度的结构或室中进行。可以通过连接到外部热源的管道将热量引入结构或室中。这种受控的加热产生黄橙色叶子。因此这些叶子含有高糖含量。例如,弗吉尼亚烟草可以根据该方法进行干燥。
根据另一个具体实施方案,步骤a的干燥通过晒干进行。在这种情况下,烟叶可以铺在架子上并暴露在阳光下12到30天。在来自太阳的直接光照和热量下,叶子变成黄色或橙色,并保持高糖含量。使用这种方法通常可以干燥东方烟草。
根据另一个具体实施方案,步骤a的干燥通过火烤进行。在这种情况下,小块木头可以在烟叶下面燃烧,这种烟叶在吸收“烟熏”气味的同时干燥。
有利地,步骤a的干燥促进高分子量烟草蛋白质,如rubisco的降解,例如通过水解机理。
步骤c至e对应于专利us5,770,698(第6栏第47行至第7栏第7行)和专利申请us2009/0162403([0032]至[0040]段)中所述类型的萃取、过滤和渗滤步骤。
优选地,步骤c中的提取在4至20℃,优选4至10℃的温度进行。
优选地,步骤c中的提取进行12至36h,优选22至26h,优选24h。
根据一个具体实施方案,步骤c中使用的溶剂为水性溶剂。优选地,步骤c中使用的水性溶剂为碳酸氢铵的水性缓冲溶液,优选浓度为2至6g/l,优选4g/l。
当然,可以使用其他类型的溶剂来进行步骤c的提取。步骤c的提取可以用有机或无机溶剂,或用有机和/或无机溶剂的混合物进行。
为了确保良好的提取效率和产率,并获得具有所需纯度性质和组成的优质提取物,本领域技术人员将容易地知道如何根据以下标准选择合适的溶剂:
-溶剂或溶剂混合物的极性(极性或非极性);
-溶剂或溶剂混合物的物理状态(例如液体、固体、超临界或气体);
-溶剂或溶剂混合物的化学性质(例如有机或无机);
-溶剂或溶剂混合物的电荷(例如离子或非离子);
-溶剂或溶剂混合物的来源;
-溶剂或溶剂混合物的混溶性;
-溶剂或溶剂混合物的溶解度。
基于所需的提取产率和提取物纯度和组成,本领域技术人员将知道使用哪种技术来选择对应于这些标准的溶剂。
优选地,步骤c中的提取通过将研磨的干燥烟叶悬浮在缓冲溶液中进行,优选研磨的干燥烟叶在缓冲溶液中的浓度为30至70g/l,优选40至60g/l,且更优选50g/l。然后通过过滤除去悬浮的固体残余物,例如通过büchner过滤(步骤d),以获得无固体残余物的研磨的干燥烟叶。
优选地,步骤d中使用的水性溶剂为注射用水(wfi)。
有利地,步骤e除去超过99%的分子量小于10kda的分子,特别是游离氨基酸、分子量小于10kda的分子量的蛋白质和肽、以及由步骤a的蛋白质降解产生的分子量小于10kda的蛋白质残余物。
优选地,在步骤f之前,将步骤e中获得的蛋白质溶液进行灭菌过滤的步骤e'。
在上述方法结束时获得的根据本发明的烟叶提取物可以如在灭菌过滤步骤d'结束时获得的那样储存,或者如在步骤f结束时获得的那样被冻干。
制备包含烟叶提取物的药物组合物
在第五方面,本发明涉及包含根据本发明的烟叶提取物的药物组合物的制备。
药物组合物可通过包括以下步骤的方法制备:
a.制备如上定义的烟叶提取物,
b.调节蛋白质浓度以获得100至200μg/ml的蛋白质浓度,
c.添加药学上可接受的赋形剂,和
d.任选地,向该提取物中加入辅助剂,优选加入甘露醇。
步骤b中使用的烟叶提取物可以是在10kda截留膜上的渗滤步骤之后直接获得的烟叶提取物,或者是在灭菌渗滤步骤之后获得的烟叶提取物,或者是冻干然后例如在盐水溶液或水中重构的烟叶提取物。
有利地,可以通过以下调节步骤b中的浓度:
-通过用水稀释以降低蛋白质浓度,
-或通过渗滤以增加蛋白质浓度。
步骤c中特别优选的药学上可接受的赋形剂是水。
可以在步骤d中添加的辅助剂可以特别是膨胀剂,例如糖如乳糖、蔗糖、海藻糖、山梨醇、葡萄糖、棉子糖、甘露醇,优选乳糖、蔗糖、海藻糖、葡萄糖或甘露醇,氨基酸如精氨酸、甘氨酸或组氨酸,优选甘氨酸,或葡聚糖或聚乙二醇类型的聚合物;或其混合物。
根据一个具体实施方案,步骤d至少包括添加甘露醇。
含有包含烟叶提取物的药物组合物的试剂盒
在第六方面,本发明涉及一种试剂盒,其包含一定剂量的烟叶提取物或根据本发明的药物组合物。
根据第一实施方案,所述试剂盒包含一个或多个剂量的烟叶提取物,优选冻干形式,以及一个或多个剂量的盐水溶液或wfi,以在紧接施用之前制备根据本发明的药物组合物。
根据另一个实施方案,所述试剂盒包含一个或多个剂量的药物组合物,随时准备施用于患者。
试剂盒可任选地包含一个或多个注射器,以通过皮下注射施用药物组合物。
试剂盒可任选地包含一个或多个贴剂,以便经皮施用药物组合物。
以下实施例旨在说明本发明。
实施例
实施例1:制备根据本发明的烟叶提取物
白肋烟叶用于制备提取物。
将100克自然干燥约三个月(法国中部,9月至12月)的白肋烟烟叶研磨。将研磨的叶子在4至10℃的温度下在加入8g碳酸氢铵的1892gwfi中悬浮24小时。然后通过布氏(büchner)过滤除去悬浮的固体残余物。
然后对提取物进行0.2μm澄清过滤。获得的提取物是棕色的。然后将提取物称重以确定在恒定体积渗滤步骤中使用的wfi的体积;在这种情况下,液体提取物的质量为1680g。
然后进行该无固体残余物的研磨的烟叶提取物的蛋白质的提取:然后将10080gwfi加入到不含固体残余物的研磨的干燥烟叶提取物中。将如此获得的11760g溶液以恒定体积相对6倍体积渗滤,截留10kda(merckmillipore),直至渗余物的质量减少至1680g。
渗滤后得到的渗余物是蛋白质混合物,其中检测到的分子量小于10kda的蛋白质的浓度比其初始浓度低99%。根据europeanpharmacopoeia5.0,2.2.2,degreeofcolorationofliquids中定义的测量标度,获得的渗余物的颜色在b2和b3之间。
在使用smh150冻干机加入例如甘露醇后,可以将该渗滤物冻干,得到冻干的烟叶提取物。
实施例2:测定根据实施例1制备的烟叶提取物的蛋白质组成
首先在聚丙烯酰胺凝胶上分离实施例1的烟叶提取物的蛋白质。为此,将待分析的提取物加入
将如此获得的蛋白质溶液用酶消化以获得蛋白质或肽片段:用胰蛋白酶(胰蛋白酶v5111,promega)进行消化,其量适于在50mmnh4co3溶液中在37℃下染色聚丙烯酰胺凝胶条带过夜。
然后通过液体纳米色谱法(u3000nanolcsystem,thermofischerscientific)分离肽消化物的肽,在pepmapc18微前置柱(5μm;
然后在配备有纳米喷雾源(thermofisherscientific)并连接到u3000nanolc装置的ltqvelos仪器(双压线性离子阱;thermofisherscientific)上通过质谱法分析肽。使用excalibur2.1软件(thermofisherscientific)以正模式获取数据,其中通过从m/z400到1600以“分辨率增强”模式进行ms扫描循环,然后在“正常分辨率”模式下对20个最强ms离子(电荷2和更高)以cid模式在氦气下进行msms扫描,碰撞能量为35ev。此前碎片化的ms离子被动态排除30秒,质量公差为50mmu。
为了鉴定目的,将肽及其片段的质量与数据库中的现有数据进行比较。为此,根据mascot搜索算法(版本2.4),使用proteomediscoverer1.4软件处理ms和msms数据,且查询被减少到tobac物种的uniprotkb/swiss–prot数据库(2015年4月发布)。
根据小于0.05的置信度值p验证蛋白质的鉴定。仅保留用至少2种具有最大置信度的肽鉴定的蛋白质。
如此鉴定的每种蛋白质的得分仅允许它们之间的蛋白质的相对分类,该分类与这些蛋白质的浓度相关。这些得分的绝对值取决于操作条件、测试样品和沉积量。
这样按其得分的降序(从最多存在到最少存在)鉴定和分类的12种蛋白质的列表如下:
p36401;e13h_tobac;葡聚糖内切-1,3–β–葡萄糖苷酶,酸性亚型pr–q′(ec3.2.1.39)((1–>3)–β–葡聚糖内切水解酶)((1–>3)–β–葡聚糖酶)(β–1,3–内切葡聚糖酶)(pr–35);mm:36995da
p17513;chip_tobac;酸性内切几丁质酶p(ec3.2.1.14)(发病机理相关的蛋白质p)(pr–p);mm:27469da
p17514;chiq_tobac;酸性内切几丁质酶q(ec3.2.1.14)(发病机理相关的蛋白质q)(pr–q);mm:27633da
p27666;e13f_tobac;葡聚糖内切-1,3–β–葡萄糖苷酶,碱性空泡亚型glb(ec3.2.1.39)((1–>3)–β–葡聚糖内切水解酶)((1–>3)–β–葡聚糖酶)(β–1,3–内切葡聚糖酶,碱性)(葡聚糖酶glb);mm:40443da
p14170;osmo_tobac;渗调蛋白;mm:26681da
p24091;chi2_tobac;内切几丁质酶b(chn–b)(ec3.2.1.14);mm:34721da
p11965;perx_tobac;形成木质素的阴离子过氧化物酶(ec1.11.1.7)(topa);mm:34674da
p13046;prr1_tobac;发病机理相关的蛋白质r主要形式(索马甜样蛋白质e22);mm:24667da
p29062;pr4a_tobac;发病机理相关的蛋白质pr–4a;mm:16221da
q03199;ipib_tobac;蛋白酶抑制剂i–b(pi–ib)(微生物丝氨酸蛋白酶主要亚型的抑制剂);mm:11916da
q03198;ipia_tobac;蛋白酶抑制剂i–a(pi–ia)(微生物丝氨酸蛋白酶次要亚型的抑制剂);mm:11880da
p29063;pr4b_tobac;发病机理相关的蛋白质pr–4b;mm:16235da
因此,烟叶提取物制备方法可以浓缩一些蛋白质并除去其他蛋白质。因此,在swiss-prot中列出的759种普通烟草(nicotianatabacum)蛋白质中,根据实施例1制备的烟叶提取物中仅主要存在6种家族和12种蛋白质。主要存在于根据实施例1制备的烟叶提取物中的12种蛋白质的分子量在10到50kda之间。
实施例3:蛋白质含量的测定
根据实施例1的烟叶提取物(在渗滤步骤之前和之后)中的蛋白质含量根据bradford方法测定。
将实施例1的提取物溶解在盐水溶液中。
制备三种标准蛋白质溶液:将50μl的2mg/ml牛血清白蛋白溶液(sigmaaldrich,产品号p0834)用950μl盐水溶液稀释20倍,以获得恰好100μg/ml的标准化溶液。
每个测试的试管含有80μl蛋白质样品和920μlbradford试剂(sigmaaldrich产品号b6916)。将bradford试剂加入每个试管后,轻轻摇动试管以产生涡旋,然后在室温下温育5分钟。将样品转移至1.5ml比色皿中,并在595nm下测量它们的吸光度1小时。
蛋白质浓度通过与制备的标准蛋白质溶液比较而测定。
测量的蛋白质量为:
渗滤前:295.45+/–9.91μg/ml
渗滤后:160.61+/–1.31μg/ml。
在渗滤步骤后测定根据实施例1的烟叶提取物的电泳图谱。将2、5、10和15μg量的蛋白质沉积在nupage凝胶上。
制备4%-12%nupage凝胶35分钟,然后置于20ml考马斯蓝中1小时,并用水冲洗过夜。使用biorad’schemidoctmxrs系统和imagelabtm软件分析凝胶。
在15kda和30kda附近检测到三个主要条带(图1)。另外两个条带在约40kda时也是可见的。
结果表明,在该烟叶提取物中,检测到的分子量大于100kda的蛋白质的量少于分子量为10-50kda的蛋白质的量。
实施例4:渗滤体积对根据本发明的烟叶提取物中的分子量小于10kda的分子的去除的影响
根据实施例1的烟叶提取物中分子量小于10kda的分子的去除根据所用的渗滤体积在渗滤步骤中监测。通过分子量小于10kda的分析示踪剂(尼古丁)的气相色谱测试进行监测。
结果如下表所示:
当渗滤体积增加时,分子量小于10kda的分子的去除越来越有效,并且当该渗滤体积是初始体积的6倍时,上述分子被完全去除。
实施例5:实施例1的提取物对人单核细胞的体外生物活性和对小鼠的体内生物活性
材料和方法:
使用的产品
pma/离子霉素(sigma–aldrich产品号p8139/i0634)
bsa(sigmaaldrich产品号a7020)
pbs(paalaboratories产品号h15–002)
吐温20(sigmaaldrich产品号p1379)
山羊抗小鼠igg(g链特异性)–碱性磷酸酶(southernbiotech产品号1030–04)
生物素-抗小鼠ige(biolegend产品号ble406904)
链霉亲和素–碱性磷酸酶(southernbiotech产品号7100–04)
细胞制备和刺激模式
通过在密度梯度(分离培养基:lms1077paalaboratories)上离心来分离来自不同健康供体的外周血单核细胞。获得的单核细胞用不同稀释度的实施例1的提取物刺激24小时或48小时。取出上清液并在刺激24小时或48小时后在-80℃下储存,以用于使用luminex技术进行细胞因子谱分析。刺激24小时后,还通过流式细胞术采集细胞进行表型分析。
细胞计数表型分析
首先用活力标记物(dyeefluor450(65-0863-14ebioscience)染色细胞,然后用直接与荧光染料偶联的抗体检测不同的膜标记物。用标记cd3和cd19鉴定t和b淋巴细胞群。用标记物nkp46或标记物cd56和cd16的组合或通过cd56表达在不存在cd3的情况下检测nk细胞。从这些细胞群中,设置“门”以分析不同的活化标记物(cd69,cd25,hla-dr)。
用于表型细胞计数分析的抗体列表如下表所示:
在每个实验中使用同种型对照,并且为该多参数表型分析创建补偿矩阵。
在navios细胞计数器(beckmancoulter10-颜色)上分析染色的样品,每管最少采集100,000个事件。然后在kaluza软件上分析获得的数据。
通过luminex和elisa分析细胞因子分泌概况
该技术基于elisa和细胞计数原理,可以同时测试多种分析物。
将独特的颜色编码微珠偶联以捕获对每种分析物具有特异性的抗体。在与待测定的样品一起孵育后,与荧光染料偶联的检测抗体将允许通过双激光光学系统(bio-plex200系统bio-rad)进行分析。第一激光识别微珠,第二激光定量与荧光染料偶联的检测抗体。可以在对细胞进行的各种刺激实验期间采集的样品上用bio-plexprohumancytokinegrp1panel17plex试剂盒(bio-rad)测定17种分析物。由没有实施例1的烟叶提取物的培养基刺激的细胞使得可以获得每种细胞因子的基础水平。
il-8elisa基于常规免疫酶促夹心技术。使用的商业试剂盒购自eurobio-diaclone
用根据实施例1的烟叶提取物免疫小鼠
七周龄雌性c57bl/6和balb/c小鼠购自charlesriver(l'arbresles,france)。在第0天和第21天向腹膜内用200μl根据实施例1的烟叶提取物免疫小鼠,该烟叶提取物被冻干并在5ml盐水溶液中重构。在免疫之前和之后从所有小鼠收集血液。离心后,将血清在-20℃冷冻。
igg和igeelisa
对于elisa实验,将一小瓶产物用2.5ml碳酸盐-碳酸氢盐缓冲液(0.1m,ph9)重构。将nuncmaxisorb96w平板与100μl根据实施例1冻干的烟叶提取物一起孵育,然后重构并孵育18小时。用pbs–0.05%吐温缓冲液洗涤平板后,将板用200μlpbs-1%bsa缓冲液在室温下饱和1小时。用pbs-0.05%吐温缓冲液洗涤平板后,将100μl在pbs-1%bsa中稀释至1/20的小鼠血清在室温下温育2小时。
elisaigg:
用pbs-吐温20缓冲液洗涤后,将100μl与碱性磷酸酶(southernbiotechnology产品号1030-04)偶联并在pbs-1%bsa中稀释的山羊抗小鼠igg二抗在温度下孵育1小时。用pbs-0.05%吐温洗涤后,加入100μl碱性磷酸酶的对硝基苯磷酸底物(sigmapnpp),且在室温下避光15分钟。然后通过加入50μl3mnaoh终止反应,并在405nm处读取光密度(od)。
elisaige
用pbs-吐温20缓冲液洗涤后,将100μl与生物素(biolegend产品号ble406904)偶联并在pbs-1%bsa中稀释的大鼠抗小鼠ige二抗在室温下孵育1小时。用pbs-0.05%吐温洗涤后,加入100μl与碱性磷酸酶(southernbiotechnology产品号7100–04)偶联的链霉亲和素,且在室温下孵育1小时(根据供应商的推荐在pbs–1%bsa中稀释112000倍)。用pbs-0.05%吐温洗涤后,加入100μl碱性磷酸酶的pnpp底物,且在室温下避光15分钟。然后通过加入50μl3mnaoh终止反应,并在405nm处读取光密度(od)。
结果:
根据实施例1的烟叶提取物在小鼠中引起特异性igg体液应答。
用根据实施例1冻干并在5ml盐水溶液中重构的烟叶提取物对小鼠进行2次免疫后,观察到针对产物组分的igg诱导。因此,4/5c57bl/6小鼠和4/5balb/c小鼠显示在第28天,即第二次疫苗接种后7天其针对烟叶提取物的igg增加(图2)。每组中唯一没有反应的小鼠具有基础igg抗体水平。balb/c小鼠的抗体滴度低于c57bl/6小鼠(图2)。
然而,用烟叶提取物接种2次小鼠后没有检测到ige体液应答。在不同血清上进行的所有测试中光密度(od)小于0.05。
烟叶提取物优选激活外周血自然杀伤细胞
通过密度梯度(ficoll)从外周血中分离单核细胞后,可以表征不同的细胞群(t和b淋巴细胞,nk细胞等)(图3)。因此,通过标记物cd56和cd16在cd3阴性群体中鉴定nk细胞或通过标记物nkp46鉴定nk细胞。在将单核细胞与根据实施例1的烟叶提取物孵育后,在nk细胞上观察到活化标记物cd69、cd25和hla-dr的表达增加,通过标记物cdi6+cd56+(cd3-)(图4a)和标记物nkp46(图4b)鉴定。对于稀释至1/2并用于cd69表达的烟叶提取物,结果更明显。因此,超过60%的nk细胞在与烟叶提取物接触24小时后表达标记物cd69(图4a-b)。静止时,不到5%的血液nk细胞表达cd69。
烟叶提取物对外周血淋巴细胞活化的影响要弱得多。因此,在静止时,2%的t淋巴细胞表达cd69,并且在用烟叶提取物培养24小时后该表达增加至6%(图5a)。用烟叶提取物致敏的t淋巴细胞上的cd25表达没有增加(图5a)。类似地,在外周血b淋巴细胞上,烟叶提取物没有显著活性,因为与该提取物共培养24小时后,少于3%的b淋巴细胞表达cd69(图5b)。
由根据实施例1的烟叶提取物在人血液单核细胞上诱导的细胞因子概况
使外周血单核细胞与根据实施例1冻干并以不同稀释度(1/2或1/20)用5mlpbs重构的烟叶提取物接触24小时,并通过luminex在上清液中进行细胞因子、趋化因子和生长因子的测定。
图6显示烟叶提取物对促炎细胞因子(il-1β、il-6、tnfα、il-17)的强烈诱导。例如,当单核细胞未置于烟叶提取物存在下时,这些细胞因子的基础水平小于10pg/ml(图6a)。
在与稀释至1/2的烟叶提取物一起温育后,测量的细胞因子il-1β、il-6和tnfα的浓度超过1000pg/ml(图6a)。当烟叶提取物稀释至1/20时,也观察到这种明显的促炎细胞因子的诱导(图6a)。测试的不同供体之间的结果相当均匀。在促进细胞介导的免疫的th1细胞因子(il-2、ifnγ、il-12)中,只有ifnγ被稀释至1/2和1/20的烟叶提取物显著刺激(图6b)。烟叶提取物诱导非常低浓度的th2细胞因子(il-4、il-5、il-13),其量级为几个pg/ml(图7a)。相反,烟叶提取物刺激单核细胞产生il-10,其中在与稀释至1/2的烟叶提取物接触的细胞上清液中发现750pg/ml的水平(图7a)。il-10最初被认为是th2细胞因子,但它也可以由称为tr1的调节性t淋巴细胞产生。
我们已经表明,烟叶提取物还可以诱导产生造血生长因子,例如g-csf,其促进中性粒细胞和趋化因子如mcp-1的扩张和募集,已知mcp-1对巨噬细胞发挥趋化作用(图7b)。然而,烟叶提取物不显著刺激其他生长因子,例如il-7或gm-csf(图7b)。当对用烟叶提取物培养48小时后收集的上清液进行测定时,发现了相同的细胞因子/趋化因子谱。
结论
根据实施例1的烟叶提取物能够在两种不同遗传背景的小鼠品系中诱导针对产物中存在的蛋白质的特异性igg体液应答。
在这些相同的小鼠中两次施用该物质后未观察到ige体液应答。
在体外,根据实施例1的烟叶提取物在外周血单核细胞中优先诱导nk细胞的活化。这种活化通过cd69、cd25和hla-dr分子的表达增加反映。
根据实施例1的烟叶提取物诱导体外促炎细胞因子,例如il-1β、il6、il-17、il-8和tnfα。这些细胞因子以高浓度存在于刺激后24小时收集的培养上清液中。
根据实施例1的烟叶提取物还诱导ifnγ、il-10、g-csf和mcp-1。然而,该提取物不会显著诱导th2细胞因子(il-4、il-5、il-13)的产生。
实施例6:根据实施例1的烟叶提取物的毒理学研究
材料和方法:
以下所有研究均使用根据实施例1的烟叶提取物进行。
在所有情况下,施用途径都是皮下施用。对啮齿动物(hanwistar大鼠)进行毒理学研究。毒理学研究根据优良实验室规范的oecd原则(数据评估中的mutualacceptanceofdata(mad),1997年11月26日(c(97)186final)和frenchministryofemploymentandsolidarity(no2000/5bis,orderof14march2000,jo23/03/2000)出版的优良实验室规范(glp)进行。
在14天的皮下毒性研究
该研究的目的是确定皮下施用(每周一次,持续2周)后根据实施例1的烟叶提取物在大鼠中的毒性。
该研究如下进行:
研究结果表明:
-任何剂量下均未观察到死亡;
-未观察到与治疗相关的临床体征,且皮下施用局部耐受良好(注射前后观察到临床体征和局部耐受,且未给予治疗时每天一次);
-对体重和食物消耗的影响(与对照组相比)无害;
-治疗和未治疗的啮齿动物之间白细胞计数存在生物学上的显著差异,但这些差异没有毒性作用;
-在蛋白质和胆固醇浓度方面观察到治疗组和未治疗组之间的差异,但这些差异保持在对照组的范围内或接近对照组的变化范围。这些影响无害;
-治疗组和对照组之间器官重量未观察到变化。
因此,以11.2和56μg蛋白质/kg/adm的剂量每周一次向wistar大鼠皮下施用根据实施例1的烟叶提取物,持续2周,是良好耐受的。
四周皮下毒性研究
目的是确定每周一次向wistar大鼠皮下施用后根据实施例1的烟叶提取物的毒性,并确定在没有治疗的情况下4周期间的任何毒性迹象的消退。
特别注意潜在的免疫现象。
该研究如下进行:
(1)以蛋白质表示
(2)最后一次施用后2天(第23天)杀死的大鼠
(3)最后一次施用后4周(第49天)杀死的大鼠
在治疗期间,在施用前观察大鼠,且在施用后至少3次观察大鼠。在观察期间,每天观察一次大鼠。
每周进行一次完整的临床检查。在每次注射之前和之后注意局部耐受性,在第一周每天一次,然后每周两次直至观察期结束。
每次施用后的那天(第1、8、15和22天)测量体温。
在测试前以及在施用的第一天和最后一天的后一天(第1天和第22天)进行眼科检查。
每周测量两次个体体重和食物消耗。
在第23天和第49/48天(分别为雄性/雌性)进行血液学、凝血、血清临床化学参数和淋巴细胞分析。尿液测试在第23天进行。
所有动物在最后一次施用后2天或在4周观察期后被杀死并进行尸体解剖。称重某些器官并用于组织病理学检查。
研究结果表明:
-在任何剂量下均未观察到死亡;
-以16.8、33.6和112.0μg/kg/adm的蛋白质表示的剂量进行皮下施用,局部耐受良好;
-未观察到与治疗相关的临床症状;
-体温不受影响;
-未观察到与治疗相关的眼部作用;
-体重和食物消耗不受影响;
-没有观察到血液学、凝血和尿液方面的显著差异;
-在治疗期结束时,雌性组3和4(中剂量和高剂量;分别为33.6和112μg/kg/adm)的肌酸激酶活性降低。这些变化不被认为是有害的,因为它们与组织病理学特征无关;
-在治疗过的雌性和用中剂量和高剂量治疗的雄性(第3组和第4组)中循环nk细胞数量略有减少;
-在观察期结束时,用高剂量(第4组)治疗的雄性中循环nk细胞的平均数量较低;
-没有观察到器官重量的变化;
-在注射部位观察到黑斑,其对应于组织病理学评估期间的皮下出血。该观察结果被认为与施用程序无关。
在治疗结束时,在第3组和第4组的注射部位观察到极小或轻微的炎性皮肤变化,而第1组和第2组几乎没有观察到炎症变化。
在观察期结束时,先前在第4组中观察到的炎症变化显示几乎完全恢复。
根据实施例1的烟叶提取物的剂量高达112μg/kg/adm的4次皮下注射是良好耐受的,并且与未治疗的大鼠相比,在治疗的大鼠中仅发生最小和可逆的炎性变化。
总之,在上述实验条件下,在wistar大鼠中根据实施例1的烟叶提取物在16.8、33.6和112μg/kg/adm的剂量下每周一次皮下施用4周的耐受性良好且与任何不利作用无关。
实施例7:施用实施例1的烟叶提取物后的临床研究
对24名吸烟者在第0天第一次皮下注射施用包含根据实施例1的烟叶提取物(其包含100μg或200μg蛋白质和甘露醇)的药物组合物,且在第29天第二次(每次每组1ml)施用。根据群组扩张的原则进行纳入,首先纳入接受100μg的6名初始患者,然后纳入接受200μg的6名初始患者,然后纳入接受100μg的另外6名患者。接受治疗的人群由24人组成,14名男性和10名女性,年龄在30至65岁之间,中位年龄为44.5岁。
应该注意的是,根据国家癌症研究所的不良事件通用术语标准(ctcae)v4.0的毒性等级,所测试的剂量均未产生3-4级毒性。
烟草消费方面受试者的初始特征如下表所示。
图8和图9显示了烟草消费的演变。
计算减少香烟数量的公式如下:
(访问时的香烟数n–纳入时的香烟数)/纳入时的香烟数。
在4周时得出的结果显示,16名吸烟者(67%的吸烟者)戒烟或减少了其至少50%的每日香烟消耗,并且24名吸烟者的每日香烟消耗量减少了60%。
在12周时得出的结果显示,15名吸烟者(63%的吸烟者)戒烟或减少了其至少50%的每日香烟消耗,并且24名吸烟者的每日香烟消耗量减少了60%。
值得注意的是,最后12名吸烟者(24名中的12名)受益于他们第一次接触临床研究中心和注射根据实施例1的烟草提取物之间的更长的延迟(有时是一个月或更长时间),而前12名吸烟者具有较短的延迟(通常只有几天)。对于这些受益于较长时间延迟的12名吸烟者,吸烟量减少了至少50%的消耗,或在3周和4周时停止吸烟的吸烟者比例为83%(12名中的10名吸烟者),而对于具有较短的延迟的12名吸烟者,该比例为50%(12名中的6名吸烟者)。这种优越的功效可以通过以下来解释,即在接受注射根据实施例1的烟草提取物之前有更多时间来增强其动机的吸烟者有更好的准备。在最后12名吸烟者中,5名在结束治疗后一周至第12周(随访结束)持续禁烟,并且8名在第12周的最后7天内持续禁烟。
接受治疗的吸烟者描述了烟对他们的吸引力以及他们对吸烟的渴望的减少,以及对烟的某种漠不关心的态度。他们注意到烟的适口性降低了。有些人谈到香烟味道的变化。他们戒烟的动机得到了加强。
在施用药物组合物之前,在所有患者中检测到针对药物组合物的igg抗体。在治疗之前,针对药物组合物的igg的平均浓度为6.07μg/ml(标准偏差:2.98μg/ml)。
在施用药物组合物后,观察到抗药物组合物igg的显著增加的浓度。因此,在施用该药物组合物后29天测量的igg浓度为7.19μg/ml(标准偏差:4.04μg/ml),并且当在药物组合物的第一次施用8周后测量时这些浓度增加至7.5μg/ml(标准偏差4.28μg/ml)。在第29天和第0天(p=0.02)之间以及第8周和第0天的测量之间(p=0.006)igg浓度的变化是显著的(t-检验显著性阈值p<0.05)。在第8周和第29天,在抗药物组合物igg的浓度之间也观察到显著性差异(p=0.029)。
对于针对药物组合物的igg浓度和戒烟之间的统计分析显示了较高水平的针对药物组合物的igg与戒烟之间的相关性(wilcoxon检验,显著性阈值p<0.05)。
在第一次施用药物组合物后一周减少其消耗达至少50%的患者在第29天(p=0.034)和第8周(p=0.044)具有更高水平的针对药物组合物的igg。
已连续7天禁烟(普遍禁烟(prevalentabstinence))的患者在第36天比在第29天(p<0.001)和第8周(p<0.001)具有更高水平的针对药物组合物的igg。
已连续7天禁烟(普遍禁烟)的患者在第12周比在第29天(p=0.013)和第8周(p=0.016)具有更高水平的针对药物组合物的igg。
直到第12周持续禁烟的患者在第29天(p=0.007)和第8周(p=0.009)具有更高水平的针对药物组合物的igg。
施用药物组合物后未检测到ige抗体。
- 还没有人留言评论。精彩留言会获得点赞!