一种改善中脑黑质多巴胺神经元活力防治帕金森病的药物的制作方法
本发明属于生物医药领域,具体涉及通过生物信息学方法筛选出一种改善中脑黑质多巴胺神经元活力防治帕金森病的药物。
背景技术:
帕金森疾病(parkinsondisease,pd)是一种以中脑黑质多巴胺神经元变性坏死为特点的中枢神经系统变性疾病,是常见的中老年神经退行性疾病,临床表现为静止性震颤、肌张力增高、运动迟缓等。虽然pd已有近二百年的研究历史,但是迄今为止,由于pd的发病机制不明确,对于该病目前无论是药物治疗还是手术治疗,只能改善其症状,不能阻止疾病的发展,更无法治愈。
pd病理上可见中脑黑质网状带多巴胺(da)能神经元变性丧失及纹状体da水平降低,因此左旋多巴(l-dopa)替代治疗是应用最广泛、最有效的方法。然而,随着pd病情的不断发展以及持续的左旋多巴用药,残存的多巴胺能神经元产生多巴胺的能力丧失,对外源性多巴胺药物的缓冲能力降低。与此同时,纹状体内多巴胺水平不能维持在正常生理状态,对纹状体中型多棘神经元表面分布的多巴胺受体形成异常的波动性刺激,从而引起各种运动并发症,累及头面部、四肢、躯干等部位。因此,探索新的治疗靶点和替代疗法,寻找新的非多巴胺能的药物已经成为对pd治疗的研究热点。
氟维司群(fulvestrant)药物是一类新型的雌激素受体阻断剂,用于抗激素疗法治疗无效,雌激素受体呈阳性的绝经后晚期乳腺癌的治疗。目前尚无氟维司群和帕金森疾病治疗相关的报道。
技术实现要素:
本发明的目的在于提供一种可以替代左旋多巴防治帕金森病及相似症状的药物。
为实现上述目的,本发明采用以下技术方案:
一种筛选改善中脑黑质多巴胺神经元活力防治帕金森病药物的方法,包括以下步骤:
s1.基因表达数据采集,下载全基因组基因表达数据集;其中所述数据集包括10个脑区的基因表达数据集(gse60862);
s2.构建正常人脑共表达网络,采用加权基因共表达方法将10个脑区的基因分为共识模块和在中脑黑质脑区的差异模块;
s3.检查由10个脑区的基因表达数据集生成的模块的保留情况,将其与其他独立的脑基因表达数据集进行评估;
s4.pd基因在10个脑区的基因表达数据集中共识模块和差异模块中的富集,从pd相关基因数据集和人类基因突变数据集收集与帕金森病相关的基因,评估每个模块中帕金森相关基因的富集程度,通过比较模块中与帕金森病相关基因重叠的基因数量和控制基因重叠的基因数量;
s5.神经元特异性分析,使用公共的细胞类型标志基因数据库来检测所保存的基因模块是否富集于特定细胞类型中;
s6.药物发现分析,由关联性图谱数据库执行,根据关联性图谱数据提供的连接性评分,选择该化合物作为候选药物;
s7.采用鱼藤酮诱导的帕金森病模型验证所筛选药物的效果,采用实时定量pcr技术,检测该药物逆转帕金森病相关基因表达的能力。
优选地,所述步骤s1中下载的全基因组基因表达数据集还包括时空基因表达数据(gse25219)、正常人脑组织基因表达数据(gse45878,gse34865)、帕金森疾病病例对照组基因表达数据(gse8397)和小鼠大脑基因表达数据(gse16496)。
优选地,所述步骤s2中采用加权基因共表达方法包括网络分析(wgcna)和diffcoex;其中wgcna用于检测所有十个脑区共同的共表达模块(“共识模块”),diffcoex用于识别与其他9个脑区相比,在中脑黑质脑区差异表达的基因模块(“差异模块”)。
优选地,所述步骤s3中其他独立的脑基因表达数据集包括:时空基因表达数据(gse25219)、正常人脑组织基因表达数据(gse45878,gse34865)、帕金森疾病病例对照组基因表达数据(gse8397)和小鼠大脑基因表达数据(gse16496);其中通过gse25219数据集筛选年龄大于13岁的样本;使用gse45878数据集分析不同脑区共表达模块的保存情况;使用gse34865数据集检测黑质脑区的模块保存程度,包括57个神经和神经病理学正常人的死后大脑的57个黑质样本;gse8397数据集用于检测pd患者黑质脑区的模块保存情况,gse16496数据集用于评估这些模块是否保存在其他物种中。
优选地,所述步骤s4中从pd相关基因数据集和人类基因突变数据集收集与帕金森病相关的基因的步骤,还包括收集了来自hgmd数据集其他基因作为控制组,所述基因在任何研究中均未被报道与神经疾病相关。
优选地,所述神经疾病包括帕金森病、阿尔茨海默病、亨廷顿舞蹈症、中风、肌萎缩性侧索硬化、脊髓小脑萎缩、脊髓肌萎缩、牛海绵状脑病、克雅氏病和原发性侧索硬化。
优选地,所述步骤s5中所述细胞类型标志基因数据库为单细胞rna序列数据库来自人类腹侧中脑,包括13种细胞类型和25种细胞亚型。
优选地,所述步骤s6中所述由关联性图谱数据库执行,通过以下方法实现:利用gse8397的基因表达数据集中的pd患者和健康对照组的黑质脑区样本,采用limmarpackage执行基因差异表达分析,然后将这些基因输入到关联性图谱数据库(cmap)中,发现具有逆转pd患者和对照组基因表达显著差异的功能的化合物作为候选化合物。
优选地,所述步骤s7中鱼藤酮诱导的帕金森病模型采用以下方法制备:在胚胎第15天(e15),从c57b/l小鼠的皮质层分离出原代神经元细胞,培养6天,使用线粒体膜电位(mmp)来确定是否成功诱导pd模型。
优选地,所述步骤s7中帕金森病相关基因包括slc6a3、slc18a2、gch1、th、dcc、snca、uchl1、vps35、gprin3、drd2、nr4a2和dnajc6。
本发明通过采用加权基因共表达网络分析和识别与生物相关的差异共表达模块的生物信息学方法。借用统计学检验将277个和帕金森病密切相关的基因匹配到基因网络模块中,得到与帕金森疾病相关的基因共表达模块,并通过关联性图谱(connectionmap,cmap)数据库和来自于帕金森病人与正常对照组中脑黑质脑区样本间的差异基因表达谱数据,得到可以明显逆转模块中异常表达基因的药物—氟维司群(fulvestrant)。通过实时定量聚合酶链反应(qt-pcr)实验证实氟维司群(fulvestrant)逆转异常基因表达的能力,实验表明,在鱼藤酮诱导的帕金森病模型原代神经中,氟维司群药物可以增加线粒体膜电位正常的原代神经元的数量,恢复神经元活性。从而说明,氟维司群具有反转帕金森病异常基因表达,恢复中脑黑质多巴胺神经元活力的能力。
本发明的另一目的在于提供氟维司群已知药物的新用途,主要是在制备改善中脑黑质多巴胺神经元活力的药物中的用途。
优选地,所述氟维司群已知药物的新用途为在制备治疗或预防帕金森的药物中的用途。
本发明的有益效果:本发明运用系统分析的生物信息学方法,发现帕金森病相关的多个通路与风险基因,对帕金森的生物靶向治疗、生物药物研制以及风险预测等具有重要意义。并在此基础上,应用多靶点药物研发的方法,发现潜在的药物。目前,用于治疗帕金森病药物都是基于单一靶点和单一通路。在本发明中,通过对不同数据库的集成系统分析来确定帕金森疾病的发病机制,克服了单一通路或靶点的局限性。并其还利用cmap数据库筛选已获批准的临床药物,节约时间,金钱,人力成本,更有利于开发出安全有效的药物。
附图说明
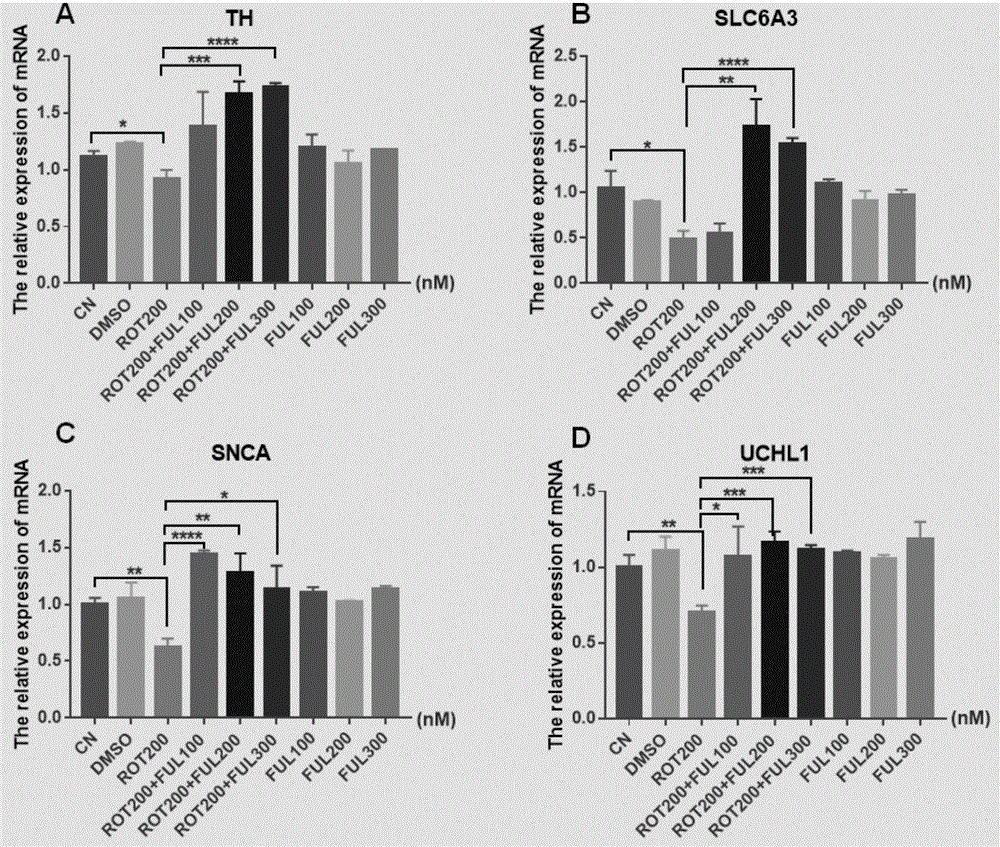
图1为氟维司群对pd基因下调的抑制作用示意图。
图2为氟维司群对神经元活性恢复的影响示意图。
具体实施方式
为了更加简洁明了的展示本发明的技术方案、目的和优点,下面结合具体实施例及其附图对本发明做进一步的详细描述。
实施例1
本实施例提供一种筛选改善中脑黑质多巴胺神经元活力防治帕金森病药物的方法,包括以下步骤:
s1.基因表达数据采集:
基因表达数据来自公共的geo数据。geo数据集包含微阵列、下一代测序以及研究学者提交的其他形式的高通量基因组数据。从geo中,我们下载了6个全基因组基因表达数据集,分别是10个脑区的基因表达数据(gse60862)、时空基因表达数据(gse25219)、正常人脑组织基因表达数据(gse45878,gse34865)、帕金森疾病病例对照组基因表达数据(gse8397)和小鼠大脑基因表达数据(gse16496)。
s2.正常人脑共表达网络的构建:
利用gse60862数据集构建基因共表达网络。采用加权基因共表达网络分析(wgcna)和diffcoex两种方法将10个脑区的基因分为共表达模块。wgcna用于检测所有十个脑区共同的共表达模块(“共识模块”);diffcoex用于识别与其他9个脑区相比,在中脑黑质脑区差异表达的基因模块(“差异模块”)。
s3.检查由gse60862数据集生成的模块的保留情况:
几个独立的脑基因表达数据集被用来评估从gse60862样本中获得的共表达模块的保存度。通过利用gse25219数据集筛选年龄大于13岁的样本。使用gse45878数据集分析不同脑区共表达模块的保存情况。使用gse34865数据集检测黑质脑区的模块保存程度,包括57个神经和神经病理学正常人的死后大脑的57个黑质样本。此外,gse8397数据集还用于检测pd患者黑质脑区的模块保存情况。最后,为了评估这些模块是否保存在其他物种中,在包括51个小鼠大脑区域的数据集gse16496中进行分析。使用r包:biomartbioconductor将小鼠基因与人类的同源基因进行“一对一”的匹配记录。
s4.pd基因在gse60862数据集中共识和差异模块中的富集:
我们在两个数据库中收集了277个与帕金森病相关的基因,即pd相关基因集(pdgset)和人类基因突变数据集(hgmd,http://www.hgmd.cf.ac.uk/ac/index.php)。pdgset是一组包含242个与pd显著相关的基因,由hu等人从200多个研究中收集。hgmd是一个收集与疾病相关的突变基因的数据集。在这个数据集中,收集了46个与pd相关的基因。此外,我们还建立了一个控制数据集,包括来自hgmd数据集的4825个基因。这些基因在任何研究中均未被报道与神经疾病相关,包括帕金森病、阿尔茨海默病、亨廷顿舞蹈症、中风、肌萎缩性侧索硬化、脊髓小脑萎缩、脊髓肌萎缩、牛海绵状脑病、克雅氏病和原发性侧索硬化等。用fet(fisherexacttest)估计每个模块中帕金森相关基因的富集程度,通过比较模块中与pd相关基因重叠的基因数量和控制基因重叠的基因数量。
s5.神经元特异性分析:
利用一组公共的细胞类型标志基因用来检测所保存的基因模块是否富集于特定细胞类型中。单细胞rna序列数据来自人类腹侧中脑,包括13种细胞类型和25种细胞亚型。利用fet对每种细胞类型的基因富集程度进行了评价,并通过实验评价了与细胞类型标志基因重叠的基因数量的统计学意义。
s6.药物发现分析:
药物发现分析由关联性图谱(cmap,http://www.broadistitute.org/cmap/)数据库执行。cmap数据库由1309种药物治疗的4个细胞系,共包括超过7000个基因表达谱组成。为了识别在pd患者和对照组中表达显著不同的基因,我们利用gse8397的基因表达数据集中的24例pd患者和11例健康对照组黑质脑区的样本,采用limmarpackage执行基因差异表达分析,如表1所示。这些基因被输入到cmap中,发现具备能逆转高度保存的模块中的pd患者和对照组的基因异常表达的功能的化合物作为候选化合物,如表2所示。根据cmap提供的连接性评分,选择该化合物作为候选药物,与cmap中的参照基因表法谱进行比对,获得比值在-1~1之间的关联系数(connectivityscore)。基因表达谱数据分成正向调控基因群与负向调控基因群进行分析,运算基因图谱的相似程度,最后给予分数平均值。score为正,表示小分子化合物或药物与某一特殊的生物过程或状态有相似或同向的联系,所研究药物与某些小分子化合物可以正向促进基因的表达;score为负,表示小分子化合物或药物与某一特殊的生物过程或状态有相反或拮抗的联系,所研究药物可以逆转这些差异的基因的表达。分数[0,1]代表两者的药物分子为正相关,称作positive;分数[-1,0]代表两者的药物分子为负相关,称作negative;它们的绝对值越大表明相关性越大。
表1:limmarpackage执行基因差异表达分析
表2:候选化合物
s7.采用鱼藤酮诱导的帕金森病模型验证所筛选药物的效果,采用实时定量pcr技术,检测该药物逆转帕金森病相关基因表达的能力。
s7.药物效果验证,鱼藤酮诱导的帕金森病模型:
(1)帕金森病模型建立:在胚胎第15天(e15),从c57b/l小鼠的皮质层分离出原代神经元细胞。使用添加有2%b27的
(2)实时定量pcr:
为了检测该药物逆转基因表达的能力,采用实时定量pcr技术。使用传统方法分离总rna,并使用纳米滴管定量(thermofisherscientific)。根据制造商的说明,使用高容量cdna逆转录试剂盒(takara,rr047a)使用300–500ng/μl总rna逆转录聚合酶链反应(rt-pcr)制备cdna。使用针对slc6a3、slc18a2、gch1、th、dcc、snca、uchl1、vps35、gprin3、drd2、nr4a2和dnajc6的tbgreentmpremixextaqtmii试剂盒(takara,rr820a)对cdna进行实时定量pcr(qpcr),其中所用引物见表3。qpcr在快速实时pcr系统(应用于rochelightcycler480ⅱ)上进行。以小鼠gapdh作为基因表达的内源性对照,用deltact计算表达的折叠变化。应用双尾t检验,用graphpadprism7.0软件(graphpadsoftware,sandiego,ca,usa)测定不同处理对基因表达的影响。数据表示为平均值±sem。p值<0.05被认为具有统计学意义。
表3:实时定量pcr(qpcr)所用引物
(3)线粒体功能测定:
使用jc-1线粒体膜电位测定试剂盒(yeasen,40706es60)测定细胞线粒体膜电位(mmp),该试剂盒是一种荧光法测定活细胞线粒体膜电位。mmp试剂盒显示低线粒体功能测定。该试剂盒显示低mmp下的蓝色荧光单体和高mmp下的红色荧光。mmp试剂盒包括阳离子染料tmre(四甲基罗丹明乙酯高氯酸盐)和线粒体膜电位干扰剂cccp(羰基氰化物3-氯苯肼)。cccp将质子从膜间空间送回线粒体基质,从而将质子从atp合成酶转移。质子的这种转移导致线粒体去极化,从而增加呼吸速率,从而使mmp短时间循环,并从atp合成中分离出电子传输。tmre是一种细胞膜渗透性荧光染料,在完整的线粒体中积累。去极化或不活跃的线粒体显示膜电位降低,导致tmre积累减少。在本发明中,6孔板中的细胞在含有1mljc-1工作缓冲液的培养基中在37℃下培养30分钟,并用pbs缓冲液洗涤。然后,用bd-celesta流式细胞仪测量荧光,并用flowjo10.0软件对输出结果进行分析。最后,用488/530纳米(绿色)和549/595纳米(红色)荧光比测定线粒体膜电位。在未经处理的对照培养物中,这些比率表示为比率的百分比。低mmp下的蓝色荧光单体和高mmp下的红色荧光。
实施例2氟维司群细胞实验证明
1、氟维司群能抑制pd基因的下调
采用实施例1步骤7的鱼藤酮诱导的帕金森病模型验证氟维司群对pd基因的影响。在鱼藤酮诱导的帕金森病模型中,发明人对皮质神经元进行了dmso、cccp、rot400nm、rot400nm+ful200nm和ful200nm五个处理。首先,用200nm鱼藤酮预处理皮质神经元2小时,然后用不同浓度(100nm、200nm和300nm)的氟维司群处理24小时。采用rt-qpcr方法对用cn(对照组)、dmso(2%)、鱼藤酮和不同浓度(100nm,200nmand300nm)的氟维司群处理的皮质神经元进行检测。dmso处理的目的是检测溶剂的作用。采用graphpadprism7.0软件进行统计分析。
结果如图1所示,分别用100nm、200nm和300nm的氟维司群治疗帕金森病模型24小时后,不同浓度的氟维司群均能抑制th、slc6a3、snca和uchl-1的下调,能逆转鱼藤酮处理后皮质神经元异常表达的pd基因。四个pd基因(th、slc6a3、snca和uchl-1)的mrna表达均显著提高。
2、氟维司群能恢复神经元的活性
发明人设计了五种针对皮质神经元的处理方法,检测氟维司群治疗后mmp的变化,处理方法分别为dmso、cccp、rot400nm、rot400nm+ful200nm和ful200nm。用jc-1法测定了这些处理组与对照组(cn)之间mmp的变化。计算结果采用flowjo10.0软件,统计结果采用graphpadprism7.0软件进行分析。mmp低的神经元数量(蓝色)和mmp正常的神经元数量(红色)。cn为对照组,dmso组为溶剂对照组,cccp组为mmp阳性对照组。用1mljc-1工作缓冲液对皮质神经元进行染色。这些细胞被染色30分钟37℃,5%的二氧化碳,然后用pbs洗净,在流式细胞分析仪通过测量和分析的比率488/530nm(绿色)和549/595nm(红色)。绿色荧光增加表示mmp降低,红色荧光增加表示mmp正常。
结果如图2所示,图2a显示了不同处理组mmp低的神经元数量(蓝色)和mmp正常的神经元数量(红色),其中ful200nm处理组(浓度为200nm的氟维司群组)能使原代神经元数目增加,使mmp正常,恢复了原代神经元的活性。图2b显示ful200nm处理组能明显降低线粒体膜电位。
综上所述:说明本发现的氟维司群(fulvestrant)药物可以有效的翻转帕金森和疾病中异常表达的基因,改善多巴胺神经元的活性,达到治疗帕金森疾病及其相似症状的效果。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!