抗-乙型淀粉样蛋白抗体及其用途的制作方法
本申请案主张于2018年5月30日提出申请之美国临时专利申请案第62/678,080号案之优先权,将该申请案之整体内容以引用方式并入本文中。
背景技术:
阿兹海默症(ad)的临床特征是渐进性记忆丧失和认知功能障碍。其病理特征之一为主要由aβ构成的细胞外老年淀粉样蛋白斑块的沉积。参见wang等人的natrevneurol.2017,13(10):612-623。大部分的ad病例为偶发性的,并且因为其疾病起源的多样性,故ad的病因仍不甚清楚。目前临床使用的药物只能暂时减缓症状并没有治愈这种疾病的作用。
在ad中,aβ沉积在大脑中促进胶质细胞活化并趋向促炎模式,而持续不断的aβ累积更加剧了随之发生的神经发炎以及增加tau蛋白的过度磷酸化,最后将导致神经元的损伤。到目前为止都无法治愈这种极具破坏性的疾病。在许多控制这种疾病的方法中,利用靶向aβ的被动免疫抗体疗法为最有可能预防或延缓ad发病的方法。参见barrera-ocampoa和loperaf.的colombmed(cali).2016dec30;47(4):203-212;us2009/0142270a1;以及us2015/0315267a1。其中,抗体可通过促进微胶质细胞对aβ的吞噬作用以减少aβ累积,被认为是达到治病效果的重要原因。然而,许多免疫疗法的临床试验都未能证实其治疗的实质益处,主要可能是起因于aβ的清除效率过低、或是引发过度严重的副作用的产生。
如上所述,微胶质细胞被认为在ad的致病机制中扮演重要的角色。其中,它们被活化并且通过形态变化和各种效应物的产生来表征;适当的反应有助于恢复大脑功能,但过多的反应则造成更多伤害。有越来越多人认为,在ad疗法中,将减少微胶质细胞介导的神经发炎与增加aβ清除率有利地结合可能是非常重要的。任何具有抗发炎特性同时促进微胶质细胞吞噬活性和恢复神经元功能的方法应该都有益于治疗此等疾病。许多预防和治疗ad的治疗策略目标在于预防淀粉样蛋白累积或提高其清除率。实际上,aβ单株抗体3d6在基因转殖小鼠模型中的研究展现了治疗功效。参见bacskaibj等人的jneurosci.2002sep15;22(18):7873-8。虽然这种抗体的人源化版本bapineuzumab在临床试验中透过淀粉样蛋白pet成像的确显示在脑中有减少aβ堆积的趋势,但其临床试验结果由于没有呈现显著的临床益处而且出现严重的副作用而宣告失败。另外,在可检测到ad的临床表现的很多年之前,脑内便可能出现微小但是影响显著的神经发炎。这种长期且逐渐扩大的神经发炎早已严重破坏了大脑的功能,使得ad治疗更加困难。因此,能在疾病早期阶段以多功能的作用进行干预,将成为一种有前景的治疗典范。然而,目前没有临床前阶段可早期诊断出ad的方法,也缺乏对ad的有效治疗。
为了满足ad治疗的迫切需求,具有多重功能的新型抗体必须要被发展出来。而这个新型抗体必须可用于减少类似ad的病状,例如,在体外和体内提高aβ的清除率,以及促进动物的神经元功能。
技术实现要素:
为了解决上述问题,在一实施例中,本文描述一种分离的抗体。该抗体包含:轻链cdr1(l-cdr1),具有seqidno:1序列、seqidno:7序列或seqidno:14序列;轻链cdr2(l-cdr2),具有seqidno:2序列或seqidno:15序列;轻链cdr3(l-cdr3),具有seqidno:3序列、seqidno:8序列、seqidno:21序列或seqidno:24序列;重链cdr1(h-cdr1),具有seqidno:4序列、seqidno:9序列、seqidno:11序列、seqidno:16序列或seqidno:25序列;重链cdr2(h-cdr2),具有seqidno:5序列、seqidno:12序列、seqidno:17序列、seqidno:19序列、seqidno:22序列或seqidno:26序列;以及重链cdr3(h-cdr3),具有seqidno:6序列、seqidno:10序列、seqidno:13序列、seqidno:18序列、seqidno:20序列、seqidno:23序列或seqidno:27序列;所述抗体对aβ1-42或n端修饰型aβ1-42皆具有特异性结合能力。在一些实施例中,该n端修饰型aβ1-42为焦麸氨酸aβ(pe-aβ3-42)。所述抗体可为含有fc区、fab片段、fab'片段、f(ab')2片段、单链抗体、单链可变区片段多聚体(scfvmultimer)、单株抗体、单价抗体、多特异性抗体、人源化抗体或嵌合抗体。
在一些实施例中,所述h-cdr1具有seqidno:16序列;所述h-cdr2具有seqidno:19序列;所述h-cdr3具有seqidno:20序列;所述l-cdr1具有seqidno:14序列;所述l-cdr2具有seqidno:15序列,以及所述l-cdr3具有seqidno:3序列。
在一些实施例中,所述h-cdr1具有seqidno:4序列;所述h-cdr2具有seqidno:5序列;所述h-cdr3具有seqidno:6序列;所述l-cdr1具有seqidno:1序列;所述l-cdr2具有seqidno:2序列,以及所述l-cdr3具有seqidno:3序列。
在一些实施例中,所述h-cdr1具有seqidno:9序列;所述h-cdr2具有seqidno:5序列;所述h-cdr3具有seqidno:10序列;所述l-cdr1具有seqidno:7序列;所述l-cdr2具有seqidno:2序列,以及所述l-cdr3具有seqidno:8序列。
在一些实施例中,所述h-cdr1具有seqidno:11序列;所述h-cdr2具有seqidno:12序列;所述h-cdr3具有seqidno:13序列;所述l-cdr1具有seqidno:7序列;所述l-cdr2具有seqidno:2序列,以及所述l-cdr3具有seqidno:3序列。
在一些实施例中,所述h-cdr1具有seqidno:16序列;所述h-cdr2具有seqidno:17序列;所述h-cdr3具有seqidno:18序列;所述l-cdr1具有seqidno:14序列;所述l-cdr2具有seqidno:15序列,以及所述l-cdr3具有seqidno:3序列。
在一些实施例中,所述h-cdr1具有seqidno:9序列;所述h-cdr2具有seqidno:22序列;所述h-cdr3具有seqidno:23序列;所述l-cdr1具有seqidno:7序列;所述l-cdr2具有seqidno:2序列,以及所述l-cdr3具有seqidno:21序列。
在一些实施例中,所述h-cdr1具有seqidno:25序列;所述h-cdr2具有seqidno:26序列;所述h-cdr3具有seqidno:27序列;所述l-cdr1具有seqidno:7序列;所述l-cdr2具有seqidno:2序列,以及所述l-cdr3具有seqidno:24序列。
在另一实施例中,本文提供一种医药组合物,该医药组合物包含任一本文所述的抗体以及医药上可接受载体。
在又另一实施例中,本文描述一种核酸建构物,该核酸建构物编码任一本文所述的抗体或该抗体的成分。
在一实施例中,本文描述一种重组细胞,该重组细胞包含该核酸建构物。
在另一实施例中,本文提供了一种治疗个体的阿兹海默症的方法,该方法包含鉴定患有阿兹海默症的个体、以及对该个体投予有效量的任一本文所述的抗体。
在一些实施例中,该鉴别步骤包含对该个体投予任一本文所述的抗体、以及测量该个体的aβ蛋白的周边血液含量;所述周边血液含量与脑aβ蛋白含量正相关。
在又另一实施例中,本文描述一种检测个体脑aβ蛋白的方法,该方法包含对该个体投予任一本文所述的抗体、以及测量该个体的aβ蛋白的周边血液含量;所述周边血液含量与脑aβ蛋白含量正相关。
在一实施例中,本文描述一种标记个体之aβ斑块的方法,所述方法包含用可侦测标记来标记任一本文所述的抗体、对个体投予经标记的抗体、以及检测该个体中该标记的位置。在一些实施例中,该标记是放射性的,且该侦测是透过正子发射断层造影术进行。
在附图和下列记载中阐述了一或多个实施例的细节。根据说明书、附图和申请专利范围,实施例的其他特征、目的和优点是显而易见。
附图说明
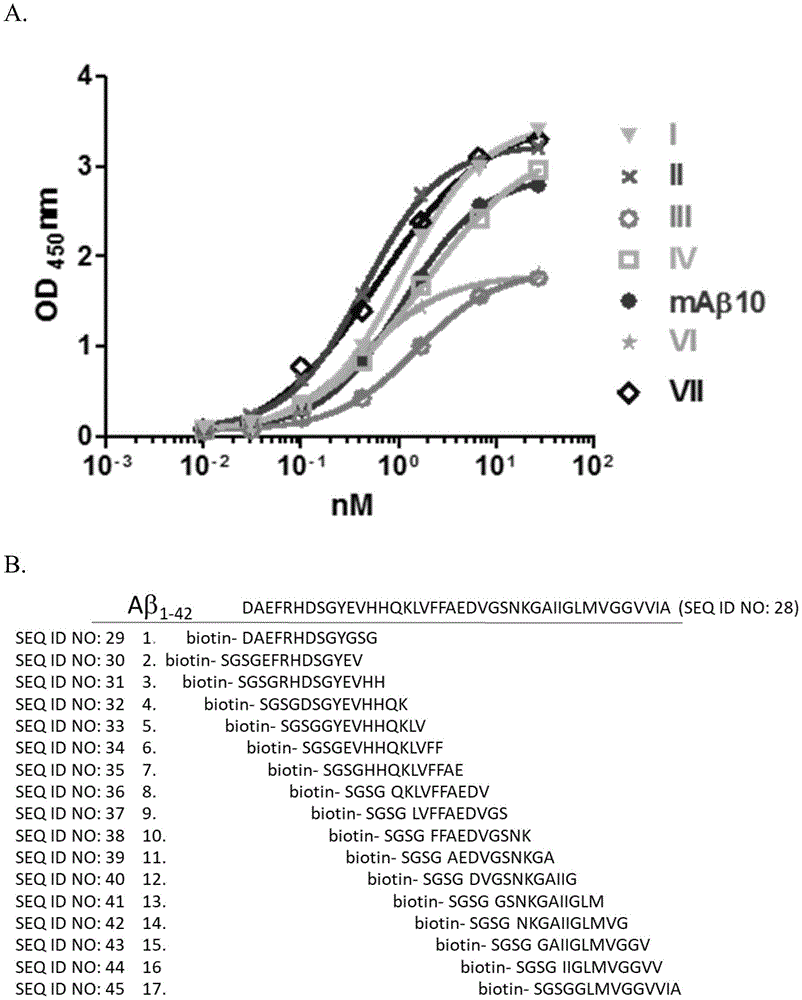
图1显示针对来自老鼠单株融合瘤aβ的抗体特性。产生分泌aβ特异性抗体的融合瘤的七种不同殖株。进行elisa以评估抗体的aβ结合亲和力(a)。该等抗体在aβn3-10具有相似的结合表位(b),并且含有在cdr-h35中所有具有七种独特序列组合的老鼠igg同种型(c)。
图2显示嵌合抗体的特性。将小鼠抗体的igg可变区构建到人类igg1主链中用来产生嵌合抗体。借由表面电浆共振(spr)评估嵌合抗体的结合亲和力(a)。评估微小胶细胞对aβ的摄取,嵌合型的先导抗体chaβ10显示出最能吞噬aβ(b)。
图3显示人源化型的先导抗体hzaβ-10的特性。通过fplc检验该先导抗体的溶解度(a)。借由elisa(b)和spr(c)评估结合亲和力。
图4显示先导抗体也可识别pe-aβ3-42。分子动力学模型预测与pe-aβ3-42结合(a),其是借由spr(b)和elisa(c)证实。
图5显示[124i]maβ-10测得脑aβ,正子发射断层造影术/计算机断层造影术(positronemissiontomography/computedtomography)分析显示maβ-10穿过血脑障壁并且可作为脑中aβ沉积的诊断探针。
图6显示先导抗体可用于预测脑中aβ的含量,其是透过监测循环中抗体诱导的aβ。腹膜内注射先导抗体促使脑aβ强烈流出至血液中。在有或没有aβ斑块形成的情况下,血清中增加的aβ含量与app/ps1小鼠中的脑aβ含量呈现正相关。
图7总结了注射maβ-10的小鼠海马回中基因表现的nextgenrna定序分析。令人惊讶的是,抗体治疗引发了许多对治疗ad有益的基因,与此同时并没有神经发炎的现象。
图8显示aducanumab和先导抗体之间的比较。比较了cdr序列相同性测定(a)、elisa所测的对aβ的结合亲和力(b)、aβ斑块的检测(c)、以及微胶质细胞对aβ的吞噬作用(d)。
具体实施方式
本文描述了识别各种aβ和n端修饰的焦麸氨酸aβ的新型抗体。
该等抗体各包含轻链cdr1(l-cdr1),具有seqidno:1序列、seqidno:7序列或seqidno:14序列;轻链cdr2(l-cdr2),具有seqidno:2序列或seqidno:15序列;轻链cdr3(l-cdr3),具有seqidno:3序列、seqidno:8序列、seqidno:21序列或seqidno:24序列;重链cdr1(h-cdr1),具有seqidno:4序列、seqidno:9序列、seqidno:11序列、seqidno:16序列或seqidno:25序列;重链cdr2(h-cdr2),具有seqidno:5序列、seqidno:12序列、seqidno:17序列、seqidno:19序列、seqidno:22序列或seqidno:26序列;以及重链cdr3(h-cdr3),具有seqidno:6序列、seqidno:10序列、seqidno:13序列、seqidno:18序列、seqidno:20序列、seqidno:23序列或seqidno:27序列。所述等抗体各自与aβ1-42或n端修饰型aβ1-42都具有特异性结合能力。
如本文所用的术语「抗体」包括具有抗原结合活性的各种抗体结构,包括但不限于单株抗体、多株抗体、全长抗体或其片段、含有fc区的抗体、fab片段,fab'片段、f(ab')2片段、单链抗体、单链可变区片段多聚体(scfvmultimer)、单价抗体、多价抗体、人源化抗体及嵌合抗体。
基于本文揭示的抗体cdr序列,技术人员将可使用本领域习知方法(例如重组法)产生不同型式的抗-aβ抗体。
以下所记载的数据表示该等抗体可用于治疗ad和早期检测脑aβ含量。n端修饰的焦麸氨酸aβ(pe-aβ3-42)非常易于聚集,并且对aβ斑块形成可能很重要。已证实该等抗体的结合表位对映于aβ胜肽的n端,特异性识别各种型式的aβ和pe-aβ3-42。因此,该等抗体在aβ清除中可能更有效。
举例而言,数据表明至少有一种抗体具有多方面功能,可减弱app/ps1小鼠的类ad病理,并使大脑中的aβ斑块穿过血脑障壁,同时将过度活化的微胶质细胞转化为具有健康和功能性形态的分枝状微胶质细胞。数据进一步指出,用抗体治疗可以增强微胶质细胞的aβ吞噬作用并改善神经元功能。
此外,已证实腹膜内注射其中一种抗体引发脑aβ强烈流出至循环中,因此在带有aβ斑块或不带有aβ斑块的app/ps1小鼠中,血液中增加的aβ含量与脑中的aβ含量呈现正相关。换言之,周边血液aβ的增加量表示增加的脑aβ含量。因此,检测抗体诱导的周边血液中(例如,血清或血浆样品中)的aβ含量可用于预测ad的所有疾病阶段的脑aβ含量。这种创新方法可作为ad风险患者的临床前诊断,并有助于监测在治疗中的ad患者的aβ病理状态。机制研究的结果进一步揭露,胶质细胞的回春作用和增加星状胶质细胞的甲状腺素运载蛋白的作用,可以部分解释该新颖抗体具有治疗和早期诊断双重功效的原因。以下阐述的研究表示,新颖抗体具有治疗ad的潜力。
为了诊断个体的ad或判断ad疾病的阶段,在对个体投予其中一种本文所述的抗体后,可测定周边血液aβ含量。可以将测得的含量与对照含量(例如来自没有ad或aβ斑块的个体的含量)或在较早时间点测得的个体含量作比较。根据比较,可以评估个体是否患有ad或ad的严重程度。为了监测个体中ad治疗的功效,可在治疗开始之前和治疗期间的一或多个时间点使用本文所述的方法测定个体中的周边血液aβ含量。周边血液aβ含量减少表示治疗有效。
可将本文所述的任何抗-aβ抗体配制成适用于各种给药途径的医药组合物,例如静脉内、关节内、结膜、颅内、腹膜内、胸膜内、肌肉内、脊髓内或皮下给药途径。该医药组合物可为水溶液或冷冻干燥制剂。该医药组合物可包含医药上可接受载体,例如缓冲剂、赋形剂、稳定剂或防腐剂。该医药组合物可包含与抗-aβ抗体一同作用的其他活性成分,例如另一种治疗剂或佐剂。
无需进一步详细说明,相信所属技术领域中具有通常知识者根据以上记载可最大程度地利用本发明。以下具体实施例应被解读为仅是说明性的,并且不以任何方式限制本揭露的其余部分。本文引述的所有参考文献均透过引用方式整体并入本文中。
实施例1:从融合瘤产生七种针对aβ的抗体殖株。
为了产生融合瘤,使用寡聚aβ(oaβ)进行小鼠免疫。将合成的aβ1–42溶解在1,1,1,3,3,3-六氟-2-丙醇(hfip)中,然后进行蒸发。将干燥膜重新溶解在1xpbs中,然后离心用来除去纤维状和聚集的aβ。使用市售的aβ抗体6e10通过西方墨点法表示所制备的oaβ的特征。结果显示,制备的oaβ寡聚体构成aβ的混合物,包括单体、二聚体和各种结构次序的oaβ,分子量范围为37-250kda。将制备的oaβ寡聚体存放在-80℃直到交由ltkbiolaboratories进行免疫用来产生单株融合瘤。通过elisa(图1a)和免疫组织化学(未显示数据)对抗体进行aβ结合亲和力分析。建立抗体的表位图谱。请见图1b。分泌针对aβ的抗体的融合瘤的七种不同殖株因而产生。结果显示该等抗体包含所有小鼠igg四个种型,而且在aβn3-10处皆具有相似的结合表位。进行融合瘤定序用来确定每种单株抗体的完整cdr序列。在图1c中列出同种型和cdr序列。
实施例2:嵌合抗体的产生
将小鼠igg可变区插入人类igg1主链中以产生嵌合抗体。以biacore进行表面电浆共振(spr)来评估七种嵌合抗体的aβ结合亲和力。请见图2a。在体外实验,进行测试抗体增强微胶质细胞吞噬aβ的作用。数据表示,所有抗体均可增强微胶质细胞对aβ的摄取,而先导抗体似乎在测定中表现最好。请见图2b。
实施例3:maβ-10的人源化
使用人类igg1框架从嵌合抗体构建人源化型式的先导抗体(hzaβ-10)。使用快速蛋白质液相层析(fplc)分析蛋白质溶解度(图3a),并且借由对app/ps1小鼠脑切片进行免疫荧光组织化学法(数据没有显示)、elisa(图3b)和spr(图3c)检测a结合特征。数据显示hzaβ-10表现出优异的aβ结合亲和力和极高的蛋白质溶解度的特殊性质,其适用于细胞株开发。
实施例4:也能识别pe-aβ3-42的新aβ抗体
n-端修饰的焦麸氨酸aβ(pe-aβ3-42)非常易于聚集,并且对aβ斑块的形成可能非常重要。该等抗体的结合表位对映于特异性识别各种型式的aβ和pe-aβ3-42的aβ胜肽的n-末端,如分子动力学模型所预测。请见图4a。来自biacore(图4b)和elisa(图4c)的数据证实,先导抗体瞄准了aβ1-42和pe-aβ3-42,表示其在aβ清除中更有效。
实施例5:[124i]maβ-10检测出脑aβ
app/ps1基因转殖小鼠透过腹膜内注射同位素标记的抗体([124i]maβ-10),并进行pet/ct分析。如图5所示,结果显示maβ-10可穿过血脑障壁并且标记大脑内的aβ斑块。因此表示,maβ-10可被开发为量测脑中aβ沉积的诊断探针。
实施例6:借由测量血清中抗体诱导的aβ含量以早期诊断ad
两剂的maβ-10治疗引发脑aβ强烈输送至血液中,并且,升高的血清aβ含量与带有aβ斑块和不带有aβ斑块的app/ps1小鼠中相应的脑中aβ含量高度相关。参见图6。通过血液样品的检测,这种新型抗体的使用可显示出疾病在各个阶段内,大脑aβ的含量,并且通过评估血清aβ来预测aβ斑块可能形成的时间。此外,血清aβ的量随着循环抗体量的减少而减少,表示抗体参与周边aβ的清除。请见图6。这种创新方法可以为有ad风险或临床前阶段的患者实施早期诊断,并有助于监测治疗中的ad患者,其aβ病理的发展状态。
实施例7:基因转录体分析
对海马回进行nextgensequencingrna-seq分析(即基因转录体分析),以检测注射maβ-10后的基因表现谱。结果显示,总共47,717个基因的基因表现有增加或减少的现象。如图7所示,许多显著被正调控的基因对ad的治疗有利,而涉及毒性和压力的基因则是被负调控。
实施例8:使用hzaβ-10的治疗使app/ps小鼠中的微胶质细胞回春
共焦成像显示,在老年app/ps1小鼠中观察到明显失去吞噬活性的钝化微胶质细胞现象的存在。而在腹膜内注射每剂剂量为30mg/kg的hzaβ-10四剂(在17天内)以后,提升了表现iba1的微胶质细胞的免疫反应性。其型态产生了显著的变化,且变成类似具有正常功能的/分枝状的微胶质细胞(数据没有显示)。这些结果表明,hzaβ-10的治疗使微胶质细胞回春并促进体内aβ斑块的清除。
实施例9:使用maβ-10治疗在app/ps1小鼠身上增加星状胶质细胞ttr、改善神经元功能和减少淀粉样蛋白斑块
共焦成像显示,在腹膜内注射每剂剂量为30mg/kg的maβ-10两剂以后,增加了星状胶质细胞之甲状腺素运载蛋白(ttr),而在年龄相符的app/ps1小鼠中的星状胶质细胞观察到低含量的ttr(数据没有显示)。共定位分析数据亦证实了ttr位在星状胶质细胞的终足内(数据没有显示)。结果表示,星状胶质细胞借由抗体诱导所产生的ttr可能参与maβ-10触发的aβ流出。令人惊讶的是,maβ-10还增加了app/ps1的海马回中map2和psd95的免疫染色。表示maβ-10可增强神经元功能(数据没有显示)。另外,每周使用maβ-10治疗一次,持续39周以后,app/ps1小鼠的淀粉样蛋白斑块因此减少(数据未示)。
实施例10:aducanumab和先导抗体的比较
aducanumab(biogen的biib037)目前正在治疗ad的iii期临床试验中。hza-10的cdr序列和aducanumab的cdr序列具有非常低的相同性。请见图8a。与aducanumab(购自creativebiolabs)相比,小鼠或人类版本的先导抗体对寡聚aβ(oaβ)和聚集的aβ具有更强的亲和力。见图8b。与aducanumab只对聚集的aβ的结合偏好相反,先导抗体对两种型式的aβ皆表现出相似的高结合亲和力。见图8b。在进行荧光组织化学法之后使用共焦成像以侦测14月龄的app/ps1小鼠脑中的aβ斑块。见图8c。连续切片用于比较两种抗体(0.2或1mg/ml)。结果显示,在检测脑aβ斑块方面,hzaβ-10比aducanumab更敏感。在可溶性或聚集的aβ-fitc处理24小时后,透过流式细胞仪评估微胶质细胞的aβ吞噬作用。结果显示,hzaβ-10在增强微胶质细胞的aβ吞噬作用方面表现优于aducanumab。参见图8d。
其他实施例
本说明书中揭示的所有特征可以任何组合方式组合。本说明书中揭示的每个特征可以由用于相同、等同或类似目的的另一特征代替。因此,除非另有明确说明,否则所揭示的每个特征仅是一系列等效或类似特征的示例。
根据以上描述,所属技术领域中具有通常知识者可轻易地确定本发明的基本特征,并且在不脱离本发明的精神和范围的情况下,可对本发明进行各种改变和修饰以使本发明适合各种用途和条件。因此,其他实施例也在以下申请专利范围的范围内。
序列表
<110>财团法人国家卫生研究院
<120>抗-乙型淀粉样蛋白抗体及其用途
<130>218384-0012pct
<150>us62/678,080
<151>2018-05-30
<160>45
<170>patentinversion3.5
<210>1
<211>17
<212>prt
<213>artificialsequence
<220>
<223>cdr-l1
<400>1
cysargserserglnthrilevalhisserasnglyasnthrtyrleu
151015
glu
<210>2
<211>7
<212>prt
<213>artificialsequence
<220>
<223>cdr-l2
<400>2
lysvalserasnargpheser
15
<210>3
<211>9
<212>prt
<213>artificialsequence
<220>
<223>cdr-l3
<400>3
pheglnglyserhisvalproleuthr
15
<210>4
<211>7
<212>prt
<213>artificialsequence
<220>
<223>cdr-h1
<400>4
thrserglymetasnvalgly
15
<210>5
<211>16
<212>prt
<213>artificialsequence
<220>
<223>cdr-h2
<400>5
hisiletrptrpaspaspasplystyrtyrasnproserleulysser
151015
<210>6
<211>12
<212>prt
<213>artificialsequence
<220>
<223>mabicdr-h3
<400>6
argargserileargglyserasptyrpheasptyr
1510
<210>7
<211>17
<212>prt
<213>artificialsequence
<220>
<223>cdr-l1
<400>7
cysargserserglnserilevalhisserasnglyasnthrtyrleu
151015
glu
<210>8
<211>9
<212>prt
<213>artificialsequence
<220>
<223>cdr-l3
<400>8
pheglnglyserleuvalproleuthr
15
<210>9
<211>7
<212>prt
<213>artificialsequence
<220>
<223>cdr-h1
<400>9
thrserglymetglyvalgly
15
<210>10
<211>14
<212>prt
<213>artificialsequence
<220>
<223>mabiicdr-h3
<400>10
argargalaleuargasnvalvalalaaspalametasptyr
1510
<210>11
<211>7
<212>prt
<213>artificialsequence
<220>
<223>cdr-h1
<400>11
thrseralavalglyvalser
15
<210>12
<211>16
<212>prt
<213>artificialsequence
<220>
<223>cdr-h2
<400>12
hisiletyrtrpaspaspasplysargtyrasnproserleulysser
151015
<210>13
<211>14
<212>prt
<213>artificialsequence
<220>
<223>mabiiicdr-h3
<400>13
argargprotyrtyrargtyraspvalaspalametasptyr
1510
<210>14
<211>17
<212>prt
<213>artificialsequence
<220>
<223>cdr-l1
<400>14
cysargserserglnasnilevalhisserasnglyasnthrtyrleu
151015
glu
<210>15
<211>7
<212>prt
<213>artificialsequence
<220>
<223>cdr-l2
<400>15
thrvalserasnargpheser
15
<210>16
<211>7
<212>prt
<213>artificialsequence
<220>
<223>cdr-h1
<400>16
serservalleuglyvalser
15
<210>17
<211>16
<212>prt
<213>artificialsequence
<220>
<223>cdr-h2
<400>17
hisiletyrtrpaspaspaspargargtyrasnproserleulysser
151015
<210>18
<211>14
<212>prt
<213>artificialsequence
<220>
<223>mabivcdr-h3
<400>18
argargglylysmetglyargglyleuaspalametasptyr
1510
<210>19
<211>16
<212>prt
<213>artificialsequence
<220>
<223>cdr-h2
<400>19
hisiletyrtrpaspaspaspargargtyrasnproserleuargser
151015
<210>20
<211>14
<212>prt
<213>artificialsequence
<220>
<223>mabvcdr-h3
<400>20
argargglylysmetglyargglyleuaspalaleuaspphe
1510
<210>21
<211>9
<212>prt
<213>artificialsequence
<220>
<223>cdr-l3
<400>21
pheglnglyserargvalproleuthr
15
<210>22
<211>16
<212>prt
<213>artificialsequence
<220>
<223>cdr-h2
<400>22
hisiletrptrpaspaspasplystyrpheasnproserleulysser
151015
<210>23
<211>12
<212>prt
<213>artificialsequence
<220>
<223>mabvicdr-h3
<400>23
argargserleulystrpleuaspalametasptyr
1510
<210>24
<211>9
<212>prt
<213>artificialsequence
<220>
<223>cdr-l3
<400>24
pheglnserserargvalproleuthr
15
<210>25
<211>7
<212>prt
<213>artificialsequence
<220>
<223>cdr-h1
<400>25
thrserglymetglyvalser
15
<210>26
<211>16
<212>prt
<213>artificialsequence
<220>
<223>cdr-h2
<400>26
hisiletyrtrpaspaspasplyssertyrasnproserleulysser
151015
<210>27
<211>13
<212>prt
<213>artificialsequence
<220>
<223>mabviicdr-h3
<400>27
argargargasntrpvalilethraspalametglutyr
1510
<210>28
<211>42
<212>prt
<213>artificialsequence
<220>
<223>abeta1-42
<400>28
aspalagluphearghisaspserglytyrgluvalhishisglnlys
151015
leuvalphephealagluaspvalglyserasnlysglyalaileile
202530
glyleumetvalglyglyvalvalileala
3540
<210>29
<211>13
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>29
aspalagluphearghisaspserglytyrglysergly
1510
<210>30
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>30
serglyserglygluphearghisaspserglytyrgluval
1510
<210>31
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>31
serglyserglyarghisaspserglytyrgluvalhishis
1510
<210>32
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>32
serglyserglyaspserglytyrgluvalhishisglnlys
1510
<210>33
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>33
serglyserglyglytyrgluvalhishisglnlysleuval
1510
<210>34
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>34
serglyserglygluvalhishisglnlysleuvalphephe
1510
<210>35
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>35
serglyserglyhishisglnlysleuvalphephealaglu
1510
<210>36
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>36
serglyserglyglnlysleuvalphephealagluaspval
1510
<210>37
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>37
serglyserglyleuvalphephealagluaspvalglyser
1510
<210>38
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>38
serglyserglyphephealagluaspvalglyserasnlys
1510
<210>39
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>39
serglyserglyalagluaspvalglyserasnlysglyala
1510
<210>40
<211>15
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>40
serglyserglyaspvalglyserasnlysglyalaileilegly
151015
<210>41
<211>15
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>41
serglyserglyglyserasnlysglyalaileileglyleumet
151015
<210>42
<211>15
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>42
serglyserglyasnlysglyalaileileglyleumetvalgly
151015
<210>43
<211>15
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>43
serglyserglyglyalaileileglyleumetvalglyglyval
151015
<210>44
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>44
serglyserglyileileglyleumetvalglyglyvalval
1510
<210>45
<211>14
<212>prt
<213>artificialsequence
<220>
<223>syntheticpolypeptide
<220>
<221>misc_feature
<222>(1)..(1)
<223>biotin
<400>45
serglyserglyglyleumetvalglyglyvalvalileala
1510
- 还没有人留言评论。精彩留言会获得点赞!
- 一种多肽——核糖体s7蛋白-11.77和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——核糖体s3蛋白9和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人核糖体蛋白 s18-13.53 和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——核糖体s19e蛋白11和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人核糖体蛋白s5-17和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——核糖体蛋白l29
- 一种新的多肽——核糖体蛋白s3-26.73和编码这种多肽的多核苷酸的制作方法
- 糖工程化抗体的制作方法
- 一种新的多肽——核糖体蛋白s4 16.28和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——核糖体蛋白 s516.94和编码这种多肽的多核苷酸的制作方法