一种胃漂浮片及其制备方法与流程
本发明属于医药技术领域,尤其是涉及一种胃漂浮片及其制备方法。
背景技术:
在现有的医药领域中,许多药物具有溶解性差、容易在胃液中失去稳定性或被胃肠液代谢而失去应有药效的弊端,提高药物剂量虽然可以提高治疗效果,但是会给机体带来药物毒性负担,加大给药量还会增加机体耐药性,因此开发胃内药物滞留载体系统成为一种有效的治疗手段。
传统技术中,有粘膜粘着剂载体系统、磁控药物载体系统、溶胀性载体系统等来增加药物在胃内的释放时间,但是均需要添加额外的成分来辅助完成,长期给药将给肝脏造成一定的伤害。
近年开发了胃内漂浮系统,其中根据漂浮机制不同可分为泡腾型和非泡腾型两种。
泡腾型中含有发泡剂,其中多为碳酸盐,这种方法存在一定的缺陷,如漂浮滞后时长,会产生酸性气体改变胃的酸性。
另一类非泡腾型虽然没有漂浮滞后时长,靠高浓度低密度的高分子材料获得漂浮效果,但是高浓度基质材料既耗费成本、又增加机体消化降解负担。
因此,这两种技术依然存在一定的应用限制。
中国专利cn109044981a公开了一种普瑞巴林胃漂浮型缓释片,包括活性成分、骨架材料、溶胀剂和赋形剂。其中,活性成分为普瑞巴林及其药学上可接受的盐、溶剂化物、水化物或配合物;所述骨架材料为羟丙甲纤维素、羟丙纤维素、丙烯酸树脂及其衍生物中的任意一种或几种的组合。
中国专利cn101371822a提供了一种新的气囊型胃滞留缓控释药物释放系统,包括:(1)由空心囊外包裹高分子成膜材料和疏水性材料组成的气囊;(2)由药物和医药上可接受的赋形剂构成的含药层,含药层包裹在气囊外,所述含药层包括药物控释层或缓释层。如果需要,还包括由药物及赋形剂组成的速释层,包裹在缓释层或控释层外。气囊内还可以装有一定量的气体发生剂,包括碳酸盐以及药学上可接受的有机酸。整个制剂的平均密度一般控制在0.6g/cm3以下,优于目前已上市的胃漂浮制剂,胃内漂浮时间远大于普通胃漂浮制剂。但该专利靠高浓度低密度的高分子材料来得到漂浮效果,会增加机体消化降解负担。
技术实现要素:
基于现有技术中存在的问题,本发明提供一种胃漂浮片及其制备方法。本发明的胃漂浮片成分简单,没有漂浮滞后时长的问题,具有较长胃内漂浮时间,且可持续性药物释放。
本发明的目的可以通过以下技术方案来实现:
本发明提供一种胃漂浮片,包括如下质量百分比的各组分:赋形剂25%~89.5%、药物5%~30%、润滑剂0.5%~5%及致孔剂5%~40%。
在本发明的一个实施方式中,所述胃漂浮片包括如下质量百分比的各组分:赋形剂38%~89.5%、药物5%~20%、润滑剂0.5%~2%及致孔剂5%~40%。
在其中一个实施方式中,所述胃漂浮片包括如下质量百分比的各组分:赋形剂50%~70%、药物15%~20%、润滑剂0.5%~1%及致孔剂14.5%~29%。
在本发明的一个实施方式中,所述赋形剂选自玉米醇溶蛋白、果胶、乙基纤维素或甜菊苷中的任意一种或多种的混合物。
在本发明的一个实施方式中,所述赋形剂优选为玉米醇溶蛋白。
在本发明的一个实施方式中,所述润滑剂选自脂肪酸盐、脂肪醇或脂肪酯中的一种或多种的混合物。
在本发明的一个实施方式中,所述脂肪酸盐优选为硬脂酸镁。
在本发明的一个实施方式中,所述致孔剂选自薄荷醇、樟脑或碳酸铵。
在本发明的一个实施方式中,所述致孔剂优选为左旋薄荷醇。
在本发明的一个实施方式中,所述药物可选为卡托普利。
本发明还提供上述胃漂浮片的制备方法,包括如下步骤:
将致孔剂磨碎、过目筛;
将赋形剂、药物、润滑剂和致孔剂混合均匀,压片;
将压片在50℃~80℃的真空干燥箱中放置12h-36h,即得胃漂浮片。
在本发明的一个实施方式中,所述目筛孔尺寸为200μm~500μm。
在本发明的一个实施方式中,所述压片压缩条件为:压缩强度70kg/cm2~90kg/cm2,压缩时间1s~10s。
基于漂浮的胃滞留药物递送系统可以有效地用于延长药物在胃中的时间。多孔片剂是一种相对较新的方法,但是机械强度差是它们的主要缺点。片剂的机械强度是药物能否在胃液中停留较长时间并持续释放以抵抗胃压力的重要参数。本发明中赋形剂、润滑剂及致孔剂的选择原因在于:由于玉米醇溶蛋白的疏水特性,可在湿润环境下进行二级结构重排,实现在消化液中长时间的良好机械稳定性;而且在37℃与介质接触时通过形成凝胶状层来充当阻滞剂,达到缓释目的。直接压片这种简单的方法也是优势之一。致孔剂升华的温度条件使得玉米醇溶蛋白片剂显示出更高的机械强度。动物体内实验证实:胃滞留时间至少能维持24小时,获得了药物在胃部的持续释放效果。
与现有技术相比,本发明的胃漂浮片具有以下优点和有益效果:
本发明的胃漂浮片主要成分为食品蛋白质,并没有额外加入发泡剂或者控制药物释放的其他成分,降低了复杂外加组分带来的胃负担和机体伤害;制备得到的多孔漂浮片没有漂浮滞后时长,延长了漂浮片在胃内的漂浮时间;并且能够在消化液中维持长时间的良好机械稳定性;在37℃与介质接触时通过形成凝胶状层来充当阻滞剂,使负载的药物能持续地获得释放,药效明显。本发明简单的组分实现了多个功能,且直接压片的制备方式简单,大大降低了制备成本。
附图说明
图1:实施例和对比例的体外漂浮能力测试结果;
图2:实施例2的胃漂浮片及市售卡托普利药片兔体内缓释后的血浆药物浓度曲线;
图3:含10%硫酸钡(w/w)的实施例2的胃漂浮片给兔口服后的x射线照片;
图中(a)、(b)、(c)、(d)分别表示胃漂浮片给兔口服后4h、8h、12h和24h的x射线照片。
具体实施方式
为了便于理解本发明,下面将参照相关附图对本发明进行更全面的描述。以下给出了本发明的较佳实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
本发明提供一种胃漂浮片,包括如下质量百分比的各组分:赋形剂25%~89.5%、药物5%~30%、润滑剂0.5%~5%及致孔剂5%~40%。
在其中一个实施方式中,所述胃漂浮片包括如下质量百分比的各组分:赋形剂38%~89.5%、药物5%~20%、润滑剂0.5%~2%及致孔剂5%~40%。
在其中一个实施方式中,所述胃漂浮片包括如下质量百分比的各组分:赋形剂50%~70%、药物15%~20%、润滑剂0.5%~1%及致孔剂14.5%~29%。
所述赋形剂选自玉米醇溶蛋白、果胶、乙基纤维素或甜菊苷中的任意一种或多种的混合物。
在其中一个实施方式中,所述赋形剂优选为玉米醇溶蛋白。玉米醇溶蛋白是一种可降解、生物相容性好的蛋白。进一步地,,本身疏水,在水中具有溶胀性;更进一步地,具有药物包裹效果,在药物载体以及组织工程支架中已得到广泛应用。
在其中一个实施方式中,所述润滑剂选自脂肪酸盐、脂肪醇或脂肪酯中的一种或多种的混合物。
在其中一个实施方式中,所述脂肪酸盐优选为硬脂酸镁。硬脂酸镁是一种食品级稳定剂,在压片时,可起到润滑易脱模的效果;更进一步地,在应用于药片中可起到润滑作用起到防粘连效果。
在其中一个实施方式中,所述致孔剂选自薄荷醇、樟脑或碳酸铵等可在100度以下升华的物质。
在其中一个实施方式中,所述致孔剂优选为左旋薄荷醇。左旋薄荷醇常温下为一种白色粉末,容易升华,并且本身具有清凉、止痛、消炎的作用,绿色安全。进一步地,被用作致孔剂可以提高药片的孔隙率;更进一步地,应用于本发明的胃漂浮片制备时可以提高其溶胀效果;更进一步地,高孔隙率提高了漂浮稳定性,延长了胃漂浮片的漂浮时长。
在其中一个实施方式中,所述药物为卡托普利。
在其中一个实施方式中,每片胃漂浮片含有卡托普利50mg。卡托普利是一种血管紧张素转换酶抑制剂,被广泛的应用于治疗高血压和某些类型的充血性心力衰竭,自身为疏水性药物,但是在胃内酸性条件下可被溶解。进一步地,常需要药学上必要的载体辅佐释放获得更好的药效。
本发明还提供上述胃漂浮片的制备方法,包括如下步骤:
将致孔剂磨碎、过目筛;
将赋形剂、药物、润滑剂和致孔剂混合均匀,压片;
将压片在50-80℃真空干燥箱中放置12h-36h,即得胃漂浮片。
在其中一个实施方式中,所述目筛孔尺寸为200μm~500μm。
在其中一个实施方式中,所述压片压缩条件为:压缩强度70kg/cm2~90kg/cm2,压缩时间1s~10s。
以下实施例中,如无特殊说明,原料均来源于市售。
实施例1(f1)
常温下,将50mg左旋薄荷醇磨碎、过300目筛;
将200mg玉米醇溶蛋白、50mg卡托普利、3mg硬脂酸镁和左旋薄荷醇混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在60℃的真空干燥箱中放置24h,即得胃漂浮片。
实施例2(f2)
常温下,将75mg左旋薄荷醇磨碎、过300目筛;
将200mg玉米醇溶蛋白、50mg卡托普利、3.25mg硬脂酸镁和左旋薄荷醇混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在70℃的真空干燥箱中放置12h,即得胃漂浮片。
实施例3(f3)
常温下,将100mg左旋薄荷醇磨碎、过300目筛;
将200mg玉米醇溶蛋白、50mg卡托普利、13.25mg硬脂酸镁和左旋薄荷醇混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在80℃的真空干燥箱中放置12h,即得胃漂浮片。
实施例4(f4)
常温下,将50mg左旋薄荷醇磨碎、过300目筛;
将300mg玉米醇溶蛋白、30mg卡托普利、5.25mg硬脂酸镁和左旋薄荷醇混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在50℃的真空干燥箱中放置36h,即得胃漂浮片。
实施例5(f5)
常温下,将160mg左旋薄荷醇磨碎、过300目筛;
将100mg玉米醇溶蛋白、120mg卡托普利、20mg硬脂酸镁和左旋薄荷醇混合均匀,过300目筛,90kg/cm2压强下压片1s;
将压片在70℃的真空干燥箱中放置36h,即得胃漂浮片。
对比例(f0)
常温下,将10mg左旋薄荷醇磨碎、过300目筛;
将200mg玉米醇溶蛋白、80mg卡托普利、2.75mg硬脂酸镁和左旋薄荷醇混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在70℃的真空干燥箱中放置18h,即得胃漂浮片。
体外测试评估
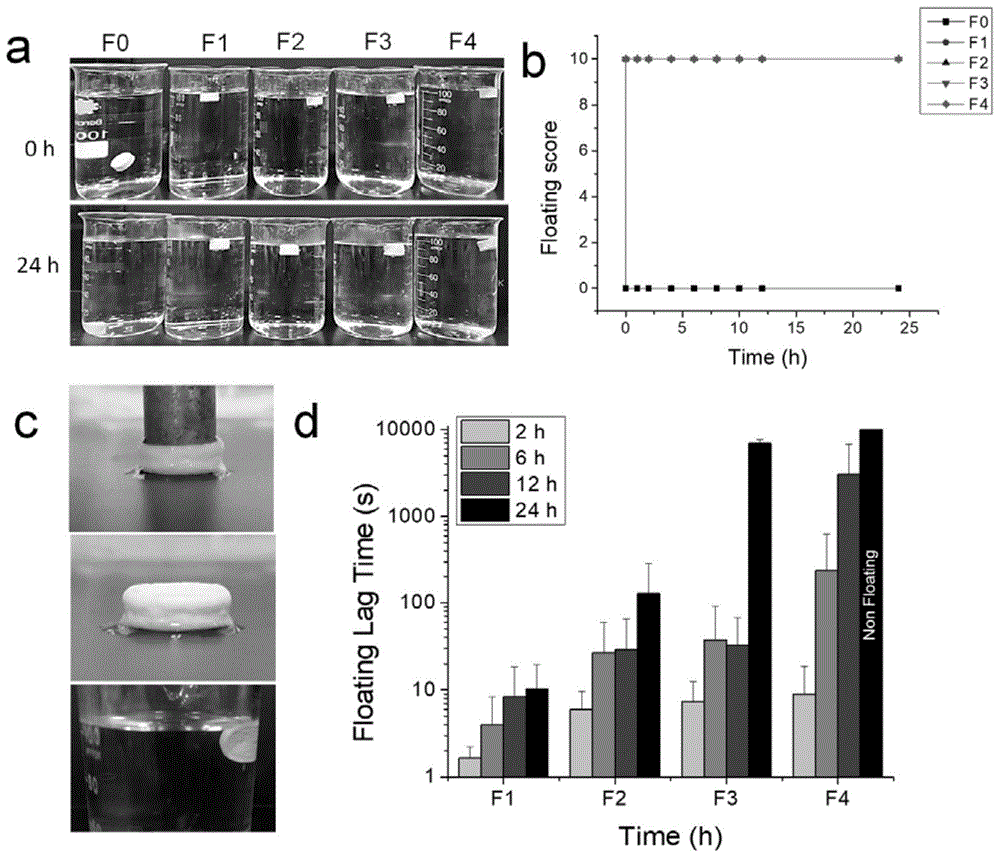
对上述实施例和对比例得到的胃漂浮片在相同环境条件下进行体外理化性能评估,包括孔隙率、药物的释放行为和漂浮能力,如图1所示。
图1为实施例和对比例的体外漂浮能力测试结果。(a)在37℃的溶出度介质中孵育0和24小时后,片剂处于漂浮状态。(b)在150rpm的搅拌条件下,所有制剂在1000ml介质中的漂浮分值。(c)从介质中移出后的片剂图片,施加2.4n的应力6s,然后将片剂再次浸入溶解介质中以观察漂浮趋势。(d)在溶出介质中孵育2、6、12和24h施加2.4n应力6s后,片剂的漂浮滞后时间(n=3)。
体内动物试验
对上述体外效果好的实施例进行兔体内缓释和漂浮时间评估,如图2-3所示:
动物:2.5kg~2.6kg新西兰兔。
分组:第一组,实施例2制备得到的胃漂浮片;第二组,市售卡托普利药片。
服用方式:吞服。
检测指标:在预设时间通过x射线观察药片的漂浮状态,并采血检测卡托普利的浓度。
图2:实施例2及市售卡托普利药片的血浆药物浓度曲线。显示本发明胃漂浮片的体内缓释效果明显。
图3:含10%硫酸钡(w/w)的实施例2给兔口服,(a)4h,(b)8h,(c)12h和(d)24h的x射线照片。显示本发明胃漂浮片的体内漂浮时长超过24小时。
实施例6(f6)
常温下,将5mg左旋薄荷醇磨碎、过300目筛;
将89.5mg玉米醇溶蛋白、5mg卡托普利、0.5mg硬脂酸镁和左旋薄荷醇混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在60℃的真空干燥箱中放置24h,即得胃漂浮片。
该实施例所得胃漂浮片在37℃的溶出度介质中孵育0和24小时后,片剂处于漂浮状态。并且制备得到的多孔漂浮片没有漂浮滞后时长,能够在消化液中维持长时间的良好机械稳定性。
实施例7(f7)
常温下,将40mg左旋薄荷醇磨碎、过300目筛;
将38mg玉米醇溶蛋白、20mg卡托普利、2mg硬脂酸镁和左旋薄荷醇混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在70℃的真空干燥箱中放置12h,即得胃漂浮片。
该实施例所得胃漂浮片在37℃的溶出度介质中孵育0和24小时后,片剂处于漂浮状态。并且制备得到的多孔漂浮片没有漂浮滞后时长,能够在消化液中维持长时间的良好机械稳定性。
实施例8(f8)
常温下,将40mg左旋薄荷醇磨碎、过300目筛;
将38mg果胶、20mg卡托普利、2mg脂肪醇和左旋薄荷醇混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在70℃的真空干燥箱中放置12h,即得胃漂浮片。
该实施例所得胃漂浮片在37℃的溶出度介质中孵育0和24小时后,片剂处于漂浮状态。并且制备得到的多孔漂浮片没有漂浮滞后时长,能够在消化液中维持长时间的良好机械稳定性。
实施例9(f9)
常温下,将40mg樟脑磨碎、过300目筛;
将38mg乙基纤维素、20mg卡托普利、2mg脂肪醇和樟脑混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在70℃的真空干燥箱中放置12h,即得胃漂浮片。
该实施例所得胃漂浮片在37℃的溶出度介质中孵育0和24小时后,片剂处于漂浮状态。并且制备得到的多孔漂浮片没有漂浮滞后时长,能够在消化液中维持长时间的良好机械稳定性。
实施例10(f10)
常温下,将40mg碳酸铵磨碎、过300目筛;
将19mg乙基纤维素、19mg甜菊苷、20mg卡托普利、2mg脂肪醇和碳酸铵混合均匀,过300目筛,80kg/cm2压强下压片2s;
将压片在70℃的真空干燥箱中放置12h,即得胃漂浮片。
该实施例所得胃漂浮片在37℃的溶出度介质中孵育0和24小时后,片剂处于漂浮状态。并且制备得到的多孔漂浮片没有漂浮滞后时长,能够在消化液中维持长时间的良好机械稳定性。以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述;然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!