取得间质性肺炎患者的病情相关信息的方法及其应用与流程
本发明涉及取得间质性肺炎患者的病情相关信息的方法。另外,本发明涉及间质性肺炎患者的病情的判定方法。进一步地,本发明涉及用于这些方法的试剂盒、用于判定间质性肺炎患者的病情的装置及计算机程序。
背景技术:
:间质性肺炎为肺的间质组织、特别是肺泡壁发生炎症及纤维化的疾病。若间质性肺炎发生进展,则由于肺纤维化而出现肺活量及气体交换能力下降、呼吸困难的症状。间质性肺炎的原因涉及多方面。例如,以胶原病为基础疾病而发生的间质性肺炎被称为结缔组织病相关性间质性肺病(connectivetissuediseaseassociatedinterstitiallungdisease:ctd-ild)。无基础疾病等原因不明的间质性肺炎被称为特发性间质性肺炎(iips)。关于间质性肺炎的治疗,ctd-ild与iips的治疗是不同的。对ctd-ild主要进行抗炎症疗法,使用类固醇等免疫抑制药。对在iips中占大部分的疾病、即特发性肺纤维化(ipf)则不进行抗炎症疗法,而是使用吡非尼酮等抗纤维化药。根据皮肤和关节等身体所见、自身抗体等血液检查来进行ctd-ild与iips的鉴别。对于ctd-ild而言,满足各种胶原病的诊断基准且可见间质性肺炎所特有的肺部病变。对于iips而言,观察不到胶原病特异性的身体所见、自身抗体等。另外有报道指出,通过测定血液中的生物标志物可对部分伴有胶原病的间质性肺炎与ipf进行鉴别。具体而言,非专利文献1记载了抗jo-1抗体阳性的间质性肺炎患者血清中的cxcl9(cxcchemokineligand9,cxc趋化因子配体9)及cxcl10(cxcchemokineligand10,cxc趋化因子配体10)的浓度显著高于ipf患者。抗jo-1抗体是作为胶原病之一的多发性肌炎/皮肌炎(pm/dm)特异性的自身抗体。但是,实际上在临床中ctd-ild与iips的鉴别并不容易。作为其原因之一,可列举在间质性肺炎中存在虽然可观察到胶原病相关症状、身体所见、自身抗体等但不满足胶原病的诊断基准的病例。这样的病例虽然具有疑似胶原病的特征,但不得不归类在iips中。但是,2015年欧州呼吸学会(ers)及美国胸腔学会(ats)提出了一种具有自身免疫特征的间质性肺炎(interstitialpneumoniawithautoimmunefeatures,ipaf)的新概念和其诊断基准(参照fischera.等,eurrespirj.,2015,vol.46,p.976-987)。ipaf的诊断基准以在临床领域、血清学领域及形态学领域中的至少2个领域中满足1个以上项目为条件。临床领域中,确认在手指、关节处是否可见胶原病特异性的症状。血清学领域中,确认是否可见胶原病特异性的自身抗体。形态学领域中,确认高分辨率ct图像或通过肺活检得到的组织中是否可见规定图案的间质性肺炎。现有技术文献非专利文献非专利文献1:richardst.j.等,characterizationandperipheralbloodbiomarkerassessmentofjo-1antibody-positiveinterstitiallungdisease,arthritisrheum.,2009,vol.60,p.2183-2192技术实现要素:发明要解决的课题ipaf的诊断基准需要由胶原病内科、呼吸内科、病理诊断科等多个专业领域的医生作出的诊断而形成。因此,例如呼吸内科的医生难以单独进行ipaf与ctd-ild的鉴别。另外,在胶原病之前可见肺部病变的病例也使鉴别诊断变得困难。即存在下述情况:即使暂时诊断为iips,但在发展过程中出现胶原病相关症状而怀疑为ipaf或ctd-ild。虽然各胶原病特异性的自身抗体等是已知的,但是对鉴别ipaf和ctd-ild有用的生物标志物目前还未出现。鉴于这种情况,本发明的目的在于,提供能够鉴别间质性肺炎患者的病情的手段。用于解决课题的手段因此,本发明提供一种取得间质性肺炎患者的病情相关信息的方法,其包括测定间质性肺炎患者的生物试样的至少1个生物标志物的步骤,生物标志物包括选自cxcl9及cxcl10中的至少1者,生物标志物的测定结果成为鉴别ipaf和ctd-ild的指标。本发明提供一种间质性肺炎患者的病情的判定方法,其包括:测定间质性肺炎患者的生物试样的至少1个生物标志物的工序;基于生物标志物的测定结果判定该患者为ipaf还是为ctd-ild的工序,生物标志物包含选自cxcl9及cxcl10中的至少1者。本发明提供一种取得ipaf患者的治疗应答性相关信息的方法,其包括测定ipaf患者的生物试样的至少1个生物标志物的步骤,生物标志物包含选自cxcl9及cxcl10中的至少1者,生物标志物的测定结果成为鉴别针对抗炎症疗法的治疗应答性的指标。本发明提供一种用于上述方法的试剂盒,其含有包含能够与cxcl9特异性结合的物质的试剂和/或包含能够与cxcl10特异性结合的物质的试剂。本发明提供间质性肺炎患者的病情的判定装置,其具备包含处理器及处于处理器控制下的存储器的计算机,存储器中记录有计算机程序,上述计算机程序使计算机执行下述步骤:取得间质性肺炎患者的生物试样中的至少1者生物标志物的测定结果的步骤;基于生物标志物的测定结果判定上述患者为ipaf或是为ctd-ild的步骤,生物标志物包含选自cxcl9及cxcl10中的至少1者。本发明提供一种用于判定间质性肺炎患者的病情的计算机程序,其记录于计算机可读介质,其记录有用于使计算机执行下述步骤的计算机程序:取得间质性肺炎患者的生物试样中的至少1者生物标志物的测定结果的步骤;基于生物标志物的测定结果判定上述患者为ipaf或是为ctd-ild的步骤,生物标志物包含选自cxcl9及cxcl10中的至少1者。发明效果根据本发明,能够取得间质性肺炎患者的病情相关信息。附图说明图1a为示出本实施方式的试剂盒的外观的一例的图。图1b为示出本实施方式的试剂盒的外观的一例的图。图2为示出间质性肺炎患者的病情的判定装置的一例的概要图。图3为示出间质性肺炎患者的病情的判定装置的硬件构成的框图。图4a为使用间质性肺炎患者的病情的判定装置的判定流程图。图4b为使用间质性肺炎患者的病情的判定装置的判定流程图。图4c为使用间质性肺炎患者的病情的判定装置的判定流程图。图4d为使用间质性肺炎患者的病情的判定装置的判定流程图。图5为示出ctd-ild、ipaf及ipf的各个患者群的血清中的cxcl9浓度的图。图6为示出ctd-ild、ipaf及ipf的各个患者群的血清中的cxcl10浓度的图。图7为基于血清中的cxcl9浓度判定患者为ctd-ild或是ipaf时的接收器工作特征(roc)曲线。图8为基于血清中的cxcl10浓度判定患者为ctd-ild或是ipaf时的roc曲线。图9为基于血清中的cxcl10浓度判定患者为ipaf或是ipf时的roc曲线。图10a为对于ipaf患者来示出抗炎症疗法治疗前的血清中的cxcl9浓度与1年间的用力肺活量恢复量(δfvc)的相关性的图。图10b为对于ipaf患者来示出抗炎症疗法治疗前的血清中的cxcl10浓度与1年间的用力肺活量恢复量(δfvc)的相关性的图。图11为基于由血清中的cxcl9及kl-6的浓度计算的预测值判定患者为ipaf或是ipf时的roc曲线。图12为基于由血清中的cxcl9及mmp9的浓度计算的预测值判定患者为ipaf或是ipf时的roc曲线。图13为基于由血清中的cxcl10及kl-6的浓度计算的预测值判定患者为ipaf或是ipf时的roc曲线。图14为基于由血清中的cxcl10及mmp9的浓度计算的预测值判定患者为ipaf或是ipf时的roc曲线。具体实施方式[1.取得间质性肺炎患者的病情相关信息的方法]本实施方式的取得间质性肺炎患者的病情相关信息的方法(以下也称为“取得方法”)中,测定间质性肺炎患者的生物试样中的至少1个生物标志物。(被检者及生物试样)在本实施方式中,被检者只要是被诊断为间质性肺炎的患者或疑似罹患了间质性肺炎的人就没有特别限定。本说明书中,“间质性肺炎患者”这一术语包括被诊断为间质性肺炎的患者及疑似罹患了间质性肺炎的人两者。被检者可以为未经治疗的间质性肺炎患者。另外,被检者可以为罹患了胶原病的间质性肺炎患者或疑似罹患了胶原病的间质性肺炎患者。间质性肺炎及胶原病的种类没有特别限定。生物试样只要是包含后述的生物标志物的试样就没有特别限定。作为这种生物试样,可列举例如血液试样、支气管肺泡洗液等。作为血液试样,可列举例如由被检者采集的血液(全血)、及由该血液制备的血浆或血清。在本实施方式中,特别优选血清。当生物试样包含细胞等不溶性杂质时,例如,可以通过离心分离、过滤等公知手段将杂质从生物试样中除去。另外,可以根据需要用合适的水性介质对生物试样进行稀释。这种水性介质只要不妨碍后述的测定就没有特别限定,可列举例如水、生理盐水、缓冲液等。缓冲液只要在中性附近的ph(例如6以上且8以下的ph)下具有缓冲作用就没有特别限定。这种缓冲液可列举例如hepes、mes、pipes等good’s缓冲液、tris缓冲生理盐水(tbs)、磷酸缓冲生理盐水(pbs)等。(生物标志物及其测定)作为生物标志物,可列举选自cxcl9及cxcl10中的至少1者。cxcl9也被称为mig(monokineinducedbyinterferonγ,干扰素γ诱导单核因子),是th1型趋化因子的一种。cxcl10也被称为ip-10(interferon-inducibleprotein-10,干扰素诱导蛋白-10),与cxcl9同样为一种th1趋化因子。cxcl9及cxcl10均为在th1细胞表面表达的cxcr3受体的配体。cxcl9及cxcl10的氨基酸序列本身是公知的,例如,可以由ncbi(nationalcenterforbiotechnologyinformation)等公知的数据库获知。本说明书中,“测定生物标志物”包括:确定生物标志物的量或浓度的值、及取得反映生物标志物的量或浓度的信息。“反映生物标志物的量或浓度的信息”是指根据生物试样或由该生物试样制备的测定试样中的生物标志物的量或浓度而变化的指标。这种指标优选为可目视或可通过机械方式测定的光学变化指标。作为光学变化指标,可列举例如发光强度、荧光强度、吸光度、浊度、显色的深度等。反映生物标志物的量或浓度的信息可以定性表示,也可以定量表示,还可以半定量表示。定性表示的信息为表示有无生物标志物的信息。定量表示的信息为利用测定仪器得到的数值(以下也称为“原始数据”)、由该数值计算的值等数值信息。作为由原始数据计算的值,可列举例如由原始数据减去阴性对照试样的值或背景值而得的值等。基于定量信息,可确定生物标志物的量或浓度的值。半定量表示的信息为将生物标志物的量或浓度通过语句、数字(表示等级)、颜色等分阶段示出的信息。例如,可以使用“检测限以下”、“少”、“中等”、“多”等语句。在本实施方式中,生物标志物的测定结果包括测定生物标志物而得到的值、信息及它们的组合。优选的实施方式中,生物标志物的测定结果为反映生物标志物的量或浓度的定量信息、和/或基于该定量信息确定的生物标志物的量或浓度的值。以下,也将反映生物标志物的量或浓度的定量信息、和/或生物标志物的量或浓度的值称为“生物标志物的测定值”。生物标志物的测定结果可以为1个生物标志物的测定值,也可以为2个生物标志物的测定值。生物标志物的测定值具体而言为cxcl9的测定值及cxcl10的测定值。另外,生物标志物的测定结果可以为使用2个以上生物标志物的测定值计算而得的值。在该计算中,可以根据需要进一步使用任意的系数和/或常数。例如,作为使用2个生物标志物的测定值计算的值,可列举2个测定值的比、积、和、差等。测定生物标志物的方法只要可以取得生物试样或由该生物试样制备的测定试样中的反映生物标志物的量或浓度的信息则没有特别限定。在本实施方式中,优选使用能够与生物标志物特异性结合的物质捕捉该生物标志物的方法。通过利用该
技术领域:
中公知的方法检测利用这样的物质捕捉的生物标志物,可以测定生物试样所含的生物标志物。作为能够与生物标志物特异性结合的物质,可列举例如抗体、适体、受体蛋白等。它们中,特别优选抗体。针对上述各生物标志物的抗体本身是公知的,通常能够获得。针对生物标志物的抗体只要是可以与生物标志物特异性结合的抗体就没有特别限定。这种抗体可以为单克隆抗体、多克隆抗体、及它们的片段(例如fab、f(ab')2、fab'等)中的任一者。另外,可以使用市售的抗体。使用抗体测定生物标志物的方法没有特别限定,可以从公知的免疫学测定法中适宜选择。作为这种测定法,可列举例如酶联免疫吸附法(elisa法)、蛋白质印迹法等。它们中,优选elisa法。elisa法的种类可以为夹心法、竞争法、直接法、间接法等中的任一者,特别优选夹心法。作为一例,以下说明通过夹心elisa法测定生物试样中的生物标志物的情况。首先,在固相上形成包含生物标志物、用于捕捉该生物标志物的抗体(以下也称为“捕捉用抗体”)、和用于检测该生物标志物的抗体(以下也称为“检测用抗体”)的复合物。该复合物可以通过将可包含生物标志物的生物试样、捕捉用抗体、和检测用抗体混合来形成。然后,使包含复合物的溶液与可以捕捉捕捉用抗体的固相接触,由此可以在固相上形成上述复合物。或者,可以使用预先固定有捕捉用抗体的固相。即,通过使固定有捕捉用抗体的固相、生物试样、和检测用抗体接触,可以在固相上形成上述复合物。需要说明的是,在捕捉用抗体及检测用抗体均为单克隆抗体时,优选彼此的表位不同。固相为能够固定捕捉用抗体的不溶性载体即可。捕捉用抗体在固相上的固定方式没有特别限定。例如,可以使捕捉用抗体和固相直接结合,也可以使捕捉用抗体和固相介由其它物质而间接结合。作为直接结合,可列举例如物理性吸附等。作为间接结合,可列举例如介由生物素与亲和素或链霉亲和素(以下也称为“亲和素类”)的组合的结合。这种情况下,通过预先用生物素修饰捕捉用抗体、使固相上预先结合有亲和素类,从而可以介由生物素和亲和素类的结合而使捕捉用抗体和固相间接结合。固相的材质没有特别限定,例如,可以从有机高分子化合物、无机化合物、生物高分子等中选择。作为有机高分子化合物,可列举胶乳、聚苯乙烯、聚丙烯等。作为无机化合物,可列举磁性体(氧化铁、氧化铬及铁氧体等)、二氧化硅、氧化铝、玻璃等。作为生物高分子,可列举不溶性琼脂糖、不溶性葡聚糖、明胶、纤维素等。可以将这些中的2种以上组合使用。固相的形状没有特别限定,可列举例如粒子、膜、微孔板、微管、试管等。它们中优选粒子,特别优选磁性粒子。本实施方式中,可以在复合物的形成工序和复合物的检测工序之间进行将未形成复合物的未反应的游离成分除去的b/f(bound/free)分离。未反应的游离成分是指未构成复合物的成分。例如,可列举未与生物标志物结合的捕捉用抗体及检测用抗体等。b/f分离的手段没有特别限定,如果固相为粒子,则通过利用离心分离仅回收捕捉了复合物的固相来实现b/f分离。如果固相为微孔板、微管等容器,通过将包含未反应的游离成分的液体除去来实现b/f分离。另外,在固相为磁性粒子时,在用磁体以磁力约束磁性粒子的状态下,通过喷嘴抽吸除去包含未反应的游离成分的液体,从而实现b/f分离,从自动化的观点出发是优选的。在除去未反应的游离成分后,可以用pbs等合适的水性介质洗涤捕捉有复合物的固相。然后,用该技术中公知的方法检测形成于固相上的复合物,可以测定生物试样所含的生物标志物。例如,在使用标记有标记物的抗体作为检测用抗体时,通过检测该标记物所产生的信号,可以测定生物试样的生物标志物。或者,在使用针对检测用抗体的标记二抗时,也可以同样地测定生物试样中的生物标志物。另外,作为使用抗体测定生物标志物的方法的例子,可以使用日本特开平1-254868号公报中记载的免疫复合物转移法。本说明书中,“检测信号”包括定性检测有无信号、定量信号强度、及半定量检测信号的强度。半定量检测是指:以“未产生信号”、“弱”、“中”、“强”等方式分阶段表示信号的强度。在本实施方式中,优选定量或半定量地检测信号强度。标记物只要产生可检测的信号就没有特别限定。例如,可以是其本身产生信号的物质(以下也称为“信号发生物质”),也可以是催化其它物质的反应而产生信号的物质。作为信号发生物质,可列举例如荧光物质、放射性同位素等。作为催化其它物质的反应而产生可检测的信号的物质,可列举例如酶。作为酶,可列举碱性磷酸酶、过氧化物酶、β-半乳糖苷酶、荧光素酶等。作为荧光物质,可列举异硫氰酸荧光素(fitc)、罗丹明、alexafluor(注册商标)等荧光色素、gfp等荧光蛋白等。作为放射性同位素,可列举125i、14c、32p等。这些中,作为标记物,优选酶,特别优选碱性磷酸酶及过氧化物酶。检测信号的方法本身在该
技术领域:
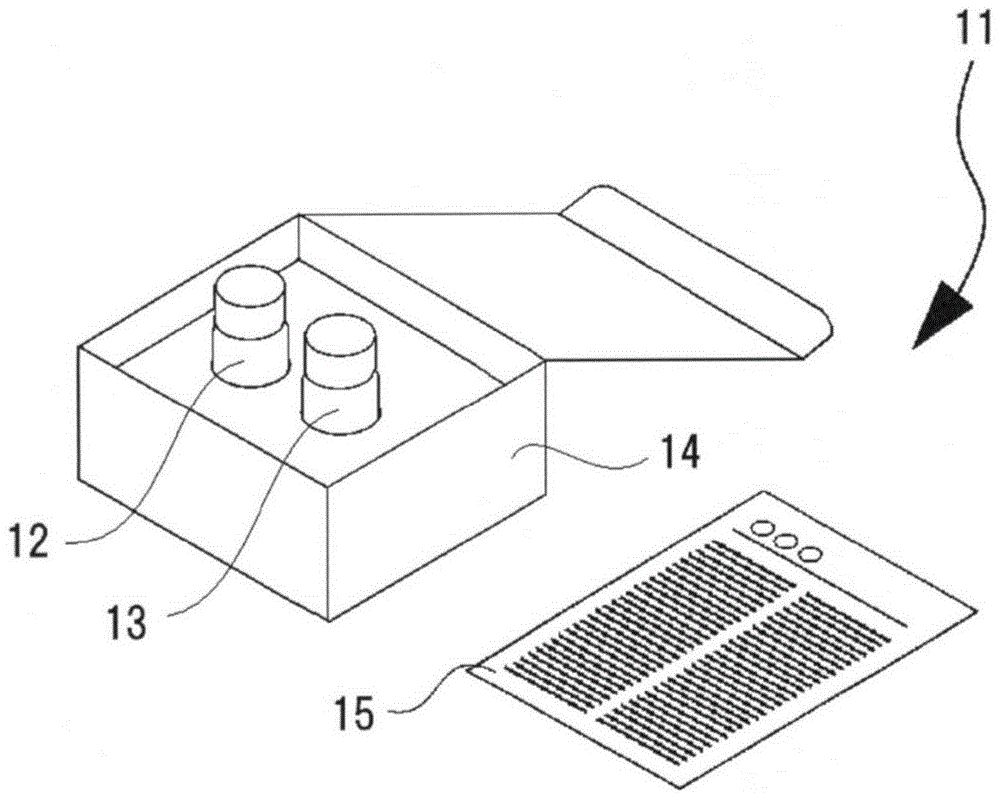
中是公知的。在本实施方式中,可以适宜选择与来自上述标记物的信号的种类相应的测定方法。例如,在标记物为酶的情况下,可以使用分光光度计等公知的装置测定通过使针对该酶的底物进行反应而产生的光、颜色等信号来进行。作为酶的底物,可以根据该酶的种类从公知的底物中适宜选择。例如,在使用碱性磷酸酶作为酶时,作为底物,可列举cdp-star(注册商标)(4-氯-3-(甲氧基螺[1,2-二氧杂环丁烷-3,2'-(5'-氯)三环[3.3.1.13,7]癸烷]-4-基)苯基磷酸二钠)、cspd(注册商标)(3-(4-甲氧基螺[1,2-二氧杂环丁烷-3,2-(5'-氯)三环[3.3.1.13,7]癸烷]-4-基)苯基磷酸二钠)等化学发光底物;5-溴-4-氯-3-吲哚基磷酸(bcip)、5-溴-6-氯-吲哚基磷酸二钠、对硝基苯基磷酸等显色底物。另外,在使用过氧化物酶作为酶时,作为底物,可列举鲁米诺及其衍生物等化学发光底物、2,2'-联氮双(3-乙基苯并噻唑啉-6-磺酸铵)(abts)、1,2-苯二胺(opd)、3,3',5,5'-四甲基联苯胺(tmb)等显色底物。在标记物为放射性同位素时,可以使用闪烁计数器等公知的装置测定作为信号的辐射线。另外,在标记物为荧光物质时,可以使用荧光用酶标仪等公知的装置测定作为信号的荧光。需要说明的是,可以根据使用的荧光物质的种类适宜确定激发波长及荧光波长。可以使用信号的检测结果作为生物标志物的测定结果。例如,在对信号的强度进行定量时,可以使用信号强度的测定值本身或由该测定值取得的值作为生物标志物的测定结果。作为由信号强度的测定值取得的值,可列举例如由该测定值减去阴性对照试样的测定值或背景值而得的值等。另外,可以将信号强度的测定值带入标准曲线来确定生物标志物的量或浓度的值。可以适宜选择阴性对照试样,可列举例如由健康人得到的生物试样等。在本实施方式中,优选通过使用固定于磁性粒子的捕捉用抗体和被标记物标记的检测用抗体的夹心elisa法,测定生物试样所含的游离蛋白质标志物。这种情况下,可以使用hiscl系列(希森美康株式会社制)等市售的全自动免疫测定装置来进行测定。(间质性肺炎患者的病情相关信息)在本实施方式中,生物标志物的测定结果成为ipaf和ctd-ild的鉴别指标。例如,如实施例所示,被诊断为ipaf的患者群的生物试样中的cxcl9及cxcl10浓度显著低于被诊断为ctd-ild的患者群。因此,在本实施方式中,可以取得生物标志物的测定结果作为间质性肺炎患者的病情相关信息。作为间质性肺炎患者的病情相关信息,可列举例如:表明间质性肺炎患者为ipaf的信息、或表明间质性肺炎患者为ctd-ild的信息。例如,在cxcl9的测定值或cxcl10的测定值低于对应于各生物标志物的规定阈值时,该测定值能表明患者为ipaf。或者,在cxcl9的测定值或cxcl10的测定值与对应于各生物标志物的规定阈值相同或更高时,该测定值能表明患者为ctd-ild。更具体的实施方式如下所述。在一实施方式中,生物标志物的测定结果为cxcl9的测定值。该实施方式中,cxcl9的测定值低于对应于cxcl9的规定阈值时,该测定值能表明患者为ipaf。在cxcl9的测定值与对应于cxcl9的规定阈值相同或更高时,该测定值能表明患者为ctd-ild。这里,对应于cxcl9的规定阈值为用于鉴别ipaf和ctd-ild的阈值。在另一实施方式中,生物标志物的测定结果为cxcl10的测定值。在该实施方式中,在cxcl10的测定值低于对应于cxcl10的规定阈值时,该测定值能表明患者为ipaf。当cxcl10的测定值与对应于cxcl10的规定阈值相同或更高时,该测定值能表明患者为ctd-ild。这里,对应于cxcl10的规定阈值为用于鉴别ipaf和ctd-ild的阈值。在又一实施方式中,生物标志物的测定结果为cxcl9的测定值及cxcl10的测定值。该实施方式中,在cxcl9的测定值低于第1阈值或cxcl10的测定值低于第2阈值时,这些测定值能表明患者为ipaf。当cxcl9的测定值与第1阈值相同或更高、且cxcl10的测定值与第2阈值相同或更高时,这些测定值能表明患者为ctd-ild。或者,在cxcl9的测定值低于第1阈值、且cxcl10的测定值低于第2阈值时,这些测定值能表明患者为ipaf。另外,在cxcl9的测定值与第1阈值相同或更高、或者cxcl10的测定值与第2阈值相同或更高时,这些测定值能表明患者为ctd-ild。这里,第1阈值为对应于cxcl9的规定阈值,第2阈值为对应于cxcl10的规定阈值。第1阈值及第2阈值为用于鉴别ipaf和ctd-ild的阈值。在又一实施方式中,生物标志物的测定结果也成为ipaf和ipf的鉴别指标。如实施例所示,被诊断为ipf的患者群的生物试样中的cxcl10浓度显著低于被诊断为ipaf的患者群。因此,间质性肺炎患者的病情相关信息可以是表明间质性肺炎患者为ipf的信息。在该实施方式中,生物标志物的测定结果为cxcl10的测定值。当cxcl10的测定值低于对应于cxcl10的规定阈值时,该测定值能表明患者为ipf。当cxcl10的测定值与对应于cxcl10的规定阈值相同或更高时,该测定值能表明患者为ipaf。这里,对应于cxcl10的规定阈值为用于鉴别ipaf和ipf的阈值。规定阈值没有特别限定,可以适宜设定。例如,可以通过积累间质性肺炎患者的生物标志物的测定值数据,从而根据经验来设定规定阈值。例如,可以如下所述地设定用于鉴别ctd-ild和ipaf的阈值。首先,从被诊断为ctd-ild的多个患者(ctd-ild群)及被诊断为ipaf的多个患者(ipaf群)采集生物试样,测定生物标志物,得到生物标志物的测定值。然后,求出能够以最高精度区别ctd-ild群和ipaf群的值,将该值设定为规定阈值。关于用于鉴别ipaf和ipf的阈值,也可以使用从被诊断为ipaf群及被诊断为ipf的多个患者(ipf群)采集的生物试样中的生物标志物的测定值同样地进行设定。在设定阈值时,优选考虑灵敏度、特异性、阳性命中率、阴性命中率等。通过本实施方式的取得方法得到的生物标志物的测定结果可以用于判定间质性肺炎患者的病情。可以令医生等医务工作者使用该测定结果来鉴别病情,也可以将该测定结果与其它信息组合来鉴别病情。这里,“其它信息”包括身体所见、组织所见或图像所见、血液检查结果、其它医学所见。(使用另一生物标志物的实施方式)本发明人发现测定作为另一生物标志物的kl-6(krebsvonderlungennr.6)及mmp9(matrixmetalloproteinase9,基质金属蛋白酶9),通过将这些的测定结果与cxcl9及cxcl10的测定结果组合能够进行ipaf和ipf的鉴别。由此,在本实施方式中,生物标志物还包含选自kl-6及mmp9中的至少1者。kl-6为唾液酸化糖链抗原的一种,作为间质性肺炎的标志物是众所周知的。mmp9为具有分解iv型胶原蛋白等活性的酶,作为与肺纤维化有关的标志物是众所周知的。kl-6及mmp9的氨基酸序列本身是公知的,例如,可以从ncbi等公共数据库获知。关于生物标志物的测定,如上所述。作为生物标志物的测定结果,可列举选自cxcl9及cxcl10中的至少1者的测定值、及选自kl-6及mmp9中的至少1者的测定值。优选地,生物标志物的测定结果为基于选自cxcl9及cxcl10中的至少1者的测定值、和选自kl-6及mmp9中的至少1者的测定值取得的值。作为这种值,可列举例如使用各生物标志物的测定值通过多变量分析而得到的值。作为通过多变量分析而得到的值,特别优选通过多元逻辑回归分析而得到的预测值。可以通过下述的回归式计算这种预测值。p=1/[1+exp{-(a1x1+a2x2+···+anxn+b)}]在上述的回归式中,x1~xn为各生物标志物的测定值,a1~an为各生物标志物的回归系数,b为常数。回归系数及常数可根据所使用的生物标志物的种类来适宜设定。例如,由从被诊断为ipaf的多个患者及被诊断为ipf的多个患者采集的生物试样中的生物标志物的测定值数据制作判别ipaf和ipf的多元逻辑模型,可以设定回归系数及常数。可以使用spssstatistics(ibm公司)等统计分析软件制作多元逻辑模型。在本实施方式中,优选由ipaf患者及ipf患者的生物标志物的测定值数据预先制作多元逻辑模型。在本实施方式中,作为基于选自cxcl9及cxcl10中的至少1者测定值和选自kl-6及mmp9中的至少1者测定值而取得的值,优选使用cxcl9的测定值与kl-6的测定值、cxcl9的测定值与mmp9的测定值、cxcl10的测定值与kl-6的测定值、或cxcl10的测定值与mmp9的测定值通过多元逻辑回归分析得到的预测值。测定作为生物标志物的选自cxcl9及cxcl10中的至少1者、和选自kl-6及mmp9中的至少1者时,生物标志物的测定结果成为ipaf与ipf的鉴别指标。具体而言,作为间质性肺炎患者的病情相关信息,可以取得表明间质性肺炎患者为ipaf的信息、或表明间质性肺炎患者为ipf的信息。例如,在生物标志物的测定结果为使用选自cxcl9及cxcl10中的至少1者测定值和选自kl-6及mmp9中的至少1者测定值通过多元逻辑回归分析而得到的预测值时,通过与阈值的比较,该预测值如下述那样表明间质性肺炎患者的病情相关信息。当预测值与规定阈值相同或更高时,该预测值能表明患者为ipaf。或者,在预测值低于规定阈值时,该预测值能表明患者为ipf。这里,规定阈值为用于鉴别ipaf和ipf的阈值。规定阈值的设定如上所述。[2.间质性肺炎患者的病情的判定方法]在本实施方式中,可以将通过上述方法得到的生物标志物的测定结果用于判定间质性肺炎患者的病情。在本实施方式的判定间质性肺炎患者的病情的方法(以下也称为“判定方法”)中,首先,测定间质性肺炎患者的生物试样中的至少1个生物标志物。该测定的细节与关于本实施方式的取得方法中的说明相同。在本实施方式的判定方法中,基于生物标志物的测定结果判定间质性肺炎患者的病情。具体而言,判定间质性肺炎患者为ctd-ild或是ipaf。生物标志物的测定结果的细节与关于本实施方式的取得方法中的说明相同。例如,在生物标志物的测定结果为cxcl9的测定值或cxcl10的测定值时,在cxcl9的测定值或cxcl10的测定值低于对应于各生物标志物的规定阈值时,判定患者为ipaf。或者,在cxcl9的测定值或cxcl10的测定值与对应于各生物标志物的规定阈值相同或更高时,判定患者为ctd-ild。对应于各生物标志物的规定阈值的细节与关于本实施方式的取得方法中的说明相同。更具体的实施方式如下所述。在一实施方式中,生物标志物的测定结果为cxcl9的测定值。该实施方式中,在cxcl9的测定值低于对应于cxcl9的规定阈值时,判定患者为ipaf。在cxcl9的测定值与对应于cxcl9的规定阈值相同或更高时,判定患者为ctd-ild。这里,对应于cxcl9的规定阈值为用于鉴别ipaf和ctd-ild的阈值。在另一实施方式中,生物标志物的测定结果为cxcl10的测定值。该实施方式中,在cxcl10的测定值低于对应于cxcl10的规定阈值时,判定患者为ipaf。在cxcl10的测定值与对应于cxcl10的规定阈值相同或更高时,判定患者为ctd-ild。这里,对应于cxcl10的规定阈值为用于鉴别ipaf和ctd-ild的阈值。在又一实施方式中,生物标志物的测定结果为cxcl9的测定值及cxcl10的测定值。该实施方式中,在cxcl9的测定值低于第1阈值、或cxcl10的测定值低于第2阈值时,判定患者为ipaf。在cxcl9的测定值与第1阈值相同或更高,且cxcl10的测定值与第2阈值相同或更高时,判定患者为ctd-ild。或者,在cxcl9的测定值低于第1阈值、且cxcl10的测定值低于第2阈值时,判定患者为ipaf。另外,在cxcl9的测定值与第1阈值相同或更高、或cxcl10的测定值与第2阈值相同或更高时,判定患者为ctd-ild。这里,第1阈值为对应于cxcl9的规定阈值,第2阈值为对应于cxcl10的规定阈值。第1及第2阈值为用于鉴别ipaf和ctd-ild的阈值。在又一实施方式中,基于生物标志物的测定结果判定间质性肺炎患者为ipaf或是ipf。该实施方式中,生物标志物的测定结果为cxcl10的测定值。在cxcl10的测定值低于对应于cxcl10的规定阈值时,判定患者为ipf。在cxcl10的测定值与对应于cxcl10的规定阈值相同或更高时,判定患者为ipaf。这里,对应于cxcl10的规定阈值为用于鉴别ipaf和ipf的阈值。在本实施方式中,生物标志物可以进一步包含选自kl-6及mmp9中的至少1者。测定选自cxcl9及cxcl10中的至少1者和选自kl-6及mmp9中的至少1者时,生物标志物的测定结果的细节与关于本实施方式的取得方法中的说明相同。优选地,生物标志物的测定结果为基于选自cxcl9及cxcl10中的至少1者测定值和选自kl-6及mmp9中的至少1者测定值而取得的值。这种值为使用各生物标志物的测定值通过多变量分析而得到的值,优选为通过多元逻辑回归分析而得到的预测值。在生物标志物的测定结果为例如使用选自cxcl9及cxcl10中的至少1者测定值和选自kl-6及mmp9中的至少1者测定值通过多元逻辑回归分析而得到的预测值时,通过该预测值与阈值的比较如下判定间质性肺炎患者的病情。在预测值与规定阈值相同或更高时,判定患者为ipaf。或者,在预测值低于规定阈值时,判定患者为ipf。这里,规定阈值为用于鉴别ipaf和ipf的阈值。规定阈值的设定如上所述。如上,本实施方式的判定方法能够对医生等医务工作者提供辅助间质性肺炎患者的病情的判定的信息。由此,对于间质性肺炎患者,能够进行与所判定的病情相应的合适治疗。例如,在ipf的治疗中使用抗纤维化药,但是在通过本实施方式的判定方法判定患者为ipaf时,则可以研究给药类固醇等免疫抑制药的方案。[3.间质性肺炎的治疗方法]本发明还包括根据通过本实施方式的判定方法而鉴别的病情来治疗间质性肺炎患者的方法。因此,本发明的一实施方式涉及间质性肺炎的治疗方法。本实施方式的间质性肺炎的治疗方法包括测定间质性肺炎患者的生物试样中的cxcl10的工序、基于cxcl10的测定结果判定上述患者为ipaf或是ipf的工序、和根据所判定的病情对上述患者给药间质性肺炎的治疗药的工序,在上述患者被诊断为ipaf时,对上述患者给药免疫抑制药,在上述患者被诊断为ipf时,对上述患者给药抗纤维化药。在判定工序中,在cxcl10的测定值与对应于cxcl10的规定阈值相同或更高时,判定患者为ipaf。或者,在cxcl10的测定值低于对应于cxcl10的规定阈值时,判定患者为ipf。这里,规定阈值为用于鉴别ipaf和ipf的阈值。另一实施方式的间质性肺炎的治疗方法包括测定间质性肺炎患者的生物试样中的至少1个生物标志物的工序、基于上述生物标志物的测定结果判定上述患者为ipaf或是ipf的工序、和根据所判定的病情对上述患者给药间质性肺炎的治疗药的工序,上述生物标志物包括选自cxcl9及cxcl10中的至少1者、和选自kl-6及mmp9中的至少1者,在上述患者被诊断为ipaf时,对上述患者给药免疫抑制药,在上述患者被诊断为ipf时,对上述患者给药抗纤维化药。在该实施方式中,生物标志物的测定结果优选为使用选自cxcl9及cxcl10中的至少1者的测定值和选自kl-6及mmp9中的至少1者的测定值通过多变量分析而得到的值。更优选生物标志物的测定结果为通过多元逻辑回归分析而得到的预测值。在判定工序中,在预测值与规定阈值相同或更高时,判定上述患者为ipaf。或者,在预测值低于规定阈值时,判定上述患者为ipf。这里,规定阈值为用于鉴别ipaf和ipf的阈值。间质性肺炎患者、生物试样、生物标志物的测定及规定阈值的细节与关于本实施方式的取得方法中的说明相同。在给药工序中,优选对患者给药治疗上有效量的免疫抑制药或抗纤维化药。作为免疫抑制药,可列举泼尼松龙、甲基泼尼松龙等类固醇药;环磷酰胺、硫唑嘌呤、环孢霉素、他克莫司等。作为抗纤维化药,可列举吡非尼酮、尼达尼布等。治疗上有效量可以根据间质性肺炎治疗指南等适宜决定。[4.取得被诊断为ipaf的患者的治疗应答性的相关信息的方法]通过ers及ats提出的ipaf诊断基准评价间质性肺炎的报道还不多。因此,对于通过该诊断基准而诊断为ipaf的患者应如何进行治疗这一点,尚不明确。但是我们认为,基本上对被诊断为ipaf的患者(以下也称为“ipaf患者”)应进行使用免疫抑制药等的抗炎症疗法。另一方面,我们也认为对于形态学领域(图像或组织)中显示普通型间质性肺炎(uip)图案的ipaf的情况,需要研究与ipf的治疗同样地不进行抗炎症疗法、而是使用抗纤维化药的方案。这里,如实施例所示,对于ipaf患者,在利用抗炎症疗法治疗前的血清中的cxcl9浓度与1年间的用力肺活量恢复量之间确认到显著性负相关。该结果表明,血清中的cxcl9浓度高的ipaf患者对抗炎症疗法的治疗应答性高。对于cxcl10,也确认到同样的倾向。由此,在本实施方式中,选自cxcl9及cxcl10中的至少1者的生物标志物的测定结果可成为鉴别ipaf患者对抗炎症疗法的治疗应答性的指标。在本实施方式的取得ipaf患者的治疗应答性的相关信息的方法中,首先,测定ipaf患者的生物试样中的选自cxcl9及cxcl10中的至少1者的生物标志物。ipaf患者可以是通过ers及ats提出的ipaf诊断基准而诊断的患者。或者,ipaf患者可以为基于本实施方式的判定方法的判定结果而诊断的患者。生物试样及生物标志物的测定细节与关于本实施方式的取得方法中的说明相同。在本实施方式中,在cxcl9的测定值或cxcl10的测定值与对应于各生物标志物的规定阈值相同或更高时,该测定值能表明ipaf患者对抗炎症疗法有应答性。或者,在本实施方式中,在cxcl9的测定值或cxcl10的测定值与对应于各生物标志物的规定阈值相同或更高时,可以判定ipaf患者对抗炎症疗法有应答性。在表明或判定ipaf患者对抗炎症疗法有应答性时,预期抗炎症疗法对该患者有效。这里,规定阈值为用于鉴别ipaf患者对抗炎症疗法的治疗应答性的阈值。这种阈值例如可以与用于鉴别ipaf和ipf的阈值相同。阈值的设定的细节与关于本实施方式的取得方法中的说明相同。更具体的实施方式如下所述。在一实施方式中,生物标志物的测定结果为cxcl9的测定值。该实施方式中,在cxcl9的测定值与对应于cxcl9的规定阈值相同或更高时,该测定值能表明ipaf患者对抗炎症疗法有应答性。或者,在本实施方式中,在cxcl9的测定值与对应于cxcl9的规定阈值相同或更高时,可判定ipaf患者对抗炎症疗法有应答性。这里,对应于cxcl9的规定阈值为用于鉴别ipaf患者对抗炎症疗法的治疗应答性的阈值。在另一实施方式中,生物标志物的测定结果为cxcl10的测定值。该实施方式中,在cxcl10的测定值与对应于cxcl10的规定阈值相同或更高时,该测定值能表明ipaf患者对抗炎症疗法有应答性。或者,在本实施方式中,在cxcl10的测定值与对应于cxcl10的规定阈值相同或更高时,可以判定ipaf患者对抗炎症疗法有应答性。这里,对应于cxcl10的规定阈值为用于鉴别ipaf患者对抗炎症疗法的治疗应答性的阈值。在又一实施方式中,生物标志物的测定结果为cxcl9的测定值及cxcl10的测定值。该实施方式中,在cxcl9的测定值与第1阈值相同或更高、且cxcl10的测定值与第2阈值相同或更高时,这些测定值能表明ipaf患者对抗炎症疗法有应答性。或者,在本实施方式中,在cxcl9的测定值与第1阈值相同或更高、且cxcl10的测定值与第2阈值相同或更高时,可以判定ipaf患者对抗炎症疗法有应答性。另外,在cxcl9的测定值与第1阈值相同或更高、或cxcl10的测定值与第2阈值相同或更高时,这些测定值能表明ipaf患者对抗炎症疗法有应答性。或者,在本实施方式中,在cxcl9的测定值与第1阈值相同或更高、或cxcl10的测定值与第2阈值相同或更高时,可以判定ipaf患者对抗炎症疗法有应答性。这里,第1阈值为对应于cxcl9的规定阈值,第2阈值为对应于cxcl10的规定阈值。第1及第2阈值为用于鉴别ipaf患者对抗炎症疗法的治疗应答性的阈值。[5.试剂盒]本发明的范围还包括用于本实施方式的方法及判定方法的试剂盒。即,提供一种试剂盒(以下也称为“试剂盒”),其含有包含能够与cxcl9特异性结合的物质的试剂和/或能够与cxcl10特异性结合的物质的试剂。能够与cxcl9及cxcl10分别特异性结合的物质的细节与关于可与本实施方式的方法中使用的生物标志物特异性结合的物质的说明相同。在本实施方式中,包含能够与cxcl9特异性结合的物质的试剂优选为包含针对cxcl9的捕捉用抗体的试剂与包含针对cxcl9的检测用抗体的试剂的组合。另外,包含能够与cxcl10特异性结合的物质的试剂优选为包含针对cxcl10的捕捉用抗体的试剂与包含针对cxcl10的检测用抗体的试剂的组合。检测用抗体可以用标记物进行标记。在标记物为酶时,试剂盒可以包含该酶的底物。捕捉用抗体、检测用抗体、标记物及底物的细节与上述本实施方式的方法中的说明相同。捕捉用抗体、检测用抗体、标记物及底物的形态没有特别限定,可以为固体(例如粉末、晶体、冻干品等),也可以为液体(例如溶液、悬浮液、乳浊液等)。在本实施方式中,可以将收容有各试剂的容器捆扎成箱而提供给用户。箱中可以附上随附文件。随附文件可以记载试剂盒的构成、使用方法、由该试剂盒得到的测定结果与间质性肺炎患者的病情的关系等。将这种试剂盒的例子示于附图。图1a所示的试剂盒中,作为包含能够与cxcl9特异性结合的物质的试剂,包括包含针对cxcl9的捕捉用抗体的试剂及包含针对cxcl9的检测用抗体的试剂,但本发明不限于该例子。参照图1a,11表示试剂盒,12表示收容有包含针对cxcl9的捕捉用抗体的试剂的第1容器,13表示收容有包含针对cxcl9的检测用抗体的试剂的第2容器,14表示包装箱,15表示随附文件。在该例中,第1容器可以收容包含针对cxcl10的捕捉用抗体的试剂,来代替包含针对cxcl9的捕捉用抗体的试剂。第2容器可以收容包含针对cxcl10的检测用抗体的试剂,来代替包含针对cxcl9的检测用抗体的试剂。该例子中,试剂盒可以进一步包含固相,所述固相用于固定针对cxcl9的捕捉用抗体。固相的细节与本实施方式的取得方法中的说明相同。图1b所示的试剂盒中,进一步包含作为包含能够与cxcl10特异性结合的物质的试剂的、包含针对cxcl10的捕捉用抗体的试剂及包含针对cxcl10的检测用抗体的试剂,但本发明不限于该例子。参照图1b,21表示试剂盒,22表示收容有包含针对cxcl9的捕捉用抗体的试剂的第1容器,23表示收容有包含针对cxcl9的检测用抗体的试剂的第2容器,24表示收容有包含针对cxcl10的捕捉用抗体的试剂的第3容器,25表示收容有包含针对cxcl10的检测用抗体的试剂的第4容器,26表示包装箱,27表示随附文件。在该例中,试剂盒可以进一步包含固相,所述固相用于分别固定针对cxcl9的捕捉用抗体及针对cxcl10的捕捉用抗体。固相的细节与本实施方式的取得方法中的说明相同。本实施方式的试剂盒可以进一步包含选自下述中的至少1种试剂:包含能够与kl-6特异性结合的物质的试剂、及包含能够与mmp9特异性结合的物质的试剂。包含能够与kl-6特异性结合的物质的试剂优选为包含针对kl-6的捕捉用抗体的试剂及包含针对kl-6的检测用抗体的试剂的组合。另外,包含能够与mmp9特异性结合的物质的试剂优选为包含针对mmp9的捕捉用抗体的试剂及包含针对mmp9的检测用抗体的试剂的组合。本实施方式的试剂盒可以包含各生物标志物的校准品。作为校准品的一例,可列举cxcl9定量用校准品及cxcl10定量用校准品。cxcl9定量用校准品例如可以具备不含cxcl9的缓冲液(阴性对照)和含已知浓度的cxcl9的缓冲液。cxcl10定量用校准品例如可以具备不含cxcl10的缓冲液(阴性对照)和含已知浓度的cxcl10的缓冲液。作为校准品的另一例,具备不含cxcl9及cxcl10中的任一者的缓冲液(阴性对照)、含已知浓度的cxcl9的缓冲液、和含已知浓度的cxcl10的缓冲液。作为校准品的另一例,具备不含cxcl9及cxcl10中的任一者的缓冲液(阴性对照)、和包含各自已知的浓度的cxcl9及cxcl10的缓冲液。在试剂盒包含选自包含能够与kl-6特异性结合的物质的试剂及包含能够与mmp9特异性结合的物质的试剂中的至少1种试剂时,该试剂盒可以包含这些生物标志物的校准品。作为校准品的一例,可列举kl-6定量用校准品及mmp9定量用校准品。kl-6定量用校准品例如可以具备不含kl-6的缓冲液(阴性对照)和包含已知浓度的kl-6的缓冲液。mmp9定量用校准品例如可以具备不含mmp9的缓冲液(阴性对照)、和包含已知浓度的mmp9的缓冲液。作为校准品的另一例,具备不含kl-6及mmp9中的任一者的缓冲液(阴性对照)、包含已知浓度的kl-6的缓冲液、和包含已知浓度的mmp9的缓冲液。作为校准品的另一例,具备不含kl-6及mmp9中的任一者的缓冲液(阴性对照)、和包含各自已知浓度的kl-6及mmp9的缓冲液。[6.装置及计算机程序]本发明的范围还包括一种用于实施本实施方式的间质性肺炎患者的病情的判定方法的装置及计算机程序。参照附图说明本实施方式的间质性肺炎患者的病情的判定装置的一例。但是,本实施方式并非仅限于该例子所示的方式。图2所示的判定装置10包含测定装置20、计算机系统30、和打印机40。测定装置20及打印机40连接于计算机系统30。测定装置的种类没有特别限定,可以根据生物标志物的测定方法适宜选择。在图2所示的例子中,测定装置20为能够检测由夹心elisa法产生的化学发光信号的市售的自动免疫测定装置,所述夹心elisa法使用固定有捕捉用抗体的磁性粒子及实施了酶标记的检测用抗体。但是,本发明不限于该例子。在通过elisa法测定生物标志物时,测定装置只要能够检测基于所用的标记物的信号就没有特别限定。将包含固定有捕捉用抗体的磁性粒子的试剂、包含实施了酶标记的检测用抗体的试剂及由间质性肺炎患者采集的生物试样安放在测定装置20中,该测定装置20使用各试剂执行抗原抗体反应,作为基于与生物标志物特异性结合的酶标记抗体的光学信息而取得化学发光信号,将得到的光学信息发送到计算机系统30。计算机系统30包含计算机主体300、输入部301和显示部302。显示部302显示被检体信息、判定结果等。计算机系统30从测定装置20接收光学信息。然后,计算机系统30的处理器基于光学信息执行硬盘313中安装的、用于判定间质性肺炎患者的病情的计算机程序。需要说明的是,如图2所示,计算机系统30可以为与测定装置20分开的设备。或者,计算机系统30为可以内置测定装置20的设备。在后者的情况下,计算机系统30本身可以成为判定装置10。可以在市售的自动免疫测定装置中搭载用于判定间质性肺炎患者的病情的计算机程序。参照图3,计算机主体300具备cpu(centralprocessingunit)310、rom(readonlymemory)311、ram(randomaccessmemory)312、硬盘313、输入输出接口314、读取装置315、通信接口316、和图像输出接口317。过总线318以可进行数据通信方式连接cpu310、rom311、ram312、硬盘313、输入输出接口314、读取装置315、通信接口316及图像输出接口317。另外,通过通信接口316以能够与计算机系统30通信的方式连接测定装置20及打印机40。cpu310能够执行rom311或硬盘313中存储的程序及下载到ram312中的程序。cpu310基于由测定装置20取得的光学信息而取得生物标志物的测定值。在测定选自cxcl9及cxcl10中的至少1者、和选自kl-6及mmp9中的至少1者时,cpu310可以取得由这些生物标志物的测定值得到的值、例如通过多元逻辑回归分析而得到的预测值。这些值的细节与关于本实施方式的取得方法中的说明相同。cpu310基于取得的值以及rom311或硬盘313中存储的规定阈值来判定间质性肺炎的病情。cpu310输出并在显示部302显示判定结果。需要说明的是,可以在制造计算机系统时由制造者预先在rom311或硬盘313中存储对应于各生物标志物的阈值。或者,可以由用户使用输入部301输入对应于各生物标志物的阈值,并存储于rom311或硬盘313。rom311由掩码rom、prom、eprom、eeprom等构成。rom311中记录有cpu310所要执行的计算机程序及在执行该计算机程序时使用的数据。rom411中记录有对应于各生物标志物的规定阈值、上述回归式等用于后述的判定流程的数据。ram312由sram、dram等构成。在读出rom311及硬盘313中记录的程序时使用ram312。另外,在执行这些程序时,将ram312作为cpu310的工作区域来使用。硬盘313安装有用于使cpu310执行的操作系统、应用程序(间质性肺炎患者的病情的判定用程序)等计算机程序及在执行该计算机程序时使用的数据。硬盘313中还可以记录对应于各生物标志物的规定阈值、上述回归式等在后述的判定流程中使用的数据。读取装置315由软盘驱动器、cd-rom驱动器、dvd-rom驱动器、usb端口、sd卡读取器、cf卡读取器、记忆棒读取器、固态驱动器等构成。读取装置315可以读取记录于便携记录介质50的程序或数据。输入输出接口314例如由usb、ieee1394、rs-232c等串行接口、scsi、ide、ieee1284等并行接口、和包括d/a变换器、a/d变换器等的模拟接口构成。输入输出接口314上连接有键盘、鼠标等输入部301。用户能够通过该输入部301向计算机主体300输入各种指令。通信接口316为例如符合ethernet(注册商标)接口、ieee802.11系列、bluetooth(注册商标)等标准的无线接口等。计算机主体300能够通过通信接口316向打印机40等发送打印数据。打印机40为例如激光打印机、喷墨打印机等。在通信接口316为无线接口时,计算机主体300能够向手机、平板终端等移动设备发送数据。图像输出接口317连接于由lcd、crt等构成的显示部302。由此,显示部302可以输出与cpu310所提供的图像数据对应的视频信号。显示部302根据所输入的视频信号来显示图像(画面)。参照图4a来说明判定装置10所执行的、间质性肺炎患者的病情的判定流程。这里,以由通过夹心elisa法而产生的化学发光信号的强度取得cxcl9的测定值,使用取得的测定值和对应于cxcl9的规定阈值,判定患者为ipaf或是为ctd-ild的情况为例进行说明。但是,本实施方式并非仅限于该例子。也可以取得cxcl10的测定值来代替cxcl9的测定值。在步骤s101中,cpu310由测定装置20取得光学信息(化学发光信号),存储于硬盘313。在步骤s102中,cpu310由取得的光学信息而取得cxcl9的测定值,存储于硬盘313。在步骤s103中,cpu310对取得的测定值和硬盘313中存储的规定阈值进行比较。在测定值低于规定阈值时,处理进入步骤s104。在步骤s104中,cpu310将表明患者为ipaf的判定结果存储于硬盘313。在测定值与规定阈值相同或更高时,处理进入步骤s105。在步骤s105中,cpu310将表明患者为ctd-ild的判定结果存储于硬盘313。在步骤s106中,cpu310输出判定结果。例如,cpu310将判定结果现实中显示部302、或者通过打印机40打印、或者发送到手机或平板终端等移动设备。由此,可以将辅助间质性肺炎患者的病情的判定的信息提供给医生等。参照图4b,以取得cxcl9的测定值及cxcl10的测定值、并且使用这些测定值和对应于各生物标志物的规定阈值进行判定的情况为例进行说明。在该例子中,第1阈值为对应于cxcl9的规定阈值,第2阈值为对应于cxcl10的规定阈值。步骤s201及s207分别与关于上述步骤s101及s106的说明相同。在步骤s202中,cpu310由取得的光学信息而取得cxcl9及cxcl10的测定值,存储于硬盘313。在步骤s203中,cpu310对取得的cxcl9的测定值和硬盘313中存储的第1阈值进行比较。在cxcl9的测定值低于第1阈值时,处理进入步骤s204。在步骤s204中,cpu310对取得的cxcl10的测定值和硬盘313中存储的第2阈值进行比较。在cxcl10的测定值低于第2阈值时,处理进入步骤s205。在步骤s205中,cpu310将表明患者为ipaf的判定结果存储于硬盘313。在步骤s203中,在cxcl9的测定值与第1阈值相同或更高时,处理进入步骤s206。在步骤s204中,在cxcl10的测定值与第2阈值相同或更高时,处理进入步骤s206。在步骤s206中,cpu310将表明患者为ctd-ild的判定结果存储于硬盘313。在该例子中,步骤s203及步骤s204的处理可以交换顺序。参照图4c,以取得cxcl10的测定值、并且使用取得的测定值和对应于cxcl10的规定阈值来判定患者为ipaf或是ipf的情况为例进行说明。步骤s301及s306分别与关于上述步骤s101及s106的说明相同。在步骤s302中,cpu310由取得的光学信息而取得cxcl10的测定值,存储于硬盘313。在步骤s303中,cpu310对取得的测定值和硬盘313中存储的规定阈值进行比较。在测定值与规定阈值相同或更高时,处理进入步骤s304。在步骤s304中,cpu310将表明患者为ipaf的判定结果存储于硬盘313。在测定值低于规定阈值时,处理进入步骤s305。在步骤s305中,cpu310将表明患者为ipf的判定结果存储于硬盘313。参照图4d,以取得cxcl9的测定值及kl-6的测定值、使用这些测定值通过上述的回归式计算预测值p、并且使用预测值p和规定阈值进行判定的情况为例进行说明。但是,本实施方式并非仅限于该例子。可以取得cxcl10的测定值来代替cxcl9的测定值。另外,可以取得mmp9的测定值来代替kl-6的测定值。步骤s401及s407分别与关于上述步骤s101及s106的说明相同。在步骤s402中,cpu310由取得的光学信息而取得cxcl9及kl-6的测定值,存储于硬盘313。在步骤s403中,cpu310根据硬盘313中存储的回归式,计算基于多元逻辑模型的预测值p,存储于硬盘313。在步骤s404中,cpu310对计算而得的预测值p和硬盘313中存储的规定阈值进行比较。在预测值p与规定阈值相同或更高时,处理进入步骤s405。在步骤s405中,cpu310将表明患者为ipaf的判定结果存储于硬盘313。在预测值p低于规定阈值时,处理进入步骤s406。在步骤s406中,cpu310将表明患者为ipf的判定结果存储于硬盘313。以下在实施例中更详细地说明本发明,但是本发明不受这些实施例限定。以下,“hiscl”为希森美康株式会社的注册商标。【实施例】[实施例1](1)生物试样作为生物试样,使用102名间质性肺炎患者的血清。102名患者中,被诊断为ctd-ild的患者(ctd-ild群)为16名,被诊断为ipaf的患者(ipaf群)为35名,被诊断为ipf的患者(ipf群)为51名。(2)生物标志物的测定(2.1)cxcl9的测定使用下述的r1~r5试剂,利用全自动免疫测定装置hiscl-5000或hiscl-2000i(希森美康株式会社)测定各患者的血清中的cxcl9浓度。·r1试剂将抗mig单克隆抗体(randox公司)通过常规方法用胃蛋白酶或ides蛋白酶消化,得到fab片段。用常规方法以生物素标记fab片段,溶解于含有1%牛血清白蛋白(bsa)及0.5%酪蛋白的缓冲液,得到r1试剂。·r2试剂将表面固定有链霉亲和素的磁性粒子(以下也称为“sta结合磁性粒子”。平均粒径2μm。每1g磁性粒子的链霉亲和素量为2.9~3.5mg)用10mmhepes缓冲液(ph7.5)洗涤3次。将洗涤后的sta结合磁性粒子以链霉亲和素浓度达到18~22μg/ml(sta结合磁性粒子的浓度达到0.48~0.52mg/ml)的方式添加到10mmhepes(ph7.5)中,得到r2试剂。·r3试剂将抗mig单克隆抗体(randox公司)用常规方法通过胃蛋白酶或ides蛋白酶消化,得到fab片段。用常规方法以碱性磷酸酶(alp)标记fab片段,溶解于含有1%bsa及0.5%酪蛋白的缓冲液,得到r3试剂。·r4试剂及r5试剂作为r4试剂,使用作为测定用缓冲液的hisclr4试剂(希森美康株式会社)。作为r5试剂,使用hisclr5试剂(希森美康株式会社),其包含作为alp的化学发光底物的cdp-star(注册商标)(appliedbiosystems公司)。利用hiscl-5000或hiscl-2000i的测定步骤如下所述。将血清(20μl)和r1试剂(50μl)混合后,添加r2试剂(30μl)。通过磁性而收集所得到的混合液中的磁性粒子,除去上清,加入hiscl洗涤液(300μl)洗涤磁性粒子。除去上清,向磁性粒子中添加r3试剂(100μl),混合。通过磁性而收集所得到的混合液中的磁性粒子,除去上清,加入hiscl洗涤液(300μl)而洗涤磁性粒子。除去上清,向磁性粒子中添加r4试剂(50μl)及r5试剂(100μl),测定化学发光强度。将得到的化学发光强度带入标准曲线,确定cxcl9浓度。(2.2)cxcl10的测定通过酶联免疫吸附测定(enzyme-linkedimmunosorbentassay,elisa)测定各患者的血清中的cxcl10浓度。cxcl10的测定步骤如下所述。在96孔板中,使通过被检体稀释液稀释了5倍的血清(100μl)与以2μg/ml致敏的抗cxcl10小鼠单克隆抗体反应2小时。用hiscl洗涤液(300μl)洗涤6次后,添加100μl的生物素化山羊抗人cxcl10抗体(0.0125μg/ml,1%bsa0.5%酪蛋白pbsph7.4),反应2小时。用hiscl洗涤液(300μl)洗涤6次后,添加100μl的链霉亲和素alp,反应20分钟。用hiscl洗涤液(300μl)洗涤6次后,添加以1:2混合后的r4及r5试剂100μl,用酶标仪对发光信号进行计数。抗cxcl10抗体使用了r&dsystems公司制造的duosetdy266。(3)测定结果将ctd-ild、ipaf及ipf的各患者群的血清中的cxcl9及cxcl10浓度分别示于图5及6。可知ipaf群及ipf群的cxcl9及cxcl10浓度显著低于ctd-ild群。因此这表明,血清中的cxcl9及cxcl10可作为能够鉴别ctd-ild和ipaf的生物标志物使用。另外,获知ipf群的cxcl10浓度显著低于ipaf群。这表明,血清中的cxcl10可作为能够鉴别ipaf和ipf的生物标志物使用。[实施例2](1)ctd-ild和ipaf的鉴别通过roc分析,对于血清中的cxcl9浓度及cxcl10浓度,求出区别实施例1的ctd-ild群(16名)和ipaf群(35名)的最适截止值。计算使用所设定的截止值的判定的灵敏度、特异性及曲线下面积(auc)。该判定中,在cxcl9或cxcl10浓度与截止值相同或更高时,判定患者为ctd-ild。另外,在cxcl9或cxcl10浓度低于截止值时,判定患者不为ctd-ild。将得到的roc曲线示于图7及8。将各生物标志物的截止值(pg/ml)、判定的灵敏度(%)、特异性(%)及auc示于表1。【表1】生物标志物截止值灵敏度(%)特异性(%)auccxcl932.587490.72cxcl10287.160800.75根据表1,在基于血清中的cxcl9浓度及cxcl10浓度的各值的判定中,auc的值为0.7以上,支持了血清中的cxcl9及cxcl10为在鉴别ctd-ild和ipaf时有用的生物标志物这一点。以往,基于胶原病的诊断基准进行ctd-ild的诊断,基于ers及ats提出的诊断基准进行ipaf的诊断。这些诊断基准包含了医生的观察结果、图像诊断等主观要素。但是,上述的结果表明,作为客观指标的生物试样中的cxcl9及cxcl10的浓度可成为用于鉴别ctd-ild和ipaf的指标。(2)ipaf和ipf的鉴别通过roc分析,对于血清中的cxcl10浓度,求出区别实施例1的ipaf群(35名)和ipf群(51名)的最适截止值。计算使用所设定的截止值的判定的灵敏度、特异性及auc。在该判定中,在cxcl10浓度与截止值相同或更高时,判定患者为ipaf。另外,在cxcl10浓度低于截止值时,判定患者不为ipaf。将得到的roc曲线示于图9。将cxcl10的截止值(pg/ml)、判定的灵敏度(%)、特异性(%)及auc示于表2。【表2】生物标志物截止值灵敏度(%)特异性(%)auccxcl10226.640960.67根据表2,基于血清中的cxcl10浓度的判定中,auc的值为约0.7,可知通过血清中的cxcl10浓度值也可以进行ipaf和ipf的鉴别。该判定的特异性特别高,由此表明:在ipaf和ipf的鉴别中,血清中的cxcl10对排除ipf疑似患者有用。如图10a所示,对于ipaf患者,以抗炎症疗法治疗前的血清中的cxcl9浓度为横轴、以1年间的用力肺活量恢复量(afvc)为纵轴进行作图时,在血清中的cxcl9浓度与δfvc之间可确认到显著的负相关。这表明,血清中的cxcl9浓度高的患者对抗炎症疗法的治疗应答性高。另外,如图10b所示,虽然关于血清中的cxcl10浓度未得到统计学上的相关性,但是该值低的患者未见用力肺活量恢复,因此确认到同样的倾向。[实施例3](1)生物试样作为生物试样,使用实施例1的间质性肺炎患者的血清。(2)生物标志物的测定(2.1)cxcl9及cxcl10的测定作为各患者的血清中的cxcl9及cxcl10浓度值,使用实施例1中取得的测定值。(2.2)kl-6的测定使用hisclkl-6试剂(积水医疗株式会社),利用iscl-5000或hiscl-2000i(希森美康株式会社)测定各患者的血清中的kl-6浓度。kl-6的测定步骤与实施例1的cxcl9的测定相同。hisclkl-6试剂中包含含有生物素标记小鼠抗kl-6单克隆抗体的r1试剂、含有sta结合磁性粒子的r2试剂、含有alp标记小鼠抗kl-6单克隆抗体的r3试剂、作为测定用缓冲液的hisclr4试剂、含有cdp-star(注册商标)的hisclr5试剂、hiscl洗涤液、及kl-6校准品。(2.3)mmp9的测定通过酶联免疫吸附测定(enzyme-linkedimmunosorbentassay,elisa)测定实施例1的各患者的血清中的mmp9浓度。mmp9的测定步骤如下所述。在96孔板中,使通过被检体稀释液稀释5倍的血清(100μl)与以0.5μg/ml致敏的抗mmp9小鼠单克隆抗体反应2小时。用hiscl洗涤液(300μl)洗涤6次后,添加100μl的生物素化山羊抗人mmp9抗体(0.1μg/ml,1%bsa0.5%酪蛋白teaph7.4),反应2小时。用hiscl洗涤液(300μl)洗涤6次后,添加100μl的链霉亲和素alp反应20分钟。用hiscl洗涤液(300μl)洗涤6次后,添加以1:2混合的r4及r5试剂100μl,用酶标仪对发光信号进行计数。抗mmp9抗体使用了r&dsystems公司的duosetdy911。(3)ipaf与ipf的鉴别使用血清中的cxcl9、cxcl10、kl-6及mmp9的浓度作为解释变量而进行多元逻辑回归分析。该分析中,使用spssstatisticsversion22.0(ibm公司)。对于cxcl9与kl-6的组合、cxcl9与mmp9的组合、cxcl10与kl-6的组合、及cxcl10与mmp9的组合,求出区别实施例1的ipaf群(35名)和ipf群(51名)的最适截止值。计算使用所设定的截止值的判定的灵敏度、特异性及auc。在该判定中,在通过多元逻辑回归分析而得到的预测值p与截止值相同或更高时,判定患者为ipaf。另外,在预测值p低于截止值时,判定患者不为ipaf。将得到的roc曲线示于图11~14。将截止值、判定的灵敏度(%)、特异性(%)及auc示于表3。【表3】生物标志物截止值灵敏度(%)特异性(%)auccxcl9及kl-60.3791350.64cxcl9及mmp90.4954810.67cxcl10及kl-60.4449830.68cxcl10及mmp90.4271750.76根据表3,在基于任一生物标志物的组合的判定中,auc的值均为约0.7。表明该组合可成为鉴别ipaf和ipf的指标。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1