一种靶向纳米系统及其制备方法和应用与流程
本发明涉及一种靶向纳米系统及其制备方法和应用,属于生物医学材料技术领域。
背景技术:
肺癌是一种致命性极强的疾病,死亡率与发病率之比为87:100,到20世纪末已成为全球所有癌症相关死亡的主要原因。2012年,全球估计新增病例180万例,肺癌相关死亡160万例,约占所有癌症相关死亡人数的19%。到2035年,全球与肺癌相关的死亡人数预计将增加到300万。肺癌的治疗方式包括手术、化疗、放射治疗或靶向治疗,具体取决于癌症分期。然而,手术通常被认为是不符合条件的,因为患者被诊断为晚期。尽管在开发新的有助于早期诊断的生物标志物方面做出了巨大的努力,但这一目标尚未实现。无论是单独使用还是与其他治疗策略相结合,化疗都是肺癌治疗中的主要关键因素。吸入性化疗为肺癌提供了几个理论上的优势,但静脉注射给药仍然是主要的治疗手段。然而现有的化疗药物,由于低生物利用度和耐药性的发展,可能会对靶向治疗区域以外的其他细胞和组织产生不利影响。因此,迫切需要高特异性的新治疗技术,以智能地将抗癌药物释放到癌细胞中。为解决这些问题,基于纳米材料的药物递送系统(ddss)已被设计并显示出良好的治疗效果。然而,大多数药物不具有生物相容性和生物降解性,从而形成潜在的毒性。此外,这些材料通常没有固有的肿瘤靶向特性。研究表明,使用特定的配体(如抗体、肽或小分子)来功能化它们,以显著提高各种化疗药物的靶向抗肿瘤效率。
一般而言,两种或多种药物的联合应用具有协同抗肿瘤作用,并可减少毒副作用。多西紫杉醇是一种基于紫杉烷的化疗药物,用于治疗非小细胞肺癌、乳腺癌和鼻咽癌等肿瘤,它通过干扰有丝分裂和间期细胞功能所需的微管网络来发挥抗肿瘤作用。姜黄素是从姜黄根中提取的一种多酚类化合物,能诱导肿瘤细胞凋亡,提高肿瘤细胞的敏感性,通过调节各种途径,包括nf-kb和pi3k/akt信号通路,达到化疗放射治疗的目的。因此,多西紫杉醇和姜黄素的组合将是治疗恶性肿瘤的绝佳药物。然而,化疗药物的耐药性和副作用等问题亟待解决。
因此,鉴于纳米药物在联合治疗中的潜力,本发明以羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯(cmcs-bape)为主体,研发了一种新的t7靶向纳米系统t7-羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯-多烯紫杉醇/姜黄素(t7-cmcs-bape-dtx/cur),用于多西紫杉醇和姜黄素的联合给药。在体外和体内对t7-cmcs-bape-dtx/cur纳米系统的粒径分布、刺激响应释放、细胞毒性、细胞摄取和渗透性进行了深入研究。结果表明,合成的纳米药物能够靶向结合肺癌细胞表面表达的tfr,并在ph/ros刺激下释放负载的多药,为今后肿瘤的精确治疗提供了可能,有望成为肺癌靶向治疗的潜在药物。
技术实现要素:
本发明的目的在于克服上述现有技术的不足之处而提供一种靶向纳米系统及其制备方法和应用,该靶向纳米系统具有特异性地到达病变器官或组织的靶向分子,减少化疗药物对正常组织的伤害,提高药物利用度,改善肺癌的治疗效果。
为实现上述目的,本发明采取的技术方案为:一种靶向纳米系统,所述靶向系统包含如下重量份的组分:羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯10~100份、多烯紫杉醇1~20份、姜黄素1~40份、t7多肽50~100份。
本发明研发了一种新型的t7靶向纳米药物t7-cmcs-bape-dtx/cur,它通过受体介导的内毒素结合肺癌细胞表面过表达的tfr,可以增强主动靶向作用,从而使纳米药物更容易进入肿瘤细胞;并且针对肺癌细胞的弱酸和高ros水平,负载在纳米载体上的多西紫杉醇和姜黄素由于其ph/ros双刺激响应能力而释放出来,多西紫杉醇和姜黄素的最佳药物组合进行协同抗肿瘤作用。
作为本发明所述靶向纳米系统的优选实施方式,所述靶向系统包含如下重量的组分:羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯50份、多烯紫杉醇10份、姜黄素20份、t7多肽80份。在该配比下,能得到反应的最佳反应效率。
作为本发明所述靶向纳米系统的优选实施方式,所述羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯的制备方法为:
(1)将4-羟甲基-苯硼酸频哪醇酯溶于二氯甲烷中,滴加pbr3,氮气保护下室温反应,减压蒸馏除去溶剂后加入乙腈,调节ph至碱性;
(2)将羧甲基壳聚糖溶于去离子水中,与步骤(1)所得溶液混合,氮气保护条件下避光反应,将混合溶液置于透析、冷冻干燥,即得羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯纳米胶束。
作为本发明所述靶向纳米系统的优选实施方式,所述羧甲基壳聚糖的重量份为1~5份,4-羟甲基-苯硼酸频哪醇酯的重量份为1~5份。
优选地,所述羧甲基壳聚糖的重量份为2.3份,4-羟甲基-苯硼酸频哪醇酯的重量份为2.6份。
作为本发明所述靶向纳米系统的优选实施方式,所述步骤(1)中,室温反应时间为1h,用5%的na2co3溶液调节ph至碱性。
作为本发明所述靶向纳米系统的优选实施方式,所述步骤(2)中,避光反应时间为24h,透析袋的截留分子量为3500da,透析时间为3天。
第二方面,本发明提供了上述靶向纳米系统的制备方法,包括以下步骤:
(1)将羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯溶于纯水中形成羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯溶液,将多烯紫杉醇、姜黄素分别溶于dmso中,形成多烯紫杉醇溶液、姜黄素溶液;超声条件下,将多烯紫杉醇溶液、姜黄素溶液滴加进入羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯溶液中,继续超声形成混合均匀的有机相;
(2)超声条件下,将有机相滴加到去离子水中,用探头超声形成乳液,将乳液透析、冷冻干燥,得到载双药的纳米复合胶束,待用;
(3)将t7多肽溶于pbs缓冲液中,加入1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)、n-羟基琥珀酰亚胺(nhs),室温搅拌,然后将步骤(2)所得的载双药的纳米复合胶束溶于pbs缓冲液中,将两种溶液混合,室温反应,反应结束后,反应液透析、冷冻干燥,即得靶向纳米系统。
作为本发明所述制备方法的优选实施方式,所述步骤(2)中,超声时间为30min,透析袋的截留分子量为1000da,透析时间为24h。
作为本发明所述制备方法的优选实施方式,所述步骤(3)中,pbs缓冲液的ph值为7.4,室温搅拌时间为0.5h,室温反应时间为4h,透析袋的截留分子量为1000d,t7多肽、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、n-羟基琥珀酰亚胺的质量比为40:1:2。
第三方面,本发明提供了上述靶向纳米系统在制备治疗肺癌的药物中的应用。
与现有技术相比,本发明的有益效果为:
(1)本发明提出了一种用于肺癌治疗的具有生物响应性的纳米递送载体及其制备方法,该纳米递送载体材料体内外具有低细胞毒性,能够负载多种化疗药物,具有特异性地到达病变器官或组织的靶向分子,减少化疗药物对正常组织的伤害,提高药物的利用度,改善肺癌的治疗效果,克服了现有化疗药物用于治疗肺癌的一些问题,解决了单一化疗药物治疗的效果不佳;同时在给药过程中易于可视化,将有助于了解纳米载体的抗癌机制,提高其抗癌效果。本发明制备操作简单,所需的原材料易得,有望在生物医学材料领域得到广泛的应用。
(2)本发明首先利用4-羟甲基-苯硼酸频哪醇酯(bape)、羧甲基壳聚糖(cmcs),通过酰胺反应合成具有生物响应性和良好生物相容性的羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯(cmcs-bape);其次与转铁蛋白受体有高亲和力的靶向多肽t7(haiyprh)缀合,增加纳米载体在肿瘤部位的富集;此外,负载姜黄素和多西紫杉醇,并在5.0-7.0范围内根据活性氧(ros)水平精确调控药物释放,解决化疗药物对正常组织伤害的问题,联合治疗肺癌。该纳米递送载体可作为一种有效的抗癌药物给药系统,具有很大的临床应用潜力,为未来多药协同抗癌治疗提供方法。
附图说明
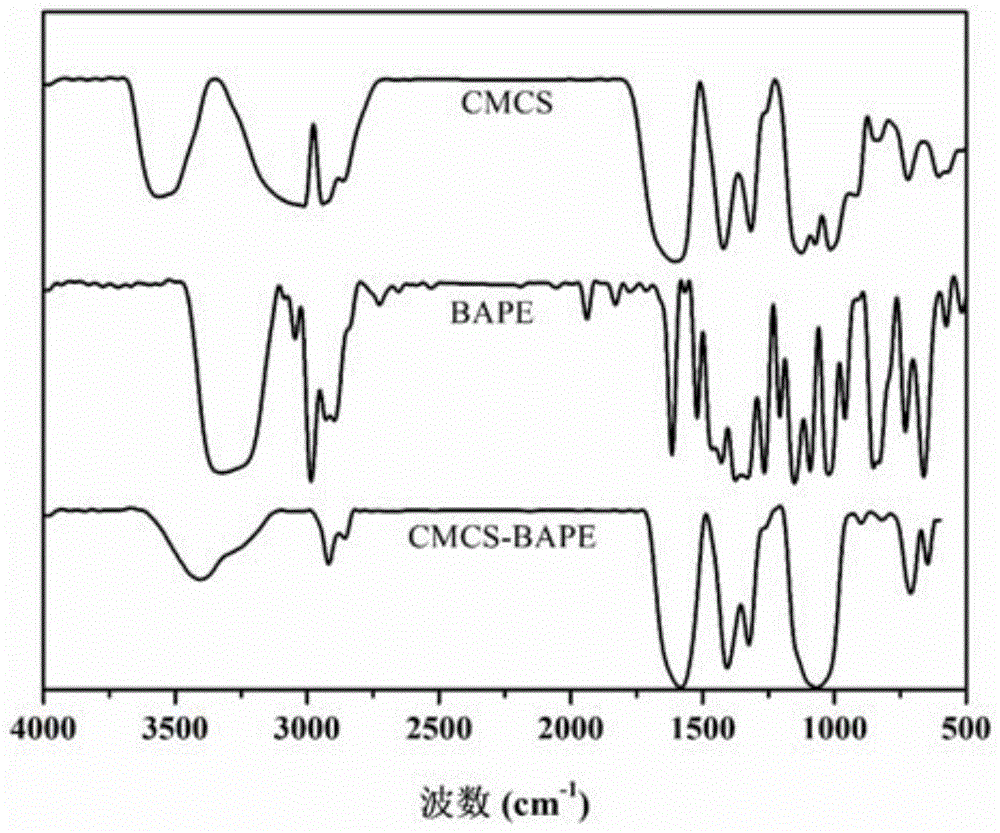
图1为cmcs、bape和cmcs-bape的红外光谱图。
图2为cmcs、cmcs-bape和cmcs-bape-t7的1h-nmr谱图。
图3为cmcs-bape和cmcs-bape-dtx/cur的透射电镜图,其中,a为cmcs-bape的透射电镜图,b为cmcs-bape-dtx/cur的透射电镜图。
图4为cmcs-bape和cmcs-bape-dtx/cur的粒径分布图,其中,a为cmcs-bape的粒径分布图,b为cmcs-bape-dtx/cur的粒径分布图。
图5为效果例1中载药胶束在不同释放介质中ros/ph双敏感体外的释放行为图,其中,a为dtx的释放行为图,b为cur的释放行为图。
图6为效果例2中cmcs-bape-t7对肺癌细胞a549、h1299和h1975活性的影响结果统计图。
图7为效果例3中体外抑制肺癌细胞a549的增殖结果统计图。
具体实施方式
为更好地说明本发明的目的、技术方案和优点,下面将结合具体实施例对本发明作进一步说明。
实施例1cmcs-bape纳米复合物胶束的制备
用分析天平称取0.23g4-羟甲基-苯硼酸频哪醇酯(bape)于烧杯中,加入5ml二氯甲烷使其溶解后,用移液枪滴加0.1mlpbr3。在氮气保护下室温反应1h,然后用旋转蒸发仪缓慢旋干后加入适量乙腈作溶剂,用5%的na2co3溶液调节溶液的ph至碱性待用。称取0.26g羧甲基壳聚糖(cmcs)溶解在适量去离子水中制成溶液,然后将两种溶液混合,在氮气保护条件下避光反应24h后,将混合溶液置于截留分子量为3500da的透析袋中透析三天,再冷冻干燥,即得cmcs-bape纳米胶束。
cmcs、bape和cmcs-bape的红外光谱图如图1所示。红外测试方法为:采用溴化钾压片法,傅立叶红外光谱仪分别测定聚合物cmcs、bape和cmcs-bape纳米胶束在4000-500cm-1范围内的红外光谱。
由图1可以看出,与cmcs相比,cmcs-bape上3440-3300cm-1处游离伯酰胺键、2900-2850cm-1处烷烃主要特征峰、1650-1500cm-1苯环骨架振动峰vc=c以及1250-1000cm-1芳香氢面内弯曲振动峰β=c-h均有所加强,说明苯硼酸频哪醇酯与羧甲基壳聚糖通过酰胺键实现偶联。
实施例2cmcs-bape-t7的制备
取5nmolt7多肽溶解在ph=7.4的pbs缓冲液中,再加入2mgedc,4mgnhs,室温搅拌活化反应0.5h;将实施例1制备的cmcs-bape纳米复合物胶束溶解在pbs中,然后将两种溶液混合,室温搅拌反应4h,用1000da透析袋将过量的edc、nhs透掉,冷冻干燥,即得到具有靶向性的纳米复合胶束,记作cmcs-bape-t7。
cmcs、cmcs-bape和cmcs-bape-t7的1h-nmr谱如图2所示。1h-nmr谱测试方法为:将cmcs、cmcs-bape和cmcs-bape-t7溶于1.0ml体积的d2o,通过核磁共振氢谱仪得到其1h-nmr谱图。
由图2可知,化学位移3.90-4.20ppm质子峰归属为羧甲基壳聚糖的o-ch2-c=o结构,化学位移6.89-7.76ppm归属为苯硼酸频哪醇酯上苯环上和频哪醇酯上的质子峰,说明该疏水端成功实现与羧甲基壳聚糖的偶联作用,化学位移4.3-1.1ppm之间有多个峰为t7肽的一系列质子峰,证明cmcs-bape-t7的成功合成。
实施例3cmcs-bape-dtx/cur的制备
称取50mg实施例1中制得的纳米复合物胶束cmcs-bape溶于纯水中形成cmcs-bape溶液,将10mg多烯紫杉醇(dtx)和20mg姜黄素(cur)分别溶于dmso中,形成多烯紫杉醇溶液、姜黄素溶液;超声条件下,将多烯紫杉醇溶液、姜黄素溶液滴加进入cmcs-bape溶液中,超声0.5h使其形成混合均匀的有机相,再在超声条件下将有机相逐滴滴加到30ml去离子水中,用探头超声30min形成乳液。继续将乳液收集在1000da的透析袋中透析24h后冷冻干燥,即得载双药的纳米复合胶束。记作cmcs-bape-dtx/cur。
透射电镜图如图3所示,其中,a为cmcs-bape的透射电镜图,b为cmcs-bape-dtx/cur的透射电镜图。透射电镜图的测试方法为:冷冻干燥后的胶束纳米粒子重新分散在水中,配置成0.5mgml-1的胶束溶液,将溶液滴在铜网的碳支持膜上,空气中自然干燥后,置于高分辨透射电镜中观察纳米粒子的总体形貌和粒径分布。
由图3可以看出,cmcs的形貌呈规则的圆球形,负载cur和dtx后,cmcs-bape纳米球略微变大,且在cmcs-bape纳米球中有许多小颗粒,我们认为这是由于姜黄素和多西紫杉醇的成功负载所引起的。
通过动态光散射对cmcs-bape和cmcs-bape-dtx/cur的粒径进行表征,如图4所示,其中,a为cmcs-bape的粒径分布图,b为cmcs-bape-dtx/cur的粒径分布图。粒径分布的测试方法为:用动态光散射(dls)测量聚合物胶束的粒径分布,实验中采用马尔文公司的zetasizernano-zs90的粒径仪和电位仪测定纳米颗粒的粒径、粒径分布,测试温度为25℃,每个样品测量三次,取平均值。
由图4可知,cmcs-bape的粒径大小约为300nm,粒径分布均匀。负载药物后,纳米载体的粒径增加,约为500nm,粒径分布均匀。载药后纳米载体的粒径变大是由于药物颗粒存在,该趋势与透射电镜结果相符。
实施例4t7-cmcs-bape-dtx/cur的制备
取0.08gt7多肽溶解在ph=7.4的pbs缓冲液中,再加入2mgedc,4mgnhs,室温搅拌活化反应0.5h;将实施例3中制备得到的载双药的纳米胶束粉末溶解在pbs缓冲液中,然后将两种溶液混合,室温搅拌反应4h,用1000da透析袋将过量的edc、nhs透掉,冷冻干燥,即得到具有靶向性的双载药纳米复合胶束,记作t7-cmcs-bape-dtx/cur。
实施例5
一种靶向纳米系统,包含如下重量份的组分:羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯10mg、多烯紫杉醇20mg、姜黄素1mg、t7多肽50mg。
本实施例靶向纳米系统的制备方法为:
(1)将实施例1中制得的纳米复合物胶束cmcs-bape溶于纯水中形成cmcs-bape溶液,将多烯紫杉醇和姜黄素分别溶于dmso中,形成多烯紫杉醇溶液、姜黄素溶液;超声条件下,将多烯紫杉醇溶液、姜黄素溶液滴加进入cmcs-bape溶液中,超声0.5h使其形成混合均匀的有机相,再在超声条件下将有机相逐滴滴加到去离子水中,用探头超声30min形成乳液。继续将乳液收集在1000da的透析袋中透析24h后冷冻干燥,即得载双药的纳米复合胶束;
(2)将t7多肽溶解在ph=7.4的pbs缓冲液中,再加入edc、nhs,室温搅拌活化反应0.5h;将步骤(1)制备得到的载双药的纳米胶束粉末溶解在pbs缓冲液中,然后将两种溶液混合,室温搅拌反应4h,用1000da透析袋将过量的edc、nhs透掉,冷冻干燥,即得到具有靶向性的双载药纳米复合胶束。
实施例6
一种靶向纳米系统,包含如下重量份的组分:羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯100mg、多烯紫杉醇1mg、姜黄素40mg、t7多肽100mg。
本实施例靶向纳米系统的制备方法同实施例5。
效果例1ros/ph双敏感体外释放行为考察
首先取1ml6mg/ml实施例3制备得到的cmcs-bape-dtx/cur放入预处理过的透析袋(截留分子量=1000da)中,然后将透析袋置于15ml离心管中,以3ml不同ph的pbs(ph=5.7和ph=7.4,含有10%吐温80)、不同浓度的h2o2作为释放介质;37℃恒温振荡器中振荡,在不同的时间点(0.5、1、3、5、8、24、48和72h)吸取1ml透析液,并补充等量恒温的相同释放介质。通过紫外分光光度计和hplc测得相对应的cur和dtx的浓度,并计算相应时间点对应的累积释放百分率。
释放百分比(%)=m1/m0×100%;
其中m1是释放药物的质量,m0是纳米系统中的总药物。
通过紫外光谱和hplc测得cur和dtx的载药率分别为6.8%和10.91%。载药胶束在不同释放介质中ros/ph双敏感体外的释放行为图如图5所示,其中,a为dtx的释放行为图,b为cur的释放行为图。由图5可知,在ph=5.3时,cmcs-bape-dtx/cur“突释”明显,在介质中加入一定量的h2o2条件下,载药胶束释放药物出现了更明显的“突释”现象,说明该载体材料具有一定的ros和ph敏感性。在肿瘤微环境中,存在过量的ros并且由于肿瘤组织代谢旺盛而偏酸性,这一特性有利于载药胶束实现在肿瘤部位快速释放药物,从而增加抗肿瘤效果。且这一过程灵敏性很高,这有利于实现在肿瘤部位的ros快速响应。
效果例2体外细胞毒性
利用cck-8法检测细胞活性的方法来评价实施例2制备得到的cmcs-bape-t7对人肺腺癌细胞(a549)、肺腺癌细胞(h1299)和人非小细胞肺腺癌细胞(h1975)的细胞毒性。具体操作步骤如下:首先将细胞以5000个/孔的密度接种于96孔板中,然后将其置于二氧化碳培养箱中培养贴壁过夜。随后,吸出原有的培养基,换上新鲜的含有不同浓度的cmcs-bape-t7的完全培养基,所选的cmcs-bape-t7的浓度范围为0-500μg/ml,每个浓度有5个平行。然后在培养箱中分别培养24h、48h和72h。然后,小心移除培养液,每孔加入培养基量50ul的cck8溶液,并设定阴性对照(空白培养基),在细胞培养箱中培养30-60min。并在酶标仪450nm波长下检测吸光度值(od值),记录并计算数据。细胞存活率(%)=(实验组吸光度-空白组吸光度)/(阴性对照组吸光度-空白组吸光度)×100%。
cmcs-bape-t7对肺癌细胞a549、h1299和h1975活性的影响结果统计图如图6所示,cmcs-bape-t7在各浓度条件下,细胞的存活率都很高,均未对a549细胞产生任何细胞毒性,当浓度达到500μg/ml时,细胞存活率也达到90%,因此,我们认为cmcs-bape-t7材料具有优良的生物相容性,能够用作安全的药物载体用于肿瘤的治疗研究。
效果例3体外抑制细胞增殖检测
为了进一步探索治疗肺癌的最佳配方,我们进行了cck-8实验,通过mtt分析评价不同浓度的多西紫杉醇和姜黄素的协同抑制肺癌作用。选用人肺腺癌细胞(a549)细胞,在96孔板中以5000个/孔的浓度培养条件良好的细胞,24h后按计划制备4组(dtx:cur配比分别为1:1,1:2,1:4,1:6),不同的组采用不同的处理方法。处理3天后,丢弃残存培养基,用cck-8试剂替换,37℃孵育1h。然后,用微孔板阅读器对结果进行测量,最后计算抑制率。
体外抑制肺癌细胞a549的增殖结果如图7所示,与其他组相比,dtx:cur配比为1:2时,t7-cmcs-bape-dtx/cur组的细胞存活率最低,证明靶向和联合治疗能够高效的抑制肺癌细胞的增长。即靶向系统包含如下重量的组分:羧甲基壳聚糖-4-羟甲基-苯硼酸频哪醇酯50份、多烯紫杉醇10份、姜黄素20份、t7多肽80份时,抑制肺癌细胞增长的效果最佳。
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
- 还没有人留言评论。精彩留言会获得点赞!