自组装生物相容性成像颗粒,其合成及其在成像技术中的用途的制作方法
本发明涉及生物相容性颗粒,其包含包埋在聚儿茶酚胺或聚血清素基质内的氧化铁纳米颗粒,所述颗粒的悬浮液,用于制备所述颗粒的悬浮液的方法,包含所述颗粒的缀合物以及所述颗粒和所述缀合物在成像技术中的用途。
背景技术:
1、磁共振成像(mri)是一种很有前景的分子成像方式,但仍然受到低灵敏度的限制(lohrke,j.et al.,adv.ther.,2016,33,1-28)。在人类组织中分子成像的相关靶的浓度通常为约10-9-10-12m,而mri检测到的临床上批准的钆螯合物浓度超过10-6m。因此,有必要采取旨在将许多造影剂产生的原子与分子靶标结合的放大策略。迄今为止,纳米尺寸的造影剂,诸如直径为10-50nm的超小颗粒氧化铁(uspio)已成为分子mri研究的主要焦点(laurent,s.et al.,chem.rev.,2008,108,2064-2110)。uspio可以与靶向部分(诸如肽或抗体)缀合,且在人类中具有良好的安全特性。然而,低灵敏度(由于每个颗粒的铁有效负载量小)、低特异性(由于通过渗透的内皮屏障被动外渗)和给药与成像之间的较长延迟(静脉内注射后长达24小时)阻碍了uspio作为靶向分子成像剂的用途(gauberti,m.et al.,front.cell.neurosci.,2014,8,389)。
2、最近,直径接近1μm的氧化铁(mpio)微粒已被用作用于分子mri的新型造影剂(mcateer,m.a.et al.,nat.med.,2007,13,1253-1258)。由于铁含量较高,mpio显示出比uspio更高的灵敏度(gauberti,m.et al.,theranostics,2018,8,1195-1212)。靶向mpio用于分子mri的适用性已在几种实验模型中得到证实,包括心血管(von zur muhlen,c.etal.,circulation,2008,118,258-267;von zur muhlen,c.et al.,j.clin.invest.,2008,118,1198-1207)和神经血管疾病(quenault,a.et al.,brain,2017,140,146-157),自身免疫性疾病(fournier,a.p.et al.,proc.natl.acad.sci.u.s.a.,2017,114,6116-6121;fournier,a.p.et al.,sci.transl.med.,2020,12,eaaz4047)和癌症(serres,s.et al.,proc.natl.acad.sci.u.s.a.,2012,109,6674-6679)。值得注意的是,mpio会被网状内皮系统从循环中快速消除,从而限制了其到达其靶标的能力(belliere,j.et al.,theranostics,2015,5,1187-1202)。因此,mpio的结构和涂层受到严格的限制,以使其积聚到足以被mri检测的高浓度。不幸的是,临床前研究中使用的mpio由聚苯乙烯基质制成,且在临床上不相容(gauberti,m.et al.,front.cell.neurosci.,2014,8,389)。uspio与肽酶可降解键的共价组装被描述为mpio的替代物,但所得产物对分子成像缺乏灵敏度(perez-balderas,f.et al.,nature communications,2017,8,14254)。
3、因此,目前仍然没有一种造影剂,将当前可获得的mpio的高灵敏度与uspio的生物相容性和生物可降解性相结合。
4、发明简述
5、发明人现已成功地开发了由uspio的自组装亚微米团簇制成的新型造影剂,其使用聚儿茶酚胺或聚血清素,特别是聚多巴胺(pda)作为包埋基质。仅使用三种试剂(氯化铁、聚儿茶酚胺或聚血清素,以及氨),产生平均直径为250nm-900nm的uspio和聚儿茶酚胺或聚血清素的亚微米团簇。由于生物相容的,亲水的和反应性的聚儿茶酚胺或聚血清素的包被(lee,h.et al.,science,2007,318,426-430;wu,d.et al.,chem.soc.rev.,2021,50,4432-4483),uspio和聚儿茶酚胺或聚血清素的簇可以用靶向部分,诸如单克隆抗体(免疫-mri),有效地官能化。这种新平台可用于体内成像方法,特别是脑、肾和肠粘膜中炎症的超灵敏分子成像。
6、因此,本发明涉及流体动力学直径为200-2000nm的颗粒,所述颗粒包含包埋在聚合物基质内的氧化铁纳米颗粒,所述聚合物基质选自聚儿茶酚胺或聚血清素。
7、本发明还涉及所述颗粒的悬浮液。
8、在另一方面,本发明提供用于制备本发明的颗粒的悬浮液的方法,其包括以下步骤:
9、a)制备氧化铁纳米颗粒的悬浮液;
10、b)用儿茶酚胺或血清素包被所述氧化铁纳米颗粒;
11、c)在所述氧化铁纳米颗粒的存在下,聚合所述儿茶酚胺或血清素;
12、d)终止所述聚合;以及
13、e)回收颗粒的悬浮液。
14、本发明还涉及包含本发明的颗粒或本发明的颗粒的悬浮液以及包含游离胺或硫醇基的分子(特别是单克隆抗体)的缀合物。
15、本发明还涉及本发明的颗粒,本发明的颗粒的悬浮液或本发明的缀合物,其用于体内成像方法。
16、本发明还涉及本发明的颗粒,本发明的颗粒的悬浮液或本发明的缀合物在成像技术中作为造影剂或作为示踪剂的用途。
17、发明详述
18、如上详述,本发明涉及流体动力学直径为200-2000nm,优选250-1250nm,更优选300-1000nm,还更优选500-1000nm的颗粒,所述颗粒包含包埋在聚合物基质内的氧化铁纳米颗粒,优选超小颗粒,所述聚合物基质选自聚儿茶酚胺或聚血清素。
19、如本文所用,表述“包含于……和……之间”应理解为包括所述范围的边界。如本文所用,相对于纳米颗粒和聚合物基质的表面的术语“包埋”是指纳米颗粒至少部分地延伸到表面,使得聚合物与纳米颗粒接触程度大于如果纳米颗粒简单地放置在聚合物基质的表面上所能达到的程度。
20、在本发明的上下文中,术语“流体动力学直径”是指以与被测量的颗粒相同的速度扩散的假想硬球的直径。其反映了溶液中颗粒的尺寸,并包括对相关颗粒进行的包被或表面改性。
21、本发明颗粒的流体动力学直径可根据本领域技术人员已知的任何方法测定。特别地,本发明的颗粒的流体动力学直径可以通过动态光散射(dls)测定,使用例如配备有633nm激光器的仪(malvern instruments,worcestershire,uk),在173°的固定散射角下,池(cell)温保持恒定在25℃。用于该测量的颗粒以20μg-200μg铁/ml水的浓度置于水中的悬浮液中。其他已知的方法是颗粒跟踪分析(pta)或其变体纳米颗粒跟踪分析(pta)。
22、例如,本发明颗粒的流体动力学直径可包含于200-2000nm、200-1250nm、200-1000nm、200-900nm、200-800nm、200-700nm、250-2000nm、250-1250nm、250-1000nm、250-900nm、250-800nm、250-700nm、300-2000nm、300-1250nm、300-1000nm、300-900nm、300-800nm、300-700nm、400-2000nm、400-1250nm、400-1000nm、400-900nm、400-800nm、400-700nm、500-2000nm、500-1250nm、500-1000nm、500-900nm、500-800nm或500-700nm。
23、掺入本发明颗粒中的氧化铁纳米颗粒,优选超小颗粒,可选自式fe2o3的磁铁矿,式fe3o4的磁铁矿或fe2o3和fe3o4的混合物。这些不同类型的氧化铁都是超顺磁性的和生物相容的,使得它们特别地用作磁共振成像(mri)中的造影剂或用作磁性颗粒成像(mpi)中的示踪剂。
24、如本文所用,术语“纳米颗粒”是指粒度小于1000nm,特别地为1-500nm,更特别地为1-300nm的材料。
25、如本文所用,术语“超小颗粒”是指粒度小于50nm,特别地为1-50nm,更特别地为1-30nm的材料。
26、特别地,掺入本发明颗粒中的氧化铁纳米颗粒,优选超小颗粒的直径为1-50nm,更特别地为1-30nm。
27、例如,掺入本发明颗粒中的氧化铁的超小颗粒的直径可为1-45nm、1-40nm、1-35nm、1-30nm、2-50nm、2-45nm、2-40nm、2-35nm、2-30nm、3-50nm、3-45nm、3-40nm、3-35nm、3-30nm、5-50nm、5-45nm、5-40nm、5-35nm、5-30nm、10-50nm、10-45nm、10-40nm、1-35nm或10-30nm。
28、本发明颗粒的聚合物基质选自聚儿茶酚胺或聚血清素。
29、特别地,本发明颗粒中的生物可降解聚合物基质可选自聚多巴胺(pda)、聚去甲肾上腺素(pne)、聚肾上腺素(pep)和聚血清素,更特别地选自聚多巴胺(pda)和聚去甲肾上腺素(pne)。更特别地,本发明颗粒中的生物可降解聚合物基质是聚多巴胺(pda)。
30、除它们的生物可降解性外,这些不同类型的聚合物对于本发明颗粒的合成及其应用具有许多优点。特别地,多种配体可以通过michael加成或schiff碱反应以高密度与聚儿茶酚胺或聚血清素缀合(lee,h.et al.,adv mater.2009,21,431-434)。需要在uspio簇的表面上缀合大量靶向部分的能力以最大化与靶标的结合并实现高灵敏度。第三,聚儿茶酚胺或聚血清素在生理ph下是亲水性的和带负电荷的,为包覆颗粒提供负ζ-电势并防止它们在溶液中积聚。它们与氧化铁形成强键,使得即使在超声处理下获得稳定的颗粒,允许分散积聚的颗粒而不破坏簇或分离缀合配体。
31、在一个实施方案中,相对于颗粒的总重量,本发明颗粒中的氧化铁浓度可为50重量%-95重量%。
32、本发明颗粒中的铁浓度可通过本领域技术人员已知的任何合适的方法测定。特别地,本发明颗粒中的铁浓度可通过菲洛嗪(ferrozine)方法或通过质谱测定。
33、本发明的颗粒可通过其多分散指数来表征。在一个实施方案中,本发明颗粒的多分散指数低于0.3,特别地,本发明颗粒的多分散指数为0.01-0.2。
34、本发明颗粒的多分散指数可以通过本领域技术人员已知的任何合适的方法测定。特别地,本发明的颗粒的多分散指数可通过动态光散射(dls)通过使用例如与用于流体动力学直径测量的相同的装置和测量条件来确定。
35、例如,本发明颗粒的多分散指数可以为0.01-0.3、0.02-0.3、0.03-0.3、0.05-0.3、0.07-0.3、0.1-0.3、0.01-0.2、0.02-0.2、0.03-0.2、0.05-0.2、0.07-0.2或0.1-0.2。
36、本发明的颗粒的特征还在于它们的ζ-电势。在一个实施方案中,本发明颗粒的ζ-电势为-50至-20mv,特别是-45至-25mv,更特别是-42至-37mv。
37、ζ-电势可通过本领域技术人员已知的任何合适的方法测定。特别地,本发明颗粒的ζ-电势可通过电泳光散射(els)测定,其中对悬浮在1mm氯化钠溶液中的颗粒进行测量。
38、在本发明的上下文中,术语“ζ-电势”是指在界面处的电势,其将可流动流体与仍附着于颗粒表面的流体分离。
39、本发明的另一个目的是根据本发明的颗粒的悬浮液。这种颗粒的悬浮液含有溶剂,该溶剂可选自水性溶液,例如水,或盐水溶液,或甘油,或甘露醇,其中悬浮本发明所述的颗粒。
40、换言之,根据本发明的颗粒的悬浮液包含悬浮在溶剂中的根据本发明的颗粒,所述溶剂选自水性溶液,例如水、盐水溶液、甘油溶液和甘露醇溶液。特别地,根据本发明的颗粒的悬浮液包含悬浮在水溶液或盐水溶液中的根据本发明的颗粒。更特别地,根据本发明的颗粒的悬浮液包含悬浮在水溶液,优选水,更优选蒸馏水中的根据本发明的颗粒。
41、根据本发明的颗粒的悬浮液中颗粒的平均流体动力学直径为250-900nm。
42、例如,根据本发明的颗粒的悬浮液中的颗粒的流体动力学直径可为200-2000nm、200-1250nm、200-1000nm、200-900nm、200-800nm、200-700nm、250-2000nm、250-1250nm、250-1000nm、250-900nm、250-800nm、250-700nm、300-2000nm、300-1250nm、300-1000nm、300-900nm、300-800nm、300-700nm、400-2000nm、400-1250nm、400-1000nm、400-900nm、400-800nm、400-700nm、500-2000nm、500-1250nm、500-1000nm、500-900nm、500-800nm或500-700nm。
43、有利地,可以控制根据本发明的颗粒的悬浮液中的颗粒的平均流体动力学直径。
44、在一个实施方案中,本发明颗粒的悬浮液中颗粒的平均流体动力学直径为250-400nm,特别为250-350nm,更特别地,本发明颗粒的平均流体动力学直径为约300nm。
45、在另一个实施方案中,本发明颗粒的悬浮液中颗粒的平均流体动力学直径为400-600nm,特别是450-550nm,更特别地,本发明颗粒的平均流体动力学直径为约500nm。
46、在另一个实施方案中,本发明颗粒的悬浮液中颗粒的平均流体动力学直径为600-900nm,特别是650-750nm,更特别地,本发明颗粒的平均流体动力学直径为约700nm。
47、本发明的另一个目的是用于制备本发明的颗粒的悬浮液的方法,其包括以下步骤:
48、a)制备氧化铁的纳米颗粒,优选超小颗粒的悬浮液,特别是具有1-50nm,更特别为1-30nm的直径;
49、b)用儿茶酚胺或血清素,特别地用儿茶酚胺,更特别地用多巴胺包被氧化铁的纳米颗粒,优选超小颗粒;
50、c)在氧化铁的纳米颗粒,优选超小颗粒的存在下,聚合儿茶酚胺或血清素;
51、d)终止所述聚合;
52、e)回收颗粒的悬浮液。
53、本发明方法的步骤a)包括制备氧化铁的纳米颗粒,优选超小颗粒的悬浮液,特别是在水中,更特别是在蒸馏水中的悬浮液。特别地,氧化铁的纳米颗粒,优选超小颗粒可选自式fe2o3的磁铁矿,式fe3o4的磁铁矿或fe2o3和fe3o4的混合物。更特别地,氧化铁的纳米颗粒,优选超小颗粒是fe3o4。
54、本发明方法的步骤a)可以根据本领域技术人员已知的任何合适的方法进行,包括例如共沉淀、溶剂热合成、热分解、多元醇法、声化学反应和溶胶-凝胶反应。特别地,本发明方法的步骤a)可以通过在碱性缓冲液中共沉淀法进行。典型地,共沉淀方法通过在碱性缓冲液中混合fecl3和fecl2(优选以2:1的摩尔比),并逐步加入氨溶液,所述氨溶液优选浓度为10%-15%(w/v),更优选浓度为13%(w/v),特别地以0.1-0.3ml/min,更特别地0.15-0.25ml/min,还更特别是以0.2ml/min的速率,直到氧化铁沉淀来进行。任选地,洗涤沉淀,优选用蒸馏水洗涤,并且再悬浮,优选在蒸馏水中。
55、本发明方法的步骤b)包括用儿茶酚胺或血清素包被铁氧化物纳米颗粒。典型地,将从步骤a)获得的氧化铁纳米颗粒的悬浮液与儿茶酚胺或血清素的溶液(特别是儿茶酚胺的溶液,更特别是多巴胺的溶液)混合,优选铁/儿茶酚胺或血清素的重量比为0.5-3.0,特别地为0.5-2.5,更特别地为1.0-2.0,还更特别地为1.0-1.5,甚至更特别地,铁/儿茶酚胺或血清素的质量比为1.2。
56、在将从步骤a)获得的氧化铁纳米颗粒的悬浮液与儿茶酚胺或血清素的溶液混合之后,本发明方法的步骤b)可包括使所得混合物均化的步骤,特别是通过超声处理,例如使用up200st超声波仪(hielscher)在70%振幅和26khz下,特别地持续1-30min,更特别地10-20min,在0℃-100℃,优选40℃-100℃的温度下。
57、本发明方法的步骤b)可进一步包括离心步骤,特别是在3000g下。
58、本发明方法的步骤c)包括聚合儿茶酚胺或血清素,特别是儿茶酚胺,更特别是多巴胺,其中包被氧化铁纳米颗粒。
59、聚合步骤可通过本领域技术人员已知的任何合适的方法进行。特别地,聚合步骤可如下进行:将碱溶液,优选氨和氧,优选来自环境空气的氧加入到在步骤b)中获得的包被有儿茶酚胺或血清素的氧化铁的超小颗粒中,并将所得混合物搅拌15min-6h,优选30min-90min,更优选60min。这使得具有聚儿茶酚胺或聚血清素的氧化铁纳米颗粒自组装。
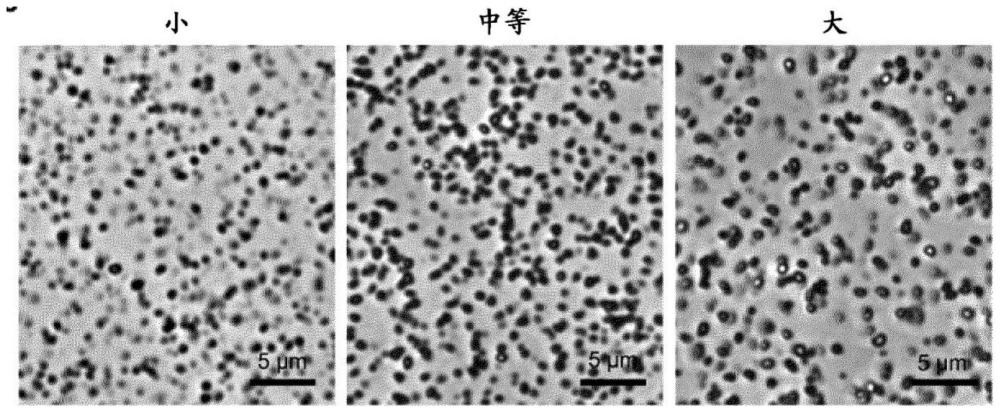
60、在步骤c)期间添加的氨的量可以控制本发明的颗粒的尺寸。
61、在一个实施方案中,在步骤c)期间加入的氨相对于1重量份铁为2.17-3.25重量份。典型地,对于120mg铁,加入2.0ml-3.0ml的13%(w/v)氨溶液。
62、根据该实施方案,颗粒的平均流体动力学直径为250-400nm,特别是250-350nm,更特别地,颗粒的平均流体动力学直径为约300nm。
63、在另一个实施方案中,在步骤c)期间加入的氨的量相对于1重量份铁为0.33-2.17重量份。典型地,对于120mg铁,加入0.3ml-2.0ml的13%(w/v)氨溶液。
64、根据该实施方案,颗粒的平均流体动力学直径为400-600nm,特别是450-550nm,更特别地,颗粒的平均流体动力学直径为约500nm。
65、在另一个实施方案中,在步骤c)期间加入的氨的量相对于1重量份铁为0.05-0.33重量份。典型地,对于120mg铁,加入0.05ml-0.3ml的13%(w/v)氨溶液。
66、根据该实施方案,颗粒的平均流体动力学直径为600-750nm,特别是650-750nm,更特别地,颗粒的平均流体动力学直径为约700nm。
67、本发明方法的步骤d)包括终止步骤c)的聚合。
68、终止步骤可通过本领域技术人员已知的任何合适的方法进行,例如,加入酸以在反应混合物中获得酸性ph,加入聚合抑制剂或替换反应介质。特别地,终止步骤通过替换反应介质来进行。典型地,将颗粒从其中进行聚合步骤c)的碱溶液中分离,特别是使用分离磁体或离心步骤,更特别是离心步骤,从而可以将颗粒保持在底层中且碱溶液作为上清液。然后,除去上清液并替换为洗涤溶液,特别是水,更特别是蒸馏水。该操作可进行多次以确保来自步骤c)的碱溶液被完全除去并被洗涤溶液替代。
69、本发明方法的步骤e)包括回收本发明颗粒的悬浮液。然后,可将这些颗粒在约3-10℃的低温下储存在水或盐水溶液中。
70、在将其注射至患者前,将本发明的颗粒的悬浮液在搅拌下保持在0-37℃,特别是4℃的温度下。
71、本发明的另一个目的是通过根据本发明的方法获得的颗粒或颗粒的悬浮液。
72、本发明的另一个目的是在通过除去步骤e)后获得的悬浮液的溶剂而分离所述颗粒的其他步骤之后,通过根据本发明的方法获得的颗粒。
73、本发明还涉及包含本发明颗粒或本发明的颗粒的悬浮液以及包含游离胺或硫醇基团分子的缀合物。
74、特别地,包含游离胺或硫醇基的分子选自蛋白质、肽、纳米抗体、单克隆抗体或包含放射性标记的金属的分子。优选地,包含游离胺或硫醇基的分子是单克隆抗体。
75、在一个实施方案中,所述缀合物包含本发明的颗粒或通过本发明的方法获得的颗粒以及至少包含游离胺或硫醇基团的分子。特别地,至少包含游离胺或硫醇基团的分子或蛋白质可以是肽、纳米抗体、单克隆抗体、包含放射性标记的金属的分子或小分子,诸如n-乙酰基半胱氨酸。更特别地,至少包含游离胺或硫醇基团的分子或蛋白质可以是肽、纳米抗体、单克隆抗体、包含放射性标记的金属的分子或n-乙酰基半胱氨酸。甚至更特别地,至少包含游离胺或硫醇基团的分子或蛋白质可以是肽、纳米抗体或单克隆抗体。优选地,至少包含游离胺或硫醇基团的分子或蛋白质可以是单克隆抗体。
76、在一个实施方案中,至少包含游离胺或硫醇基团的分子可以是用至少包含游离胺或硫醇基团的连接子修饰的分子。换言之,至少包含游离胺或硫醇基团的分子是其中游离胺或硫醇基团由连接子部分保持的分子。
77、在本发明的上下文中,术语“连接子(linker)”或“连接子部分”是指用于将分子连接至本发明的颗粒或通过本发明的方法获得的颗粒的接头。
78、在本发明的上下文中,术语“缀合物”是指由连接在一起的两个或更多个分子组成的分子。本发明的缀合物典型地由根据本发明的颗粒与蛋白质、肽、纳米抗体或单克隆抗体连接组成。本发明的颗粒还可以与放射性标记的金属,诸如铜64或镓68连接,特别是在用于正电子发射断层扫描(pet)成像技术的情况下。
79、特别地,所述单克隆抗体可选自免疫球蛋白g(igg)、血管细胞粘附分子1(vcam-1)、细胞间粘附分子1(icam-1)、p-选择素、e-选择素或粘膜地址素细胞粘附分子1(madcam-1)。更特别地,所述单克隆抗体可选自血管细胞粘附分子1(vcam-1)、细胞间粘附分子1(icam-1)或粘膜地址素细胞粘附分子1(madcam-1)。更特别地,所述单克隆抗体可以是血管细胞粘附分子1(vcam-1)或粘膜地址素细胞粘附分子1(madcam-1)。
80、在一个实施方案中,所述单克隆抗体可选自血管细胞粘附分子1(vcam-1)、细胞间粘附分子1(icam-1)、p-选择素、e-选择素或粘膜地址素细胞粘附分子1(madcam-1)。更特别地,所述单克隆抗体可选自血管细胞粘附分子1(vcam-1)、细胞间粘附分子1(icam-1)或粘膜地址素细胞粘附分子1(madcam-1)。更特别地,所述单克隆抗体可以是血管细胞粘附分子1(vcam-1)或粘膜地址素细胞粘附分子1(madcam-1)。
81、特别地,至少包含游离胺或硫醇基团的分子可以是纤维蛋白溶解剂。在一个实施方案中,所述纤维蛋白溶解剂通过具有至少一种游离胺或硫醇基团的连接子部分与本发明的颗粒或通过本发明的方法获得的颗粒结合。
82、特别地,至少包含游离胺或硫醇基团的分子是可以是组织纤溶酶原激活物或其片段的蛋白质,例如重组组织纤溶酶原激活物(rtpa),诸如阿替普酶(alteplase)、瑞替普酶(reteplase)或替奈普酶(tenecteplase)。在一个实施方案中,可以是组织纤溶酶原激活物或其片段的蛋白质通过至少具有游离胺或硫醇基团的连接子部分与本发明的颗粒或通过本发明的方法获得的颗粒结合。
83、相对于缀合物的总重量,缀合物中根据本发明颗粒的量可为50重量%-99重量%,特别是65重量%-95重量%,更特别是80重量%-95重量%,还更特别是85重量%-95重量%。
84、在制备后,将本发明的缀合物在搅拌下保持在0-37℃,特别是4℃的温度下,直至其注射至患者。
85、为用于体内成像方法,本发明的颗粒或通过本发明的方法获得的颗粒或本发明的缀合物必须在成像步骤之前施用于患者。本发明的颗粒或本发明的缀合物可作为制剂以有效量通过任何可接受的施用方式施用,优选通过静脉内、动脉内或口服途径。
86、因此,本发明的另一个目的是本发明的颗粒,本发明的颗粒的悬浮液,通过本发明的方法获得的颗粒或颗粒的悬浮液或本发明的缀合物,其用于体内成像方法中。
87、本发明的颗粒,本发明的颗粒的悬浮液,通过本发明的方法获得的颗粒或颗粒的悬浮液或本发明的缀合物在成像领域中具有多种应用。
88、特别地,本发明的颗粒,本发明的颗粒的悬浮液,通过本发明的方法获得的颗粒或颗粒的悬浮液或本发明的缀合物可用于成像技术,诸如磁共振成像(mri)、磁性颗粒成像(mpi)、光声成像或正电子发射断层扫描(pet)。更特别地,它们可用于磁共振成像(mri)。
89、在光声成像的情况下,本发明颗粒的吸收光谱特别适于获得良好的可视化。实际上,例如聚多巴胺主要在近红外(波长约700nm)吸收,且与主要在远红外(波长约900nm)吸收的氧合血红蛋白有很好的区别。
90、在正电子发射断层摄影术(pet)的情况下,本发明的颗粒或通过本发明的方法获得的颗粒可在缀合和/或放射性标记步骤之后使用。然后,可使用放射性标记的金属,诸如铜64或镓68。
91、所有这些技术都可用于体内诊断。本发明颗粒的作用方式使它们适用于所有类型的成像。特别地,本发明的缀合物可用于脑、心脏、肺、肾和肠粘膜中炎症的分子成像,更特别地用于脑、肾和肠粘膜中炎症的分子成像。
92、本发明还涉及使用本发明的颗粒,本发明的颗粒的悬浮液,通过本发明的方法获得的颗粒或颗粒的悬浮液或本发明的缀合物的体内诊断方法。
93、本发明还提供了包含本发明的颗粒,本发明的颗粒的悬浮液,通过本发明的方法获得的颗粒或颗粒的悬浮液或本发明的缀合物的组合物。所述组合物还可包含至少一种药学上可接受的载体、稀释剂、赋形剂和/或佐剂。
94、此类组合物可含有本发明的颗粒,本发明的颗粒的悬浮液,通过本发明的方法获得的颗粒或颗粒的悬浮液,或在溶剂中的本发明的缀合物,例如0.3m甘露醇的溶液。
95、在其注射前,本发明的颗粒可悬浮在与向人类患者注射相容的任何生理介质中。这种生理介质的实例是甘露醇或甘油,特别是甘露醇溶液或甘油溶液,更特别是0.3m甘露醇溶液。
96、本发明的另一个目的是一种成像方法,其中例如通过注射施用于患者含有本发明颗粒的组合物,本发明颗粒的悬浮液,通过本发明方法获得的颗粒或颗粒的悬浮液或本发明的缀合物,且包括成像步骤。
97、本发明的另一个目的是本发明的颗粒,本发明的颗粒的悬浮液,通过本发明的方法获得的颗粒或颗粒的悬浮液或本发明的缀合物在成像技术中作为造影剂或作为示踪剂的用途。
98、定义
99、下面的定义和解释是针对整个申请中,包括说明书和权利要求书,使用的术语。
100、除非另外指明,当描述本发明的颗粒时,所用术语应根据以下定义来解释。
101、如本文所用,术语“生物相容的”是指,当与活组织接触放置时,例如体内,不会对活组织造成显著损害的材料。在某些实施方案中,如果材料对细胞无毒,则是“生物相容的”。在某些实施方案中,如果材料在体外添加到细胞中导致小于或等于20%的细胞死亡,和/或它们在体内施用不诱导显著的炎症或其他的这类不良作用,则其为“生物相容的”。
102、如本文所用,术语“生物可降解的”是指当引入细胞中时分解成(例如,通过细胞机制,诸如通过酶促降解,通过水解和/或通过其组合)细胞可再使用或处置而对细胞无显著毒性作用的组分的材料。在某些实施方案中,通过生物可降解材料的分解产生的组分是生物相容的,因此在体内不诱导显著的炎症和/或其他不良作用。在一些实施方案中,生物可降解的聚合物材料分解成它们的组分单体。在一些实施方案中,生物可降解材料(包括例如生物可降解聚合物材料)的分解涉及酯键的水解。可替代地或另外地,在一些实施方案中,生物可降解材料(包括例如生物可降解聚合物材料)的分解涉及氨基甲酸酯键的裂解。在本发明的上下文中,示例性的可生物降解的聚合物包括,例如,聚多巴胺(pda)、聚去甲肾上腺素(pne)、聚肾上腺素(pep)和聚血清素(pst),特别优选聚多巴胺(pda)。
103、如本文所用,相对于纳米颗粒和聚合物基质的表面的术语“包埋”,是指纳米颗粒至少部分地延伸到表面中,使得聚合物与纳米颗粒接触的程度相比如果纳米颗粒简单地放置在聚合物基质表面上所能达到的程度更高。
104、如本文所用,术语“悬浮液”是指包含液体和精细分散的固体材料的材料的非均质混合物。
105、术语“患者”是指等待或接受医疗治疗,或者正在或将是医疗过程的对象的温血动物,更优选人。
106、术语“人”是指两种性别和处于任何发育阶段(即新生儿、婴儿、少年、青少年、成人)的受试者。在一个实施方案中,人是青少年或成人,优选成人。
107、术语“施用(administration)”或其变体(例如“施用(administering)”)是指将活性剂或活性成分,单独或作为药学上可接受的组合物的一部分,提供给具有待治疗的病症、症状或疾病的患者。
108、“药学上可接受的”是指药物组合物的成分彼此相容且对其患者无害。
109、如本文所用,术语“赋形剂”是指与药物组合物或药物中的活性剂或活性成分一起配制的物质。用于治疗用途的可接受的赋形剂在药学领域中是熟知的,且描述于,例如remington's pharmaceutical sciences,21st edition 2011中。赋形剂的选择可根据预期的施用途径和标准药学实践来选择。赋形剂在对其接受者无害的意义上必须是可接受的。至少一种药学上可接受的赋形剂可以是,例如粘合剂、稀释剂、载体、润滑剂、崩解剂、润湿剂、分散剂、悬浮剂等。
110、如本文所用,术语“药物载体”是指用作溶剂或稀释剂的载体或惰性介质,在其中配制和/或施用药物活性剂。药物载体的非限制性实例包括乳膏、凝胶、洗剂、溶液和脂质体。
111、参考以下实施例和附图将更好地理解本发明。这些实施例旨在示例本发明的具体实施方案,而不旨在限制本发明的范围。
技术实现思路
- 还没有人留言评论。精彩留言会获得点赞!