一种磷化钴材料及其制备方法与应用
1.本发明属于电池材料技术领域。更具体地,涉及一种磷化钴材料及其制备方法与应用。
背景技术:
2.磷化钴作为一种过渡金属化合物,具有理论比容量高,化学稳定性好、氧化还原电位较低的特点,被广泛应用于锂离子电池负极领域。磷化钴的物相相态较多,常见的相态主要为cop和co2p。目前报道的制备磷化钴的方法主要有化学气相沉积法、程序升温法、有机金属分解法、溶剂热合成法、氢等离子体还原法、电解熔融盐等。然而上述方法普遍存在一些缺点,如添加不同p/co的量、反应的温度和所负载的载体会影响生成的相的种类,难以可控合成磷化钴的物相,得到的产物为cop相还是co2p相是不确定的,通过对产物进行测定后,才能确定使用该方法得到的产物为哪种相态的材料。除此之外,若要同时制备cop相和co2p相的材料,需要两种制备方法进行制备,操作非常不方便。如中国专利申请公开了一种磷化二钴/碳复合材料,采用的方法是直接将红磷作为磷源与钴源通过水热反应进行制备,虽然制备得到的磷化二钴/碳复合材料具有一定的导电性及循环性,但其产物经过测定才能确定是co2p相,且产物只有co2p相,不能控制cop和co2p两相的生成。可见,现有技术中制备磷化钴材料的方法中,还依旧存在有不能控制cop和co2p两相生成的问题。
技术实现要素:
3.本发明要解决的技术问题是克服现有制备磷化钴材料的方法中,反应过程中不能控制cop和co2p两相生成的缺陷和不足,提供一种能控制cop和co2p两相生成的磷化钴材料的制备方法。
4.本发明的目的是提供一种磷化钴材料。
5.本发明的另一目的是提供一种磷化钴复合材料的制备方法。
6.本发明的另一目的是提供一种磷化钴复合材料。
7.本发明的另一目的是提供一种磷化钴材料和磷化钴复合材料在锂离子电池中的应用。
8.本发明的上述目通过以下技术方案实现:
9.一种磷化钴材料的制备方法,包括如下步骤:
10.将甘油酸钴与0.1~1.5mol/l植酸溶液在有机溶液中反应5~60min,后处理得粉红色固体,在氩氢气体氛围中煅烧0.5~3小时,即得;
11.所述甘油酸钴与0.1~1.5mol/l植酸溶液的添加量比值为:0.1g:(8.5~10.5)ml。
12.本发明创造性采用0.1~1.5mol/l植酸溶液与甘油酸钴进行反应,在反应中,采用0.1~1.5mol/l植酸作为磷源。一方面,植酸为有机酸,反应在室温下进行,且在反应中不会产生剧毒易爆炸的ph3气体,反应绿色安全;另一方面,植酸中氢离子不断电离,电离出来的氢离子与甘油酸钴反应,使甘油酸钴中的co游离出来达到刻蚀中空结构的目的,同时植酸
进入甘油酸钴中空结构内部,在甘油酸钴内部与剩余的钴原子发生螯合作用形成不溶性含磷化合物,通过调控甘油酸钴与植酸的反应时间最终达到控制两相生成的目的。但植酸的浓度过低(小于0.1mol/l),不能达到刻蚀钴盐的作用,只能得到含钴的碳复合材料;植酸的浓度过高(大于1.5mol/l),与甘油酸钴的刻蚀过程太快,无法调控时间得到co2p相。
13.优选地,所述甘油酸钴的制备方法为:依次向钴盐中加入异丙醇和丙三醇,在150~220℃密封条件下水热反应完全,离心2~3次、洗涤、干燥即得。
14.优选地,所述丙三醇与异丙醇的体积比为1:(3~8)。
15.优选地,所述钴盐与异丙醇、丙三醇的比值为:0.1g:(30~50)ml:(5~10)ml。
16.更优选地,所述钴盐为硝酸钴或其水合物。
17.优选地,所述水热反应的时间为2~6h。
18.优选地,所述离心的转速设置为10000~12000r/min,时间为4~6min。
19.优选地,所述洗涤用无水乙醇洗涤。
20.优选地,所述干燥的温度为70~90℃,时间为5~8h。
21.优选地,所述0.1~1.5mol/l植酸溶液由植酸体积比为40~60%的植酸水溶液溶于有机溶剂中得到。
22.优选地,所述氩氢气体中氢气的浓度为3~6%。
23.优选地,所述煅烧的温度为600~900℃。
24.优选地,所述有机溶剂为无水乙醇或甲醇。
25.优选地,所述煅烧的升温速率为1~2℃/min。
26.优选地,所述煅烧之前还包括在200~500℃下预煅烧2~3h。
27.更优选地,所述预煅烧的升温速率为1~2℃/min。
28.优选地,所述反应时间为5~30min时,得到的磷化钴材料为co2p相,所述反应时间为40min~60min时,得到的磷化钴材料为cop相,所述反应时间为30~40min时,得到的磷化钴材料为cop与co2p的混合相。
29.优选地,所述反应的方式为搅拌反应,搅拌的转速为400~600r/min。
30.优选地,所述后处理包括真空抽滤、洗涤、干燥。
31.更优选地,所述洗涤用无水乙醇洗涤。
32.更优选地,所述干燥的温度为70~90℃,时间为5~8h。
33.本发明进一步保护一种磷化钴材料,由上述制备方法制备得到。
34.优选地,所述磷化钴材料的结构为中空球状结构。
35.本发明进一步保护一种磷化钴复合材料的制备方法,包括如下步骤:
36.将甘油酸钴与0.1~1.5mol/l植酸溶液在有机溶液中反应5~60min,后处理得粉红色固体,将粉红色固体与氧化石墨烯分散液在有机溶剂中反应1.5~3小时,煅烧,即得磷化钴复合材料;
37.所述甘油酸钴与0.1~1.5mol/l植酸溶液的添加量比值为:0.1g:(8.5~10.5)ml。
38.优选地,所述粉红色固体与氧化石墨烯的质量比为(5~8):1。
39.优选地,所述氧化石墨烯为单层氧化石墨烯。
40.优选地,所述有机溶剂为无水乙醇或甲醇。
41.本发明进一步保护一种磷化钴复合材料,由上述制备方法制备得到。
42.本发明进一步保护上述磷化钴材料和磷化钴复合材料在锂离子电池中的应用。
43.本发明具有以下有益效果:
44.本发明采用植酸溶液与甘油酸钴进行反应,反应过程中能通过控制反应的时间来调整所得磷化钴材料的相态及形貌,操作方法简单,条件温和,能有效减少ph3等有毒气体产生,降低空气污染;制备得到的磷化钴材料不仅自身具有优异的导电率、比容量、倍率性能和循环性能,将其与单层氧化石墨烯制备得到的磷化钴复合材料也具有优异的导电率、比容量、倍率性能和循环性能。
附图说明
45.图1为实施例1~7制备得到的磷化钴材料的xrd图谱,并与标准谱图进行对比图。
46.图2为对比例1~4制备得到的磷化钴材料的xrd图谱,并与标准谱图进行对比图。
47.图3为实施例3制备得到甘油酸钴的sem图。
48.图4为实施例6制备得到甘油酸钴的sem图。
49.图5为实施例3制备得到甘油酸钴的tem图。
50.图6为实施例6制备得到甘油酸钴的tem图。
51.图7为实施例3制备得到磷化钴材料co2p@c的sem图。
52.图8为实施例6制备得到磷化钴材料cop@c的sem图。
53.图9为实施例3制备得到磷化钴材料co2p@c的tem图。
54.图10为实施例6制备得到磷化钴材料cop@c的tem图。
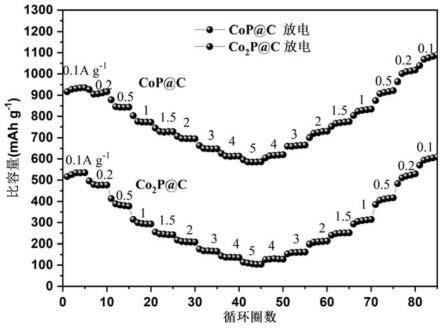
55.图11为实施例3、6制备得到的磷化钴材料半电池的倍率性能图。
56.图12为实施例3、6制备得到的磷化钴材料半电池的循环稳定性测试结果图。
57.图13为实施例8制备得到的磷化钴复合材料半电池的性能图。
具体实施方式
58.以下结合说明书附图和具体实施例来进一步说明本发明,但实施例并不对本发明做任何形式的限定。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。
59.除非特别说明,以下实施例所用试剂和材料均为市购。
60.实施例1磷化钴材料的制备
61.s1.准确称取0.108g的六水合硝酸钴co(no3)3·
6h2o固体,投入到100ml烧杯中,再依次加入40ml异丙醇和8ml的丙三醇溶液,磁力搅拌30min得到紫红色的钴溶液,随后将溶液转入到高压反应釜的聚四氟乙烯内胆中,放置在鼓风干燥箱中,在180℃条件下水热反应6h,转入到离心管中离心3次,每次转速设置为10000r/min,时间为5min,每次离心结束用无水乙醇溶液洗涤一次,将离心得到黄褐色固体放置在真空干燥箱中,在80℃下干燥6h,得到干燥的甘油酸钴,在研钵中研磨4~5min,得到较细的甘油酸钴粉末。
62.s2.用量程为1000ul移液枪准确移取909ul植酸体积比为50%的植酸水溶液加入到装有9ml无水乙醇的50ml烧杯当中,制成1mol/l植酸乙醇混合溶液。
63.s3.准确称量步骤s1中得到甘油酸钴粉末100mg投入到盛有15ml无水乙醇的50ml烧杯中,并加入步骤s2得到的植酸混合溶液,在磁力搅拌器上室温搅拌反应5min左右(整个
过程转速为600r/min),反应结束后,迅速将反应溶液在真空抽滤器中抽滤,抽滤时用无水乙醇冲洗,抽滤结束后得到粉红色固体,将表面覆有粉红色固体的滤纸取下,放入到80℃的真空干燥箱中干燥5h。
64.s4.将步骤s3中干燥后的粉红色固体研磨2~3min得到粉红色粉末,投入到瓷舟中,放入管式炉中煅烧,先以1℃/min的升温速率升温至200℃保温预煅烧2h,再以1℃/min的升温速率升温至800℃保温煅烧2h,随后冷却18h,得到黑色的磷化钴材料。
65.实施例2磷化钴材料的制备
66.与实施例1的区别在于,将步骤s3中加入步骤s2得到的植酸乙醇混合溶液,在磁力搅拌器上室温搅拌反应5min改为反应10min,其余步骤的试剂、条件均与实施例1一致。
67.实施例3磷化钴材料的制备
68.与实施例1的区别在于,将步骤s3中加入步骤s2得到的植酸乙醇混合溶液,在磁力搅拌器上室温搅拌反应5min改为反应20min,其余步骤的试剂、条件均与实施例1一致。
69.实施例4磷化钴材料的制备
70.与实施例1的区别在于,将步骤s3中加入步骤s2得到的植酸乙醇混合溶液,在磁力搅拌器上室温搅拌反应5min改为反应30min,其余步骤的试剂、条件均与实施例1一致。
71.实施例5磷化钴材料的制备
72.与实施例1的区别在于,将步骤s3中加入步骤s2得到的植酸乙醇混合溶液,在磁力搅拌器上室温搅拌反应5min改为反应40min,其余步骤的试剂、条件均与实施例1一致。
73.实施例6磷化钴材料的制备
74.与实施例1的区别在于,将步骤s3中加入步骤s2得到的植酸乙醇混合溶液,在磁力搅拌器上室温搅拌反应5min改为反应50min,其余步骤的试剂、条件均与实施例1一致。
75.实施例7磷化钴材料的制备
76.与实施例1的区别在于,将步骤s3中加入步骤s2得到的植酸乙醇混合溶液,在磁力搅拌器上室温搅拌反应5min改为反应60min,其余步骤的试剂、条件均与实施例1一致。
77.对比例1磷化钴材料的制备
78.与实施例1的区别在于,将步骤s2中植酸的乙醇混合溶液浓度改为0.01mol/l,其余步骤的试剂、条件均与实施例1一致。
79.对比例2磷化钴材料的制备
80.与实施例1的区别在于,将步骤s2中植酸的乙醇混合溶液浓度改为0.01mol/l,将步骤s3中加入步骤s2得到的植酸乙醇混合溶液,在磁力搅拌器上室温搅拌反应5min改为反应60min,其余步骤的试剂、条件均与实施例1一致。
81.对比例3磷化钴材料的制备
82.与实施例1的区别在于,将步骤s2植酸的乙醇混合溶液浓度改为2mol/l,其余步骤的试剂、条件均与实施例1一致。
83.对比例4磷化钴材料的制备
84.与实施例1的区别在于,将步骤s2植酸的乙醇混合溶液浓度改为2mol/l,将步骤s3中加入步骤s2得到的植酸乙醇混合溶液,在磁力搅拌器上室温搅拌反应5min改为反应60min,其余步骤的试剂、条件均与实施例1一致。
85.结构表征:
86.将实施例1~7与对比例1~4制备得到的磷化钴材料进行xrd表征,并与标准的cop和co2p以及co的标准谱图进行对比,结果如图1、图2。
87.如图1所示:cop#pdf29-0497和co2p#pdf32-0306分别为cop相和co2p相的标准xrd谱图。当植酸混合溶液在磁力搅拌器上室温搅拌反应时间为5~30min时,得到的产物为co2p相,即实施例1~4制备得到磷化钴材料的结构式为co2p@c;反应时间为30~40min时,产物为cop相与co2p相的混合物;反应时间为40~60min时,得到的产物为cop相,即实施例5~7制备得到磷化钴材料的结构式为cop@c。
88.如图2所示:co#pdf15-0806为co的标准xrd谱图。在其他条件不变情况下,当植酸浓度为0.05mol/l时,反应5min到60min得到的产物均为co相,得不到cop相或co2p相的产物;当植酸浓度为2mol/l时,反应5min到60min,产物均为cop相,得不到co2p相的产物。
89.将实施例3和实施例6中得到的甘油酸钴与磷化钴材料用sem和tem进行结构表征,结果如3~10。
90.如图3~6所示:实施例3与实施例6制备得到的甘油酸钴均为实心球结构。
91.如图7~10所示:实施例3制备得到的co2p@c与实施例6制备得到的cop@c均为中空结构。
92.实施例8磷化钴复合材料cop@c@rgo的制备
93.s1.准确称取0.108g的六水合硝酸钴co(no3)3·
6h2o固体,投入到100ml烧杯中,再依次加入40ml异丙醇和8ml的丙三醇溶液,磁力搅拌30min得到紫红色的钴溶液,随后将溶液转入到高压反应釜的聚四氟乙烯内胆中,放置在鼓风干燥箱中,在180℃条件下水热反应6h,转入到离心管中离心3次,每次转速设置为10000r/min,时间为5min,每次离心结束用无水乙醇溶液洗涤一次,将离心得到黄褐色固体放置在真空干燥箱中,在80℃下干燥6h,得到干燥的甘油酸钴,在研钵中研磨4~5min,得到较细的甘油酸钴粉末。
94.s2.用量程为1000ul移液枪准确移取909ul的50%植酸溶液加入到装有9ml无水乙醇的50ml烧杯当中,制成植酸的乙醇混合溶液。
95.s3.准确称量步骤s1中得到甘油酸钴粉末100mg投入到盛有15ml无水乙醇的50ml烧杯中,并加入步骤s2得到的植酸混合溶液,在磁力搅拌器上室温搅拌反应5min左右(整个过程转速为600r/min),反应结束后,迅速将反应溶液在真空抽滤器中抽滤,抽滤时用无水乙醇冲洗,抽滤结束后得到粉红色固体,将表面覆有粉红色固体的滤纸取下,放入到80℃的真空干燥箱中干燥5h。
96.s4.将步骤s3中干燥后的粉红色固体研磨2~3min得到粉红色粉末,取72mg得到粉红色粉末投入含有100ml无水乙醇的烧杯中,磁力搅拌10min,随后按照6:1的质量比往上述混合液中加入6ml浓度为2mg/ml的单层氧化石墨烯分散液,磁力搅拌2h,后离心、干燥6h得cop@c@rgo前驱体。
97.s5.将步骤s4所得cop@c@rgo前驱体投入到瓷舟中,放入管式炉中煅烧,先以1℃/min的升温速率升温至200℃保温预煅烧2h,再以1℃/min的升温速率升温至800℃保温煅烧2h,随后冷却18h,得到磷化钴复合材料cop@c@rgo。
98.实验例1:实施例3、6制备得到的磷化钴材料和实施例8制备得到的磷化钴复合材料制备成半电池的性能研究
99.半电池的制备:
100.将实施例3、6制备得到的磷化钴材料和实施例8制备得到的磷化钴复合材料(活性物质)、科琴黑(导电剂)和粘结剂pvdf(聚偏氟乙烯)按质量比8:1:1在nmp(n-甲基吡咯烷酮)中混合均匀,然后涂在铜箔上,并置于真空干燥箱中80℃干燥10小时。取出之后切成直径为10mm的电极圆片,以此作为负极片,将金属锂片作为对电极,聚丙烯微孔膜celgard2400为隔膜,电解液为1m的lipf6/ec+dmc(体积比1:1),在充满氩气保护的手套箱中组装cr2032型纽扣半电池。使用现有技术手段测试其电化学性能。
101.实施例3、6制备得到的磷化钴材料半电池的倍率性能检测:分别采用0.1a/g、0.2a/g、0.5a/g、1a/g、1.5a/g、2a/g、3a/g、4a/g、5a/g的电流对其进行检测,先从0.1a/g~5a/g进行测试,再反向从5a/g~0.1a/g进行测试,结果如图11。
102.如图11所示:实施例3制备得到的co2p@c、实施例6制备得到的cop@c两相材料在在0.1~5a/g的电流大小下分别发挥出了533、474、383、295、244、209、167、136、105mah/g和934、910、842、772、727、695、647、611、584mah/g的比容量,展现了良好的倍率性能,反向从5a/g~0.1a/g进行测试后电池容量均得到回复且略有提升,说明在经过5a/g大电流测试之后材料结构没有被破坏。
103.实施例3、6制备得到的磷化钴材料半电池的循环稳定性测试:采用1a/g的电流对半电池进行充放电,结果如图12。
104.如图12所示:实施例3制备得到的co2p@c、实施例6制备得到的cop@c半电池稳定循环500圈,其中co2p@c几乎无容量损失而cop@c也仍然有初始容量的92%,说明该两相材料具有较好的循环稳定性。
105.实施例8制备得到的磷化钴复合材料半电池的倍率性能和循环稳定性:采用上述的方法进行研究,结果如图13。
106.如图13所示:实施例8掺杂还原氧化石墨烯之后制备得到的磷化钴复合材料cop@c/rgo半电池与cop@c半电池相比,小电流倍率下的放电比容量有所提高。
107.上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1