磺胺类药物半抗原及其制备方法和应用与流程
本发明涉及一种半抗原及其制备方法和应用,具体涉及磺胺类药物半抗原及其制备方法和应用。技术背景磺胺类药物(Sulfonamides,SAs)是一类具有对氨基苯磺酰胺结构、用于预防和治疗细菌感染性疾病的化学治疗药物。因具有广谱、稳定、经济、易用以及联合抗菌增效剂效果可提高数十倍的特点,常以亚治疗浓度的药物做为饲料添加剂来预防疾病的发生,提高饲料的转化率和促进动物生长,其中常用的SAs就有十几种。但该类药物存在严重副作用,人体中长期存在会导致许多细菌对磺胺类药物产生耐药性,且有潜在的致癌性,因此已引起了国内外的高度重视。我国以及美国、欧盟等国家规定了动物性食品中总磺胺以及单个磺胺的最高残留限量(MRLs)为0.1mg/kg,其中磺胺二甲基嘧啶(SM2)的MRLs为0.025μg/ml。目前,磺胺类药物残留的检测方法主要有微生物学法、理化分析方法和免疫法等。微生物学法简便、费用低,但操作费时且敏感性、特异性都较差,在定性定量上都存在困难,不能满足现代残留检测的需要,甚至有些检测结果还达不到最高残留限量的要求;理化法常作为确证方法用于测定动物组织中的药物残留,如气相色谱(GC)、高效液相色谱(HPLC)、气-质联用(GC-MS)、液-质联用(HPLC-MS)等,这些方法灵敏、准确,特异性强、分离度好,可以同时测定多种药物,但需要昂贵的仪器、样品的前处理复杂、繁琐费时、检测的成本较高,不能现场操作,而且需专业人员操作,所以限制了其应用;与之相比,酶联免疫方法具有特异性好、灵敏度高、操作简便、检测成本低、适合于批量样品的筛选检测等优点,而且所需设备少,操作简单易学,成本低廉,能够更好地满足我国畜禽养殖户、屠宰场、食品企业、政府职能监管部门等开展检测工作。
技术实现要素:
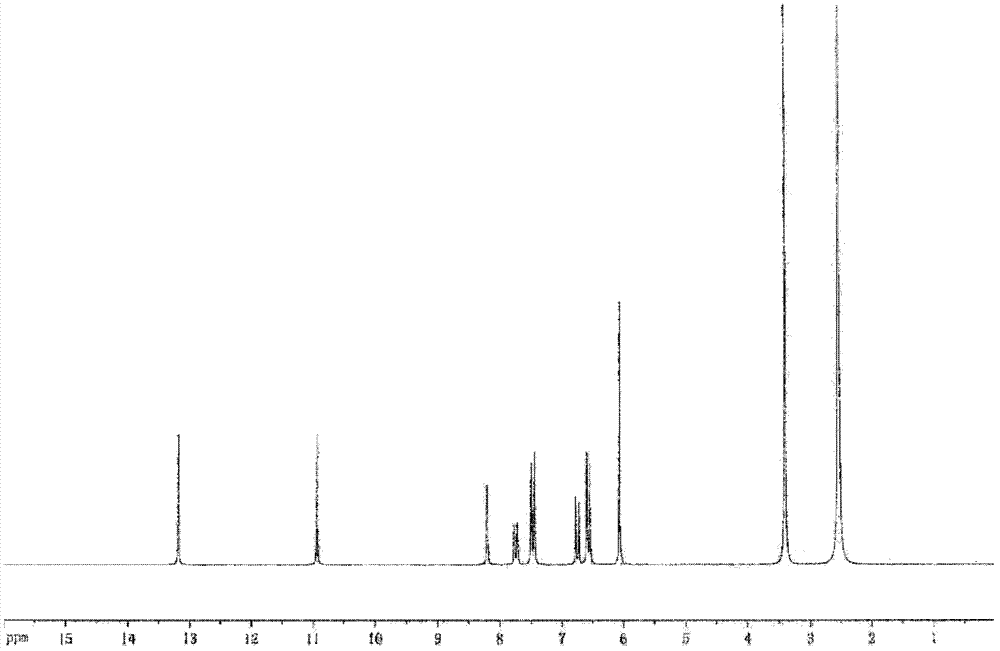
本发明的目的是提供一种磺胺类药物半抗原及其制备方法。本发明提供的磺胺类药物半抗原,分子结构式为:本发明提供的磺胺类药物半抗原的制备方法,包括如下步骤:a)于25ml单口瓶中加入6-氨基烟酸、乙醇和12mol/L盐酸,加热回流,反应8h,TLC监测,反应完毕,减压除去溶剂,溶于饱和NaHCO3水溶液,乙酸乙酯萃取,无水Na2SO4干燥,柱层析(乙酸乙酯/石油醚,2/1,v/v)纯化;b)于25ml单口瓶中加入a)所得产物、三乙胺(Et3N)和CH2Cl2,搅拌溶解后,加入催化剂4-二甲氨基吡啶(DMAP)。缓慢滴入4-乙酰氨基苯磺酰氯的二氯甲烷溶液,TLC监测,5h,反应完毕后处理,干燥,柱层析纯化(乙酸乙酯/石油醚,1/10,v/v);c)于25ml单口瓶中加入b)所得产物和2mol/LNaOH水溶液,加热回流,TLC监测,反应10h,完毕,调节pH4~5,有固体析出,即为磺胺类药物半抗原。本发明的另一个目的是上述磺胺类药物半抗原在免疫检测中的应用,具体包括由所述磺胺类药物半抗原与载体蛋白偶联得到的磺胺类药物抗原,及由所得磺胺类药物抗原免疫动物制备得到的磺胺类药物抗体。其中所述载体蛋白可为鼠血清蛋白、甲状腺蛋白、牛血清白蛋白、兔血清蛋白、人血清蛋白、卵清蛋白、血蓝蛋白或纤维蛋白原,所述抗体为磺胺类药物单克隆抗体。本发明还提供由上述磺胺类药物抗体制备的酶联免疫试剂盒,及其在检测动物源性样本中磺胺类药物残留的应用。本发明提供的磺胺类药物半抗原既最大程度地保留了磺胺母核的化学结构,又通过化学合成改造引入了可以与蛋白质偶联的—COOH,合成方法简单,纯度、产率较高;用该半抗原作为原料,制备适于动物免疫的抗原体系免疫动物,所得抗体的效价、特异性、亲和力都比较好;所得的抗体用于酶联免疫试剂盒,可以同时检测磺胺嘧啶、磺胺间甲氧嘧啶、磺胺甲基异噁唑、磺胺噻唑、酞酰磺噻唑、磺胺甲噻二唑、磺胺吡啶七种药物,使用方便、检测成本低、检测方法高效、准确、快速、可同时检测大批量的样本,适于动物源性样本中磺胺类药物残留的现场监控和大量样本的筛查。本发明的磺胺类药物半抗原在磺胺类药物的检测中发挥重要作用。附图说明图1:磺胺类药物半抗原合成路线图图2:磺胺类药物半抗原核磁共振氢谱图图3:磺胺类药物酶联免疫试剂盒标准曲线具体实施方式下面结合具体的实施例来进一步阐述本发明。应理解,这些实施例仅用于说明本发明,而不用来限制本发明的范围。实施例1磺胺类药物半抗原的合成和鉴定一、磺胺类药物半抗原的合成(合成路线如图1)a)于25ml单口瓶中加入6-氨基烟酸0.87g,乙醇20ml,12mol/L盐酸3.7ml,加热回流,反应8h,TLC监测,反应完毕,减压除去溶剂,溶于饱和NaHCO3水溶液,乙酸乙酯萃取,无水Na2SO4干燥,柱层析(乙酸乙酯/石油醚,2/1,v/v)纯化;b)于25ml单口瓶中加入a)所得产物0.89g,三乙胺(Et3N)1.6ml,CH2Cl210ml,搅拌溶解后,加入催化剂4-二甲氨基吡啶(DMAP)。缓慢滴入4-乙酰氨基苯磺酰氯的2ml二氯甲烷溶液,TLC监测,5h,反应完毕后处理,干燥,柱层析纯化(乙酸乙酯/石油醚,1/10,v/v);c)于25ml单口瓶中加入b)所得产物1g,2mol/LNaOH水溶液120ml,加热回流,TLC监测,反应10h,完毕,调节pH4~5,有固体析出,即为磺胺类药物半抗原。二、磺胺类药物半抗原的鉴定取合成的磺胺类药物半抗原经核磁共振氢谱测定,如图2所示,图谱中6.7~8.2ppm左右的三个峰为吡啶环上的H信号峰,11ppm左右的单峰为磺胺键上的N—H峰,13.1ppm左右的单峰为羧基峰,说明半抗原合成成功。实施例2磺胺类药物抗原将磺胺类药物半抗原与载体蛋白进行偶联得到磺胺类药物抗原。一、免疫原的制备——磺胺类药物半抗原-牛血清白蛋白偶联物合成取12mg磺胺类药物半抗原,溶解于1mlN,N-二甲基甲酰胺(DMF)中,得到溶液I;取15mg碳化二亚胺(EDC)用0.2ml水充分溶解后于加入I中,室温下搅拌24h,得到溶液Ⅱ;称取牛血清白蛋白(BSA)40mg,使之充分溶解在3mlPBS(pH7.2)中,将溶液Ⅱ逐滴缓慢滴加到蛋白溶液中,并于室温下搅拌24h;用0.01mol/LPBS4℃透析3天,每天换3次透析液,以除去未反应的小分子物质,即得到磺胺类药物免疫原;分装,于-20℃保存备用。二、包被原的制备——磺胺类药物半抗原-卵清蛋白偶联物合成取15mg磺胺类药物半抗原用0.8mlDMF溶解,冷却至10℃,得到溶液I;取氯甲酸异丁酯10μl加入I中,10℃搅拌反应30min;取30mg卵清蛋白用2.2ml50mmol/LNa2CO3溶解,10℃反应4h,然后4℃过夜;用0.01mol/LPBS4℃透析3天,每天换3次透析液,以除去未反应的小分子物质,即得到磺胺类药物包被原;分装,于-20℃保存备用。三、磺胺类药物抗原的鉴定将载体蛋白、磺胺类药物半抗原、磺胺类药物半抗原-载体蛋白偶联物用pH7.4的PBS配成0.5mg/ml的溶液,以0.01mol/LpH7.4PBS调零,用紫外分光光度计在波长200~800nm范围内扫描,得到载体蛋白、磺胺类药物半抗原、磺胺类药物半抗原-载体蛋白偶联物的吸收曲线,并计算其结合比。结果发现,三者出现不同的吸收曲线,表明磺胺类药物半抗原与载体蛋白偶联成功,半抗原与牛血清白蛋白的结合比为(18~22):1,与卵清蛋白的结合比为(16~21):1。实施例3磺胺类药物单克隆抗体一、磺胺类药物单克隆抗体的制备动物免疫:将免疫原注入到Balb/c小鼠体内,免疫剂量为150μg/只,使其产生多克隆抗体血清。细胞融合和克隆化:小鼠血清测定结果较高后,取其脾细胞,按8:1比例与SP2/0骨髓瘤细胞融合,采用间接竞争ELISA测定细胞上清液,筛选阳性孔。利用有限稀释法对阳性孔进行克隆化,直到得到分泌单克隆抗体的杂交瘤细胞株。细胞冻存和复苏:将磺胺类药物的单克隆杂交瘤细胞株用冻存液制成1×109个/ml的细胞悬液,在液氮中长期保存。复苏时取出冻存管,立即放入37℃水浴中速融,离心去除冻存液后,移入培养瓶内培养。单克隆抗体的生产与纯化:将Balb/c小鼠腹腔注入灭菌石蜡油0.5ml/只,7天后腹腔注射磺胺类药物的单克隆杂交瘤细胞株6×105个/只,7天后采集腹水。用辛酸-饱和硫酸铵法进行腹水纯化,-20℃保存。二、单克隆抗体效价的测定用间接竞争ELISA法测定抗体的效价为1:(50000~100000)。间接竞争ELISA方法:用磺胺类药物半抗原-卵清蛋白偶联物包被酶标板,加入磺胺嘧啶标准品溶液、酶标二抗和单克隆抗体工作液,25℃反应30min,倒出孔内液体,用PBST洗涤液洗涤3~5次,用吸水纸拍干;加入底物显色液,25℃反应15min后,加入终止液终止反应;设定酶标仪于波长450nm处测定每孔吸光度值。三、单克隆抗体的特异性抗体特异性是指它同特异性抗原结合的能力与同该类抗原类似物结合能力的比较,常用交叉反应率作为评价标准。交叉反应越小,抗体的特异性则越高。本实验将磺胺嘧啶、磺胺间甲氧嘧啶、磺胺甲基异噁唑、磺胺噻唑、酞酰磺噻唑、磺胺甲噻二唑、磺胺吡啶、磺胺二甲基嘧啶、磺胺二甲氧嘧啶、磺胺喹噁啉、磺胺甲基嘧啶11种磺胺类药物做系列稀释,分别与单克隆抗体进行间接竞争ELISA,制作标准曲线,分析得到IC50,然后按下式计算交叉反应率:结果显示各磺胺类药物的交叉反应率为:磺胺嘧啶100.0%、磺胺间甲氧嘧啶97.6%、磺胺甲基异噁唑169.0%、磺胺噻唑188.0%、酞酰磺噻唑62.8%、磺胺甲噻二唑103%、磺胺吡啶51.9%、磺胺二甲基嘧啶<1%、磺胺二甲氧嘧啶<1%、磺胺喹噁啉<1%、磺胺甲基嘧啶<1%。本发明抗体可以同时检测磺胺嘧啶、磺胺间甲氧嘧啶、磺胺甲基异噁唑、磺胺噻唑、酞酰磺噻唑、磺胺甲噻二唑、磺胺吡啶7种磺胺类药物。实施例4由磺胺类药物单克隆抗体制备的酶联免疫试剂盒一、酶联免疫试剂盒的组成(1)包被磺胺类药物半抗原-载体蛋白偶联物的酶标板;(2)用辣根过氧化物酶标记的羊抗鼠抗抗体;(3)磺胺类药物单克隆抗体工作液;(4)磺胺嘧啶标准品溶液6瓶,浓度分别为0μg/L、0.5μg/L、1.5μg/L、4.5μg/L、13.5μg/L、40.5μg/L;(5)底物显色液由A液和B液组成,A液为过氧化脲,B液为四甲基联苯胺;(6)终止液为2mol/L硫酸;(7)浓缩洗涤液为pH7.2,含0.8%~1.2%吐温-20、0.01‰~0.03‰硫柳汞防腐剂、0.1~0.3mol/L的碳酸盐缓冲液,所述百分比为重量体积百分比;(8)浓缩复溶液为pH7.6,含8%~12%酪蛋白、0.1~0.3mol/L的磷酸盐缓冲液,所述百分比为重量体积百分比。本试剂盒的主要试剂以工作液的形式提供,检验方法方便易行,具有特异性高、灵敏度高、精确度高、准确度高等特点,同时采用一步法,节省了检测时间。二、酶联免疫试剂盒检测实际样本的应用1.样品前处理(1)鲜牛奶前处理方法取50μl鲜牛奶样本,加入450μl复溶工作液中,混匀;取50μl用于分析(2)组织(鸡肉、猪肉、鱼、虾)前处理方法用均质器均质组织样本后,称取2.0±0.05g均质物至50ml聚苯乙烯离心管中,加入4mlpH=6的磷酸盐缓冲液涡动成糊状,再加入6ml乙酸乙酯,振荡1min,4000rpm室温(20-25℃/68-77℉)离心5min;取3ml上清液至10ml干净玻璃试管中,于50~60℃水浴氮气流下吹干;加入1ml正己烷,用涡旋仪涡动30s,再加入1ml复溶工作液,涡动10s,4000rpm室温(20-25℃/68-77℉)离心5min;除去上层正己烷相,取下层水相50μl用于分析。(3)蜂蜜前处理方法称取1.0±0.05g蜂蜜样本至50ml聚苯乙烯离心管中;加入1ml1mol/L盐酸溶液,用振荡器振荡至蜂蜜全部溶解;放入37℃培养箱中孵育30min;取出,加入1ml1mol/L氢氧化钠溶液和1mlpH=6的磷酸盐缓冲液,再分别加入2ml乙腈和6ml乙酸乙酯,用振荡器振荡1min,4000rpm室温(20-25℃/68-77℉)离心10min;取4ml上层有机相至10ml干净玻璃试管中,于50~60℃水浴氮气流下吹干;加0.5ml复溶工作液溶解;取50μl用于分析。(4)尿液前处理方法取50μl尿液样本,加入150μl洗涤工作液中,混匀;取50μl用于分析。2.用试剂盒检测向包被有磺胺类药物包被抗原的酶标板微孔中加入磺胺嘧啶标准品溶液或样品溶液50μl,随即加入辣根过氧化物酶标记的羊抗鼠抗抗体50μl/孔,再加入磺胺类药物单克隆抗体工作液50μl/孔,用盖板膜盖板后,置25℃恒温箱中避光反应30min,倒出孔内液体,每孔加入250μl洗涤液,30s后倒出孔内液体,如此重复操作洗板5次,用吸水纸拍干;每孔加入底物显色液A液过氧化脲50μl,底物显色液B液四甲基联苯胺(TMB)50μl,轻轻振荡混匀,用盖板膜盖板后置25℃恒温箱中避光显色15min,每孔加入终止液2mol/L硫酸50μl,轻轻振荡混匀,用酶标仪波长设定在450nm处,测定每孔吸光度值(OD值)。3.检测结果分析用所获得的每个浓度的标准品溶液的吸光度平均值(B)除以第一个标准品溶液(0标准)的吸光度值(B0)再乘以100%,得到百分吸光度值。以磺胺嘧啶标准品浓度(μg/L)的对数值为X轴,百分吸光度值为Y轴,绘制标准曲线图,如图3所示。用同样的办法计算样品溶液的百分吸光度值,从标准曲线上读出样本所对应的浓度,乘以其对应的稀释倍数,再乘以每种药物对应的交叉反应率,即为样本中磺胺类药物的实际浓度。三、酶联免疫试剂盒技术参数的确定最低检测限:对20份空白样本进行检测,从标准曲线上查出对应于各百分吸光度值的浓度,以20份样本磺胺类药物浓度的平均值加上3倍标准差表示检测限,结果得该方法对牛奶样本的最低检测限为5μg/L,对动物组织、蜂蜜样本的最低检测限为0.5μg/kg,对尿液样本的最低检测限为2μg/L。准确度和精密度:ELISA测定的准确度以回收率表示,精密度以变异系数表示。取空白样本,以50、100、200μg/kg三个浓度的磺胺类药物对其进行添加回收试验(添加浓度超出曲线测量范围,需要把样本酌情稀释后再进行检测,),结果得该方法对牛奶样本的回收率为85%±15%,对动物组织样本的回收率为75%±10%,对蜂蜜样本的回收率为90%±10%,对尿液样本的回收率为95%±15%,批内变异系数<15%,批间变异系数<25%。经测定本发明试剂盒在2~8℃至少可以保存12个月。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1