提高脱水穿心莲内酯水溶性、酯-水分配系数的方法及新型脱水穿心莲内酯、制备、应用与流程
本发明涉及一种提高脱水穿心莲内酯水溶性和/或酯-水分配系数的方法及一种PEG修饰的新型脱水穿心莲内酯化合物及其制备方法和应用。
背景技术:
药物的溶解度是制剂研制中关注的首要问题之一,也是制剂能否有效吸收的关键之一。
脱水穿心莲内酯具有祛热解毒、消炎止痛的功效,对细菌性与病毒性上呼吸道感染及痢疾有特殊疗效,被誉为天然抗生素药物。最近的研究还表明,脱水穿心莲内酯还具有利胆保肝、抗肿瘤及其抗艾滋病等功效。然而,由于脱水穿心莲内酯的水溶性差,25℃条件水中溶解度C=0.027mg/mL,导致其疗效性低,使得其在临床上的应用受到一定的限制。
针对临床上病毒感染急症的需求,需要在脱水穿心莲内酯中引入亲水基团,以增强其水溶性,提高其疗效。目前,已在临床上应用的脱水穿心莲内酯针剂药物有穿琥宁、炎琥宁、莲必治等,其药物主要成分为脱水穿心莲琥珀酸内酯单钾盐化合物。然而,临床上应用的(即已商品化)的脱水穿心莲针剂药物在使用中表现出过敏反应、消化道反应、血液系统反应、以及致热原样反应等不良反应。
因此,有必要发展一种新型的水溶性脱水穿心莲内酯药物,改善其水溶性和/或脂水分配系数,生物相容性好,避免现有脱水穿心莲针剂药物的不良反应,提高药效,更适合临床应用。
技术实现要素:
本发明的第一个目的在于提供一种提高脱水穿心莲内酯水溶性和/或酯-水分配系数的方法。
本发明的第二个目的在于提供一种PEG修饰的新型脱水穿心莲内酯化合物。
本发明的第三个目的在于提供上述PEG修饰的新型脱水穿心莲内酯化合 物的制备方法。
本发明的第四个目的在于提供上述PEG修饰的新型脱水穿心莲内酯化合物的应用。
为达到上述第一个目的,本发明采用下述技术方案:
一种提高脱水穿心莲内酯水溶性和/或酯-水分配系数的方法,该方法利用PEG类化合物作为亲水基团取代基对脱水穿心莲内酯类化合物进行结构修饰来提高脱水穿心莲内酯水溶性和/或酯-水分配系数;
所述脱水穿心莲内酯类化合物为穿心莲内酯和/或脱水穿心莲内酯。
该方法可利用不同结构的、不同聚合度的PEG类化合物。优选地,PEG类化合物选自聚乙二醇PEG、聚乙二醇单醚mPEG中的一种或两种以上混合物。
更优选地,所述聚乙二醇单醚mPEG的结构式为R-O(CH2CH2O)n-CH2CH2OH;聚合度n为1-8;R为H、C1-C4的烷烃中的一种。C1-C4的烷烃指-CH3、-C2H5、-C3H7、-C4H9。
优选地,所述结构修饰是:将PEG类化合物氧化成PEG羧酸来修饰脱水穿心莲内酯类化合物,或者将PEG类化合物与酸酐反应生成PEG酸酐半酯来修饰脱水穿心莲内酯类化合物。
更优选地,所述酸酐为琥珀酸酐、戊二酸酐或邻苯二酸酐。
为达到上述第二个目的,本发明采用下述技术方案:
采用前述的将PEG类化合物作为亲水基团取代基对脱水穿心莲内酯类化合物进行结构修饰,得到了一种新型脱水穿心莲内酯化合物(简写为DA),分子结构式为:
其中,
R1为H,R2选自结构式L10、L20、L30中的一种;
R2为H,R1选自结构式L10、L20、L30中的一种;或者
R1与R2相同,选自结构式L10、L20、L30中的一种;
其中,
结构式L10、L20、L30分别为:
式中,R为H、C1-C4的烷烃中的一种;m为1-2;n为1-8。
本发明的新型脱水穿心莲内酯化合物为单取代脱水穿心莲内酯或双取代脱水穿心莲内酯。
为达到上述第三个目的,本发明采用下述技术方案:
上述新型脱水穿心莲内酯化合物的制备方法,包括以下步骤:
1.1)将PEG类化合物氧化成PEG羧酸,为L1;或者,将PEG类化合物与酸酐反应生成PEG酸酐半酯,为L2或L3;
式中,R为H、C1-C4的烷烃中的一种;m为1-2;n为1-8;
1.2)将脱水穿心莲内酯类化合物与步骤1.1)得到的L1、L2或L3按照一定摩尔比溶于有机溶剂中,在催化剂、脱水剂存在下反应;
待反应完成后,向其中加入盐酸水溶液,搅拌,得到的水相用有机溶剂 萃取,得到萃取液;
萃取液用饱和食盐水洗涤,将得到的有机相干燥,减压蒸馏除去有机溶剂,得到粗产物;
粗产物经硅胶层析色谱柱分离,得到新型脱水穿心莲内酯化合物DA-双或DA-C19;
其中,所述脱水穿心莲内酯类化合物为穿心莲内酯和/或脱水穿心莲内酯;
新型脱水穿心莲内酯化合物DA-双或DA-C19的结构式为:
当脱水穿心莲内酯类化合物与步骤1.1)得到的L1、L2或L3按照摩尔比1:2-5反应时,产物为新型脱水穿心莲内酯化合物DA-双,结构式中,R1与R2相同,选自结构式L10、L20、L30中的一种;
当脱水穿心莲内酯类化合物与步骤1.1)得到的L1、L2或L3按照摩尔比1:1-1.8反应时,产物为新型脱水穿心莲内酯化合物DA-C19,结构式中,R2为H,R1选自结构式L10、L20、L30中的一种;
其中,
结构式L10、L20、L30分别为:
式中,R为H、C1-C4的烷烃中的一种;m为1-2;n为1-8。
上述新型脱水穿心莲内酯化合物的制备方法,包括以下步骤:
2.1)将PEG类化合物氧化成PEG羧酸,为L1;或者,将PEG类化合物与酸酐反应生成PEG酸酐半酯,为L2或L3;
式中,R为H、C1-C4的烷烃中的一种;m为1-2;n为1-8;
2.2)对脱水穿心莲内酯类化合物的C19-OH进行保护;
2.3)将C19-OH保护后的脱水穿心莲内酯类化合物与步骤2.1)得到的L1、L2或L3按照摩尔比1:1-1.8溶于有机溶剂中,在催化剂、脱水剂存在下反应;
待反应完成后,向其中加入盐酸水溶液,搅拌,得到的水相用有机溶剂萃取,得到萃取液;
萃取液用饱和食盐水洗涤,将得到的有机相干燥,减压蒸馏除去有机溶剂,得到粗产物;
粗产物经硅胶层析色谱柱分离,得到C19保护的聚乙二醇穿心莲内酯;
2.4)将C19保护的聚乙二醇穿心莲内酯脱保护,得到新型脱水穿心莲内酯化合物DA-C3;
其中,所述脱水穿心莲内酯类化合物为穿心莲内酯和/或脱水穿心莲内酯;
新型脱水穿心莲内酯化合物DA-C3的结构式为:
结构式中,R1为H,R2选自结构式L10、L20、L30中的一种;
其中,
结构式L10、L20、L30分别为:
式中,R为H、C1-C4的烷烃中的一种;m为1-2;n为1-8。
制备DA-C3的流程示意式为:
R’为三甲基氯甲烷(TrCl)、2-四氢吡喃(THP)、三甲基氯硅烷(TMSCl)、叔丁基二甲基氯硅烷(TBDMSCl)、叔丁基二苯基氯硅烷(TBDPSCl)、三异丙基氯硅烷(TIPSCl)、三氟甲磺酸三甲基硅酯(TMSOTf)、三氟甲磺酸叔丁基二甲基硅酯(TBDMSOTf)或三氟甲磺酸叔丁基二苯基硅酯 (TBDPSOTf)。
该方法可利用不同结构的、不同聚合度的PEG类化合物。优选地,步骤1.1)和2.1)中,PEG类化合物选自聚乙二醇PEG、聚乙二醇单醚mPEG中的一种或两种以上混合物。优选地,所述聚乙二醇单醚mPEG的结构式为R-O(CH2CH2O)n-CH2CH2OH;聚合度n为1-8;R为H、C1-C4的烷烃中的一种。C1-C4的烷烃指-CH3、-C2H5、-C3H7、-C4H9。
优选地,步骤1.1)和2.1)中,所述酸酐为琥珀酸酐、戊二酸酐或邻苯二酸酐。
步骤1.1)和2.1)中,将PEG类化合物氧化成PEG羧酸,可参考文献Sarmenio Saliba,Clara Valverde Serrano,Juliane Keilitz,Myrtil L.Kahn,Christophe Mingotaud,Rainer Haag,Jean-Daniel Marty,Chem.Mater.2010,22,6301-6309。
制备过程为:
其中,R为H、C1-C4的烷烃中的一种;n为1-8。
步骤1.1)和2.1)中,将PEG类化合物与酸酐反应生成PEG酸酐半酯,可参考文献Karthik Vikram Siva Shanmugam,J.Scott Parent,and Ralph A.Whitney,Ind.Eng.Chem.Res.2012,51,8957-8965。
制备过程为:
式中,R为H、C1-C4的烷烃中的一种;m为1-2;n为1-8。
步骤2.2)中,对脱水穿心莲内酯类化合物的C19-OH进行保护可参考文 献Chunlei Tang,Guolong Gu,Bin Wang,Xin Deng,Xiaoyun Zhu,Hai Qian,and Wenlong Huang,Chem.Biol.DrugDes.2014,83,324-333。
优选地,步骤2.2)中,采用以下化合物中的一种对C19-OH进行保护:三甲基氯甲烷(TrCl)、2-四氢吡喃(THP)、三甲基氯硅烷(TMSCl)、叔丁基二甲基氯硅烷(TBDMSCl)、叔丁基二苯基氯硅烷(TBDPSCl)、三异丙基氯硅烷(TIPSCl)、三氟甲磺酸三甲基硅酯(TMSOTf)、三氟甲磺酸叔丁基二甲基硅酯(TBDMSOTf)或三氟甲磺酸叔丁基二苯基硅酯(TBDPSOTf)。
步骤1.2)和2.3)中,在催化剂、脱水剂存在下反应时,采用薄层色谱(TLC)板检测反应的进展。
优选地,步骤1.2)和2.3)中,反应温度为0-110℃。
优选地,步骤1.2)和2.3)中,催化剂选自二甲胺、二乙胺、三甲胺、三乙胺、N,N-二异丙基乙胺、二异丙胺、二丁胺、吡啶、N-甲基吡啶、4-二甲氨基吡啶、六亚甲基四胺、吗啉、N-甲基吗啉、哌啶、四氢吡咯、N-甲基四氢吡咯中的一种或两种以上混合物。
优选地,步骤1.2)和2.3)中,脱水剂选自N,N-二环己基碳二亚胺(DCC)、N,N-二异丙基碳二亚胺(DIC)、1-乙基-(3-二甲氨基丙基)碳二亚胺盐酸盐(EDC-HCl)中的一种或两种以上混合物。
萃取用有机溶剂和溶剂用有机溶剂可相同,可不同。优选地,步骤1.2)中,有机溶剂选自二氯甲烷、三氯甲烷、四氯化碳、1,2-二氯乙烷、苯、甲苯、二甲苯、氯苯、二氯苯、四氢呋喃、乙腈、乙酸乙酯、乙酸甲酯、乙酸丙酯、二甲亚砜、环丁砜、N,N-二甲基甲酰胺、吡啶、丙酮、甲基丁酮、N-甲基吡咯烷酮、甲基异丁酮、2-丁酮、环己酮、环己烷、二氧六环中的一种或两种以上混合物。步骤2.3)中,有机溶剂选自二氯甲烷、三氯甲烷、四氯化碳、1,2-二氯乙烷、苯、甲苯、二甲苯、氯苯、二氯苯、四氢呋喃、乙腈、乙酸乙酯、乙酸甲酯、乙酸丙酯、二甲亚砜、环丁砜、N,N-二甲基甲酰胺、吡啶、丙酮、甲基丁酮、N-甲基吡咯烷酮、甲基异丁酮、2-丁酮、环己酮、环己烷、二氧六环、乙醇、甲醇、异丙醇、正丁醇、乙酸、乙酸酐中的一种或两种以上混合物。
步骤2.4)中,脱保护反应可参考文献Chunlei Tang,Guolong Gu,Bin Wang,Xin Deng,Xiaoyun Zhu,Hai Qian,and Wenlong Huang,Chem.Biol.Drug Des.2014,83,324-333。
优选地,步骤2.4)中,采用酸法脱保护基或碱法脱保护基;采用酸法脱 保护基时的酸为甲酸、乙酸或氢溴酸;采用碱法脱保护基时的碱为四烷基氟化胺(TBAF)、碳酸钾或氨水。
本发明还提供上述新型脱水穿心莲内酯化合物的应用。该化合物可制成脱水穿心莲内酯制剂来应用。
本发明的有益效果如下:
1、本发明通过利用PEG作为亲水基团,提高了脱水穿心莲内酯类化合物的水溶性和/或酯-水分配系数,改善了脱水穿心莲内酯制剂的药效和生物利用度。
2、本发明利用PEG作为亲水基团,原料来源方便,价格低廉;生物相容性好,毒性低。
3、本发明可通过引入不同聚合度的PEG,来方便的调控新型脱水穿心莲内酯的水溶性和酯-水分配系数。
4、本发明的新型脱水穿心莲内酯制剂为水溶性的中性分子,遇含水环境易溶解,不需要添加助溶剂。
5、本发明的新型脱水穿心莲内酯的溶解度和酯-水分配系数不受环境影响(尤其是pH值),有利于在不同pH值环境中的溶解和吸收。
6、本发明的新型脱水穿心莲内酯的溶解度与穿心莲内酯或脱水穿心莲内酯相比,可提高多达10倍以上,同时,由于大幅度提高了药物的水溶性,以水等液体为介质的制剂中药物的浓度大幅度提高(提高10倍以上),明显增加药物的药效;新型脱水穿心莲内酯制剂中,药物的含量与穿心莲内酯或脱水穿心莲内酯相比,可降低达10倍以上,降低了脱水穿心莲内酯制剂的成本;新型脱水穿心莲内酯的酯-水分配系数(logP)不小于1.0,新型脱水穿心莲内酯制剂的酯-水分配系数logP≥1.0为特征的药物性能改善。
附图说明
下面结合附图对本发明的具体实施方式作进一步详细的说明。
图1示出实施例4化合物的核磁共振氢谱(1H NMR)图。
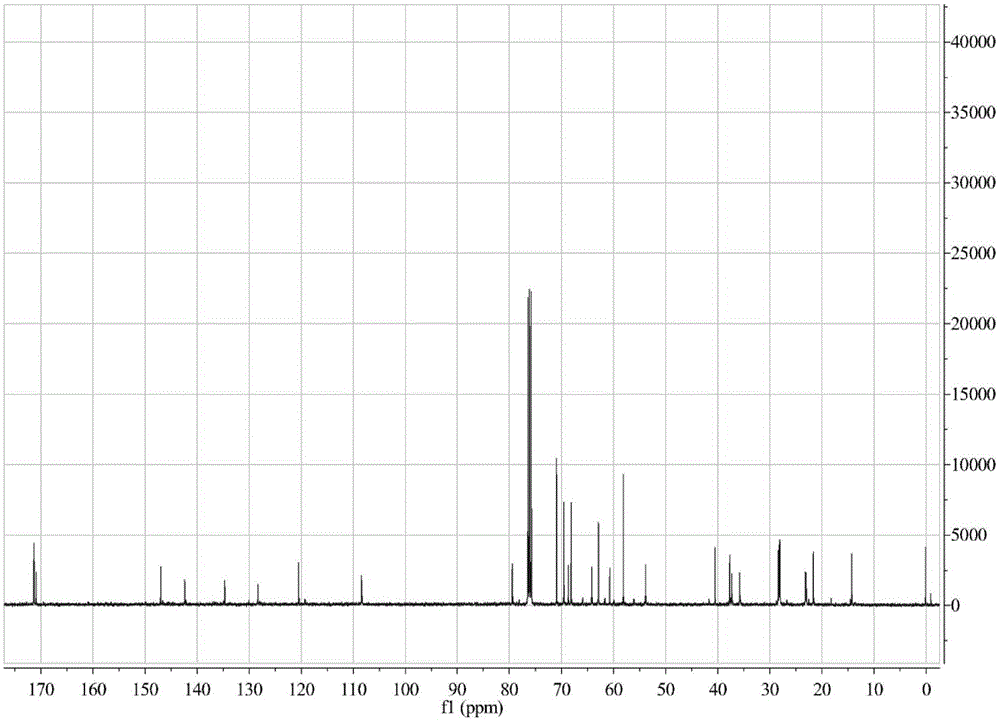
图2示出实施例4化合物的碳谱(13C-NMR)图。
图3示出实施例4化合物的高分辨质谱(HRMS)图。
图4示出实施例10化合物的核磁共振氢谱(1H NMR)图。
图5示出实施例10化合物的碳谱(13C-NMR)图。
图6示出实施例10化合物的高分辨质谱(HRMS)图。
具体实施方式
为了更清楚地说明本发明,下面结合优选实施例对本发明做进一步的说明。本领域技术人员应当理解,下面所具体描述的内容是说明性的而非限制性的,不应以此限制本发明的保护范围。
参考文献Sarmenio Saliba,Clara Valverde Serrano,Juliane Keilitz,Myrtil L.Kahn,Christophe Mingotaud,Rainer Haag,Jean-Daniel Marty,Chem.Mater.2010,22,6301-6309,将PEG类化合物氧化成PEG羧酸。
参考文献Karthik Vikram Siva Shanmugam,J.Scott Parent,and Ralph A.Whitney,Ind.Eng.Chem.Res.2012,51,8957-8965,将PEG类化合物与酸酐反应生成PEG酸酐半酯。
参考文献Chunlei Tang,Guolong Gu,Bin Wang,Xin Deng,Xiaoyun Zhu,Hai Qian,and Wenlong Huang,Chem.Biol.Drug Des.2014,83,324-333,对脱水穿心莲内酯类化合物的C19-OH进行保护。
一、双取代的脱水穿心莲内酯化合物(DA-双)的制备。
实施例1.二乙二醇单甲醚脱水穿心莲内酯(DA-双-1)
将穿心莲内酯(245mg,0.7mmol)或脱水穿心莲内酯(232m,g 0.7mmol))和二乙二醇单甲醚(225mg,1.68mmol)溶于40mL二氯甲烷中。依次加入EDC-HCl(326mg,1.7mmol)和DMAP(20mg,0.17mmol),室温搅拌14小时。反应完毕后,加入盐酸水溶液(0.1N,50mL),室温搅拌10分钟后,用二氯甲烷(20mL)萃取,共萃取三次。合并萃取液,用饱和食盐水(30mL)洗涤。有机相加入无水Na2SO4干燥,过滤后减压蒸馏掉有机溶剂,粗产品经硅胶层析色谱柱分离(洗脱剂为V石油醚:V乙酸乙酯:V乙酸=20:10:1) 得化合物DA-双-1,产率73%。
常规方法测得DA-双-1在水中的溶解度C=0.05mg/mL(25℃);酯-水分配系数logP=2.2。
实施例2.三乙二醇单甲醚脱水穿心莲内酯(DA-双-2)
按实施例1合成方法合成。用三乙二醇单甲醚替代实施例1的二乙二醇单甲醚。化合物DA-双-2产率70%。
常规方法测得化合物DA-双-2在水中的溶解度C=0.25mg/mL(25℃);酯-水分配系数logP=1.0。
实施例3.四乙二醇单甲醚脱水穿心莲内酯(DA-双-3)
按实施例1合成方法合成。用三乙二醇单甲醚替代实施例1的二乙二醇单甲醚。化合物DA-双-3产率65%。
常规方法测得化合物DA-双-3在水中的溶解度C=0.66mg/mL(25℃);酯-水分配系数logP=0.7。
实施例4.二乙二醇单甲醚琥珀酸酐脱水穿心莲内酯(DA-双-4)
按实施例1合成方法合成。用二乙二醇单甲醚琥珀酸酐半酯替代实施例1的二乙二醇单甲醚羧酸。化合物DA-4产率75%。
常规方法测得化合物DA-双-4在水中的溶解度C=0.048mg/mL(25℃);酯-水分配系数logP=2.1。
图1示出实施例4化合物的核磁共振氢谱(1H NMR)图。
图2示出实施例4化合物的碳谱(13C-NMR)图。
图3示出实施例4化合物的高分辨质谱(HRMS)图。
表1示出实施例2和实施例4化合物在不同pH值缓冲溶液中的溶解度和脂-水分配系数。
表1.化合物2和10在不同pH中的溶解度和脂-水分配系数(25℃)
注:a:纯水,b:PBS缓冲溶液
从表1中可以看出,本发明的新型脱水穿心莲内酯的溶解度和酯-水分配系数不受pH值,有利于在不同pH值环境中的溶解和吸收。
实施例5.三乙二醇正丁醚琥珀酸酐脱水穿心莲内酯(DA-双--5)
按实施例1合成方法合成。用三乙二醇正丁醚琥珀酸酐半酯替代实施例1的二乙二醇单甲醚羧酸。化合物DA-双-5产率72%。
常规方法测得化合物DA-双-5在水中的溶解度C=0.23mg/mL(25℃);酯-水分配系数logP=1.2。
二、C19-单取代的穿心莲内酯化合物(DA-C19)的制备。
实施例6.六乙二醇单甲醚琥珀酸酐脱水穿心莲内酯(DA-C19-1)
将穿心莲内酯(245mg,0.7mmol)或脱水穿心莲内酯(232mg,0.7mmol))和六乙二醇单甲醚琥珀酸酐半酯(415.8mg,1.05mmol)溶于40mL甲苯中。依次加入DCC(1.7mmol)和DMAP(20mg,0.17mmol),110℃回流4小时。反应完毕后,加入盐酸水溶液(0.1N,50mL),室温搅拌10分钟后,水相用二氯甲烷(20mL)萃取,共萃取三次。合并有机液,用饱和食盐水(30mL)洗涤。有机相加入无水Na2SO4干燥,过滤后减压蒸馏掉有机溶剂,粗产品经硅胶层析色谱柱分离(洗脱剂为V石油醚:V乙酸乙酯:V乙酸=20:10:1)得化合物DA-C19-1,产率58%。
常规方法测得化合物DA-C19-1在水中的溶解度C=230mg/mL(25℃);酯-水分配系数logP=1.0。
实施例7.mPEG350单甲醚邻苯二甲酸酐脱水穿心莲内酯(DA-C19-2)
按实施例6合成方法合成。用mPEG350琥珀酸酐半酯替代实施例6的六乙二醇单甲醚琥珀酸酐半酯。化合物DA-C19-2产率50%。
常规方法测得化合物DA-C19-2在水中的溶解度C=0.66mg/mL(25℃);酯-水分配系数logP=1.0。
实施例8.mPEG400单甲醚邻苯二甲酸酐脱水穿心莲内酯(DA-C19-3)
按实施例6合成方法合成。用mPEG400单甲醚邻苯二甲酸酐半酯替代实施例6中的六乙二醇单甲醚琥珀酸酐半酯。化合物DA-C19-3产率60%。
常规方法测得化合物DA-C19-3在水中的溶解度C=0.82mg/mL(25℃);酯-水分配系数logP=1.1。
三、C3-单取代的脱水穿心莲内酯化合物的制备。
实施例9.三乙二醇单甲醚戊二酸酐半酯脱水穿心莲内酯(DA-C3-1)
合成路线如下:
具体合成方法:
(i)DA-C3-Tr的合成。参照文献Chem.Biol.DrugDes.2014,83,324-333。
(ii)DA-C3-Tr-PA的合成。将DA-C3-Tr-穿心莲内酯(415.1mg,0.7mmol)或DA-C3-Tr-脱水穿心莲内酯(402.5mg,0.7mmol)和三乙二醇单甲醚戊二酸酐半酯(236mg,0.85mmol)溶于40mL二氯甲烷中。依次加入EDC-HCl(326mg,1.7mmol)和DMAP(20mg,0.17mmol),室温搅拌14小时。反应完毕后,加入盐酸水溶液(0.1N,50mL),室温搅拌10分钟后,用二 氯甲烷(20mL)萃取,共萃取三次。合并萃取液,用饱和食盐水(30mL)洗涤。有机相加入无水Na2SO4干燥,过滤后减压蒸馏掉有机溶剂,粗产品经硅胶层析色谱柱分离(洗脱剂为V石油醚:V乙酸乙酯:V乙酸=20:10:1)得化合物DA-C3-Tr-PA,产率65%。
(iii)DA-C3-1的合成。DA-C3-Tr-PA的酸解脱保护反应参照文献Chem.Biol.DrugDes.2014,83,324-333。
常规方法测得化合物DA-C3-1在水中的溶解度C=0.13mg/mL(25℃);酯-水分配系数logP=2.2。
实施例10.四乙二醇单甲醚琥珀酸酐半酯脱水穿心莲内酯脱水穿心莲内酯(DA-C3-2)
按实施例9合成方法合成。用四乙二醇单甲醚琥珀酸酐半酯替代实施例9的三乙二醇单甲醚戊二酸酐半酯。化合物DA-C3-2总产率35%。
常规方法测得化合物DA-C3-2在水中的溶解度C=0.56mg/mL(25℃);酯-水分配系数logP=1.0。
图4示出实施例10化合物的核磁共振氢谱(1H NMR)图。
图5示出实施例10化合物的碳谱(13C-NMR)图。
图6示出实施例10化合物的高分辨质谱(HRMS)图。
实施例11.mPEG350琥珀酸酐半酯脱水穿心莲内酯(DA-C3-3)
按实施例9合成方法合成。用mPEG350琥珀酸酐半酯替代实施例9的三乙二醇单甲醚戊二酸酐半酯。化合物DA-C3-3总产率30%。
常规方法测得化合物DA-C3-3在水中的溶解度C=253mg/mL(25℃);酯-水分配系数logP=1.0。
实施例12-14
与实施例1相同,唯一区别在于,穿心莲内酯和二乙二醇单甲醚的摩尔比分别为1:2、1:3.5、1:5。结果与实施例1类似。
实施例15-39
与实施例1相同,唯一区别在于,溶解用有机溶剂和萃取用有机溶剂均分别为三氯甲烷、四氯化碳、1,2-二氯乙烷、苯、甲苯、二甲苯、氯苯、二氯苯、四氢呋喃、乙腈、乙酸乙酯、乙酸甲酯、乙酸丙酯、二甲亚砜、环丁砜、N,N-二甲基甲酰胺、吡啶、丙酮、甲基丁酮、N-甲基吡咯烷酮、甲基异丁酮、2-丁酮、环己酮、环己烷、二氧六环。
实施例40-54
与实施例1相同,唯一区别在于,催化剂为二甲胺、二乙胺、三甲胺、三乙胺、N,N-二异丙基乙胺、二异丙胺、二丁胺、吡啶、N-甲基吡啶、六亚甲基四胺、吗啉、N-甲基吗啉、哌啶、四氢吡咯、N-甲基四氢吡咯。
实施例55、56
与实施例1相同,唯一区别在于,脱水剂为N,N-二环己基碳二亚胺(DCC)、N,N-二异丙基碳二亚胺(DIC)。
实施例57-59
与实施例6相同,唯一区别在于,穿心莲内酯和六乙二醇单甲醚琥珀酸酐半酯的摩尔比分别为1:1、1:0.9、1:1.8。结果与实施例6类似。
实施例60-62
与实施例6相同,唯一区别在于,反应温度为0℃、50℃、80℃。
实施例63-70
与实施例9相同,唯一区别在于,R’为2-四氢吡喃(THP)、三甲基氯硅烷(TMSCl)、叔丁基二甲基氯硅烷(TBDMSCl)、叔丁基二苯基氯硅烷(TBDPSCl)、三异丙基氯硅烷(TIPSCl)、三氟甲磺酸三甲基硅酯(TMSOTf)、三氟甲磺酸叔丁基二甲基硅酯(TBDMSOTf)或三氟甲磺酸叔丁基二苯基硅酯(TBDPSOTf)。结果与实施例1类似。
实施例71-73
与实施例9相同,唯一区别在于,穿心莲内酯和三乙二醇单甲醚戊二酸酐半酯的摩尔比分别为1:1、1:0.9、1:1.8。结果与实施例9类似。
显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定,对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动,这里无法对所有的实施方式予以穷举,凡是属于本发明的技术方案所引伸出的显而易见的变化或变动仍处于本发明的保护范围之列。
- 还没有人留言评论。精彩留言会获得点赞!