烟草中一种具有抗烟草花叶病毒活性的倍半萜类化合物、其制备方法和用途与流程
本发明属于烟草化学技术领域,具体涉及一种从烟草中首次提取得到的倍半萜类化合物。同时,本发明还涉及该化合物的制备方法和其在抗烟草花叶病毒中的用途。
背景技术:
植物病毒是仅次于真菌的一类病原物,是迄今为止人们发现的最小微生物之一。植物病毒是内含感染性核酸,外披蛋白质外壳的实体,其特征是能感染寄主细胞和通过感染引起病害现象。常见的植物病毒病约有1000多种,多由716种植物病毒造成,植物病毒的危害仅次于真菌。植物病毒病一直是农业生产中的一大危害,素有植物“癌症”之称,由于病毒在植物细胞中绝对寄生,其复制所需的物质、能量、场所完全依赖寄主,且植物没有完整的免疫代谢系统,使得植物病毒病的防治较为困难,给农业生产造成了极大损失。因此病毒病的防治成了全球植物保护工作面临的重要问题,也是植物病毒理论和实践中的重要研究领域。烟草是一种经济作物,由烟草花叶病毒引起的烟草病害是世界各烟区的重要病毒病害,烟草花叶病毒病严重影响了烟叶的产量和质量。据报道,全球每年仅因烟草花叶病毒病造成的损失就达1亿多美元。为了寻找较好的防治植物病毒病的资源,人们进行了多方面的探索和研究。倍半萜(sesquiterpenes)是指分子中含15个碳原子的天然萜类化合物。倍半萜类化合物分布较广,在植物体内常以醇、酮、内酯等等形式存在于挥发油中,是挥发油中高沸点部分的主要组成部分。多具有较强的香气和生物活性,是医药、食品、化妆品工业的重要原料,也是重要的植物源性药物来源之一。为了研究这类化合物的构效关系,可进一步研究和开发更多的倍半萜类化合物,从中寻找有效的先导化合物和活性基团。本发明从云南烤烟烟叶中分离得到了一种新的倍半萜类化合物,该化合物至今尚未见到相关报道,值得一提的是该化合物具有显著的抗烟草花叶病病毒活性。
技术实现要素:
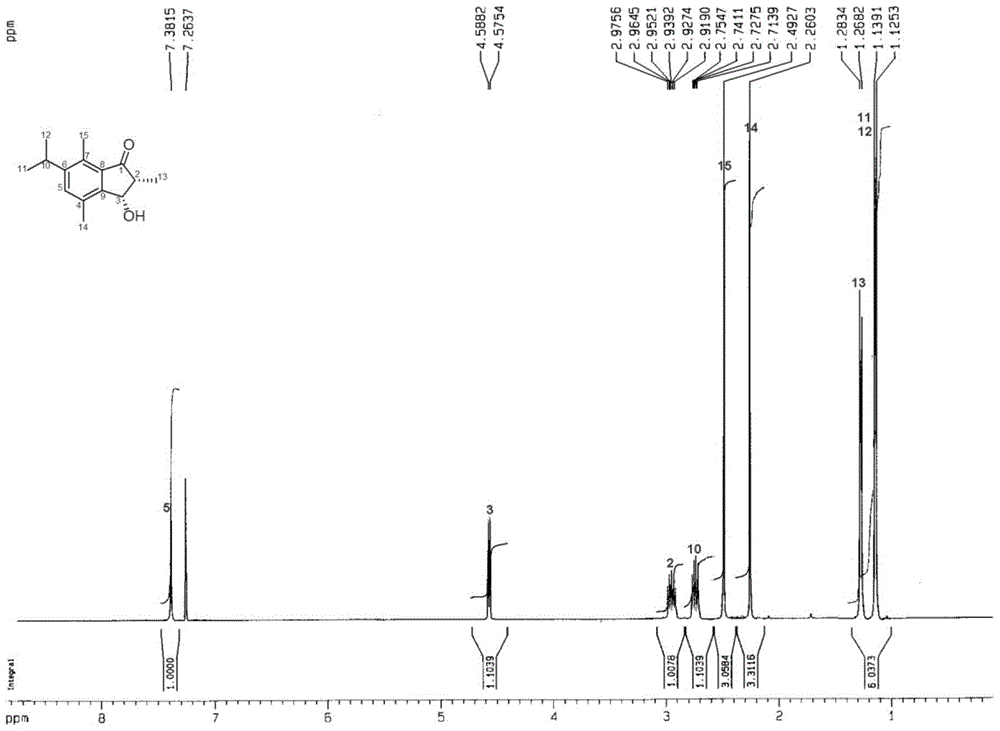
本发明的目的在于提供一种新的倍半萜类化合物。本发明的另一个目的是提供一种制备所述倍半萜类化合物的方法。本发明的目的还在于提供所述倍半萜化合物在抗烟草花叶病毒中的用途。除非另有说明,本发明中所采用的百分数均为重量百分数。本发明第一方面涉及一种从烟草中分离的倍半萜类化合物,其具有下述结构式:该化合物的命名为(2R,3S)-2,3-二氢-3-羟基-6-异丙基-2,4,7-三甲基茚-1-酮,分子式为C15H20O2。其英文名为:[(2R,3S)-2,3-dihydro-3-hydroxy-6-isopropyl-2,4,7-trimethylinden-1-one],为浅黄色胶状物。本发明第二方面涉及一种根据本发明第一方面所述的倍半萜化合物的制备方法,该制备方法包括以下步骤:(1)制备烟草提取物浸膏:以烟草烟叶为原料,将烟叶粉碎或切成小段,并用第一溶剂浸泡并提取所述烟叶3~5次,每次24h~72h,将提取液合并、过滤并浓缩后得到所述烟草提取物浸膏;其中所述第一溶剂是选自甲醇、乙醇或丙酮的有机溶剂与水的混合物,当所述第一溶剂为甲醇或乙醇与水的混合物时,其中甲醇或乙醇占该第一溶剂的80wt%~100wt%,当所述第一溶剂为丙酮与水的混合物时,其中丙酮占该第一溶剂的60wt%~90wt%;且第一溶剂:烟草=(2-4):(4-6),重量比;(2)硅胶柱层析:将上述烟草提取物浸膏与其2-4重量倍的160~300目硅胶混合后干法装柱,然后用体积比依次为1:0、20:1、9:1、8:2、7:3、6:4、1:1和1:2的氯仿-丙酮溶液进行梯度洗脱,将其中体积为8:2的氯仿-丙酮溶液洗脱时得到的洗脱液称为第一洗脱液;(3)高压液相色谱分离纯化:将上述第一洗脱液通入高压液相色谱进行分离纯化,该高压液相色谱采用21.2mm×250mm、5μm的C18色谱柱,流动相流速为20mL/min,流动相为55%的甲醇,紫外检测器检测波长为283nm,第一洗脱液每次进样200μL,每次进样后色谱峰保留时间为25.2min时所对应的洗脱液,称为第二洗脱液,将该第二洗脱液脱除溶剂后即得所述倍半萜化合物。在本发明优选的实施方案中,所述制备方法还包括以下进一步提纯的步骤:将在所述高压液相色谱分离之后得到的所述倍半萜化合物再次溶于纯甲醇,并以纯甲醇为流动相,通过凝胶柱进行层析分离,得到进一步提纯的所述倍半萜化合物。在本发明优选的实施方案中,所述制备方法步骤(2)中,在与所述160~300目硅胶混合之前,先将所述烟草提取物浸膏用其1.5~3重量倍的选自纯甲醇、纯乙醇或纯丙酮的第二溶剂溶解后与为烟草提取物浸膏的0.8~1.2重量倍的80~100目硅胶拌样。本发明第三方面涉及根据本发明第一方面所述的倍半萜类化合物在制备抗烟草花叶病毒药物中的用途。本发明优点如下:本发明的倍半萜类化合物结构新颖,且具有抗烟草花叶病毒活性,可作为抗烟草花叶病毒药物研发的先导性化合物用于抗烟草花叶病毒药物制剂研发。附图说明图1为本发明倍半萜类化合物的核磁共振碳谱;图2为本发明倍半萜类化合物的核磁共振氢谱;图3为本发明倍半萜类化合物的主要HMBC相关图示。具体实施方式本发明所制备的倍半萜类化合物的结构是通过以下方法测定出来的。本发明化合物为浅黄色胶状物;紫外光谱(溶剂为甲醇),λmax(logε)283(3.25),248(3.59),210nm;红外光谱(溴化钾压片)νmax3360,1683,1600,1542,1465,1347,1215,1058,890,575cm-1;高分辨质谱(HRESIMS)给出准分子离子峰m/z231.1393[M-H]-(计算值231.1385)。结合1H和13CNMR谱给出一个分子式C15H20O2,不饱和度为6。从1H和13CNMR谱(数据归属见表1)信号可以看出化合物中有一个1,2,3,4,5-五取代的苯环、一个异丙基、3个甲基、一个氧化次甲基、一个次甲基,一个酮羰基;除去苯环的不饱和度4,羰基的不饱和度1,化合物中还应有一个环。根据H-3和C-9、C-2、C-1、C-4、C-8,以及H-2和C-1、C-3、C-8、C-9的HMBC相关(图3)可证实C-1、C-2和C-3与苯环间形成了一个5元碳环,该化合物为二氢茚-1-酮类结构。化合物的母核确定后,剩余的甲基、异丙基和羟基为母核上的取代基。根据H-10和C-5、C-6、C-7,H-11,12和C-6,以及H-5和C-10的HMBC相关可证实异丙基取代在母核的C-6位;根据H-13和C-1、C-2、C-3,以及H-3和C-13的HMBC相关,可证实该甲基取代在母核的C-2位;根据H-14和C-4、C-5和C-9,以及H-5和C-14的HMBC相关,可证实该甲基取代在母核的C-4位;根据H-15和C-6、C-7和C-8的HMBC相关,可证实该甲基取代在母核的C-7位;此外化合物中还应有一个羟基取代在母核的C-3位,以满足化合物中存在氧化的次甲基。化合物的比旋光度为+14.8,且其CD谱在326.8nm处有正的科顿效应[λmax(Δε)326.8(+18.2)nm],和文献(J.Nat.Prod.2011,74,2010–2013)对比可证实化合物中两个手性碳的构型为2R,3S。至此本化合物的结构得以确定。表1.化合物的1HNMR和13CNMR数据(CCl3)本发明化合物是首次被分离出来的,通过上述核磁共振和质谱测定方法确定为倍半萜类化合物,并表征了其具体结构。采用半叶法进行了本发明化合物的抗烟草花叶病毒活性测试,结果表明本化合物的相对抑制率为45.6%,超过了阳性对照宁南霉素的相对抑制率31.5%,说明本化合物具有很好的抗烟草花叶病毒活性。活性检测结果揭示了本发明的化合物在制备抗轮状烟草花叶病毒药物中有良好的应用前景。本发明的化合物结构简单、活性较好,可作为抗烟草花叶病毒药物研发的先导性化合物用于抗烟草花叶病毒药物制剂研发。下面结合附图和实施例对本发明作进一步的详细说明,但不以任何方式对本发明加以限制,基于本发明教导所作的任何变换或改进,均落入本发明的保护范围。本发明所用原料不受地区和品种限制,任何来源地的烟草均可以实现本发明,下面以来源于云南中烟工业有限责任公司不同产地的烟草原料对本发明做进一步说明。除非另有说明,本发明中所采用的百分数均为重量百分数。实施例1一种倍半萜类化合物C15H20O2的制备方法,具体包括以下步骤:(1)制备烟草提取物浸膏:以烟草烟叶为原料,将烟叶粉碎或切成小段,并用第一溶剂浸泡并提取所述烟叶4次,每次54h,将提取液合并、过滤并浓缩后得到所述烟草提取物浸膏;其中所述第一溶剂是选自甲醇、乙醇或丙酮的有机溶剂与水的混合物,当所述第一溶剂为甲醇或乙醇与水的混合物时,其中甲醇或乙醇占该第一溶剂的95wt%,当所述第一溶剂为丙酮与水的混合物时,其中丙酮占该第一溶剂的70wt%;且第一溶剂:烟草=3:5,重量比;(2)硅胶柱层析:将所述烟草提取物浸膏用其2.5重量倍的选自纯甲醇、纯乙醇或纯丙酮的第二溶剂溶解后与为烟草提取物浸膏的1.2重量倍的80~100目硅胶拌样,再与烟草提取物浸膏3重量倍的250目硅胶混合后干法装柱,然后用体积比依次为1:0、20:1、9:1、8:2、7:3、6:4、1:1和1:2的氯仿-丙酮溶液进行梯度洗脱,将其中体积为8:2的氯仿-丙酮溶液洗脱时得到的洗脱液称为第一洗脱液;(3)高压液相色谱分离纯化:将上述第一洗脱液通入高压液相色谱进行分离纯化,该高压液相色谱采用21.2mm×250mm、5μm的C18色谱柱,流动相流速为20mL/min,流动相为55%的甲醇,紫外检测器检测波长为283nm,第一洗脱液每次进样200μL,每次进样后色谱峰保留时间为25.2min时所对应的洗脱液,称为第二洗脱液,将该第二洗脱液脱除溶剂后即得所述倍半萜化合物。所述制备方法还包括以下进一步提纯的步骤:将在所述高压液相色谱分离之后得到的所述倍半萜化合物再次溶于纯甲醇,并以纯甲醇为流动相,通过凝胶柱进行层析分离,得到进一步提纯的所述倍半萜化合物。实施例2所用烟草样品来源于云南玉溪,品种为玉溪K326。将烟叶取样2.0kg粉碎以95%的甲醇提取5次,每次提取24h,提取液合并,过滤,减压浓缩得烟草提取物浸膏105g。将上述烟草提取物浸膏用其2.0重量倍的纯甲醇溶解后用120g的100目粗硅胶拌样,再与0.6kg的160目硅胶混合后装柱进行硅胶柱层析,用体积配比为1:0、20:1、9:1、8:2、7:3、6:4、1:1、1:2的氯仿-丙酮梯度洗脱,TLC监测合并相同的部分,得到8个部分,其中体积配比为8:2的氯仿-丙酮洗脱部分用安捷仑1100半制备高效液相色谱分离,以55%的甲醇为流动相,ZorbaxSB-C18(21.2×250mm,5μm)制备柱为固定相,流动相流速为20ml/min,紫外检测器检测波长为283nm,每次进样200μL,收集每次进样后色谱峰保留时间为25.2min时所对应的洗脱液,多次累加后脱除溶剂;所得产物再次用纯甲醇溶解,再以纯甲醇为流动相,用SephadexLH-20凝胶柱层析分离,即得进一步提纯的倍半萜化合物。实施例3所用烟草样品来源于云南大理,品种为云烟200。将烟叶取样3.5kg切碎,以95%的乙醇提取4次,每次提取48h,提取液合并,过滤,减压浓缩得烟草提取物浸膏250g。将上述烟草提取物浸膏用其2.0重量倍的纯甲醇溶解后用250g的80目粗硅胶拌样,再与1.2kg的200目硅胶混合后装柱进行硅胶柱层析,用体积配比为1:0、20:1、9:1、8:2、7:3、6:4、1:1、1:2的氯仿-丙酮梯度洗脱,TLC监测合并相同的部分,得到8个部分,其中体积配比为8:2的氯仿-丙酮洗脱部分用安捷仑1100半制备高效液相色谱分离,以55%的甲醇为流动相,ZorbaxSB-C18(21.2×250mm,5μm)制备柱为固定相,流动相流速为20ml/min,紫外检测器检测波长为283nm,每次进样200μL,收集每次进样后色谱峰保留时间为25.2min时所对应的洗脱液,多次累加后脱除溶剂;所得产物再次用纯甲醇溶解,再以纯甲醇为流动相,用SephadexLH-20凝胶柱层析分离,即得进一步提纯的倍半萜化合物。实施例4所用烟草样品来源于云南昆明,品种为红花大金元。将烟叶取样5kg粉碎,以75%的丙酮用超声提取3次,每次提取72h,提取液合并,过滤,减压浓缩得烟草提取物浸膏380g。将上述烟草提取物浸膏用其1.6重量倍的纯甲醇溶解后用400g的90目粗硅胶拌样,再与2.4kg的180目硅胶混合后装柱进行硅胶柱层析,用体积配比为1:0、20:1、9:1、8:2、7:3、6:4、1:1、1:2的氯仿-丙酮梯度洗脱,TLC监测合并相同的部分,得到8个部分,其中体积配比为8:2的氯仿-丙酮洗脱部分用安捷仑1100半制备高效液相色谱分离,以55%的甲醇为流动相,ZorbaxSB-C18(21.2×250mm,5μm)制备柱为固定相,流速为20ml/min,紫外检测器检测波长为283nm,每次进样200μL,收集每次进样后色谱峰保留时间为25.2min时所对应的洗脱液,多次累加后脱除溶剂;所得产物再次用纯甲醇溶解,再以纯甲醇为流动相,用SephadexLH-20凝胶柱层析分离,即得进一步提纯的倍半萜化合物。实施例5-化合物结构的鉴定取实施例1制备的化合物,以上述方法制备得到的倍半萜类化合物的结构通过以下方法进行测定。本发明化合物为浅黄色胶状物;紫外光谱(溶剂为甲醇),λmax(logε)283(3.25),248(3.59),210nm;红外光谱(溴化钾压片)νmax3360,1683,1600,1542,1465,1347,1215,1058,890,575cm-1;高分辨质谱(HRESIMS)给出准分子离子峰m/z231.1393[M-H]-(计算值231.1385)。结合1H和13CNMR谱给出一个分子式C15H20O2,不饱和度为6。从1H和13CNMR谱(数据归属见表1)信号可以看出化合物中有一个1,2,3,4,5-五取代的苯环、一个异丙基、3个甲基,一个氧化次甲基、一个次甲基,一个酮羰基;除去苯环的不饱和度4,羰基的不饱和度1,化合物中还应有一个环。根据H-3和C-9、C-2、C-1、C-4、C-8,以及H-2和C-1、C-3、C-8、C-9的HMBC相关(图3)可证实C-1、C-2和C-3与苯环间形成了一个5元碳环,该化合物为二氢茚-1-酮类结构。化合物的母核确定后,剩余的甲基、异丙基和羟基为母核上的取代基。根据H-10和C-5、C-6、C-7,H-11,12和C-6,以及H-5和C-10的HMBC相关可证实异丙基取代在母核的C-6位;根据H-13和C-1、C-2、C-3,以及H-3和C-13的HMBC相关,可证实该甲基取代在母核的C-2位;根据H-14和C-4、C-5和C-9,以及H-5和C-14的HMBC相关,可证实该甲基取代在母核的C-4位;根据H-15和C-6、C-7和C-8的HMBC相关,可证实该甲基取代在母核的C-7位;此外化合物中还应有一个羟基取代在母核的C-3位,以满足化合物中存在氧化的次甲基。化合物的比旋光度为+14.8,且其CD谱在326.8nm处有正的科顿效应[λmax(Δε)326.8(+18.2)nm],和文献(J.Nat.Prod.2011,74,2010–2013)对比可证实化合物中两个手性碳的构型为2R,3S。至此本化合物的结构得以确定。实施例6-8分别取实施例2-4制备的化合物,为黄色胶状物。测定方法与实施例5相同,确认实施例2-4中制备的化合物均为倍半萜类化合物(2R,3S)-2,3-二氢-3-羟基-6-异丙基-2,4,7-三甲基茚-1-酮。实施例9取实施例1-4制备的任一倍半萜类化合物进行抗烟草花叶病毒活性试验,试验情况如下:采用半叶法,在药剂的质量浓度均为50mg/L时对本发明化合物进行抗烟草花叶病毒活性测定。在5~6龄烤烟的植株上,选取适用于测试的叶片(叶行正常,无病无虫),先将叶片均匀撒上细金刚砂,用毛笔将备用的烟草花叶病毒源(3.0×10-3)均匀抹在撒有金刚砂的叶片上,待所有中选的叶片接毒结束后,立即放在盛有药液的培养皿中处理20min,取出,擦去叶片上水珠和药液,将两个半叶复原排放在铺有卫生纸保湿的玻璃缸中,并盖上玻璃盖,控温(23±2)℃,放在温室自然光照射,2~3d即可见枯斑.每个处理都设另一半叶为对照,另外设有1组为商品宁南霉素的处理作为对比,按下公式计算相对抑制率。XI%=(CK-T)/CK×100%X:相对抑制率(%),CK:浸泡于清水中半片接毒叶的枯斑数(个),T浸泡于药液中半片接毒叶的枯斑数(个)。结果明本化合物的相对抑制率为45.6%,超过对照宁南霉素的相对抑制率31.5%,说明化合物有很好的抗烟草花叶病毒活性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1