一种131I标记的间碘苄胍的制备方法与流程
本发明涉及放射性药物领域,具体涉及一种131I标记的间碘苄胍的制备方法。
背景技术:
131I是一种理想的应用于诊断和治疗的放射性核素,能同时释放γ射线和β射线,物理半衰期为8.04d。间碘苄胍是一种胍乙腚衍生物,结构上类似于去甲肾上腺素,都是间位有取代基的苯环,间碘苄胍有极性较大的胍基,主要是间位碘取代而产生不同的药理作用。由于肾上腺细胞需要摄取胍乙腚,生物合成儿茶酚胺类物质,故间碘苄胍具有肾上腺靶向性。当肾上腺髓质存在高选择性病灶(嗜铬细胞瘤)或增生灶(肿瘤细胞异常增殖)时,放射性同位素131I标记的间碘苄胍易于进入肿瘤细胞,使细胞摄取量的明显增多,表现为放射性增加或浓集,从而使肾上腺清晰显影。β射线,能量高(最高能峰为607kev),当其在细胞内达到一定的浓集后,可发挥杀伤作用并抑制细胞增殖,治疗癌症。由于β射线的射程(2~8μm)小于细胞直径(9μm),故对于正常组织的破坏和影响很小。间碘苄胍被高选择病灶摄取后,131I-间碘苄胍在肿瘤与肝的放射性活度比值可达680:1,3700-9250MBq(兆贝克),即100-250mCi(毫居)可使肿瘤部位获得20Gy(戈瑞)的吸收剂量,这样的辐射剂量能抑制或破坏肿瘤组织,从而达到治疗目的。131I-间碘苄胍对恶性嗜铬细胞瘤疗效显著,尤其可以改善症状,控制血压,降低儿茶酚胺量等,对于毫米级大小的亚临床肿瘤,每克肿瘤组织吸收剂量在>10Gy时,可达到肿瘤消失、治愈的目的,手术或局限性放疗仅能治疗肉眼所见的肿瘤;对于骨转移患者在给药后3~5天,骨疼痛缓解的效果明显,6个月随访的存活率达100%。
1994年,美国FDA批准131I-间碘苄胍(Iobenguane Sulfate I 131TM,NDA20-084)用于诊断嗜铬细胞瘤和神经母细胞瘤。目前临床上使用的131I-间碘苄胍采用同位素交换法制备,得到的产品131I-间碘苄胍中含有大量稳定的无放射性间碘苄胍(载体),放射性比活度(131I的放射性活度与131I-间碘苄胍质量之比,即单位质量产品中所含131I核素的放射性活度)低,小于25mCi/mg,用于疾病的诊断显像时,用药量高会产生高血压、恶心、头 昏等副作用。用于疾病的治疗时,由于治疗量的放射性比活度需要达到20-60mCi/mg,效果不佳。由于有载体131I-间碘苄胍存在弊端,无载体131I-间碘苄胍的制备和应用研究逐渐得到重视,研究表明,无载体131I-间碘苄胍的放射性比活度达到200mCi/mg左右,其诊断和治疗效果优于有载体131I-间碘苄胍。与商业化的有载体131I-间碘苄胍相比,无载体131I-间碘苄胍的制备要复杂得多,需要在标记后使用放射性高效液相色谱仪对标记产物进行纯化,不利于大规模制备和临床应用。无载体131I-间碘苄胍的合成方法是将碘标记在特定位置上,通过激活分子中一个带有合适的离去基团位点来实现的(离去基团有:碘、溴、重氮化的苯胺以及锡、硼、三硅和铊的衍生物)。目前研究方法包括固相合成法和液相合成法。固相合成法是将131I-间碘苄胍的前体用化学方法固定在树脂上,标记之后131I-间碘苄胍从树脂脱落,进入溶液。Hunter报道了利用固相合成的方法在树脂上制备无载体131I-间碘苄胍,此法分离简单,得到的产物纯度高,杂质少,但是该树脂要求达到注射用级别,反应近乎苛刻,仅见于实验室制备和文献报道,无法投入实际生产。有些利用锡取代前体化合物制备的131I-间碘苄胍带入锡和其他有毒杂质,难以去除,无法应用于临床。
目前所有技术制备的131I-间碘苄胍,均为在工厂或实验室制备后运输至医院供临床使用,一方面放射性物质的运输要求高,成本高,另一方面其含有的放射性碘具有衰变性,其效能随时在损失,时间越长,损失越大。
技术实现要素:
本发明的目的是提供一种具有高放射性比活度的无载体131I-间碘苄胍的制备方法。
为实现上述目的,本发明采用以下技术方案:
一方面,本发明提供一种制备具有高放射性比活度的无载体131I-间碘苄胍的方法,包括如下步骤:将N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍,缓冲溶液,氧化剂及Na131I常温反应20分钟,再加入还原剂加热至100℃反应20分钟。反应结束后静置,冷却至室温,加入阴离子交换树脂,轻轻搅拌2分钟。吸取上清液,过微孔滤膜,即得标记物131I-间碘苄胍,所述氧化剂选自双氧水或N-氯代琥珀酰亚胺,所述还原剂选自三氟乙酸或焦亚硫酸钠。
优选的,所述氧化剂选自双氧水或N-氯代琥珀酰亚胺,所述还原剂选自三氟乙酸或焦亚硫酸钠。
更优选的,所述氧化剂和还原剂的摩尔比为1:1.2。
优选的,所述氧化剂的用量为0.17μmol,所述还原剂的用量为0.21μmol。
优选的,所述N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍、氧化剂和还原剂的摩尔比为0.1:(0.1-0.5):(0.12-0.6)。
更优选的,所述N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍、氧化剂和还原剂的摩尔比为0.1:0.15:0.18。
优选的,所述缓冲溶液选自乙酸或磷酸二氢钾/氢氧化钠。
更优选的,所述缓冲溶液乙酸500μl或磷酸二氢钾和氢氧化钠的摩尔比为1:0.3。
优选的,所述磷酸二氢钾的用量为25μmol,所述氢氧化钠的用量为7.5μmol。
更优选的,所述N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍、氧化剂、还原剂、磷酸二氢钾和氢氧化钠的摩尔比为0.1:0.15:0.18:21:6.3。
优选的,所述Na131I的放射性活度约为1-100mCi。
更优选的,所述Na131I的放射性活度约为13mCi。
优选的,所述阴离子交换树脂为717阴离子树脂。
更优选的,所述阴离子交换树脂为自制小型抛弃型阴离子树脂填充柱。
优选的,所述微孔滤膜的孔径为0.22μm。
另一方面,本发明还提供一种采用上述任一方法制备得到的131I-间碘苄胍。
本发明具有积极有益的效果:
分别采用双氧水--三氟乙酸或N-氯代琥珀酰亚胺--焦亚硫酸钠作为氧化剂和还原剂,磷酸二氢钾和氢氧化钠作为缓冲溶液,标记N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍,制备得到的131I-间碘苄胍,经阴离子交换树脂和0.22μm微孔滤膜过滤,去除了反应副产物,锡量降低至痕量。放射化学纯度高,稳定性好。无载体(没有放射性的间碘苄胍)存在,比活度高,临床诊断治疗效果好。标记反应条件温和简单,可以在医院完成制备,避免运输带来的高额成本和药品的衰变损失。
附图说明
图1 131I-间碘苄胍的紫外HPLC图谱。
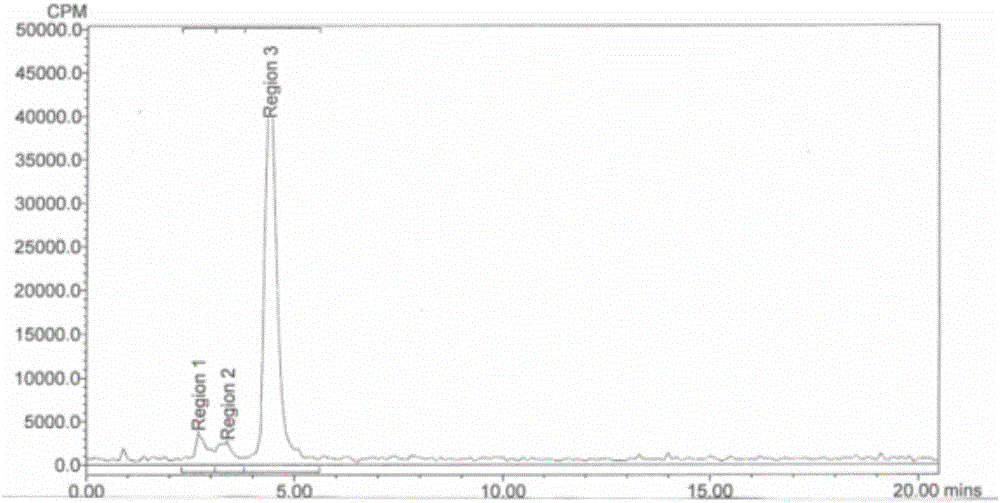
图2 131I-间碘苄胍的放射性HPLC图谱。
图3 树脂处理后131I-间碘苄胍的紫外HPLC图谱。
图4 树脂处理后131I-间碘苄胍的放射性HPLC图谱。
具体实施方式
下面结合实施例对本发明作更进一步的说明,但本发明的实施方式不限于此。下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
一、N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍的合成
1)3-碘-苄胍碳酸氢盐(A)的合成
间碘苄胺盐酸盐(5g,18.6mmol)与氨基腈(1.17g,27.6mmol)混合,加热到100℃,熔融状态下保持6h,冷却至室温,加水10ml溶解,再加入KHCO3(1.86g,18.6mmol)溶于10ml水中,得粗品4.7g化合物A,收率75.2%,mp 124-126℃。
2)N,N’-二(叔丁氧羰基)-3-碘-苄胍(B)的合成
用NaOH(2.22g,55.5mmol)水溶液溶解化合物A(3g,9.3mmol),加入溶有(Boc)2O(4.06g,18.6mmol)的THF溶液中,混合加热回流1h,得到白色沉淀,用乙醇-水(v:v=3:7)溶液洗涤多次,得产品3.8g,产率86.0%。
3)N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍(C)的合成
在100ml圆底烧瓶中加入化合物B(1g,2.10mmol),Pd(PPh3)2Cl2(0.15g,0.21mmol),双(三丁基锡)(2.44g,4.21mmol),1,4-二氧六环作溶剂30ml,在氮气保护下100℃回流2h。冷却,过滤,制备色谱分离得0.86g产物,产率64.2%。
二、标记N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍制备131I-间碘苄胍
实施例1:向10ml管制西林瓶中依次加入N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍70μg,醋酸500μl,30%双氧水溶液16.5μl,Na131I溶液13.5mCi(0.1ml),生理盐水1ml,常温反应20分钟。加入三氟乙酸100μl加热至100℃反应20分钟。反应结束后静置,冷却至室温,加入717阴离子交换树脂1g,轻轻搅拌2分钟。吸取上清液,0.22μm微孔滤膜过滤,即得标记物131I-间碘苄胍。
实施例2:向10ml管制西林瓶中依次加入N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍70μg,醋酸500μl,30%双氧水溶液16.5μl,Na131I溶液13.5mCi(0.1ml),生理盐水1ml,常温反应20分钟。加入三氟乙酸100μl加热至100℃反应20分钟。反应结束后静置,冷却至室温,用针筒抽出反应液注入自制小型抛弃型717阴离子交换树脂填充柱过柱,再用1ml生理盐水洗脱。合并溶液,用0.22μm滤膜的针头过滤器过滤,即得标记物131I-间碘苄胍。
实施例3:向10ml管制西林瓶中依次加入N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍70μg,N-氯代琥珀酰亚胺25μg,磷酸二氢钾3.4mg,氢氧化钠0.3mg,Na131I溶液13.5mCi(0.1ml),生理盐水1.5ml,常温反应20分钟。加入焦亚硫酸钠40μg,加热至100℃反应20分钟。反应结束后静置,冷却至室温,加入717阴离子交换树脂1g,轻轻搅拌2分钟。吸取上清液,0.22μm微孔滤膜过滤,即得标记物131I-间碘苄胍。
实施例4:向10ml管制西林瓶中依次加入N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍70μg,N-氯代琥珀酰亚胺25μg,磷酸二氢钾3.4mg,氢氧化钠0.3mg,Na131I溶液13.5mCi(0.1ml),生理盐水1.5ml,常温反应20分钟。加入焦亚硫酸钠40μg,加热至100℃反应20分钟。反应结束后静置,冷却至室温,用针筒抽出反应液注入自制小型抛弃型717阴离子交换树脂填充柱过柱,再用1ml生理盐水洗脱。合并溶液,用0.22μm滤膜的针头过滤器过滤,即得标记物131I-间碘苄胍。
对比例1:向玻璃试管中依次加入间碘苄胍硫酸盐1mg,硫酸亚锡0.5mg,维生素C0.1mmol,硫酸铜0.43mg及放射性活度为5mCi的Na131I溶液,放入沸水浴中加热30分钟,取出后放到烧杯中,静置30秒,吸取上清液,过0.22μm滤膜,即得标记物131I-间碘苄胍。
对比例2:向10ml管制西林瓶中依次加入N,N’-二(叔丁氧羰基)-3-(三丁基锡基)-苄胍70μg,氯胺T 50μg,,磷酸二氢钾3.4mg,氢氧化钠0.3mg,Na131I溶液13.5mCi(0.1ml),生理盐水1.5ml,常温反应20分钟。加入焦亚硫酸钠40μg,加热至100℃反应20分钟。反应结束后静置,冷却至室温,过0.22μm滤膜,即得标记物131I-间碘苄胍。三、131I-间碘苄胍放射化学纯度测定
实验材料:采用薄层层析(TLC)法,支持物为聚酰胺薄膜,展开剂为双系统:系统①的展开剂为乙酸乙酯:乙醇=1:1(V/V),系统②的展开剂为正丙醇:10%氨水=3:1(V/V),将聚酰胺薄膜切割成0.5*10cm规格的层析条,展开剂置于试管约0.5cm深。
实验方法及结果:取实施例1-3和对比例的标记产物适量用毛细管点样于聚酰胺薄膜一端(距离层析条边沿约1cm),约1分钟待点样自然挥发至干,点样处朝下放入展开剂饱和的试管中,盖上盖子。分别以乙酸乙酯:乙醇=1:1(V/V)和正丙醇:10%氨水=3:1(V/V)作为展开剂,照上行色谱法展开。待展开剂展开至距前沿约0.5cm时,取出层析条,自然挥发至干。
结果显示,①乙酸乙酯:乙醇=1:1(V/V)为展开剂的各斑点Rf值为:131I-间碘苄胍0.0,游离碘0.6。②展开剂为正丙醇:10%氨水=3:1(V/V),为展开剂的各斑点Rf值为:131I-间碘苄胍0.15,对碘苄胺0.35,游离碘0.75。
层析条按展开剂的展开距离平均切割成10份,分别放入γ-计数,用γ-count测量放射性计数,按照下述计算公式得出实施例1-4和对比例1-2中游离碘以及对碘苄胺纯度,并计算131I-间碘苄胍放射化学纯度(见表1)。
游离碘(%)=游离碘的放射性计数率/系统一的放射性计数率总和*100%
对碘苄胺(%)=对碘苄胺的放射性计数率/系统二的放射性计数率总和*100%
131I-间碘苄胍(%)=100%-(游离碘(%)+对碘苄胺(%))
四、高效液相测定131I-间碘苄胍中杂质含量并测定其放射性比活度
HPLC(waters泵1525-检测器2487)C18填料5μm,4.6×250mm;检测波长254nm,流速1mL/min;
流动相:氯化铵(1mol/L):氨水(含量25%):甲醇=1:2:27;
图1和图2分别是131I-间碘苄胍样品的HPLC紫外分析图谱和放射性分析图谱。
在图2的γ计数图谱中,在RT=5min处的吸收峰对应的是131I-间碘苄胍的吸收峰,与纯的间碘苄胍在同一系统中的保留时间吻合。
从图2可以看到,影响标记率的峰主要是同位素碘(131I),当把标记的溶液用阴离子交换树脂进行处理,再把标记后的水溶液用0.22μm针头过滤器过滤,除掉溶液中的极性较小,水不溶含三丁基锡基团的副产物后,用同样的系统进行HPLC检测,结果如图3,图4。
从HPLC图谱(图3,图4)中可以发现,经过阴离子交换树脂的处理和0.22μm滤膜的过滤,不仅放射性元素(131I-,RT=4min)从体系中清除了,而且溶液中的很多杂质也消除了。
以间碘苄胍原料为对照品,HPLC法紫外检测器测得化学量,同时放射性检测器测得放射性活度,分别测得实施例1-4和对比例1-2中131I-间碘苄胍放射性比活度(见表1)。
表1 131I-间碘苄胍放射化学纯度和放射性比活度
五、131I-间碘苄胍中锡含量测定
由于反应液中三丁基锡基团毒性较大,临床使用要求限量在1ppm。采用原子荧光光度法进行锡的含量检测,考察经过处理后的溶液中三丁基锡的含量。
采用AFS-9700型原子荧光光度计,未检测出锡。因仪器的检测限为0.23ng/mL,故样品中锡量应小于0.23*10-6/1=0.23ppm,显著小于临床使用限度要求1ppm,提示其制备的 131I-间碘苄胍毒性大大降低。
综上可见,本发明制备的131I-间碘苄胍放射化学纯度高,无间碘苄胍载体存在,比活度高。特别是采用双氧水--三氟乙酸或N-氯代琥珀酰亚胺--焦亚硫酸钠作为氧化剂和还原剂制备的131I-间碘苄胍放射化学纯度高于以氯胺T—焦亚硫酸钠作为氧化剂和还原剂制备的无载体131I-间碘苄胍,其放射性比活度高于传统热交换法制备的有载体131I-间碘苄胍。特别是采用阴离子交换树脂处理后,经微孔滤膜过滤,去除了131I-间碘苄胍溶液中的反应副产物,锡量降低至痕量,适合临床诊断和治疗使用。标记反应条件温和简单,可以在医院完成制备,避免运输带来的高额成本和药品的衰变损失。其中以实施例2方法制备的131I-间碘苄胍放射化学纯度和放射性比活度均最高,操作最为简单,效果最好。
- 还没有人留言评论。精彩留言会获得点赞!