一种温度传感器及其应用的制作方法
本发明涉及一种温度传感器及其应用,属于生物工程技术领域。
背景技术:
生物对温度的应激反应的能力是必不可少的,如热休克蛋白和分子伴侣蛋白,在各种热冷冲击响应中起作用,对生物体感应温度变化的响应转录和转录后水平起调节作用。基于RNA的温度响应调节系统,利用了单股的自然趋势RNA分子在温度响应中改变二级结构,导致RNA稳定性或翻译率改变。以RNA为基础的温度传感器在细菌体内是常见的。大自然产生的RNA热敏元件,是经过长期的温度诱导,有很长的序列,在较低温度下核糖体结合位点形成发卡结构。这些热敏元件包含对RNase酶裂解位点,原产于大肠杆菌和许多其他生物,存在于靶基因的5/端非编码区。在低温度,裂解位点形成茎环结构隐退,基因表达通畅。在高温,裂解位点阀杆展开,允许对mRNA的降解,无法表达基因序列。
热阻遏RNA功能有各种温度传感器机制。例如,RpoS的表达在大肠杆菌中受DsrA的调控。DsrA可以采取两种结构的构象,其中一个(F形式)将结合到目标Mrna并将RBS暴露。在较低的温度下,F形式增加了稳定性,热阻遏表达目标基因。然而,两种形式之间的稳定性差异机制是未知的。另一被研究的热阻遏RNA热敏传感器是大肠杆菌的CSPAmRNA。
这些自然产生的RNA的温度传感器,很难在工程系统中实现应用。例如,RpoS机理复杂,研究的甚少,而CSPA热敏传感器非常大的而且需要CSPA编码序列的参与。这些特性阻碍了它们在生物学中的应用。
技术实现要素:
本发明旨在设计长度短、机制简单的RNA热敏元件,这些热敏元件的响应在不同的温度下存在差异。在较低的温度下,形成发卡结构。在高温下,发夹是不稳定的,实现转录和翻译。
本发明提供4条RNA热敏元件,序列分别如SEQ ID NO.1~4所示。
通过检测荧光蛋白的表达强度分析上述RNA热敏元件对于温度的响应情况。在枯草芽孢杆菌中表达时,在20℃、25℃、30℃、37℃条件下,荧光强度逐渐增强。在20℃条件下荧光强度最低,在37℃条件下荧光强度最高。如图1所示,对照组在20℃、25℃、30℃、37℃条件下,荧光强度不发生变化。如图2-5所示,荧光强度在不同的温度下高低不同。
本发明还提供一种梯度RNA热敏元件,由序列如SEQ ID NO.1~4所示的4个RNA组成。
本发明还提供一种调控蛋白表达的方法,是将目的基因RBS序列替换为编码序列如SEQ ID NO.1~4任一所示的RNA热敏元件的序列。在20-37℃范围内,采用不同RNA热敏元件,实现不同温度下的不同的蛋白表达量。
本发明还提供一种温度传感器,是含有序列如SEQ ID NO.1~4所示的RNA热敏元件中的至少一种,或者含有编码序列如SEQ ID NO.1~4所示的RNA热敏元件中的至少一种的脱氧核糖核酸序列。将编码所述标记蛋白的基因的RBS序列替换为编码序列如SEQ ID NO.1~4任一所示的RNA热敏元件的序列,然后根据标记蛋白的表达量可以提示当前表达体系所处环境的温度范围。
所述标记蛋白可以是绿色荧光蛋白。
本发明设计的长度短、机制简单的RNA热敏元件,这些热敏元件响应到具体到温度。这些热敏元件将在类似的温度传感器系统的建设中起到一定作用。同时,可应用于理性调控细胞的代谢系统。
附图说明
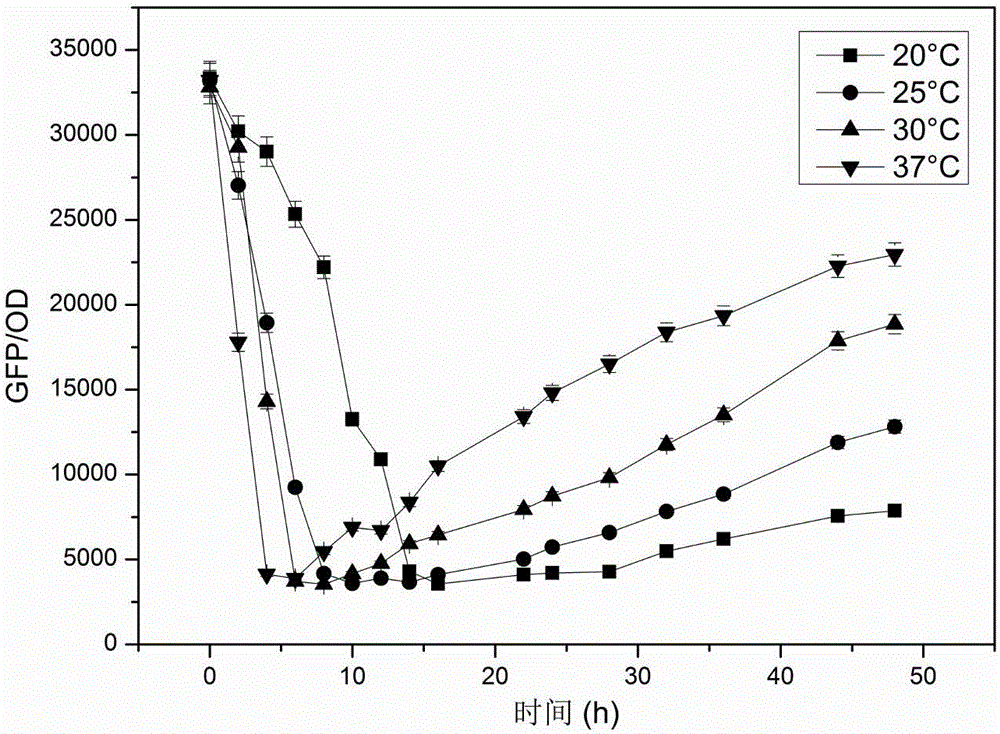
图1是构建的对照菌株在4种温度下的荧光强度变化趋势;
图2是构建的温控序列1在4种温度下的荧光强度变化趋势;
图3是构建的温控序列2在4种温度下的荧光强度变化趋势;
图4是构建的温控序列3在4种温度下的荧光强度变化趋势;
图5是构建的温控序列4在4种温度下的荧光强度变化趋势。
具体实施方式
实施例1质粒构建方法
绿色荧光蛋白因荧光性质稳定,大量表达对细胞没有毒性,检测方便的特点,我们选择绿色荧光蛋白作为检测热敏元件的表达效果。以质粒Phtc-gfp(该质粒的构建方法参见Sen Yang,Zhen Kang,Wenlong Cao,Guocheng Du,&Chen,2015)为模板,通过设计引物F、R0、R1、R2、R3、R4进行PCR,将原有RBS序列GATGCAGCTTAATAAAAGGTGGTGAACTACT分别替换为编码如下(1)~(4)所示的设计的RNA热敏元件的基因序列:
(1)GAUGUACCUUAAUAAAAGGUGGUGAACUACUAUG,
(2)GAUGUUACCUUAAUAAAAGGUGGUGAACUACUAUG,
(3)GAUGCUACCUUAAUAAAAGGUGGUGAACUACUAUG人工序列
(4)GAUGCUACCUAAAAAAGGUGGUGAACUACUAUG,以原有RBS序列作为对照。PCR产物磷酸化连接转入E.coli JM109扩增,提纯后转入B.subtilis 168进行表达。
实施例2温度传感器的检测
将长出的菌落挑入含3mL的卡纳抗性的LB液体培养基中进行12h的培养,再将菌液按10%的接种量接入含200μL发酵培养基的96孔平板,每个样品做三个平行,分别加入4个96孔板中,在20℃、25℃、30℃、37℃条件下,转速90rpm,培养48小时。每隔一段时间使用Synergy H4全功能酶标仪在激发光490nm,发射光530nm,Gain值是70,检测高度7mm条件下测荧光强度,并在600nm波长下检测菌体浓度,并绘制出荧光强度变化趋势图(如图1至图5所示)。图2所示温控序列1荧光强度变化趋势可以看出,37℃的荧光强度比20℃荧光强度高15000,荧光强度增加1.9倍;图3所示温控序列2荧光强度变化趋势可以看出,37℃的荧光强度比20℃荧光强度高3156,荧光强度增加2.2倍;图4所示温控序列3荧光强度变化趋势可以看出,37℃的荧光强度比20℃荧光强度高9339,荧光强度增加3.3倍;图5所示温控序列4荧光强度变化趋势可以看出,37℃的荧光强度比20℃荧光强度高19758,荧光强度增加10倍。可以看出,温控序列4的温控效果优于温控序列1、2和3,37℃的荧光强度与20℃的荧光强度相差最大,效果最好。
SEQUENCE LISTING
<110> 江南大学
<120> 一种温度传感器及其应用
<160> 11
<170> PatentIn version 3.3
<210> 1
<211> 34
<212> RNA
<213> 人工序列
<400> 1
gauguaccuu aauaaaaggu ggugaacuac uaug 34
<210> 2
<211> 35
<212> RNA
<213> 人工序列
<400> 2
gauguuaccu uaauaaaagg uggugaacua cuaug 35
<210> 3
<211> 35
<212> RNA
<213> 人工序列
<400> 3
gaugcuaccu uaauaaaagg uggugaacua cuaug 35
<210> 4
<211> 33
<212> RNA
<213> 人工序列
<400> 4
gaugcuaccu aaaaaaggug gugaacuacu aug 33
<210> 5
<211> 31
<212> DNA
<213> 人工序列
<400> 5
gatgcagctt aataaaaggt ggtgaactac t 31
<210> 6
<211> 35
<212> DNA
<213> 人工序列
<400> 6
tttcagcatc tatttatcac ataagatgac aattg 35
<210> 7
<211> 57
<212> DNA
<213> 人工序列
<400> 7
gatgcagctt aataaaaggt ggtgaactac tatgggtaag ggagaagaac ttttcac 57
<210> 8
<211> 57
<212> DNA
<213> 人工序列
<400> 8
gatgtacctt aataaaaggt ggtgaactac tatgggtaag ggagaagaac ttttcac 57
<210> 9
<211> 58
<212> DNA
<213> 人工序列
<400> 9
gatgttacct taataaaagg tggtgaacta ctatgggtaa gggagaagaa cttttcac 58
<210> 10
<211> 58
<212> DNA
<213> 人工序列
<400> 10
gatgctacct taataaaagg tggtgaacta ctatgggtaa gggagaagaa cttttcac 58
<210> 11
<211> 56
<212> DNA
<213> 人工序列
<400> 11
gatgctacct aaaaaaggtg gtgaactact atgggtaagg gagaagaact tttcac 56
- 还没有人留言评论。精彩留言会获得点赞!